2. 江苏省农业科学院农业资源与环境研究所, 农业部长江下游平原农业环境重点实验室, 南京 210014
2. Institute of Agricultural Science and Environment, Jiangsu Academy of Agricultural Sciences, Key Lab of Agri-environment in Downsteam of Yangtze Plain, Ministry of Agriculture, Nanjing 210014
近20来, 随着我国工业和农业的迅速发展, 大量磷随着生活污水、工业废水的排放和农田磷肥的使用而进入水体, 引起水体富营养化, 对水生生态环境和人类健康产生重大危害.因此, 为了保护水体生态平衡和人类健康, 发展低能、高效的除磷技术对缓解水体富营养化至关重要(Li et al., 2014;孙丽华等, 2016).
目前, 水体除磷方法主要有化学沉淀法、生物法、反渗透法、吸附法等(Zamparas et al., 2013;Saad et al., 2007;Ma et al., 2011;吴文清等, 2012;林建伟等, 2015).化学沉淀法虽然工艺简单, 但产生大量难处理的污泥难以达到排放标准.生物法运行周期长, 操作严格, 菌种稳定性差.反渗透法操作成本高.吸附法由于其高效、低耗、稳定性好、易操作、没有二次污染物生成等特点被认为是去除磷的有效方法(Zhao et al., 1998;Özacar et al., 2003;Hano et al., 1997;石中亮等, 2011), 而且通过吸附-脱附过程可从废水中回收磷, 从而部分解决天然磷矿储量耗尽导致未来磷资源稀缺的问题.常见的吸附剂有氧化铝(Shin et al., 1996;于清泉等, 2016)、活性炭(陈翠玲等, 1996)、沸石(肖举强等, 2003)等, 但这些吸附剂投入使用后很难回收利用.纳米四氧化三铁在近几十年来受到了很大的关注, 纳米四氧化三铁除了具有一般的纳米材料所具有的纳米效应以外, 还具有超顺磁性, 在外加磁场的作用下, 很容易实现固液分离(丁程程等, 2011;Chen et al., 2011;Zach-Maor et al., 2011;Zachmaor et al., 2011;詹艳慧等, 2013), 适用于水污染治理中的大面积动态吸附(Uheida et al., 2016;Wong et al., 2007).
但纳米四氧化三铁粒子间由于磁性偶极矩相互吸引, 在水溶液中容易发生团聚, 导致比表面积减少、吸附活性位点降低、吸附能力下降.丁程程等(2011)、Lai等(2016)的实验结果均显示单纯的纳米四氧化三铁由于团聚导致吸附磷的效率较低.为了减小纳米四氧化三铁颗粒的团聚, 通常对纳米四氧化三铁进行表面修饰, 提高其稳定性和吸附性能.常见的修饰材料包括天然矿物和有机高分子材料, 如SiO2、ZrO2、聚乙烯醇、聚乙二醇等.提高纳米四氧化三铁吸附磷的效率, 研究最多的都是从提高纳米四氧化三铁分散性出发, 从其表面电荷方面分析较少.本研究不仅从提高纳米四氧化三铁的分散性出发, 还考虑增加其表面正电荷, 使得纳米四氧化三铁表现出优异的吸附性能.
磷在水中显负电, 选择正电性的改性剂来改性四氧化三铁, 能够通过强化静电吸引作用促进对磷的吸附.本文采用聚乙烯亚胺作为改性剂, 是因为聚乙烯亚胺是现存材料中拥有最高阳离子密度(张伟等, 2007)的高分子聚合物, 用聚乙烯亚胺来改性纳米四氧化三铁, 不仅能够提高四氧化三铁颗粒的分散性, 还能使四氧化三铁表面带有丰富的正电荷.目前, 国内外用聚乙烯亚胺来改性四氧化三铁的研究主要是作为基因载体, 多数在四氧化三铁生成后再对其改性, 这种改性方法反应时间长(李成奎等, 2010), 且颗粒分散性一般(蔡元元等, 2010).本文将Jian等(2008)的方法进行改进, 将聚乙烯亚胺与前驱体铁盐混合, 通过化学共沉淀法制备出聚乙烯亚胺改性的纳米四氧化三铁复合材料, 该种方法耗时短, 颗粒分散性好.实验研究了复合材料对水体中磷的去除性能, 探讨了此复合材料去除磷的机制, 为纳米四氧化三铁聚合物复合材料的制备和应用提供了研究基础.
2 材料与方法(Materials and methods) 2.1 实验材料六水合三氯化铁(分析纯, ≥99%)购自国药集团化学试剂有限公司;七水合硫酸亚铁(分析纯, ≥99%)购自南京化学试剂有限公司;聚乙烯亚胺(M, W, 10000, 99%)购自阿拉丁集团;氨水(NH3, 分析纯, ω%, 25%~28%)购自南京化学试剂;磷酸二氢钾(分析纯, 99.5%)购自南京化学试剂;钼酸铵(分析纯, 99%)购自天津市科密欧化学试剂;酒石酸锑钾(分析纯, 99%)购自西陇化工股份有限公司;抗坏血酸(分析纯, 99.7%)购自国药集团.
2.2 实验方法 2.2.1 聚乙烯亚胺改性纳米四氧化三铁复合材料(Fe3O4/PEI)的制备Fe3O4/PEI采用化学共沉淀法(Feyzi et al., 2016;Jian et al., 2008)制备, 具体步骤如下:量取250 mL去离子水于500 mL三口烧瓶里, 在室温下通氮气30 min排尽烧瓶里的空气.称量5.7525 g FeCl3·6H2O和2.9616 g FeSO4·7H2O于烧瓶里, 机械搅拌30 min, 继续通氮气.称取1.0 g左右PEI溶解在50 mL去离子水中, 用恒流泵将PEI溶液缓慢加入到铁盐溶液中, 在室温下机械搅拌1 h.向三口烧瓶里滴加30 mL浓氨水, 有黑色沉淀生成, 在60 ℃水浴锅继续通氮气反应2 h.冷却至室温, 用去离子水洗涤3次, 无水乙醇洗涤3次, 在真空干燥箱干燥12 h.
纳米Fe3O4亦是通过化学共沉淀法(Feyzi et al., 2016)制备, 步骤同Fe3O4/PEI.
2.2.2 磷的吸附实验用磷酸二氢钾配制含磷溶液(以P计), 用1 mol·L-1 NaOH和1 mol·L-1 HCl调节pH.量取100 mL含磷溶液(10、20、50、75、100 mg·L-1)于150 mL锥形瓶里, 加入Fe3O4/PEI复合材料, 密封后置于恒温振荡箱中, 在25 ℃, 210 r·min-1转速下振荡, 定时取样(0、15、30、45、60、90、120、150、180 min), 用0.22 μm微孔滤膜过滤, 用钼锑抗分光光度法测定磷酸根的浓度.所有反应设置3个平行实验.在此过程中, 考察溶液pH值、吸附剂投加量和磷初始浓度对吸附磷效率的影响.η=(C0-C)/C0, 其中,η是吸附效率, C0是磷的初始浓度, c是任意t时刻磷的浓度.
2.2.3 磷的解析实验解析实验在不同pH下进行, 用1 mol·L-1NaOH和HCl调节.将吸附后的Fe3O4/PEI投入到100 mL不同pH的水溶液中, 在25 ℃恒温振荡箱里以210 r·min-1转速振荡, 定时取样, 直至达到解析平衡.用钼锑抗分光光度法测定磷的浓度.所有反应均设置3个平行.在此过程中, 考察溶液pH值对解析磷效率的影响.
2.2.4 表征与分析采用德国Bruker公司的D2PHASER型X射线衍射仪(XRD)分析Fe3O4/PEI的晶型结构.采用荷兰Philips公司的Tecnai 12型的透射电子显微镜(TEM)观察Fe3O4/PEI的形貌大小.采用美国Thermo Scientific公司的NicoletS10型的傅里叶红外光谱仪测定Fe3O4/PEI的特征官能团.采用英国马尔文公司的Zetasizer Nano Zs90型电位仪测定Fe3O4/PEI表面电荷.采用日本岛津的UV-2600型紫外分光光度仪测定磷的浓度.采用S ΙΙ NanoTechnology Ιnc公司的EXSTAR series TG/DTA7200型Thermogravimetry/Differential Thermal Analyzer来测定聚乙烯亚胺的负载量.
3 结果(Results) 3.1 聚乙烯亚胺改性纳米四氧化三铁的表征 3.1.1 XRD表征分析图 1是纯Fe3O4和Fe3O4/PEI的XRD图谱, 衍射角为15°~80°.图中出现Fe3O4的6个特征吸收峰(2θ=30.1°、35.5°、43.1°、53.4°、57.0°、62.6°), 分别对应Fe3O4的6个晶面(220)、(311)、(400)、(422)、(511)、(440).图中未出现其他杂质峰, 说明结晶质量良好, 与Fe3O4标准图谱一致, 说明本实验所制备的Fe3O4/PEI为尖晶石型(Lin et al., 2013).聚乙烯亚胺改性的Fe3O4的特征衍射峰与纯的Fe3O4几乎一致, 表明聚乙烯亚胺作为改性剂对Fe3O4晶型未产生影响.
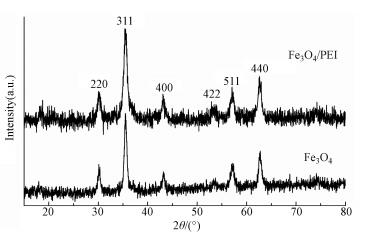 |
| 图 1 Fe3O4和Fe3O4/PEI的XRD图谱 Fig. 1 XRD pattern of the Fe3O4 and Fe3O4/PEI |
图 2是纯Fe3O4与Fe3O4/PEI的透射电镜(TEM)图, 从图中可知, 纯Fe3O4与Fe3O4/PEI颗粒均呈类球状.由图 2a可知, 单纯的Fe3O4颗粒之间团聚很严重, 粒径在20 nm左右.从图 2b可看出Fe3O4/PEI颗粒之间分散较好, 没有发生团聚现象, 且粒径较Fe3O4颗粒小, 在5~15 nm之间.是因为PEI包覆在Fe3O4表面, 空间位阻效应和电荷排斥作用变大, 足以克服磁性粒子之间的范德华力和磁性引力, 从而提高了纳米粒子的分散性(张伟等, 2007)
 |
| 图 2 Fe3O4 (a)与Fe3O4/PEI (b)的透射电镜图 Fig. 2 Transmission electron micrograph of Fe3O4 (a) and Fe3O4/PEI (b) |
图 3是Fe3O4、PEI、Fe3O4/PEI和Fe3O4/PEI-磷红外图谱.与纯Fe3O4相比, Fe3O4/PEI出现了位于2822、1570、1294 cm-1的3个新的特征吸收峰, 2822 cm-1归属于亚甲基的C—H键的伸缩振动峰.1570 cm-1归属于N—H键的面内弯曲振动峰.1294 cm-1归属于C—N键的伸缩振动峰.这些特征吸收峰表明聚乙烯亚胺成功包覆于四氧化三铁表面, 聚乙烯亚胺与四氧化三铁之间可能形成了配位键.Fe3O4/PEI-磷出现了1048 cm-1新的特征吸收峰, 1048 cm-1归属于P—O键伸缩振动峰(Liu et al., 2014;Yin et al., 2010), 说明磷成功吸附在Fe3O4/PEI表面.
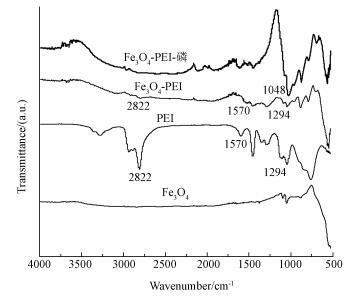 |
| 图 3 Fe3O4、PEI和Fe3O4/PEI的红外光谱 Fig. 3 The FTIR spectra of Fe3O4、PEI and Fe3O4/PEI |
图 4是Fe3O4和Fe3O4/PEI的热重图.用热失重TG测定聚乙烯亚胺的含量(李成奎等, 2010).从图中可知, Fe3O4发生一次失重, 在80~150 ℃失去的是其表面未蒸干的水分, 失重为1.5%.Fe3O4/PEI发生两次失重, 分别在80~150 ℃和200~560 ℃, 在80~150 ℃失去的是Fe3O4/PEI表面未蒸干的水分, 失重为2.5%.在200~560 ℃失去的是聚乙烯亚胺, 聚乙烯亚胺在200~560 ℃发生分解, 失重为17.5%.在560 ℃以后没有失重现象, 表明Fe3O4/PEI表面的水分及聚乙烯亚胺已经分解完全.热重分析图表明, 用化学共沉淀法制备的Fe3O4/PEI复合材料含17.5%的聚乙烯亚胺.
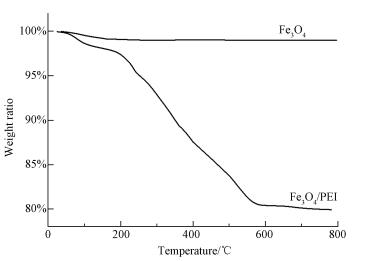 |
| 图 4 Fe3O4/PEI热重分析图 Fig. 4 Thermogravimetric analysis graph of Fe3O4/PEI |
图 5是Fe3O4和Fe3O4/PEI在不同pH下的Zeta电位值.裸Fe3O4的等电点在pH=6.5左右(汤智等, 2015), 当pH小于6.5时表面带正电荷, 当pH大于6.5时表面带负电荷.在碱性条件下, Fe3O4表面电荷为负值.由图 5可知, 在pH 2~9时, Fe3O4/PEI的Zeta电位均为正值, 尤其在碱性条件下仍为正, 说明聚乙烯亚胺已经很好的包覆在四氧化三铁表面, 使得材料表面的正电荷增加, 从而有利于对磷酸根的吸附.在酸性条件下, Fe3O4和Fe3O4/PEI均有部分铁离子溶出, 在pH 2、3、5、7时, Fe3O4和Fe3O4/PEI溶出的铁离子质量比分别为:0.9%、0.006%、0.002%、0.001%和0.55%、0.003%、0.001%、0, 说明Fe3O4/PEI较Fe3O4在酸性条件下稳定.随着pH的增加, Fe3O4/PEI的Zeta电位降低是因为聚乙烯亚胺在四氧化三铁表面发生了水解(张伟等, 2007), 当溶液pH增加时, 反应利于向左边进行, 从而降低Fe3O4/PEI表面电位:
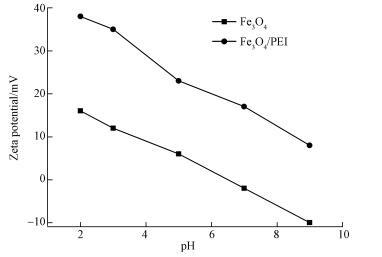 |
| 图 5 Fe3O4和Fe3O4/PEI Zeta电位随pH变化 Fig. 5 Zeta potential of Fe3O4 and Fe3O4/PEI varied with pH |

|
(1) |
研究纳米Fe3O4、PEI和复合材料Fe3O4/PEI吸附磷效率的差异.取200 mg Fe3O4、35 mg PEI和200 mg Fe3O4/PEI, 分别加入100 mL的50 mg·L-1磷溶液, 空白实验为不添加任何吸附剂.在pH=3, 温度为25 ℃, 转速为210 r·min-1下, 反应3 h, 测定磷的浓度, 结果如图 6所示.由图 6可知, PEI对磷酸根有25%的吸附效率, 是因为PEI在水溶液里呈正电性, 通过静电吸引吸附磷酸根.Fe3O4对磷的吸附效率为75%, 而Fe3O4/PEI达到91%, 一方面是因为PEI修饰后的Fe3O4分散均匀, 活性位点多于团聚的Fe3O4, 另一方面是因为PEI修饰使得Fe3O4表面正电荷增加, 对磷酸根静电引力增强, 进而提高吸附效率.
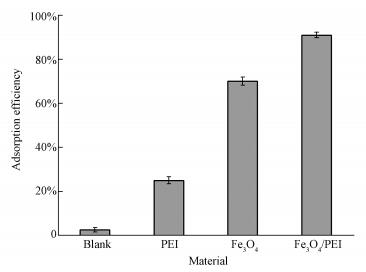 |
| 图 6 不同材料对吸附磷的影响 Fig. 6 The adsorption performance of different materials on of phosphate |
在磷初始浓度为50 mg·L-1, 温度为25 ℃, 转速为210 r·min-1下, 考察在不同pH(2、3、5、7、9)磷溶液中, 200 mg Fe3O4/PEI复合材料对磷的吸附情况, 结果如图 7a所示.由图可知, Fe3O4/PEI对磷的吸附受pH值影响明显, 随着pH值的增大, Fe3O4/PEI对磷的吸附效率降低.在溶液pH值为3、5、7、9时, 磷的主要形式是H2PO4-和H2PO42-.溶液的pH值决定四氧化三铁表面的胺基被质子化的程度, 质子化的胺基可以吸附磷酸根.Fe3O4/PEI对磷酸根的吸附随着pH值的增加而降低是因为Fe3O4/PEI表面的胺基在更高的pH值下较难被质子化, 所以Fe3O4/PEI表面所带的正电荷随着pH的增加慢慢趋于中性, 所以Fe3O4/PEI对磷酸根的静电吸引力减弱, 对磷的吸附效率降低.在pH=2时, 虽然胺基更容易质子化, 但磷的主要形式是中性的H3PO4和负一价的H2POO4-, 质子化的胺基不能吸引中性的H3PO4, 导致Fe3O4/PEI在pH=2时吸附磷的效率不是很高(Lin et al., 2013).因此, Fe3O4/PEI吸附磷酸根的最佳pH为3, 吸附效率达91%.
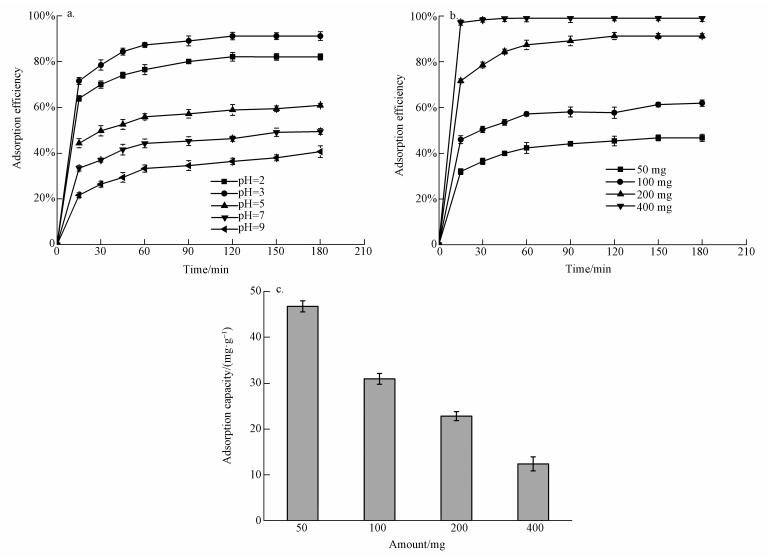 |
| 图 7 pH(a)、Fe3O4/PEI投加量对吸附率(b)和吸附量(c)的影响 Fig. 7 Effect of pH(a), Fe3O4/PEI dosage on adsorption efficiency(b) and adsorption capacity(c) of phosphate |
在磷初始浓度为50 mg·L-1, pH=3, 温度为25 ℃, 转速为210 r·min-1下, 考察投加量(50、100、200、400 mg)对Fe3O4/PEI复合材料吸附磷的影响, 结果如图 8b和8c所示.由图可知, 吸附效率随着投加量的增加而增加, 这是因为在一定磷浓度下, 投加量越大, 吸附材料比表面积越大, 表面可供利用的吸附活性位点越多, 吸附效率就越高的原因.Fe3O4/PEI复合材料对磷的吸附量随着Fe3O4/PEI投加量的增加而降低, 这是因为随着Fe3O4/PEI投加量的增加, 单位质量吸附材料表面空闲的吸附活性位点就越多.当投加量为200 mg时吸附效率达到91%, 吸附反应几乎达到完全, 而投加量增加至400 mg时吸附效率为98%, 说明单纯的增加投加量并没有太大的增加吸附效率, 所以从吸附效率和经济效益考虑, 最佳投加量为200 mg.
3.2.4 磷初始浓度对Fe3O4/PEI吸附磷的影响设置磷的浓度为10~100 mg·L-1(10、20、50、75、100), 在pH=3, 温度为25 ℃, 转速为210 r·min-1条件下, 考察磷初始浓度对200 mg Fe3O4/PEI复合材料吸附磷的影响, 结果如图 8所示.由图可知, 随着磷初始浓度的增加, Fe3O4/PEI吸附磷的效率降低, 而吸附量却在增大.这是因为一定量Fe3O4/PEI吸附材料的表面活性位点是一定的, 随着磷初始浓度的增加, 在吸附过程中, Fe3O4/PEI表面活性位点逐渐被占据直至达到饱和状态, 因此吸附效率降低而吸附量却相应增大.在浓度为10 mg·L-1时吸附效率达到最大, 为91%, 在浓度为100 mg·L-1时吸附量达到最大, 为30 mg·g-1.
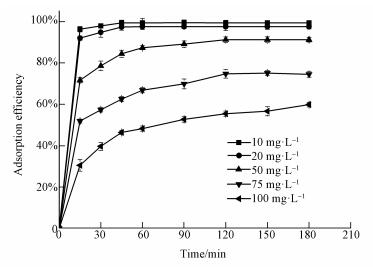 |
| 图 8 磷初始浓度对吸附率影响 Fig. 8 Effect of phosphate initial concentration on adsorption efficiency a of phosphate |
称量200 mg Fe3O4/PEI吸附剂, 投入到100 mL浓度为50 mg·L-1的磷酸溶液, 分别加入50 mg·L-1的Cl-、HCO3-、SO42-、NO3-溶液和50 mg·L-1的腐殖酸、脂肪酸、硝基酚、氨基酸进行磷酸根的吸附实验.在pH为3的条件下研究共存离子和天然有机物对Fe3O4/PEI吸附磷酸根的影响, 结果如表 1所示.
| 表 1 共存离子和共存有机物对Fe3O4/PEI吸附磷的影响 Table 1 The effect of competing anions and organics on adsorption of phosphate by Fe3O4/PEI |
由表 1可知, 加入共存离子Cl-、HCO3-、SO42-、NO3-使得Fe3O4/PEI吸附磷的效率有所降低, 吸附效率降低是因为带正电的Fe3O4/PEI与共存阴离子产生了静电引力, 减弱了与磷酸根的静电引力, 从而降低吸附磷的效率.共存天然有机物对磷的去除影响较小, 说明共存有机物没有与磷竞争吸附活性位点.
3.2.6 离子强度对Fe3O4/PEI吸附磷的影响分别用0.05、0.1、0.5、1.0 mol·L-1 NaCl溶液配制50 mg·L-1的磷酸溶液, 投入200 mg Fe3O4/PEI吸附剂, 在pH为3的条件下考察离子强度对Fe3O4/PEI吸附磷酸根的影响, 结果如表 2所示.
| 表 2 离子强度对Fe3O4/PEI吸附磷的影响 Table 2 The effect of ionic strength on adsorption of phosphate by Fe3O4/PEI |
由表 2可看出, 离子强度对Fe3O4/PEI去除磷的影响不大, 离子强度越强, Fe3O4/PEI吸附磷的效率略有降低, 是因为Cl-浓度增大, Fe3O4/PEI对Cl-静电引力增强, 对磷酸根的静电引力减弱.离子强度达到一定程度时, Fe3O4/PEI对Cl-静电引力达到饱和, 对磷酸根的吸附效率也达到稳定.
3.2.7 反应动力学研究准二级动力学模型是一种描述物理化学反应常用的模型, 见式(2).
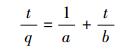
|
(2) |
式中, q为吸附量(mg·L-1), t为反应时间(min), a、b均为常数.
利用准二级动力学方程, 对磷的吸附量数据进行拟合.结果如图 9a所示.由图可知, 准二级动力学方程能够较好的描述磷的吸附反应进程.Fe3O4/PEI对磷的吸附是由表面反应过程控制, 不是吸附质扩散过程控制.斜率1/b随着初始浓度的增大而降低, 表明反应速率随着浓度的增加而降低.当浓度为10 mg·L-1和20 mg·L-1时, 斜率分别为0.20和0.11, 而当浓度增加到50 mg·L-1以上时, 斜率降到0.04以下.可能是因为在较高浓度下, Fe3O4/PEI吸附材料吸附磷的能力快要接近饱和, 此时吸附材料的投加量是反应速率的控制条件, 因此吸附反应速率随着浓度的增加而降低.
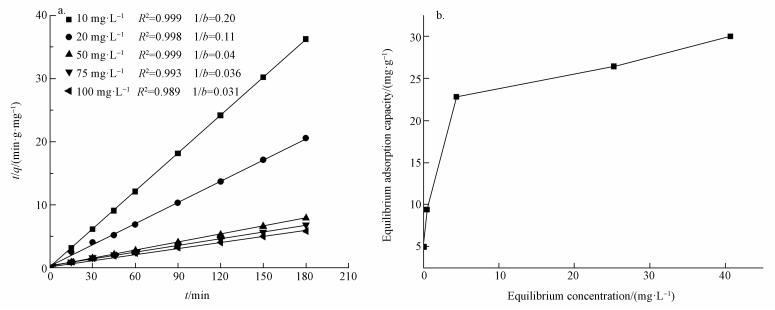 |
| 图 9 Fe3O4/PEI吸附磷准二级反应动力学(a)和吸附等温线(b)拟合曲线 Fig. 9 Plots of pseudo-second-order kinetics(a) and adsorption isotherms(b) of phosphate removal by Fe3O4/PEI |
在pH=3, 温度为25 ℃, 对浓度为10、20、50、75、100 mg·L-1的磷溶液进行吸附实验, Fe3O4/PEI对磷的吸附等温线如图 9b所示.由图可知, Fe3O4/PEI对磷的吸附量随着磷平衡浓度的增加而增加.选用Langmuir和Freundlich两种等温吸附方程对图 9b的数据进行拟合.Langmuir吸附等温线方程如下:
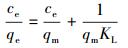
|
(3) |
式中, ce为平衡时磷的浓度(mg·L-1), qe和qm为平衡时吸附量和最大吸附量(mg·L-1), KL是吸附能力常数(L·mg-1), 代表着吸附能力的强弱.
Freundlich吸附等温线方程如下:
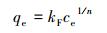
|
(4) |
直线方程式可表示为:
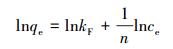
|
(5) |
式中, qe和ce定义如上, kF是Freundlich常数(L·mg-1), n是异质因子.Langmuir和Freundlich两种等温吸附模型拟合出的具体参数值见表 3.
| 表 3 Fe3O4/PEI吸附磷热力学参数 Table 3 Thermodynamic parameters of phosphate adsorption on Fe3O4/PEI |
从表 3可看出, Fe3O4/PEI对磷的吸附更符合Langmuir吸附等温模型, 该模型的R2为0.993, 最大吸附量为29.88 mg·L-1.
3.2.9 解析与重复利用性吸附剂具有较好的解析性能在实际应用中是很重要的.如上图 7a所示, Fe3O4/PEI复合材料对磷的吸附效率随着pH的增加而降低, 很有可能是因为被吸附的磷在较高的pH下发生了解析.图 10是磷在不同pH下的解析效率.
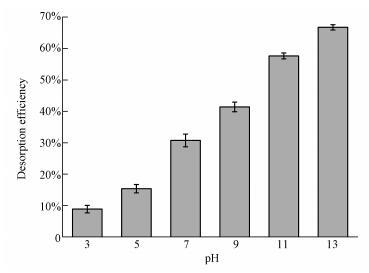 |
| 图 10 不同pH下磷的解析效率 Fig. 10 Desorption efficiency of phosphate from the Fe3O4/PEI with different pH |
由图可知, 随着pH的增加, 磷的解析效率增加, 在pH=13时, 解析效率达到65%, 在较低pH下, 吸附效率只有12%.
在pH 3~7, -NH2易发生质子化.质子化的(Fe3O4)-NH3+利于通过静电吸引吸附带负点的磷酸根, 酸性越强, 质子化程度越高, 越不利于磷酸根的解析.
在pH 7~9, OH-浓度逐渐增大, 争夺质子化(Fe3O4)-NH3+的H+, 使得质子化的(Fe3O4)-NH3+慢慢趋于中性(Fe3O4)-NH2, 对磷酸根的静电吸引减弱, 导致磷酸根解析效率增加.
在pH 9~13, OH-浓度继续增大, 争夺-NH2上的H, 使得中性(Fe3O4)-NH2变成带负电的(Fe3O4)-NH-, (Fe3O4)-NH-通过静电排斥, 促进磷酸根在Fe3O4/PEI表面发生解析.
为了考察Fe3O4/PEI复合材料吸附磷的重复性, 吸附-解析实验重复进行5次.设置实验条件:在100 mL 50 mg·L-1磷溶液, pH=3, 温度为25 ℃, 转速为210 r·min-1条件下, 加入200 mg Fe3O4/PEI复合材料, 反应3 h后, 测定上清液浓度并将其过滤掉, 用1.0 mol·L-1NaOH溶液将吸附剂进行解析.再加入新鲜的100 mL 50 mg·L-1磷溶液, 按照上述实验条件重复进行5次, 结果如图 11所示.由图可知, 吸附剂在第5次利用时吸附效率还能保持75%, 说明Fe3O4/PEI吸附剂活性稳定, 重复利用性强.
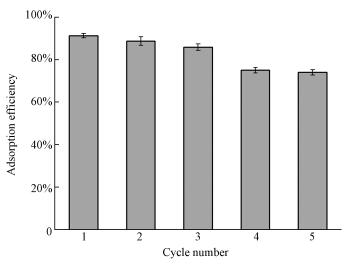 |
| 图 11 Fe3O4/PEI重复利用性 Fig. 11 Reusability of Fe3O4/PEI on adsorption of phosphate |
采用1.0 mol·L-1NaOH溶液对吸附磷饱和后的Fe3O4/PEI复合材料进行再生, 结果显示有80%左右被吸附在Fe3O4/PEI复合材料上的磷被脱附下来.说明1.0 mol·L-1NaOH溶液可以较好的实现吸附磷饱和后的Fe3O4/PEI材料进行再生.
3.2.11 Fe3O4/PEI复合材料与磷的吸附机理Zeta电位结果显示Fe3O4/PEI复合材料表面带正电, 它与带负电的磷酸根之间存在一定的静电引力.Fe3O4/PEI复合材料吸附磷的效率随着pH的增加而降低这一趋势说明Fe3O4/PEI与磷的吸附机制是静电吸引, 与文献(詹艳慧等, 2013)报道Fe3O4吸附磷的机制一致.Fe3O4/PEI比表面积大, 表面能高, 红外表征显示Fe3O4/PEI-磷出现了P—O键的特征吸收峰, 说明Fe3O4/PEI与磷之间是化学吸附.已有文献(Zach-Maor et al., 2011)报道, Fe3O4吸附磷的机制是Fe3O4与磷的配位体交换.配位体交换方式如图 12所示.所以Fe3O4/PEI复合材料吸附磷的机制既有静电吸引又有配位体交换.
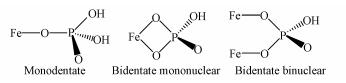 |
| 图 12 磷与Fe3O4/PEI可能的结合方式 Fig. 12 Possible formation mechanism of phosphate surface complexes |
1) 以PEI为改性剂, 通过化学共沉淀法制备出Fe3O4/PEI复合材料, 通过TEM测试表征可知, 该种方法制备出来的Fe3O4/PEI复合材料呈类球形, 颗粒之间分散较好, 粒径在5~20 nm.
2) FTIR和Zeta电位测试结果表明, PEI成功负载在Fe3O4上, PEI与Fe3O4形成了配位键, 改性后的Fe3O4表面带有丰富的正电荷.热重测试分析结果显示有17.5%的PEI负载在Fe3O4表面.
3) Fe3O4/PEI复合材料吸附磷受pH影响较大, 吸附效率随着pH的增加而降低, 在pH=3时吸附效率最好, 达到91%.Fe3O4/PEI对磷的吸附行为符合Langmuir吸附等温线.Fe3O4/PEI对磷的吸附是个快速反应过程, 反应在3 h内基本完成.同时, 准二级动力学模型也能很好的解释磷吸附动力学过程.
4) 解析磷的最佳条件是在强碱性溶液里, 在pH=13时, 磷的解析效率能达到65%左右.改性后的Fe3O4在第5次重复利用后还能保持75%以上的较高效率, 说明改性后的Fe3O4重复利用性好.
蔡元元, 高福平, 周晶, 等. 2010. PEI修饰磁性Fe3O4纳米粒的制备和表征[J]. 科技导报, 2010, 28(19): 68–72.
|
Chen B, Chen Z, Lv S. 2011. A novel magnetic biochar efficiently sorbs organic pollutants and phosphate[J]. Bioresource Technology, 102(2): 716–723.
DOI:10.1016/j.biortech.2010.08.067
|
陈翠玲, 蒋爱凤, 阴云剑, 等. 1996. 活性炭对磷吸附作用的研究[J]. 河南科技学院学报(自然科学版), 1996, 24(4): 19–22.
|
丁程程, 潘纲, 张美一. 2011. 淀粉改性纳米四氧化三铁的制备及其除磷效能的研究[J]. 环境工程学报, 2011, 5(10): 2167–2172.
|
Feyzi M, Norouzi L. 2016. Preparation and kinetic study of magnetic Ca/Fe3O4@SiO2 nanocatalysts for biodiesel production[J]. Renewable Energy, 94: 579–586.
DOI:10.1016/j.renene.2016.03.086
|
Hano T, Takanashi H, Hirata M, et al. 1997. Removal of phosphorus from wastewater by activated alumina adsorbent[J]. Water Science & Technology, 35(7): 39–46.
|
Jian P, Zou F, Lu L, et al. 2008. Preparation and characterization of PEG-PEI/Fe3O4 nano-magnetic fluid by co-precipitation method[J]. Transactions of Nonferrous Metals Society of China, 18(2): 393–398.
DOI:10.1016/S1003-6326(08)60069-2
|
李成魁, 严彪, 杜春风, 等. 2010. PEI包覆磁性Fe3O4纳米颗粒的制备及性能研究[J]. 金属功能材料, 2010, 17(4): 41–44.
|
Li G, Gao S, Zhang G, et al. 2014. Enhanced adsorption of phosphate from aqueous solution by nanostructured ron(Ⅲ)-copper(Ⅱ) binary oxides[J]. Chemical Engineering Journal, 235(1): 124–131.
|
Lai L, Xie Q, Chi L, et al. 2016. Adsorption of phosphate from water by easily separable Fe3O4@SiO2 core/shell magnetic nanoparticles functionalized with hydrous lanthanum oxide[J]. Journal of Colloid & Interface Science, 465: 76–82.
|
Lin Y F, Chen H W, Chen Y C, et al. 2013. Application of magnetite modified with polyacrylamide to adsorb phosphate in aqueous solution[J]. Journal of the Taiwan Institute of Chemical Engineers, 44: 45–51.
DOI:10.1016/j.jtice.2012.09.005
|
林建伟, 方巧, 詹艳慧. 2015. 镧-四氧化三铁-沸石复合材料制备及去除水中磷酸盐和铵[J]. 环境化学, 2015, 34(12): 2287–2297.
DOI:10.7524/j.issn.0254-6108.2015.12.2015031905 |
Liu F, Yang J, Zuo J, et al. 2014. Graphene-supported nanoscale zero-valent iron: removal of phosphorus from aqueous solution and mechanistic study[J]. Journal of Environmental Sciences, 26(8): 1751–1762.
DOI:10.1016/j.jes.2014.06.016
|
Ma Z, Li Q, Yue Q, et al. 2011. Adsorption removal of ammonium and phosphate from water by fertilizer controlled release agent prepared from wheat straw[J]. Chemical Engineering Journal, 171(3): 1209–1217.
DOI:10.1016/j.cej.2011.05.027
|
ÖzacarM. 2003. Adsorption of phosphate from aqueous solution onto alunite[J]. Chemosphere, 2003, 51(4): 321–327.
|
Saad R, Belkacemi K, Hamoudi S. 2007. Adsorption of phosphate and nitrate anions on ammonium-functionalized MCM-48: effects of experimental conditions[J]. Journal of Colloid & Interface Science, 311(2): 375–381.
|
石中亮, 宋永强, 郭星, 等. 2011. 磁性多孔Fe(OH)3微球制备及其在含磷废水处理中的应用[J]. 过程工程学报, 2011, 11(4): 684–688.
|
Shin H S, Kim M J, Nam S Y, et al. 1996. Phosphorus removal by hydrotalcite-like compounds (HTLcs)[J]. Water Science & Technology, 34(1/2): 161–168.
|
孙丽华, 田海龙, 段茜, 等. 2016. 3种含铁吸附剂对水中磷酸盐的吸附性能[J]. 水处理技术, 2016, 42(1): 45–48.
|
汤智, 赵晓丽, 吴丰昌, 等. 2015. 不同来源腐殖酸在纳米四氧化三铁上的吸附及对其沉降性的影响[J]. 环境化学, 2015, 34(8): 1520–1528.
DOI:10.7524/j.issn.0254-6108.2015.08.2015013005 |
Uheida A, Salazaralvarez G, Björkman E, et al. 2006. Fe3O4 and gamma-Fe2O3 nanoparticles for the adsorption of Co2+ from aqueous solution[J]. Journal of Colloid & Interface Science, 298(2): 501–507.
|
Wong K S, Wong K H, Ng S, et al. 2007. Adsorption of copper ion on magnetite-immobilised chitin[J]. Water Science & Technology A Journal of the International Association on Water Pollution Research, 56(7): 135–143.
|
吴文清, 黄少斌, 张瑞峰, 等. 2012. 一种新型改性吸附剂对水中痕量磷的吸附特征[J]. 中国环境科学, 2012, 32(11): 1991–1998.
DOI:10.3969/j.issn.1000-6923.2012.11.010 |
肖举强, 李玉金, 郑辉. 2003. 沸石除磷性能研究[J]. 环境研究与监测, 2003, 16(3): 252–254.
|
修瑞瑞, 何世颖, 宋海亮, 等. 2016. 改性硅藻土负载纳米零价铁去除水中硝酸盐氮[J]. 化工学报, 2016, 67(9): 3888–3894.
|
Yin Y, Zhang H, Wu P, et al. 2010. Iron phosphate nanostructures synthesized by microwave method and their applications in biosensing[J]. Nanotechnology, 21(42): 80–83.
|
于清泉. 2016. 大比表面积氧化铝吸附剂的制备及其对水中六价铬的去除[D]. 北京: 北京化工大学
http://cdmd.cnki.com.cn/Article/CDMD-10010-1016323318.htm |
Zach-Maor A, Semiat R, Shemer H. 2011. Adsorption-desorption mechanism of phosphate by immobilized nano-sized magnetite layer: interface and bulk interactions[J]. Journal of Colloid & Interface Science, 363(2): 608–614.
|
Zachmaor A, Semiat R, Shemer H. 2011. Synthesis, performance, and modeling of immobilized nano-sized magnetite layer for phosphate removal[J]. Journal of Colloid & Interface Science, 357(2): 440–446.
|
Zamparas M, Drosos M, Georgiou Y, et al. 2013. A novel bentonite-humic acid composite material Bephos for removal of phosphate and ammonium from eutrophic waters[J]. Chemical Engineering Journal, 225: 43–51.
DOI:10.1016/j.cej.2013.03.064
|
Zhao D, Sengupta A K. 1998. Ultimate removal of phosphate from wastewater using a new class of polymeric ion exchangers[J]. Water Research, 32(5): 1613–1625.
DOI:10.1016/S0043-1354(97)00371-0
|
詹艳慧, 林建伟, 王虹, 等. 2013. 四氧化三铁-沸石复合材料去除水中铵和磷酸盐研究[J]. 上海海洋大学学报, 2013, 22(3): 376–383.
|
张伟, 沈辉, 夏建汉, 等. 2007. 聚乙烯亚胺改性水基磁性液体的吸附特性[J]. 纳米技术与精密工程, 2007, 5(2): 125–128.
|
 2017, Vol. 37
2017, Vol. 37


