2. 南京师范大学环境学院, 南京 210023;
3. 重庆工商大学环境与生物工程学院, 重庆 400067;
4. 浙江大学苏州工业技术研究院, 苏州 215163
2. School of Environment, Nanjing Normal University, Nanjing 210023;
3. College of Environmental and Biological Engineering, Chongqing Technology and Business University, Chongqing 400067;
4. Suzhou Industrial Technology Research Institute of Zhejiang University, Suzhou 215163
稀土由于其独特的性能和广泛的应用, 已引起世界科学界、技术界的广泛关注, 被称为21世纪的战略元素, 成为新材料的发展方向(颉茂华等, 2014).在已知的稀土储量中, 中国约占世界储量的36%, 具有矿点分布合理, 稀土品位高, 矿种比较齐全等优点(赵卓等, 2013; 李梅等, 2009).稀土元素特殊的电子结构决定了其特殊的功能, 同一种结构的稀土元素可以有多种化学和物理特性.基于稀土元素在光学和电磁学上的特殊性质, 稀土已成为一种被广泛应用于新技术和新领域的材料.La是镧系元素中最轻的稀土元素, 镧系氢氧化物(La(OH)3)由于其光学、电子、磁力性质, 独特的电子结构和具有4f层的传递模型受到了越来越高的关注(Stouwdam et al., 2003; Zhuang et al., 2007; Dong et al., 2015).
半导体光催化被认为是环境治理和能源转化最有前景的技术(王怡中等, 1999; Yu et al., 2014).目前, 人们已研制了各种各样的半导体光催化剂.在丰富的半导体材料中, 发现半导体La(OH)3是一种有效的光催化剂.有文献报道了La(OH)3纳米棒在降解刚果红溶液中具有较好光催化活性(Wang et al., 2014).董等(2015)采用沉淀法制备出La(OH)3纳米棒具有较高的去除NO的光催化活性; Xiao等(2016)采用水热法制备出La(OH)3纳米棒同样具有较高的去除NO的光催化活性.文献报道的光催化剂La(OH)3其形貌均为一维纳米棒结构.而Tang等(2004)采用添加柠檬酸作为保护剂水热制备出La(OH)3纳米球.由此推测, 采用以柠檬酸作为保护剂水热制备La(OH)3纳米球理应也具备较高的光催化活性.
在本研究中, 采用La(NO3)3·6H2O和KOH作为前驱体, 以柠檬酸作为保护剂, 通过水热法制备出La(OH)3纳米球.随后通过对样品的表征和光催化活性测试, 评估柠檬酸的加入量对样品形貌及活性的影响.结果表明, 柠檬酸的量对样品的形貌及活性有较大影响.柠檬酸与La(NO3)3·6H2O的物质的量的比为2:1时, 制备的样品为形貌均匀的纳米球, 具有最高的去除NO的光催化活性, 其UV光催化活性能达到46.4%.这可能是由表面电子和空穴的有效分离作用导致的.与此同时, 提出了La(OH)3纳米球样品的光催化活性机理.更重要的是La(OH)3光催化剂所具有的光化学稳定性和耐用性对催化剂的实际应用很关键.本工作为La(OH)3纳米球光催化应用提供了新思路.
2 实验部分(Experimental) 2.1 催化剂制备本研究中所用的试剂均为分析纯.称取1.083 g(0.0025 mol)La(NO3)3·6H2O和一定量的柠檬酸于100 mL聚四氟乙烯釜中, 加入50 mL去离子水, 不停搅拌至全部溶解; 往聚四氟乙烯釜中快速加入KOH溶液(0.2 mol·L-1, 20 mL), 此时的无色溶液变成胶体; 继续磁力搅拌30 min.将得到的前驱体胶体在180 ℃下加热处理12 h, 冷却至室温后, 将所得的固体样品过滤, 用水和乙醇清洗离心4次, 并在60 ℃下烘干, 获得最终的La(OH)3样品.为了研究柠檬酸加入量对La(OH)3形貌及光催化活性的影响, 柠檬酸的加入量与La(NO3)3·6H2O的物质的量的比分别为1:1、2:1和4:1, 得到的样品分别标记为citric acid:La=1:1、citric acid:La=2:1和citric acid:La=4:1.
2.2 催化剂的表征采用X射线衍射仪(XRD: model D/max RA, Rigaku Co., 日本)分析样品的材料成分、内部原子或分子结构或形态等信息; 采用扫描电子显微镜(SEM: JEOL model JSM-6490, 日本)表征样品的形貌结构; 采用紫外-可见漫反射(UV-vis DRS: UV2450PC, SHIMADZU, 日本)和光致发光光谱(PL: F-7000, HITACHI, 日本)分析样品的光学性质.
2.3 催化剂的活性评估在室温下, 通过监测连续流反应器中μg·L-1 NO的浓度来对光催化活性进行评价.将0.2 g样品超声分散在直径为12 cm的玻璃圆盘中, 于60 ℃下烘干, 自然冷却后放入容积为4.5 L(30 cm×15 cm×10 cm)的矩形反应器中心, 反应器上面覆盖了一层石英玻璃, 以保证反应器的密闭性.一个8 W的紫外灯(280 nm)垂直安置在反应器上方20 cm处.采用标准空气和原始浓度为100 mg·L-1 NO标准气体来配置低浓度的NO.调节空气流速为2.4 L·min-1, NO气体流速为15 mL·min-1, 通过三通阀将空气流和NO气流混合, 得到初始浓度为500 μg·L-1NO.将稀释后的NO通入反应器中, 待NO浓度稳定后开灯.NOx分析仪(Thermo Scientific, 42i-TL)每隔1 min进行采样检测并记录NO、NO2及NOx(NOx包括NO和NO2)的浓度.NO的去除率(η)可用式(1)计算.
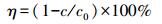
|
(1) |
式中, c代表开灯后反应器出口处的NO浓度(mg·L-1); c0代表开灯前达到吸附解吸平衡时的NO浓度(mg·L-1).
3 结果与讨论(Results and discussion) 3.1 晶体结构分析图 1为所制备样品的XRD图谱.从图中可以看出, 所有样品的衍射峰可以完全索引到La(OH)3六边晶相(JCPDS-ICDD Card No. 36-1481).没有检测到其它杂质峰, 表明所有样品均为高纯度相.值得注意的是, citric acid:La=1:1样品的结晶度比citric acid:La=2:1和citric acid:La=4:1样品高出很多, 而citric acid:La=2:1样品的结晶度比citric acid:La=4:1稍高.说明随着柠檬酸加入量的增加, 样品的衍射峰强度降低, 增加柠檬酸的量能降低样品的结晶度.从后面的SEM形貌结构分析知道, citric acid:La=1:1样品为纳米棒结构, 而citric acid:La=2:1和citric acid:La=4:1样品为纳米球结构.说明柠檬酸的加入量能改变La(OH)3形貌, 从而对结晶度有较大影响.
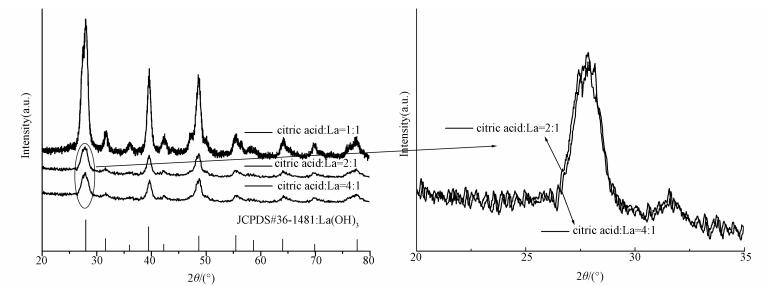 |
| 图 1 citric acid:La=1:1、citric acid:La=2:1和citric acid:La=4:1样品的XRD图谱 Fig. 1 XRD patterns ofcitric acid:La=1:1, citric acid:La=2:1 and citric acid:La=4:1 |
通过SEM对样品的形貌进行表征.图 2为citric acid:La=1:1、citric acid:La=2:1和citric acid:La=4:1的SEM图.由图可知, citric acid:La=1:1(图 2a和2b)由纳米棒和少部分纳米球构成, 纳米棒长度不一, 长度约为50~300 nm, 纳米球直径为30 nm左右.citric acid:La=2:1由形貌均匀的纳米球构成(图 2c和2d), 样品分散性好, 没有发生团聚现象, 纳米球直径为30 nm左右.citric acid:La=4:1(图 2e和2f)由纳米球构成, 且发生团聚现象, 直径长度不一, 约为15~80 nm.当柠檬酸与La(NO3)3·6H2O的物质的量的比从1:1增加至2:1时, 生成产物La(OH)3的形貌发生改变.从以一维为主的纳米棒变为形貌均匀的三维纳米球.可能的原因是柠檬酸的加入限制了La(OH)3纳米晶体沿着c轴方向生长(Tang et al., 2004), 当柠檬酸的量适中时, 即citric acid:La=2:1时, 形成形貌均匀的纳米球.当继续增加柠檬酸的量, 有部分纳米球发生团聚.以上说明柠檬酸的加入量对样品的形貌及均匀性均有较大影响.由此可以知道, 柠檬酸与La(NO3)3·6H2O的物质的量的比对La(OH)3形貌和均匀性有较大影响.柠檬酸与La(NO3)3·6H2O的物质的量的比为1:1至2:1时影响形貌, 2:1至4:1时影响均匀性.
 |
| 图 2 citric acid:La=1:1 (a, b)、citric acid:La=2:1 (c, d)和citric acid:La=4:1 (e, f)样品的SEM图 Fig. 2 SEM images of citric acid:La=1:1 (a, b), citric acid:La=2:1 (c, d)and citric acid:La=4:1 (e, f) |
PL光谱表征样品的光学性质, 可用于检测光催化过程中载流子的产生、转移和复合.图 3为所制备样品的光致发光光谱图.由图可见, 所有样品均在330~420 nm处有一个较宽的发射峰.且当柠檬酸和La(NO3)3·6H2O的物质的量的比为2:1时, 所得到的峰强度最弱.众所周知, PL发射峰强度越低, 表明电子-空穴对分离效率越高.而图中citric acid:La=2:1样品的发射峰强度低于citric acid:La=1:1, 表明改变形貌能有效降低电子-空穴对的复合率, 此外citric acid:La=2:1样品的发射峰强度低于citric acid:La=4:1, 表明纳米球形貌均匀性对载流子分离效率同样有影响, 形貌均一无团聚能增强表面电子和空穴的转移能力(Tang et al., 2013; Liang et al., 2013).因此, 柠檬酸和La(NO3)3·6H2O的物质的量的比为2:1时, PL发射峰强度越低, 电子-空穴对的分离效率越高(Dong et al., 2015).
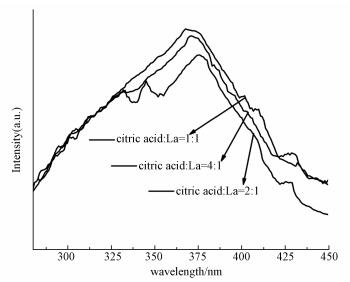 |
| 图 3 citric acid:La=1:1、citric acid:La=2:1和citric acid:La=4:1样品在室温下的PL光谱 Fig. 3 Room temperature PL spectra of citric acid:La=1:1, citric acid:La=2:1 andcitric acid:La=4:1 samples |
众所周知, 半导体的光催化活性与其光学性质有着非常密切的关系.图 4a为citric acid:La=2:1样品的紫外-可见漫反射光谱.citric acid:La=2:1的吸收边界为292 nm.通过UV-vis DRS可以计算带隙能.吸收系数(α)与入射光子能量(hv)之间的关系, 可以用以下公式表示: α=Bd(hv-Eg)1/2/hv, Bd是吸收常数.图 4b的曲线是由图 4a中的数据得来的.图 4b中曲线的切线与横轴直线相交, 交点的值就是citric acid:La=2:1带隙能的近似值.可以估算citric acid:La=2:1的带隙能为4.24 eV(Wu et al., 2009).
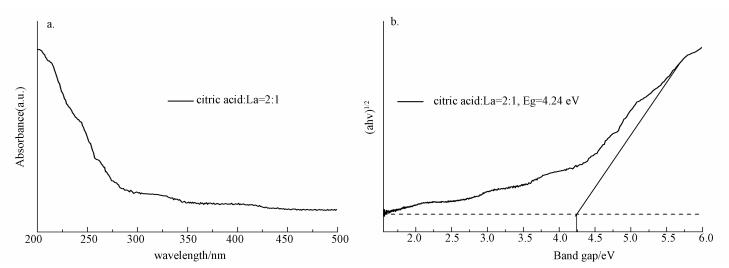 |
| 图 4 citric acid:La=2:1样品的紫外-可见漫反射光谱(a)和(αhν)1/2光子能的对比图(b) Fig. 4 UV-vis DRS (a) and plot of (αhν)1/2 versus photon energy (hν) (b) ofcitric acid:La=2:1 sample |
半导体的价带边沿电位可以通过如下经验公式计算: EVB = X-Ec + 0.5Eg, 其中X是半导体的电负性, La(OH)3的X为5.67, Ec是自由电子能, 大概为4.5 eV, Eg是带隙能(Zhang et al., 2009; Cao et al., 2013).此外, 导带势能(ECB)可以通过公式ECB = EVB-Eg确定.计算的citric acid:La=2:1导带和价带势能列于表 1中.
| 表 1 citric acid:La=2:1样品的电负性, 计算的导带位置, 新导带位置, 计算的价带位置和带隙能 Table 1 Absolute electronegativity, calculated CB edge, new CB position, calculated VB position and band gap energy for citric acid:La=2:1 at the point of zero charge |
以上面表征分析结果为基础, 在紫外光照射下, 电子-空穴对的产生和转移路径, 催化机理如图 5所示, 在UV光照射下, citric acid:La=2:1的本质带隙(4.24 eV)通过价带上的电子转移到导带产生电子-空穴对.考虑到citric acid:La=2:1的能带结构, 导带电位为-0.95 eV, 比O2/·O2-的氧化还原电位(-0.33 eV)更负, 导带电子能将O2还原成·O2-.citric acid:La=2:1价带的空穴电位为3.29 eV, 比OH-/·OH的氧化还原电位(1.99 eV)更正, 所以电子和空穴分离以后, 空穴可以将OH-氧化成·OH.·OH和·O2-是最主要的氧化物种(Dong et al., 2014).
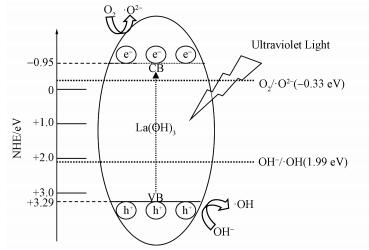 |
| 图 5 citric acid:La=2:1在紫外光照射下的光催化机理示意图 Fig. 5 Photocatalytic mechanism scheme of citric acid:La=2:1 under ultraviolet light irradiation |
基于前面的结果和分析, 在citric acid:La=2:1表面产生活性·OH和·O2-的途径如下:
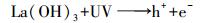
|
(2) |
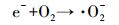
|
(3) |
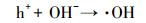
|
(4) |
NO可以和产生的·OH和·O2-反应生成HNO2和HNO3, 最后通过简单的水洗去除(Zhou et al., 2014; Li et al., 2014).包含的4个反应过程如下:
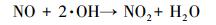
|
(5) |
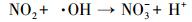
|
(6) |
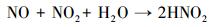
|
(7) |
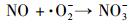
|
(8) |
为了研究样品在紫外光下对污染物的净化能力, 使用NO来评估样品的光催化性能.图 6a是样品在紫外光(280 nm)下对NO (c/c0)的去除活性图.c0是NO的初始浓度, c是NO经过光催化反应一定时间t之后的浓度.根据现有文献报道, 在没有光催化剂的帮助时, NO的去除可以忽略(Sun et al., 2017; Dong et al., 2014).经过30 min的UV光照射后, citric acid:La=1:1的NO去除率为41.6%.随着物质的量的比的升高, citric acid:La=2:1的NO去除率最佳, 达到46.4%.可能的原因是三维的纳米球结构更容易促进光生载流子的分离.当物质的量的比升高为4:1时, 样品对NO的去除率有微弱的下降, 为43.7%.可能的原因是柠檬酸加入量过多, 制备样品的过程中溶解度受到抑制, 由此导致citric acid:La=4:1的形貌不均匀, 比表面积降低, 减小的比表面积减少了催化剂表面的活性位点, 最终导致光催化活性降低.因此可以初步判断, 由于制备过程中柠檬酸的加入量而导致制备的La(OH)3材料的形貌生长方向和均一性发生了变化, 这些变化使得光催化活性有所不同, 从而柠檬酸的加入量对La(OH)3光催化剂的光催化活性有较大影响.
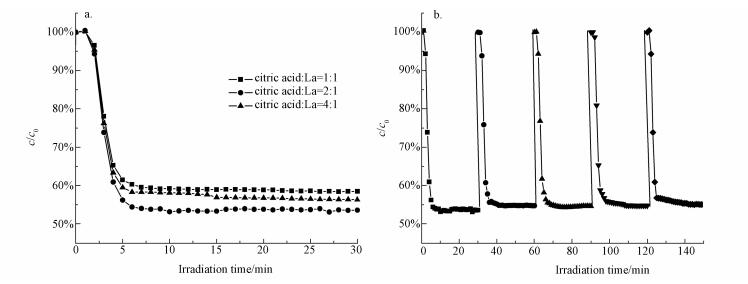 |
| 图 6 光催化剂去除空气中NO的紫外光催化活性(a)和citric acid:La=2:1循环光催化测试(b) Fig. 6 Photocatalytic oxidation of NO over the as-prepared samples (a), cycling runs of the citric acid:La=2:1 in air under UV light irradiation (b) |
光催化材料的实际应用要求其具有良好光化学稳度性.理想的光催化剂应在反复光照后仍能保持光化学稳定性和持久性(Tian et al., 2015; Xiong et al., 2015).图 6b为citric acid:La=2:1在长时间光照下的紫外光催化活性.经过5次循环以后, citric acid:La=2:1的光催化活性没有明显下降, 表明citric acid:La=2:1在光催化过程中是相对稳定的.citric acid:La=2:1的光化学稳定性归因于citric acid:La=2:1纳米球的三维结构, 能够将反应物和产物快速的转移和运输, 而不是堆积在一起, 从而有效地防止光催化剂失活.
4 结论(Conclusions)1) 本研究以La(NO3)3·6H2O和KOH作为前驱体, 以柠檬酸作为保护剂, 通过水热法制备出La(OH)3纳米球.
2) 当柠檬酸与La(NO3)3·6H2O的物质的量的比为2:1时, 制备得到的样品为形貌均匀的纳米球, 具有最佳的去除NO的光催化活性.当柠檬酸与La(NO3)3·6H2O的物质的量的比从1:1增加到2:1时, 活性明显升高, 可能的原因是三维的纳米球结构更容易促进光生载流子的分离; 继续提高摩尔比, citric acid:La=4:1活性下降, 这是因为柠檬酸加入量过多, 制备样品的过程中溶解度受到抑制, 由此导致citric acid:La=4:1样品纳米球形貌不均一, 发生团聚, 比表面积降低, 减少了催化剂表面的活性位点, 最终导致光催化活性降低.
3) 在光催化过程中, 羟基自由基(·OH)和超氧自由基(·O2-)是最主要的氧化物种.NO可以和产生的·OH和·O2-反应生成HNO2和HNO3, 最后通过简单的水洗去除.
在此之前, 尚没有已报道的文献是利用三维La(OH)3纳米球应用于光催化降解污染物.本工作不仅提供了一种简单的水热方法制备三维La(OH)3纳米球应用于光催化领域, 而且考察了形貌均匀性在促进光催化效率中的作用.本工作的实验结果为环境污染物的高效降解提供了一种新材料.
Cao J, Li X, Lin H L, et al. 2013. Surface acidetching of (BiO)2CO3 to construct (BiO)2CO3/BiOX(X=Cl, Br, I) heterostructure form ethylorange removal under visible light[J]. Applied Surface Science, 266: 294–299.
DOI:10.1016/j.apsusc.2012.11.172
|
Dong F, Li Q Y, Sun Y J, et al. 2014. Noble metal-like behavior of plasmonic bi particles as a cocatalyst deposited on (BiO)2CO3 microspheres for efficient visible light photocatalysis[J]. ACS Catalysis, 4(12): 4341–4350.
DOI:10.1021/cs501038q
|
Dong F, Wang Z Y, Li Y H, et al. 2014. Immobilizationof polymeric g-C3N4 on structured ceramic foam for efficient visible light photocatalyticair purification with real indoor illumination[J]. Environmental Science and Technology, 48(17): 10345–10353.
DOI:10.1021/es502290f
|
Dong F, Xiao X, Jiang G G, et al. 2015. Surface oxygen-vacancy induced photocatalytic activity of La(OH)3nanorods prepared by a fast and scalable method[J]. Physical Chemistry Chemical Physics, 17(24): 16058–16066.
DOI:10.1039/C5CP02460A
|
Dong F, Feng X, Zhang Y X, et al. 2015. An anion-exchange strategy for 3D hierarchical (BiO)2CO3/amorphous Bi2S3 heterostructures with increased solar absorption and enhanced visible light photocatalysis[J]. RSC Advances, 5(16): 11714–11723.
DOI:10.1039/C4RA15798B
|
李梅, 柳召刚. 2009. 稀土元素及其分析化学[M]. 北京: 化学工业出版社: 1–14.
|
Liang J, Cao Y Q, Lin H, et al. 2013. A template-free solution route for the synthesis of well-formed One-dimensional Zn2GeO4 nanocrystals and its photocatalyticbehavior[J]. Inorganic Chemistry, 52(12): 6916–6922.
DOI:10.1021/ic302698z
|
Li D, Bai X J, Xu J, et al. 2014. Synthesis of CdWO4Nanorods and investigation of the photocatalytic activity[J]. Physical Chemistry Chemical Physics, 16(1): 212–218.
DOI:10.1039/C3CP53403K
|
Stouwdam J W, Hebbink G A, Huskens J, et al. 2003. Lanthanide-doped nanoparticles with excellent luminescent properties inorganic media[J]. Chemistry of Materials, 15(24): 4604–4616.
DOI:10.1021/cm034495d
|
Sun Y J, Xiao X, Dong X A, et al. 2017. Heterostructured BiOI@La(OH)3nanorods with enhanced visible light photocatalytic NO removal[J]. Chinese Journal of Catalysis, 38(2): 217–226.
DOI:10.1016/S1872-2067(17)62753-0
|
Tang B, Ge J C, Wu C J, et al. 2004. Sol-solvothermal synthesis and microwave evolution of La(OH)3 nanorods to La2O3 nanorods[J]. Nanotechnology, 15(9): 1273–1276.
DOI:10.1088/0957-4484/15/9/027
|
Tang Z R, Yin X, Zhang Y H, et al. 2013. One-pot, high-yield synthesis of one-dimensional ZnO nanorods with well-defined morphology as a highly selective photocatalyst[J]. RSC Advances, 3(17): 5956–5965.
DOI:10.1039/c3ra40362a
|
Tian N, Huang H W, Liu C Y, et al. 2015. In situ co-pyrolysis fabrication of CeO2/g-C3N4 n-n type heterojunction for synchronously promoting photo-induced oxidation and reduction properties[J]. Journal of Materials Chemistry A, 3(33): 17120–17129.
DOI:10.1039/C5TA03669K
|
王怡中, 符雁. 1999. 二氧化钛悬浆体系太阳光催化降解甲基橙研究[J]. 环境科学学报, 1999, 19(1): 63–67.
|
Wu Z B, Don F, Liu Y, et al. 2009. Enhancement of the visible light photocatalytic performance of C-doped TiO2 by loading with V2O5[J]. Catalysis Communications, 11(2): 82–86.
DOI:10.1016/j.catcom.2009.08.015
|
Wang Y, Liu S, Cai Y, et al. 2014. La(OH)3:Ln3+ (Ln=Sm, Er, Gd, Dy, and Eu) nanorods synthesized by a facile hydrothermal method and their enhanced photocatalytic degradati on of Congored in the aqueous solution[J]. Ceramics International, 40: 5091–5095.
DOI:10.1016/j.ceramint.2013.09.119
|
颉茂华, 果婕欣, 杜凤莲. 2014. 2014-2020年中国稀土战略储备量研究基于动态规划法视角[J]. 资源与产业, 2014, 16(4): 14–20.
|
Xiong T, Huang H W, Sun Y J, et al. 2015. In situ synthesis of a C-Doped (BiO)2CO3 hierarchical self-assembly effectively promoting visible light photocatalysis[J]. Journal of Materials Chemistry A, 3(11): 6118–6127.
DOI:10.1039/C5TA00103J
|
Xiao X, Zhang W D, Yu J Y, et al. 2016. Mechanistic understanding of ternary Ag/AgCl@La(OH)3 nanorods as novel visible light plasmonicphotocatalysts[J]. Catalysis Science & Technology, 6(13): 5003–5010.
|
Yu H J, Zhao Y F, Zhou C, et al. 2014. Carbon quantum dots/TiO2 composites for efficient photocatalytic hydrogen evolution[J]. Journal of Materials Chemistry A, 2(10): 3344–3351.
DOI:10.1039/c3ta14108j
|
Zhuang J L, Liang L F, Sung H H Y, et al. 2007. Controlled hydrothermal growth and up-conversion emission of NaLnF4(Ln=Y, Dy-Yb)[J]. Inorganic Chemistry, 46(13): 5404–5410.
DOI:10.1021/ic070220e
|
Zhang X, Zhang L Z, Xie T F, et al. 2009. Low-Temperature synthesis and high visible-light-induced photocatalytic activity of BiOI/TiO2heterostructures[J]. Journal of Physical Chemistry C, 113(17): 7371–7378.
DOI:10.1021/jp900812d
|
赵卓, 彭鹏. 2013. 稀土催化材料在环境保护中的应用[M]. 北京: 化学工业出版社: 1–20.
|
Zhou Y, Zhang X J, Zhang Q, et al. 2014. Role of graphene on the band structure and interfacial interaction of Bi2WO6/graphene composites with enhanced photocatalytic oxidation of NO[J]. Journal of Materials Chemistry A, 2(39): 16623–16631.
DOI:10.1039/C4TA03762F
|
 2017, Vol. 37
2017, Vol. 37


