能源是人类生存与发展的重要保障, 随着经济与社会的发展, 人类对于能源尤其是液体燃料的需求日益增多(IEA, 2015), 但化石燃料储量有限且难再生, 生物质能源作为唯一可再生的碳源, 具备广阔的应用前景与发展潜力(IEA, 2016).污水生化处理过程中产生的二次污染物污泥作为一种储量巨大的生物质固体废弃物, 富含大量有机质, 如脂肪、蛋白质及糖类等可供利用(Suzuki et al., 1988), 且现有处置技术如填埋、土地利用和焚烧均会带来不同程度的二次污染(Qian et al., 2017).通过热液化技术制成生物质油, 不仅能够提供良好的液体燃料原料, 也能起到固体废弃物减量化和无害化的效果(Ma et al., 2017), 在能源与环保领域具有双重意义.
热液化技术是在高温(220~370 ℃)、高压(10~25 MPa)、惰性气体(N2)或还原性气体(H2)气氛下, 将生物质在亚临界或者超临界溶剂中转化为高能量密度的黑色粘稠液体燃料生物质油的技术(Peterson et al., 2008).相比热解、焚烧、气化(Fonts et al., 2012; Werle et al., 2010; Rulkens, 2007)等资源化技术, 热液化能够有效利用生物质全组分转化为液态燃料, 反应条件更温和.目前热液化技术主要采用水作溶剂(Xu et al., 2008; 周磊等, 2012), 水作为一种大量存在于生物质中的绿色溶剂, 具有良好的应用前景, 但也存在相应的问题:①水的超临界点高, TC=374.3 ℃, PC=22.1 MPa, 若在超临界条件下实现热液化操作, 环境苛刻, 对反应设备要求高;②以水为溶剂的污泥热液化生物质油产率较低, 一般在30%以下;③以水为溶剂获得的污泥热液化生物质油氮、氧含量高, 热值低, 相比原油含氮量(0.05%~0.5%)(孙衍卿等, 2015), 生物质油含氮量一般在6%~9%, 含氮过高易使油在二次加工中造成催化剂中毒, 储藏时产生胶质与沉淀, 降低生物质油的稳定性(梁景程等, 2010).原油含氧量一般只有1‰, 不超过2%~3%, 生物质油所含的氧化合物大部分集中在胶质、沥青中, 降低了生物质油热值;④生物质油中存在大量环烷烃、芳香烃、高分子化合物, 加重了油的粘度, 影响油在输油管线中的速度等(Barreiro et al., 2016).
为了提高生物质油产率和品质, 学者们(Biswas et al., 2017; Liu et al., 2008; Mazaheri et al., 2010; Yan et al., 2016; Yuan et al., 2011)使用甲醇、乙醇、丙酮、正己烷等有机溶剂代替水用于微藻、秸秆等生物质热液化.与水相比, 有机溶剂临界温度、临界压力较低, 反应条件温和, 获得的生物质油产率、热值均较高.但目前针对污泥的热液化研究中, 溶剂大多仅限于水, 很少涉及有机溶剂(Qian et al., 2017; Ma et al., 2017; Jarvis et al., 2017; Malins et al., 2015).本研究选取4种溶剂(水、乙醇、正己烷、水-乙醇共溶剂)开展污泥热液化研究, 分别探究溶剂种类和反应温度对污泥热液化目标产物生物质油产率和性质的影响, 以寻求更合适的热液化溶剂, 提高生物质油产率及品质, 实现固体废弃物–市镇污水处理产物污泥向高品质液体燃料的高效转化.
2 材料与方法(Materials and methods) 2.1 实验材料实验原料污泥取自北京清河污水处理厂二沉池, 含水率为84.52%, 该污泥经105 ℃烘干至恒重, 破碎, 过80目筛, 于4 ℃干燥环境密封储藏.污泥原料组分分析见表 1.
| 表 1 污泥样品性质 Table 1 Properties of sewage sludge |
热液化过程发生于有效容积为600 mL的高温高压反应釜, 反应釜额定最高操作温度为400 ℃, 额定最高操作压力为35 MPa, 磁力搅拌器转速为0~1000 r·min-1, 装置示意图如图 1所示.
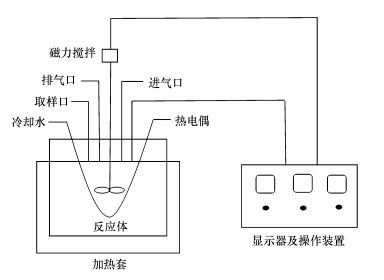 |
| 图 1 热液化装置示意图 Fig. 1 Schematic diagram of thermochemical liquefaction system |
称取60 g污泥、240 mL溶剂(水、乙醇、正己烷、水-乙醇共溶剂)于反应釜中混合均匀, 密封反应釜, 通入N2以排空釜内空气, 再排出N2确保反应系统内初始压力为零.开启磁力搅拌装置, 设置反应温度, 电力加热至设定温度, 维持该温度反应30 min后降温.待反应釜冷却至40 ℃后, 用气袋从排气口处收集气相产物, 打开反应釜, 倒出釜内反应物, 用CH2Cl2清洗反应釜内壁及搅拌装置, 收集反应物及CH2Cl2洗液并过滤.固相残渣经CH2Cl2洗涤3次以上, 置于105 ℃烘箱内烘干至恒重以脱除溶剂及CH2Cl2, 称重.经过滤的液相混合物再进一步分液、旋蒸, 所得黑色粘稠状液体即为热液化目标产物生物质油, 具体操作流程见图 2.液化实验中设置6个反应温度, 即210、240、270、300、330和360 ℃.
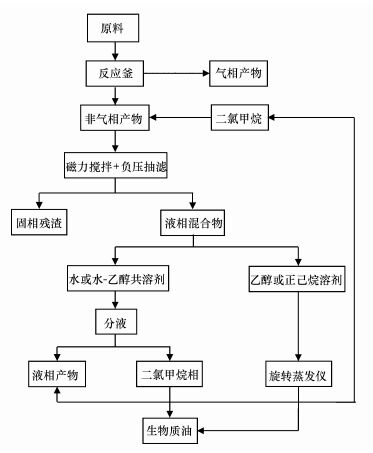 |
| 图 2 污泥热液化与产物分离操作流程 Fig. 2 Thermochemical liquefaction of sewage sludge and products separation procedure |
原料污泥含水率及各有机质含量采用CJ/T221-2005标准测定;污泥和生物质油元素含量采用CE-440型元素分析仪(EAI, 美国)测定, 燃烧管温度为1300 ℃, 载气流速为20 mL·min-1;热重分析采用TG-600型热重分析仪(岛津, 日本), 氮气为载气, 流量为200 mL·min-1, 升温速度为10 ℃·min-1;生物质油的组成测定采用QP 2010 GC-MS气质联用仪(岛津, 日本);色谱条件:色谱柱Varian DB-5(30 m×0.25 mm×0.25 μm), 载气为氮气, 流速1 mL·min-1, 柱前压5.88 kPa, 火焰离子检测器, 检测室温度为290 ℃;质谱条件为:载气氦气, 电离电压70 eV, 电离电流3.4 A, 倍增器电压1.4 kV, 扫描质量范围0~500 u.
2.5 热液化计算方法生物质油产率Y1、有机物转化率Y2、生物质油氮元素富集率Y3、高热值HHV计算公式如式(1)~(4)所示.
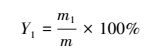
|
(1) |
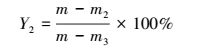
|
(2) |
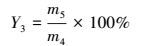
|
(3) |
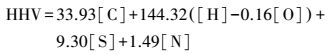
|
(4) |
式中, HHV为生物质油热值(MJ·kg-1);m为原污泥质量(g);m1为生物质油质量(g);m2为固相残渣质量(g);m3为污泥无机物质量(g);m4为污泥总氮质量(g);m5为生物质油总氮质量(g);[C]、[H]、[O]、[N]、[S]分别为碳、氢、氧、氮、硫元素百分比含量.
3 结果与讨论(Results and discussion) 3.1 不同溶剂及反应温度对生物质油产率影响分析污泥分别在4种溶剂下进行热液化反应, 生物质油产率如图 3所示.以水作溶剂对污泥热液化处理, 240 ℃时生物质油产率最低(13.60%), 可能由于低温时, 只有脂质分解成小分子, 缩聚成生物质油, 蛋白质等分解后的小分子尚游离在液相中未团聚成油;330 ℃时生物质油产率最高(44.45%), 与Huang等(2011)的研究相比提高了7%左右, 这可能是由于原料组成上造成的差距, 在此温度下的热液化过程中, 裂解产物通过缩聚、环化或聚合作用生成生物质油, 反应可能更彻底(Teri et al., 2014; Kumar et al., 2017).高温、高压下水的物化性质发生变化, 是热液化反应的良好溶剂和催化剂;接近临界点时, 水的粘度、介电常数(25 ℃、0.1 MPa时, 介电常数为78 Fm-1, 350 ℃、20 MPa时降低为14.07 Fm-1)降低, 疏水性有机化合物(如游离脂肪酸等)溶解度增加, 使亚临界水成为快速均匀、高效优良的反应介质.高温促进水解离, 电离常数KW升高, 促进水热环境中酸/碱催化反应进行, 加速生物质水解, 利于离子反应, 加速碳水化合物脱水反应、醛醇裂解等(Toor et al., 2011; Akhtar et al., 2011).在一定范围内, 反应温度越高生物质油产率越高.但温度过高会使部分有机质炭化, 使生物质油产率降低, 且加热消耗能量增多, 不利于能量平衡(Garcia Alba et al., 2011; Anastasakis et al., 2011).实验中当温度提升到360 ℃后产率也有显著下降, 因而实验没有继续增加反应温度.
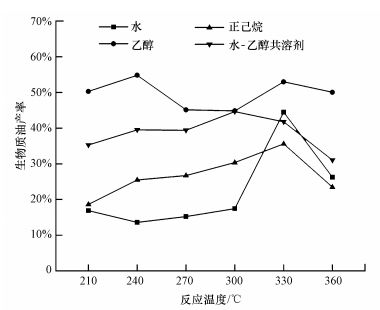 |
| 图 3 不同溶剂对生物质油产率影响 Fig. 3 Effect of solvent type on biocrude yield |
研究认为(Huang et al., 2015; Demirbas, 2001), 热液化反应分3个阶段进行:①生物质解聚, 形成单体生物小分子, 如酯类、蛋白质、碳水化合物等有机物解聚;②通过裂解、脱水、脱羧、脱氨等作用分解形成不稳定轻链生物质;③生物活性成分通过缩合反应、环化反应和聚合反应等, 重新排列组合再生成目标产物生物质油, 具体如图 4所示.热液化过程中, 水解与聚合反应同时发生, 温度较低时, 水解占据主导地位, 热液化程度较低, 一些有机物并没有完全参与到反应中, 而存于液相或固相, 温度升高至一定程度, 裂解及再聚合反应加强, 提高生物油产率及热值(Zhang, 2010).生物质油产量明显高于原污泥中脂质含量(8.01%), 表明在热液化过程中, 蛋白质和碳水化合物均可转化成生物质油, Brown等(2010)选取微拟球藻进行热液化反应也有类似结论.Biller等(2011)对不同种类有机物进行热液化处理, 发现碳水化合物、脂质和蛋白质热液化生成生物质油的趋势为:脂质>蛋白质>碳水化合物.
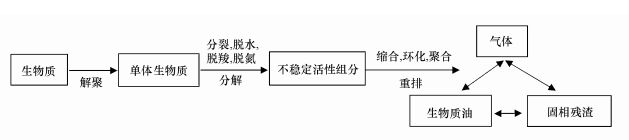 |
| 图 4 生物质热液化基本反应路径 Fig. 4 The basic reaction pathways for the thermochemical liquefaction of biomass |
选用乙醇时生物质油产率随温度升高呈现先升高后降低再升高的趋势, 最高产率为54.82%(240 ℃), 最低产率为44.82%(300 ℃).乙醇作为绿色溶剂, 具有良好的溶剂性能, 其温和的临界温度、临界压力(TC=241.3 ℃, PC=6.38 MPa), 在亚、超临界状态具有更好的供氢效应和溶解力, 又因恰好处于超临界状态, 240 ℃时产率最高, 且乙醇作为反应底物与中间体进行自由基反应, 促进生物质液化形成生物质油, 减少残渣(LI et al., 2010).
正己烷作溶剂时, 生物质油产率随温度升高由初始的18.62%逐渐升至35.58%(330 ℃), 随后下降至23.47%.正己烷的超临界点为TC=234.2 ℃, PC=3.03 MPa, 在亚/超临界时能有效转化污泥中的有机质为生物质油, 液化过程中生物质裂解生成活性分子, 同时伴随脱O、N、S杂原子基团(如脱羧基、脱羰基、脱氨基等)的反应(刘芳奇等, 2016; Sarwono et al., 2016; Patel et al., 2016).
采用正己烷作热液化溶剂的效果(最高产率35.58%)远不及乙醇溶剂(最高产率54.82%), 且乙醇最佳液化温度(240 ℃)更低, 更节能, 因而采用乙醇溶剂更合理.但有机溶剂成本高, 且生产有机溶剂的过程和纯有机溶剂热液化的副产物都会危害环境(Kang et al., 2013).此外, 完全使用有机溶剂用于污泥热液化, 需要对污泥进行干燥, 额外增加费用(Zhang et al., 2014), 因而采用有机溶剂与水的混合溶液参与热液化, 如能在减少有机溶剂用量的同时提升生物质油产率, 效果高效环保.因此, 考虑将水与乙醇按照1:1比例混合作为溶剂, 进行污泥热液化实验.
在水-乙醇共溶剂参与时, 生物质油产率随温度升高呈先升高后降低趋势, 210 ℃下的产率最低(35.28%), 300 ℃下的产率最高(44.63%).水-乙醇共溶剂(1:1)临界温度为314 ℃, 在亚/超临界状态下, 水-乙醇热液化性能提升.一方面, 水的介电常数εr迅速下降, 水分子由极性变为非极性, 使得水分子与有机分子更具亲和力, 增加对有机物的溶解力, 且温度升高, 水分子化学活性增强, 等温压缩率升高, 促进离子、极性非离子和自由基反应(Akiya et al., 2002; Feng et al., 2014; Peng et al., 2016);另一方面, 乙醇对油性产物有很高的溶解性能, 乙醇在液化过程中同时扮演反应基质和供氢体角色.在适量的水溶剂作用下, 产生协同作用, 提高生物质油产量, 抑制残渣生成(刘燕, 2013; Peng et al., 2016).
污泥在不同溶剂(水、乙醇、正己烷、水-乙醇共溶剂)参与下进行热液化反应, 采用乙醇或者水-乙醇共溶剂的生物质油产率最高, 300 ℃时两者产油率持平, 乙醇溶剂在240 ℃时获得实验中最高产率(54.82%).采用正己烷的效果不明显, 略优于水溶剂.根据溶剂极性将其分为3类:极性质子、偶极非质子和非极性溶剂(文婕英等, 2010).水与乙醇作为极性质子溶剂, 易使极性溶质分子形成不稳定的活性中间体, 具有催化作用, 促进离子形成, 利于单分子反应(如SN1反应), 故而有乙醇参与的反应, 生物质油产率均较高;而正己烷作为非极性溶剂, 无法供氢, 油的产率略低.相同温度下, 生物质油产率生成趋势为:乙醇>水-乙醇共溶剂>正己烷>水.
3.2 不同溶剂与反应温度对污泥内有机物转化率的影响分析污泥在不同溶剂下进行热液化反应, 采用有机物转化率衡量污泥减量化效果.如图 5所示, 不同溶剂下的转化效率排序为:水-乙醇共溶剂>乙醇>水>正己烷.高温有利于提高污泥有机物转化率, 有机物最高转化效率为96.4%, 一般70%以上的有机物都得到转化.污泥中有机物除产生生物质油外, 部分转移到液相和气相中, 液相产物中COD值可达数万mg·L-1, 气相产物主要以CO2、CH4为主(Jena et al., 2011).虽然水-乙醇共溶剂下产油率略低于乙醇, 但有机物转化率最高, 这主要是利用水与乙醇混合产生协同效应, 使整个反应处于超临界状态, 发挥超临界流体高扩散性、低极性、低表面张力等特性, 提高对大分子的溶解性能(牟天成等, 2006), 促进有机物的转化, 故而转化率最高.相反, 正己烷溶剂对污泥中有机物溶解能力有限, 大量中间产物易发生缩聚结焦, 不能有效促进有机物转化, 不适合作污泥热液化溶剂.
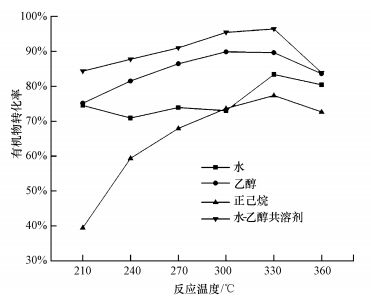 |
| 图 5 不同溶剂和温度下的污泥有机物转化率 Fig. 5 Effect of temperature on the liquefaction conversion of organic matters in sewage sludge with different solvent |
对生物质油进行元素分析, 结果如表 2所示.污泥经热液化反应转化为生物质油后, 除氧含量减少外, 碳、氮、氢、硫元素均得到富集.生物质油碳含量(最高75.68%)远超过污泥中碳含量(35.93%), 且温度越高越有利于碳富集.氢含量总体变化趋势平缓, 在9.10%~9.98%之间.相比污泥中的氧含量(28.95%), 生物质油氧含量降低, 一般在10%以下.生物质油中含有氮、硫等杂原子, 且有一定富集, 其中, 氮元素主要来自污泥中蛋白质脱氨氮反应.高氮、氧含量易降低油的热化学稳定性及热值, 因而脱氮、脱氧的机制仍需进一步研究(Torri et al., 2012).另一种解释生物质油元素组成方式可通过原子比, H/C(氢碳比)是描述化学结构和分子量的参数, 生物质油H/C在0.13~0.14之间, 推测油中有大量环状结构(尤其芳香环结构)生成, O/C(氧碳比)显著低于污泥中的相应值, 表明污泥热液化是脱氧的过程.生物质油热值远高于污泥热值, 一般在36 MJ·kg-1以上, 是能量回收的过程, 对缓解能源危机有极大帮助.
| 表 2 生物质油元素及热值分析 Table 2 Analysis of element and heat value of biocrude |
为考虑氮元素迁移转化规律, 特引用式(3)计算生物质油氮元素富集率, 表征污泥中氮元素迁移至生物质油的比例, 结果如图 6所示.不同溶剂对生物质油的氮元素富集率影响不同, 采用水或正己烷溶剂, 油的氮元素富集率随反应温度升高呈上升趋势, 当采用乙醇时, 呈现相反趋势, 最终达到平衡状态.采用乙醇时, 氮元素富集率最高, 污泥中约75%的氮转移至生物质油中, 采用水时, 氮元素富集率最低(14.28%, 210 ℃), 表明溶剂对污泥热液化氮元素迁移转化具有重要的影响作用.
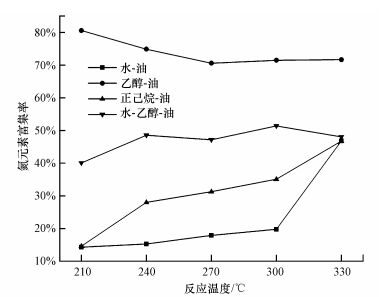 |
| 图 6 不同溶剂和温度下的生物质油氮元素富集率 Fig. 6 Effect of temperature on nitrogen enrichment ratio in biocrude from thermochemical liquefaction of sewage sludge |
利用GC-MS对生物质油进行分析, 由于生物质油成分复杂, 选取各介质中峰面积百分比较高的10种物质进行分析, 结果如表 3所示.其中, 峰面积百分比代表生物质油中各化合物在色谱峰中的面积比, 间接表示生物质油各化合物比例, 但与真实浓度还有差别(Villadsen et al., 2012).
| 表 3 生物质油化学组成及相对含量 Table 3 Relative contents of compounds in biocrude from different solvents |
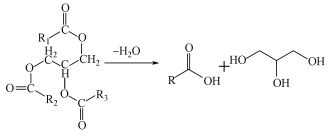
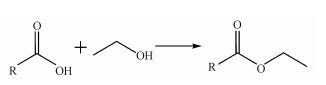
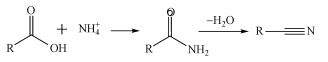
不同溶剂对生物质油成分影响显著.以水为溶剂, 生物质油主要是酸类(27.87%)、酰胺类(27.52%);采用乙醇时, 生物质油成分主要是酯类(51.15%)、烷烃类(22.08%);采用正己烷时, 生物质油成分多为酰胺、腈类等含氮化合物(41.03%)、酸类(11.95%)及烷烃(4.99%);采用水-乙醇共溶剂时, 生物质油成分主要是酯类(59.19%).在乙醇参与热液化反应时, 生物质油中含有更多酯类物质, 与生物柴油类似.水溶剂生成较多脂肪酸类, 添加乙醇后多为酯类物质, 间接表明乙醇不仅提供反应场所, 而且参与反应, 是良好的氢供体.以正己烷为溶剂生物质油含氮量较高, 可能是部分含氮化合物不溶于正己烷一类非极性溶剂, 不易在正己烷中发生水解或脱氨等反应.参考藻类等生物质热液化产生的气体主要为CO2、NH3等(Jena et al., 2011), 污泥中有机质与微藻类似, 猜测污泥热液化有NH3产生且气相产物刺激性气味较淡, NH3含量相对较少, 根据质量守恒, 氮元素在生物质油中富集.腈类化合物可能是酰胺类化合物发生脱水反应生成.虽然生物质油中含有大量酯类物质, 性质与生物柴油类似, 但含氧基团使得生物质油的可燃性降低, 若将生物质油利用, 仍需对其进行催化加氢等相应的改性处理(杨雷等, 2016).由于GC-MS检测中, 一些大分子物质无法检出, 且无法定性分析, 仅对可检测出物质探究可能生成途径, 具体如下所示:①当采用水或正己烷作溶剂, 污泥中油脂在亚临界水中水解, 产生甘油和脂肪酸, 脂肪酸通常是含有12~20个碳原子的直链酸或烯酸, 衍生出各酸类物质(式(5));②当加入乙醇溶剂, 污泥中油脂水解后, 酸类物质与乙醇发生酯化或转酯基反应生成各种酯类(式(6));③脂肪酸上的羧基和氨基酸水解后的氨气在亚临界水中可以进一步发生脱水反应生成长链酰胺, 酰胺脱水产生腈类(式(7)).
|
(5) |
|
(6) |
|
(7) |
实验选取不同溶剂下最大产率的生物质油在氮气氛围内进行热重(TG)/差热(DTA)分析, 尽管可能发生热解, 但其可以提供生物质油沸程分布大致范围(Anastasakis et al., 2011), 具体如图 7、表 4所示.根据生物质油组分沸程分布特点, TG曲线呈现失重由慢变快后又放缓至恒定状态的趋势.水或正己烷作溶剂, 温度≥150 ℃, 失重加快, 而乙醇或水-乙醇共溶剂, 失重在温度≥100 ℃时加快, 主要是生物质油中轻组分物质挥发, 温度≤450 ℃, 失重最快, 且失重量最多(83%~93%), 此时可能发生裂解等反应, 温度≥450 ℃, 失重达到平衡状态.
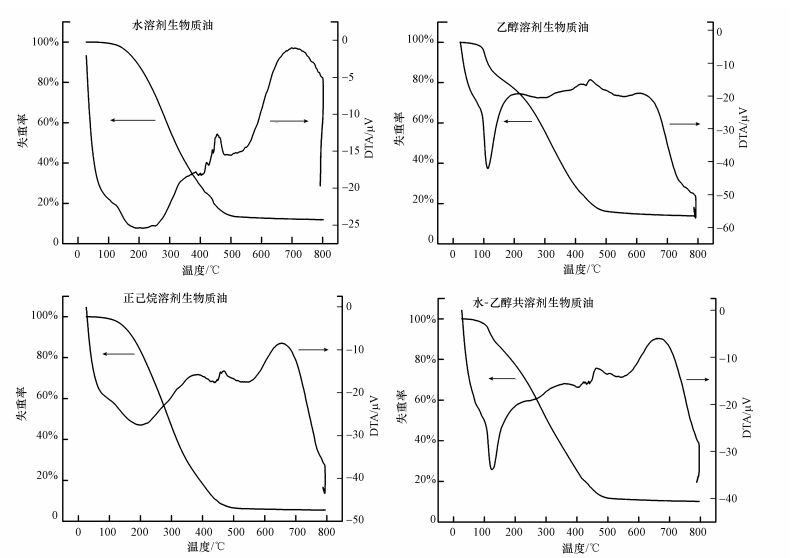 |
| 图 7 生物质油热重分析 Fig. 7 Thermo gravimetric analysis of biocrude |
| 表 4 生物质油沸程分布 Table 4 Boiling point distribution of biocrude |
参考石油工业依据沸点的不同将生物质油分为汽油组分、石蜡油组分、柴油组分、燃油组分、重油组分5类.4种溶剂下生物质油柴油组分含量最高, 其次是燃油组分(正己烷溶剂下生物质油除外), 上述组分占生物质油组分的50%以上.不同溶剂对生物质油沸点分布影响不同, 采用乙醇或水-乙醇共溶剂, 生物质油汽油组分提高, 分别为19.5%和17.01%, 表明在乙醇参与下, 生物质油含有更多小分子化合物.沸点≤350 ℃, 轻馏组分分别占总生物质油组分的59.23%、58.95%、70.43%、62.26%, 表明生物质油是一种可进行分离、精炼生产燃料、化学品的优良原料(Tian et al., 2011).沸点≥500 ℃, 各生物质油重油组分类似, 在1%~2%之间, 较均衡.
4 结论(Conclusions)1) 不同溶剂最佳反应温度不同, 乙醇、水-乙醇共溶剂分别在240、300 ℃时的生物质油产率最高, 分别为54.82%、44.63%.相同温度下, 生物质油产率排序为:乙醇>水-乙醇共溶剂>正己烷>水.
2) 热液化反应对污泥减量化、资源化效果明显, 污泥中70%以上的有机物得到转化, 最高转化率为96.4%, 转化效率排序为:水-乙醇共溶剂>乙醇>水>正己烷.
3) 溶剂对生物质油品质影响显著, 加入适量乙醇溶剂, 生物质油以酯类、烷烃为主, 油品质较好, 水或正己烷溶剂生物质油主要以酸类、烷烃类和部分含氮化合物如酰胺等为主.
4) 生物质油的沸程分布以柴油组分(250~350 ℃)和燃油组分(350~500 ℃)居多, 添加乙醇溶剂后可以提高生物质油汽油组分(30~170 ℃)含量.
5) 综合生物质油产率、品质、污泥减量化效果, 水-乙醇共溶剂更适合作为污泥热液化溶剂.
Akhtar J, Amin N A S. 2011. A review on process conditions for optimum bio-oil yield in hydrothermal liquefaction of biomass[J]. Renewable and Sustainable Energy Reviews, 15(3): 1615–1624.
DOI:10.1016/j.rser.2010.11.054
|
Akiya N, Savage P E. 2002. Roles of water for chemical reactions in high-temperature water[J]. Chemical Reviews, 102(8): 2725–2750.
DOI:10.1021/cr000668w
|
Anastasakis K, Ross A B. 2011. Hydrothermal liquefaction of the brown macro-alga Laminaria saccharina:effect of reaction conditions on product distribution and composition[J]. Bioresource Technology, 102(7): 4876–4883.
DOI:10.1016/j.biortech.2011.01.031
|
Barreiro D L, Gómez B R, Ronsse F, et al. 2016. Heterogeneous catalytic upgrading of biocrude oil produced by hydrothermal liquefaction of microalgae:State of the art and own experiments[J]. Fuel Processing Technology, 148: 117–127.
DOI:10.1016/j.fuproc.2016.02.034
|
Biller P, Ross A B. 2011. Potential yields and properties of oil from the hydrothermal liquefaction of microalgae with different biochemical content[J]. Bioresource Technology, 102(1): 215–225.
DOI:10.1016/j.biortech.2010.06.028
|
Biswas B, Kumar A A, Bisht Y, et al. 2017. Effects of temperature and solvent on hydrothermal liquefaction of Sargassum tenerrimum algae[J]. Bioresource Technology.
DOI:10.1016/j.biortech.2017.03.045
|
Brown T M, Duan P, Savage P E. 2010. Hydrothermal liquefaction and gasification of Nannochloropsis sp[J]. Energy & Fuels, 24(6): 3639–3646.
|
Demirbaş A. 2001. Biomass resource facilities and biomass conversion processing for fuels and chemicals[J]. Energy Conversion and Management, 42(11): 1357–1378.
DOI:10.1016/S0196-8904(00)00137-0
|
Feng S, Yuan Z, Leitch M, et al. 2014. Hydrothermal liquefaction of barks into bio-crude–Effects of species and ash content/composition[J]. Fuel, 116: 214–220.
DOI:10.1016/j.fuel.2013.07.096
|
Fonts I, Gea G, Azuara M, et al. 2012. Sewage sludge pyrolysis for liquid production:A review[J]. Renewable and Sustainable Energy Reviews, 16(5): 2781–2805.
DOI:10.1016/j.rser.2012.02.070
|
Garcia Alba L, Torri C, Samorì C, et al. 2011. Hydrothermal treatment (HTT) of microalgae:evaluation of the process as conversion method in an algae biorefinery concept[J]. Energy & Fuels, 26(1): 642–657.
|
Huang H, Yuan X. 2015. Recent progress in the direct liquefaction of typical biomass[J]. Progress in Energy and Combustion Science, 49: 59–80.
DOI:10.1016/j.pecs.2015.01.003
|
Huang H, Yuan X, Zeng G, et al. 2011. Thermochemical liquefaction characteristics of microalgae in sub-and supercritical ethanol[J]. Fuel Processing Technology, 92(1): 147–153.
DOI:10.1016/j.fuproc.2010.09.018
|
I EA. 2015. World Energy Outlook 2015[M]. Paris: OECD Publishing.
|
I EA. 2016. Renewables Information 2016[M]. Paris: OECD Publishing.
|
Jarvis J M, Billing J M, Hallen R T, et al. 2017. Hydrothermal liquefaction biocrude compositions compared to petroleum crude and shale oil[J]. Energy & Fuels, 31(3): 2896–2906.
|
Jena U, Das K C, Kastner J R. 2011. Effect of operating conditions of thermochemical liquefaction on biocrude production from Spirulina platensis[J]. Bioresource Technology, 102(10): 6221–6229.
DOI:10.1016/j.biortech.2011.02.057
|
Kang S, Li X, Fan J, et al. 2013. Hydrothermal conversion of lignin:A review[J]. Renewable and Sustainable Energy Reviews, 27: 546–558.
DOI:10.1016/j.rser.2013.07.013
|
Kumar G, Shobana S, Chen W, et al. 2017. A review of thermochemical conversion of microalgal biomass for biofuels:chemistry and processes[J]. Green Chemistry, 19(1): 44–67.
DOI:10.1039/C6GC01937D
|
Li H, Yuan X, Zeng G, et al. 2010. The formation of bio-oil from sludge by deoxy-liquefaction in supercritical ethanol[J]. Bioresource Technology, 101(8): 2860–2866.
DOI:10.1016/j.biortech.2009.10.084
|
梁景程, 马守涛, 徐群. 2010. 原油评价中总氮含量的分析[J]. 石油与天然气化工, 2010, 39(2): 165–167.
|
刘芳奇, 吴诗勇, 黄胜, 等. 2016. 污泥的正己烷亚/超临界萃取及其产物特征[J]. 华东理工大学学报(自然科学版), 2016, 42(4): 460–466.
|
刘燕. 2013. 稻壳在混合溶剂(乙醇-水)中热液化制生物油的研究[D]. 长沙: 湖南大学. 66
http://cdmd.cnki.com.cn/Article/CDMD-10532-1014233408.htm |
Liu Z, Zhang F. 2008. Effects of various solvents on the liquefaction of biomass to produce fuels and chemical feedstocks[J]. Energy Conversion and Management, 49(12): 3498–3504.
DOI:10.1016/j.enconman.2008.08.009
|
Ma W, Du G, Li J, et al. 2017. Supercritical water pyrolysis of sewage sludge[J]. Waste Management, 59: 371–378.
DOI:10.1016/j.wasman.2016.10.053
|
Malins K, Kampars V, Brinks J, et al. 2015. Bio-oil from thermo-chemical hydro-liquefaction of wet sewage sludge[J]. Bioresource Technology, 187: 23–29.
DOI:10.1016/j.biortech.2015.03.093
|
Mazaheri H, Lee K T, Bhatia S, et al. 2010. Sub/supercritical liquefaction of oil palm fruit press fiber for the production of bio-oil:effect of solvents[J]. Bioresource Technology, 101(19): 7641–7647.
DOI:10.1016/j.biortech.2010.04.072
|
牟天成, 韩布兴. 2006. 超临界流体的共溶剂效应和混合流体研究进展[J]. 化学进展, 2006, 18(1): 19–23.
|
Patel B, Hellgardt K. 2016. Hydrothermal liquefaction and in situ supercritical transesterification of algae paste[J]. RSC Advances, 6(89): 86560–86568.
DOI:10.1039/C6RA11376A
|
Peng X, Ma X, Lin Y. 2016. Investigation on characteristics of liquefied products from solvolysis liquefaction of Chlorella pyrenoidosa in ethanol-water systems[J]. Energy & Fuels, 30(8): 6475–6485.
|
Peng X, Ma X, Lin Y, et al. 2016. Effect of process parameters on solvolysis liquefaction of Chlorella pyrenoidosa in ethanol-water system and energy evaluation[J]. Energy Conversion and Management, 117: 43–53.
DOI:10.1016/j.enconman.2016.03.029
|
Peterson A A, Vogel F, Lachance R P, et al. 2008. Thermochemical biofuel production in hydrothermal media:a review of sub-and supercritical water technologies[J]. Energy & Environmental Science, 1(1): 32–65.
|
Qian L, Wang S, Savage P E. 2017. Hydrothermal liquefaction of sewage sludge under isothermal and fast conditions[J]. Bioresource Technology, 232: 27–34.
DOI:10.1016/j.biortech.2017.02.017
|
Rulkens W. 2007. Sewage sludge as a biomass resource for the production of energy:overview and assessment of the various options[J]. Energy & Fuels, 22(1): 9–15.
|
Sarwono R, Pusfitasari E D, Ghozali M, et al.2016.Hydrothermal liquefaction of palm oil empty fruit bunch (EFB) into bio-oil in different organic solvents[Z].AIP Publishing.60015
|
孙衍卿, 孙震, 张景来. 2015. 污泥水热液化水相产物中氮元素变化规律的研究[J]. 环境科学, 2015, 36(6): 2210–2215.
|
Suzuki A, Nakamura T, Yokoyama S, et al. 1988. Conversion of sewage sludge to heavy oil by direct thermochemical liquefaction[J]. Journal of Chemical Engineering of Japan, 21(3): 288–293.
DOI:10.1252/jcej.21.288
|
Teri G, Luo L, Savage P E. 2014. Hydrothermal treatment of protein, polysaccharide, and lipids alone and in mixtures[J]. Energy & Fuels, 28(12): 7501–7509.
|
Tian Y, Zuo W, Ren Z, et al. 2011. Estimation of a novel method to produce bio-oil from sewage sludge by microwave pyrolysis with the consideration of efficiency and safety[J]. Bioresource Technology, 102(2): 2053–2061.
DOI:10.1016/j.biortech.2010.09.082
|
Toor S S, Rosendahl L, Rudolf A. 2011. Hydrothermal liquefaction of biomass:a review of subcritical water technologies[J]. Energy, 36(5): 2328–2342.
DOI:10.1016/j.energy.2011.03.013
|
Torri C, Garcia Alba L, Samori C, et al. 2012. Hydrothermal treatment (HTT) of microalgae:detailed molecular characterization of HTT oil in view of HTT mechanism elucidation[J]. Energy & Fuels, 26(1): 658–671.
|
Villadsen S R, Dithmer L, Forsberg R, et al. 2012. Development and application of chemical analysis methods for investigation of bio-oils and aqueous phase from hydrothermal liquefaction of biomass[J]. Energy & Fuels, 26(11): 6988–6998.
|
文婕英, 白林, 朱彦荣. 2010. 氢键对有机取代反应和加成反应的影响[J]. 广东化工, 2010, 37(11): 71–72.
DOI:10.3969/j.issn.1007-1865.2010.11.035 |
Werle S, Wilk R K. 2010. A review of methods for the thermal utilization of sewage sludge:The polish perspective[J]. Renewable Energy, 35(9): 1914–1919.
DOI:10.1016/j.renene.2010.01.019
|
Xu C, Lancaster J. 2008. Conversion of secondary pulp/paper sludge powder to liquid oil products for energy recovery by direct liquefaction in hot-compressed water[J]. Water Research, 42(6/7): 1571–1582.
|
Yan W, Duan P, Wang F, et al. 2016. Composition of the bio-oil from the hydrothermal liquefaction of duckweed and the influence of the extraction solvents[J]. Fuel, 185: 229–235.
DOI:10.1016/j.fuel.2016.07.117
|
杨雷, 邓博中, 李元良, 等. 2016. Box-Behnken响应面法优化粪便直接液化制取生物质油工艺条件的研究[J]. 可再生能源, 2016, 34(10): 1554–1560.
|
Yuan X, Wang J, Zeng G, et al. 2011. Comparative studies of thermochemical liquefaction characteristics of microalgae using different organic solvents[J]. Energy, 36(11): 6406–6412.
DOI:10.1016/j.energy.2011.09.031
|
Zhang J, Zhang Y. 2014. Hydrothermal liquefaction of microalgae in an ethanol–water co-solvent to produce biocrude oil[J]. Energy & Fuels, 28(8): 5178–5183.
|
Zhang Y. 2010. Hydrothermal liquefaction to convert biomass into crude oil[J]. Biofuels from Agricultural Wastes and Byproducts, 42(37): 201–232.
|
周磊, 韩佳慧, 张景来, 等. 2012. 污泥直接液化制取生物质油试验研究[J]. 可再生能源, 2012, 30(3): 69–72.
|
 2017, Vol. 37
2017, Vol. 37


