2. 江苏省农业科学研究院农业资源与环境研究所, 南京 210014
2. Institute of Agricultural Science and Environment, Jiangsu Academy of Agricultural Sciences, Nanjing 210014
随着人类工业、生活污水的排放, 加之农业面源污染, 导致地表水氨氮污染严重.过量的氨氮会引起水体富营养化, 使藻类大量增殖, 对水体生态平衡和人类健康产生了严重的危害(姜瑞等, 2013).因此, 迫切需要寻找一种安全、高效又经济的低浓度氨氮污染水体的去除技术.
目前, 低浓度氨氮(≤50 mg·L-1)废水的处理方法主要有:折点加氯法、沉淀法、离子交换法等(姜瑞等2013;刘莉峰等, 2014).近年来, 半导体光催化技术因具有耐腐蚀、无毒、稳定性高、绿色环保、高效低耗能等优点(靳立民等, 2004; Hu et al., 2006), 在氨氮废水的治理中被逐渐应用(焦宏涛, 2008).其中, 以TiO2为催化剂处理氨氮废水的研究报道相对较多, 通过掺杂和负载处理, TiO2系列催化剂对氨氮的去除率大约在41%~90%之间(郑凤英等, 2007; 刘国光等, 2008).ZnO作为一种廉价的光催化剂, 有关其处理氨氮废水的报道较少.研究发现, 纳米ZnO具有高光敏性、低毒性、良好的光学性能和化学稳定性(于晓彩等, 2010; Kıranşan et al., 2015; Pimentel et al., 2015), 在氨氮废水的去除方面有潜在的应用价值(Rezaee et al., 2012).但纳米ZnO应用于水处理时, 仍存在许多不足, 如在水中易团聚, 分散性差; 光催化结束后只能离心分离, 难以重复利用和实际应用.
通过引入聚合物, 形成ZnO纳米粒子/聚合物复合材料, 将聚合物作为纳米粒子载体, 利用聚合物分子链之间的排斥作用可有效防止纳米粒子的团聚, 能很好地解决上述不足, 并且已见文献报道(Iknur et al., 2015; Farzana et al., 2014).研究发现, 将纳米ZnO分散于聚合物基质, 所得复合材料兼具纳米ZnO光催化性能和聚合物的延展性等优点(Antonio Carmona et al., 2015).在众多聚合物中, 聚甲基丙烯酸甲酯(PMMA)作为一种无毒环保的热塑型材料, 耐碱、耐烯酸、化学稳定性良好, 且兼具质轻、价廉、易于成型等优点.PMMA能够透过73.5%的紫外光, 与纳米ZnO结合能够提高纳米ZnO的分散性和光学性能; 而且以PMMA大颗粒微球作为载体, 可使原本需经过离心才可分离回收的纳米ZnO可通过简单的过滤即可得到, 解决了催化剂回收难的问题.
因此, 本文通过水热法制备纳米ZnO, 并采用热粘固法负载于PMMA微球表面, 制备纳米ZnO-PMMA复合材料, 研究复合材料对水中低浓度氨氮的去除性能, 探讨此复合材料对氨氮去除的机制, 以期为纳米ZnO聚合物复合材料的制备和应用提供参考.
2 材料和方法(Materials and methods) 2.1 实验材料六水合硝酸锌(化学纯)购自阿拉丁试剂(上海)有限公司; 聚甲基丙烯酸甲酯、羧甲基纤维素钠(CMC)均为化学纯, 购自国药集团化学试剂有限公司; 无水乙醇.氯化铵、氢氧化钠及盐酸均为分析纯, 购自南京化学试剂有限公司; 配制溶液和清洗仪器均采用去离子水.
2.2 ZnO-PMMA催化剂制备纳米ZnO光催化剂通过水热法制备(周小岩等, 2014; 商桑斌等, 2002), 具体步骤如下:称取14.875 g Zn (NO3)2·6H2O, 溶于100 mL去离子水, 并加入1.0 g CMC; 称取10 g NaOH, 溶解于100 mL去离子水; 然后在上述溶液中缓慢滴加NaOH溶液, 得到均匀白色混浊液, 在磁力搅拌器中搅拌60 min; 将溶液转移至200 mL水热反应釜中, 填充度为80%, 120 ℃下恒温反应12 h.所得白色沉淀物用去离子水和无水乙醇分别洗涤3次并离心, 最后放入鼓风干燥箱中60 ℃干燥12 h, 即得到纳米ZnO粉体.
制得的纳米ZnO通过热粘固法负载于PMMA上, 具体步骤为:取一定比例的纳米ZnO和PMMA均匀混合于坩埚内, 将坩埚置于烘箱, 设置温度为120 ℃; 当达到PMMA的玻璃化温度转化点(大约104 ℃), 纳米ZnO将牢固地负载于PMMA上.将所得复合材料放入干燥器中冷却至室温, 用去离子水冲洗、抽滤, 60 ℃下干燥即得ZnO-PMMA光催化剂.
2.3 光催化去除氨氮实验由已干燥的NH4Cl (分析纯)配制100 mg·L-1的氨氮废水, 根据需要分别稀释至10、20、30、50、70 mg·L-1.取100 mL氨氮溶液加入石英管, 投入制备的催化剂, 放置于恒温水浴反应器中, 磁力搅拌, 先于黑暗处暗吸附30 min, 达到吸附平衡.然后打开125 W汞灯, 平行照射石英管, 同时向溶液中通入少量恒定的空气.为减小氨氮吹脱和人为操作所产生的误差, 每组实验设置不加入催化剂的空白作为对照, 并且每个实验条件设3个平行.按设定时间取样, 用孔径0.45 μm微孔滤膜过滤, 测定水中氨氮浓度, 根据公式(1)计算氨氮的去除率.分别考察ZnO负载量、不同氨氮初始浓度、催化剂用量及反应液pH对氨氮去除能力的影响.
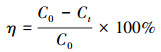
|
(1) |
式中, η为氨氮去除率, C0为水中初始的氨氮浓度(mg·L-1), Ct为反应t时间时水中的氨氮浓度(mg·L-1).
2.4 表征及分析方法采用德国Bruker公司的D8 ADVANCE型X射线衍射仪(XRD)分析催化剂的物相结构.采用美国赛默飞世尔公司的Evolution 220紫外分光光度计分析样品的紫外吸收情况.采用日本HITACHI公司的扫描电子显微镜(SEM)观察催化剂的形貌.采用AAS-600火焰原子吸收光谱仪测定实际ZnO负载量.采用MAPADA UV-3200分光光度计在420 nm处测定水中氨氮含量, 在220 nm和275 nm处测定水中硝酸盐氮含量.在540 nm处测定水中亚硝酸盐氮含量.采用Thermo Scientific iCAP Q ICP-MS测定水中Zn2+浓度.
3 结果(Results) 3.1 结构分析 3.1.1 催化剂XRD分析图 1是纳米ZnO和ZnO-PMMA的XRD图谱, 衍射角范围为25°~65°.由图 1可知, 制备的纳米ZnO与JCPDS卡片上ZnO标准谱图(00-036-1415)一致, 所得ZnO样品为六方晶系的纤锌矿结构, 各衍射峰的晶面指数分别为(100)、(002)、(101)、(102)、(110)和(113), 未出现其他杂质峰, 结晶质量良好.ZnO-PMMA的XRD图谱中ZnO各特征衍射峰清晰, 且峰形与纳米ZnO基本一致, 可见PMMA作为载体对纳米ZnO晶型未产生影响.
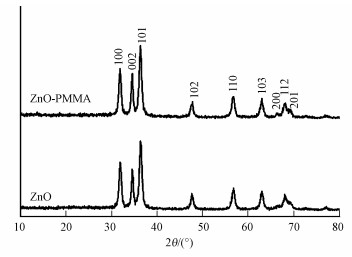 |
| 图 1 纳米ZnO、ZnO-PMMA的XRD图谱 Fig. 1 XRD pattern of the catalyst ZnO、ZnO-PMMA |
纳米ZnO呈片状, 为单片状或花朵状, 纳米花是由多个纳米片晶体通过共享边界融合生长而成, 尺寸为200~400 nm, 纯纳米ZnO团聚程度高, 分散性不好(图 2d).ZnO-PMMA复合材料中(图 2b), 纳米ZnO均匀地分布于PMMA微球的表面(图 2a), 表面ZnO的分散性显著提高, 团聚程度低(图 2c).
 |
| 图 2 PMMA (a)、ZnO-PMMA (b、c)和ZnO (d) Fig. 2 SEM images of the catalyst PMMA (a)、ZnO-PMMA (b, d) and ZnO (d) |
图 3是纳米ZnO和ZnO-PMMA的全波长扫描图谱.由图可见, 样品在200~400 nm紫外区有明显吸收, 且复合材料比ZnO的吸收强度有所提高.一方面是由于PMMA能够透过73.5%的紫外光; 另一方面, 负载后的材料表面ZnO分布均匀且分散, 使得ZnO-PMMA复合材料对紫外光的吸收增强, 有利于光催化反应的进行.
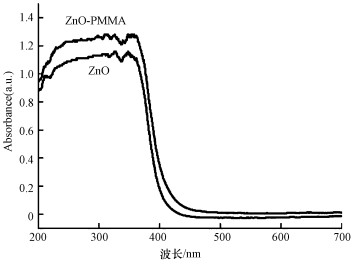 |
| 图 3 纳米ZnO、ZnO-PMMA的全波长扫描图 Fig. 3 UV-Vis spectra of the catalyst ZnO and ZnO-PMMA |
分别设置m(ZnO):m(PMMA)=10:1、5:1、2:1和1:1, 在100 mL的50 mg·L-1氨氮废水中分别加入0.1 g上述比例的催化剂, 设置pH=12.0, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h, 考察纳米ZnO的负载量对氨氮去除的影响, 结果见图 4.由图 4可知, 随着PMMA微球表面ZnO含量不断增加, 氨氮的去除率也不断升高, 当m(ZnO):m(PMMA)=5:1时, 达到最佳负载比例, 此时氨氮去除率为66%.继续增加ZnO负载量, 光催化活性反而降低.这是由于微球表面过量的ZnO堆积使活性位点无法充分暴露, 减少了与紫外光、氨氮分子的接触, 氨氮的去除效率降低.因此, 本文采用m(ZnO):m(PMMA)=5:1为最佳负载量.
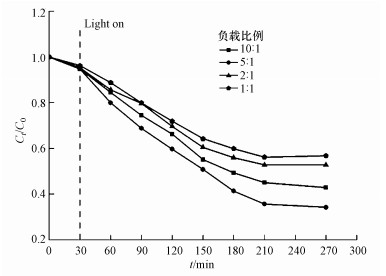 |
| 图 4 不同ZnO负载量对氨氮去除的影响 Fig. 4 Influence of the ZnO loading on the removal of ammonia nitrogen |
取氨氮浓度为10~70 mg·L-1的模拟废水100 mL, 设置pH=12.0, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h, 考察氨氮初始浓度对催化效果的影响, 结果如图 5所示.由图 5可知, 氨氮浓度10 mg·L-1时, 去除率最高, 随着初始氨氮浓度的增加, 去除率逐渐降低.以-ln (C/C0)对反应时间t进行线性拟合, 再将表观速率常数kapp对初始氨氮浓度进行拟合, 结果见图 6.可知, 在实验浓度范围内, ZnO-PMMA去除低浓度氨氮符合准一级反应方程, 表观速率常数随初始氨氮浓度的增加而减小.这可能是由于高浓度的氨氮覆盖了催化剂表面的活性位点, 导致催化剂表面产生的·OH和·O2-浓度减少, 影响催化活性.但总体而言, ZnO-PMMA催化剂对10~50 mg·L-1的低浓度氨氮都具有一定的去除率, 并且去除效果较稳定.
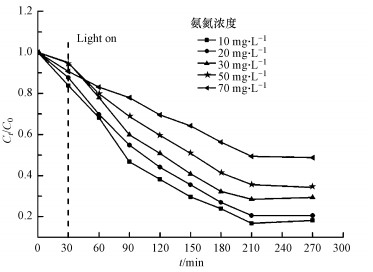 |
| 图 5 不同氨氮初始浓度对去除效果的影响 Fig. 5 Degradation rate of different initial concentration of ammonia nitrogen |
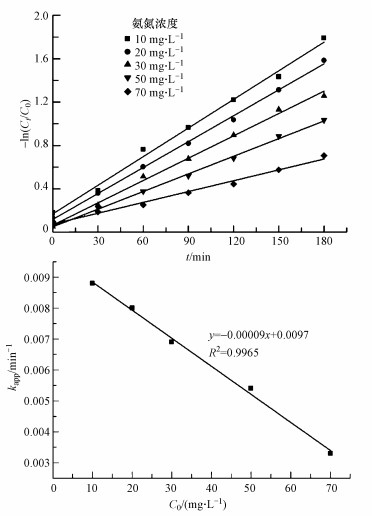 |
| 图 6 ZnO-PMMA去除氨氮的动力学图 Fig. 6 Kinetics of ZnO-PMMA removal of ammonia nitrogen |
取50 mg·L-1的模拟氨氮废水100 mL, 设置催化剂用量为0~3.0 g·L-1, pH=12.0, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h, 考察催化剂用量对氨氮去除的影响, 结果见图 7.由图 7可知, 当催化剂用量从0.5 g·L-1增加到2.0 g·L-1时, 氨氮去除率从37%增至70%.当催化剂用量达到最佳去除上限, 继续增加催化剂用量时, 氨氮去除率降低.这是由于增加光催化剂的用量, 相应地增加了催化剂表面的活性位点数量, 使·OH和·O2-产量增加, 从而光催化效率提高.然而当光催化剂用量过多时, 造成悬浮液的透明度降低, 在散射和屏蔽作用的双重影响下, 增加了光的反射, 降低了紫外光的利用率, 空穴-电子对数量减少, 从而影响反应效率(李元昊等, 2013; 陈晓慧等, 2007).催化剂的过量堆叠, 也使其表面无法充分接受紫外光, 降低了催化效率.综合催化效率和经济效益, 本文选择催化剂用量为1.0 g·L-1.
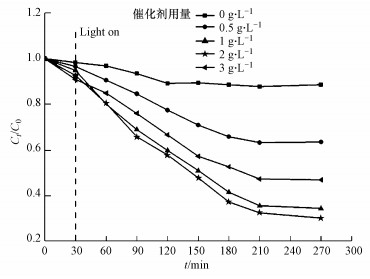 |
| 图 7 催化剂用量对氨氮去除的影响 Fig. 7 Influence of the catalyst dosage on the removal of ammonia nitrogen |
pH对氨氮去除有明显影响, 取50 mg·L-1的模拟氨氮废水100 mL, 调节水样pH分别为4.0、7.0、9.0、11.0、12.0, 设置催化剂用量1.0 g·L-1, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h.由图 8可知, 在酸性及中性条件下, 氨氮去除率非常低; 碱性条件下光催化活性高.
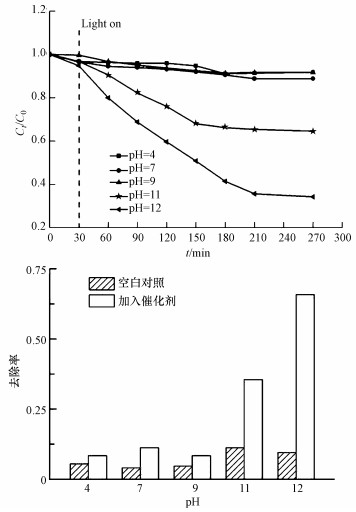 |
| 图 8 pH对氨氮去除的影响 Fig. 8 Influence of pH on the removal of ammonia nitrogen |
据文献报道, 纳米ZnO的零点电位为9.0±0.3(Zhang et al., 2005).当溶液呈酸性时, 氨氮废水中的N主要以NH4+形式存在, 且低于零点点位时ZnO表面呈正电性, 静电斥力阻碍了氨氮与催化剂接触, 催化效果非常小.pH在零点电位附近时, 也几乎没有光催化活性.光催化过程中, 催化剂表面的光生电子和空穴数量对去除效率起决定性作用(Yao et al., 2004).因此, 在酸性和中性条件下, 不能提供充足的·OH进行光催化反应.而当pH为碱性时, 溶液中存在大量的OH-与空穴·OH, 光催化能力增强.且在空白实验下, 氨氮去除率最高仅为10%左右, 说明实验条件下氨氮以吸附和以NH3形式被吹脱的量很少, 主要以光催化去除为主.根据本实验结果, 选择pH=12为最佳反应条件.
3.2.5 不同材料催化效果的比较及产物研究取0.1 g负载比例为5:1的ZnO-PMMA、0.077 g ZnO+ 0.023 g PMMA (简单混合), 以及0.077 g的ZnO和0.023 g的PMMA, 分别加入100 mL的50 mg·L-1氨氮废水.设置pH=12.0, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h, 研究复合材料ZnO-PMMA、纳米ZnO和PMMA对氨氮废水去除率的差异, 结果见图 9.由图 9可知, 聚合物PMMA本身不具备催化活性, 对氨氮无去除效果; PMMA与纳米ZnO简单混和后, ZnO的光催化活性并没有提高; PMMA与纳米ZnO通过热粘固作用后形成复合材料, 具有协同效应, 去除率从41%提高到66%, 如预期提高了催化活性.分析其原因可能如下:①纯ZnO易发生团聚, 在水中分散性差, PMMA与ZnO通过热粘合作用形成复合微球, ZnO均匀零散地分布于PMMA微球的各部分, 使得其分散性提高, 且ZnO的晶体结构不发生变化; ②PMMA本身的特殊性质, 能透过73.5%的紫外光, 复合材料利用紫外光的效率增加, 由全波长扫描图可见, 负载后材料的紫外吸收增强.
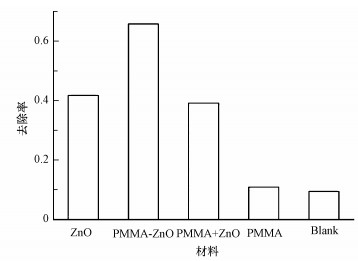 |
| 图 9 不同材料对氨氮去除的影响 Fig. 9 Influence of the different materials on the removal of ammonia nitrogen |
ZnO-PMMA光催化去除水中的氨氮, 最理想的状态是将氨氮转化为氮气.因此, 对反应产物进行了初步的研究, 取50 mg·L-1的模拟氨氮废水100 mL, 设置pH=12.0, 催化剂ZnO-PMMA用量1.0 g·L-1, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h, 分别检测了反应结束水样中硝酸盐氮及亚硝酸盐氮的含量, 结果见表 1.从表 1可知, 水样中硝酸盐氮和亚硝酸盐氮含量非常低, 分别为0.122 mg·L-1和0.056 mg·L-1, 说明氨氮大部分被催化氧化为氮气, ZnO-PMMA材料具有将氨氮降解为氮气的良好的光催化氧化选择性.反应前后的过滤液中均未检测到Zn2+, 说明在催化反应中未有金属溶出, 催化剂性能稳定.
| 表 1 ZnO-PMMA光催化产物检测 Table 1 Product concentration of ZnO-PMMA photocatalytic reaction |
取0.1 g负载比例为5:1的ZnO-PMMA, 加入100 mL的50 mg·L-1氨氮废水, 设置pH=12.0, 反应温度30 ℃, 黑暗吸附30 min, 紫外光照射4 h.反应后滤出上清液进行分析, 再加入100 mL的50 mg·L-1氨氮废水, 按照上述实验条件重复进行, 考察ZnO-PMMA的重复利用性, 结果如图 10所示.由图 10可知, 随着重复次数的增加, 氨氮去除率略有降低, 但在第4次重复时去除率仍保持在61%以上.说明ZnO-PMMA催化剂活性稳定, 重复利用性强.
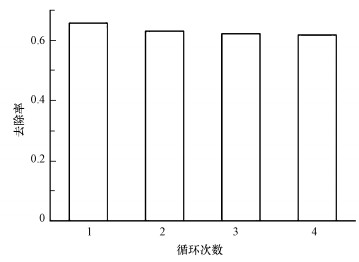 |
| 图 10 催化剂ZnO-PMMA的重复利用 Fig. 10 Reuse of the ZnO-PMMA |
已有文献报道, 纳米ZnO使用广泛, 但具有一定的生物毒性(Zheng et al., 2011); 且由于纯纳米ZnO尺寸小, 催化结束后只能高速离心回收, 应用于实际生活污水、农业废水时无法回收, 会对环境、生物造成一定损害.将纳米ZnO固定在100 μm左右的PMMA微球表面, 即可通过简单的过滤得到, 减轻了对环境潜在的负面影响, 同时,ZnO-PMMA回收后还可循环使用, 具有良好的经济效益.
4 结论(Conclusions)1)以Zn (NO3)2·6H2O为锌源, 采用水热法制备纳米ZnO, 并通过热粘固法制备ZnO-PMMA复合材料, 所得纳米ZnO为六方晶系纤锌矿结构, 尺寸为200~400 nm, 在PMMA表面分布均匀, 分散性好, 团聚程度低.
2)采用复合材料ZnO-PMMA光催化去除初始浓度为50 mg·L-1的氨氮废水, 在汞灯365 nm光照作用下, 催化剂用量为1.0 g·L-1, 初始pH=12.0, 温度30 ℃, 光照4 h时, 氨氮去除率可达66%, 反应产物为氮气.
3)相较于纯纳米ZnO, 复合材料ZnO-PMMA不易团聚, 在溶液中分散性; 且提高了对紫外光的利用率, 光催化效率提高; 同时, 解决了纳米ZnO难以回收的缺点, 使纳米材料可以简单方便地回收使用, 为实际应用创造了条件, 减轻了对环境的潜在影响, 符合绿色化学的原则.
| [${referVo.labelOrder}] | Antonio Carmona I D, Martínez-Amador S Y, Martínez-Gutiérrez H, et al. 2015. Semiconducting polyurethane/polypyrrole/polyaniline for microorganism immobilization and wastewater treatment in anaerobic/aerobic sequential packed bed reactors[J]. Applied Polymer Science, 132(28) . DOI:10.1002/app.42242 |
| [${referVo.labelOrder}] | 陈晓慧, 柳丽芬, 杨凤林, 等. 2007. CdS/TiO2光催化去除水体中氨氮的研究[J]. 感光科学与光化学, 2007, 25(2) : 89–101. |
| [${referVo.labelOrder}] | Farzana M H, Meenakshi S. 2014. Visible light-driven photoactivity of zinc oxide impregnated chitosan beads for the detoxification of textile dyes[J]. Applied Catalysis A:General, 503 : 124–134. |
| [${referVo.labelOrder}] | Hu X, Hu C, Qu J. 2006. Photocatalytic decomposition of acetaldehyde and Escherichia coli using NiO/SrBi2O4 under visible light irradiation[J]. Applied Catalysis B Environmental, 69(1/2) : 17–23. |
| [${referVo.labelOrder}] | Iknur A, Sökmen. 2015. Buoyant Photocatalyst based on ZnO immobilized on polystyrene beads for pollutants treatment[J]. Clean Soil Air Water, 43(7) : 967–1114. |
| [${referVo.labelOrder}] | 焦宏涛. 2008. 光催化技术在氨氮降解中的应用[J]. 山西建筑, 2008, 34(29) : 216–217. |
| [${referVo.labelOrder}] | 姜瑞, 曾红云, 王强. 2013. 氨氮废水处理技术研究进展[J]. 环境科学与管理, 2013, 38(6) : 131–134. |
| [${referVo.labelOrder}] | 靳立民, 王凤英, 王连寿, 等. 2004. 光催化氧化处理难降解污水的应用前景[J]. 油气田环境保护, 2004, 14(2) : 19–22. |
| [${referVo.labelOrder}] | Kıranşan M, Khataee A, Karaca S, et al. 2015. Artificial neural network modeling of photocatalytic removal of a disperse dye using synthesized of ZnO nanoparticles on montmorillonite[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 140C : 465–470. |
| [${referVo.labelOrder}] | 李元昊, 丁忠浩, 陶小明, 等. 2013. 油田氨氮废水的纳米TiO2光催化处理[J]. 湖北农业科学, 2013, 52(21) : 5186–5188. |
| [${referVo.labelOrder}] | 刘国光, 郭小阳, 郑立庆, 等. 2008. Zr/TiO2纳米管的制备及其光催化活性的初步研究[J]. 环境科学学报, 2008, 28(4) : 710–713. |
| [${referVo.labelOrder}] | 刘莉峰, 宿辉, 李凤娟, 等. 2014. 氨氮废水处理技术研究进展[J]. 工业水处理, 2014, 34(11) : 13–17. |
| [${referVo.labelOrder}] | Pimentel A, Rodrigues J, Duarte P, et al. 2015. Effect of solvents on ZnO nanostructures synthesized by solvothermal method assisted by microwave radiation:a photocatalytic study[J]. Journal of the Chemical Society Perkin Transactions, 50(17) : 1259–1264. |
| [${referVo.labelOrder}] | Rezaee A, Darvishi Cheshmeh Soltani R, Khataee A R, et al. 2012. Optimization of combined photocatalytic involving immobilized ZnO nanoparticles and electrochemical processes for ammoniacal nitrogen removal from aqueous solutions[J]. Journal of Materials Environtal Science, 3(5) : 955–966. |
| [${referVo.labelOrder}] | 商桑斌, 杨幼平, 刘开宇. 2002. 均相成核-水热法制备纳米氧化锌[J]. 精细化工中间体, 2002, 32(4) : 25–28. |
| [${referVo.labelOrder}] | Yao W F, Xu X H, Wang H, et al. 2004. Photocatalytic property of perovskite bismuth titanate[J]. Applied Catalysis B Environmental, 52(2) : 109–111. DOI:10.1016/j.apcatb.2004.04.002 |
| [${referVo.labelOrder}] | 于晓彩, 陈月霞, 刘培. 2010. 纳米ZnO在处理含镉废水中的应用[J]. 沈阳化工大学学报, 2010, 24(2) : 122–125. |
| [${referVo.labelOrder}] | 郑凤英, 李顺兴, 钱沙华, 等. 2007. 水杨酸和5-磺基-水杨酸表面修饰纳米TiO2吸附去除对硝基苯酚[J]. 环境科学学报, 2007, 27(1) : 64–68. |
| [${referVo.labelOrder}] | 周小岩, 于建平, 刘彦民, 等. 2014. 不同形貌纳米ZnO的光催化性能研究[J]. 化工科技, 2014, 22(1) : 7–11. |
| [${referVo.labelOrder}] | Zheng X, Wu R, Chen Y. 2011. Effect of ZnO nanoparticles on wastewater biological nitrogen and phosphorous removal[J]. Environmental Science & Technology, 45 : 2826–2832. |
| [${referVo.labelOrder}] | Zhang Y R, Wan J. 2005. A novel approach of preparing TiO2 films at low temperature and its application in photocatalytic degradation of methyl orange[J]. Hazard Master, 177 : 750–754. |
 2017, Vol. 37
2017, Vol. 37


