2. 江苏省物质循环与污染控制重点实验室, 南京 210023;
3. 南京师范大学地理科学学院, 南京 210023;
4. 云南省环境科学研究院(中国昆明高原湖泊国际研究中心), 昆明 650032
2. Jiangsu Provincial Key Laboratory of Materials Cycling and Pollution Control, Nanjing 210023;
3. School of Geography Science, Nanjing Normal University, Nanjing 210023;
4. Yunnan Institute of Environmental Science(Kunming China International Research Center for Plateau Lake), Kunming 650032
腐殖质是一类无定形大分子物质, 广泛存在于土壤、水体及沉积物中(Senesi, 1990; Matthews et al., 1996; Klavins et al., 1997; Fooken et al., 2000).在土壤中, 腐殖质是土壤有机质的主体, 约占总量的65%, 对土壤的理化性质有重要影响(李学垣, 2001).土壤腐殖质中含有羰基、羧基、羟基、酚羟基等多种活性官能团, 这些官能团能通过离子键、共价键、分子间范德华力等作用力与土壤中的重金属离子、矿物质及毒性有机污染物等发生相互作用, 进而对这些物质的环境行为产生影响(李廷强等, 2004; O′Driscoll et al., 2006).此外, 土壤腐殖质作为全球重要的碳库, 对全球及区域范围内的碳循环有着深刻影响(Battin et al., 2009).通过腐殖质的溶解性特征, 可将其分为富里酸、胡敏酸、胡敏素3类, 其中, 胡敏酸仅在pH > 3时溶于水, 富里酸在所有pH条件下皆可溶于水, 而胡敏素难溶于水(李学垣, 2001).这3类腐殖质由于自身理化性质的差异, 导致其结合有机污染物、络合重金属离子等的能力也不同(张耀玲, 2013).
目前, 滇池流域土壤和水体污染严重, 但相关研究主要集中在氮、磷等营养元素的含量及分布等方面, 对有机质的研究也大都仅限于水体(阳利永等, 2012; 胡斌等, 2012; 程庆霖等, 2014).而土壤中的有机质及其与之结合的营养元素、重金属元素和有机污染物可通过地表径流和地下渗漏等方式迁移到水体中, 从而影响水体的性质.因此, 研究土壤腐殖质不同组分的含量、分布和性质差异, 有利于了解腐殖质与污染物的交互作用, 以及在碳循环中的行为和作为植物生长肥料的活性等, 进而为重金属污染及有机污染的治理、局部碳平衡和提高作物产量提供参考.
在对腐殖质的研究中, 目前较多采用联合树脂提取法(张耀玲, 2013).该提取法得到的腐殖质较为纯净, 胡敏酸和富里酸分离较为完全.但是, 土壤有机质组成复杂, 联合树脂不能吸附的有机质对环境同样有重要影响, 而且, 联合树脂分离出来的腐殖质难以代表土壤活性有机质的整体性质.相比而言, 传统的碱性焦磷酸钠提取法能将土壤中活性有机质(在植物根系和微生物作用下可以释放的有机质)较为完全地提取出来, 从而可以更全面地表征土壤活性有机质的特性.
基于此, 本研究选择环滇池流域的东南部、柴河小流域、双龙水库流域、大河流域为研究区域, 利用紫外-可见光谱和三维荧光光谱相结合的技术, 分析焦磷酸钠提取法所提取的土壤腐殖质不同组分含量和光学特征, 从而了解它们在物质组成、结构特征和来源之间的差异, 以期为深入研究滇池流域污染物的地球化学循环提供理论依据和数据支持.
2 材料与方法(Materials and methods) 2.1 研究区概况滇池位于昆明市西南, 东经102°31′~102°56′, 北纬24°32′~ 25°17′之间, 是云南省最大的淡水湖, 总流域面积2920 km2.气候属于亚热带湿润季风气候, 平均气温14.7 ℃, 年均降雨量1006 mm.成土母质有中生代紫色砂页岩、碳酸盐、第四纪冲积母质、坡积物、第四纪湖积风化母质, 土壤类型主要有红壤、黄棕壤、水稻土(胡斌等, 2012).
2.2 采样时间和地点2014年7月在滇池流域共采集0~20 cm土壤样品46个, 每个样点处采集一个样品, 其中, 柴河流域12个, 滇池流域东部10个, 大河流域8个, 双龙水库流域16个.样点经纬度用GPS进行定位.土壤采集后用黑色聚乙烯自封袋密封带回实验室.避光条件下自然风干, 研磨至过200目筛, 封存于聚乙烯袋中待用.采样点分布如图 1所示.
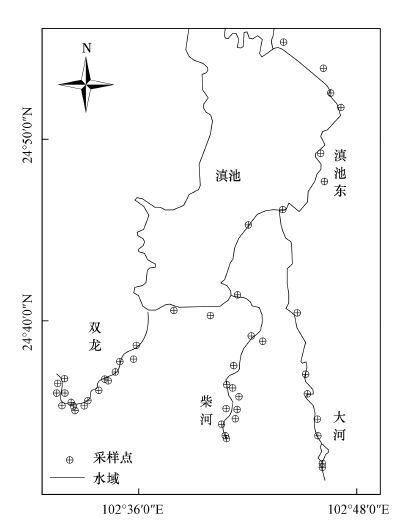 |
| 图 1 滇池流域土壤采样点分布图 Fig. 1 Distribution of soil samples in Dianchi Lake basin |
土壤腐殖质提取采用碱性焦磷酸钠提取法(刘春生等, 1996).用碱性焦磷酸钠溶液浸取出土壤活性腐殖质(P-HEs), 通过调节溶液pH, 分离出胡敏酸(P-HAs)和富里酸(P-FAs), 为了保持土壤有机质性质完整, 土壤中部分小分子有机质也划入富里酸范围.采用Whatman-F滤膜进行抽滤, 滤膜在实验前经过450℃灼烧4 h以去除有机质;实验过程在25 ℃的避光条件下进行;滤液保存于4 ℃棕色玻璃瓶中待测.溶解有机碳(DOC)使用TOC分析仪进行测定.
2.4 光谱参数紫外-可见光谱通过岛津UV-3600光度计测定, 以超纯水为空白, 用10 mm的石英比色皿在240~800 nm范围内扫描, 波段间隔为1 nm.三维荧光光谱使用Lumina 荧光分光光度计测定, 扫描速度为1200 nm·min-1, 间隔时间为20 ms, 扫描范围:激发波长(λEx)为200~400 nm, 发射波长(λEm)为250~550 nm, 带宽均为10 nm.文中有关紫外-可见分光及三维荧光光谱特征参数的表述如表 1所示.
| 表 1 光谱参数描述 Table 1 Description of spectrum parameters |
如图 2所示, 测得滇池流域土壤P-FAs含量为1.49~9.77 g·kg-1, 平均含量为5.75 g·kg-1, 变异系数为40.96%; P-HAs含量为0.42~4.30 g·kg-1, 平均含量为2.33 g·kg-1, 变异系数为36.36%;P-HEs含量为1.93~13.48 g·kg-1, 平均含量为7.92 g·kg-1,变异系数为37.7%.土壤P-FAs含量高于P-HAs, P-HAs约占P-HEs的1/3.
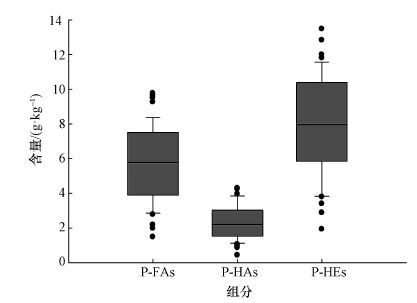 |
| 图 2 滇池流域土壤腐殖质组分含量 Fig. 2 Contents of soil humic fractions in Dianchi Lake basin |
不同土壤利用方式下腐殖质含量及组成会有较大差别.如图 3所示, 在菜地、荒地、草地、湿地4种用地类型中, P-HEs、P-HAs、P-FAs均体现出菜地<荒地<草地<湿地的变化特征.
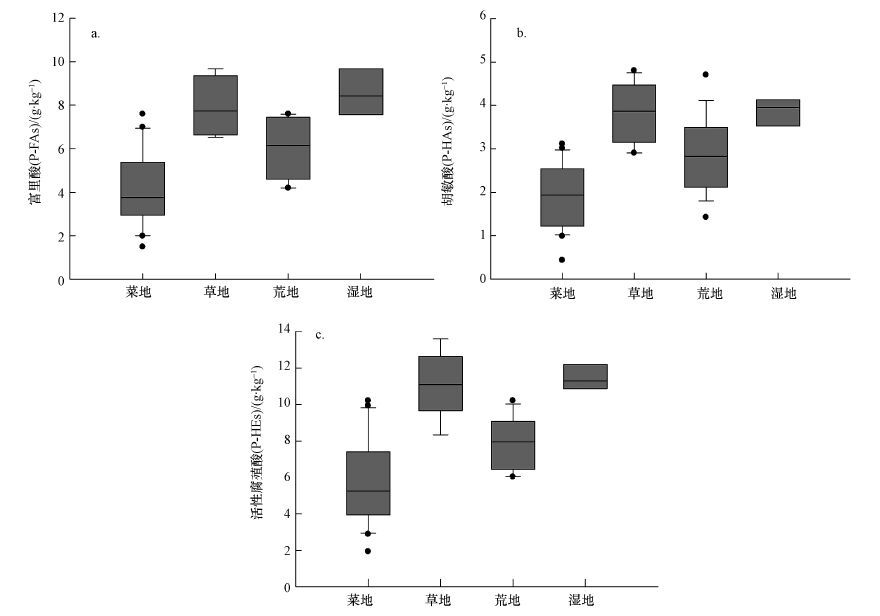 |
| 图 3 滇池流域不同土地类型下P-FAs(a)、P-HAs(b)、P-HEs(c)含量 Fig. 3 Contents of P-FAs(a), P-HAs(b)and P-HEs(c)under different land use types in Dianchi Lake basin |
P-FAs、P-HAs和P-HEs的分子量大小、芳香性、疏水性可通过紫外-可见光谱特征参数来体现, 其统计分析结果呈现在表 2中.
| 表 2 滇池流域土壤腐殖质组分的紫外-可见光谱特征参数及分布 Table 2 Characteristic parameters and its distribution of UV-Vis absorption spectrum from soil humic fractions in Dianchi Lake basin |
SUVA260可用以表征腐殖质疏水性的强弱, 数值越大代表疏水性越强, 疏水组分越多.P-FAs 的SUVA260明显小于P-HAs, 说明胡敏酸比富里酸含有更多疏水组分.
SUVA285可用来表征腐殖质的芳香性, 数值越大则腐殖质芳香度越高, 芳香族基团含量越高.P-HAs的SUVA285均值为17.16±2.40, 高于P-FAs的SUVA285均值11.29±2.15, 表明胡敏酸比富里酸含有更多芳香族基团, 胡敏酸中芳香族CC相对含量较高(Kang et al., 2002).芳香族物质不易溶于水, 这也解释了胡敏酸含有较多疏水组分的现象.
E2/E3(a250/a360) 与腐殖质的分子量及芳香度关系密切, 且呈现负相关关系(Kang et al., 2002).本研究中P-FAs的E2/E3均值为4.67±0.72, 明显大于P-HAs的E2/E3均值2.70±0.28.结合SUVA285结果中胡敏酸的芳香度更高, 可知胡敏酸具有更大的相对分子量.
Sr能够定性反映有机质的地化特征(Helms et al., 2008), 如分子量和光化学潜能, 且与分子量呈反比(Helms et al., 2008; Xiao et al., 2013).结果显示, P-FAs的Sr值大于P-HAs的, 说明富里酸相对分子量小于胡敏酸, 光化学潜能也较低.
从变异系数来看, SUVA260、SUVA285和E2/E3的都呈现出P-HAs<P-HEs<P-FAs的变化特征.但Sr值显示出不同的结果, P-FAs的Sr值变异系数(12.05%)小于P-HAs(18.82%), 且P-HEs的Sr值变异系数(11.56%)比其两个组分(P-FAs、P-HAs)都要小.
3.3 活性腐殖质及其组分荧光光谱特性P-FAs中主要出现类富里酸荧光峰A峰和类蛋白荧光峰B峰.P-HAs中主要出现B峰、可见光区类腐殖酸荧光峰C峰和D峰.P-HEs中同时出现A峰、B峰、C峰和D峰.通常认为, A峰和C峰主要由外源物质的腐殖化形成, B峰则由生物降解来源的色氨酸和酪氨酸形成, 其出现与有机质中芳香环氨基酸结构有关, 但也有学者报道称该峰的出现与人类活动导致的污染有关;D峰则是本地产物降解形成的荧光峰, D峰与腐殖质中的羰基和羧基结构有关(Stedmon et al., 2003; 2005; Cory et al., 2005; 傅平青等, 2005).
从图 4a、4b中可以看出, P-FAs和P-HAs中都出现了B峰, 说明胡敏酸和富里酸中都含有类蛋白峰, 形成过程中都受到微生物的作用;此外, P-FAs中出现的A峰和P-HAs中出现的C峰说明富里酸和胡敏酸受到外源物质如枯枝落叶、生物残体的腐殖化过程贡献;P-HAs中出现C峰和D峰, 说明胡敏酸中含有较多的羰基和羧基结构.图 4c中, A、B、C、D峰在P-HEs中都有出现, 说明滇池流域土壤活性腐殖质受到微生物和外源物质的共同影响, 同时, 因为组分种类多, 含有羰基、羧基、醌类等多种荧光官能团.
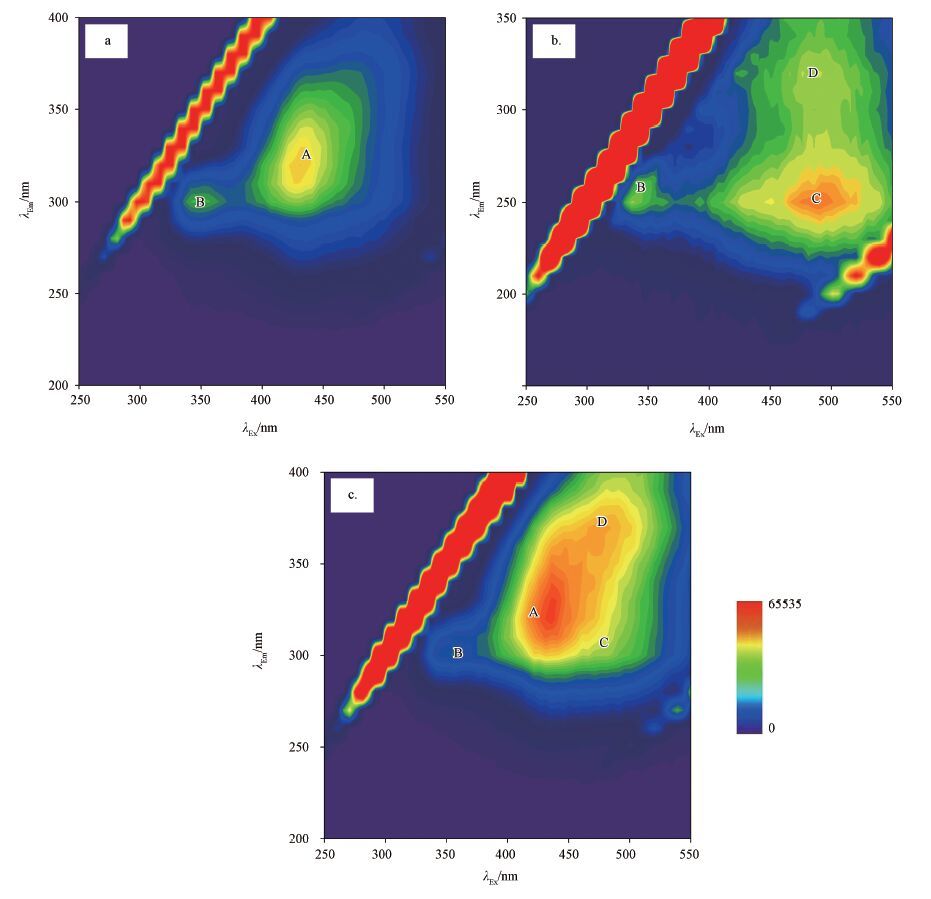 |
| 图 4 滇池流域土壤P-FAs(a)、P-HAs(b)、P-HEs(c)的典型三维荧光光谱 Fig. 4 Typical 3D-EEM spectra of soil P-FAs(a), P-HAs(b)and P-HEs(c)in Dianchi Lake basin |
荧光光谱显示了腐殖质中含有的荧光物质种类, 但要进行定量化的分析, 需要对荧光相关指标进行统计分析.滇池流域土壤P-FAs、P-HAs、P-HEs的BIX、FI统计结果列于表 3中.
| 表 3 滇池流域土壤腐殖质组分的荧光特征参数 Table 3 Characteristic parameter of fluorescence from soil humic fractions in Dianchi Lake basin |
自生源指数BIX是指在254 nm激发波长下, 380 nm和440 nm发射波长处的荧光强度值比, 用以反映有机质自生源相对贡献率, 同时可以评价生物可利用性的高低.BIX数值越大, 说明物质自生源性越强, 同时具有越强的生物可利用性.一般认为BIX<0.6表示弱自生源性, 0.6<BIX<1表示中等自生源性, BIX>1表示强自生源性(Leenheer et al., 2003).富里酸BIX为0.58±0.28, 小于胡敏酸的1.07±0.96, 富里酸具有较小的变异系数, 而活性腐殖质BIX为0.44±0.13, 变异系数比富里酸和胡敏酸都小.
荧光指数FI是指370 nm激发波长下, 450 nm和500 nm发射波长处的荧光强度之比, 是评价有机质来源的重要指标, 可以衡量有机质中芳香物质与非芳香物质相对贡献率和降解程度.该数值与有机质中外源物质所占比重、芳香物质贡献率和降解程度呈正相关关系(Leenheer et al., 2003).富里酸FI为1.55±0.14, 大于胡敏酸的1.10±0.22, 富里酸变异系数较小, 活性腐殖质FI为1.33±0.16, 变异系数小于胡敏酸而大于富里酸.
4 讨论(Discussion) 4.1 活性腐殖质的组成特点及形成原因土壤胡敏酸占有机质的比例常用来表征土壤肥力, 从结果中可知, 滇池流域土壤肥力较低.土壤中有机质腐殖化后首先以相对分子量大的胡敏酸形式存在, 随后在微生物或光降解的作用下, 分解形成富里酸, 最后矿化形成CO2(李学垣, 2001).滇池流域气候温暖湿润, 光照充足, 有利于有机质的分解.胡敏酸在分解过程中形成富里酸, 而富里酸结构相对稳定, 分解较慢, 最终形成富里酸含量大于胡敏酸的现象.当地较大的生物量提供了丰富的有机质原料, 使这一现象更为明显.
从变异系数来看, P-FAs、P-HEs、P-HAs含量变化幅度均较大, 这与滇池流域土壤利用方式的多样性有关:采样区域用地类型有各种农业用地(菜地、花地等)、林地、撂荒地、湿地及河流阶地等.自然状态下的土壤植物生长量少, 对有机质消耗也相对较少, 腐殖质含量高;人工干扰较强的土壤由于施肥耕种等作用, 大量消耗土壤有机质, 腐殖质含量低(McGill et al., 1986; 张金波等, 2005).菜地人工利用率高, 大量消耗土壤中有机质, 导致土壤腐殖质含量大大降低;荒地人工干预小, 但由于微生物作用和光降解作用, 土壤有机质会不断分解, 土壤有机质含量也相对不高;草地具有一定的植物生物量, 草的光合作用固定了大气中的二氧化碳, 土壤有机质呈现较高的现象;湿地生物量大, 同时处于厌气条件下, 有机质分解慢, 因而有机质含量最高.
前文的分析中得出胡敏酸比富里酸具有更大的分子量、更强的芳香性和疏水性.而胡敏酸Sr值变异系数大于富里酸, 且活性腐殖质的变异系数比富里酸和胡敏酸更小, 这一点与其他特征参数不相符合.Sr的变化一般来自于有机质组成的差异(Carder et al., 1989).富里酸易溶于水, 不同来源的富里酸易随水迁移, 从而相对均匀地分布于整个流域范围内, 使富里酸组成差异不明显.而不易迁移的胡敏酸受到当地的生态环境影响, 具有与当地环境相一致的组成, 在研究区域内不同采样点之间差异变得显著.同时, 实验中P-FAs中含有部分小分子物质和人类活性产生的外源性物质, 这些小分子物质具有较为单一的结构, 从而使P-FAs的组成差异减小.活性腐殖质Sr值的异常可能是由高浓度溶液产生的内滤效应造成的.
4.2 光谱特征参数相关性分析前人的研究大多数是通过对紫外-可见吸收光谱和荧光光谱的独立分析, 得到腐殖质的性质, 却鲜有分析吸收光谱和荧光光谱特征之间相关关系的.但是, 吸收光谱和荧光光谱都是从一定角度去反映有机质的结构特性, 将两者结合进行分析将有利于更全面地揭示腐殖质的光学特征及它们产生的原因.
如表 4所示, P-FAs的Sr值与BIX具有显著相关性;P-HAs的Sr值与BIX也具有显著相关性;P-HEs的Sr值与BIX具有显著相关性, E2/E3与FI值具有显著相关性;其他分光特征值与荧光特征值之间相关性不显著.
| 表 4 滇池流域土壤腐殖质组分的紫外-可见吸收光谱与荧光光谱参数相关性 Table 4 Correlations between ultraviolet-visible absorption spectrum parameters and fluorescence spectrum from soil humic fractions in Dianchi Lake basin |
所提取富里酸中含有部分小分子物质, 这代表着土壤中的降解产物和人类活动产生的有机质也包含在其中, 因此, 其自生源指数也较低;Sr值可以反映光化学潜能大小, 人类活动所产生的主要是一些污染物质, 比如农药残留等, 这部分物质性质相对稳定, 对光的敏感程度较弱, 光化学潜力弱, 而其中的自然有机质含有多种生色官能团, 具有较强光化学活性.因此, 代表光化学潜力的Sr值与代表自生源性的BIX值具有一定的相关关系.胡敏酸中自然有机质含量更高, 且含有更多的生色官能团, 对光照更为敏感(Becker et al., 1966), 因此, Sr值与BIX值具有显著的相关性.土壤活性腐殖质由富里酸和胡敏酸组成, 其光化学潜能与自生源性也具有显著相关性.活性腐殖质的E2/E3值与FI具有显著相关性, 且呈现负相关关系, 表明大分子物质具有更强芳香性, 这与前面所得结论相符合.
综合以上分析可以得出, 自生源性和光降解潜力具有正相关关系, 自生源性腐殖质具有更强的光化学活性, 因此, 胡敏酸比富里酸具有更强的光化学与生物活性;滇池流域土壤活性腐殖质兼具外源输入物质和自生源物质.
4.3 滇池流域土壤腐殖质来源光学指标示踪对于自生源指数BIX, P-FAs均值为0.577±0.283, 表现出较弱的自生源特性, 其生物可利用性也较低;P-HAs均值为1.070±0.956, 具有强自生源特性, 也具有较强的生物利用性, 有助于微生物生物群落的形成, 而微生物活动会增加土壤中类蛋白组分, 因此, 在部分胡敏酸样品中会出现较强的类蛋白峰(Stedmon et al., 2005).滇池流域地处亚热带湿润季风气候带, 多雨导致易溶于水的富里酸随水迁移, 从而大大降低了其自生源性;根据分光的结果, 胡敏酸疏水性较强, 不容易迁移, 更多的会停留在产生地, 从而体现出强自生源特性.
P-FAs的变异系数为49.05%, 小于P-HAs的变异系数89.35%, 这也可以说明富里酸的迁移使其在整个流域范围内结构分布相对均匀, 不同地点的结构差异变小.P-HEs的BIX值应该介于其两个组分(P-FAs、P-HAs)之间, 但实测结果表明, P-HEs的BIX值比其两个组分(P-FAs、P-HAs)都要小, 且流域内不同地点间差异也较小, 可能是因为P-HEs样品中有机质含量过高, 荧光光谱会产生多种荧光峰相互叠合的情况, 出现内滤效应(Lakowicz et al., 2006), 影响了荧光峰的位置, 降低准确性.但是, 从数值上也可以看出, 活性腐殖质具有弱自生源特性.
荧光指数FI中, P-HAs的均值为1.10±0.22, 表明富里酸具一定的外源特性, 降解程度较高.同时, P-FAs较大的FI表示富里酸中含有更多的芳香结构, 这一点与前面紫外-可见分光分析结果及BIX指数指示结果不符合.原因是本次采样时间为夏季, 较大的光照强度会使腐殖质发生光降解反应, 这一特点在分光吸光度和BIX指标上会有所体现.而FI同时容易受到腐殖质来源、光学特性及历史光照的影响, 较为不稳定(Helms et al., 2008), 富里酸具有一定的外源特性, 导致其FI值偏大.因此, 在利用FI指标评价腐殖质性质时, 需要结合采样点周边环境及土壤性质等进行分析.
综合而言, 滇池流域土壤胡敏酸具有强自生源性, 大部分生成于土壤中, 由土壤有机质经过腐殖化过程产生且滞留于形成地;富里酸具有一定外源特性, 部分产生于土壤有机质的腐殖化, 一部分由人类活动输入.滇池流域土壤活性腐殖质自生源性弱, 受到人为活动和自然过程综合影响, 同时有一定的降解程度.
5 结论(Conclusions)1) 滇池流域土壤中富里酸含量高于胡敏酸, 土壤活性腐殖质以富里酸为主.滇池流域多样的土地利用方式使土壤腐殖质组成具有较大空间差异.从土地利用类型上来看, 滇池流域土壤活性腐殖质及其组分富里酸和胡敏酸的碳含量均表现为菜地<荒地<草地<湿地.
2) 滇池流域土壤中胡敏酸比富里酸具有更大的分子量、更高的疏水性和芳香性.腐殖质的这种特性使富里酸易迁移, 而胡敏酸更可能滞留在形成地.
3) 自生源性和光降解潜力具有正相关关系, 自生源性物质具有更强的光化学活性;滇池流域土壤活性腐殖质兼具外源物质和自生源性物质, 并经历了一定的降解过程.
4) 富里酸具有弱自生源特性, 生物可利用性低;而胡敏酸具有强自生源特性和较高的生物可利用性, 有利于微生物群落的形成与发展.活性腐殖质具有弱自生源特性, 因此, 所具有的光化学与生物活性低.
| [${referVo.labelOrder}] | Battin T J, Luyssaert S, Kaplan L A, et al. 2009. The boundless carbon cycle[J]. Nature Geoscience, 2(9) : 598–600. DOI:10.1038/ngeo618 |
| [${referVo.labelOrder}] | Becker K H, Bechara J, Brockmann K J. 1993. Studies on the formation of H2O2 in the ozonolysis of alkenes[J]. Atmospheric Environment. Part A. General Topics, 27(1) : 57–61. DOI:10.1016/0960-1686(93)90070-F |
| [${referVo.labelOrder}] | Carder K L, Steward R G, Harvey G R, et al. 1989. Marine humic and fulvic acids:Their effects on remote sensing of ocean chlorophyll[J]. Limnology and Oceanography, 34(1) : 68–81. DOI:10.4319/lo.1989.34.1.0068 |
| [${referVo.labelOrder}] | 程庆霖, 郑丙辉, 王圣瑞, 等. 2014. 滇池水体有色溶解性有机质(CDOM)三维荧光光谱特征[J]. 光谱学与光谱分析, 2014, 34(3) : 698–703. |
| [${referVo.labelOrder}] | Cory R M, McKnight D M. 2005. Fluorescence spectroscopy reveals ubiquitous presence of oxidized and reduced quinones in dissolved organic matter[J]. Environmental Science & Technology, 39(21) : 8142–8149. |
| [${referVo.labelOrder}] | 傅平青, 刘丛强, 吴丰昌. 2005. 溶解有机质的三维荧光光谱特征研究[J]. 光谱学与光谱分析, 2005, 25(12) : 2024–2028. |
| [${referVo.labelOrder}] | Fooken U, Liebezeit G. 2000. Distinction of marine and terrestrial origin of humic acids in North Sea surface sediments by absorption spectroscopy[J]. Marine Geology, 164(3) : 173–181. |
| [${referVo.labelOrder}] | 高洁, 江韬, 李璐璐, 等. 2015. 三峡库区消落带土壤中溶解性有机质(DOM)吸收及荧光光谱特征[J]. 环境科学, 2015, 36(1) : 151–162. |
| [${referVo.labelOrder}] | Helms J R, Stubbins A, Ritchie J D, et al. 2008. Absorption spectral slopes and slope ratios as indicators of molecular weight,source,and photobleaching of chromophoric dissolved organic matter[J]. Limnology and Oceanography, 53(3) : 955–969. DOI:10.4319/lo.2008.53.3.0955 |
| [${referVo.labelOrder}] | 胡斌, 和树庄, 陈春瑜, 等. 2012. 滇池流域土壤氮磷分布特征及关键影响因素研究[J]. 土壤学报, 2012, 49(6) : 1178–1184. |
| [${referVo.labelOrder}] | Jaffrain J, Gérard F, Meyer M, et al. 2007. Assessing the quality of dissolved organic matter in forest soils using ultraviolet absorption spectrophotometry[J]. Soil Science Society of America Journal, 71(6) : 1851–1858. DOI:10.2136/sssaj2006.0202 |
| [${referVo.labelOrder}] | Kalbitz K, Geyer S, Geyer W. 2000. A comparative characterization of dissolved organic matter by means of original aqueous samples and isolated humic substances[J]. Chemosphere, 40(12) : 1305–1312. DOI:10.1016/S0045-6535(99)00238-6 |
| [${referVo.labelOrder}] | Kang K H, Shin H S, Park H. 2002. Characterization of humic substances present in landfill leachates with different landfill ages and its implications[J]. Water Research, 36(16) : 4023–4032. DOI:10.1016/S0043-1354(02)00114-8 |
| [${referVo.labelOrder}] | Klavins M, Apsite E. 1997. Sedimentary humic substances from lakes in Latvia[J]. Environment International, 23(6) : 783–790. DOI:10.1016/S0160-4120(97)00090-1 |
| [${referVo.labelOrder}] | Lakowicz J R. 2006. Principles of Fluorescence Spectroscopy(3rd edtion)[M]. New York: Springer. |
| [${referVo.labelOrder}] | Leenheer J A, Wershaw R L, Brown G K, et al. 2003. Characterization and diagenesis of strong-acid carboxyl groups in humic substances[J]. Applied Geochemistry, 18(3) : 471–482. DOI:10.1016/S0883-2927(02)00100-2 |
| [${referVo.labelOrder}] | 李廷强, 杨肖娥. 2004. 土壤中水溶性有机质及其对重金属化学与生物行为的影响[J]. 应用生态学报, 2004, 15(6) : 1083–1087. |
| [${referVo.labelOrder}] | 李学垣. 2001. 土壤化学[M]. 北京: 高等教育出版社: 19–49. |
| [${referVo.labelOrder}] | 刘春生, 杨守祥. 1996. 农业化学分析[M]. 北京: 中国农业大学出版社. |
| [${referVo.labelOrder}] | Matthews B J H, Jones A C, Theodorou N K, et al. 1996. Excitation-emission-matrix fluorescence spectroscopy applied to humic acid bands in coral reefs[J]. Marine Chemistry, 55(3) : 317–332. |
| [${referVo.labelOrder}] | McGill W B, Cannon K R, Robertson J A, et al. 1986. Dynamics of soil microbial biomass and water-soluble organic C in Breton L after 50 years of cropping to two rotations[J]. Canadian Journal of Soil Science, 66(1) : 1–19. DOI:10.4141/cjss86-001 |
| [${referVo.labelOrder}] | O'Driscoll N J, Siciliano S D, Peak D, et al. 2006. The influence of forestry activity on the structure of dissolved organic matter in lakes:implications for mercury photoreactions[J]. Science of the Total Environment, 366(2) : 880–893. |
| [${referVo.labelOrder}] | Senesi N. 1990. Molecular and quantitative aspects of the chemistry of fulvic acid and its interactions with metal ions and organic chemicals:Part II[J]. The fluorescence spectroscopy approach[J].Analytica Chimica Acta, 232 : 77–106. DOI:10.1016/S0003-2670(00)81226-X |
| [${referVo.labelOrder}] | Stedmon C A, Markager S, Bro R. 2003. Tracing dissolved organic matter in aquatic environments using a new approach to fluorescence spectroscopy[J]. Marine Chemistry, 82(3) : 239–254. |
| [${referVo.labelOrder}] | Stedmon C A, Markager S. 2005. Tracing the production and degradation of autochthonous fractions of dissolved organic matter by fluorescence analysis[J]. Limnology and Oceanography, 50(5) : 1415–1426. DOI:10.4319/lo.2005.50.5.1415 |
| [${referVo.labelOrder}] | 苏冬雪, 王文杰, 邱岭, 等. 2012. 落叶松林土壤可溶性碳,氮和官能团特征的时空变化及与土壤理化性质的关系[J]. 生态学报, 2012, 32(21) : 6705–3714. |
| [${referVo.labelOrder}] | Veeken A, Nierop K, de Wilde V, et al. 2000. Characterisation of NaOH-extracted humic acids during composting of a biowaste[J]. .Bioresource Technology, 72(1) : 33–41. DOI:10.1016/S0960-8524(99)90096-2 |
| [${referVo.labelOrder}] | Xiao Y H, Sara-Aho T, Hartikainen H, et al. 2013. Contribution of ferric iron to light absorption by chromophoric dissolved organic matter[J]. Limnology and Oceanography, 58(2) : 653–662. DOI:10.4319/lo.2013.58.2.0653 |
| [${referVo.labelOrder}] | 阳利永, 吴献花, 赵斌, 等. 2012. 滇池柴河流域不同土地利用方式土壤养分剖面分异[J]. 水土保持研究, 2012, 19(5) : 95–99. |
| [${referVo.labelOrder}] | 张金波, 宋长春, 杨文燕. 2005. 土地利用方式对土壤水溶性有机碳的影响[J]. 中国环境科学, 2005, 25(3) : 343–347. |
| [${referVo.labelOrder}] | 张耀玲.2013.近海环境中天然有机质的分离与表征[D].上海:华东师范大学 |
 2017, Vol. 37
2017, Vol. 37


