2. 四川省低成本废水处理技术国际科技合作基地, 绵阳 621010;
3. 云南开发规划设计院, 昆明 650217
2. International Cooperation Base of Low-cost Wastewater Treatment Technology in Sichuan Province, Mianyang 621010;
3. Yunnan Development Planning and Design Institute, Kunming 650217
随着核工业的发展, 人类对核能这种清洁、高效能源的需求逐渐增加.然而, 核能的开发利用给人类带来巨大的经济和社会效益的同时, 也不可避免的产生了大量放射性核废物.锶-90(90Sr)是一种放射性重金属, 具有化学毒性和放射性的双重危害, 是核事故中污染生态环境的主要核素之一(Yakout et al., 2015); 锶的化学性质类似于钙(Ogawa et al., 2012; Davis et al., 2000), 比较容易形成可溶性化合物, 因而锶的同位素在生态系统中比较容易流动, 通过水、土、动植物进入环境中, 给人体健康和生态环境带来极大危害(Krestinina et al., 2010).目前, 对于锶的处理方法主要有吸附法(Ghaemi et al., 2011; Tu et al., 2015)、沉淀法(Pacary et al., 2010; Warrant et al., 2013)、离子交换法(Ma et al., 2011; Guan et al., 2011)、溶剂萃取法(Ansari et al., 2008)、色层分离法和膜分离法等.在这些方法中, 吸附法以其高效、廉价、无污染的优点引起人们广泛的关注(Tu et al., 2015).
生物碳(biochar)也称生物质碳, 是指生物质在限氧条件下热裂解得到的一类含碳的、稳定的、高度芳香化的固态物质(Beesley et al., 2011).原料来源主要有农作物秸秆(Ahmad et al., 2012; 陈再明等, 2013)、污泥(Chen et al., 2015)、动物粪便(Song et al., 2012)、稻壳(Masulili et al., 2010)等.不同原料制备的生物质碳的孔隙结构、表面性质、pH及养分含量等性质存在一定的差异(Luo et al., 2015), 而这些又是影响生物碳吸附能力的关键因素(Tong et al., 2011).生物碳因其孔隙结构发达、比表面积巨大和独特的表面化学性质(Chen et al., 2014), 已广泛应用于水、土中多种重金属(Zhang et al., 2015; Ahmad et al., 2014; Mohan et al., 2014)和有机污染物(Xu et al., 2015; Ogbonnaya et al., 2013; Mohan et al., 2014)的吸附去除, 这些研究表明, 生物碳具有良好的吸附去除污染物的性能, 成为污染环境治理的重要材料(Zhang et al., 2015).
生物碳的吸附行为可以影响重金属离子在环境中的迁移转化、生态效应及受污染环境的修复等(Bolan et al., 2013; Hsu et al., 2009).李瑞月等(2015)研究发现, 玉米秸秆碳的有机碳及官能团含量较高, 孔隙结构较好, 比表面积大, 可能主要通过表面吸附及官能团的络合作用去除溶液中Pb2+、Cd2+. Mohan等(2007)用木材或树皮快速热解制得的生物碳吸附Pb2+、Cd2+、As3+, 表明生物碳对金属离子的吸附作用主要是离子交换. Hamilton等(2016)表明生物碳作为土壤改良剂, 添加到珊瑚土壤可提供足够的K来抑制土壤和植物吸收137Cs. Kimura等(2014)发现生物碳能够减少放射性铯的浓度小于10 Bq·kg-1, 在中性和碱性条件下吸附放射性铯的能力取决于源材料及其激活条件.Yakout等(2015)用水稻秸秆生物碳吸附锶, 吸附动力学符合准二级动力学模型, 最大吸附量是120 mg·g-1, 大于以往吸附剂的吸附量, 吸附过程是放热反应, 且吸附机制主要为离子交换.
生物碳对核素具有良好的吸附性能, 可有效降低核泄漏后核素在环境中的迁移效率, 及其带来的生态风险.颗粒粒径是生物碳吸附效率的重要影响因素, 但不同粒径生物碳对核素离子的吸附影响还不清楚.本文选择常见的农业废弃物玉米秸秆为原料, 用限氧裂解法制备不同粒度(d50为9.31、20.26、60.77、70.71和101.9 μm)的玉米秸秆生物碳.选择锶为代表, 基于稳定核素锶和放射性核素锶具有相似的化学性质, 选用稳定核素88Sr模拟90Sr进行研究, 采取批量吸附的方法, 比较研究不同粒径生物碳对锶的吸附特性(吸附动力学, 吸附等温曲线)及pH的影响, 结合FTIR和SEM-EDX表征, 探讨了生物碳上的有机组分和无机矿物组分在吸附锶过程中的作用.
2 材料与方法(Materials and methods) 2.1 主要试剂氯化锶、氢氧化钠、盐酸均为分析纯.
2.2 生物碳的制备采用限氧裂解法制备生物碳样品.本研究选取玉米秸秆作为研究对象, 采用分级式冲击磨为粉碎设备, 优化其结构参数和运行工艺参数, 并通过调节分级机频率制备不同粒径的玉米秸秆粉体, 将不同粒径的玉米秸秆粉体于100 ℃烘干24 h后, 称取5种粒径的玉米秸秆粉体于坩埚中, 压实后盖上盖子(限氧状态), 置于马弗炉中在350 ℃下碳化(升温速率为5 ℃·min-1, 保温6 h), 冷却至室温后得到生物碳, 置于干燥塔中, 作后续表征及实验用.本文选择350 ℃作为裂解温度是基于在实验温度范围内(100、350、500、700 ℃), 350 ℃裂解的生物碳对锶吸附性能最佳.较低温度碳化的生物碳由于其具有更为丰富的极性官能团, 对重金属具有较好的吸附能力(Ahmad et al., 2014). 张明等(2015)也研究表明在350 ℃左右, 获得性能优良的浒苔生物碳, 虽然比表面积较低, 但对萘具有较强的吸附去除能力.
2.3 结构表征参照《木碳和木碳试验方法》(GB/T17664-1999) 测定生物碳中灰分的含量.生物碳的CHN百分比含量采用CHN元素分析仪测定, O元素含量通过差减法得到; 样品平行测定2次, 用平均值计算各吸附剂中有机质组分H/C和(O+N)/C的原子比.粒度分布采用LS13320激光粒度干法分析测定, 测试范围: 0.375~2000 μm; 根据粒径分析结果(图 1), 5个生物碳样品分别标记为BC-9.31、BC-20.26、BC-60.77、BC-71.07、BC-101.9, 其后面数字代表样品的中值径(单位μm).生物碳比表面积(SA)采用全自动比表面和孔径分布分析仪测定:样品在100 ℃条件下真空脱气12 h后, 在液氮温度77 K时测定吸附剂对液氮的吸附作用, 最后采用多点BET法计算比表面积. Zeta电位(ZS90) 测定:称取30 mg生物碳样品于具有不同pH的20 mL的水溶液中(pH由NaOH和HCl调节).盖上盖子, 振荡悬浮后置于暗处, 取含有生物碳颗粒的悬液测定Zeta电位, 同时利用pH计测定上清液pH.采用KBr压片法制样, 傅立叶变换红外光谱仪(Nicolet-5700) 测定生物碳红外光谱图; 扫描范围: 400~4000 cm-1, 分辨率:优于0.5 cm-1, 波数精度: 0.01 cm-1, 信噪比: 100000:1 RMS, 测试温度为25 ℃, 相对湿度为35%~45%. LTD-S440扫描电子显微镜下观察生物碳表面形貌, 并进行能谱分析.
 |
| 图 1 玉米秸秆生物碳的粒径分布 Fig. 1 Particle size distribution of biochar derived from maize straw |
称取15 mg生物碳样品于8 mL样品瓶中, 加入8 mL不同浓度的氯化锶溶液.样品瓶加盖内垫聚四氟乙烯垫片的盖子, 于(25±0.5) ℃、150 r·min-1避光条件下水平振荡.吸附实验结束后, 取上清液过0.45 μm水相滤膜, 取一定量滤液用原子吸收光谱仪(Perkin Elmer AA700) 测定浓度, 测定波长为460.7 nm.吸附动力学实验中, 锶初始浓度为7.89 mg·L-1, 设置6个时间点(1、3、6、12、24、48 h), 每个时间点设置2个平行(添加生物碳)和2组空白对照(不加生物碳).吸附等温曲线绘制中锶初始浓度为3~100 mg·L-1, 共设置10个浓度点, 吸附时间设为24 h, 每个浓度也设置2个平行和2组空白对照. pH影响实验中, 用0.1 mol·L-1的NaOH和HCl配制不同初始pH值的锶溶液(浓度为7.15 mg·L-1), 共设置1.93、3.05、4.74、6.88、8.02、8.82、9.75、10.07和11. 85共9个初始pH值(在实验pH范围内锶的水解几乎可忽略, logβ1=-13.29, logβ2= -28.51) (Cole et al., 2000), 每个pH值设置2个平行和2组空白对照.
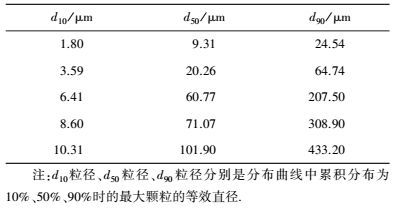
3 结果与讨论(Results and discussion) 3.1 生物碳的结构组成特征生物碳的粒径分布见图 1和表 1.比表面积、灰分和元素组成特征见表 2.如表 2所示, 生物碳的比表面积和灰分含量随着粒径的减小而增大, 中值径d50由101.9 μm减小至9.31 μm, 生物碳比表面积由0.67 m2·g-1增大至3.82 m2·g-1, 相差5.7倍.将生物碳d50与其比表面积作图, 发现两者呈线性负相关(y = 3.94-0.03x, R2= 0.97).灰分含量由23.3%增大至30.9%, 生物碳颗粒大小不同导致灰分含量的差异, 与比表面积不同在限氧裂解过程中接触的氧气体积不同有关.粒径越小, 比表面积越大, 限氧裂解过程中接触的氧气越多, 因此生物碳中灰分最多.如BC-9.31的粒径最小, 比表面积最大, 限氧裂解过程中接触的氧气最多, 因此生物碳中灰分最多, C、N含量最低.
| 表 1 玉米秸秆生物碳的粒径分布 Table 1 Particle size distribution of biochar derived from maize straw |
| 表 2 玉米秸秆生物碳的比表面积和元素组成 Table 2 Surface area (SA) and elemental compositions of biochar derived from maize straw |
粒径大小不仅与比表面积、灰分含量息息相关, 还影响生物碳的元素组成特征.随着粒径的增加, 生物碳的含碳量先增加后降低再升高, 而N、O的含量则先降低后增高再减小.生物碳的芳香性和极性可以通过原子比H/C、(O+N)/C来描述, 即H/C越小, 芳香性越高, 生物碳结构越稳定; (O+N)/C比值越大, 极性越大.随颗粒粒径的增大, 生物碳芳香性略有增强; 而生物碳的极性则随粒径增加, 先降低后增加再减小, 极性最小的是BC-60.77 [(O+N)/C, 0.23].
生物碳的FTIR光谱图如图 2所示. 图 2看出:在3400、2920、1639、1425、1384、1160、780、559和470 cm-1等处有较明显的吸收峰, 表明生物碳表面含有丰富的羟基、羧基、酯羰基、吡啶等官能团(简敏菲等, 2016).其中3400 cm-1附近的宽峰为羟基的O-H的伸缩振动(Inyang et al., 2010; Mohamed et al., 2010), 2920 cm-1处为脂肪性CH2的不对称伸缩振动(Xiao et al., 2014; Keiluweit et al., 2010), 在1639 cm-1处为芳环C=C和C=O的伸缩振动(Kloss et al., 2012; Keiluweit et al., 2010), 1425 cm-1处为C=C的伸缩振动、α-C-H2的弯曲振动, 1384 cm-1处为O-H的弯曲振动, 1160处为脂肪链C-C和醇羟基峰, 1047、780和470 cm-1处的吸收峰为无机矿物Si-O-Si振动吸收(Yang et al., 2008).当d50由9. 31 μm增大至101.90 μm时, 生物碳中的Si-O-Si峰随着粒径的减小而略有增强, 这与灰分含量增加有关, 但生物碳表面有机官能团组成非常相似.
 |
| 图 2 玉米秸秆生物碳的红外光谱图 Fig. 2 FTIR spectra of biochar derived from maize straw |
生物碳对锶的吸附动力学曲线见图 3.在最初的6h内, 生物碳的吸附速率较快, 之后便很快趋于平衡.最细的生物碳BC-9.31吸附速率最快, 1 h内锶去除率就超过了70%, BC-20.26、BC-60.77、BC-71.07和BC-101.9也在12 h后达到表观平衡状态.说明颗粒粒径越小, 比表面积越大, 吸附速率越快, 越易达到平衡.
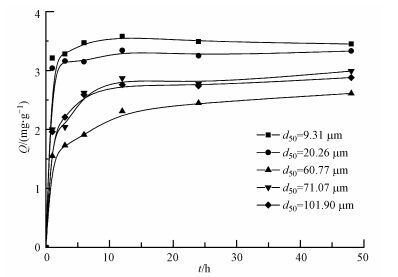 |
| 图 3 玉米秸秆生物碳吸附锶的动力学曲线(锶初始浓度为7. 89 mg·L-1) Fig. 3 Kinetics of strontium adsorption onto biochar derived from maize straw(Initial concentration of strontium for 7.89 mg·L -1) |
分别采用准一级、准二级和颗粒内扩散方程对吸附动力学结果进行拟合.拟合方程分别见式(1)、(2) 和(3).
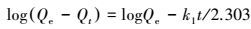
|
(1) |
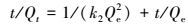
|
(2) |
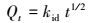
|
(3) |
式中, Qt和Qe分别为t时刻和吸附平衡时锶的吸附量(mg·g-1); t为吸附时间(h); k1、k2和kid分别为准一级动力学(h-1)、准二级动力学(mg·g-1·h-1)和颗粒内扩散(mg·g-1·h-0. 5)模型的速率常数.拟合结果见表 3, 准二级动力学模型的相关系数R2均大于0.99, 说明准二级动力学方程更适合描述生物碳对锶的吸附过程.颗粒最细的BC-9.31吸附速率最大(4.48 mg·g-1·h-1), 是BC-20.26的3倍(1.55 mg·g-1·h-1), 更是BC-60.77的20倍(0.22 mg·g-1·h-1).通常意义上讲, 颗粒粒径越大, 比表面积越小, 吸附速率应该越小.然而, 随着颗粒粒径的进一步增大, 吸附速率却几乎保持不变, 如BC-60.77(0.22 mg·g-1·h-1)、BC-71.07(0.31 mg·g-1·h-1)和BC-101.9(0.23 mg·g-1·h-1).
| 表 3 玉米秸秆生物碳吸附锶的准一级、准二级和颗粒内扩散动力学模型拟合参数 Table 3 Regression parameters of pseudo-first-order, pseudo-second-order and intraparticle diffusion models for the adsorption of strontium by biochar derived from maize straw |
将生物碳的颗粒粒径d50与吸附速率k2拟合, 发现两者呈良好的指数关系(图 4).如图 4所示, 粒径与吸附速率呈指数关系, 25 μm为临界粒径:当d50小于25 μm时, 生物碳的吸附速率随粒径减小而迅速增大; 而当d50大于25 μm时, 生物碳对锶的吸附速率几乎保持不变, 改变粒径的大小对吸附速率没有太大影响.因此, 在25 μm以下调节颗粒尺寸可获得理想的吸附效果, 而在d50大于25 μm时调节颗粒尺寸不能带来预期的吸附效果.
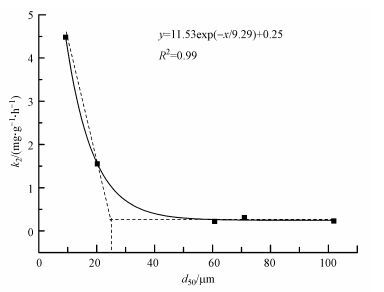 |
| 图 4 玉米秸秆生物碳粒径与锶吸附速率的关系 Fig. 4 Relationship between particle size of biochar derived from maize straw and adsorption rate of strontium |
玉米秸秆生物碳对锶的吸附等温曲线见图 5.由图 5可知, 在低浓度段(0~40 mg·L-1), 锶的吸附量随着溶液浓度的升高而迅速增大, 但溶液浓度进一步增大时(40~80 mg·L-1), 锶在生物碳上的吸附量则趋于平衡.这可解释为当溶液的初始浓度较低时, 吸附剂能够提供充足的吸附位点、活性基团, 而随着溶液初始浓度的不断增加, 吸附位点逐渐饱和, 活性基团相对减少, 则吸附剂达到吸附饱和(El Ashtoukhy et al., 2008).玉米秸秆生物碳对锶的吸附容量为23.81 mg·g-1, 而水稻秸秆碳对锶的吸附容量高达120 mg·g-1(Yakout et al., 2015).这与水稻秸秆碳含有较高的碳酸盐、磷酸盐等无机矿物组分有关, 其PO43-、CO32-可以和重金属离子产生沉淀(李瑞月等, 2015).
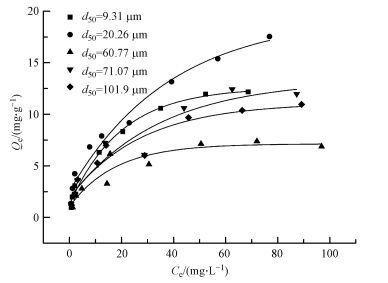 |
| 图 5 玉米秸秆生物碳对锶的吸附等温曲线 Fig. 5 Adsorption isotherm of strontium onto biochar derived from maize straw |
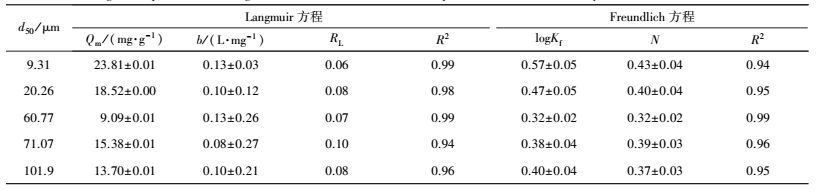
从表 4可知, 玉米秸秆碳对锶的吸附符合Langmuir和Freundlich吸附等温模型.生物碳对锶的吸附容量(Qm)与颗粒粒度显著相关, 随着粒径的增大, 锶的吸附容量先降低后增高又减小.粒径最小的BC-9.31 (23.81 mg·g-1)吸附容量最大, 吸附容量最小的则是BC-60.77(9.09 mg·g-1), 两者相差2.6倍.与此不同的是, 两种生物碳吸附速率则相差20倍(如上所述).可见, 颗粒大小对吸附速率的影响程度要强于对吸附容量的影响.
| 表 4 玉米秸秆生物碳吸附锶的吸附等温曲线的Langmuir和Freundlich拟合参数 Table 4 Regression parameters of Langmuir and Freundlich model for adsorption isotherm of strontium by biochar derived from maize straw |
pH是影响生物碳吸附重金属的重要因素(Kolodyńska et al., 2012).生物碳对溶液中锶的吸附去除率与初始pH值的关系见图 6.在实验pH范围内(1.93~11.8), 5种粒径的生物碳对锶的吸附去除率随pH值增加而逐渐增加. pH值较低时(1.93~4.74), 吸附去除率急剧升高(3.94~9.17倍); 而pH值较高时(4.74~11.8), 吸附去除率缓慢提高(1.11~1.68倍), 且随着pH的增加, 颗粒粒径对生物碳吸附锶的去除率差异减小.如pH值为1.93时, 颗粒粒径的不同会导致吸附率有3.1倍的差异(BC-9.31/BC-60.77);而pH值增至4.70时, 这种吸附率差异只有1.5倍(BC-9.31/BC-60.77); pH值增至11.8时, 各生物碳的吸附去除率已基本相当.因此, 随pH的增加, 颗粒粒径对生物碳吸附锶的影响显著减小.
 |
| 图 6 溶液pH对玉米秸秆生物碳吸附锶的影响 Fig. 6 Effect of solution pH on the adsorption of strontium by biochar derived from maize straw |
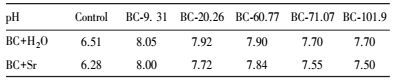
生物碳吸附锶前后的pH值如图 7所示, 在实验pH范围内(1.93~11.85), 5种粒径的生物碳吸附前后pH值的变化趋势均呈S型, 分为5个阶段.第1阶段:初始pH为1.93时, 吸附前后pH几乎保持不变(平衡pH/初始pH=1).第2阶段: pH值为1.93~8.02时, 反应平衡后的溶液pH值显著增大(平衡pH/初始pH>1).第3阶段:初始pH为8.02时, 吸附前后pH几乎保持不变(平衡pH/初始pH=1).第4阶段: pH值为8.02~11.85时, 反应平衡后的溶液pH值显著降低(平衡pH/初始pH<1).第5阶段:初始pH为11.85时, 吸附前后pH几乎保持不变(平衡pH/初始pH=1). pH在3.04~10.07之间, 5种粒径的生物碳吸附锶达到平衡时, pH都在8附近, 可见生物碳具有缓冲作用.
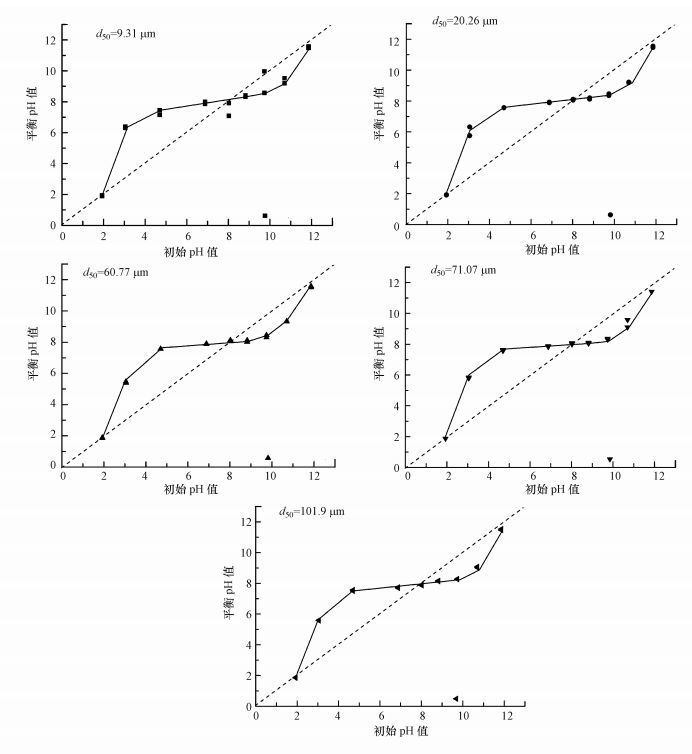 |
| 图 7 玉米秸秆生物碳吸附锶前后的pH值变化 Fig. 7 pH value of strontium solution before and after adsorption of biochar derived from maize straw |
如上所述, 颗粒粒径和pH是生物碳吸附锶的重要影响因子, 而其影响机制又与吸附机理息息相关.以下通过SEM-EDX(图 8)、FTIR(图 9)、吸附构效关系(图 10)、pH分析(表 5)、Zeta电位(图 11、12)分析来探讨生物碳吸附锶的位点和作用机制.
 |
| 图 8 玉米秸秆生物碳吸附锶后的SEM-EDX谱图 Fig. 8 SEM-EDX spectrum of biochar derived from maize straw after adsorption of strontium |
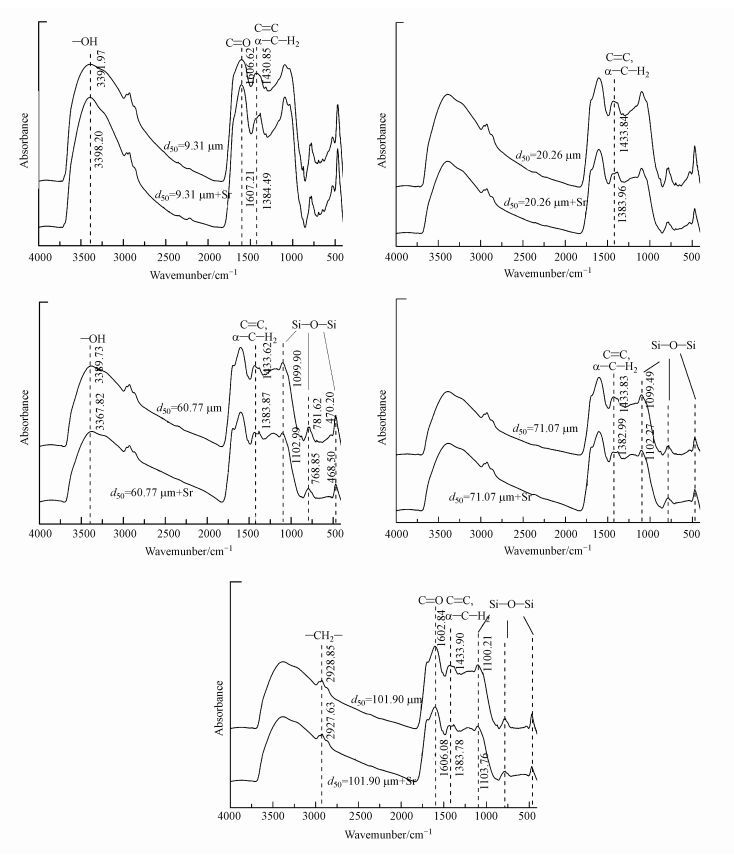 |
| 图 9 玉米秸秆生物碳吸附锶前后的红外光谱 Fig. 9 FTIR spectrum of biochar derived from maize straw before and after adsorption of strontium |
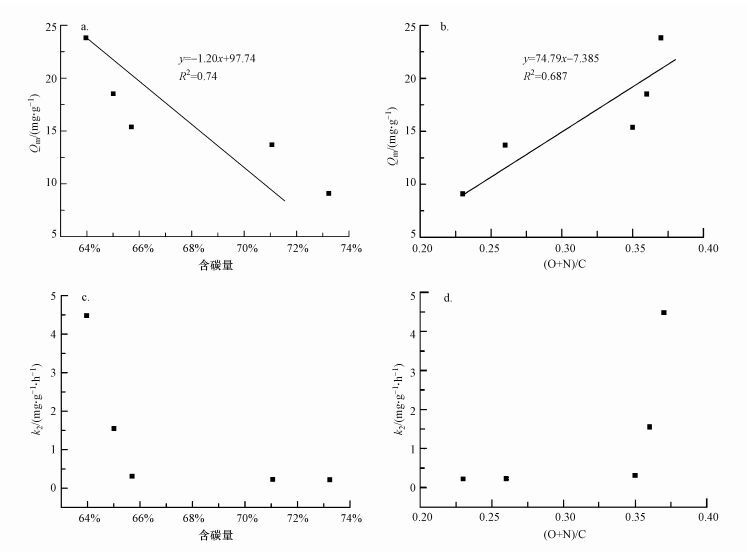 |
| 图 10 玉米秸秆生物碳的含碳量(C)与锶饱和吸附容量的关系(a), 玉米秸秆生物碳的极性参数(O+N)/C与锶饱和吸附容量的关系(b), 玉米秸秆生物碳的含碳量(C)与锶吸附速率k2之间的关系(c), 玉米秸秆生物碳的极性参数(O+N)/C与锶吸附速率k2之间的关系(d) Fig. 10 Relationship between carbon content (C)of biochar derived from maize straw and saturated adsorption capacity of strontium (a), polarity indices (i. e., atomic ratio (O+N)/C) of biochar derived from maize straw and saturated adsorption capacity of strontium (b), carbon content (C)of biochar derived from maize straw and adsorption rate of strontium (c), polarity indices (i. e., atomic ratio (O+N)/C) of biochar derived from maize straw and adsorption rate of strontium (d) |
| 表 5 玉米秸秆生物碳的pH值 Table 5 pH of maize straw derived biochar |
 |
| 图 11 玉米秸秆生物碳的Zeta电位 Fig. 11 Zeta potential of biochar derived from maize straw in water at different solution pHs |
 |
| 图 12 锶的吸附去除率与玉米秸秆生物碳表面负电荷的关系 Fig. 12 Relationship between adsorption rate of strontium and the amount of surface negative charge of biochar derived from maize straw |
SEM-EDX分析发现, 锶(Sr)的谱图与Si重合度较高(图 8中a、b、c、d分别代表Ca、C、Si、Sr的谱图), 表明生物碳中的Si对核素锶有一定的绑定作用.随着粒径的减小, 灰分含量增大, 也有助于矿物对锶的吸附.但利用灰分吸附锶, 效果却很差(相同固液比时灰分几乎无吸附).这与Si的存在形态有关, 350 ℃裂解的生物碳中Si主要为无定型态, 而灰分中的Si主要以SiO2形态存在, 其水解生成表面基团硅醇(-SiOH)与锶发生离子交换(Khalid et al., 2000).
为进一步探讨官能团对生物碳吸附锶的机制, 对比了5种粒径玉米秸秆生物碳吸附锶前后的红外光谱.如图 9所示, 5种粒径的生物碳吸附锶后, 红外峰都发生了一定的变化. BC-9. 31的-OH峰吸附后由3392移至3398 cm-1, 伸缩振动峰-C=O峰由1606移至1607 cm-1, C=C伸缩振动、α-C-H2弯曲振动峰由1431移至1385 cm-1. BC-20.26的C=C伸缩振动、α-C-H2弯曲振动峰由1434移至1384 cm-1. BC-60.77的-OH峰吸附后由3390移至3398 cm-1, C=C伸缩振动、α-C-H2弯曲振动峰由1434移至1384 cm-1, Si-O-Si振动峰发生位置偏移. BC-71. 07的α-C-H2弯曲振动峰由1434移至1383 cm-1, Si-O-Si振动峰由1099移至1102 cm-1. BC-101.9的伸缩振动峰-C=O峰由1603移至1606 cm-1, α-C-H2弯曲振动峰由1434移至1384 cm-1, Si-O-Si振动峰由1100移至1103 cm-1. 5种粒径的生物碳的相似之处在于值于1433 cm-1的C=C伸缩振动、α-C-H2弯曲振动峰漂移至1383 cm-1附近.这表明锶与该有机官能团发生了络合, C电子云密度降低, 能量下降.
生物碳与锶反应后3390、1603、1431cm-1处峰波数发生转移, 说明表面的-OH、-C=O、C=C和α-C-H2等有机基团均与锶的吸附过程有关(Jain et al., 2010; Bansal et al., 2009), 生物碳由于具有高度芳香化和杂环化结构, 其丰富的含氧官能团、芳香类化合物提供的π电子与重金属形成稳定结构, 可以定性判定阳离子-π作用存在于生物碳对锶吸附过程中.无机矿物Si-O-Si振动峰在1099、781、470cm-1处发生峰波数转移与波峰削弱, 说明无机矿物中SiO2参与吸附反应(Khalid et al., 2000).
SEM-EDX和FTIR分析表明, 生物碳的无机矿物和有机碳组分均参与了锶的吸附行为, 但各组分的相对吸附贡献率及粒径和pH的影响机制尚不得而知.大量研究表明, 生物碳吸附重金属的机制包括静电吸附、离子交换、官能团络合等作用(Yakout et al., 2015; 李瑞月等, 2015; Jain et al., 2010), 而各吸附机制的相对贡献率又受到pH的影响.为探讨生物碳对锶的吸附构效关系, 分别拟合了生物碳含碳量和极性参数与锶吸附容量及吸附速率的相关性曲线(图 10).如图 10a所示, 生物碳含碳量与锶的饱和吸附量呈负相关关系, 生物碳含碳量越大, 其吸附容量越小, 这表明含碳组分对锶的吸附贡献较小.与此相反的是, 生物碳的极性指数与锶的饱和吸附量呈良好的正相关关系(图 10b).生物碳极性越大, 锶的吸附容量越大, 这也再次说明极性官能团在锶吸附过程中占有重要贡献.生物碳含碳量与锶的吸附速率的拟合曲线呈L型, 拐点在碳含量65%.当碳含量小于65%时, 吸附速率急剧增加; 而碳含量大于65%时, 锶的吸附速率基本不变(0.22~0.31 mg·g-1·h-1), 说明含碳量越大吸附速率越小(图 10c).生物碳的极性指数则与锶的吸附速率呈反L型曲线关系(图 10d), 拐点在极性指数0.35.当极性指数大于0.35时, 吸附速率快速增加, 而之前吸附速率几乎保持不变.极性指数对于锶的吸附容量和速率显著的影响表明, 极性官能团是生物碳吸附锶的主要贡献位点.
生物碳自身pH是影响锶吸附的重要参数, 也是粒径的重要影响机制.如表 5所示, 生物碳呈弱碱性(pH, 7.70~8.05), 且粒径越小碱性越强, 表明生物碳颗粒粒径越小, 其对质子的吸附能力越强.吸附锶后, 生物碳溶液的碱性减弱, 这主要归因于质子与锶离子发生了竞争吸附.如果质子和锶吸附机制相一致的话, 理论上颗粒粒径越小, 生物碳对锶的吸附容量越大.但事实并非如此, 如BC-60.77吸附容量最小, 但生物碳溶液pH的增幅却位居第二, 表明锶离子吸附与质子吸附机制存在显著差异.
表面电荷是生物碳吸附重金属离子的另一重要参数, 对其吸附性能和吸附机制均有重要影响.当溶液pH﹤pHpzc (等电点)时, 生物碳表面带正电荷, 生物碳表面的金属离子与溶液中的金属离子发生交换, 从而减少溶液中重金属含量; 当溶液pH﹥pHpzc时, 生物碳表面带负电荷, 生物碳通过静电作用吸附溶液中的重金属, 同时, 重金属离子在吸附过程中与生物碳表面的羟基、羧基等含氧官能团发生离子交换反应及氢键吸附(安增莉等, 2011).玉米秸秆生物碳在水中的Zeta电位随溶液的pH变化见图 11, 随着溶液pH的上升, 生物碳的Zeta电位由正值逐渐变为负值, 表明生物碳表面电性由正电荷转变为负电荷. 5种生物碳的Zeta电位曲线非常相似(曲线几乎重叠), 其等电点pHpzc约为2.45.当溶液pH﹤2.45时, 生物碳表面带正电荷, 生物碳吸附重金属离子的机制以离子交换为主, 且生物碳的吸附去除率较低.当溶液pH﹥2.45时, 随着溶液pH的增加, Zeta电位急剧降低, 生物碳表面负电荷急速增加, 静电吸附作用显著增强.生物碳对锶的吸附去除率与表面负电荷量呈线性正相关, 表明静电吸引是生物碳吸附锶的重要机制(图 12).不同粒径的生物碳吸附性能的显著差异与其具有相似的表面电荷特征的矛盾表明, 除了静电吸引外还存在其他重要的吸附机制.构效关系表明极性官能团是锶的主要吸附位点, 因此,推断颗粒粒径带来的吸附差异主要来自生物碳极性官能团的络合作用.随着pH的增加, 极性官能团的水解逐渐增强, 表面电荷逐渐增强, 静电吸附贡献逐渐增加而官能团络合等吸附贡献率逐渐降低, 这也就造成了不同粒径的生物碳颗粒之间的吸附性能差异逐渐减小(当pH值增至11. 8时, 各生物碳的吸附去除率最高且已基本相当, 图 6).
综上所述, 碱性生物碳带负电荷, 其极性官能团是锶的主要吸附位点, 其吸附机制包括静电吸附和官能团络合等作用.颗粒粒径带来的吸附差异机制主要来自极性官能团的络合作用, 而随着pH增加静电吸附贡献逐渐增强, 使得颗粒粒径的差异因此逐渐减小.
4 结论(Conclusions)1) 粒径大小不仅与比表面积、灰分含量息息相关, 还影响生物碳的元素组成特征.随着粒径的增加, 生物碳的比表面积减小, C含量先增加后降低又升高, 而N、O的含量则先降低后增高又减小, 灰分含量降低后略有增加.生物碳的芳香性随着粒径的增大略有增强, 而极性则随粒径增大, 先降低后增加又减小.生物碳呈弱碱性(pH, 7.70~8.05) 且粒径越小碱性越强, 呈负电(pHpzc, 2.45) 且表面电荷特征与粒径没有显著相关性.
2) 生物碳的颗粒粒径对核素锶的吸附速率和吸附容量均有显著影响.生物碳对锶的吸附动力学符合准二级动力学模型(R2, 0.99), 实验粒径范围内(9.31~101.9 μm), 生物碳的吸附速率差异高达20倍.颗粒最细的BC-9.31吸附速率最大(4.48 mg·g-1·h-1), BC-20.26次之(1.55 mg·g-1·h-1), 而BC-60.77、BC-71.07、BC-101.9的吸附速率几乎相当(0.21~0.31 mg·g-1·h-1).粒径与生物碳吸附速率呈指数相关, 临界粒径d50为25 μm, 低于该粒径生物碳的吸附速率呈指数增加, 而高于该粒径生物碳吸附速率基本不变.生物碳对锶的等温吸附曲线符合准Langmuir模型(R2, 0.94~0.99), 饱和吸附容量为9.09~23.81 mg·g-1.相较而言, 粒径大小对生物碳对锶吸附容量的影响程度要远远小于对吸附速率的影响; 研究结果为如何调控颗粒粒径提高生物碳的吸附效率提供理论参考.
3) 生物碳对锶的吸附能力受溶液pH值影响. 5种粒径的生物碳对锶的吸附去除率随pH值增加而逐渐增加. pH值较低时(1.93~4.74), 吸附去除率急剧升高(3.94~9.17倍); 而pH值较高(4.74~11.8), 吸附去除率缓慢提高(1.11~1.68倍).颗粒粒径对生物碳吸附锶的影响受pH控制, pH越小, 颗粒粒径对生物碳吸附锶的影响越显著; pH越大, 颗粒粒径对生物碳吸附锶的影响差异越小.
4) 极性指数对于锶的吸附容量和速率显著的影响表明极性官能团是秸秆玉米生物碳吸附锶的主要位点, 其主要吸附机制是静电吸附和官能团络合作用.颗粒粒径带来的吸附差异机制主要来自极性官能团的络合作用, 而随着pH增加静电吸附贡献逐渐增强, 使得颗粒粒径带来的吸附差异逐渐减小.
| [${referVo.labelOrder}] | Ahmad M, Rajapaksha A U, Lim J E, et al. 2014. Biochar as a sorbent for contaminant management in soil and water:a review[J]. Chemosphere, 99(3): 19–33. |
| [${referVo.labelOrder}] | Ahmad M, Lee S S, Dou X, et al. 2012. Effects of pyrolysis temperature on soybean stover-and peanut shell-derived biochar properties and TCE adsorption in water[J]. Bioresource Technology, 118: 536–544. DOI:10.1016/j.biortech.2012.05.042 |
| [${referVo.labelOrder}] | Ansari S A, Mohapatra P K, Raut D R, et al. 2008. Separation of Am(Ⅲ) and trivalent lanthanides from simulated high-level waste using a hollow fiber-supported liquid membrane[J]. Separation and Purification Technology, 63(1): 239–242. DOI:10.1016/j.seppur.2008.03.037 |
| [${referVo.labelOrder}] | 安增莉, 侯艳伟, 蔡超, 等. 2011. 水稻秸秆生物碳对Pb2+的吸附特性[J]. 环境化学, 2011, 30(11): 1851–1857. |
| [${referVo.labelOrder}] | Bansal M, Singh D, Garg V K. 2009. A comparative study for the removal of hexavalent chromium from aqueous solution by agriculture wastes' carbons[J]. Journal of Hazardous Materials, 171(1): 83–92. |
| [${referVo.labelOrder}] | Beesley L, Moreno Jiménez E, Gomez Eyles J L, et al. 2011. A review of biochar' potential role in the remediation, revegetation and restoration of contaminated soils[J]. Environmental Pollution, 159(12): 3269–3282. DOI:10.1016/j.envpol.2011.07.023 |
| [${referVo.labelOrder}] | Bolan N S, Choppala G, Kunhikrishnan A, et al. 2013. Microbial transformation of trace elements in soils in relation to bioavailability and remediation[J]. Reviews of Environmental Contamination and Toxicology, 225: 1–56. |
| [${referVo.labelOrder}] | Chen T, Zhou Z, Xu S, et al. 2015. Adsorption behavior comparison of trivalent and hexavalent chromium on biochar derived from municipal sludge[J]. Bioresource Technology, 190: 388–394. DOI:10.1016/j.biortech.2015.04.115 |
| [${referVo.labelOrder}] | 陈再明, 陈宝梁, 周丹丹. 2013. 水稻秸秆生物碳的结构特征及其对有机污染物的吸附性能[J]. 环境科学学报, 2013, 33(1): 9–19. DOI:10.11654/jaes.2013.01.002 |
| [${referVo.labelOrder}] | 陈再明, 方远, 徐义亮, 等. 2012. 水稻秸秆生物碳对重金属Pb2+的吸附作用及影响因素[J]. 环境科学学报, 2012, 32(4): 769–776. |
| [${referVo.labelOrder}] | Chen Z M, Xiao X, Chen B L, et al. 2014. Quantification of chemical states, dissociation constants and contents of oxygen-containing groups on the surface of biochar produced at different temperatures[J]. Environmental Science & Technology, 49(1): 309–317. |
| [${referVo.labelOrder}] | Cole T, Bidoglio G, Soupioni M, et al. 2000. Diffusion mechanisms of multiple strontium species in clay[J]. Geochimica Et Cosmochimica Acta, 64(3): 385–396. DOI:10.1016/S0016-7037(99)00324-5 |
| [${referVo.labelOrder}] | Davis J, Cook N D, Pither R J. 2000. Biologic mechanisms of 89SrCl2 incorporation into type I collagen during bone mineralization[J]. Journal of Nuclear Medicine, 41(1): 183–188. |
| [${referVo.labelOrder}] | El Ashtoukhy E S, Amin N K, Abdelwahab O. 2008. Removal of lead (Ⅱ) and copper (Ⅱ) from aqueous solution using pomegranate peel as a new adsorbent[J]. Desalination, 223(1): 162–173. |
| [${referVo.labelOrder}] | Ghaemi A, Torab Mostaedi M, Ghannadi Maragheh M. 2011. Characterizations of strontium (Ⅱ) and barium (Ⅱ) adsorption from aqueous solutions using dolomite powder[J]. Journal of Hazardous Materials, 190(1): 916–921. |
| [${referVo.labelOrder}] | Guan W, Pan J, Ou H, et al. 2011. Removal of strontium (Ⅱ) ions by potassium tetratitanate whisker and sodium trititanate whisker from aqueous solution:equilibrium, kinetics and thermodynamics[J]. Chemical Engineering Journal, 167(1): 215–222. DOI:10.1016/j.cej.2010.12.025 |
| [${referVo.labelOrder}] | Hsu N H, Wang S L, Lin Y C, et al. 2009. Reduction of Cr(Ⅵ) by crop-residue-derived black carbon[J]. Environmental Science & Technology, 43(23): 8801–8806. |
| [${referVo.labelOrder}] | Hamilton T F, Martinelli R E, Kehl S R, et al. 2016. A preliminary assessment on the use of biochar as a soil additive for reducing soil-to-plant uptake of cesium isotopes in radioactively contaminated environments[J]. Journal of Radioanalytical and Nuclear Chemistry, 307(3): 2015–2020. DOI:10.1007/s10967-015-4520-8 |
| [${referVo.labelOrder}] | Inyang M, Gao B, Pullammanappallil P, et al. 2010. Biochar from anaerobically digested sugarcane bagasse[J]. Bioresource Technology, 101(22): 8868–8872. DOI:10.1016/j.biortech.2010.06.088 |
| [${referVo.labelOrder}] | Jain M, Garg V K, Kadirvelu K. 2010. Adsorption of hexavalent chromium from aqueous medium onto carbonaceous adsorbents prepared from waste biomass[J]. Journal of Environmental Management, 91(4): 949–957. DOI:10.1016/j.jenvman.2009.12.002 |
| [${referVo.labelOrder}] | 简敏菲, 高凯芳, 余厚平. 2016. 不同裂解温度对水稻秸秆制备生物碳及其特性的影响[J]. 环境科学学报, 2016, 36(5): 1757–1765. |
| [${referVo.labelOrder}] | Krestinina L, Preston D L, Davis F G, et al. 2010. Leukemia incidence among people exposed to chronic radiation from the contaminated Techa River, 1953-2005[J]. Radiation and Environmental Biophysics, 49(2): 195–201. DOI:10.1007/s00411-009-0257-5 |
| [${referVo.labelOrder}] | Kimura K, Hachinohe M, Klasson K T, et al. 2014. Removal of radioactive cesium (134Cs plus 137Cs) from low-level contaminated water by charcoal and broiler litter biochar[J]. Food Science and Technology Research, 20(6): 1183–1189. DOI:10.3136/fstr.20.1183 |
| [${referVo.labelOrder}] | Keiluweit M, Nico P S, Johnson M G, et al. 2010. Dynamic molecular structure of plant biomass-derived black carbon (biochar)[J]. Environmental Science & Technology, 44(4): 1247–1253. |
| [${referVo.labelOrder}] | Kloss S, Zehetner F, Dellantonio A, et al. 2012. Characterization of slow pyrolysis biochar:effects of feedstocks and pyrolysis temperature on biochar properties[J]. Journal of Environmental Quality, 41(4): 990–1000. DOI:10.2134/jeq2011.0070 |
| [${referVo.labelOrder}] | Koodyńska D, Wnㄆtrzak R, Leahy J J, et al. 2012. Kinetic and adsorptive characterization of biochar in metal ions removal[J]. Chemical Engineering Journal, 197: 295–305. DOI:10.1016/j.cej.2012.05.025 |
| [${referVo.labelOrder}] | Khalid N, Ahmad S, Toheed A, et al. 2000. Potential of rice husks for antimony removal[J]. Applied Radiation and Isotopes, 52(1): 31–38. DOI:10.1016/S0969-8043(99)00115-3 |
| [${referVo.labelOrder}] | Luo L, Xu C, Chen Z, et al. 2015. Properties of biomass-derived biochar:Combined effects of operating conditions and biomass types[J]. Bioresource Technology, 192: 83–89. DOI:10.1016/j.biortech.2015.05.054 |
| [${referVo.labelOrder}] | 李瑞月, 陈德, 李恋卿, 等. 2015. 不同作物秸秆生物碳对溶液中Pb2+、Cu2+的吸附[J]. 农业环境科学学报, 2015, 34(5): 1001–1008. DOI:10.11654/jaes.2015.05.025 |
| [${referVo.labelOrder}] | Mohamed A W, Salah J, Naceur J. 2010. Ammonium biosorption onto sawdust:FTIR analysis, kinetics and adsorption isotherms modeling[J]. Bioresource Technology, 101(14): 5070–5075. DOI:10.1016/j.biortech.2010.01.121 |
| [${referVo.labelOrder}] | Ma B, Oh S, Shin W S, et al. 2011. Removal of Co2+, Sr2+ and Cs+ from aqueous solution by phosphate-modified montmorillonite (PMM)[J]. Desalination, 276(1): 336–346. |
| [${referVo.labelOrder}] | Masulili A, Utomo W, Hadi S, et al. 2010. Characteristics of rice huskbiochar and its influence on the properties of acid sulfate soils and rice growth in West Kalimantan[J]. Agricultural Science, 2(1): 39–47. |
| [${referVo.labelOrder}] | Mohan D, Pittman C U, Bricka M, et al. 2007. Sorption of arsenic, cadmium, and lead by n chars produced from fast pyrolysis of wood and bark during bio-oil production[J]. Journal of Colloid and Interface Science, 310(1): 57–73. DOI:10.1016/j.jcis.2007.01.020 |
| [${referVo.labelOrder}] | Mohan D, Sarswat A, Ok Y S, et al. 2014. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent-A critical review[J]. Bioresource Technology, 160: 191–202. DOI:10.1016/j.biortech.2014.01.120 |
| [${referVo.labelOrder}] | Ogbonnaya U, Semple K T. 2013. Impact of biochar on organic contaminants in soil:a tool for mitigating risk[J]. Agronomy, 3(2): 349–375. DOI:10.3390/agronomy3020349 |
| [${referVo.labelOrder}] | Ogawa K, Washiyama K. 2012. Bone target radiotracers for palliative therapy of bone metastases[J]. Current Medicinal Chemistry, 19(20): 3290–3300. DOI:10.2174/092986712801215865 |
| [${referVo.labelOrder}] | Pacary V, Barré Y, Plasari E. 2010. Method for the prediction of nuclear waste solution decontamination by coprecipitation of strontium ions with barium sulphate using the experimental data obtained in non-radioactive environment[J]. Chemical Engineering Research and Design, 88(9): 1142–1147. DOI:10.1016/j.cherd.2010.01.006 |
| [${referVo.labelOrder}] | Song W, Guo M. 2012. Quality variations of poultry litter biochar generated at different pyrolysis temperatures[J]. Journal of Analytical and Applied Pyrolysis, 94: 138–145. DOI:10.1016/j.jaap.2011.11.018 |
| [${referVo.labelOrder}] | Tu Y J, You C F, Chen Y R, et al. 2015. Application of recycled iron oxide for adsorptive removal of strontium[J]. Journal of the Taiwan Institute of Chemical Engineers, 53: 92–97. DOI:10.1016/j.jtice.2015.02.020 |
| [${referVo.labelOrder}] | Tong X J, Li J Y, Yuan J H, et al. 2011. Adsorption of Cu(Ⅱ)by biochar generated from three crop straws[J]. Chemical Engineering Journal, 172(2): 828–834. |
| [${referVo.labelOrder}] | Warrant R W, Reynolds J G, Johnson M E. 2013. Removal of 90Strontium and 241Am from concentrated Hanford chelate-bearing waste by precipitation with strontium nitrate and sodium permanganate[J]. Journal of Radioanalytical and Nuclear Chemistry, 295(2): 1575–1579. DOI:10.1007/s10967-012-1948-y |
| [${referVo.labelOrder}] | Xiao X, Chen B L, Zhu L Z. 2014. Transformation, morphology, and dissolution of silicon and carbon in rice straw-derived biochar under different pyrolytic temperatures[J]. Environmental Science & Technology, 48(6): 3411–3419. |
| [${referVo.labelOrder}] | Xu W Q, Pignatello J J, Mitch A W. 2015. Reduction of nitroaromatics sorbed to black carbon by direct reaction with sorbed sulfides[J]. Environmental Science & Technology, 49(6): 3419–3426. |
| [${referVo.labelOrder}] | Yakout S M, Elsherif E. 2015. Investigation of strontium (Ⅱ) sorption kinetic and thermodynamic onto straw-derived biochar[J]. Particulate Science and Technology, 33(6): 579–586. DOI:10.1080/02726351.2015.1008712 |
| [${referVo.labelOrder}] | Yang H, Xu R, Xue X, et al. 2008. Hybrid surfactant-templated mesoporous silica formed in ethanol and its application for heavy metal removal[J]. Journal of Hazardous Materials, 152(2): 690–698. DOI:10.1016/j.jhazmat.2007.07.060 |
| [${referVo.labelOrder}] | Zhang F, Wang X, Yin D X, et al. 2015. Efficiency and mechanisms of Cd removal from aqueous solution by biochar derived from water hyacinth (Eichornia crassipes)[J]. Journal of Environmental Management, 153: 68–73. DOI:10.1016/j.jenvman.2015.01.043 |
| [${referVo.labelOrder}] | 张明, 徐立恒, 吕黎. 2015. 浒苔生物碳对水中萘的吸附作用[J]. 科技导报, 2015, 33(14): 78–81. DOI:10.3981/j.issn.1000-7857.2015.14.014 |
 2017, Vol. 37
2017, Vol. 37