Degradation of Rhodamine B in aqueous solution by glow discharge electrolysis plasma
1 引言(Introduction)
罗丹明B(RhB)属于蒽醌染料, 该染料组成及结构复杂, 化学稳定性强, 废水色度高, 可生化降解性差, 为有毒难降解有机物(王春英等, 2015).由于RhB结构稳定, 其吸收光谱受溶液pH值影响较小, 因而利用RhB作为模型污染物来评价降解性能已成为有机废水降解研究的热点(徐云兰等, 2012).
与RhB相关的有机废水难以采用传统的物化或生化法处理.近年来, 以光催化氧化、紫外(UV)辐照、O3/UV氧化、H2O2/UV氧化、电化学氧化等为代表的高级氧化技术为难降解有机废水的处理提供了新思路(Ribeiro et al., 2015).辉光放电电解等离子体(GDEP)作为一种新型的高级氧化技术, 为染料等难降解有毒有机物处理提供了一个可供选择的新方法(Joshi et al., 2013).GDEP采用特殊工艺制作的铂丝为阳极, 石墨碳棒为阴极, 当两极间的电压足够高时, 阳极与周围电解液之间产生·OH、·O、·H、H2O2等高活性粒子, 由于·OH的氧化能力(2.80 V)仅次于F2(2.87 V), 高于H2O2(1.77 V), 因而GDEP产生的·OH是一种强氧化剂.另外, ·OH的电子亲和能高达569.3 kJ, 因此, 还具有很强的加成反应特性(Cheng et al., 2016).作为反应的中间产物, ·OH一旦形成, 会诱发一系列自由基链反应, 通过亲电加成、脱氢反应等途径无选择地攻击水体中的各种有机污染物, 最终降解为CO2、H2O和其他矿物质(Jiang et al., 2014; Brisset et al., 2008).再者, GDEP过程中同时伴随紫外(UV)辐照、热辐射、冲击波等物理化学效应, 在多种效应协同作用下最终将有机污染物矿化(Wang et al., 2012).该方法的优点在于:装置简单、操作容易、绿色环保、无二次污染, 且降解彻底(脱色率达95%以上) (李敏睿等, 2015;陆泉芳等, 2006).
目前, 利用GDEP降解有机污染物的研究主要集中于有机物的种类、降解条件的简单优化及降解动力学上(Wang et al., 2012; Jiang et al., 2014), 通过加入Fe2+来协同研究降解行为的报道较少, 且对降解过程中不同因素对降解效果的影响研究并不系统;再者, 降解过程中溶液电导率、pH变化及机理方面的研究更少.基于此, 本文以硫酸钠溶液为电解质, 以罗丹明B(RhB)为模型污染物, 利用紫外分光光度计研究放电电压、溶液浓度、溶液pH、催化剂等对染料降解的影响, 用发射光谱法研究GDEP产生的活性组分, 并通过测定降解过程中溶液的pH和电导率及结合红外光谱相关数据的变化粗略探讨降解机理, 以期为GDEP降解有机污染物的工业化应用提供理论依据.
2 材料与方法(Materials and methods)
2.1 试剂和仪器
罗丹明B(RhB)为生物试剂, 购自天津市光复精细化工研究所;Na2SO4、FeCl2、FeCl3、HCl、CH2Cl2等均为分析纯, 购自国药集团化学试剂公司.LW100J1型直流稳压稳流电源(上海力友电器有限公司), 内置电流表和伏特表;自制铂电极:直径为0.5 mm的铂丝一端封存于锥形石英管中并露出锥口1 mm, 另一端链接导线;直径5 mm的碳棒;pH-211型酸度计(意大利Hanna公司);DDSJ-308F型电导率仪(上海雷磁仪器厂);UV 757CRT Ver 2.00紫外-可见分光光度计(上海科恒实业发展有限公司);八通道高分辨光纤光谱仪(AvaSpec-ULS 2048, 荷兰AvaSpec公司), 波长范围200~1070 nm, 分辨率0. 07 nm, 积分时间1.1 ms;DH 334 T-18U-03型ICCD相机(英国Andor公司);FTS 3000型傅里叶红外光谱仪(美国DIGLAB公司).
2.2 实验装置和实验方法
实验装置见文献(陆泉芳等, 2006).反应液总体积为200 mL, 阴极为直径5 mm的碳棒, 阳极为直径0.5 mm的铂丝.由2 g·L-1 Na2SO4配制浓度分别为10、20、30、40 mg·L-1的RhB溶液作为模拟染料废水, 降解过程中温度保持在(30±2) ℃.
以紫外-可见分光光度计对RhB水溶液进行全波段扫描(200~800 nm), RhB的最大吸收波长为553 nm.降解液的脱色率(η)按下式计算:

|
(1) |
式中, A0和At分别为初始溶液的吸光度和放电t min后溶液的吸光度.发射光谱测量装置见文献(杨恕修等, 2016).
3 结果与分析(Results and discussion)
3.1 电流-电压曲线
图 1为2 g·L-1 Na2SO4溶液中放电的电流-电压(I-U)特性曲线.从图 1可以看出, 电流-电压曲线可分为4部分:AB段(0~200 V), 电流与电压成正比, 遵循欧姆定律和法拉第电解定理;BC段(200~380 V), 焦耳热的作用导致阳极针状电极产生大量水蒸汽泡, 由于水蒸汽的绝缘性, 电流随电压升高而波动下降;CD段(380~500 V), 阳极针尖汽泡被部分击穿, 产生稳定的蒸汽鞘, 同时发出微弱的紫色闪光;DE段(500~650 V), 电流随电压升高而增大, 阳极针尖周围发出明亮的辉光, 产生等离子体, 由于等离子体是可以导电的气体, 因而正常放电下, 电压越高, 电流越大, 产生的辉光越强, DE段称为完全的GDEP过程.由于电压低于550 V时产生的辉光弱, 不易检测到活性粒子, 而电压高于650 V时, 能量较高而Pt针尖变得红热, 再继续升高电压会使阳极过热而熔化损坏, 因此, 降解染料的最佳电压为550~650 V.
图 1内插图为550、600、650 V电压下的辉光照片, 可以看出, 随电压升高, 辉光增强, 产生的等离子体的体积增大.另外也可以看出, 辉光呈现黄色, 这是Na+的焰色反应的缘故.
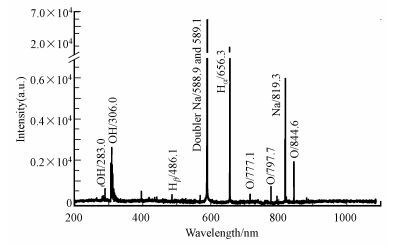
3.2 辉光放电电解等离子体的发射光谱
图 2为600 V电压下GDEP的发射光谱.由图 2可以看出, 波长为283.0~306.0 nm的谱线为OH(A-X)跃迁谱带, 486.1和656.3 nm处为氢原子的Hβ和Hα线;777.1、797.7和844.6 nm处为激发态O原子的跃迁谱线(Jamroz et al., 2012).这是由于在放电过程中电极周围有大量的水被汽化, 电子激发汽化的水分子产生大量·OH、·H、·O(Liu et al., 2012).同时, 588.9和819.3nm处有Na的原子谱线, 说明电解液为钠离子的溶液.
在辉光放电电解过程中, 蒸汽鞘层中的水分子受到高能电子的轰击, 被激发的水分子在极短时间(ps)内分解生成·OH、·H和·O, 其主要分解反应见式(2)~(10) (Liu et al., 2012; Sun et al., 2006; Itikawa et al., 2005).
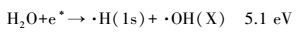
|
(2) |
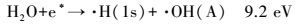
|
(3) |
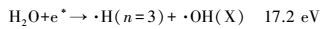
|
(4) |

|
(5) |
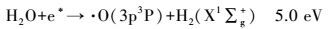
|
(6) |

|
(7) |

|
(8) |

|
(9) |

|
(10) |
当电压达到600 V以上时, 可以很明显地同时观察到OH跃迁谱带、Hα和Hβ跃迁谱线、激发态O原子的跃迁谱线和Na谱线.这是由于此时电子碰撞能量超过了20.4 eV, 同时发生了反应(2)~(10), 生成了大量的·OH、·H、·O.当然, 水分子被激发产生的各种自由基之间也会发生如下反应(Locke et al., 2012):

|
(11) |

|
(12) |

|
(13) |
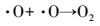
|
(14) |

|
(15) |

|
(16) |
3.3 GDEP降解RhB的紫外光谱
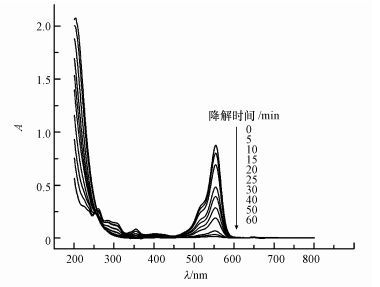
600 V电压下, 200 mL 20 mg·L-1 RhB的紫外-可见光谱随放电时间的变化见图 3.由图 3可知,RhB在259、284、307、355和553 nm处存在明显的吸收峰, 且553 nm处的峰最强.其中, 259和284 nm处为苯环的特征吸收峰, 563 nm处为苯环与C=N和C=C键大共轭体系的特征吸收峰, 即可见光的生色团(徐云兰等, 2012).经过GDEP降解后, 大部分吸收峰都逐渐下降, 表明苯环及C=N和C=C都遭到了破坏.放电60 min后, 吸光度A已趋于0, 说明GDEP对染料RhB的降解效果显著.
3.4 降解液的pH和电导率的变化
图 4为200 mL 60 mg·L-1的RhB在不同放电时间内降解液的pH和电导率的变化.可以看出, 随放电时间的延长, 溶液的pH由最初的5.41逐渐下降到120 min时的4.71, 而后又呈现上升的趋势, 140 min时上升到4.80.相反地, 溶液的电导率先逐渐增大, 然后又存在下降的趋势, 在降解120 min时, 溶液的电导率由1.94 mS·cm-1增大到2.93 mS·cm-1, 之后逐渐减小, 140 min时的电导率为2.81 mS·cm-1.由此说明, GDEP降解RhB的过程中, 不断有酸性中间产物和带电离子产生, 之后这些中间产物降解为CO2、H2O和简单无机盐, 导致pH先减小后增大, 电导率先增大后缓慢减小(李敏睿等, 2015).
3.5 不同电压下脱色率随时间的变化
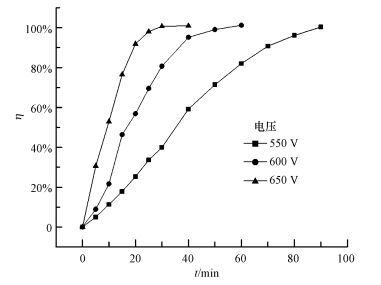
在pH=6.13、20 mg·L-1的RhB的溶液中, 考察了不同放电电压下脱色率(η)随时间的变化关系, 结果见图 5.从图 5可以看出, 同一时间内, 放电电压越大, 脱色率越高.如40 min时, 电压为550、600、650 V的脱色率分别达到59.2%、95.2%、99.9%.这是因为电压升高, 辉光增强, 产生的·OH、·O、·H、H2O2等高活性粒子浓度增加, 导致RhB氧化降解的速率增大.理论上说电压越高脱色速率越快, 但电压高, 能耗大, 且当电压大于650 V时, 阳极铂丝红热而熔化损坏.因此, 选用600 V为最佳放电电压.
3.6 不同初始RhB浓度对脱色率的影响
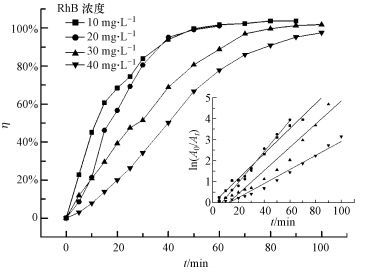
不同RhB初始浓度对脱色率的影响见图 6.RhB初始浓度为10、20、30和40 mg·L-1时, 放电30 min, 脱色率分别为83.9%、80.5%、51.5%和34.2%;放电60 min, 脱色率分别达到99.8%、95.8%、88.8%和77.8%.说明随RhB初始浓度的增大, 脱色率逐渐降低, 延长降解时间有利于高浓度RhB的降解.图 6内插图为ln(A0/At)与时间t的关系, 可以看出线性效果较好, 说明GDEP降解RhB的过程遵从动力学准一级反应.
3.7 溶液pH对脱色率的影响
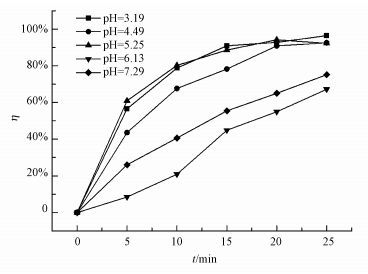
研究发现, 当RhB初始pH值在3.0~8.0之间变化时, 其UV-Vis谱图未发生明显改变, 最大吸收波长约为553 nm, 表明在实验pH范围内, pH不会影响RhB的化学结构.初始溶液pH对RhB脱色率的影响见图 7, 可以看出, 放电15 min时, pH为3.19、4.49、5.26、6.13、7.29时的脱色率分别为91.0%、78.3%、88.6%、44.9%、55.4%%, pH对RhB脱色率的影响顺序为:η(pH=3.19) ≈ η (pH=5.26) > η (pH=4.49) >η (pH=7.29) > η (pH=6.13).为了避免酸对环境的影响, 如果不加催化剂, 可以考虑用pH=5.26的溶液;如果加入催化剂, 可以考虑用pH=3.19的溶液.因为当pH=5.26时, 加入Fe2+在GDEP降解RhB后, 溶液中有Fe(OH)3的棕色絮状沉淀产生, 导致降解溶液呈现棕色或淡棕色而带来二次污染.
3.8 不同催化剂对脱色效果的影响
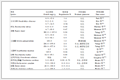
研究发现, 加入Fe2+的量少时, 反应速度慢, 起不到催化作用的效果;加入Fe2+的量过多时, 降解后溶液表现为Fe3+的颜色而导致二次污染, 综合考虑, 加入0.03 mmol效果最佳.因此, 保持其他条件不变, 在不同pH的RhB溶液中分别加入0.03 mmol Fe2+和Fe3+, 同时与未加催化剂的染料的脱色效果进行比较, 结果见表 1.可以看出, Fe2+的催化效果高于Fe3+, 且当pH=3.19时, Fe2+对RhB的脱色率在5 min时可达到98.3%.这进一步说明放电过程中除产生·OH、·H、·O等活性粒子外, 还产生H2O2.当Fe2+存在时, 可与放电产生的H2O2构成Fenton试剂, 生成大量·OH.其机理如式(17)、(18) 所示(Wang et al., 2012), 反应(18) 产生的HO2·又可继续进行如式(19) 所示的反应(李敏睿等, 2015).
表 1(Table 1)
|
表 1 不同pH下催化效果的比较
Table 1 The comparison of the catalytic effect with different pH
|
表 1 不同pH下催化效果的比较
Table 1 The comparison of the catalytic effect with different pH
|
 |
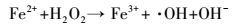
|
(17) |

|
(18) |

|
(19) |
在pH为3.13~4.49时催化效果最好, 这是因为酸性条件下Fe2+及Fe3+可很好地存在, 而在中性和碱性条件下, 它们会生成Fe(OH)3的沉淀, 影响·OH的生成.
图 8为pH=3.19的溶液中加入Fe2+降解5 min前后的紫外光谱, 可以看出, 5 min后降解完全, 吸收峰约为零, 无新的吸收峰产生, 脱色率达到95.6%.
3.9 降解机理的粗略探讨
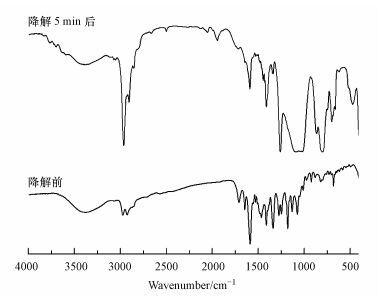
本文测定了降解前和降解20 min后RhB的红外光谱(降解20 min后, 有机物用二氯甲烷萃取, 旋蒸), 结果见图 9.降解前, 3339 cm-1处为O-H伸缩振动, 2973和2927 cm-1处分别为-CH3和-CH2-中C-H的伸缩振动, 1591 cm-1为苯环C=C骨架振动, 1468和1338 cm-1处分别为-CH2-和-CH3中的C-H面内弯曲振动, 1411 cm-1处为-COOH反对称伸缩振动峰, 1274和1244 cm-1处为C-N伸缩振动, 1176、1130和1074 cm-1处为C-O-C伸缩振动, 817和682 cm-1处为苯环C-H面外弯曲振动吸收峰, 这些峰与RhB的红外标准谱图一致.降解20 min后, 3396 cm-1处为O-H伸缩振动, 2960 cm-1处为-CH3中C-H伸缩振动, 1593 cm-1处的峰减弱, 此峰为羧基反对称峰, 1409 cm-1处为羧基对称伸缩振动峰;1274和1244 cm-1处的C-N位移至1258 cm-1处, C-O-C伸缩振动峰加强且移向低波数(1103~1022 cm-1处), 798和696 cm-1处为苯环的面外弯曲振动吸收峰, 由此说明放电过程中发生了复杂的化学变化.综合发射光谱、紫外光谱、溶液pH和电导率的变化, 推断其初步的降解机理为:当RhB存在时, ·OH首先与RhB发生羟基化反应, 形成加成产物;接着RhB的结构被破坏, 生成羧酸类物质;最终生成CO2、H2O和无机盐.
4 结论(Conclusions)
1) GDEP的发射光谱中存在·OH、·H、·O, 放电电压越高, RhB脱色速率越快, 在最佳电压为600 V时, 60 min内可使200 mL 20 mg·L-1的RhB的脱色率达到95%以上.
2) GDEP过程中, RhB的吸光度随反应时间的延长而降低.降解过程中, 259、284、307、355和553 nm处的吸光度逐渐下降, 但最大吸收波长移动很小.
3) 降解过程中溶液的pH值先降低后升高, 而电导率先增大后减小, 说明在GDEP降解RhB过程中产生了酸性中间体和带电离子.
4) Fe2+的催化效果高于Fe3+, 且当pH=3.19时, Fe2+对RhB的脱色率在5 min时可达到98.3%, 证明放电过程中有H2O2产生, 同时其与Fe2+构成Fenton试剂, 生成大量·OH.
5) GDEP作用下, RhB的降解机理为:·OH化作用生成羧酸类物质, 它们继续与活性物种反应, 最终生成CO2、H2O和简单无机盐.


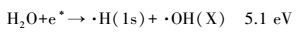
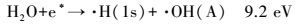
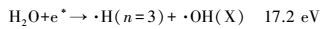

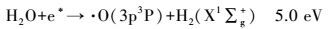










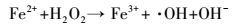



 2017, Vol. 37
2017, Vol. 37



