2. 中国科学院生态环境研究中心, 中国科学院饮用水科学与技术重点实验室, 北京 100085
2. Key Laboratory of Drinking Water Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085
有机砷是一种常见的污染物, 有关有机砷中甲基砷对水环境的污染已被广泛报道, 常见的甲基砷包括一甲基砷(MMA)和二甲基砷(DMA)等.环境中的甲基砷主要来源于以下2个方面:一是人类和大多数动物的尿砷代谢(李景岩等, 2011);二是农药生产过程中的不恰当处置及含砷除草剂的滥用(Xu et al., 2008).人们在地下水中已发现了高浓度的有机砷, 例如, 在台湾东北部和西北部大部分地区的地下水中均发现了DMA的存在, Del Razo等(1990)研究发现, 从北墨西哥收集的井水水样中DMA的浓度高达20 μg·L-1.此外, 鱼类体内DMA的含量曾被发现高达475 ng·g-1(Velez et al., 1996).同样, 一些研究表明, 甲基砷能够导致小白鼠的DNA损伤和染色体畸变, 诱发肿瘤(Xu et al., 2007).因此, 针对水中甲基砷的去除方法已经受到了越来越多的关注, 寻找一种高效而低成本的除砷技术显得十分必要.
前期的研究多关注于As(Ⅲ)和As(Ⅴ)等无机砷的去除, 主要是利用絮凝(Hu et al., 2012)、吸附(Cao et al., 2012)、沉淀(Tresintsi et al., 2012)等方法, 由于这些方法对As(Ⅲ)的去除效果差强人意, 利用化学氧化如次氯酸盐、臭氧氧化、芬顿氧化等将As(Ⅲ)转化为As(Ⅴ)成为了提高砷去除率的有效方法.有机砷的去除近些年才引起人们的关注, 研究表明, 二甲基砷很难通过传统的氧化或絮凝(Hu et al., 2015)去除.而吸附材料如铁氧化物、铝氧化物、氧化钛等对甲基砷的去除效率远低于无机砷(Xu et al., 2007;Wei et al., 2011).刘文婧等(2016)应用TiO2研究了甲基砷(DMA和MMA)的光催化转化过程, 在反应过程中, MMA和DMA被转化成As(Ⅴ), 然后被TiO2吸附去除, 其中, 主要通过活性氧基团如·OH、HO2·等降解有机砷.而将有机砷氧化为As(Ⅴ)极大地改善了溶液中总砷的去除效率.
近年来, 随着高级氧化技术(AOPs)的不断发展, 其在难降解有机废水处理上发挥了越来越重要的作用.芬顿法作为高级氧化技术的一种, 与传统的其他处理方法相比具有较为明显的优势, 其特点在于利用廉价的Fe2+与H2O2反应生成·OH, 进而降解各种有机污染物.有研究通过芬顿反应快速地氧化有机砷(如氯苯砷酸和洛克沙砷), 同时将产生的无机砷絮凝吸附去除(Xie et al., 2016).尽管在芬顿反应中砷能够通过氧化并被絮体吸附而高效去除, 但Fe2+投量很难与H2O2浓度匹配, 无法发挥最大的催化产生·OH的能力, 从而无法保证最佳的处理效率;此外, H2O2也存在存储的安全风险.相比于传统芬顿法, 电芬顿法具有可原位产生H2O2, 且产物H2O2利用率高等优点, 因而逐渐受到广泛关注.基于此, 本研究利用一种能够在线同时产生2种芬顿试剂(Fe2+/H2O2)的双阴极感应电芬顿反应方法, 在电芬顿反应体系中引入感应铁阳极, 通过感应电化学反应发生Fe2+的阳极溶出反应溶出Fe2+.同时, 利用感应电芬顿方法研究其在不同初始pH、电流密度及不同污染物初始浓度下对DMA的降解效果与机理.
2 材料与方法(Materials and methods) 2.1 实验材料硫酸(H2SO4)、氢氧化钠(NaOH)、无水硫酸钠(Na2SO4)购自国药化学试剂公司, 二甲基砷酸钠C2H6AsNaO2·3H2O(J & K, China)、一甲基砷酸钠CH4AsNaO3·1.5H2O(Sigma, USA)、砷酸钠Na2HAsO4·7H2O(Sigma, USA)均为分析纯, 活性炭纤维(ACF)由山东雪圣科技有限公司提供;实验所用水由Milli-Q超纯水机制得(18.2 MΩ);电源为DH1718E-4型直流双路跟踪稳压稳流电源(北京大华电子);铁棒为市购, 使用前在碱性溶液中浸泡并用砂纸打磨.
2.2 感应电芬顿降解DMA实验过程感应电芬顿降解DMA实验中, 在特制石英反应器中加入120 mL浓度为5 mg·L-1的DMA储备液.阳极采用尺寸为2.5 cm×5 cm的RuO2/Ti网状电极, 阴极为2个4 cm×5 cm的活性炭纤维电极.用0.2 mol·L-1 H2SO4或0.2 mol·L-1 NaOH调节溶液pH值, 电解质为0.05 mol·L-1的Na2SO4, O2流量为50 mL·min-1.ACF电极在使用前用反应的DMA溶液多次吸附达到饱和, 用以消除吸附对实验结果的影响.在铁棒经碱性溶液中浸泡并用砂纸打磨处理后, 将其固定于2个阴极之间靠近阳极的位置, 其中, 铁棒直径为4 mm, 浸入长度为5.5 cm, 经计算浸入面积为690.8 mm2.实验装置如图 1所示.通电后开始实验, 分别在0、5、10、20、30、60、90、120、180、240 min取样, 用0.22 μm膜过滤并稀释.
 |
| 图 1 感应电芬顿实验装置示意图 Fig. 1 Sketch map of experimental device on the field-induced electro-Fenton process |
将反应过程中形成的水合羟基铁絮体和ACF阴极加盐酸溶解, 采用高效液相色谱电感耦合等离子体质谱联用技术(HPLC-ICP-MS)测定水样、絮体和ACF阴极中DMA、MMA、As(Ⅲ)和As(Ⅴ)浓度, 检测条件为:Hamilton PRP-X100色谱柱(250 mm×4.1 mm, 10 μm), 柱温30 ℃, 进样量20 μL, 流动相为15 mmol·L-1 (NH4)2HPO4缓冲溶液(用冰醋酸调节pH=6), 流速为等速(1.0 mL·min-1), RF入射功率为1380 W, 载气为高纯氩气, 载气流速1.12 L·min-1, 泵速0.3 r·s-1, 检测质量数m/z=75(As)(Liu et al., 2013).采用ESR波谱仪(Bruker A300-10/12 ESR波谱仪)测定自由基种类和浓度, 使用的自由基加和试剂为DMPO.检测条件为:中心场强3511.940 C, 扫描宽度为100.000 G, 解析点1024, 微波频率为9.857 GHz, 功率2.301 mW(奚倩等, 2014).实验开始前配制体积分数10%的DMPO溶液, 现用现配, 冷冻保存.在检测时, 取得反应溶液后马上与之前配好的10%的DMPO充分混合并立即测定, DMPO在所测水样中的体积分数为1%.
Fe2+浓度用传统的邻菲罗啉分光光度法检测:取反应溶液1 mL, 加入1 mL邻菲罗啉和1 mL醋酸-醋酸钠溶液, 定容至10 mL, 于λ=510 nm处用紫外/可见分光光度仪(U-3010, 日立公司)测定有色络合物的吸光度, 检测限为1.1×10-4 mg·L-1.H2O2浓度的测定方法:取1.50 mL待测溶液于石英比色皿中, 依次加入0.75 mL邻苯二甲酸氢钾(0.1 mol·L-1)和0.75 mL KI(0.4 mol·L-1)溶液, 混合均匀, 静置2 min, 于λ= 352 nm处测定吸光度(ε=10-6 mol·L-1)(Ge et al., 2004).
3 结果与讨论(Results and discussion) 3.1 感应电芬顿降解DMA 3.1.1 初始pH对DMA降解的影响研究了不同初始pH值时感应电芬顿DMA的降解效率, 结果如图 2a所示, 其中, 电流密度J=2 mA·cm-2, 氧气通量50 mL·min-1, DMA溶液初始浓度C0=5 mg·L-1.反应240 min后, 在初始pH值分别为2、3、4、5和7时, DMA去除率分别为88.0%、94.4%、91.7%、86.0%和68.5%, 酸碱度显著影响DMA的去除效果.酸性介质中, 阴极不断将O2还原为H2O2, 并与溶出的Fe2+发生芬顿反应, 本实验中pH=3时去除效果最好, 这与前人研究一致(Rivas et al., 2016; Guivarch et al., 2003).当pH为2时, DMA降解效率下降, 与形成了不同铁的络合物有关, 例如, 在电芬顿体系中[Fe(Ⅱ)(H2O)6 ]2+与H2O2反应要比[Fe(Ⅱ)(OH)(H2O)5]+与H2O2反应更慢(式(1)), 从而导致·OH产量变少(Xie et al., 2016);而且在pH低于3时, 会有大量的·OH被H+分解掉.当pH值高于3时, 虽然较高的pH利于电絮凝产生絮体将污染物聚集吸附去除, 但生成的铁络合物既会阻止感应电芬顿反应中Fe2+与H2O2的反应, 又会影响Fe3+/Fe2+的界面转化过程, 从而阻碍了·OH的生成(Xu et al., 2004);同时, 界面上溶出的Fe3+和Fe2+水解形成的沉淀会导致H2O2分解, 同样会使·OH的产量下降, 最终导致氧化效率下降(Guedes et al., 2003).经检测, 反应过程中pH大致在3.0~3.6之间, 因此, 在感应电芬顿去除DMA时, 初始pH宜保持在3左右.
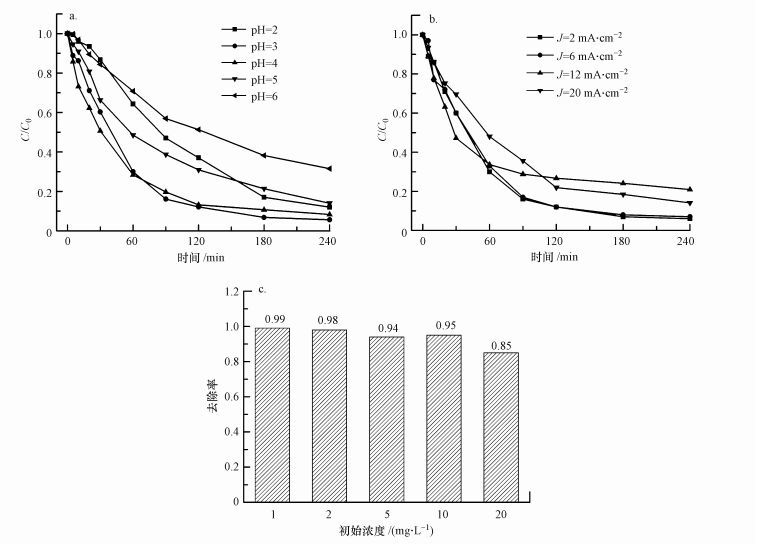 |
| 图 2 不同因素对感应电芬顿反应的影响(a.pH, b.电流密度, c. DMA初始浓度) Fig. 2 Effect of different factors on the Field-Induced Electro-Fenton process(a.pH, b.current density, c.initial DMA concentration) |

|
(1) |
不同电流密度(J)对DMA的去除率如图 2b所示, 其中, 初始pH= 3, 氧气通量50 mL·min-1, DMA初始浓度C0=5 mg·L-1.电流密度分别为2、6、12和20 mA·cm-2, 反应240 min时, DMA去除率分别为94.4%、93.0%、79.1%和85.9%.通常, 随着电流密度的提高, 电生的H2O2浓度和从铁棒表面溶解产生的Fe2+均会相应提高, 产生更多的·OH, 从而氧化能力增强.但DMA的降解效率并不是随电流密度的增大而增大的, 当电流强度超过H2O2生成所需的能量, H2O2会进一步被电化学还原, 从而使电流效率降低(李建斐等, 2015;王玉玲等, 2002);而且当H2O2浓度升高、·OH的产量增加时, 过量的·OH在发生自身猝灭的同时也被H2O2捕获, 造成H2O2与·OH相互消耗(Kremer et al., 1999).感应电芬顿过程中H2O2的生成速率如表 1所示.
| 表 1 感应电芬顿反应中H2O2的生成速率 Table 1 The production rate of H2O2 on the field-induced electro-Fenton process |
本研究感应电芬顿反应中Fe2+来源于感应电极反应, 一是在电场作用下, 处在电场中的铁棒表面会产生感应电流, 铁棒的两面分别对着2个阴极,带有正电, 相当于阳极的作用, 铁棒上就会发生Fe2+溶出反应(式(2)).二是反应体系中pH在3.0左右, 铁电极与溶液中H+发生氧化还原反应生成Fe2+(式(3)), 其中, Fe2+的溶出速率如表 2所示.

|
(2) |
| 表 2 感应电芬顿反应中Fe2+的溶出速率 Table 2 The dissolution rate of Fe2+ on the field-induced electro-Fenton process |
随着电流密度的增大, 单位时间内铁棒上溶出的Fe2+增多, 当Fe2+浓度高于电生H2O2的浓度时, 过多的Fe2+捕获芬顿反应产生的·OH生成Fe3+(式(4)), 从而使·OH利用率降低(Benitez et al., 2001).再加上芬顿反应生成的Fe3+, 过量的Fe3+会与OH-反应生成水合羟基铁.铁的絮体在吸附污染物的同时, 会导致H2O2分解成H2O和O2, 降低氧化降解能力.并且生成的Fe3+也会与H2O2反应生成低氧化能力的HO2·, 从而使DMA去除率降低(Neyens et al., 2003).

|
(4) |
由图 2c可知(初始pH=3, 电流密度J=2 mA·cm-2, 氧气通量50 mL·min-1), DMA溶液在初始浓度分别为1、2、5、10和20 mg·L-1, 反应时间为240 min时, DMA的去除率分别为99.0%、98.0%、94.4%、95.0%和85.0%.由图可知, 随着DMA初始浓度的提高, 感应电芬顿对DMA的去除率呈降低趋势.这是由于一定电流密度下感应电芬顿反应产生·OH的浓度是一定的, 单位时间内氧化降解的DMA分子数是一定的.因此, 当DMA初始浓度提高时, 单位时间内DMA去除率会相应降低.
当DMA初始浓度增加时, 溶液中有机物浓度会保持一个相对较高的值, 在某种程度上增大了有效碰撞几率, 使得电解产生的·OH得到更有效的利用, DMA降解效率相对较高.同时, 较高的初始浓度有利于絮体对污染物的吸附去除.这解释了反应进行240 min后各个初始浓度处理效果有差别但相差不大的原因.因此, 在反应过程中·OH浓度一定时, 合适的有机物浓度有利于提高感应电芬顿反应的效能.
3.2 感应电芬顿降解二甲基砷机理研究认为, ·OH是芬顿和电芬顿主要氧化活性物种.本研究中应用自旋捕捉剂(DMPO)捕捉体系内性质极不稳定的·OH, 通过ESR波谱仪检测了·OH生成情况, 结果如图 3a所示.电流密度为J=2 mA·cm-2, 分别在反应0 min和30 min取样.由图可知, 0 min时没有检出·OH, 在反应30 min时出现了峰高为1:2:2:1的·OH特征峰(艾仕云等, 2003), 表明感应电芬顿与电芬顿情况类似, ·OH是主要氧化活性物种.
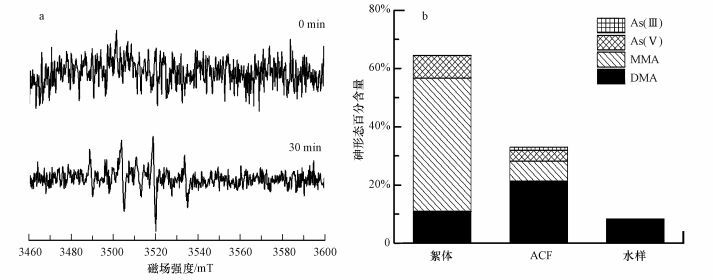 |
| 图 3 感应电芬顿反应过程分析(a.感应电芬顿ESR谱图, b.反应240 min砷形态含量分布) Fig. 3 Analysis of the field-induced electro-Fenton(a.ESR of the field-induced electro-Fenton, b.Content distribution of arsenic in 240 min) |
经感应电芬顿催化降解后, 砷主要以DMA、MMA、As(Ⅴ)和As(Ⅲ)形式存在, 分布在水、铁的水合羟基氧化物及ACF电极表面.在感应电芬顿催化降解DMA过程中, 一部分DMA被·OH降解为MMA和As(Ⅴ), 一部分DMA被水合羟基铁吸附(Boye et al., 2003), 同时少量的DMA会随着水合羟基铁沉积在ACF阴极表面.
在反应时间240 min即反应结束时, 各种形态砷的分布如图 3b所示, 水样中砷含量为8.0%, 主要以DMA为主;水中悬浮态的水合羟基铁絮体中的砷含量为62.1%, 主要以MMA形式存在, 还检测出了DMA和As(Ⅴ);ACF电极中砷含量为30.0%, 检测出DMA、MMA、As(Ⅴ)和As(Ⅲ), 其中, DMA含量最高.阴极ACF表面检测出As(Ⅲ), 有可能是阴极存在电子的还原过程, 将部分As(Ⅴ)还原为As(Ⅲ).
综上所述, 该感应电芬顿去除二甲基砷的反应过程是:感应铁电极溶出的Fe2+与阴极产生的H2O2反应生成·OH将DMA降解为MMA, MMA被进一步氧化成As(Ⅲ)和As(Ⅴ);同时, 感应铁电极溶出铁离子发生水解, 生成水合羟基铁, 也将DMA及降解产物吸附去除.
其中, 感应电芬顿去除DMA的机理分析如图 4所示.反应体系中持续通氧使其处于氧饱和状态, 通电后在阴极活性炭纤维表面O2与H+反应生成H2O2, Fe2+逐渐从感应铁阳极上溶出与H2O2反应生成·OH, 新生的·OH在溶液中扩散将DMA结构中的甲基氧化取代生成MMA, 并且·OH继续将MMA氧化为As(Ⅲ)和As(Ⅴ).同时,在体系生成的水合羟基铁絮体表面发生脱-OH的螯合反应将DMA、MMA、As(Ⅲ)和As(Ⅴ)吸附在絮体表面, 从而达到污染物去除的目的.
 |
| 图 4 感应电芬顿去除DMA机理 Fig. 4 Mechanism of DMA removal by the field-induced electro-Fenton process |
1) 本研究构建了RuO2/Ti为阳极、ACF为双阴极、铁棒为感应牺牲阳极的电芬顿体系, 在线生成的Fe2+和H2O2高效产生·OH.该感应电芬顿体系对DMA有很好的去除效果, DMA去除率可达94.4%.
2) 感应电芬顿对初始浓度5 mg·L-1 DMA去除的最佳条件为:反应时间240 min, 初始pH=3, 电流密度为2 mA·cm-2, 氧气通量为50 mL·min-1.
3) 感应电芬顿反应产生·OH, ·OH将DMA降解为MMA、As(Ⅲ)和As(Ⅴ), 同时, 反应过程产生的水合羟基铁絮体对DMA及降解产物有很强的吸附作用.因此, 本研究的双阴极感应电芬顿体系能够高效地去除DMA, 并且通过絮凝完全去除水溶液中的降解产物.
| [${referVo.labelOrder}] | 艾仕云, 杨娅, 鲜跃仲, 等. 2004. 纳米TiO2光诱导产生羟基自由基的ESR研究[J]. 华东师范大学学报, 2004(3): 76–81. |
| [${referVo.labelOrder}] | Benitez F J, Acero J L, Real F J, et al. 2001. The role of hydroxyl radicals for the decomposition of p-hydroxy phenylacetic acid in aqueous solutions[J]. Water Research, 35(5): 1338–1343. DOI:10.1016/S0043-1354(00)00364-X |
| [${referVo.labelOrder}] | Boye B, Dieng M M, Brillas E. 2003. Electrochemical degradation of 2, 4, 5-trichlorophenoxyacetic acid in aqueous medium by peroxi-coagulation[J]. Effect of pH and UV light[J].Electrochimica Acta, 48(7): 781–790. |
| [${referVo.labelOrder}] | Cao C Y, Qu J, Yan W S, et al. 2012. Low-cost synthesis of flowerlike α-Fe2O3 nanostructures for heavy metal ion removal:Adsorption property and mechanism[J]. Langmuir, 28(9): 4573–4579. DOI:10.1021/la300097y |
| [${referVo.labelOrder}] | Del Razo L M, Arellano M A, Cebrian M E. 1990. The oxidation states of arsenic in well water from a chronic arsenicism area of northern Mexico[J]. Environmental Pollution, 64(2): 143–153. DOI:10.1016/0269-7491(90)90111-O |
| [${referVo.labelOrder}] | Ge J, Qu J. 2004. Ultrasonic irradiation enhanced degradation of azo dye on MnO2[J]. Applied Catalysis B:Environmental, 47(2): 133–140. DOI:10.1016/j.apcatb.2003.08.001 |
| [${referVo.labelOrder}] | Guedes A M F M, Madeira L M P, Boaventura R A. 2003. Fentonoxidation of cork cooking wastewater-overall kinetic analysis[J]. Water Research, 37(13): 3061–3069. DOI:10.1016/S0043-1354(03)00178-7 |
| [${referVo.labelOrder}] | Guivarch E, Trevin S, Lahitte C, et al. 2003. Degradation of azo dyes in water by electro-Fenton process[J]. Environmental Chemistry Letters, 1(1): 38–44. DOI:10.1007/s10311-002-0017-0 |
| [${referVo.labelOrder}] | Hu C Z, Liu H J, Chen G X, et al. 2012. Effect of aluminum speciation on arsenic removal during coagulation process[J]. Separation and Purification Technology, 86(8): 35–40. |
| [${referVo.labelOrder}] | Hu C Z, Chen Q X, Liu H J, et al. 2015. Coagulation of methylated arsenic from drinking water:Influence of methyl substitution[J]. Journal of Hazardous Materials, 293: 97–104. DOI:10.1016/j.jhazmat.2015.03.055 |
| [${referVo.labelOrder}] | Kremer M L. 1999. Mechanism of the Fenton reaction[J]. Evidence for a new intermediate[J].Physical Chemistry Chemical Physics, 1(15): 3595–3605. DOI:10.1039/a903915e |
| [${referVo.labelOrder}] | 李景岩, 张爱君. 2011. 砷代谢与砷毒性作用机制的关系[J]. 中国地方病防治杂志, 2011, 15(5): 345–347. |
| [${referVo.labelOrder}] | 刘文婧, 景传勇. 2016. 纳米二氧化钛光催化转化甲基砷的研究[J]. 环境科学学报, 2016, 36(1): 172–177. DOI:10.11654/jaes.2016.01.023 |
| [${referVo.labelOrder}] | 李建斐, 李一兵, 孙猛, 等. 2015. 纳米Fe3C/炭纤维非均相电芬顿降解二甲基砷的研究[J]. 环境科学学报, 2015, 36(9): 3230–3236. |
| [${referVo.labelOrder}] | Neyens E, Baeyens J. 2003. A review of classic Fenton's peroxidation as an advanced oxidation technique[J]. Journal of Hazardous Materials, 98(1/3): 33–50. |
| [${referVo.labelOrder}] | Rivas F J, Navarrete V, Beltrán F J, et al. 2004. Simazine Fenton's oxidation in a continuous reactor[J]. Applied Catalysis B:Environmental, 48(4): 249–258. DOI:10.1016/j.apcatb.2003.11.009 |
| [${referVo.labelOrder}] | Tresintsi S, Simeonidis K, Vourlias G, et al. 2012. Kilogram-scale synthesis of iron oxy-hydroxides with improved arsenic removal capacity:study of Fe (Ⅱ) oxidation-precipitation parameters[J]. Water Research, 46(16): 5255–5267. DOI:10.1016/j.watres.2012.06.049 |
| [${referVo.labelOrder}] | Velez D, Ybanez N, Montoro R. 1996. Monomethylarsonic and dimethylarsinic acid contents in seafood products[J]. Agric Food Chem, 44(3): 859–864. DOI:10.1021/jf950506e |
| [${referVo.labelOrder}] | Wei Y T, Zheng Y M, Chen J P. 2011. Uptake of methylated arsenic by a polymeric adsorbent:Process performance and adsorption chemistry[J]. Water Research, 45(6): 2290–2296. DOI:10.1016/j.watres.2011.01.002 |
| [${referVo.labelOrder}] | Xie X D, Hu Y A, Cheng H F. 2016. Rapid degradation of p-arsanilic acid with simultaneous arsenic removal from aqueous solution using Fenton process[J]. Water Research, 89: 59–67. DOI:10.1016/j.watres.2015.11.037 |
| [${referVo.labelOrder}] | Xu Z, Jing C, Li F, Meng X. 2008. Mechanisms of photocatalytical degradation of monomethylarsonic and dimethylarsinic acids using nanocrystalline titanium dioxide[J]. Environmental Science & Technology, 42(7): 2349–2354. |
| [${referVo.labelOrder}] | Xu T l, Cai Y, O'Shea K E, et al. 2007. Adsorption and photocatalyzed oxidation of methylated arsenic species in TiO2 suspensions[J]. Environmental Science & Technology, 41(15): 5471–5477. |
| [${referVo.labelOrder}] | Xu X R, Zhao Z Y, Li X Y, et al. 2004. Chemical oxidative degradation of methyl tert-butyl ether in aqueous solution by Fenton's reagent[J]. Chemosphere, 55(1): 73–79. DOI:10.1016/j.chemosphere.2003.11.017 |
| [${referVo.labelOrder}] | 奚倩, 赵雅娉, 张警予, 等. 2014. 利用电子自旋共振技术研究海参提取液体外抗氧化活性[J]. 食品与机械, 2014(5): 35–40. |
| [${referVo.labelOrder}] | 王爱民, 曲久辉, 宋玲玲, 等. 2006. 活性炭纤维电极生成羟基自由基降解酸性红B[J]. 化学学报, 2006, 64(8): 767–771. |
| [${referVo.labelOrder}] | 王玉玲, 蔡乃才, 王亚平, 等. 2002. 新型双功能复合电极的制备及其加速水中有机污染物降解作用的研究[J]. 高等学校化学学报, 2002, 23(6): 1151–1155. |
 2017, Vol. 37
2017, Vol. 37