2. 安徽工业大学生物膜法水质净化及利用技术教育部工程研究中心, 马鞍山 243032
2. Water Purification by Biofilm Method and Utilization, Engineering Research Center of Ministry of Education, Anhui University of Technology, Ma'anshan 243032
重金属铬在水体中主要以Cr(Ⅲ)和Cr(Ⅵ)2种形态存在,其中,Cr(Ⅵ)是一种急性致癌物质,迁移性和毒性远高于Cr(Ⅲ).美国环保署和世界卫生组织规定饮用水中Cr(Ⅵ)浓度≤0.05 mg·L-1(Hu et al., 2009).我国水质标准中规定饮用水中Cr(Ⅵ)浓度≤0.05 mg·L-1,地表水中Cr(Ⅵ)浓度≤0.15 mg·L-1,排放废水中Cr(Ⅵ)和总铬最大允许排放浓度分别为0.05和0.15 mg·L-1.因此,去除水中铬,尤其是Cr(Ⅵ),对保护公众健康和生态环境具有重要意义.目前,含铬废水的主要处理方法有化学沉淀法、溶剂提取法、反渗透法、还原法和吸附法等(Yu et al., 2013).由于吸附法具有操作简单、成本较低、处理效果好等优点,已被广泛用于处理含铬废水(Wu et al., 2010).
粘土矿物凹凸棒石因具有良好的吸附性能和价格便宜等优点被广泛应用于水处理领域(Frini Srasra et al., 2010),但对阴离子如Cr(Ⅵ)的吸附量较低(Chen et al., 2011).近年来有学者采用水热碳化法对凹凸棒石进行有机改性,从而提高凹凸棒石的吸附性能,这是由于凹凸棒石表面被嫁接—CH、—OH、>C=O、>C=C和—COOH等有机官能团,常用的碳源有葡萄糖、木糖、果糖、蔗糖、纤维素和氯乙酸等(Chen et al., 2011; 徐艳青等, 2013; Wu et al., 2011, 2014; Zhang et al., 2015).壳聚糖是通过甲壳素脱乙酰基而制得的一种天然阳离子多聚糖,具有生物相容性、环境友好性等特点,其分子链上含有丰富的羟基和氨基等活性基团.单纯壳聚糖在较高pH条件下对重金属离子(如Cu2+、Cd2+和Pb2+等)具有良好的吸附性能(Kyzas et al., 2016).相反,酸性越强越有利于壳聚糖吸附去除Cr(Ⅵ),这是由于Cr(Ⅵ)在水溶液中以CrO42-、HCrO4-、HCr2O7-和Cr2O72-形态存在.但壳聚糖在酸性条件下易软化流失,限制其实际应用.为了提高在酸性条件下的稳定性,必须对壳聚糖进行改性,如与戊二醛、环氧氯丙烷和乙二胺等发生交联反应(Saleh et al., 2015).但交联改性过程会导致壳聚糖吸附性能的降低.近年的研究表明,壳聚糖可以作为生物质碳源,水热碳化产物表面富含丰富的羟基和氨基等官能团,又有一定的抗酸性和机械强度(张显等, 2015).Zhou等(2015)以壳聚糖为碳源,采用一步水热碳化法对凹凸棒石进行有机改性,所得复合材料对亚甲基蓝的吸附量高达226 mg·g-1,显著高于碳纳米管(46.2 mg·g-1)、埃尔祖鲁姆产粘土(6.3 mg·g-1)、粉末活性炭(91 mg·g-1)等.从理论上分析,该复合材料具有较好的吸附去除Cr(Ⅵ)的性能,以及一定的还原性能,即脱毒功能,在酸性条件下可将Cr(Ⅵ)还原成Cr(Ⅲ).这是由于其表面含丰富的含氧基团和氨基等活性基团,但目前还没发现相关报道.
鉴于此,本研究选择壳聚糖为生物质碳源,采用水热碳化法对凹凸棒石表面进行有机改性,得到纳米复合材料(AT@CS纳米复合材料),并采用扫描电镜(SEM)、拉曼(Raman)光谱、元素分析(EA)、X光电子能谱(XPS)、Zeta电位分析、热重分析(TGA)等手段对复合材料进行表征分析.同时,通过静态吸附实验,研究复合材料吸附去除Cr(Ⅵ)的性能,主要考察温度对复合材料吸附去除Cr(Ⅵ)的影响,探讨吸附动力学和热力学规律,并在此基础上对吸附去除机制进行初步探讨.以期为含Cr(Ⅵ)废水吸附处理提供实验数据支撑和理论依据.
2 材料与方法(Materials and methods) 2.1 化学试剂与仪器试剂:凹凸棒石来源于明光市官山,XRD分析结果表明,其含有少量石英和蒙脱石;壳聚糖、活性炭、二苯碳酰二肼、丙酮、K2Cr2O7、NaOH、HCl、NaCl等购于国药集团化学试剂有限公司,其中,壳聚糖为生化试剂,其他均为分析纯试剂.
仪器:场发射扫描电子显微镜(S-4800,日本Hitachi)、激光共焦拉曼光谱仪(Renishaw inVia, 英国Renishaw)、元素分析仪(2400Ⅱ,美国PE)、X射线光电子能谱仪(ESCALAB 250Xi,美国ThermoFisher Scientific)、Zeta电势测定仪(Nano-ZS90,英国Malvern)、热重分析仪(DTG-60H,日本Shimadzu)、可见分光光度计(722S,上海精科)等.
2.2 吸附剂的制备壳聚糖碳化改性凹凸棒石的制备过程在参考文献(Zhou et al., 2015)的基础上略有改变,具体步骤如下:称取1.0 g凹凸棒石和4.0 g壳聚糖置于250 mL烧杯中,加入75 mL蒸馏水,超声分散后将溶液转移到100 mL聚四氟乙烯水热反应釜中,再将反应釜放到180 ℃高温炉中反应24 h;自然冷却后,用无水乙醇和蒸馏水各洗涤3次,离心分离后烘干,研磨过筛后得到凹凸棒石@壳聚糖碳纳米复合材料,记为AT@CS吸附剂.
2.3 吸附剂的表征通过S-4800场发射扫描电子显微镜观察所制样品的微观形貌;利用Renishaw inVia激光共焦拉曼光谱仪表征样品的结构和化学特征(激发器532 nm,1 mW);采用ESCALAB 250Xi X光电子能谱仪对样品进行分析(样品用单色化AlKα激发);样品中C、H、N的定量分析采用美国PE 2400Ⅱ元素分析仪;利用Nano-ZS90型Zeta电位仪测定不同pH条件下吸附剂表面的Zeta电位的大小;采用DTG-60H热重差热分析仪在空气氛围、10 ℃·min-1升温速率条件下,从室温加热至800 ℃,分析样品中各组分的含量.
2.4 吸附实验 2.4.1 吸附动力学称取若干份0.050 g AT@CS吸附剂,加入20 mL K2Cr2O7溶液(200 mg·L-1,pH=2),在298 K、150 r·min-1的条件下振荡至吸附平衡,离心分离后测定上清液中Cr(Ⅵ)和总铬的浓度.
2.4.2 温度对吸附动力学的影响称取若干份0.050 g AT@CS吸附剂,加入30 mL K2Cr2O7溶液(500 mg·L-1,pH=2),在不同温度(298、308、318 K)、转速150 r·min-1的条件下振荡,在设定的时间取样,离心分离,测定上清液中总铬的浓度.
2.4.3 吸附等温线称取若干份0.050 g AT@CS吸附剂,分别加入到40 mL K2Cr2O7溶液(100~600 mg·L-1,pH=2) 中,在298、308、318和328 K,150 r·min-1的条件下振荡至吸附平衡,离心分离后测定上清液中总铬的浓度.
2.5 分析方法Cr(Ⅵ)浓度采用二苯碳酰二肼比色法测定;总铬浓度测定时首先采用高锰酸钾将Cr(Ⅲ)氧化成Cr(Ⅵ),然后测定Cr(Ⅵ)浓度,即为总铬浓度;Cr(Ⅲ)浓度为总铬浓度与Cr(Ⅵ)浓度之差.
AT@CS吸附剂的活性点位主要来自凹凸棒石表面沉积的纳米碳层,又称碳基吸附剂(Chen et al., 2011).碳基吸附剂表面含有还原性基团,如CxOH和氨基,在强酸性条件下能将Cr(Ⅵ)还原成Cr(Ⅲ).以CxOH表示的还原反应过程见式(1) 和(2)(Hu et al., 2009; Wu et al., 2010).
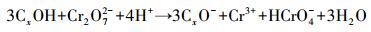
|
(1) |
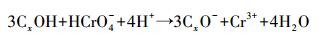
|
(2) |
如果采用吸附前后Cr(Ⅵ)浓度减少量来计算吸附量,得到的是表观吸附量,远大于实际吸附量(王诗生等, 2016).鉴于此,本文采用吸附前后总铬浓度减少量来计算吸附量.
3 结果与讨论(Results and discussion) 3.1 吸附剂的表征图 1为凹凸棒石和AT@CS的扫描电镜图.由图 1a可知,凹凸棒石的显微结构包含3个层次:一是凹凸棒石的基本结构单元,即棒状单晶体;二是由棒晶紧密平行聚集而成的棒晶束;三是由棒晶及棒晶束间相互聚集而形成的各种聚集体.由图 1b可知,改性凹凸棒石的棒状单晶没有改变,但长度略有减小,且表面包裹纳米炭;另外还发现大量片状物质,这是由于聚集体表面负载纳米碳所致.图 1c为放大100000倍的改性凹凸棒石图片,可清晰看到凹凸棒石棒晶表面凹凸不平,表面负载无定形的纳米碳.结果表明,凹凸棒石只是壳聚糖水热碳化碳沉积的异相核.
 |
| 图 1 凹凸棒石(a)和AT@CS(b, c)的SEM图 Fig. 1 SEM micrographs of attapulgite(a) and AT@CS(b, c) |
图 2为AT@CS的拉曼光谱图,该谱图在1377 cm-1(D峰)和1590 cm-1(G峰)处有2个很强的振动峰,为无定形碳或无序化石墨振动产生.D峰和G峰的强度比值(ID/IG)可衡量碳材料的石墨化程度,ID/IG越小,碳材料的石墨化(结晶性)程度越高(Demir Cakan et al., 2009).图 2中ID/IG (0.66) 比较大,说明所制备的碳材料石墨化程度很低,即结晶性很差.表明凹凸棒石表面负载的是无定形碳,这和扫描电镜的结果基本一致.
 |
| 图 2 AT@CS拉曼光谱图 Fig. 2 Raman spectrum of AT@CS |
图 3为凹凸棒石和AT@CS的XPS图谱.由图 3可知,AT@CS中含有Mg、Al、Si、C、O、N和Fe等元素.除C和N元素外,其他元素均为凹凸棒石的构成元素(Bradley, 1940).对AT@CS进行元素分析,其中,C、H、N分别为42.41%、4.39%、6.38%,表明壳聚糖碳化产物成功负载在凹凸棒石表面.
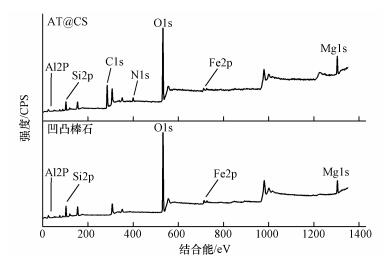 |
| 图 3 凹凸棒石和AT@CS样品的宽扫描XPS谱图 Fig. 3 XPS spectrum of attapulgite and AT@CS samples |
图 4a为AT@CS吸附剂C1s高分辨率XPS图谱.由图 4a可知,C1s谱分为4个峰,结合能为284.5 eV(42.55%)的峰为脂肪烃碳、芳香烃碳和C—NH2中的碳;285.3 eV(28.19%)处的峰为C—OH中的碳;286.7 eV(21.28%)处的峰为C=O中的碳;288.3 eV(7.98%)处的峰为COOR中的碳(Shibagaki et al., 2000; Swiatkowski et al., 2004; Wu et al., 2014).N1s谱(图 4b)只能分为一个NH2峰,结合能为400.01 eV(Wang et al., 2012).结果表明,壳聚糖水热碳化后使凹凸棒石表面负载丰富的C=O、C—OH、COOR和—NH2等活性基团.
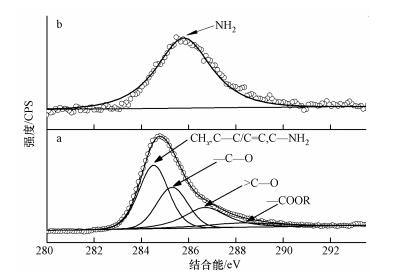 |
| 图 4 AT@CS样品C1s(a)和N1s(b)的高分辨率XPS谱图 Fig. 4 C1s(a) and N1s(b) high resolution XPS spectrum of AT@CS sample |
不同pH条件下,凹凸棒石和AT@CS吸附剂表面Zeta电势的测定结果见图 5.由图 5可知,凹凸棒石等电点(pHzpc)约为3.8.当pH<3.8时,凹凸棒石表面带正电;当pH>3.8时,凹凸棒石表面带负电.表明当pH<3.8,有利于吸附凹凸棒石吸附阴离子Cr(Ⅵ).AT@CS等电点(pHzpc)约为4.2,大于凹凸棒石.这是由于AT@CS吸附剂表面含有氨基、羟基、羧基等官能团,使等电点(pHzpc)增加(Yue et al., 2013).
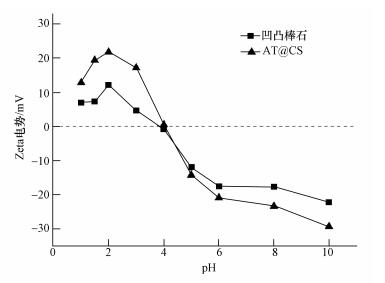 |
| 图 5 不同pH条件下凹凸棒石和AT@CS样品的Zeta电位 Fig. 5 Zeta potential of attapulgite and AT@CS samples obtained at different pH |
图 6为凹凸棒石和AT@CS吸附剂的热重损失曲线.由图 6可以看出,凹凸棒石在120 ℃前质量损失约为11%,这是由自由水损失所造成的; 在120~200 ℃,质量损失约为8%,这是由结合水损失造成的(Chen et al., 2011).对于AT@CS,在200 ℃之前,热重损失曲线与凹凸棒石基本一致; 在200~550 ℃,热重损失约53%,这是由凹凸棒石表面沉积的碳层在空气中氧化热分解造成的; 550 ℃以上,吸附剂质量基本保持不变,约为初始质量的27%.结果表明,壳聚糖水热碳化产物成功负载在凹凸棒石表面.
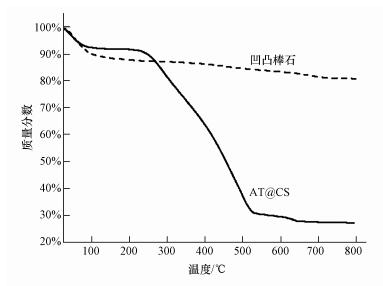 |
| 图 6 凹凸棒石和AT@CS样品的TGA曲线 Fig. 6 TGA curves of attapulgite and AT@CS samples |
AT@CS吸附剂去除Cr(Ⅵ)过程中溶液中Cr(Ⅵ)、总铬和Cr(Ⅲ)浓度随时间的变化情况见图 7.由图 7可知,溶液中的Cr(Ⅵ)和总铬浓度随时间延长而逐渐降低,在0~2 h,浓度降低较快,2~4 h,浓度下降速率减缓,4 h后浓度基本保持不变.吸附平衡时,Cr(Ⅵ)去除率为98.3%,总铬去除率为92.2%.Cr(Ⅲ)浓度随时间延长而逐渐升高,4 h时基本达到平衡.综上可认为,4 h为吸附平衡时间.
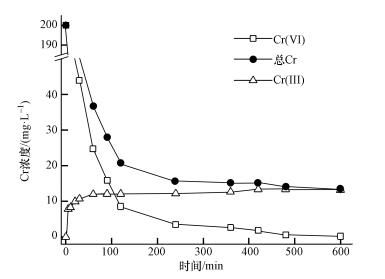 |
| 图 7 时间对Cr(Ⅵ)去除的影响 Fig. 7 Time profile of the removal of Cr (Ⅵ) |
吸附平衡时,如果以Cr(Ⅵ)为基准,计算吸附量为78.6 mg·g-1;以总铬为基准,计算吸附量为73.8 mg·g-1.这是由于Cr(Ⅵ)被吸附剂表面的还原性基团(如氨基、羟基)还原成Cr(Ⅲ),释放到溶液中去,释放到溶液中的部分Cr(Ⅲ)被重新吸附(Hu et al., 2009; Wu et al., 2010;Chen et al., 2011).因此,本研究的吸附量是基于总铬的减少量.
为了研究AT@CS吸附剂的吸附性能,利用准一级动力学模型(式(3))、准二级动力学模型(式(4))和颗粒内扩散模型(式(5))对吸附总铬的动力学实验数据进行了拟合.
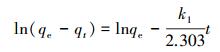
|
(3) |
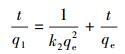
|
(4) |

|
(5) |
式中,qe、qt分别为平衡时刻和t时刻的吸附量(mg·g-1),t为吸附时间(min),k1为准一级动力学模型的吸附速率常数(min-1),k2为准二动力学模型的吸附速率常数(g·mg-1·min -1),kip为颗粒内扩散速率常数(mg·L-1·min-1/2).
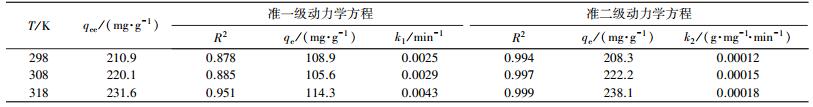
拟合后所得到的动力学参数见表 1.由表 1可知,准二级动力学模型能较好地拟合对总铬的吸附动力学过程(R2>0.99),拟合的理论值(74.6 mg·g-1)更接近实验值(73.8 mg·g-1).
| 表 1 吸附总铬的动力学参数 Table 1 Adsorption kinetics parameters for total chromium |
图 8表示的是温度对AT@CS吸附总铬动力学过程的影响.由图 8可以看出,随着温度的升高,吸附量逐渐增大,表明升温有利于吸附.采用准一级动力学模型、准二级动力学模型对不同温度下AT@CS吸附总铬的动力学实验数据进行拟合,拟合结果见表 2.由表 2可知,在不同温度下,准二级动力学模型拟合的R2均显著大于准一级动力学模型拟合的结果,表明准二级动力学模型符合AT@CS吸附总铬的动力学过程,并且k2随着温度的升高而增大,说明吸附反应为吸热反应,温度升高有利于吸附反应的进行.
 |
| 图 8 温度对吸附总铬的动力学影响 Fig. 8 Effect of temperature on the adsorption kinetics for total chromium |
| 表 2 不同温度下吸附总铬的动力学拟合参数 Table 2 Fitting parameters of adsorption kinetic for total chromium at different temperature |
根据Arrhenius公式计算吸附活化能,其表达式如下:

|
(6) |
式中,k2为准二级动力学方程的吸附速率常数(g·mg-1·min-1),T为绝对热力学温度(K),Ea为表观吸附活化能(kJ·mol-1),R为气体常数(8.314 J·mol-1·K-1).
以lnk2对1/T作图,结果见图 9, 由直线的斜率确定AT@CS对总铬的表观吸附活化能为13.4 kJ·mol-1.通常情况下,物理吸附的活化能为5~40 kJ·mol-1,而化学吸附的活化能为40~800 kJ·mol-1, 表明此吸附过程中物理吸附占主导地位.分析原因如下:一是在酸性条件下,AT@CS表面存在的含氧基团和氨基质子化带正电,通过静电作用吸附Cr(Ⅵ),这是吸附的主要作用力(Hu et al., 2009; Wu et al., 2010; Yu et al., 2013);另外,这些含氧基团和氨基还可以通过配位作用吸附Cr(Ⅵ),这是吸附的非主要作用力(Chen et al., 2011);二是在酸性条件下,AT@CS表面存在的还原性基团(如CxOH)将Cr(Ⅵ)还原成Cr(Ⅲ),部分Cr(Ⅲ)通过配位作用又被重新吸附在其表面,这也是吸附的非主要作用力(Hu et al., 2009; Wu et al., 2010; Chen et al., 2011; Yu et al., 2013).
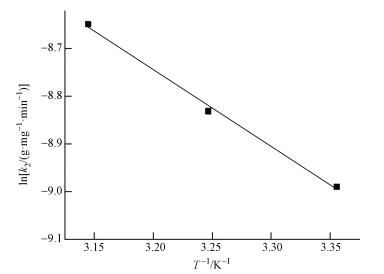 |
| 图 9 lnk2与1/T的关系 Fig. 9 Relationship of lnk2 and 1/T |
不同温度下,AT@CS对总铬的吸附等温线如图 10所示.分别用Langmuir方程(式(7))和Freundlich方程(式(8))对实验数据进行拟合,以可决系数作为评价标准.
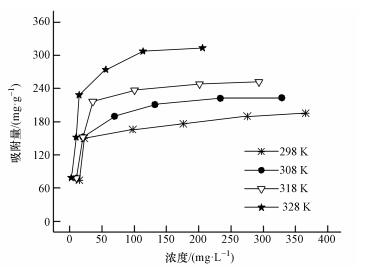 |
| 图 10 不同温度下吸附总铬的吸附等温线 Fig. 10 Adsorption isotherm for total chromium at different temperature |
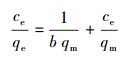
|
(7) |
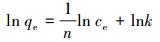
|
(8) |
式中,ce为总铬的平衡浓度(mg·L-1),c0为总铬的初始浓度(mg·L-1),qt为总铬的平衡吸附量(mg·L-1),qm为单层饱和吸附量(mg·L-1),b为平衡常数,n和k为常数,与温度、吸附剂种类、采用的计量单位有关.
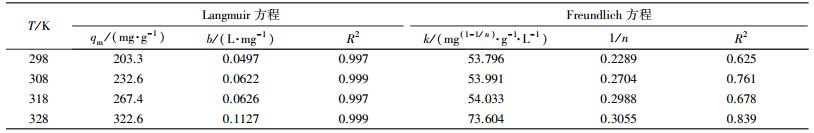
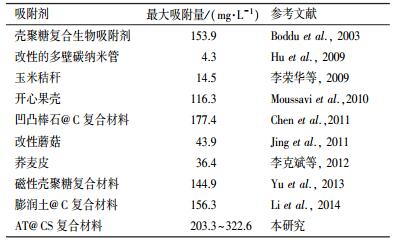
Langmuir和Freundlich等温方程拟合结果见表 3.由表 3可知,对总铬的吸附过程更适合用Langmuir等温线模型来描述,表明为单分子层吸附;在298、308、318和328 K时,理论最大吸附量分别为203.3、232.6、267.4和322.6 mg·g-1.AT@CS与其他吸附剂吸附去除Cr(Ⅵ)和总铬的效果对比研究见表 4.
| 表 3 不同温度下吸附总铬的等温线拟合参数 Table 3 Fitting parameters of adsorption isotherm for total chromium |
| 表 4 不同吸附剂对水中Cr(Ⅵ)吸附量的比较 Table 4 Comparison of adsorption capacities for Cr(Ⅵ) in aqueous solution on different adsorbents |
AT@CS对总铬的吸附热力学参数:吸附自由能变(ΔG0)、吸附焓变(ΔH0)和吸附熵变(ΔS0)可以通过式(9)~(11) 计算.
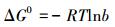
|
(9) |
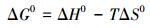
|
(10) |
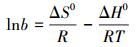
|
(11) |
式中,b(Langmuir常数)为吸附平衡常数(L·mg-1),ΔG0为吸附自由能变(kJ·mol-1),ΔH0为吸附焓变(kJ·mol-1),ΔS0为吸附熵变(J·mol-1·K-1).
根据公式(11),以lnb和1/T作图,结果见图 11.由直线的斜率计算吸附焓变ΔH0,再分别按照式(9) 和(10) 计算出ΔG0和ΔS0,计算的热力学参数见表 5.
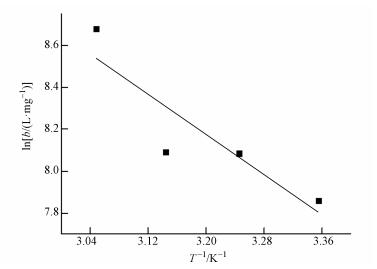 |
| 图 11 lnb与1/T的关系 Fig. 11 Relationship of lnb and 1/T |
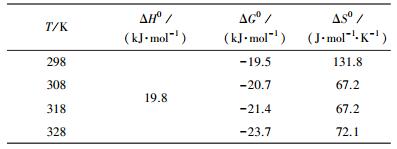
| 表 5 吸附总铬的热力学参数 Table 5 Adsorption thermodynamic parameters for total chromium |
吸附是吸附质和吸附剂间各种作用力共同作用的结果,不同作用力在吸附过程中所放出的热量不同.因此,可以通过测定总铬在AT@CS上的吸附热(即吸附焓变ΔH0)来判断吸附的主要作用力,有助于探明吸附机理.有研究报道(Oepen et al., 1991),各种作用力引起的吸附热范围分别为范德华力4~10 kJ·mol-1,疏水键力约为5 kJ·mol-1,氢键力约为2~40 kJ·mol-1,配位基交换约为40 kJ·mol-1,偶极间作用力为2~29 kJ·mol-1,化学键力大于60 kJ·mol-1.由表 5可知,ΔH0为19.8 kJ·mol-1,表明该吸附过程是吸热的,温度升高有利于吸附反应的进行;该吸附既有静电吸附,也有配位吸附,且以静电吸附为主.这与由表观吸附活化能所得到的研究结果基本一致.
吸附自由能变(ΔG0)可以反映吸附过程推动力的大小,ΔG0的绝对值越大,表明吸附推动力越大.有研究表明,物理吸附的ΔG0为-20~0 kJ·mol-1,化学吸附的ΔG0为-400~-80 kJ·mol-1(Chen et al., 2009).由表 5可知,在研究的温度范围内,ΔG0为-19.5~-23.7 kJ·mol-1,表明该吸附是一自发过程,同样说明既有静电吸附,也有配位吸附,但以静电吸附为主.不同温度下ΔG0的绝对值大小顺序为|ΔG0|(328 K)>|ΔG0|(318 K)>|ΔG0|(308 K)>|ΔG0|(298 K),表明总铬在AT@CS上的吸附随温度升高自发进行的趋势更加明显,但差别不是很大.
在固/液吸附体系中,同时存在溶质的吸附和溶剂的解吸,溶质分子吸附在吸附剂上,自由度减小,是熵减小的过程,而溶剂分子的解吸是熵增大的过程.吸附过程的熵变是两者的总和,因此,固/液吸附过程的熵变可能为负值,也可能为正值.通过研究熵变可以进一步了解吸附过程的本质, AT@CS对总铬的吸附熵变(ΔS0)均大于0,表明在吸附过程中,水分子的解吸引起的熵增大于总铬(Cr(Ⅵ)和Cr(Ⅲ)之和)吸附引起的熵减,最终导致吸附体系的混乱度增加.
4 结论(Conclusions)1) 以壳聚糖作为生物质碳源,经水热反应得到碳化改性的凹凸棒石.EA、拉曼光谱、XPS等分析表明,壳聚糖碳化后使凹凸棒石表面负载丰富的C=O、C—OH、COOR和—NH2等活性基团.
2) 对总铬的吸附行为符合准二级动力学方程,表观吸附活化能为13.4 kJ·mol-1,表明此吸附过程既有物理吸附(静电吸附),也有化学吸附(配位吸附),但以物理吸附(静电吸附)为主.
3) 对总铬的吸附等温线符合Langmuir方程,为单层吸附.在298、308、318和328 K时,理论最大吸附量分别为203.3、232.6、267.4和322.6 mg·g-1,表明AT@CS是一种新型环保高性能的除铬材料.通过热力学计算发现,ΔH0为19.8 kJ·mol-1,表明该吸附是一吸热过程,以静电吸附为主;ΔG0<0,表明总铬在AT@CS上的吸附是一个自发过程;ΔS0>0,表明该吸附是一熵增过程.
| [${referVo.labelOrder}] | Bradley W F. 1940. The structural scheme of attapulgite[J]. American Mineralogist, 25(6): 405–410. |
| [${referVo.labelOrder}] | Boddu V M, Abburi K, Talbott J L, et al. 2003. Removal of hexavalent chromium from wastewater using a new composite chitosan biosorbent[J]. Environmental Science and Technology, 37(19): 4449–4456. DOI:10.1021/es021013a |
| [${referVo.labelOrder}] | Chen L F, Liang H W, Yu S H, et al. 2011. Synthesis of an attapulgite clay@carbon nanocomposite adsorbent by a hydrothermal carbonization process and their application in the removal of toxic metal ions from water[J]. Langmuir, 27(14): 8998–9004. DOI:10.1021/la2017165 |
| [${referVo.labelOrder}] | Chen L, Gao X. 2009. Thermodynamic study of Th(IV) sorption on attapulgite[J]. Applied Radiation and Isotopes, 67(1): 1–6. DOI:10.1016/j.apradiso.2008.05.014 |
| [${referVo.labelOrder}] | Demir Cakan R, Baccile N, Antonietti M, et al. 2009. Carboxylate-rich carbonaceous materials via one-step hydrothermal carbonization of glucose in the presence of acrylic acid[J]. Chemistry of Materials, 21(3): 484–490. DOI:10.1021/cm802141h |
| [${referVo.labelOrder}] | Frini Srasra N, Srasra E. 2010. Acid treatment of south tunisian palygorskite:removal of Cd(Ⅱ) from aqueous and phosphoric acid solutions[J]. Desalination, 250(1): 26–34. DOI:10.1016/j.desal.2009.01.043 |
| [${referVo.labelOrder}] | Hu J, Chen C L, Zhu X X, et al. 2009. Removal of chromium from aqueous solution by using oxidized multiwalled carbon nanotubes[J]. Journal of Hazardous Materials, 162(2/3): 1542–1550. |
| [${referVo.labelOrder}] | Jing X B, Cao Y R, Zhang X Y, et al. 2011. Biosorption of Cr(Ⅵ) from simulated wastewater using a cationic surfactant modified spent mushroom[J]. Desalination, 269(1/3): 120–127. |
| [${referVo.labelOrder}] | Kyzas G Z, Lazaridis N K, Kostoglou M. 2013. On the simultaneous adsorption of a reactive dye and hexavalent chromium from aqueous solutions onto grafted chitosan[J]. Journal of Colloid Interface Science, 407: 432–441. DOI:10.1016/j.jcis.2013.05.052 |
| [${referVo.labelOrder}] | 李克斌, 王勤勤, 党艳, 等. 2012. 荞麦皮生物吸附去除水中Cr(Ⅵ)的吸附特性和机理[J]. 化学学报, 2012, 70(7): 929–937. |
| [${referVo.labelOrder}] | 李荣华, 张增强, 孟昭福, 等. 2009. 玉米秸秆对Cr(Ⅵ)的生物吸附及热力学特征研究[J]. 环境科学学报, 2009, 29(7): 1434–1441. |
| [${referVo.labelOrder}] | Li T, Shen J F, Huang S T, et al. 2014. Hydrothermal carbonization synthesis of a novel montmorillonite supported carbon nanosphere adsorbent for removal of Cr(Ⅵ) from wastewater[J]. Applied Clay Science, 93/94(3): 48–55. |
| [${referVo.labelOrder}] | Moussavi G, Barikbin B. 2010. Biosorption of chromium(Ⅵ) from industrial wastewater onto pistachio hull waste biomass[J]. Chemical Engineering Journal, 162(3): 893–900. DOI:10.1016/j.cej.2010.06.032 |
| [${referVo.labelOrder}] | Oepen B V, Kördel W, Klein W. 1991. Sorption of nonpolar and polar compounds to soils:processes, measurement and experience with the applicability of the modified OECD-Guideline[J]. Chemosphere, 22(3/4): 285–304. |
| [${referVo.labelOrder}] | Saleh T A, Haladu S A, Ali S A. 2015. A novel cross-linked pH-responsive tetrapolymer:synthesis, characterization and sorption evaluation towards Cr(Ⅲ)[J]. Chemical Engineering Journal, 269: 9–19. DOI:10.1016/j.cej.2015.01.083 |
| [${referVo.labelOrder}] | Shibagaki K, Motojima S. 2000. Surface properties of carbon micro-coils oxidized by a low concentration of oxygen gas[J]. Carbon, 38(15): 2087–2093. DOI:10.1016/S0008-6223(00)00065-8 |
| [${referVo.labelOrder}] | Swiatkowski A, Pakula M, Biniak S. 2004. Infiuence of the surface chemistry of modified activated carbon on its electrochemical behavior in the presence of lead(Ⅱ) ions[J]. Carbon, 42(15): 3057–3069. DOI:10.1016/j.carbon.2004.06.043 |
| [${referVo.labelOrder}] | 王诗生, 李正军, 梁丽珠, 等. 2016. 凹凸棒石@C纳米复合材料对Cr(Ⅵ)吸附-还原作用[J]. 环境科学学报, 2016, 36(7): 2468–2475. |
| [${referVo.labelOrder}] | Wang X B, Liu J, Xu W Z. 2012. One-step hydrothermal preparation of amino-functionalized carbon spheres at low temperature and their enhanced adsorption performance towards Cr(Ⅵ) for water purification[J]. Colloids & Surfaces A:Physicochemical & Engineering Aspects, 415: 288–294. |
| [${referVo.labelOrder}] | Wu J, Zhang H, He P J, et al. 2010. Cr(Ⅵ) removal from aqueous solution by dried activated sludge biomass[J]. Journal of Hazardous Materials, 176(1/3): 697–703. |
| [${referVo.labelOrder}] | Wu X P, Gao P, Zhang X L, et al. 2014. Synthesis of clay/carbon adsorbent through hydrothermal carbonization of cellulose on palygorskite[J]. Applied Clay Science, 95(3): 60–66. |
| [${referVo.labelOrder}] | Wu X P, Zhu W Y, Zhang X L, et al. 2011. Catalytic deposition of nanocarbon onto palygorskite and its adsorption of phenol[J]. Applied Clay Science, 52(4): 400–406. DOI:10.1016/j.clay.2011.04.011 |
| [${referVo.labelOrder}] | 徐艳青, 吴雪平, 刘存, 等. 2013. 生物质碳源度凹凸棒石有机改性及其吸附性能的影响[J]. 化学反应工程与工艺, 2013, 29(2): 119–124. |
| [${referVo.labelOrder}] | Yue M, Zhang M, Liu B, et al. 2013. Characteristics of amine surfactant modified peanut shell and its sorption property for Cr(Ⅵ)[J]. Chinese Journal of Chemical Engineering, 21(11): 1260–1268. DOI:10.1016/S1004-9541(13)60621-7 |
| [${referVo.labelOrder}] | Yu Z H, Zhang X D, Huang Y M. 2013. Magnetic chitosan-iron(Ⅲ) hydrogel as a fast and reusable adsorbent for chromium(Ⅵ) removal[J]. Industrial & Engineering Chemistry Research, 52(34): 11956–11966. |
| [${referVo.labelOrder}] | 张显, 吴天星, 宋小平, 等. 2015. 一步溶剂热法合成磁性壳聚糖微球及其对汞离子的吸附[J]. 硅酸盐学报, 2015, 43(8): 1143–1149. |
| [${referVo.labelOrder}] | Zhang Z F, Wang W B, Wang A Q. 2015. Highly effective removal of methylene blue using functionalized attapulgite via hydrothermal process[J]. Journal of Environmental Sciences, 33(7): 106–115. |
| [${referVo.labelOrder}] | Zhou Q, Gao Q, Luo W J, et al. 2015. One-step synthesis of amino-functionalized attapulgite clay nanoparticles adsorbent by hydrothermal carbonization of chitosan for removal of methylene blue from wastewater[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 470: 248–257. |
 2017, Vol. 37
2017, Vol. 37