随着印染工业的发展, 我国纺织、造纸等行业每年会使用数十万吨染料, 由此产生了大量的染料废水, 而印染废水是目前国内外公认的难处理工业废水之一(季雪琴等, 2016; 梁威等, 2004).印染废水具有水量大、有机毒物含量高、成分复杂及难降解等特点, 尤其是废水中残留的染料组分即使浓度很低, 排入水体也会造成水体透光率降低, 导致水体系统的破坏, 而且染料初步降解后的产物多为联苯胺等一些致癌的芳香类化合物(王慧等, 2008).常用的染料废水处理方法主要有物理化学法和生物法, 其中, 活性炭吸附是去除水体中有机染料较为常用的一种方法, 但活性炭的高成本限制了该方法的广泛应用.因此, 开发成本更低、效益更高的吸附材料受到研究者的广泛关注(Park et al., 2015; Ur Rehman et al., 2016; Xiao et al., 2014; Yu et al., 2015).
生物炭作为一种新型高效、廉价的吸附剂具有很好的吸附效果.研究发现, 生物炭具有高度芳香化的结构, 其表面含有羧基、酚羟基、羰基、酸酐等基团, 这些结构特性使生物炭具备了良好的吸附特性及稳定性(俞花美等, 2014).生物炭原料来源广泛, 目前已有学者采用农业废弃物(Li et al., 2016; Park et al., 2015; Xiao et al., 2014)、林业废弃物(Ding et al., 2016; Ur Rehman et al., 2016)和工业有机废弃物(Fan et al., 2016; Lonappan et al., 2016)等制备生物炭, 均表现出良好的吸附性能.我国拥有丰富的秸秆资源, 年产量可达7亿多吨.近年来, 随着我国农村生活能源结构的变化和集约化生产的发展, 秸秆逐步变成了一种无用的负担物, 就地焚烧现象日趋严重.传统的焚烧处理方式不仅浪费了资源, 还会污染环境, 因此, 急需开发清洁高效的农业废弃物资源化利用技术.目前, 制备生物炭的方法主要有限氧(或无氧)条件下的热解法和水热法2种, 与热解生物炭相比, 水热生物炭具有产率高, 进而可以产生较高总能量等优点(孙克静等, 2014).因此, 本文利用农业废弃物玉米叶和玉米杆, 通过水热法制备生物炭, 对含有亚甲基蓝染料的废水进行处理.
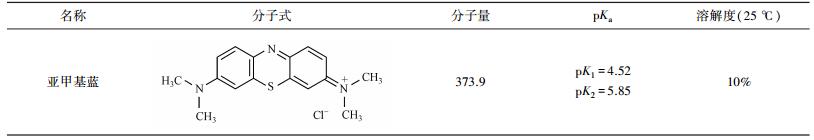
2 材料与方法(Materials and methods) 2.1 实验材料与仪器亚甲基蓝购自天津市北辰方正试剂厂, 基本性质见表 1;玉米叶和玉米秆采自锦州地区农村.仪器包括:电子分析天平(JJ224BC)、鼓风干燥箱(DHG-9245A)、马弗炉(XMT)、高速台式离心机(TGL-10C)、恒温振荡培养箱(HZQ-X100)、紫外可见分光光度计(752N).
| 表 1 亚甲基蓝的基本性质 Table 1 The properties of methylene blue |
采用水热法制备生物炭样品, 具体操作为:选取玉米叶(RML)与玉米杆(RMS)分别作为制备生物炭的原料, 采用去离子水清洗, 在80 ℃下烘干12 h, 粉碎后过80目筛, 储存于干燥器中备用.将粉碎后的原材料(玉米叶、玉米秆)分别称取5 g, 加入60 mL水并一起放入100 mL反应釜中, 在鼓风烘箱中密闭恒温(140 ℃)维持20 h.反应结束后冷却到室温将所得的生物炭固体粉末过80目筛, 得到玉米叶和玉米秆2种水热反应生物炭, 分别命名为ML和MS, 产率分别为42.56%和54.12%.
2.3 生物炭的表征通过场发射扫描电镜(FE-SEM, Hitachi S-4800) 表征生物炭的表面形貌特征.比表面积由ASAP2460全自动快速比表面积分析仪进行测定, 根据BET吸附方程求得结果.用傅里叶变换红外光谱仪(FT-IR, Varian Scimitar 2000) 测定生物炭的红外光谱, 采用KBr压片制样, 扫描波数范围为400~4000 cm-1.生物炭表面零点电位(pHzpc)测试(Xiao et al., 2005):在一系列50 mL具塞磨口锥形瓶中分别加入25 mL 0.01 mol·L-1 NaCl水溶液, 用1 mol·L-1 HCl和NaOH溶液调节pH值在2~12之间, 用N2吹脱3~5 min以去掉溶解在溶液中的CO2, 此时的pH值记作pH0;将75 mg待测试样品加入到每个瓶中, 加盖后25 ℃下振荡48 h, 测定上清液pH值, 记作pHf;分别以pH0-pHf为纵坐标, pH0为横坐标作图, 其中, pH0-pHf=0即为等电点, 此时, 待测试样品表面净电荷为零.
2.4 生物炭对亚甲基蓝的吸附批试验 2.4.1 吸附平衡时间将200 mL 10 mg·L-1的亚甲基蓝置于250 mL具塞锥形瓶中, 投加0.05 g生物炭, 然后将锥形瓶放进恒温振荡培养箱, 在(25±1) ℃条件下以150 r·min-1的转速振荡, 分别于5、10、20、40、60、90、120、180、240、360、600、960、1440 min时取样;用移液器取3 mL上清液置于离心管内, 在8000 r·min-1下离心分离5 min, 然后用移液器取液2 mL, 稀释后于665 nm波长处用紫外可见分光光度计测试亚甲基蓝的浓度.每个处理设3个平行, 取平均值进行分析.
2.4.2 亚甲基蓝初始浓度对吸附的影响如2.4.1节所述, 其他实验条件不变, 将亚甲基蓝浓度分别设置为5、10、15、20、30、40、60、80 mg·L-1, 加入到具塞锥形瓶中, 加入生物炭后振荡24 h, 吸附平衡后取出上清液离心, 测定溶液中亚甲基蓝的浓度.
2.4.3 生物炭投加量对吸附的影响如2.4.1节所述, 其他实验条件不变, 加入不同量的生物炭放入到配好的亚甲基蓝溶液中, 使生物炭投加量分别为0.10、0.25、0.50、0.75、1.00 g·L-1, 室温下振荡24 h, 测试亚甲基蓝浓度.
2.4.4 反应体系温度对吸附的影响如2.4.1节所述, 其他实验条件不变, 将装有生物炭的亚甲基蓝溶液的锥形瓶, 分别放入到30、35、40、45 ℃的振荡反应器中振荡24 h, 测试亚甲基蓝浓度.
2.4.5 溶液初始pH对吸附的影响如2.4.1节所述, 其他实验条件不变, 将亚甲基蓝溶液的pH分别调为1、3、5、7、9、11、13, 在室温下振荡24 h, 测试其浓度.
2.5 数据分析 2.5.1 吸附性能生物炭对亚甲基蓝的吸附量和去除率的计算公式分别如式(1) 和(2) 所示.
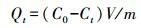
|
(1) |
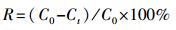
|
(2) |
式中, Qt为t时刻生物炭对亚甲基蓝的吸附量(mg·g-1);R为亚甲基蓝去除率;C0为亚甲基蓝的初始浓度(mg·L-1);Ct为t时刻溶液中亚甲基蓝浓度(mg·L-1);V为溶液的体积(L);m为生物炭的质量(g).
2.5.2 吸附动力学方程准一级动力学方程(Lagergren, 1898)见式(3), 准二级动力学方程(Ho et al., 1999)见式(4), 其中, 利用准二级动力学参数可以计算初始吸附速率h(式(5)), 颗粒内扩散模型(Weber et al., 1963)见式(6).
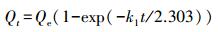
|
(3) |
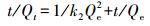
|
(4) |
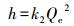
|
(5) |
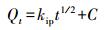
|
(6) |
式中, k1为准一级速率常数(min-1);k2为准二级速率常数(g·mg-1·min-1);t为反应时间(min);Qt、Qe分别为t时刻的吸附量和吸附达到平衡时的吸附量(mg·g-1);kip为颗粒内扩散速率常数(mg·g-1·min0.5);C为常数, 表示生物炭边界层, C会随生物炭表面异质性和亲水性基团的增加而降低, C值越大说明边界层对吸附的影响越大.如果吸附过程中发生颗粒内扩散作用, 那么Qt对t1/2作图为直线;如果直线过原点, 那么颗粒内扩散就是唯一限速因素.
2.5.3 吸附等温线方程Langmuir吸附等温线和Freundlich吸附等温线分别如式(7) 和(8) 所示.
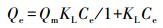
|
(7) |
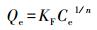
|
(8) |
式中, Qe为吸附平衡时生物炭对亚甲基的吸附量(mg·g-1);Qm为生物炭对亚甲基的饱和吸附量(mg·g-1);KL为Langmuir吸附平衡常数(L·mg-1);KF为Freundlich吸附平衡常数(mg·g-1·mg-n·L-n);Ce为吸附平衡时溶液的亚甲基蓝浓度(mg·L-1), 1/n为Freundlich指数.
3 结果与讨论(Results and discussions) 3.1 生物炭样品的表征 3.1.1 生物炭的表面形貌和比表面积扫描电镜(SEM)结果如图 1所示.从图 1a可以发现, 玉米叶基生物炭表面有较多不平整、不均匀孔状结构, 这些不规则的孔状结构能够促进生物炭对污染物的吸附;在图 1b中可以观察到, 玉米杆基生物炭呈现不定形层状褶皱结构, 表面粗糙有利于材料的吸附.
 |
| 图 1 所制备样品的扫描电镜图(a.玉米叶基生物炭, b.玉米杆基生物炭) Fig. 1 SEM images of biochars from ML(a) and MS(b) |
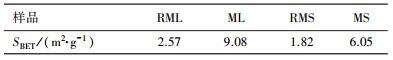
玉米叶和玉米杆经过水热炭化后比表面积均有所增加(表 2).由表 2可知, 经水热炭化后玉米叶基生物炭的比表面积增加了3.53倍, 玉米杆基生物炭的比表面积增加了3.32倍, 玉米叶基生物炭的比表面积为玉米杆基生物炭的1.50倍.
| 表 2 生物质炭化前后的比表面积 Table 2 Specific surface area of biomass before and after charring |
如图 2a所示, 生物质原料经水热炭化后表面官能团对应的吸收峰变强.在3000~3700 cm-1范围内可见宽而强的吸收峰, 源于羟基自由基的伸缩振动, 说明生物炭具有大量的羧基、羟基和羰基等含氧官能团(Ur Rehman et al., 2016).2916 cm-1处是脂肪性—CH2不对称和对称C—H伸缩振动峰(Yu et al., 2015);1630和1604 cm-1处对应于羧基、酯基或醛基C=O的伸缩振动;1440和1514 cm-1处对应于芳香环和吡啶环的C=C伸缩振动(Park et al., 2015; Xiao et al., 2014);1321和1371 cm-1处对应于O—C=O的伸缩振动(Wang et al., 2015; Wang et al., 2016);1059、1111、1163 cm-1处对应于C—O—C和—OCH3 (Faheem et al., 2016; 王章鸿等, 2015);897和838 cm-1处分别对应于呋喃γ-CH2和芳香性C—H的伸缩振动(Park et al., 2015; 李力等, 2012);781 cm-1处对应于—COO—的弯曲振动(Ur Rehman et al., 2016);478 cm-1处对应于官能团Si—O—Si(Xiao et al., 2014).当玉米叶基生物炭吸附亚甲基蓝之后(图 2c), 对比谱图可以发现, 1600 cm-1处出现了新的吸收峰, 这是由于生物炭吸附了亚甲基蓝所致, 说明生物炭表面的羧基、酯基或醛基对亚甲基蓝的吸附起到了一定的作用;此外, 对应O—C=O官能团位于1371和1321 cm-1处的2个吸收峰的位置发生了微小的红移, 而且1371与1321 cm-1处2个峰的比例也有所降低, 说明O—C=O官能团在亚甲基蓝吸附的过程中也起到了很重要的作用.图 2d为玉米杆基生物炭吸附亚甲基蓝前后红外谱图的对比, 在1600 cm-1附近吸附前后没有发生明显的变化, 在1371和1321 cm-1处发生了与玉米叶基生物炭类似的变化, 在1059和1036 cm-1处2个峰的比例降低.
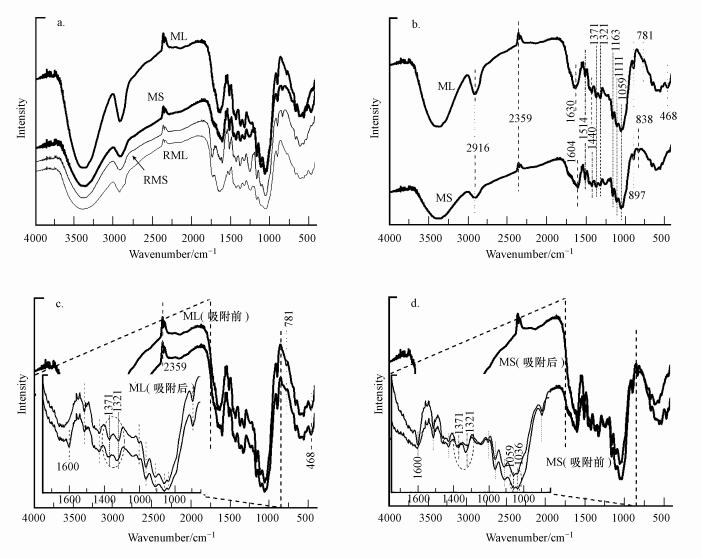 |
| 图 2 两种生物质(a)和相应生物炭(b)及其吸附前后(c, d)的红外光谱 Fig. 2 FT-IR spectrum of biomass(a), biochar(b) and biochar before and after sorption of methylene blue(c, d) |
在200 mL 10 mg·L-1的亚甲基蓝溶液中添加RML、ML、RMS、MS 4种吸附材料后, 在(25±1) ℃条件下以150 r·min-1的转速振荡40 min, 其对亚甲基蓝的吸附性能比较如图 3所示.结果显示:经过水热炭化, 玉米叶对亚甲基蓝的吸附量由12.38 mg·g-1增加到19.19 mg·g-1, 增加了54.95%, 去除率由31.64%提高到47.78%, 提高了51.03%;玉米杆对亚甲基蓝的吸附量由8.49 mg·g-1增加到12.48 mg·g-1, 增加了47.04%, 去除率由21.68%提高到31.08%, 提高了43.32%.这主要是由于经过水热炭化, 生物质表面的官能团被更多的暴露出来(图 2a), 更加有利于亚甲基蓝的吸附.
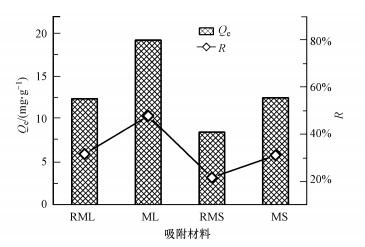 |
| 图 3 生物质水热炭化前后吸附性能比较 Fig. 3 Comparison of adsorption capacity of biomass before and after hydrothermal charring |
图 4a为生物炭在不同时间下对亚甲基蓝的去除率曲线.2种生物炭对10 mg·L-1亚甲基蓝溶液的吸附主要有3个阶段:在初始5 min内, 2种生物炭对亚甲基蓝的吸附速率很快, 玉米叶生物炭(ML)和玉米杆生物炭(MS)对亚甲基蓝的去除率分别达到37.60%和28.95%, 这是由于初始阶段生物炭表面与液相主体的亚甲基>蓝浓度最大, 在传质推动力作用下表现出迅速的吸附速率.在5~360 min时吸附速率较快, 去除率随着时间的延长呈现缓慢上升的趋势, 主要是由于随着生物炭对亚甲基蓝的吸附作用, 生物炭表面与液相主体中亚甲基蓝的浓度差逐渐减小, 从而导致吸附速率也会逐渐降低.在360 min以后, 吸附速率较慢, 吸附-解吸处于动态平衡.由图可知, 玉米叶和玉米秆生物炭对亚甲基蓝的吸附表现出相似的趋势, 玉米叶生物炭的吸附效果明显强于玉米秆生物炭.
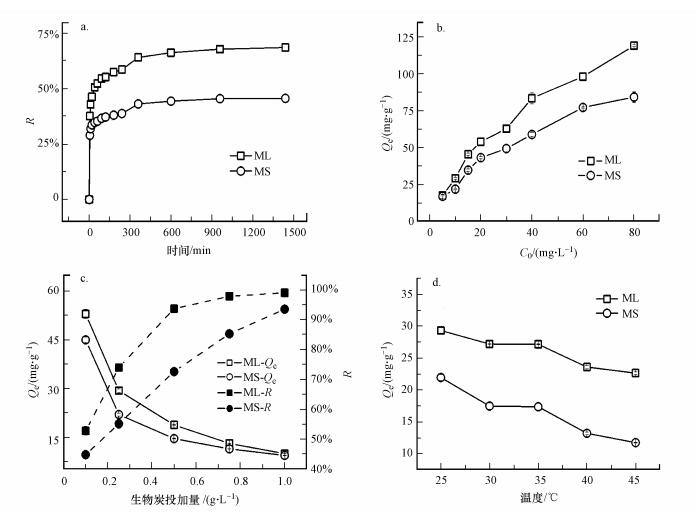 |
| 图 4 实验条件对生物炭吸附亚甲基蓝的影响(a.接触时间;b.亚甲基蓝初始浓度;c.生物炭投加量;d.反应体系温度) Fig. 4 The effect of experiment factors on adsorption of methylene blue by the biochars (a.contact time, b.initial concentration of methylene blue, c.biochar dose, d.reaction temperature) |
图 4b为玉米叶基和玉米秆基生物炭对不同浓度亚甲基蓝溶液的吸附曲线.由图可知, 随着亚甲基蓝浓度的增加, 2种生物炭对亚甲基蓝的吸附量也会增加.当亚甲基蓝的浓度从5 mg·L-1上升到80 mg·L-1时, 玉米叶基和玉米杆基生物炭对亚甲基蓝的平衡吸附量分别从17.69和17.03 mg·g-1增加到119.00和84.25 mg·g-1.这主要是由于在生物炭表面与液相主体之间亚甲基蓝浓度差的增加而导致具有更高的传质速率(Ur Rehman et al., 2013).图中显示, 对于不同浓度亚甲基蓝的吸附, 玉米叶基生物炭的吸附量明显高于玉米杆基生物炭.
3.3.3 生物炭投加量对吸附的影响生物炭投加量对亚甲基蓝吸附效果的影响如图 4c所示.由图可知, 在亚甲基蓝浓度为10 mg·L-1, 生物炭投加量为0.1~1 g·L-1时, 2种生物炭对亚甲基蓝的平衡吸附量随着生物炭投加量的增加而下降, 表现出相似的趋势.生物炭投加量为0.1 g·L-1时, 2种生物炭对亚甲基蓝的平衡吸附量分别为52.92和44.96 mg·g-1, 而当投加量增加到1.0 g·L-1时, 亚甲基蓝的平衡吸附量分别下降至9.90和9.35 mg·g-1.这是由于随着生物炭投加量的增加, 污染物在液相中的平衡浓度相对降低, 吸附容量相应下降所致.与此相反, 2种生物炭对亚甲基蓝的去除率随着生物炭投加量的增加而增大, 当生物炭投加量为0.1 g·L-1时, 2种生物炭对亚甲基蓝的去除率分别为52.92%和44.96%, 当投加量增加到1.0 g·L-1时, 2种生物炭对亚甲基蓝的去除率分别上升到98.98%和93.52%.2种生物炭对亚甲基蓝平衡吸附量和去除率相反的变化趋势与Ur Rehman等(2013; 2016)的研究结果一致.
3.3.4 反应体系温度对吸附的影响图 4d考察了反应体系温度对2种生物炭吸附亚甲基蓝的影响.由图可知, 2种生物炭对亚甲基蓝的平衡吸附量随着温度的升高表现出相似的变化趋势, 均随着温度的升高而降低.在25 ℃时, 玉米叶基生物炭和玉米杆基生物炭的平衡吸附量分别为29.29和21.94 mg·g-1, 当体系反应温度上升到45 ℃时, 2种生物炭的平衡吸附量分别下降至22.63和11.76 mg·g-1.这可能是由于随着反应温度的升高, 亚甲基蓝分子的无序性增强, 因而不利于吸附反应的进行, 温度的升高反而抑制了亚甲基蓝在2种生物炭上的吸附, 说明2种生物炭对亚甲基蓝的吸附是放热反应.Gürses等(20016;2004) 在研究黏土矿物对亚甲基蓝的吸附时也发现了类似的规律, Yang等(2011)在研究氧化石墨烯对亚甲基蓝的吸附时也得出了类似的结论.
3.3.5 溶液初始pH对吸附的影响溶液初始pH同样是影响水中生物炭吸附污染物的一个重要因素, 这主要是因为pH值不仅决定着溶液中污染物的质子化状态, 同时也影响到吸附剂表面的电荷状态(吴海露等, 2015).不同pH条件下2种生物炭在对亚甲基蓝溶液的吸附效果如图 5a所示.由图可知, 2种生物炭对亚甲基蓝的平衡吸附量变化趋势相似, 在所研究范围内均随着pH值的升高而明显增加, 在碱性环境中的吸附能力强于酸性环境.这主要是由于亚甲基蓝在溶液中以阳离子形式存在, 在较低pH时, 溶液中存在较多的H+, 会与亚甲基蓝阳离子在生物炭表面竞争活性吸附位点;随着pH值的增加, OH-浓度增大, 当溶液pH值增加到大于2种生物炭表面的零点电位(根据图 5b可知, 玉米叶基生物炭为5.40, 玉米杆基生物炭为6.10) 时, 生物炭表面呈负电状态而与溶液中的亚甲基蓝正离子通过静电作用相互吸引, 从而增强了生物炭对亚甲基蓝的吸附性能.Fan等(2016)研究的城市污泥和茶叶废物生物炭对亚甲基蓝的吸附也表现出相似的规律.
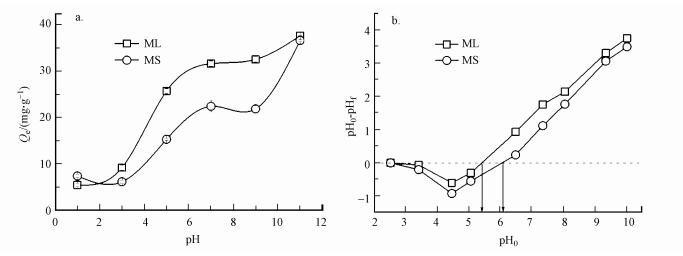 |
| 图 5 溶液pH对亚甲基蓝吸附的影响(a)和零点电位的测试(b) Fig. 5 Effect of solution pH on the adsorption of methylene blue on biochar(a) and the test of pHzpc (b) |
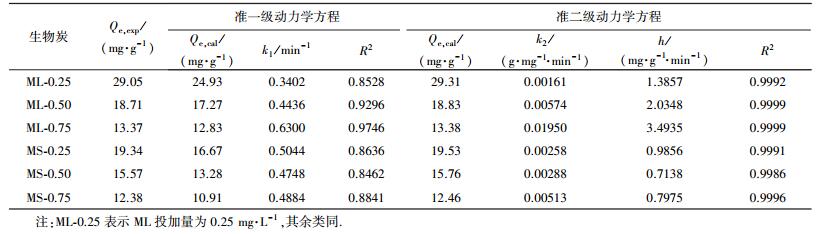
不同投加量下2种生物炭对溶液中亚甲基蓝的准一级动力学方程、准二级动力学方程拟合曲线如图 6所示, 拟合参数见表 3.由拟合结果可知, 准一级动力学方程的R2为0.8462~0.9746, 而准二级动力学方程的R2为0.9986~0.9999;且与准一动力学方程相比, 由准二级动力学方程拟合得到的平衡吸附量与实验得出的平衡吸附量更为接近, 可见2种生物炭对亚甲基蓝的吸附过程更适合用准二级动力学方程进行拟合, 即吸附速率与溶液浓度的平方成线性关系.准二级吸附动力学方程包含吸附的所有过程, 既有物理吸附, 又有化学吸附, 且以化学吸附为主要控制步骤, 能更真实地反映亚甲基蓝在2种生物炭的吸附机制(孙航等, 2016).化学键的形成是准二级动力学的重要影响因素, 经吸附前后红外光谱的比对进一步确认了在吸附过程中有化学键的形成, 说明生物炭对亚甲基蓝的吸附过程主要受化学吸附控制.在不同投加量条件下, 玉米叶基生物炭对亚甲基蓝的吸附量及初始速率常数均高于玉米杆基生物炭, 说明玉米叶更具有制成生物炭净化污水的潜质.
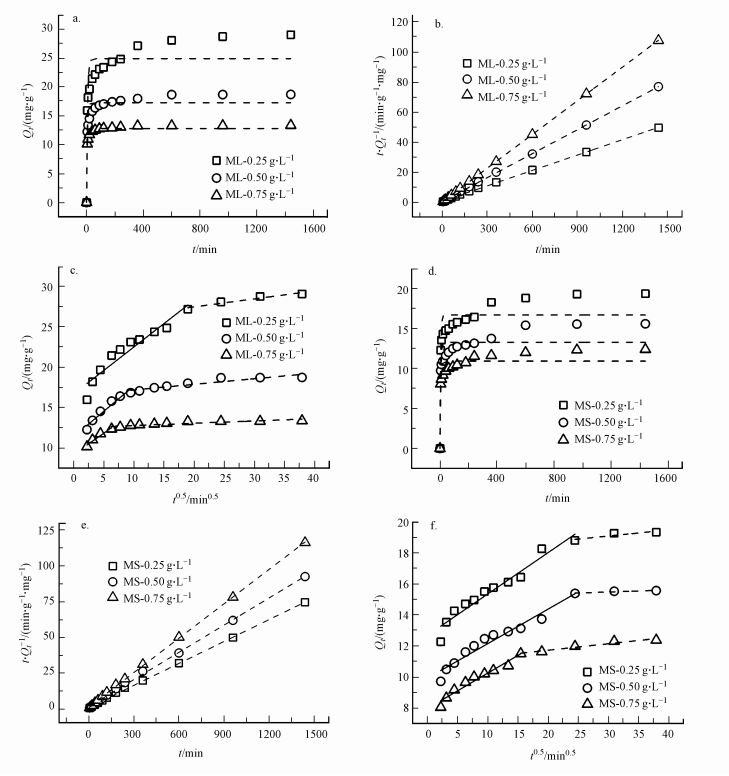 |
| 图 6 生物炭对亚甲基蓝的吸附动力学拟合曲线(a, d.准一级动力学方程;b, e.准二级动力学方程;c, f.颗粒内扩散方程) Fig. 6 Different kinetic plots for the adsorption of methylene blue onto biochars (a, d. pseudo first order kinetic model; b, e. pseudo second order kinetic model; c, f. intraparticle diffusion model) |
| 表 3 不同原料合成生物炭的准一级、二级吸附方程动力学参数 Table 3 The pseudo-first and second-order adsorption kinetic fitting parameters of biochar prepared under different raw materials |
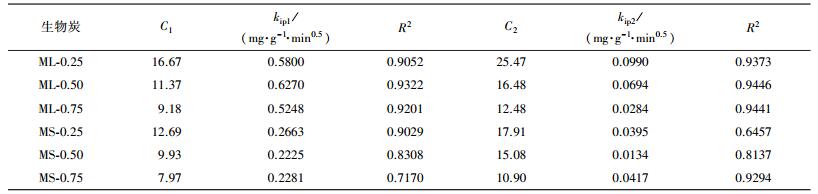
采用颗粒内扩散方程可以对生物炭吸附亚甲基蓝的过程做进一步的分析, 明确吸附速率的控制阶段, 结果如图 6c和6f所示, 拟合参数见表 4.Weber等(1963)认为, 如果颗粒内扩散方程为通过原点的线性关系式, 说明吸附过程仅仅由内扩散在起作用;如果不过原点, 则说明液膜扩散在吸附过程中也起到一定的作用.本文中, 2种生物炭对亚甲基蓝的吸附量Q对t1/2拟合曲线均为不通过原点的直线, 说明吸附过程中的颗粒内扩散不是唯一的控制步骤, 液膜扩散也起着一定的作用.这个吸附过程分为2个线性阶段:第一阶段为亚甲基蓝的瞬时吸附, 主要是跨液膜到生物炭表面的扩散阶段(即液膜扩散作用);第二阶段为亚甲基蓝在生物炭孔隙的扩散(即内扩散作用).且由表 4可知, 扩散速率常数为kip1>kip2, 这是由于随着亚甲基蓝向生物炭孔隙扩散量的增加, 扩散阻力增加所致;边界层C1<C2, 说明亚甲基蓝在2种生物炭表面的扩散进行较快, 吸附过程的主要限速步骤是颗粒内扩散.在相同生物炭投加剂量下, 玉米叶基生物炭的扩散速率常数及边界层厚度均大于玉米杆基生物炭, 这与2种生物炭表面理化性质的不同有关.
| 表 4 不同原料合成生物炭的颗粒内扩散方程动力学参数 Table 4 The intraparticle diffusion adsorption kinetic fitting parameters of biochar prepared under different raw materials |
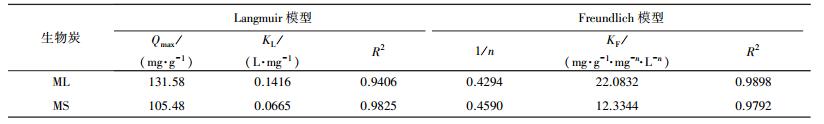
根据吸附动力学结果, 采用langmuir方程和Freundlich方程拟合数据, 结果如图 7所示, 拟合所得的吸附等温线参数见表 5.Freundlich模型中吸附常数KF反映了吸附剂吸附能力的强弱, 1/n反映了吸附剂吸附位点占能量分布的特征, KF值越大, 表明吸附能力越强, 1/n值越小, 表明吸附强度越大.亚甲基蓝在2种生物炭上的吸附等温线均表现出非线性, 玉米叶基生物炭拟合1/n值(0.4294) 小于玉米杆基生物炭(0.4590), 说明玉米叶基生物炭吸附等温线的非线性更强, 具有更高的吸附性能;玉米叶基生物炭对亚甲基蓝的吸附符合Freundlich模型, R2为0.9898, 说明吸附在生物炭表面是多分子层吸附过程, 在吸附质浓度较高时吸附量会持续增加(Surchi, 2011; 武丽君等, 2016);而亚甲基蓝在玉米杆基生物炭上的吸附更符合Langmuir模型, R2为0.9825, 说明吸附近似单分子层吸附, 随着初始浓度的增加, 其平衡吸附量也随之增加并逐渐达到平衡, 理论最大吸附量(105.4766 mg·g-1)是玉米叶基生物炭的80.16%.2种生物炭对亚甲基蓝吸附机制差异的主要原因可能是:① 两种生物炭表面官能团的差异及裸露程度不同;② 两种生物炭的比表面积大小不同.
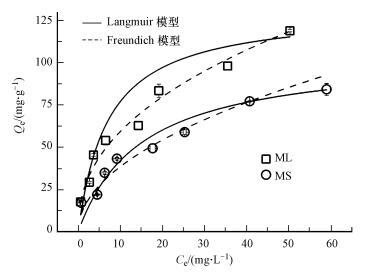 |
| 图 7 亚甲基蓝在生物炭上的吸附等温线 Fig. 7 Adsorption isotherms of methylene blue onto biochars |
| 表 5 不同原料生物炭吸附亚甲基蓝的Langmuir和Freundlich吸附等温方程拟合参数 Table 5 The methylene blue adsorption isotherm equations fitting parameters of Langmuir and Freundlich models of biochar prepared under different raw materials |
通过式(8) 可以求无量纲平衡常数RL(也称分离因子), 可以判断吸附材料是否可以有效吸附污染物.
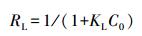
|
(9) |
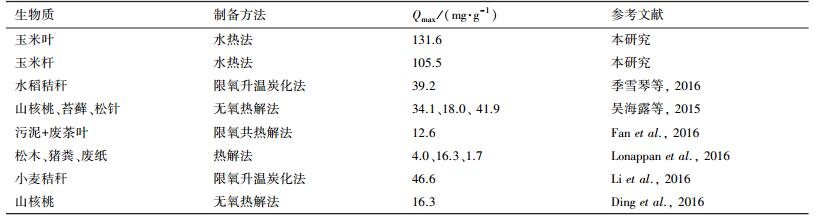
式中, KL为langmuir平衡常数(L·mg-1);C0为溶液初始浓度(mg·L-1).如果RL=0, 为不可逆吸附;0<RL<1, 则说明有利于吸附, 吸附容易进行;RL=1, 为线性吸附;RL>1, 说明不利于吸附(Mckay et al., 1982; Zheng et al., 2009; Zheng et al., 2008).经过计算, 求得玉米叶基生物炭和玉米杆基生物炭的RL分别为0.0811~0.5855和0.1582~0.7505, 因此, 2种生物炭均有利于亚甲基蓝在其表面吸附.此外, 将玉米叶基和玉米杆基生物炭与已报道的其他来源生物质制备的生物炭对亚甲基蓝的吸附性能进行了比较, 结果如表 6所示.玉米叶基生物炭对亚甲基蓝具有较高的吸附性能, 最大吸附量是文献报道值的3~77倍, 这可能与玉米叶基生物炭表面官能团和内部结构有关, 说明其对亚甲基蓝污染水体具有潜在的处理能力.
| 表 6 各种生物炭对亚甲基蓝最大吸附量的比较 Table 6 Comparison of the maximum adsorption capacities of MB onto biochar from various biomass |
1) 生物质原料玉米叶和玉米杆经过水热炭化后对亚甲基蓝的吸附性能有了明显的提升, 玉米叶经炭化后吸附量增加了54.95%, 对亚甲基蓝的去除率增加了51.03%;玉米杆经炭化后吸附量增加了47.04%, 对亚甲基蓝的去除率增加了43.32%.
2) 两种生物炭对亚甲基蓝的吸附在1440 min内均可以达到吸附平衡;随着亚甲基蓝浓度的增加, 2种生物炭对亚甲基蓝的吸附量也会增加;2种生物炭对亚甲基蓝的吸附量随着生物炭投加量的增加而下降, 去除率随着生物炭投加量的增加而下降;吸附量随着反应体系温度的升高而降低, 随着pH的增加而增大.
3) 两种生物炭的吸附动力学数据均能被准二级动力学方程很好地拟合, 结合颗粒内扩散模型的拟合结果, 亚甲基蓝在2种生物炭上的吸附过程由外部液膜扩散作用和颗粒内扩散作用共同控制, 且以颗粒内扩散作用为主.
4) 玉米叶基生物炭对亚甲基蓝的吸附符合Freundlich模型(R2=0.9898), 说明吸附在生物炭表面是多分子层吸附过程, 在吸附质浓度较高时吸附量会持续增加;而亚甲基蓝在玉米杆基生物炭上的吸附更符合Langmuir模型(R2=0.9825), 说明吸附近似单分子层吸附, 随着初始浓度的增加, 其吸附量也随之增加并逐渐达到平衡.
| [${referVo.labelOrder}] | Ding Z, Wan Y, Hu X, et al. 2016. Sorption of lead and methylene blue onto hickory biochars from different pyrolysis temperatures:Importance of physicochemical properties[J]. Journal of Industrial and Engineering Chemistry, 37: 261–267. DOI:10.1016/j.jiec.2016.03.035 |
| [${referVo.labelOrder}] | Faheem, Yu H X, Liu J, et al. 2016. Preparation of MnOx-loaded biochar for Pb2+ removal:Adsorption performance and possible mechanism[J]. Journal of the Taiwan Institute of Chemical Engineers, 66: 313–320. DOI:10.1016/j.jtice.2016.07.010 |
| [${referVo.labelOrder}] | Fan S S, Tang J, Wang Y, et al. 2016. Biochar prepared from co-pyrolysis of municipal sewage sludge and tea waste for the adsorption of methylene blue from aqueous solutions:Kinetics, isotherm, thermodynamic and mechanism[J]. Journal of Molecular Liquids, 220: 432–441. DOI:10.1016/j.molliq.2016.04.107 |
| [${referVo.labelOrder}] | Gürses A, Doğar Ç, Yalçın M, et al. 2006. The adsorption kinetics of the cationic dye, methylene blue, onto clay[J]. Journal of Hazardous Materials, 131(1/3): 217–228. |
| [${referVo.labelOrder}] | Gürses A, Karaca S, Doğar Ç, et al. 2004. Determination of adsorptive properties of clay/water system:methylene blue sorption[J]. Journal of Colloid and Interface Science, 269: 310–314. DOI:10.1016/j.jcis.2003.09.004 |
| [${referVo.labelOrder}] | Ho Y S, McKay G. 1999. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 34(5): 451–465. DOI:10.1016/S0032-9592(98)00112-5 |
| [${referVo.labelOrder}] | 季雪琴, 吕黎, 陈芬, 等. 2016. 秸秆生物炭对有机染料的吸附作用及机制[J]. 环境科学学报, 2016, 36(5): 1648–1654. |
| [${referVo.labelOrder}] | 李力, 陆宇超, 刘娅, 等. 2012. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2012, 31(11): 2277–2283. |
| [${referVo.labelOrder}] | 梁威, 胡洪营. 2004. 印染废水生物强化处理技术研究进展[J]. 环境污染治理技术与设备, 2004, 5(1): 8–11. |
| [${referVo.labelOrder}] | Lagergren S. 1898. About the theory of so-called adsorption of soluble substances[J]. Kungliga Svenska Vetenskapsakademiens Hanklingar, 24: 1–39. |
| [${referVo.labelOrder}] | Li G, Zhu W, Zhang C, et al. 2016. Effect of a magnetic field on the adsorptive removal of methylene blue onto wheat straw biochar[J]. Bioresource Technology, 206: 16–22. DOI:10.1016/j.biortech.2015.12.087 |
| [${referVo.labelOrder}] | Lonappan L, Rouissi T, Das R K, et al. 2016. Adsorption of methylene blue on biochar microparticles derived from different waste materials[J]. Waste Management, 49: 537–544. DOI:10.1016/j.wasman.2016.01.015 |
| [${referVo.labelOrder}] | Mckay G, Blair H, Gardner J. 1982. Adsorption of dyes on chitin Ⅰ.Equilibrium studies[J]. Journal of Applied Polymer Science, 27: 3043–3057. DOI:10.1002/app.1982.070270827 |
| [${referVo.labelOrder}] | Park J H, Ok Y S, Kim S H, et al. 2015. Evaluation of phosphorus adsorption capacity of sesame straw biochar on aqueous solution:influence of activation methods and pyrolysis temperatures[J]. Environmental Geochemistry and Health, 37: 969–983. DOI:10.1007/s10653-015-9709-9 |
| [${referVo.labelOrder}] | Surchi K M S. 2011. Agricultural wastes as low cost adsorbents for Pb removal:kinetics, equilibrium and thermodynamics[J]. International Journal of Chemistry, 3(3): 103. |
| [${referVo.labelOrder}] | 孙航, 蒋煜峰, 胡雪菲, 等. 2016. 添加生物炭对西北黄土吸附克百威的影响[J]. 环境科学学报, 2016, 36(3): 1015–1020. |
| [${referVo.labelOrder}] | 孙克静, 张海荣, 唐景春. 2014. 不同生物质原料水热生物炭特性的研究[J]. 农业环境科学学报, 2014, 33(11): 2260–2265. DOI:10.11654/jaes.2014.11.027 |
| [${referVo.labelOrder}] | Ur Rehman M S, Kim I, Rashid N, et al. 2016. Adsorption of brilliant green dye on biochar prepared from lignocellulosic bioethanol plant waste[J]. Clean-Soil Air Water, 44: 55–62. DOI:10.1002/clen.v44.1 |
| [${referVo.labelOrder}] | Ur Rehman M S, Munir M, Ashfaq M, et al. 2013. Adsorption of Brilliant Green dye from aqueous solution onto red clay[J]. Chemical Engineering Journal, 228(14): 54–62. |
| [${referVo.labelOrder}] | 王慧, 周月霞, 柏仕杰, 等. 2008. 染料废水生物法处理技术的研究进展[J]. 厦门大学学报(自然科学版), 2008, 47(2): 286–290. |
| [${referVo.labelOrder}] | 王章鸿, 郭海艳, 沈飞, 等. 2015. 热解条件对生物炭性质和氮、磷吸附性能的影响[J]. 环境科学学报, 2015, 35(9): 2805–2812. |
| [${referVo.labelOrder}] | 吴海露, 车晓冬, 丁竹红, 等. 2015. 山核桃、苔藓和松针基生物质炭对亚甲基蓝及刚果红的吸附性能研究[J]. 农业环境科学学报, 2015: 1575–1581. DOI:10.11654/jaes.2015.08.021 |
| [${referVo.labelOrder}] | 武丽君, 王朝旭, 张峰, 等. 2016. 玉米秸秆和玉米芯生物炭对水溶液中无机氮的吸附性能[J]. 中国环境科学, 2016, 36(1): 74–81. |
| [${referVo.labelOrder}] | 俞花美, 陈淼, 邓惠, 等. 2014. 蔗渣基生物质炭的制备、表征及吸附性能[J]. 热带作物学报, 2014, 35(3): 595–602. |
| [${referVo.labelOrder}] | Wang J, Chen B L. 2015. Adsorption and coadsorption of organic pollutants and a heavy metal by graphene oxide and reduced graphene materials[J]. Chemical Engineering Journal, 281: 379–388. DOI:10.1016/j.cej.2015.06.102 |
| [${referVo.labelOrder}] | Wang J, Chen B L, Xing B S. 2016. Wrinkles and folds of activated graphene nanosheets as fast and efficient adsorptive sites for hydrophobic organic contaminants[J]. Environmental Science & Technology, 50: 3798–3808. |
| [${referVo.labelOrder}] | Weber W J, Morris J C. 1963. Kinetics of adsorption on carbon from solution[J]. Journal of the Sanitary Engineering Division, 89: 31–60. |
| [${referVo.labelOrder}] | Xiao B, Thomas K M. 2005. Adsorption of aqueous metal ions on oxygen and nitrogen functionalized nanoporous activated carbons[J]. Langmuir, 21: 3892–3902. DOI:10.1021/la047135t |
| [${referVo.labelOrder}] | Xiao X, Chen B L, Zhu L Z. 2014. Transformation, morphology, and dissolution of silicon and carbon in rice straw-derived biochars under different pyrolytic temperatures[J]. Environmental Science & Technology, 48: 3411–3419. |
| [${referVo.labelOrder}] | Yang S T, Chen S, Chang Y, et al. 2011. Removal of methylene blue from aqueous solution by graphene oxide[J]. Journal of Colloid and Interface Science, 359: 24–29. DOI:10.1016/j.jcis.2011.02.064 |
| [${referVo.labelOrder}] | Yu Z H, Zhou L, Huang Y F, et al. 2015. Effects of a manganese oxide-modified biochar composite on adsorption of arsenic in red soil[J]. Journal of Environmental Management, 163: 155–162. DOI:10.1016/j.jenvman.2015.08.020 |
| [${referVo.labelOrder}] | Zheng H, Liu D, Zheng Y, et al. 2009. Sorption isotherm and kinetic modeling of aniline on Cr-bentonite[J]. Journal of Hazardous Materials, 167: 141–147. DOI:10.1016/j.jhazmat.2008.12.093 |
| [${referVo.labelOrder}] | Zheng H, Wang Y, Zheng Y, et al. 2008. Equilibrium, kinetic and thermodynamic studies on the sorption of 4-hydroxyphenol on Cr-bentonite[J]. Chemical Engineering Journal, 143: 117–123. DOI:10.1016/j.cej.2007.12.022 |
 2017, Vol. 37
2017, Vol. 37