藻类是水生生态系统的主要初级生产者, 常作为水环境质量变化的指示物种(Jiang et al., 2014; Liu et al., 2008), 也是水生生态毒理研究的实验物种之一(Ouyang et al., 2012; 2013).溶解性有机质(dissolved organic carbon, DOM)是指水溶液中能够通过0.45 μm滤膜的一类有机化合物, 通常以总有机碳(TOC)表征.DOM结构复杂, 来源广泛, 在水生生态系统中普遍存在, 而且化学滞留时间长, 是联系生物与非生物环境的“桥梁”(何伟, 2014).基于以上原因, DOM已经成为了环境科学领域目前的研究热点之一.腐殖质类的DOM源于碎屑的生物地球化学降解, 并很难进行进一步的降解, 可以在水体中存在较长的时间, 因此研究腐殖质类DOM(如富里酸, 胡敏酸等)的生物化学性质及行为是DOM研究中较为重要的部分(D′Andrilli et al., 2013).
铜作为一种广泛存在于水环境中的重金属, 毒性显著(徐珑等, 2005).由于自然水体组成多样, 铜的生物有效性问题也十分复杂.其中, DOM与铜之间的相互作用是一项重要影响因素.研究发现富含DOM的样品相对自然和人工海水具有较高的铜EC50(Sánchez Marín et al., 2010).富里酸存在条件下, 对盘管虫线虫幼虫进行铜暴露, 富里酸能够对受试生物起到有效的保护作用(Qiu et al., 2007).另有研究表明, DOM与铜的络合物也可能被翡翠贻贝吸收, 特别是一些小分子的DOM, 如组氨酸、半胱氨酸等(Zhong et al., 2012).
目前, DOM对铜毒性效应影响方面的研究已有一些报道(李光林等, 2003; Tait et al., 2016; Taylor et al., 2015; 王静等, 1992); 同时, 以藻类为受试生物进行的传统藻类毒理学研究方法着重计算LC50、EC50等反映致死率的指标, 无法区分暴露实验中出现的活细胞与死细胞(Stauber et al., 2002).并且, 传统的藻类毒性研究方法多关注物质毒性, 从化学角度解释DOM对铜毒性效应的影响机理, 如富里酸可络合铜离子, 能有效降低铜离子的活度, 降低铜对藻类的毒害作用(Ma et al., 2003; Ytreberg et al., 2011a; Ytreberg et al., 2011b); 而对于从藻类角度, 分析其生理特征(如光合作用与细胞凋亡)对毒性物质(如铜)的响应机制的研究较少(Ouyang et al., 2012; 2013).本文拟采用叶绿素荧光技术及流式细胞术等近年来应用于藻类细胞毒性研究的新技术方法(Ouyang et al., 2012; 2013), 研究富里酸存在条件下铜对普通小球藻光合作用与细胞生理的影响, 以便从相对微观的尺度上了解在DOM和铜共存条件下藻类生理生态的响应机制.
叶绿素荧光分析技术以光合作用理论为基础, 以生物体内的叶绿素荧光为探针, 研究生物光合生理状况以及各种外界因素对光合作用的影响(Maxwell and Johnson, 2000), 可以进行快速、灵敏和无损伤的检测(Govindjee, 1995; Krause, 1988; Maxwell and Johnson, 2000).流式细胞术(flow cytometry, FCM)是一种自动分析细胞或生物粒子的技术, 能够帮助区分活细胞与死细胞并对单个细胞进行快速多参数检测(Stauber et al., 2002), 在此基础上测定所需的生理参数能够更加准确地反映体系中活细胞而非细胞总体的生理水平, 有利于更为准确地获得藻类在胁迫条件下细胞水平上的响应, 近年来也被不断运用于藻类毒理学研究中(Franklin et al., 2001a; Franklin et al., 2001b; Yu et al., 2007).
本文在分析不同浓度的富里酸存在条件下铜对普通小球藻光合作用与细胞生理的影响时, 通过对富里酸-铜的复合暴露实验及富里酸单独暴露实验的结果进行比较分析, 减少由于富里酸的加入对实验结果讨论产生的干扰.同时结合叶绿素荧光分析与流式细胞术在测定物质毒性大小的基础上, 检测小球藻在光合作用与细胞生理等方面各项参数的变化, 着重关注外界胁迫下单个小球藻细胞在细胞层面上的生理响应, 并对小球藻细胞生理水平变化的机理进行探讨.使得研究从现象观察进入到细胞水平, 有助于深入了解物质毒性作用机理和相应的藻细胞响应机制, 为DOM对铜生物毒性影响的研究提供理论基础.
2 实验材料与方法(Materials and methods) 2.1 实验材料 2.1.1 受试生物及预培养受试生物选择普通小球藻(Chlorella vulgaris), 实验中所用普通小球藻购自中国科学院武汉水生生物研究所淡水藻种库, 藻种编号1068.普通小球藻作为受试生物具有以下优势:① 生长条件相对简单, 繁殖速率高; ② 细胞结构及遗传物质相对简单, 便于微观尺度上的研究; ③ 国内外有很多相关的研究报道, 利于研究结果的比较.
使用BG11液体培养基对普通小球藻进行培养, 培养条件为:GXZ-280B智能型光照生物培养箱(宁波东南仪器有限公司), 光强4000 Lux, 光暗比14 h:10 h, 温度(24±1) ℃.静止培养, 每天摇动2~3次且随机更换位置.由于BG11培养基中含有铜, 为减少干扰, 在进行暴露实验之前将普通小球藻在无铜BG11培养基中预培养至少3 d, 以除去原有的铜.
2.1.2 实验试剂BG11培养基的主要成分均购自国药; 富里酸标样Suwannee River Fulvic Acid Standard Ⅰ (SRFAS Ⅰ)购自国际腐殖酸协会(IHSS); CuSO4·5H2O用于暴露实验, 购自国药; NaOH用于调节富里酸体系pH, 购自西陇化工; 荧光素二乙酸酯(FDA)和碘化丙啶(PI)用于流式分析中的细胞染色, 购自Sigma公司.
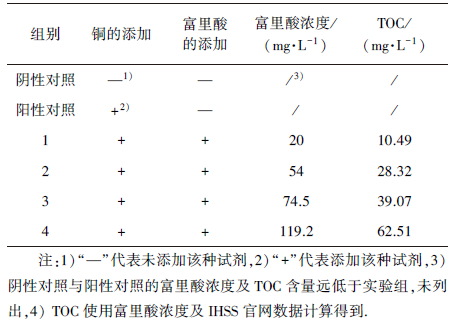
2.2 实验方法选取生长状态良好且处于指数生长期的普通小球藻(初始藻密度约为106个·mL-1)接种于含50 mL无铜培养液的150 mL锥形瓶中.使用SRFAS Ⅰ的水溶液作为暴露试剂, 暴露前使用0.01 mol·L-1的NaOH溶液调节富里酸水溶液pH为6.5~7.5.实验中设置阴性对照, 阳性对照及4个实验组, 每组设3个重复.各对照组及实验组的试剂添加情况及富里酸含量见表 1, 阳性对照和实验组铜的终浓度设为5 μmol·L-1(Ouyang et al., 2012; 宋淑芳, 2012)(铜的环境背景浓度约为0.15 μmol·L-1, 可忽略不计).样品共暴露96 h, 每隔24 h进行相应指标的测定.
| 表 1 对照组及实验组试剂添加情况及富里酸含量 Table 1 Reagents addition and the contents of fulvic acid in control groups and fulvic acid treatments |
复合暴露实验前进行富里酸单独暴露普通小球藻的补充实验, 实验中富里酸的浓度梯度, 具体实验流程及操作与上述复合暴露实验相同.
2.3 生理生态指标测定 2.3.1 光合作用使用叶绿素荧光仪测定普通小球藻的光诱导曲线, 进一步计算光合作用相关参数值.实际测定时, 样品进行25 min暗适应后, 利用MAXI-Imaging-PAM进行光诱导曲线的测定, 并进一步计算光合作用相关参数值:Fv/Fm(最大光合作用效率, 表征植物光合作用的潜力, 当植物收到胁迫时, Fv/Fm会有所降低); ФPSII(实际光合作用效率); ETR(表观光合电子传递速率)(Govindjee, 1995; Krause, 1988; Lazár, 1999; Maxwell and Johnson, 2000).
2.3.2 细胞生理使用流式细胞仪完成细胞生理指标的测量, 选择FDA和PI两种染色剂对藻细胞进行染色.FDA本身没有荧光效应, 但进入藻细胞后经脂酶水解后的产物能发出荧光, 当藻细胞的脂酶活性变化时, FDA的水解产物浓度也将随之变化, 其荧光强度即发生改变, 因此FDA染色荧光可以指示细胞是否死亡, 并且可用于评估细胞的脂酶活性(Franklin et al., 2001a; Stauber et al., 2002; Yu et al., 2007).正常藻细胞的PI荧光较弱, 当藻细胞膜受影响破裂后, PI能够进入细胞与核酸类物质结合, 引起PI荧光的大幅度增加, 因此, PI染色荧光可用于评估细胞膜完整性(Franklin et al., 2001b; Yu et al., 2007; Liu et al., 2008).实验中同时测量叶绿素a自发荧光(表征叶绿素a含量)和FSC(前向角散射光, 可以表征细胞体积大小变化).
测定时, 使用FDA-PI双染法(FDA使用丙酮溶解, 最终浓度25 μmol·L-1; PI的最终浓度10 μmol·L-1)对藻细胞暗处染色5 min, 检测FITC-A通道(Ex:488 nm, Em:500~560 nm), PE-A通道(Ex:488 nm, Em:549~601 nm), PerCP-Cy5-5-A通道(Ex:488 nm, Em:655~735 nm)和FSC-A通道(可与其它荧光同时检测)荧光, 进一步分析得到受影响细胞比例及平均荧光强度(Median fluorescence intensity, MFI).
2.4 数据处理使用FlowJo 7.6.1对流式细胞仪测定数据分析得到普通小球藻各检测通道的细胞荧光分布直方图.通过阴性对照各通道的细胞荧光分布, 确定受影响细胞的范围, 并进一步计算不同细胞所占比例以及平均荧光强度(Median fluorescence intensity, MFI).由于在藻类培养过程中会出现藻细胞正常死亡的现象, 因此本文使用相对阴性对照的正常细胞比例和MFI值(阳性对照或实验组/阴性对照×100%)进行讨论.
使用Excel 2010进行统计分析, 结果表现为:3个平行的算术均值±标准差.差异显著性分析、单因素方差分析、双因素方差分析等由SPSS 20.0统计软件完成, 差异显著性水平设为0.05, 其中p > 0.05和p < 0.05分别表示无显著性差异和有显著性差异.
3 结果(Results) 3.1 光合作用针对富里酸存在条件下, 铜对普通小球藻光合作用的影响, 使用叶绿素荧光仪测得阳性对照与实验组的普通小球藻的Fv/Fm, ФPSII和ETR相对值(相对阴性对照的比值, 下同)变化如图 1所示.阳性对照组与20 mg·L-1富里酸处理组的Fv/Fm相对阴性对照没有明显差别(p>0.05);高浓度富里酸(>20 mg·L-1)实验组明显高于阴性对照(p<0.05), 随着富里酸浓度的升高, 普通小球藻的Fv/Fm水平也有所升高.
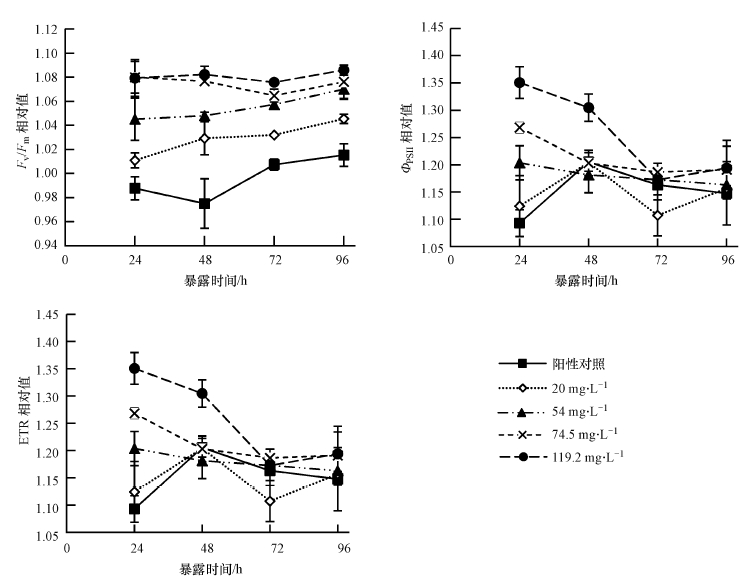 |
| 图 1 富里酸存在条件下, 铜对普通小球藻Fv/Fm, ФPSII和ETR的影响 Fig. 1 The effects of copper on the Fv/Fm, ФPSII and ETR of C. vulgaris in the presence of fulvic acid |
对于实际光合作用效率ФPSII和表观光合电子传递速率ETR, 阴性对照与阳性对照无显著区别(p>0.05), 与实验组有显著区别(p<0.05).实验组的ФPSII和ETR水平均高于阳性对照, 但不同实验组之间并未表现出显著差异.暴露24 h后, 随着富里酸浓度的增加, ФPSII和ETR有所上升; 但是随着暴露时间的延长, 不同实验组的结果相互趋近.
富里酸单独作用下, 普通小球藻的Fv/Fm, ФPSII和ETR相对值变化见图 2, 富里酸对普通小球藻的光合作用有促进的作用, 20 mg·L-1和54 mg·L-1富里酸处理组的普通小球藻的Fv/Fm与阴性对照无显著差别, 但74.5 mg·L-1和119.2 mg·L-1的富里酸会使Fv/Fm显著升高.20 mg·L-1的富里酸对ФPSII和ETR无显著影响, 但较高浓度的富里酸会使其水平升高.随着富里酸浓度的升高, 各光合作用参数的水平均有升高, 并在24 h时有最大值.
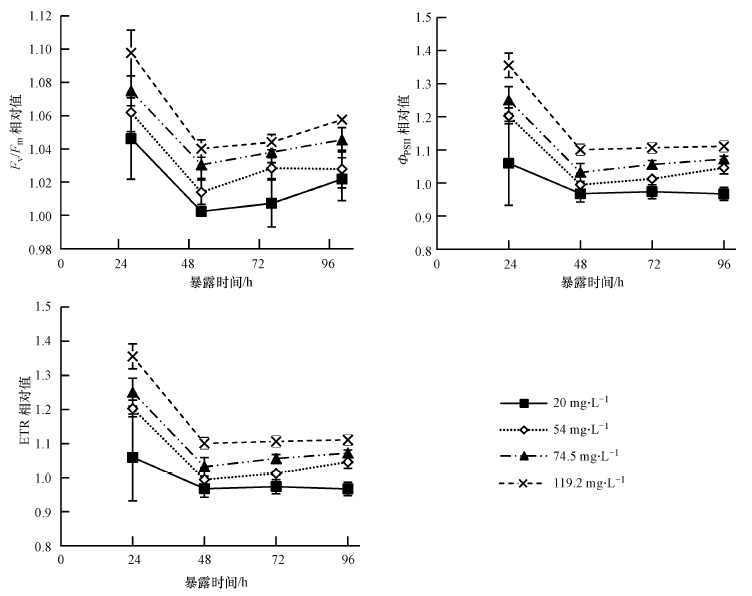 |
| 图 2 富里酸对普通小球藻Fv/Fm, ФPSII和ETR的影响 Fig. 2 The effects of fulvic acid on the Fv/Fm, ФPSII and ETR of C. vulgaris |
进一步对富里酸单独作用及富里酸与铜复合作用下普通小球藻的光合作用参数值进行分析发现:对于Fv/Fm, 当富里酸的浓度为20 mg·L-1时, 单独作用和复合作用的结果间无明显差别, 但当富里酸的浓度≥54 mg·L-1时, 单独作用下的参数值明显低于复合作用; 对于实际光合作用效率ФPSII和表观光合电子传递速率ETR, 富里酸单独作用下的参数值均与复合作用时有显著差异.
3.2 细胞生理流式细胞仪测得实验结束时(暴露96 h), 各对照组和实验组普通小球藻的FDA染色荧光如图 3所示; 实验过程中普通小球藻的FDA荧光正常细胞比例及FDA-MFI变化如图 4所示.图 3中, 蓝色区域代表正常细胞, 并可用于进一步计算正常细胞比例, 红色区域代表受影响的细胞.铜对普通小球藻的正常细胞比例有明显影响, 阳性对照的正常细胞比例最低.阴性对照与高浓度富里酸(>20 mg·L-1)处理组之间无显著差别, 20 mg·L-1的富里酸处理组明显高于阳性对照, 低于阴性对照和其它实验组.随着暴露时间的延长, 20 mg·L-1的富里酸处理组和阳性对照的普通小球藻正常细胞比例逐渐升高, 但仍然低于阴性对照.进一步分析得到阴性对照的FDA-MFI, 与74.5 mg·L-1和119.2 mg·L-1富里酸处理组无显著差别(p>0.05), 但阳性对照、20 mg·L-1和54 mg·L-1富里酸处理组的FDA-MFI明显高于阴性对照.
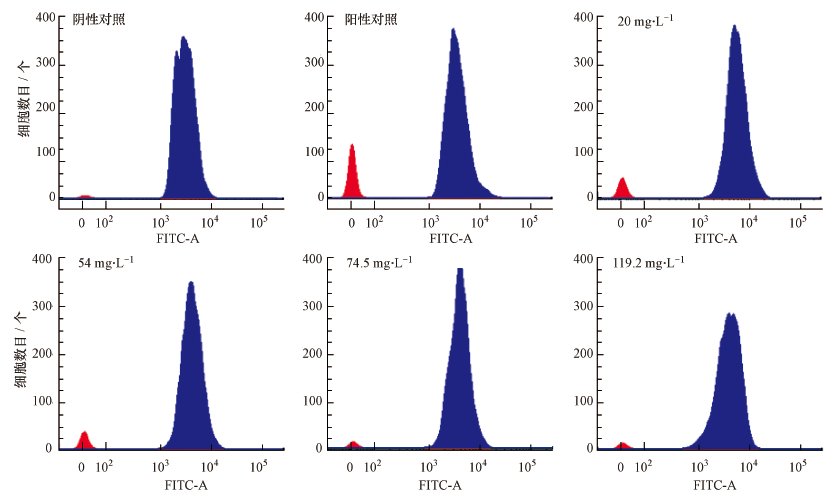 |
| 图 3 普通小球藻的FDA染色荧光(96 h) Fig. 3 The FDA staining fluorescence of C. vulgaris (after exposure for 96 h) |
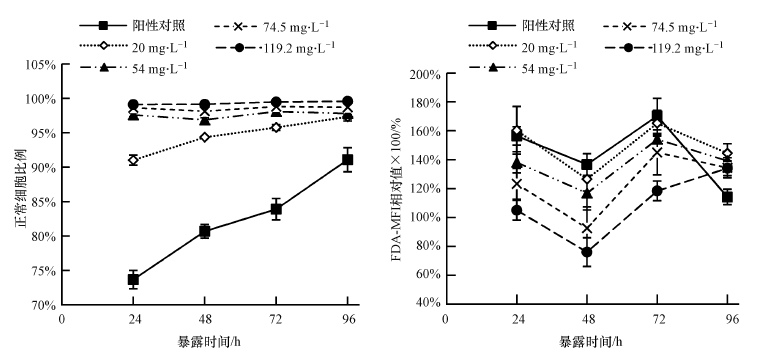 |
| 图 4 富里酸存在条件下, 铜对普通小球藻正常细胞比例和FDA-MFI的影响 Fig. 4 The effects of copper on the proportions of normal algal cells and FDA-MFI in the presence of fulvic acid |
富里酸作用下, 铜对普通小球藻PI染色荧光的影响如图 5所示.阴性对照受影响的细胞比例与高浓度富里酸(>20 mg·L-1)处理组无显著差别, 阳性对照的受影响细胞比例则显著高于其他实验组和阴性对照(p<0.05).受影响细胞比例相对值由高到低, 依次是阳性对照>20 mg·L-1>54 mg·L-1>74.5 mg·L-1>119.2 mg·L-1富里酸处理组, 富里酸的加入减弱了铜对小球藻的毒性, 且在铜浓度一定的条件下, 增加富里酸的浓度在一定程度上可以减少受影响的细胞数目.阳性对照和实验组测得的细胞膜通透性均高于阴性对照(p<0.05), 74.5 mg·L-1和119.2 mg·L-1富里酸处理组的细胞膜通透性无显著差异, 均高于阳性对照以及20 mg·L-1和54 mg·L-1富里酸处理组.
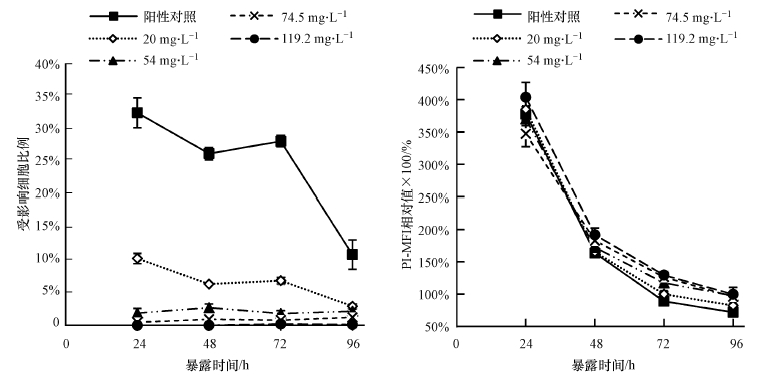 |
| 图 5 富里酸作用下, 铜对普通小球藻PI染色荧光的影响 Fig. 5 The effects of copper on the proportions of affected algal cells and PI-MFI in the presence of fulvic acid |
实验浓度的富里酸对普通小球藻的FDA染色荧光, FSC及叶绿素a自发荧光均无显著影响, 但会显著提高PI染色荧光.富里酸单独暴露下的普通小球藻PI染色荧光值均高于阴性对照, 如图 6所示.相同浓度的富里酸, 单独暴露下和与铜复合暴露下的普通小球藻PI染色荧光间具有显著差异.
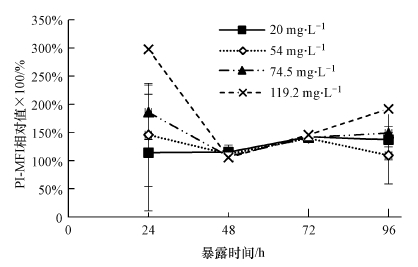 |
| 图 6 富里酸对普通小球藻PI-MFI的影响 Fig. 6 The effects of fulvic acid on the PI-MFI of C. vulgaris |
不同浓度富里酸作用下, 铜对普通小球藻叶绿素a自发荧光的影响如图 7所示, 实验组和阳性对照的叶绿素a自发荧光值均高于阴性对照, 但随暴露时间增加, 荧光值逐渐降低, 接近阴性对照.
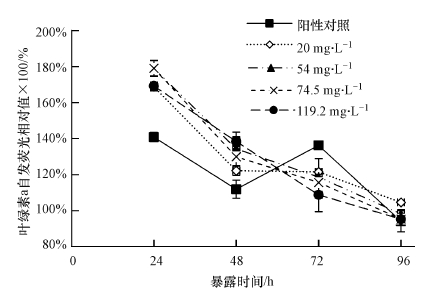 |
| 图 7 富里酸存在条件下, 铜对普通小球藻叶绿素a自发荧光的影响 Fig. 7 The effects of copper on the values of chlorophyll a fluorescence of C. vulgaris in the presence of fulvic acid |
不同浓度富里酸作用下, 铜对普通小球藻FSC荧光的影响如图 8所示.阳性对照和实验组的FSC荧光均明显高于阴性对照, 即藻细胞体积大于阴性对照.其中阳性对照与较低浓度的富里酸处理组(≤54 mg·L-1)无显著差异, 高于高浓度富里酸处理组(>54 mg·L-1).
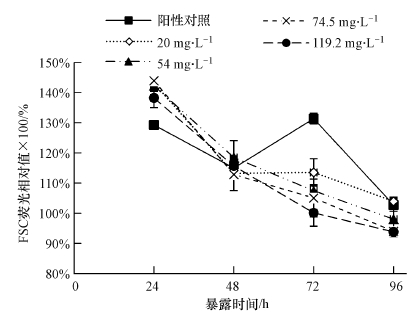 |
| 图 8 富里酸存在条件下, 铜对普通小球藻FSC荧光的影响 Fig. 8 The effects of copper on the FSC-MFI of C. vulgaris in the presence of fulvic acid |
阳性对照和富里酸处理组的光合参数Fv/Fm, ФPSII和ETR均高于阴性对照.根据富里酸单独暴露的实验结果, 富里酸能够使小球藻的Fv/Fm, ФPSII和ETR升高, 当富里酸的浓度≥54 mg·L-1时, 富里酸单独作用下的光合参数值显著低于复合作用, 可以认为复合暴露下普通小球藻光合参数的升高除富里酸的影响外, 铜也起到了一定作用.铜可以稳定叶绿素a进而促进植物光合作用(洪法水等, 2001; 胡筑兵等, 2006), 同时铜对小球藻的光合作用也有一定的抑制作用(Bauman et al., 2009; 欧阳慧灵, 2013).铜对植物光合作用的抑制机理主要通过增加植物体内活性氧的产量, 导致膜脂过氧化, 使类囊体片层结构解体破坏, 进而影响光合作用(Vassilev et al., 2003; Patsikka et al., 2001).本实验中, 实验组的铜对小球藻的光合作用既存在促进作用, 也存在抑制作用.在“铜饥饿”处理后, 实验暴露过程中仍使用无铜营养盐, 阴性对照一直处于铜元素缺乏状态, 影响了小球藻的光合作用水平.对于阳性对照和富里酸处理组, 暴露前期, 铜对光合作用的促进作用表现较为明显, 主要是由于铜的加入稳定了叶绿素a, 在这一阶段, 实际光合作用效率ФPSII和表观光合电子传递速率ETR水平较高, 同时也检测到了较强的叶绿素a自发荧光.但随着暴露时间延长, 铜对小球藻的光合作用主要表现出抑制性.实验中, 光合参数ФPSII和ETR, 以及叶绿素a自发荧光均在24 h时具有最大值, 而在24 h后迅速降低, 可以发现铜对光合作用的促进过程非常短暂, 主要集中在藻细胞与铜接触最初的24 h.除铜对光合作用的促进作用外, 普通小球藻的光合作用在受到重金属的胁迫时反应通常会相对滞后, 这也是光合参数及叶绿素a自发荧光在暴露实验初期没有显著下降的原因之一(欧阳慧灵, 2013).最大光合作用效率Fv/Fm能够表征植物光合作用的潜力, 当植物收到胁迫时, Fv/Fm会有所降低.本实验中, 铜的浓度一定, 随着富里酸浓度的升高, Fv/Fm的水平也在升高.通常小分子, 生物来源的DOM与铜结合后的产物也能够被细胞吸收(Buck et al., 2007; Zhong et al., 2012), 但由于富里酸分子量较大, 与铜络合后会降低藻细胞对其的吸收, 从而降低其生物毒性, 表现为Fv/Fm水平的升高.富里酸浓度越高, 络合态的铜所占比例越高, 生物毒性越低; 当富里酸浓度达到一定水平时, 络合态的铜所占比例几乎不再变化, 再增加富里酸浓度, 毒性效应基本不变.因此, 74.5和119.2 mg·L-1富里酸处理组的Fv/Fm水平在整个暴露实验过程中高于其他处理组, 但是两个处理组之间未表现出明显差异.
通过FDA染色荧光的结果分析正常藻细胞的比例可以发现, 铜对于小球藻细胞具有明显的毒性, 增加了细胞死亡率, 而富里酸的加入会降低铜的毒性效应, 降低藻细胞死亡率.与最大光合作用效率Fv/Fm类似, 当富里酸浓度增加到一定程度时(74.5 mg·L-1和119.2 mg·L-1), 藻细胞的正常细胞比例不再随富里酸浓度的升高而升高.阳性对照, 以及20和54 mg·L-1富里酸处理组的FDA-MFI相对较高, 但此处较高水平的FDA-MFI并不是因为脂酶活性较高, 当铜的暴露浓度较低时, 藻细胞的FDA荧光值将高于对照组, 主要是源于细胞膜极化导致细胞对FDA的吸收增加(Franklin et al., 2001a).随富里酸浓度增加, 自由形态的铜离子所占比例减小, 细胞膜的极化作用也不断减弱, FDA-MFI逐渐减小.随暴露时间增加, 极化作用减弱, 表现为FDA荧光值的降低.根据PI染色荧光结果, 铜和富里酸均有增加小球藻细胞膜通透性的作用, 结合FDA染色荧光数据, 富里酸单独作用时的正常细胞比例与阴性对照无显著差异(p>0.05).可以认为富里酸能够使藻细胞的细胞膜通透性增加, 但是不具有致死性; 铜也具有增强藻细胞细胞膜通透性的作用, 并会造成细胞死亡, 这也与之前铜对光合作用的抑制机理具有一定的一致性.阳性对照和实验组均会使普通小球藻的FSC荧光升高, 表明藻细胞体积有增大的趋势, 可能是由于体积较小的藻细胞更易受铜胁迫而死亡.体积较小的藻细胞通常为新生细胞, 各项机能还未完善, 因此对铜的耐受性也较弱.随暴露时间延长, 阳性对照和实验组的各项光合和细胞生理指标均趋近阴性对照, 可以认为是小球藻在受到胁迫后耐受性增加, 对环境适应的结果, 使得普通小球藻的光合作用和细胞生理得到了一定的恢复.
5 结论(Conclusions)1) 富里酸能够促进普通小球藻的光合作用; 铜在暴露初期, 藻细胞缺乏铜元素时能够稳定叶绿素a, 增强藻细胞的实际光合作用效率ФPSII和表观光合电子传递速率ETR, 随暴露时间延长, 对光合作用的抑制表现明显; 富里酸能够有效减弱铜的光合毒性, 增强藻细胞的光合作用潜力.
2) 铜能够增大普通小球藻细胞的体积, 增强细胞膜通透性, 并导致藻细胞死亡; 富里酸的加入能够明显降低藻细胞的死亡率, 高浓度的富里酸可以有效降低因铜导致的藻细胞体积的增大.
3) 普通小球藻具有一定的耐受性和环境适应性, 暴露后期在光合作用和细胞生理方面均会有一定程度的恢复.
Buck K N, Ross J R M, Flegal A R, et al. 2007. A review of total dissolved copper and its chemical speciation in San Francisco Bay, California[J]. Environmental Research, 105(1): 5–19.
DOI:10.1016/j.envres.2006.07.006
|
D'Andrilli J, Foreman C M, Marshall A G, et al. 2013. Characterization of IHSS Pony Lake fulvic acid dissolved organic matter by electrospray ionization Fourier transform ion cyclotron resonance mass spectrometry and fluorescence spectroscopy[J]. Organic Geochemistry, 65(6): 19–28.
|
Franklin N M, Stauber J L, Lim R P. 2001. Development of flow cytometry-based algal bioassays for assessing toxicity of copper in natural waters[J]. Environmental Toxicology and Chemistry, 20(1): 160–170.
DOI:10.1002/etc.v20:1
|
Franklin N M, Adams M S, Stauber J L, et al. 2001. Development of an improved rapid enzyme inhibition bioassay with marine and freshwater microalgae using flow cytometry[J]. Archives of Environmental Contamination and Toxicology, 40(4): 469–480.
DOI:10.1007/s002440010199
|
Govindjee E. 1995. Sixty-three years since Kautsky: chlorophyll a fluorescence[J]. Australian Journal of Plant Physiology, 22(2): 131–160.
DOI:10.1071/PP9950131
|
何伟. 2014. 巢湖水体溶解性有机质及其环境效应研究[D]. 北京: 北京大学. 1-215
|
洪法水, 魏正贵, 赵贵文, 等. 2001. 金属叶绿素a配位结构的研究[J]. 生物化学与生物物理进展, 2001, 28(3): 381–386.
|
胡筑兵, 陈亚华, 王桂萍, 等. 2006. 铜胁迫对玉米幼苗生长、叶绿素荧光参数和抗氧化酶活性的影响[J]. 植物学通报, 2006, 23(2): 129–137.
|
Jiang Y J, He W, Liu W X, et al. 2014. The seasonal and spatial variations of phytoplankton community and their correlation with environmental factors in a large eutrophic Chinese lake (Lake Chaohu)[J]. Ecological Indicators, 40: 58–67.
DOI:10.1016/j.ecolind.2014.01.006
|
Krause G H. 1988. Photoinhibition of photosynthesis. An evaluation of damaging and protective mechanisms[J]. Physiologia Plantarum, 74(3): 566–574.
DOI:10.1111/ppl.1988.74.issue-3
|
Lazár D. 1999. Chlorophyll a fluorescence induction[J]. Biochimica et Biophysica Acta, 1412(1): 1–28.
DOI:10.1016/S0005-2728(99)00047-X
|
Liu W, Chen S, Quan X, et al. 2008. Toxic effect of serial perfluorosulfonic and perfluorocarboxylic acids on the membrane system of a freshwater alga measured by flow cytometry[J]. Environmental Toxicology and Chemistry, 27(7): 1597–1604.
DOI:10.1897/07-459.1
|
Ma M, Zhu W Z, Wang Z J, et al. 2003. Accumulation, assimilation and growth inhibition of copper on freshwater alga (Scenedesmus subspicatus 86.81 SAG) in the presence of EDTA and fulvic acid[J]. Aquatic Toxicology, 63: 221–228.
DOI:10.1016/S0166-445X(02)00179-0
|
Maxwell K, Johnson G N. 2000. Chlorophyll fluorescence—a practical guide[J]. Journal of Experimental Botany, 51(345): 659–668.
DOI:10.1093/jxb/51.345.659
|
Ouyang H L, Kong X Z, He W, et al. 2012. Effects of five heavy metals at sub-lethal concentrations on the reproduction and photosynthesis of Chlorella vulgaris[J]. Chinese Science Bulletin, 57(10): 785–793.
|
欧阳慧灵. 2013. 重金属、化感物质和磷胁迫对普通小球藻生理生态的影响[D]. 北京: 北京大学. 1-86
|
Ouyang H L, Kong X Z, Lavoie M, et al. 2013. Photosynthetic and cellular toxicity of cadmium in Chlorella vulgaris[J]. Environmental Toxicology and Chemistry, 32(12): 2762–2770.
DOI:10.1002/etc.2362
|
Qiu J W, Tang X, Zheng C B, et al. 2007. Copper complexation by fulvic acid affects copper toxicity to the larvae of the polychaete Hydroides elegans[J]. Marine Environmental Research, 64(5): 563–573.
DOI:10.1016/j.marenvres.2007.06.001
|
Sánchez-Marín P, Santos-Echeandía J, Nieto-Cid M, et al. 2010. Effect of dissolved organic matter (DOM) of contrasting origins on Cu and Pb speciation and toxicity to Paracentrotus lividus larvae[J]. Aquatic Toxicology, 96(2): 90–102.
DOI:10.1016/j.aquatox.2009.10.005
|
宋淑芳. 2012. 铜和铬对小球藻的致毒机理及解毒方法研究[D]. 杭州: 浙江大学. 1-124
http://cdmd.cnki.com.cn/article/cdmd-10335-1012318166.htm |
Stauber J L, Franklin N M, Adams M S. 2002. Applications of flow cytometry to ecotoxicity testing using microalgae[J]. Trends in Biotechnology, 20(4): 141–143.
DOI:10.1016/S0167-7799(01)01924-2
|
Tait T N, Cooper C A, Mcgeer J C, et al. 2016. Influence of dissolved organic matter (DOM) source on copper speciation and toxicity to Brachionus plicatilis[J]. Environmental Chemistry, 13: 496–506.
|
Taylor N S, Kirwan J A, Yan N D, et al. 2015. Metabolomics confirms that dissolved organic carbon mitigates copper toxicity[J]. Environmental Toxicology & Chemistry, 35(3): 635–644.
|
徐珑, 杨曦, 张爱茜, 等. 2005. 水环境中的光化学研究进展[J]. 化学进展, 2005, 17(3): 412–415.
|
Ytreberg E, Karlsson J, Hoppe S, et al. 2011. Effect of Organic Complexation on Copper Accumulation and Toxicity to the Estuarine Red Macroalga Ceramium tenuicorne: A Test of the Free Ion Activity Model[J]. Environmental Science & Technology, 45(7): 3145–3153.
|
Ytreberg E, Karlsson J, Ndungu K, et al. 2011. Influence of salinity and organic matter on the toxicity of Cu to a brackish water and marine clone of the red macroalga Ceramium tenuicorne[J]. Ecotoxicology & Environmental Safety, 74(4): 636–642.
|
Yu Y, Kong F, Wang M, et al. 2007. Determination of short-term copper toxicity in a multispecies microalgal population using flow cytometry[J]. Ecotoxicology and Environmental Safety, 66(1): 49–56.
DOI:10.1016/j.ecoenv.2005.10.014
|
张守仁. 1999. 叶绿素荧光动力学参数的意义及讨论[J]. 植物学通报, 1999, 16(4): 444–448.
|
Zhong H, Evans D, Wang W X. 2012. Uptake of dissolved organic carbon-complexed 65Cu by the green mussel Perna viridis[J]. Environmental Science & Technology, 46(4): 2383–2390.
|
 2017, Vol. 37
2017, Vol. 37