2. 中国科学院生态环境研究中心环境水质学国家重点实验室, 北京 100085;
3. 东北师范大学环境学院, 长春 130117;
4. 邢台市环境保护局, 邢台 054000;
5. 邢台市邢台县环境保护局, 邢台 054000
2. State Key Laboratory on Environmental Aquatic Chemistry, Research Center for Eco-Environmental Science, Chinese Academy of Sciences, Beijing 100085;
3. School of Environment, Northeast Normal University, Changchun 130117;
4. Xingtai Environmental Protection Agency, Xingtai 054000;
5. Xingtai County Environmental Protection Agency, Xingtai 054000
磷(P)是淡水生态系统中重要的营养元素(Cade-Menun et al., 2006).农业、工业和生活污水的过量排放导致水体中磷含量急剧增加, 引起淡水生态系统富营养化频发, 水质恶化, 进而影响淡水生态系统健康(Carpenter, 2008).针对湖库的磷形态特征及富营养问题的研究已经有很多, 但有关典型人工河流生态系统中磷形态特征的研究还很少(Deborde et al., 2007; Matzinger et al., 2007).20世纪50年代到60年代, 为了分流洪水, 降低洪涝灾害, 人们在海河流域修建了许多人工河流.近30年, 随着海河流域人口的急剧增加和工农业的飞速发展, 导致流域污废水排放量增加, 人工河流的功能由泄洪变为污水排放渠道, 大量磷随着污废水进入人工河流, 上覆水和沉积物中磷大量积累, 增加了人工河流富营养化爆发的风险.另一方面, 人工河流河道蜿蜒度小, 河岸带形态单一, 坡降小, 河流闸坝林立, 河流水流缓滞, 加剧了河流富营养化程度(张文强等, 2016).因此, 有关磷在人工河流生态系统中的形态特征和循环转化过程亟需深入研究.
核磁共振(NMR)技术是现代科学中用途广泛的分析手段, 它可以快速准确地分析土壤、动植物组织、沉积物等环境样品(Simpson et al., 2012).液相31P核磁共振(31P-NMR)能够根据振动频率的不同分析磷化合物形态(Cardoza et al., 2004; Reitzel et al., 2006).通过液相31P-NMR分析, 膦酸酯、正磷酸盐、磷酸单酯、磷酸二酯(磷酯和DNA磷)、焦磷酸盐和多磷酸盐等被成功检测(Cade-Menu et al., 2005).因此, 液相31P-NMR不仅可以提供海洋、湖泊沉积物中磷的组成和形态特征信息, 也可以提供磷的生物地球化学循环过程信息.
生物质磷(Biogenic-P)与生物的新陈代谢密切相关, 被用来描述所有有机磷化合物、焦磷酸盐和多磷酸盐(Ahlgren et al., 2005).生物质磷是沉积物磷的重要组成部分, 占NaOH-EDTA提取总磷的平均比例为25.6%(Shinohara et al., 2012), 主要通过腐殖质、浮游植物和细菌的沉淀进行累积, 形成最初的磷储蓄库, 参与到磷的循环过程中.随着研究的深入, 人们发现在磷的内源负荷中, 生物质磷的矿化和对正磷酸盐的释放将会影响水体的整体生产力(Ahlgren et al., 2006).近几年, 国内学者利用核磁共振技术开展了有关有机磷形态的研究, 但对于生物质磷的研究较少, 且由于分析技术不够成熟, 对于生物质磷的形态特征和转化过程认识也不够深入.
目前, 运用核磁共振技术分析湖库磷形态特征的研究较多, 但运用31P核磁共振分析人工河流中生物质磷形态特征和循环转化过程的研究较少.因此, 本研究以滏阳新河沉积物为研究对象, 运用液相31P-NMR技术分析生物质磷化合物的形态和变化特征, 以期深入认识磷在人工河流系统中的传递和转化过程, 并为深入认识磷的生物地球化学循环过程提供支持.
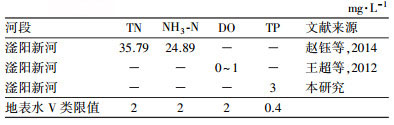
2 材料和方法(Materials and methods) 2.1 样点布置海河流域位于我国华北地区, 流域面积31.8×104 km2, 其中, 山丘和高原面积18.9×104 km2, 占60%;平原面积12.9 km2, 占40%.1998—2010年, 流域年均地表水资源量为118×108 m3, 水资源严重匮乏, 面临较大的富营养化问题.海河流域囊括了北京、天津、河北、山西等8个省、自治区、直辖市的全部或部分地区, 总人口数约1.5亿, 经济社会发展迅速、人口密度较高是海河流域的鲜明特征.滏阳新河是海河流域典型的人工河流, 主河道长33 km, 宽1600~1700 m, 横跨衡水市和邢台市.为了提高滏阳河泄洪能力, 海河流域在1967—1968年修建完成滏阳新河, 主要接纳来自北澧河、洨河和滏阳河的洪水.随着经济和人口的高速增长, 滏阳新河逐渐变成纳污河流.污染物的大量排放导致滏阳新河水体磷含量急剧增加, 复合污染较严重(表 1).水体中TN和NH3-N平均浓度分别超过地表水环境质量标准(GB3838—2002) Ⅴ类限值(2.0 mg·L-1)17.9倍和12.4倍, DO平均浓度低于地表水Ⅴ类限值(2 mg·L-1), 低氧现象严重, TP平均浓度超过地表水Ⅴ类限值(0.4 mg·L-1)7.5倍.
| 表 1 文献资料中的常规水质指标数据 Table 1 Data concerning conventional water quality indicators in literature |
本研究中, 沿滏阳新河流向依次布设5个采样点, 研究河段设有4座闸坝, 以河段上游艾辛庄闸坝(闸坝a)规模最大.样点与闸坝间隔布设, 相对位置如图 1所示.样点1布设在艾辛庄闸坝上游, 距艾辛庄闸坝约200 m, 样点2布设在滏阳新河衡水段上游、c闸坝上游, 距c闸坝约10 km, 样点3布设在滏阳新河衡水段下游、d闸坝上游, 距d闸坝约2 km, 样点4、5分别布设在滏阳新河衡水段下游(图 1).
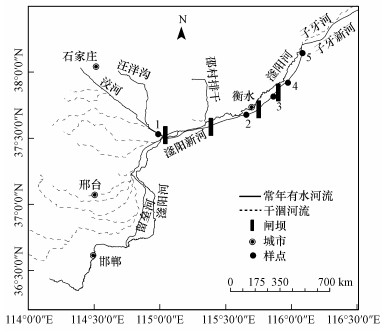 |
| 图 1 滏阳新河采样点示意图 Fig. 1 Location of sampling sites in Fuyangxin River |
于2012年7月进行样品采集.利用自重力沉积物采集器(奥地利UWITEC)采集沉积物表层约5 cm的样品, 为了取得具有代表性的样品, 根据样点实际情况, 每个样点平行采集3个沉积物样品, 且平行样点之间距离不少于500 m.同一样点的平行样品合并混匀, 所有样品立即在-18 ℃下冷冻保存.水样在表层采集.
沉积物中的总磷(TP)和无机磷(IP)测定:称取沉积物样品两份, 每份0.5 g, 一份于550 ℃马弗炉中灰化2 h, 然后用1 mol·L-1 HCl提取16 h, 另一份直接用1 mol·L-1 HCl提取16 h, 分别对其中的TP和IP进行提取和分析.沉积物中OP含量由TP和IP的差值得到(Aspila et al., 1976).沉积物pH测定:去CO2水与过20目筛沉积物以2.5 mL/1 mg的水土比混合后, 利用pH计测定.沉积物有机质(OM)含量测定:将去除水分的沉积物样品置于马弗炉中550 ℃处理4 h, 通过灼烧前后的质量差值得到(Jensen et al., 1992).上覆水中的TP采用《水与废水监测分析方法(第四版)》钼锑抗分光光度法测定, 具体操作为:5%的过硫酸钾溶液消解, 10%的抗坏血酸与钼酸盐溶液显色, 700 nm波长处比色.
2.3 沉积物OP提取与液相31P-NMR分析本研究中选择沉积物与提取液的比例为1 g/10 mL, 提取时间为16 h, 提取剂选择0.25 mol·L-1 NaOH和50 mmol·L-1 EDTA的混合溶液.具体操作步骤为:称取3 g沉积物放入离心管中, 加入30 mL 0.25 mol·L-1 NaOH和50 mmol·L-1 EDTA的混合溶液, 在室温下提取16 h(Turner et al., 2003b); 冷冻离心40 min, 取适量提取液稀释来分析IP和TP, 分析方法采用钼锑抗分光光度法.提取液中的OP由TP与IP的差值得出(Aspila et al., 1976).剩余上清液用冷冻干燥机冷干至粉末状, 用于31P-NMR分析.研究表明, 冻干的提取液不会改变磷的组成(Hupfer et al., 1995; Hupfer et al., 2004).
称取提取所得的干燥粉末300 mg, 溶于0.6 mL D2O和0.1 mL 10 mol·L-1 NaOH的混合溶液中, 于室温超声30 min, 超声完毕后静止平衡5 min.向平衡溶液中加入2%的碳酸氢钠-连二亚硫酸钠缓冲溶液以减少Fe和Mn等顺磁性离子的干扰.混合溶液在转速为14000 r·min-1的高速离心机中离心15 min, 将离心获得的上清液转移至5 mm的核磁共振管中上机检测, 获得图谱.核磁共振仪选用瑞士BRUKER公司的BRUKERAV400, 运行条件为:温度20 ℃, 31P共振频率129.53 MHz, 31P谱的脉冲为12.00 usec, 脉冲功率3.00 dB, 循环延迟3.6 s, 扫描20000次左右(白秀玲等, 2011).对图谱进行解析, 所有31P化学位移均参照85%的H3PO4(δ=0 ppm), 根据参照文献(Turner et al., 2003a; Cade-Menun et al., 2005)中主要磷形态峰值的位移确定其组成, 分别为正磷酸盐(Ortho-P, δ=6~7 ppm)、焦磷酸盐(Pyro-P, δ=-3.5~-4.5 ppm)、磷酸单酯(Mono-P, δ=4~6 ppm)、膦酸盐(Phon-P, δ=12~23 ppm)、磷酯(Lipids-P, δ=1~3 ppm)和DNA磷(DNA-P, δ=0~-1 ppm).最后对沉积物有机磷不同组分图谱进行积分, 根据不同组分所占比例及NaOH-TP含量, 计算沉积物中不同组分有机磷的含量.
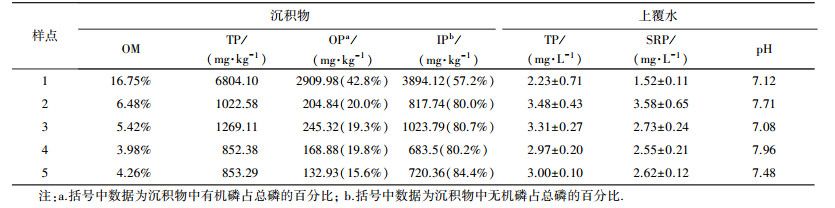
3 结果(Results) 3.1 沉积物及上覆水理化特征滏阳新河沉积物及上覆水理化特征见表 2.对于这5个样点的沉积物来说, TP含量为852.38~6804.10 mg·kg-1, 变化幅度较大, 最高值出现在艾辛庄大坝附近的样点1, 接近7000 mg·kg-1.滏阳新河沉积物中TP含量的平均值为2160.29 mg·kg-1, 其中IP占主要部分; OP含量为132.93~2909.98 mg·kg-1, 占TP的比例为15.6%~42.8%.上覆水pH为7.08~7.96, 平均值为7.47.有机质(OM)含量随着沉积物TP含量的变化而变化, 为3.98%~16.75%, 平均值为7.38%.上覆水中TP和SRP(活性磷)浓度变化较大, 分别为2.23~3.48 mg·L-1与1.52~3.58 mg·L-1.
| 表 2 沉积物及表层水基本理化性质 Table 2 Physical chemical properties of sediments in and concentration of total P in the water column |
滏阳新河沉积物的核磁共振图谱如图 2所示.利用31P-NMR技术在NaOH-EDTA提取液中共检测到6类磷化合物, 分别为膦酸盐(Phon-P, δ=12~23 ppm)、正磷酸盐(Ortho-P, δ=6~7 ppm)、磷酸单酯(Mono-P, δ=4~6 ppm)、磷酯(Lipids-P, δ=1~3 ppm)、DNA磷(DNA-P, δ=0 ppm)及焦磷酸盐(Pyro-P, δ=-3.5~-4.5 ppm)(Turner et al., 2003; Cade-Menun, 2005; Cade-Menun et al., 2006).样点2和4未检测到膦酸盐, 样点4和5未检测到磷酯.
 |
| 图 2 滏阳新河沉积物NaOH-EDTA提取物核磁共振图谱(a)和标准图谱(b)(A.膦酸盐, B.正磷酸盐, C.磷酸单酯, D.磷酸二酯, E.磷酯, F.DNA磷, G.焦磷酸盐)(修改自Cade-Menun, 2005) Fig. 2 31P-NMR spectra of NaOH-EDTA extracts(a) and NaOH-TP extracts in P fraction(b) of the sediments in Fuyangxin River (A.Phon-P, B.Ortho-P, C.Mono-P, D.Diesters-P, E.Lipids-P, F.DNA-P, G.Pyro-P) |
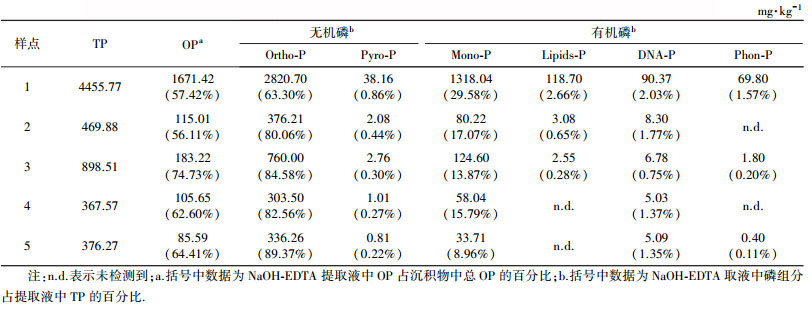
滏阳新河沉积物中磷化合物的含量和相对分布如表 3所示.NaOH-EDTA提取液中OP含量为85.59~1671.42 mg·kg-1, 回收率为56.15%~74.69%.正磷酸盐(Ortho-P)是NaOH-EDTA提取液的主要组成部分, 含量为303.50~2820.70 mg·kg-1, 占比为63.30%~89.37%.焦磷酸盐(Pyro-P)含量远低于正磷酸盐, 含量为0.81~38.16 mg·kg-1, 占比为0.22%~0.86%.磷酸单酯(Mono-P)也是NaOH-EDTA提取液的主要组成部分, 含量为33.71~1318.04 mg·kg-1, 占NaOH-EDTA提取液中TP的百分比为8.96%~29.58%.DNA-P含量为5.03~90.37 mg·kg-1, 占NaOH-EDTA提取液中TP的百分比为0.75%~2.03%.磷酯(Lipids-P)和膦酸盐(Phon-P)含量分别为n.d.~118.70 mg·kg-1和n.d.~69.80 mg·kg-1, 占NaOH-EDTA提取液中TP的百分比分别为0.28%~2.66%和0.11%~1.57%.
| 表 3 液相31P NMR检测的NaOH-EDTA提取液中磷化合物的含量 Table 3 Concentrations of P compounds in NaOH-EDTA extracts of the sediments determined by solution 31P-NMR |
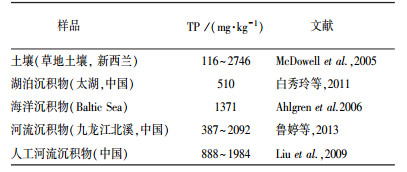
滏阳新河磷污染比较严重, 上覆水中TP和SRP的平均浓度分别为3.0 mg·L-1和2.6 mg·L-1, 分别超过我国地表水环境质量标准(GB3838-2002) Ⅴ类水标准(0.4 mg·L-1)7.5倍和6.5倍.滏阳新河沉积物累积了大量的磷, 样点1中的含量高达6804.10 mg·kg-1, 平均含量也达到2160.29 mg·kg-1, 远高于全国土壤磷平均含量(500 mg·kg-1), 也高于该区域背景值(545 mg·kg-1, 张文强等, 2016).沉积物中磷的含量高于土壤、湖泊沉积物和海洋沉积物(表 4).上覆水和沉积物中磷含量差异较大, 根据实验结果可知, 在滏阳新河沉积物中, 磷酸二酯和焦磷酸盐的含量较低, 平均占比分别为0.72%和0.42%;另一方面, 磷酸二酯和焦磷酸盐是不稳定态磷, 被认为是河流沉积物中磷的主要来源, 矿化速度相对较快, 并释放磷酸盐至孔隙水, 最终进入上覆水, 导致上覆水和沉积物中磷含量差异巨大.
| 表 4 相关文献中通过31P-NMR提取的TP数据 Table 4 Data concerning extracted TP by 31P-NMR spectroscopy in literature |
滏阳新河的补给水源以沿岸生活和生产废水为主, 污废水携带磷进入水体:滏阳新河两岸覆盖农田, 灌溉和雨水冲刷导致的地表径流磷含量较高; 水体上游工业废水的排放导致水体磷含量进一步升高.丰水期, 水量较大, 流速较快, 磷不易沉积, 水质相对较好; 枯水期, 水量较少, 流速缓慢, 同时由于滏阳新河形态特点和闸坝的截留作用, 进一步加速了磷的沉积, 外源的持续输入导致水体磷含量相对较高, 水质较差.Pernet Coudrier等(2012)研究发现, 北京及其周边地区每天向海河流域释放4.4 t磷, 外源输入量较大; 大气沉降也会携带磷进入水体, 成为水体中磷输入的又一重要来源, 对磷的生物地球化学循环过程产生重要影响(Gross et al., 2013).因此可以推测, 海河流域水体磷含量高与华北地区雾霾关系密切; 当大量污染物输入河流生态系统, 水体溶解氧(DO)浓度降低(<63 μmol·L-1), 导致磷从沉积物重新释放(Sulugambari et al., 2016), 滏阳新河复合污染严重, 高浓度氨氮、低DO增加了磷重新释放的风险; Sulugambari等(2016)研究发现, 在冬天和春天, 电缆细菌使硫化亚铁重新溶解, 导致亚铁离子结合P形成Fe-oxide-P, 沉积在缺氧层; 在夏天, 当沉积物-水界面氧气耗尽, Fe-oxide-P会释放磷酸盐到孔隙水和上覆水, 增加了磷的生物可利用性.另一方面, 由于滏阳新河为人工河流, 河道蜿蜒度小, 河岸带单一, 闸坝众多, 流速缓慢, 进一步加剧了河流富营养化程度, 导致滏阳新河沉积物中磷的含量逐渐升高.
Qu等(2010)研究显示, 在1970—2000年间, DIN和DIP的主要来源分别为农业和城市污水, 预测在2030—2050年间, 这些污染源将占据主导地位.近年来, 大量含磷化肥随地表径流入河, 城镇生活污水大量排放, 导致河流水体磷素急剧增加.研究显示(李惠敏等, 2000), 1980—2007年, 工业与城镇污废水产生量由31.4×108 t增加到47.5×108 t.将来如果不进行控制, 磷污染会越来越严重.
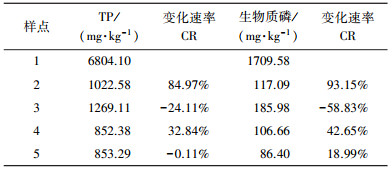
4.2 生物质磷在人工河流系统中的变化关于滏阳新河沉积物的试验数据显示(表 5), 从样点1到样点5, TP和生物质磷含量呈逐渐递减趋势, 其中, 样点1~2降幅明显, 降幅分别为84.97%和93.15%.在关于子牙河的研究中, 沿河流流向, TP降幅为87.05%(张文强等, 2016); 样点2~5, TP和生物质磷降幅较小, TP降幅分别为-24.11%、32.84%和-0.11%, 生物质磷降幅分别为-58.83%、42.65%和18.99%, 生物质磷降幅高于TP.沿艾辛庄大坝水流方向, TP和生物质磷在样点1和样点2含量差异明显, 分析样点图可知, 由于规模相对较大的艾辛庄闸坝的修建, 导致河流流量间歇性波动, 使人工河流具有和自然河流相似的磷沉积量, 对磷截留量影响较大; TP和生物质磷在样点2~5含量差异较小, 分析样点图可知, 样点2~5之间建有3座小型闸坝, 可以推测小型闸坝对磷的沉积作用较小; 另一方面, 人工河流河道蜿蜒度小, 河岸带单一, 坡降小, 物理连续性差, 对磷的沉降作用较小.样点1~5, TP含量为853.29~6804.1 mg·kg-1, 其中, 样点1的TP含量最高, 接近7000 mg·kg-1; 生物质磷含量为86.40~1709.58 mg·kg-1, 占TP的比例为10.13%~25.13%, 其中, 样点1的生物质磷含量最高, 接近2000 mg·kg-1.
| 表 5 沿坝方向沉积物中TP和生物质磷含量变化 Table 5 The concentrations of TP and biogenic-P as the distance from Aixinzhuang dam |
自20世纪60年代起, 为灌溉和防洪, 人们在海河流域修建了许多人工河流, 滏阳新河是海河流域大量人工河流的缩影(张文强等, 2016).为了调控水量, 在人工河流系统修建了许多闸坝, 闸坝极大改变了河流在生态系统中的作用.艾辛庄闸坝规模较大, 相对于其它3座小型闸坝, 调蓄作用明显, 截留约85%的TP, 在一定程度上破坏了河流的连续统, 阻断了河流作为物质传输和能量流动的廊道.例如, 在卡里巴湖修建的卡里巴大坝截留了约87%的TP; 迪芬贝克湖截留了流入南萨斯喀彻温河约94%的TP(Maavara et al., 2015).Maavara等(2015)通过理论模型预测, 在2000年, 闸坝截留的TP为42 Gmol·a-1, 相当于全世界河流TP负荷的12%, 同时相当于1970年闸坝TP截留量的2倍.因此, 建有大型闸坝的自然河流在一定程度上具有了人工河流的特点, 人为改造和人为干预较严重的自然河流会阻断物质和能量在河段上下游的传输, 均可认为是人工河流.另一方面, 闸坝的运行引起河流流量的间歇性波动(Perner Coudrier et al., 2012).河流流量的间歇性波动使部分河段干涸, 导致沉积物在坝前或坝后累积, 可以想象, 一旦截留量超过河段的累积容量, 在水量较大时, 水流对坝前沉积物脉冲式的冲刷将增加河段下游水污染事件爆发的风险.Zhang等(2016)研究发现, 一旦科纳温戈水库达到沉积物储存容量, 流经科纳温戈闸坝至下游的TP负荷将增加70%, 水污染事件爆发风险较高.
从核磁共振检测结果看, 滏阳新河沉积物生物质磷主要包括膦酸盐、磷酸单酯、磷酯、DNA磷和焦磷酸盐.生物质磷含量为86.40~1709.58 mg·kg-1, 占比为10.13%~25.13%.在NaOH-EDTA提取液中未检测到聚磷酸盐.聚磷酸盐是沉积物中不稳定态磷, 矿化相对较快(Hupfer et al., 2004; Reitzel et al., 2006).焦磷酸盐来源于酯类或者在碱性提取过程中水解的聚磷酸盐(Hupfer et al., 1995).聚磷酸盐和焦磷酸盐被认为是磷化合物中最不稳定的磷, 在磷循环过程中起重要作用(Ahlgren et al., 2005).磷酸单酯是NaOH-EDTA提取液中生物质磷的主要组成部分.来自于粪便、植物、浮游动物和藻类的肌醇磷酯是磷酸单酯的主要组成部分, 它们被认为无生物可利用性(Turner et al., 2002; 2006).但一些研究显示, 在厌氧条件下, 肌醇磷酯可能会释放磷酸盐(Livingstone et al., 1982; Golterman et al., 1998).表层水中DO的浓度为0.87 mg·L-1, 沉积物-水界面处于缺氧状态, 在缺氧状态下, 磷酸单酯将会被矿化.磷酸二酯是沉积物中的不稳定态P, 半衰期为21年, 主要包括DNA磷、磷酯和磷壁酸盐(Turner et al., 2003b; Ahlgren et al., 2005; Cade-Menun, 2005).磷酸二酯和焦磷酸盐可能是河流沉积物中磷的主要来源.
5 结论(Conclusions)1) 滏阳新河上覆水中TP和SRP的平均浓度分别超过我国地表水环境质量标准GB3838—2002 Ⅴ类水标准(0.4 mg·L-1)7.5倍和6.5倍.沉积物中TP平均含量高达2160.29 mg·kg-1, 高于该区域背景值(545 mg·kg-1).表明由于沿河污染物的大量输入及多闸坝的截留作用, 导致磷在沉积物中大量累积, 增加了滏阳新河富营养化的风险.
2) 利用液相31P核磁共振技术, 在滏阳新河沉积物中共检测到6种磷化合物, 分别为:正磷酸盐(Ortho-P)、磷酸单酯(Mono-P)、磷酯(Lipids-P)、DNA磷(DNA-P)、焦磷酸盐(Pyro-P)、膦酸盐(Phon-P).其中, 磷酸单酯为有机磷的主要组成成分.
3) 滏阳新河沉积物中生物质磷包括膦酸盐(Phon-P, 0.11%~1.57%)、磷酸单酯(Mono-P, 8.96%~29.58%)、磷酯(Lipids-P, 0.28%~2.66%)、DNA磷(DNA-P, 0.75%~2.03%)和焦磷酸盐(Pyro-P, 0.22%~0.86%), 其中, 磷酸单酯是生物质磷的主要组成部分.
4) 在人工河流系统中, 闸坝附近TP、生物质磷的含量和变化率最高, 分别为6804.1 mg·kg-1、1709.58 mg·kg-1和84.97%、93.15%.生物质磷变化率高于TP.艾辛庄闸坝对滏阳新河磷传输影响较大, 人工河流形态对磷传输影响较小.
6 建议与展望(Suggestions and prospection)本研究利用31P核磁共振技术为海河流域多闸坝人工河流的水流量调度与水生态构建提供了数据支持与理论参考.① 大型闸坝对人工河流物质与能量传输过程影响较大, 应适当加强大型闸坝对水流量的调控和管理; ② 河流流量较大时, 水流的不断冲刷具有将闸坝上游污染物释放到下游的风险, 应加强闸坝下游水污染突发事件的预警与监测.
本文研究重点为海河流域典型人工河流滏阳新河, 研究结果显示, 闸坝与河流形态、岸边带对河流物质传输影响较大.我国河流复合污染比较严重, 同时河流闸坝众多, 河流形态多样, 人为干预的河流中磷的分布及传输过程有待进一步研究, 基于以上分析, 将来可以扩大河流的研究范围, 以得到人为干预河流中磷的分布及传输过程.
Ahlgren J, Tranvik L, Gogoll A, et al. 2005. Sediment depth attenuation of biogenic phosphorus compounds measured by 31P-NMR[J]. Environmental Science & Technology, 39: 867–872.
|
Ahlgren J, Reitzel K, Tranvik L, et al. 2006. Degradation of organic phosphorus compounds in anoxic Baltic Sea sediments:A 31P nuclear magnetic resonance study[J]. Limnology and Oceanography, 51(5): 2341–2348.
DOI:10.4319/lo.2006.51.5.2341
|
Aspila K I, Agemian H, Chau A S Y. 1976. A Semi-automated method for the determination of inorganic organic and total phosphate in sediments[J]. Analyst, 101: 187–197.
DOI:10.1039/an9760100187
|
白秀玲, 周云凯, 李斌, 等. 2011. 利用31P核磁共振技术优化太湖沉积物有机磷的化学提取方法[J]. 环境科学学报, 2011, 31(5): 996–1003.
|
Cade-Menun B J. 2005. Characterizing phosphorus in environmental and agricultural samples by 31P nuclear magnetic resonance spectroscopy[J]. Talanta, 66: 359–371.
DOI:10.1016/j.talanta.2004.12.024
|
Cade-Menun B J, Navaratnam J A, Walbridge M R. 2006. Characterizing dissolved and particulate phosphorus in water with 31P nuclear magnetic resonance spectroscopy[J]. Environmental Science & Technology, 40: 7874–7880.
|
Cade-Menun B J, Benitez Nelson C R, Pellechia P, et al. 2005. Refining 31P nuclear magnetic resonance spectroscopy for marine particulate samples:Storage conditions and extraction recovery[J]. Marine Chemistry, 97: 293–306.
DOI:10.1016/j.marchem.2005.05.005
|
Carpenter S R. 2008. Phosphorus control is critical to mitigating eutrophication[J]. Proceeding of the National Academy of Science of the United States of America, 105(12): 11039–11040.
|
Cardoza L A, Korir A K, Otto W H, et al. 2004. Applications of NMR spectroscopy in environmental science[J]. Progress in Nuclear Magnetic Resonance Spectroscopy, 45: 209–238.
DOI:10.1016/j.pnmrs.2004.06.002
|
Deborde J, Anschutz P, Chaillou G, et al. 2007. The dynamics of phosphorus in turbid estuarine systems:Example of the Gironde estuary(France)[J]. Limnology and Oceanography, 52(2): 862–872.
DOI:10.4319/lo.2007.52.2.0862
|
Golterman H, Paing J, Serrano L, et al. 1998. Presence of and phosphate release from polyphosphates or phytate phosphate in lake sediments[J]. Hydrobiologia, 364: 99–104.
|
Gross A, Nishri A, Angert A. 2013. Use of phosphate oxygen isotopes for identifying atmospheric sources:A case study at lake Kinneret[J]. Environmental Science & Technology, 47(6): 2721–2727.
|
Hupfer M, Gächter R, Ruegger H. 1995. Polyphosphate in lake sediments:31P NMR spectroscopy as a tool for its identification[J]. Limnology and Oceanography, 40: 610–617.
DOI:10.4319/lo.1995.40.3.0610
|
Hupfer M, Rübe B, Schmieder P. 2004. Origin and diagensis of polyphosphate in lake sediments:A 31P-NMR study[J]. Limnology and Oceanography, 49(1): 1–10.
DOI:10.4319/lo.2004.49.1.0001
|
Jensen H S, Kristensen P, Jeppesen E, et al. 1992. Iron:phosphorus ratio in surface sediment as an indicator of phosphate release from aerobic sediments in shallow lakes[J]. Hydrobiologia, 235/236: 731–743.
DOI:10.1007/BF00026261
|
鲁婷, 陈能汪, 陈朱虹, 等. 2013. 九龙江河流-库区系统沉积物磷特征及其生态学意义[J]. 环境科学学报, 2013, 31(5): 996–1003.
|
李惠敏, 霍家明, 于卉. 2000. 海河流域水污染现状与水资源质量状况综合评价[J]. 水资源保护, 2000(4): 12–14.
|
Livingstone D, Khoja T M, Whitton B A. 1982. Laboratory studies on phosphorus sources for an upper Teesdale Calothrix[J]. British Phycological Journal, 17: 235.
|
Mcdowell R W, Condron L M, Stewart I, et al. 2005. Chemical nature and diversity of phosphorus in new zealand pasture soils using 31P nuclear magnetic resonance spectroscopy and sequential fractionation[J]. Nutrient Cycling in Agroecosystems, 72(3): 241–254.
DOI:10.1007/s10705-005-2921-8
|
Matzinger A, Schmid M, Veljanoska S, et al. 2007. Eutrophication of ancient Lake Ohrid:Global warming amplifies detrimental effects of increased nutrient inputs[J]. Limnology and Oceanography, 52(1): 338–353.
DOI:10.4319/lo.2007.52.1.0338
|
Maavara T, Parsons C T, Ridenour C, et al. 2015. Global phosphorus retention by river damming[J]. Proceedings of the National Academy of Sciences, 112(51): 15603–15608.
|
Pernet Coudrier B, Qi W X, Liu H J, et al. 2012. Sources and pathways of nutrients in the semi-arid region of Beijing -Tianjin, China[J]. Environmental Science & Technology, 46: 5294–5301.
|
Qu H J, Kroeze C. 2010. Past and future trends in nutrients export by rivers to the coastal waters of China[J]. Science of the total Environment, 408: 2075–2086.
DOI:10.1016/j.scitotenv.2009.12.015
|
Reitzel K, Ahlgren J, Gogoll A, et al. 2006. Characterization of phosphorus in sequential extracts from lake sediments using 31P nuclear magnetic resonance spectroscopy[J]. Canadian Journal of Fisheries & Aquatic Sciences, 63: 1686–1699.
|
Reitzel K, Ahlgren J, Gogoll A, et al. 2006. Effects of aluminum treatment on phosphorus, carbon, and nitrogen distribution in lake sediment:a 31P NMR study[J]. Water Research, 40: 647–654.
DOI:10.1016/j.watres.2005.12.014
|
Rusu V, Postolachi L, Povar I, et al. 2012. Dynamics of phosphorus forms in the bottom sediments and their interstitial water for the Prut River(Moldova)[J]. Environmental Science and Pollution Research, 19(8): 3126–3131.
DOI:10.1007/s11356-012-0920-2
|
Simpson A J, Simpson M J, Soong R. 2012. Nuclear magnetic resonance spectroscopy and its key role in environmental research[J]. Environmental Science & Technology, 46(21): 11488–11496.
|
Shinohara R, Imai A, Kawasaki N, et al. 2012. Biogenic phosphorus compounds in sediment and suspended particles in a shallow eutrophic lake:a 31P uuclear magnetic resonance(31P-NMR)study[J]. Environmental Science & Technology.
DOI:10.1021
|
Sulugambari F, Seitaj D, Meysman F J R, et al. 2016. Cable bacteria control iron–phosphorus dynamics in sediments of a coastal hypoxic basin[J]. Environmental Science & Technology, 50(3): 1227–1233.
|
Turner B L, Papházy M J, Haygarth P M, et al. 2002. Inositol phosphates in the environment[J]. Philosophical Transactions of the Royal Society of London, 357(1420): 449–469.
DOI:10.1098/rstb.2001.0837
|
Turner B L, Mahieu N, Condron L M. 2003a. The phosphorus composition of temperate pasture soils determined by NaOH-EDTA extraction and solution 31P-NMR spectroscopy[J]. Organic Geochemistry, 34: 1199–1210.
DOI:10.1016/S0146-6380(03)00061-5
|
Turner B L, Mahieu N, Condron L M. 2003b. Phosphorus-31 nuclear magnetic resonance spectral assignments of phosphorus compounds in soil NaOH-EDTA extracts[J]. Soil Science Society of America Journal, 67: 497–510.
DOI:10.2136/sssaj2003.4970
|
Turner B L, Richardson A E, Mullaney E J, et al. 2006. Inositol Phosphates:Linking Agriculture and the Environment[M]. Oxfordshire: CABI Publishing.
|
王超, 单保庆. 2012. 子牙河水系水和沉积物好氧氨氧化微生物分布特征[J]. 环境科学学报, 2012, 32(12): 2943–2950.
|
张文强, 李洁, 金鑫, 等. 2016. 基于31P-NMR与SMT方法的海河流域典型河流沉积物中磷形态特征研究[J]. 环境科学学报, 2016, 36(6): 1891–1900.
|
张文强, 单保庆. 2013. 基于液相31P核磁共振(NMR)技术的巢湖沉积物中有机磷形态研究[J]. 环境科学学报, 2013, 33(7): 1967–1973.
|
赵钰, 单保庆, 张文强, 等. 2014. 子牙河水系河流氮素组成及空间分布特征[J]. 环境科学学报, 2014, 35(1): 143–149.
|
Zhang Q, Hirsch R M, Ball W P. 2016. Long-term changes in sediment and nutrient delivery from Conowingo Dam to Chesapeake Bay:Effects of reservoir sedimentation[J]. Environmental Science & Technology, 50(4): 1877–1886.
|
 2017, Vol. 37
2017, Vol. 37