铅是大气、水体及土壤环境中最常见的重金属污染物之一(王春梅等, 2003; 李继强等, 2001), 它会通过饮用水或食物链等途径侵入人体并且蓄积, 进而对人体生命健康造成威胁(王林等, 2000; 杨宵霖等, 1998; 郑惠等, 2008; 董兆敏等, 2011).因此, 治理和修复环境中的铅污染备受关注(Wang et al., 2015; Kumar et al., 2014).生物炭是生物质在缺氧条件下加热裂解产生的富碳固体产物(Zeng et al., 2011), 由于具有制备过程操作简单、成本低廉及吸附性能良好等优点, 已成为一种实用性较好且绿色环保的吸附材料.
目前, 利用生物炭去除水体中重金属(Kalinke et al., 2016; Park et al., 2016)、农药(Taha et al., 2014)、抗生素(Pezoti et al., 2016)等的报道较多.其中, 有部分研究关注利用不同原料制备的生物炭及其对铅的吸附去除效果, 如利用胡麻秸秆生物炭(Park et al., 2016)、甘蔗渣和橙皮生物炭(Ahmed et al., 2016)、市政污泥生物炭(Zhang et al., 2013)等对铅进行吸附, 最大吸附量约为27.30~172.00 mg·g-1.花椰菜(Brassica oleracea L.)是十字花科芸薹属甘蓝种(Brassica species)中的一个变种(朱惠霞等, 2011; 李文萍等, 2014).作为重要的经济作物, 花椰菜在世界贸易市场占据重要地位.根据联合国粮食及农业组织(FAO)的统计, 2011年我国花椰菜总产量已达到约9025278 t, 占全球总产量的43.21%(李文萍等, 2014).近年来, 花椰菜的种植面积在全世界范围内都在持续不断的增加, 由此产生的花椰菜根和叶废弃物数量巨大.然而, 对于此类全球性的废弃物资源目前还没有合理的应用和处理处置方式.传统的处理方式仅仅是堆置和焚烧, 这种处理方式造成了资源浪费和环境污染.目前, 有关使用花椰菜根和叶制备成生物炭, 并作为吸附材料去除废水中Pb(Ⅱ)的研究还鲜有报道.
本文以农业废弃物花椰菜的根和叶为原料, 采用限氧裂解法制备花椰菜根基(BCR)和叶基生物炭(BCL), 并利用扫描电镜(SEM)、能谱分析(EDS)、红外光谱(FTIR)及比表面测定(BET)等手段讨论2种生物炭的结构和性质.同时, 研究BCR和BCL对水溶液中Pb(Ⅱ)的吸附性能及其影响因素(吸附时间、吸附温度、溶液初始pH值、初始浓度及不同共存离子), 并进行动力学模型、等温吸附模型拟合以探讨BCR和BCL的吸附机理, 以期为农业废弃物资源的高效利用、廉价吸附材料的低成本制备及重金属的污染防治提供理论依据.
2 材料与方法(Materials and methods) 2.1 主要试剂及仪器试剂:硝酸铅(分析纯)购自天津市凯信化学工业有限公司; 硝酸钠、氯化钙均为分析纯, 购自天津市光复科技发展有限公司; 氢氧化钠(分析纯)购自成都市科龙化工试剂厂; 硝酸(优级纯)购自白银良友化学试剂有限公司; 试验用水为超纯水.
仪器:Thermo ICE3000火焰原子吸收光谱仪(美国赛默-飞世尔有限公司); NEXUS670傅里叶变换红外光谱仪(美国Nicolet公司); JSM-5600LV低真空扫描电子显微镜(日本电子光学公司); IE250X射线能量色散光谱仪(英国牛津仪器公司); Tristar Ⅱ 3020物理吸附仪(美国麦克仪器公司); Malvern Zetasizer Nano zen3600激光粒度仪(英国马尔文仪器有限公司); pH2700 pH计(美国Oakton公司); KS-5D-12马弗炉(上海鸿都电子科技有限公司).
2.2 生物炭的制备花椰菜根和叶采自甘肃省定西市农耕地.将菜根和菜叶用自来水清洗干净后再用超纯水润洗3次, 置于干净通风处自然风干, 用粉碎机粉碎后过20目筛(0.85 mm)备用.采用500 ℃限氧裂解法(陈再明等, 2013)制备花椰菜根基和叶基生物炭, 将已制备的2种粉末分别装入坩埚中, 压实后置于马弗炉中, 升温速率为20 ℃·min-1, 热解温度达到500 ℃后保持6 h, 待冷却至室温后取出.制得的生物炭需要用超纯水反复冲洗至pH恒定, 80 ℃下烘干, 过100目筛(0.15 mm)后装入密封袋中, 置于干燥器中备用.制备好的花椰菜根基和叶基生物炭分别标记为BCR、BCL.
2.3 生物炭的表征采用BET法分析2种生物炭(BCR和BCL)的表面积和孔结构; 利用扫描电镜观察2种生物炭吸附前后的表面形貌及变化; 采用能谱分析测定BCR和BCL的元素含量及吸附Pb(Ⅱ)后的能谱分层图像; 利用红外光谱分析2种生物炭吸附前后的表面官能团及变化; 利用马尔文Zetasizer测定2种生物炭的Zeta电位; 利用pH计测定其pH; 生物炭的产率为生物炭制备前后的质量比.
2.4 吸附实验 2.4.1 动力学吸附配制初始浓度分别为300和350 mg·L-1的Pb(NO3)2溶液, 以0.01 mol·L-1的NaNO3为背景溶液, 用0.1 mol·L-1的NaOH和HNO3调节溶液的pH为5.00.基于预实验, 生物炭的投加量为0.8 g·L-1, 在25 ℃、200 r·min-1下恒温振荡, BCR吸附实验分别在5 min、10 min、20 min、40 min、1 h、2 h、3 h、4 h、5 h、6 h、8 h和10 h时取样, BCL吸附实验分别在5 min、20 min、30 min、1 h、2 h、4 h、6 h、8 h、10 h、12 h和15 h时取样, 4000 r·min-1离心5 min, 过滤, 用火焰原子吸收光谱仪测定溶液中Pb(Ⅱ)的浓度, 每个样品均做平行样.
2.4.2 等温吸附线配制浓度分别为200、250、300、350、400、450、500、550和600 mg·L-1的Pb(NO3)2溶液, 以0.01 mol·L-1的NaNO3为背景溶液, 调节溶液的pH为5.00.生物炭的投加量为0.8 g·L-1, 在15、25和35 ℃下恒温振荡24 h, 离心过滤, 测定溶液中Pb(Ⅱ)的浓度, 每个样品均做平行样.
2.4.3 不同共存离子的影响配制浓度为200~600 mg·L-1的Pb(NO3)2溶液, 以0.01 mol·L-1的CaCl2为背景溶液, 调节溶液的pH为5.00.生物炭的投加量为0.8 g·L-1, 在25 ℃下恒温振荡24 h, 离心过滤, 测定溶液中Pb(Ⅱ)的浓度, 每个样品均做平行样.
2.4.4 溶液pH的影响配制浓度为300 mg·L-1的Pb(NO3)2溶液, 以0.01 mol·L-1的NaNO3为背景溶液, 调节溶液的初始pH分别为1.01、2.04、3.00、4.07、5.01、5.19、5.45、6.01、7.04和8.02.生物炭的投加量为0.8 g·L-1, 在25 ℃下恒温振荡24 h, 离心过滤, 测定溶液中Pb(Ⅱ)的浓度及振荡后溶液的pH值, 每个样品均做平行样.
2.5 数据处理 2.5.1 去除率和吸附量吸附平衡后, 2种生物炭对Pb(Ⅱ)的吸附效果用去除率(R)和吸附量(Qe)来表示, 计算公式如下:
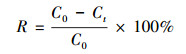
|
(1) |
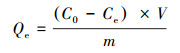
|
(2) |
式中, C0、Ct和Ce分别是溶液中重金属离子的初始浓度、t时刻的浓度和平衡时的浓度(mg·L-1); V为加入的溶液体积(mL); m为生物炭的质量(g); R表示t时刻的去除率; Qe为生物炭对重金属的平衡吸附量(mg·g-1).
2.5.2 模型模拟用于吸附动力学研究的准一级动力学模型、准二级动力学模型和颗粒内扩散模型分别如式(3)~(5) 所示, Langmuir吸附等温模型和Freundlich吸附等温模型如式(6)~(7) 所示.
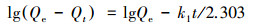
|
(3) |
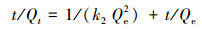
|
(4) |
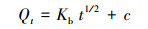
|
(5) |
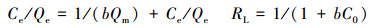
|
(6) |
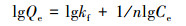
|
(7) |
式中, Qt、Qm分别为t时刻生物炭对重金属的吸附量和最大吸附量(mg·g-1); k1、k2和kb分别为准一级(min-1)、准二级(mg·g-1·min-1)和颗粒内扩散模型(mg·g-1·min-0.5)的速率常数; c为截距; b(L·mg-1)、n和kf(mg1-n·g-1·L-n)分别为Langmuir方程和Freundlich方程的吸附常数, 其中, b表示生物炭表面的吸附位点对重金属离子的亲和力大小, n表示吸附强度的大小, kf表示吸附容量.
2.5.3 吸附热力学利用公式(8)~(10) 计算Gibbs自由能(ΔG, kJ·mol-1)、焓变(ΔH, kJ·mol-1)和熵变(ΔS, kJ·mol-1·K-1).
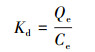
|
(8) |
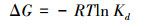
|
(9) |
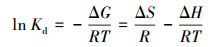
|
(10) |
式中, Kd表示吸附过程的表观平衡分配常数, R是理想气体常数(8.314 J·mol-1·K-1), T表示绝对温度(K).
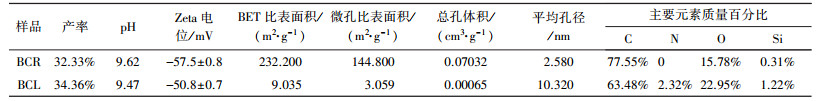
3 结果与讨论(Results and discussion) 3.1 生物炭的基本理化性质及表征 3.1.1 生物炭的基本理化性质花椰菜根基和叶基生物炭的基本理化性质见表 1.从表中可知, 2种生物炭pH均呈碱性, 表面均带负电, 且BCR的Zeta电位大于BCL, 二者的比表面积、孔隙结构、孔径、表面官能团等存在较大的差别.其中, BCR的比表面积、微孔比表面积和总孔体积均远大于BCL的相应值, 可能是由于花椰菜根基内部结构相对比较疏松, 根体内部含有更多的易挥发成分, 在裂解过程中形成更多的孔道.通常生物炭的比表面积越大, 则在吸附反应中可提供的活性位点越多, 从而对重金属具备更强的物理吸附作用(石夏颖, 2014).BCL的N、O含量较高, 说明其表面可能含有更多的官能团, BCL可能主要通过官能团的络合作用去除溶液中的Pb(Ⅱ).
| 表 1 生物炭基本理化性质 Table 1 The basic physico-chemical property of biochars |
BCL的平均孔径明显大于BCR的平均孔径, 同时BCR和BCL的微孔比表面积分别占比表面积的62.37%和33.85%, 说明花椰菜叶基生物炭表面含有较少的中孔和微孔孔隙, 含有较多的宏孔孔隙; 而花椰菜根基生物炭表面含有大量的中孔和微孔孔隙, 从而降低了其孔隙的平均孔径.2种生物炭的N2吸附-脱附等温实验(图 1)也证明了这一结论, 说明BCR的孔隙结构较BCL好.
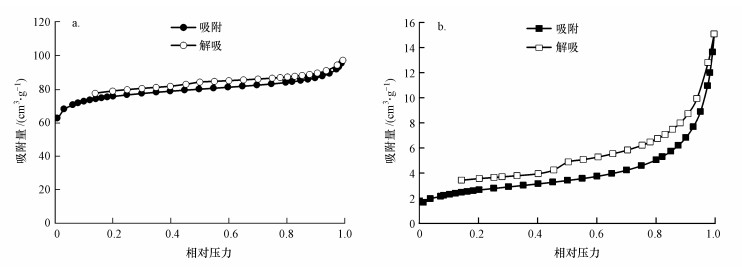 |
| 图 1 生物炭的氮气吸附-脱附等温线(a.根基, b.叶基) Fig. 1 Nitrogen adsorption-desorption isotherms of the biochars |
根据国际纯粹与应用化学联合会(IUPAC)分类, BCR的N2吸附-脱附等温线符合类型Ⅰ和类型Ⅳ等温线, 表明花椰菜根基生物炭孔隙结构主要是微孔和介孔, 并存在较多的孔道(Jing et al., 2014).BCL的N2吸附-脱附等温线符合类型Ⅰ和类型Ⅱ等温线, 表明花椰菜叶基生物炭主要是少量微孔和介孔的孔隙结构.
3.1.2 扫描电镜和能谱分析用扫描电镜分析了BCR和BCL本身及吸附Pb(Ⅱ)后的表面形貌变化.从图 2a中可以看出, 花椰菜根基生物炭(BCR)具有长条形的孔道和不定形的片层结构, 孔壁表面孔隙致密, 孔径较小, 并且多个层状的表面增加了BCR的比表面积和孔隙孔容, 这与表 1中的结果相符.在吸附实验中, BCR将会提供更多的吸附位点, 从而增加其物理吸附量(石夏颖, 2014).从图 2c中可以看到, 花椰菜叶基生物炭(BCL)具有类似于叶子本身的茎状结构, 加热后叶子内部易挥发成分逸出后留下类似于气孔的孔道结构, 孔隙排布比较规律, 可能会暴露更多的活性位点, 这样有利于进行化学吸附(李瑞月等, 2015).吸附Pb(Ⅱ)后, BCR和BCL表面的孔隙结构均消失, 表面出现一些小颗粒团(图 2b, 2d), 这与程启明等(2014)研究生物炭吸附前后的形貌的结果一致.
 |
| 图 2 生物炭吸附Pb(Ⅱ)前后的SEM图(a.根基-吸附前, b.根基-吸附后, c.叶基-吸附前, d.叶基-吸附后, ×500倍) Fig. 2 SEM images of biochars before and after adsorption Pb(Ⅱ) (×500) |
本文用能谱图像展示了生物炭吸附Pb(Ⅱ)前后的特征, 结果如图 3所示.图 3a和3c分别是BCR和BCL吸附前的能谱图, 其C、O、Pb的质量百分比分别为77.55%、15.78%、0和63.48%、22.95%、0.图 3b和3d分别是BCR和BCL吸附Pb(Ⅱ)后的能谱图, 其C、O、Pb元素的质量百分比分别为69.10%、15.17%、14.46%和54.13%、19.17%、10.98%.吸附前后的能谱图表明, C元素含量的减少可能归因于Pb元素的吸附, O元素含量的减少可能是由于生物炭含有金属氧化物或者碳酸盐类存在, 其与Pb(Ⅱ)发生了反应而造成其含量降低, Pb元素由无到有.图 3e和3f分别是BCR和BCL吸附Pb(Ⅱ)后的能谱分层图像, 可以进一步证实Pb(Ⅱ)被生物炭吸附.
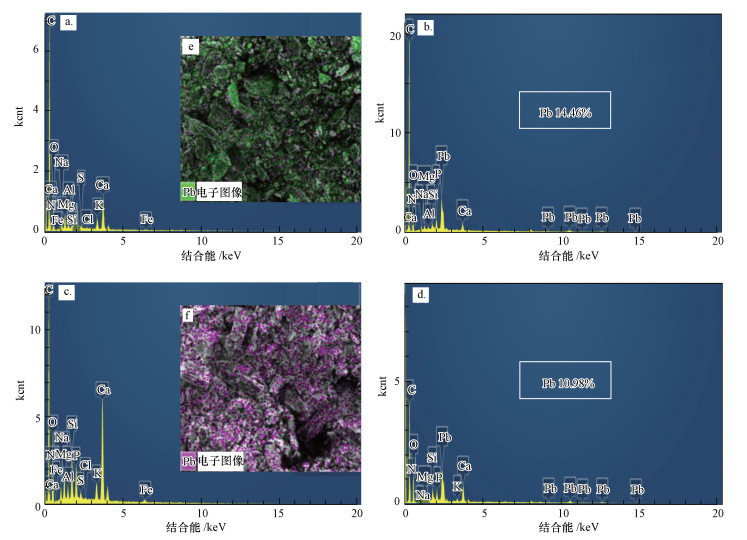 |
| 图 3 生物炭吸附Pb(Ⅱ)前后EDS图(a.根基-吸附前, b.根基-吸附后, c.叶基-吸附前, d.叶基-吸附后, e, f.能谱分层图) Fig. 3 EDS images of biochars before and after Pb(Ⅱ) adsorption |
图 4为BCR和BCL吸附Pb(Ⅱ)前后的红外光谱图.可以看出, BCR和BCL分别在3400.5和3418.9 cm-1处的峰被认为是O—H的伸缩振动峰(Guo et al., 2008; Chandraiah, 2016), 吸附Pb(Ⅱ)后, 吸收峰分别移到3415.5和3420.0 cm-1处.BCR和BCL在1572.6和1578.0 cm-1, 以及1044.3和1034.0 cm-1处分别对应的是芳环的C=C(Kyzas et al., 2015)和酚类或氢氧基团中C—O的伸缩振动峰(Ding et al., 2016).BCR和BCL分别在1420.1和1426.1 cm-1处的峰被认为是羧基的C=O的伸缩振动峰, 吸附后分别移到1384.2和1384.7 cm-1处, 产生了一个碳酸盐的伸缩振动峰, 可能是因为形成了碳酸铅之类的沉淀(Trakal et al., 2014; Xu et al., 2013).此外, BCR和BCL在吸附Pb(Ⅱ)后, 分别在681.3和679.0 cm-1处出现2个新的波峰, 被认为是碳酸盐的伸缩振动峰(Xu et al., 2013).
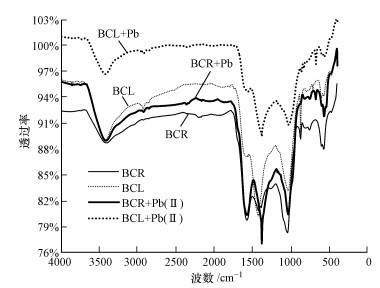 |
| 图 4 生物炭吸附Pb(Ⅱ)前后红外光谱图 Fig. 4 FTIR spectra of biochars before and after Pb(Ⅱ) adsorption |
BCL在2924.3和2855.3 cm-1处有2个吸收峰, 分别对应的是不对称脂肪性—CH2和对称C—H伸缩振动峰(李瑞月等, 2015; Venkateswarlu et al., 2013), 在1795.3和1739.3 cm-1处存在2个吸收峰, 可能是由于不饱和烃类的吸收峰和羧基或内酯基中C=O的伸缩振动引起的(石夏颖, 2014; Kyzas et al., 2015), 吸附后这2个峰均消失.BCL在1559.5和1541.4 cm-1处存在C—H和N—H伸缩振动峰(Mohan et al., 2015), 吸附后此峰消失.可以看出, 花椰菜根基和叶基生物炭本身含有丰富的官能团, 为其吸附Pb(Ⅱ)提供更多潜在的吸附位点.
对比花椰菜根基和叶基生物炭吸附Pb(Ⅱ)前后的FTIR红外光谱图可以看出, 2种生物炭在吸附Pb(Ⅱ)后官能团的特征峰值有明显的变化.其中, O—H特征峰值逐渐减弱, 说明此处官能团在吸附Pb(Ⅱ)时能够提供氢键作用(Chen et al., 2011).随着吸附的持续进行, O—H、C—O及羧基的C=O特征峰处在吸附Pb(Ⅱ)时能够进行离子交换作用(陈再明等, 2013), 同时叶基生物炭还含有N—H伸缩振动峰, 其也可与Pb(Ⅱ)之间发生离子交换.此外, 2种生物炭分别在不同的特征峰(即羧基的C=O、内酯基中的C=O及芳香环和杂环化合物特征峰)值处产生了新的碳酸盐的伸缩振动峰, 说明BCR和BCL具有高度芳香化和杂环化结构, 在吸附进程中, Pb(Ⅱ)可以与其丰富的含氧官能团及芳香环化合物发生阳离子-π电子作用而形成稳定的结构(陈再明等, 2013; Uchimiya et al., 2010), 并且该作用是2种生物炭吸附Pb(Ⅱ)的主要机制(Swiatkowski et al., 2004; Wang et al., 2015).
3.2 吸附动力学图 5为2种生物炭对Pb(Ⅱ)吸附的动力学曲线.由图 5可知, 在Pb(Ⅱ)初始浓度分别为300和350 mg·L-1的条件下, 吸附5 min时, BCR对Pb(Ⅱ)的去除率分别为59.29%、43.73%, BCL对Pb(Ⅱ)的去除率分别为40.25%、34.35%;吸附1 h时, BCL对Pb(Ⅱ)的去除率分别为59.56%、52.90%.说明花椰菜根基生物炭的吸附速率比叶基生物炭快.BCR对300和350 mg·L-1 Pb(Ⅱ)的吸附分别在3和6 h左右基本达到平衡; 而BCL的吸附过程相对较慢, 对Pb(Ⅱ)的吸附分别在6和10 h左右基本达到平衡.说明BCR比BCL达到吸附平衡的时间短, 同时说明平衡时间受到初始浓度的影响, 初始浓度越大, 达到吸附平衡所需时间越长, 这可能与2种生物炭的吸附进程有关.吸附进程分为2个阶段:首先是快速吸附阶段, 这可能主要是由物理吸附控制(Ahmad et al., 2014; Mohan et al., 2014), 溶液中的Pb(Ⅱ)快速占据表面的吸附位点; 然后进入缓慢吸附阶段, 这可能主要归因于化学吸附(Ahmad et al., 2014; Mohan et al., 2014).对于不同的初始浓度, 溶液中Pb(Ⅱ)的量不同, 其扩散速率也不同.
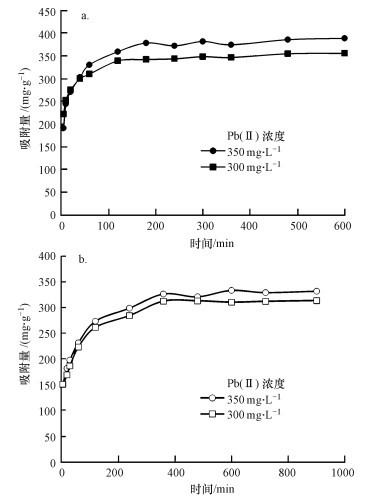 |
| 图 5 吸附时间对2种生物炭吸附Pb(Ⅱ)效果的影响(a.根基, b.叶基) Fig. 5 Effects of contact time on the adsorption of Pb(Ⅱ) by biochars |
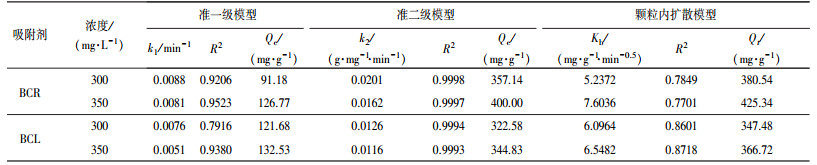
为了进一步研究2种生物炭的动力学吸附特性, 分别采用准一级模型、准二级模型及颗粒内扩散模型对吸附后的数据进行线性拟合.由表 2可知, 准一级动力学和颗粒内扩散模型对BCR和BCL吸附Pb(Ⅱ)的拟合结果较差, 其可决系数R2较低, 说明这2种模型不适用于分析花椰菜根基和叶基生物炭对Pb(Ⅱ)的吸附特性.而准二级动力学模型有很好的拟合效果, 可决系数R2均大于0.999, 能够较好地反映2种生物炭对Pb(Ⅱ)的吸附过程, 表明2种生物炭对Pb(Ⅱ)的主导吸附是化学吸附, 生物炭与Pb(Ⅱ)之间可能存在电子对共用、离子交换和表面络合等相互作用(Yang et al., 2014; 安增莉等, 2011).本文研究结果与丁文川等(2012)和张越等(2015)研究结果相似.k2是准二级动力学模型拟合后得到的反应速率常数, 可以反映吸附进程的快慢, 即k2值越大, 所需平衡时间越短.由表 2可知, BCR的k2值大于BCL的k2值, 且初始浓度为300 mg·L-1时的k2值大于350 mg·L-1时的k2值, 进一步证明了上述结论, 与实验结果一致.
| 表 2 两种生物炭对Pb(Ⅱ)的吸附动力学拟合参数 Table 2 Fitting parameters of kinetic models for Pb(Ⅱ) adsorption on biochars |
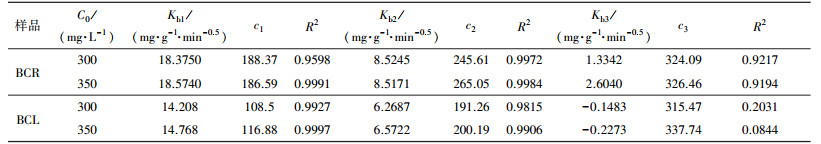
基于表 2数据, 用颗粒内扩散模型拟合后的可决系数较低, 所以在整体上呈非线性, 因而利用颗粒内扩散模型对实验数据进行分段拟合, 结果如表 3所示.从表中数据可以看出, 颗粒内扩散模型能较好地进行分段拟合, 除了BCL的第3阶段, 其它可决系数R2都大于0.91, 说明吸附过程伴随着多线性, 表明在吸附过程中发生多个步骤.一般地, 吸附过程可以分为3个阶段:第1阶段为膜扩散, 即大孔扩散; 第2和第3阶段为粒子内扩散, 即微孔扩散(Han et al., 2010).BCR和BCL对Pb(Ⅱ)的吸附过程经颗粒内扩散模型拟合分为3个阶段, 首先拟合线段不经过原点; 3个阶段的速率常数Kb随着时间的延长逐渐变小, 第1阶段的扩散速率很快, 当生物炭表面吸附饱和后, 进行颗粒内部孔隙的扩散, 随着扩散的持续进行, 扩散速率逐渐变慢, 直至达到吸附平衡; c值与液膜厚度有关, 随着吸附过程的进行, c值逐渐增大.BCL的第3阶段拟合效果较差, 这是由BCL本身的孔隙结构造成的, 其结果与表 1、图 1表征结果相符.总体来说, 孔扩散不是速率控制的唯一步骤, 可能会有表面吸附和颗粒内扩散, 这与肖薇(2015)和Liu等(2016)的研究结果相似.
| 表 3 颗粒内扩散模型分段拟合结果 Table 3 Intra-particle diffusion parameters |
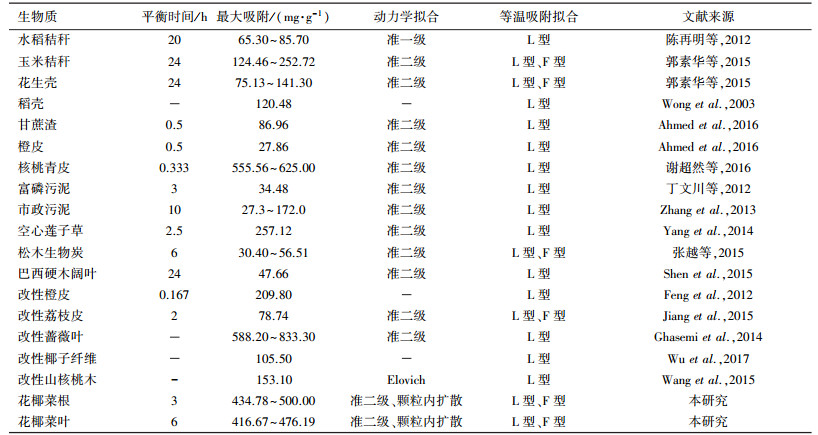
通过与其他研究者的生物炭吸附材料对Pb(Ⅱ)的吸附平衡时间对比发现, 花椰菜根基和叶基生物炭吸附Pb(Ⅱ)的平衡时间较短(表 4).同时, 表 4中列举了不同生物炭对Pb(Ⅱ)的吸附性能, 经过对比可以看出, 花椰菜根基和叶基生物炭对溶液中Pb(Ⅱ)的吸附量远高于由秸秆、污泥、硬木等制备的生物炭, 说明BCR和BCL具有较大的吸附量和优质的吸附效果, 表明这2种生物炭对污水中的污染物有极佳的去除效果, 是极具潜力的吸附材料.
| 表 4 不同生物炭对Pb(Ⅱ)吸附能力的比较 Table 4 Comparison of Pb(Ⅱ) adsorption capacity in different biochars |
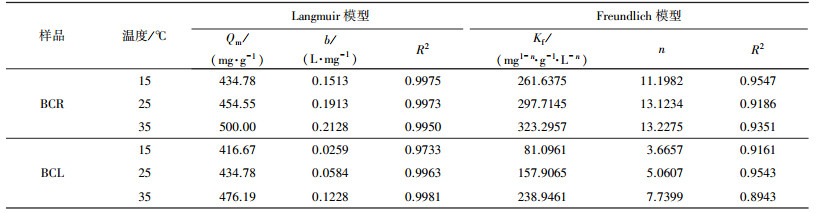
本研究采用Langmuir等温吸附模型和Freundlich等温吸附模型对实验数据进行拟合, 结果见图 6和表 5.从表 5中可以看出, Langmuir模型和Freundlich模型的拟合结果均较好, 说明BCR和BCL对Pb(Ⅱ)的整个吸附过程既有物理吸附又有化学吸附.李瑞月等(2015)和Yang等(2014)的研究与本文结果一致.表中BCR和BCL在15、25、35 ℃的最大吸附量分别是434.78、454.55、500.00 mg·g-1和416.67、434.78、476.19 mg·g-1, 可以看出随着温度的升高, 吸附量逐渐增大, 说明高温有利于BCR和BCL对Pb(Ⅱ)的吸附, 即此吸附是自发进行的, 相关研究也得出相同的结论(Kamari et al., 2014).同时可以看出, BCR的最大吸附量大于BCL, 说明BCR的吸附性能优于BCL.用分离因子RL可以进一步说明2种生物炭的吸附性能(Kamari et al., 2014; 魏建文等, 2014), 其中包括不利吸附(RL > 1)、优惠吸附(0 < RL < 1)、线性吸附(RL=1) 和不可逆吸附(RL=0).经计算, BCR和BCL的RL值均为0~1, 表明2种生物炭对Pb(Ⅱ)的吸附均为优惠吸附.
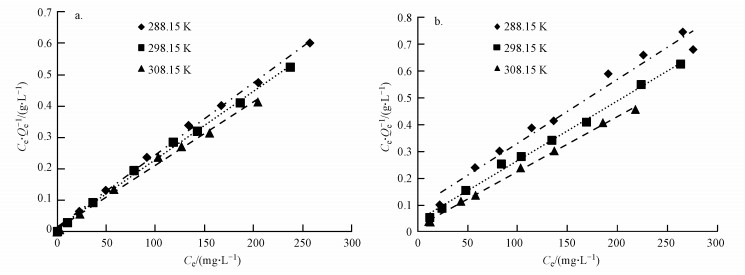 |
| 图 6 两种生物炭对Pb(Ⅱ)的吸附等温拟合(a.根基, b.叶基) Fig. 6 Isotherm of Pb(Ⅱ) adsorption on biochars |
| 表 5 两种生物炭对Pb(Ⅱ)的等温吸附模型拟合参数 Table 5 Fitting parameters of isotherm models for Pb(Ⅱ) adsorption on biochars |
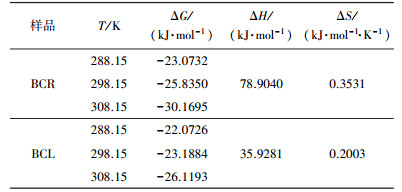
根据公式(8)~(10) 计算热力学参数, 以lnKd对1/T作图, 其拟合的直线截距和斜率分别为ΔS和ΔH.当ΔG值为-80~-20 kJ·mol-1时, 为物理吸附和化学吸附(Lin et al., 2011).从表 6可知, ΔG值为负值, 表明2种生物炭对Pb(Ⅱ)的吸附过程是自发的, 由物理吸附和化学吸附共同控制, 且随着温度的升高, ΔG的绝对值逐渐增大, 说明升高温度有利于该吸附反应的发生, 这与等温吸附模型的结果一致.2种生物炭ΔH值为正值, 说明2个过程均为吸热过程.吸附过程ΔS值为正值, 说明吸附向着混乱度增加的方向进行.通过对BCR与BCL吸附热力学参数的对比可知, 随温度的升高, BCR对Pb(Ⅱ)的吸附反应比BCL更强烈, 吸附过程自发性更强, 从而使得在相同实验条件下BCR的吸附量大于BCL的吸附量.
| 表 6 吸附热力学参数 Table 6 Thermodynamics adsorption parameters |
在不同共存离子(Na+、Ca2+)条件下, 2种生物炭对水溶液中Pb(Ⅱ)的吸附效果如图 7所示.在相同共存离子条件下, 随着溶液初始浓度的增大, 花椰菜根基和叶基生物炭对Pb(Ⅱ)的吸附量逐渐增加, 直至达到吸附平衡.在不同共存离子同种生物炭条件下, 共存离子为Ca2+比Na+对吸附过程的影响明显, 对水溶液中Pb(Ⅱ)的吸附量明显较低, 说明离子所带电荷越高, 对生物炭吸附Pb(Ⅱ)影响越大, 表明在吸附进程中阳离子会与Pb(Ⅱ)产生竞争吸附; 共存金属离子所带电荷越高, 可能越不利于生物炭吸附Pb(Ⅱ), 这与肖薇(2015)的研究结果相似.袁广翔等(2011)研究了Ca2+与Na+对浆料Zeta电位的影响, 发现与Na+相比, Ca2+更容易使吸附剂吸附过程的Zeta电位值过高甚至达到正值, 从而影响吸附剂的性能, 进一步阐明了共存离子对2种生物炭吸附效果的影响.
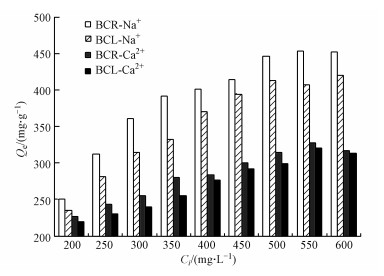 |
| 图 7 不同离子对2种生物炭吸附Pb(Ⅱ)的影响 Fig. 7 Effects of different ionics on adsorption of Pb(Ⅱ) by biochars |
不同初始pH条件下2种生物炭对水溶液中Pb(Ⅱ)的去除率及吸附前后溶液pH的变化如图 8所示.在初始pH为2.04时, BCR和BCL对Pb(Ⅱ)的去除率分别为21.35%和17.30%, 而在pH为3.00时, 去除率分别达到80.24%和67.88%, 即当初始pH为2~3时去除率急剧增大.随后BCR在pH值为3.20左右时去除率达到最大值, 在pH值为3.20~5.01时去除率呈缓慢下降趋势, 这与安增莉等(2011)的研究结果相似; 在pH值为5.01~5.45左右时去除率逐渐缓慢增加.而BCL在pH值为3.00~5.45左右时, 去除率持续缓慢增加.在pH值为5.45~6.01时, BCR和BCL对Pb(Ⅱ)的去除率急剧增加达到100%;在pH值为6.01~8.02时, 去除率继续保持在100%的水平.
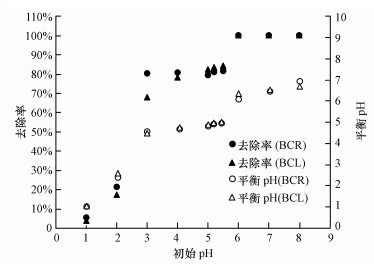 |
| 图 8 pH对2种生物炭吸附Pb(Ⅱ)的影响 Fig. 8 Effect of pH on adsorption of Pb(Ⅱ) by biochars |
增加溶液的pH值能够加快生物炭表面的去质子化进程, 并且创造更多的负电点位来提高Pb2+的去除率(Mohan et al., 2014).在pH值较低时, 即初始pH为1.01~2.04的强酸环境下, 溶液中H+、Pb2+和[Pb(H2O)6]2+之间对吸附位点存在较强烈的竞争, 不利于Pb2+吸附在生物炭表面, 这与丁文川等(2012)和张越等(2015)的研究结果相似.随着溶液pH值的增大, 溶液中Pb2+的存在形态发生变化, 水合结构中的H2O将逐步被OH-取代, 由Pb2+和[Pb(H2O)6]2+逐步转化成氢氧络离子([Pb(OH)6]4-)形态(Xiao et al., 2009), 去除率不断增大, 即增加溶液的pH可以降低Pb2+与质子对吸附位点的竞争, 导致去除效率的提高(Yang et al., 2014; Kołodyńska et al., 2012).在pH值较高时, 即在pH大于5.45时, Pb2+主要结合生成Pb(OH)2等沉淀, 此时溶液中Pb2+自由离子逐渐减少, 实际吸附容量逐渐下降, 在pH大于6.01时去除率达到100%.基于上述分析, BCR的最佳吸附pH值为3.20左右, BCL为5.45左右, 与安增莉等(2011)的研究结果相似.室温条件下Pb(OH)2的溶度积为1.2×10-15(郭素华等, 2015), 在本实验条件下可计算出开始生成Pb(OH)2沉淀的理论pH为5.49, 与实验所得结果5.45相近.在初始pH为5.01~8.02时, 吸附后溶液的平衡pH值均低于初始pH值, 这是由于生物炭本身的酸度使得溶液具有较强的缓冲能力, Mohan等(2014)和Shen等(2015)也得出了相似的结果.实验结果表明, 2种生物炭的初始pH为3.00~8.02时对Pb(Ⅱ)具有很好的去除效果, 这2种吸附进程对pH的适应范围较宽, 有利于花椰菜根基和叶基生物炭在实际环境下的应用.
4 结论(Conclusions)1) 2种生物炭都具有丰富的表面官能团, 花椰菜根基生物炭的孔隙结构优于叶基生物炭.根基生物炭比表面积较大, 表面含有大量的中孔和微孔孔隙; 叶基生物炭表面含有较多的宏孔孔隙.花椰菜根基生物炭在吸附反应中提供了较多的吸附位点, 从而增加了其对Pb(Ⅱ)的物理吸附量.
2) 准二级动力学模型和颗粒内扩散模型能够很好地描述花椰菜根基和叶基生物炭对Pb(Ⅱ)的吸附行为.2种生物炭对Pb(Ⅱ)的吸附过程均符合Langmuir吸附等温模型和Freundlich吸附等温模型, 表明整个吸附过程既有物理吸附又有化学吸附.
3) 花椰菜根基生物炭的吸附速率较快, 在较短的时间就能达到吸附平衡.花椰菜根基生物炭和叶基生物炭对Pb(Ⅱ)的最大吸附量分别可达到434.78~500.00 mg·g-1和416.67~476.19 mg·g-1, 远高于现有文献报道中生物炭对Pb(Ⅱ)的最大吸附量.根基和叶基生物炭的最佳吸附pH值分别为3.20和5.45左右.
Ahmad M, Rajapaksha A U, Lim J E, et al. 2014. Biochar as a sorbent for contaminant management in soil and water: a review[J]. Chemosphere, 99: 19–33.
DOI:10.1016/j.chemosphere.2013.10.071
|
Ahmed A, Li J. 2016. Removal of Pb(Ⅱ) from aqueous solution by using biochars derived from sugar cane bagasse and orange peel[J]. Journal of the Taiwan Institute of Chemical Engineers, 61: 367–375.
DOI:10.1016/j.jtice.2016.01.005
|
安增莉, 侯艳伟, 蔡超, 等. 2011. 水稻秸秆生物炭对Pb(Ⅱ)的吸附特性[J]. 环境化学, 2011, 30(11): 1851–1857.
|
Chandraiah M R. 2016. Facile synthesis of zero valent iron magnetic biochar composites for Pb(Ⅱ) removal from the aqueous medium[J]. Alexandria Engineering Journal, 55: 619–625.
DOI:10.1016/j.aej.2015.12.015
|
Chen X C, Chen G C, Chen L G, et al. 2011. Adsorption of copper and zinc by biochars produced from pyrolysis of hardwood and corn straw in aqueous solution[J]. Bioresource Technology, 102(19): 8877–8884.
DOI:10.1016/j.biortech.2011.06.078
|
陈再明, 陈宝梁, 周丹丹. 2013. 水稻秸秆生物碳的结构特征及其对有机污染物的吸附性能[J]. 环境科学学报, 2013, 33(1): 9–19.
DOI:10.11654/jaes.2013.01.002 |
陈再明, 方远, 徐义亮, 等. 2012. 水稻秸秆生物碳对重金属Pb(Ⅱ)的吸附作用及影响因素[J]. 环境科学学报, 2012, 32(4): 769–776.
|
程启明, 黄青, 刘英杰, 等. 2014. 花生壳与花生壳生物炭对镉离子吸附性能研究[J]. 农业环境科学学报, 2014, 33(10): 2022–2029.
DOI:10.11654/jaes.2014.10.020 |
丁文川, 杜勇, 曾晓岚, 等. 2012. 富磷污泥生物炭去除水中Pb(Ⅱ)的特性研究[J]. 环境化学, 2012, 31(9): 1375–1380.
|
Ding Z H, Wan Y S, Hu X, et al. 2016. Sorption of lead and methylene blue onto hickory biochars from different pyrolysis temperatures:Importance of physicochemical properties[J]. Journal of Industrial and Engineering Chemistry, 37: 261–267.
DOI:10.1016/j.jiec.2016.03.035
|
董兆敏, 吴世闽, 胡建英. 2011. 中国部分地区铅暴露儿童健康风险评价[J]. 中国环境科学, 2011, 31(11): 1910–1916.
|
Feng N C, Guo X Y. 2012. Characterization of adsorptive capacity and mechanisms on adsorption of copper, lead and zinc by modified orange peel[J]. Transactions of Nonferrous Metals Society of China, 22(5): 1224–1231.
DOI:10.1016/S1003-6326(11)61309-5
|
Ghasemi M, Naushad M, Ghasemi N, et al. 2014. Adsorption of Pb(Ⅱ) from aqueous solution using new adsorbents prepared from agricultural waste:Adsorption isotherm and kinetic studies[J]. Journal of Industrial and Engineering Chemistry, 20(4): 2193–2199.
DOI:10.1016/j.jiec.2013.09.050
|
郭素华, 许中坚, 李方文, 等. 2015. 生物炭对水中Pb(Ⅱ)和Zn(Ⅱ)的吸附特征[J]. 环境工程学报, 2015, 9(7): 3215–3222.
DOI:10.12030/j.cjee.20150723 |
Guo X, Zhang S, Shan X Q. 2008. Adsorption of metal ions on lignin[J]. Journal of Hazardous Materials, 151(1): 134–142.
DOI:10.1016/j.jhazmat.2007.05.065
|
Han R, Zhang L, Song C, et al. 2010. Characterization of modified wheat straw, kinetic and equilibrium study about copper ion and methylene blue adsorption in batch mode[J]. Carbohydrate Polymers, 79: 1140–1149.
DOI:10.1016/j.carbpol.2009.10.054
|
Jiang R X, Tian J Y, Zheng H, et al. 2015. A novel magnetic adsorbent based on waste litchi peels for removing Pb(Ⅱ) from aqueous solution[J]. Journal of Environmental Management, 155: 24–30.
|
Jing X R, Wang Y Y, Liu W J, et al. 2014. Enhanced adsorption performance of tetracycline in aqueous solutions by methanol-modified biochar[J]. Chemical Engineering Journal, 248: 168–174.
DOI:10.1016/j.cej.2014.03.006
|
Kalinke C, Mangrich A S, Marcolino L H, et al. 2016. Biochar prepared from castor oil cake at different temperatures:A voltammetric study applied for Pb(Ⅱ), Cd(Ⅱ) and Cu(Ⅱ) ions preconcentration[J]. Journal of Hazardous Materials, 318: 526–532.
DOI:10.1016/j.jhazmat.2016.07.041
|
Kamari A, Yusoff S N M, Abdullah F, et al. 2014. Biosorptive removal of Cu(Ⅱ), Ni(Ⅱ) and Pb(Ⅱ) ions from aqueous solutions using coconut dregs residue:Adsorption and characterisation studies[J]. Journal of Environmental Chemical Engineering, 2(4): 1912–1919.
DOI:10.1016/j.jece.2014.08.014
|
Kołodyńska D, Wnętrzak R, Leahy J J, et al. 2012. Kinetic and adsorptive characterization of biochar in metal ions removal[J]. Chemical Engineering Journal, 197: 295–305.
DOI:10.1016/j.cej.2012.05.025
|
Kumar R, Rani M, Gupta H, et al. 2014. Trace metal fractionation in water and sediments of an urban river stretch[J]. Chemical Speciation and Bioavailability, 26(4): 200–209.
DOI:10.3184/095422914X14142369069568
|
Kyzas G Z, Deliyanni E A. 2015. Modified activated carbons from potato peels as green environmental-friendly adsorbents for the treatment of pharmaceutical effluents[J]. Chemical Engineering Research and Design, 97: 135–144.
DOI:10.1016/j.cherd.2014.08.020
|
李继强, 陈锡永, 唐意佳, 等. 2001. 某冶炼厂环境铅污染及其对人群健康影响的研究[J]. 环境与健康杂志, 2001, 18(3): 151–154.
|
李瑞月, 陈德, 李恋卿, 等. 2015. 不同作物秸秆生物炭对溶液中Pb(Ⅱ)、Cd(Ⅱ)的吸附[J]. 农业环境科学学报, 2015, 34(5): 1001–1008.
DOI:10.11654/jaes.2015.05.025 |
李文萍, 林俊城, 黄科. 2014. 全球花椰菜生产与贸易现状分析[J]. 中国蔬菜, 2014(9): 5–10.
|
Lin J W, Zhan Y H, Zhu Z L, et al. 2011. Adsorption of tannic acid from aqueous solution onto surfactant-modified zeolite[J]. Journal of Hazardous Materials, 193: 102–111.
DOI:10.1016/j.jhazmat.2011.07.035
|
Liu Y, Zhang Z H, Wang P, et al. 2016. Surface charge modification of chloromethylated polystyrene beads with NaH for the removal of sulfamonomethoxine[J]. Journal of the Taiwan Institute of Chemical Engineers, 65: 22–27.
DOI:10.1016/j.jtice.2016.04.037
|
Mohan D, Kumar H, Sarswat A, et al. 2014. Cadmium and lead remediation using magnetic oak wood and oak bark fast pyrolysis bio-chars[J]. Chemical Engineering Journal, 236: 513–528.
DOI:10.1016/j.cej.2013.09.057
|
Mohan D, Sarswat A, Ok Y S, et al. 2014. Organic and inorganic contaminants removal from water with biochar, a renewable, low cost and sustainable adsorbent--a critical review[J]. Bioresource Technology, 160: 191–202.
DOI:10.1016/j.biortech.2014.01.120
|
Mohan D, Singh P, Sarswat A, et al. 2015. Lead sorptive removal using magnetic and nonmagnetic fast pyrolysis energy cane biochars[J]. Journal of Colloid and Interface Science, 448: 238–250.
DOI:10.1016/j.jcis.2014.12.030
|
Park J H, Ok Y S, Kim S H, et al. 2016. Competitive adsorption of heavy metals onto sesame straw biochar in aqueous solutions[J]. Chemosphere, 142: 77–83.
DOI:10.1016/j.chemosphere.2015.05.093
|
Pezoti O, Cazetta A L, Bedin K C, et al. 2016. NaOH-activated carbon of high surface area produced from guava seeds as a high-efficiency adsorbent for amoxicillin removal:Kinetic, isotherm and thermodynamic studies[J]. Chemical Engineering Journal, 288: 778–788.
DOI:10.1016/j.cej.2015.12.042
|
Shen Z T, Jin F, Wang F, et al. 2015. Sorption of lead by Salisbury biochar produced from British broadleaf hardwood[J]. Bioresource Technology, 193: 553–556.
DOI:10.1016/j.biortech.2015.06.111
|
石夏颖. 2014. 油料作物生物炭的制备、表征及其对Cr(Ⅵ)和Cu(Ⅱ)的吸附性能研究[D]. 兰州: 兰州交通大学
http://cdmd.cnki.com.cn/article/cdmd-10732-1014421774.htm |
Swiatkowski A, Pakula M, Biniak S, et al. 2004. Influence of the surface chemistry of modified activated carbon on its electrochemical behaviour in the presence of lead(Ⅱ) ions[J]. Carbon, 42(15): 3057–3069.
DOI:10.1016/j.carbon.2004.06.043
|
Taha S M, Amer M E, Elmarsafy A E, et al. 2014. Adsorption of 15 different pesticides on untreated and phosphoric acid treated biochar and charcoal from water[J]. Journal of Environmental Chemical Engineering, 2(4): 2013–2025.
DOI:10.1016/j.jece.2014.09.001
|
Trakal L, Bingol D, Pohorely M, et al. 2014. Geochemical and spectroscopic investigations of Cd and Pb sorption mechanisms on contrasting biochars:engineering implications[J]. Bioresource Technology, 171: 442–451.
DOI:10.1016/j.biortech.2014.08.108
|
Uchimiya M, Lima I M, Thomas K K, et al. 2010. Immobilization of heavy metal ions (Cu(Ⅱ), Cd(Ⅱ), Ni(Ⅱ), and Pb(Ⅱ)) by broiler litter-derived biochars in water and soil[J]. Journal of Agricultural and Food Chemistry, 58(9): 5538–5544.
DOI:10.1021/jf9044217
|
Venkateswarlu S, Rao Y S, Balaji T, et al. 2013. Biogenic synthesis of Fe3O4 magnetic nanoparticles using plantain peel extract[J]. Materials Letters, 100: 241–244.
DOI:10.1016/j.matlet.2013.03.018
|
王春梅, 欧阳华, 王金达, 等. 2003. 沈阳市环境铅污染对儿童健康的影响[J]. 环境科学, 2003, 24(5): 17–22.
|
Wang H Y, Gao B, Wang S S, et al. 2015. Removal of Pb(Ⅱ), Cu(Ⅱ), and Cd(Ⅱ) from aqueous solutions by biochar derived from KMnO4 treated hickory wood[J]. Bioresource Technology, 197: 356–362.
DOI:10.1016/j.biortech.2015.08.132
|
王林, 章有馀, 张学莉, 等. 2000. 成都市幼儿体铅水平与环境铅污染的关系[J]. 四川环境, 2000, 19(3): 43–45.
|
魏建文, 韦真周, 廖雷, 等. 2014. 氨基修饰介孔分子筛SBA-15对水中Pb(Ⅱ)吸附性能[J]. 环境工程学报, 2014, 8(5): 1825–1830.
|
Wang Z Y, Liu G C, Zheng H, et al. 2015. Investigating the mechanisms of biochar's removal of lead from solution[J]. Bioresource Technology, 177: 308–317.
DOI:10.1016/j.biortech.2014.11.077
|
Wong K K, Lee C K, Low K S, et al. 2003. Removal of Cu and Pb from electroplating wastewater using tartaric acid modified rice husk[J]. Process Biochemistry, 39(4): 437–445.
DOI:10.1016/S0032-9592(03)00094-3
|
Wu W D, Li J H, Lan T, et al. 2017. Unraveling sorption of lead in aqueous solutions by chemically modified biochar derived from coconut fiber:A microscopic and spectroscopic investigation[J]. Science of the Total Environment, 576: 766–774.
DOI:10.1016/j.scitotenv.2016.10.163
|
Xiao F, Howard H J C. 2009. Comparison of biosorbents with inorganic sorbents for removing copper (Ⅱ) from aqueous solutions[J]. Journal of Environmental Management, 90(10): 3105–3109.
DOI:10.1016/j.jenvman.2009.05.018
|
肖薇. 2015. 改性热解炭的表征及对水体中污染物的吸附研究[D]. 郑州: 郑州大学
http://cdmd.cnki.com.cn/Article/CDMD-10459-1015301434.htm |
谢超然, 王兆炜, 朱俊民, 等. 2016. 核桃青皮生物炭对重金属铅、铜的吸附特性研究[J]. 环境科学学报, 2016, 36(4): 1190–1198.
|
Xu X Y, Cao X D, Zhao L. 2013. Comparison of rice husk-and dairy manure-derived biochars for simultaneously removing heavy metals from aqueous solutions:role of mineral components in biochars[J]. Chemosphere, 92(8): 955–961.
DOI:10.1016/j.chemosphere.2013.03.009
|
杨宵霖, 郑舜琼, 刘廷筑, 等. 1998. 环境铅污染对妇女生育功能危害的调查[J]. 环境与健康杂志, 1998, 15(4): 154–156.
|
Yang Y, Wei Z B, Zhang X L, et al. 2014. Biochar from Alternanthera philoxeroides could remove Pb(Ⅱ) efficiently[J]. Bioresource Technology, 171: 227–232.
DOI:10.1016/j.biortech.2014.08.015
|
袁广翔, 张玉娟, 戴红旗, 等. 2011. 钙离子与钠离子对浆料Zeta电位的影响[J]. 环境工程学报, 2011, 35(3): 119–123.
|
Zeng F, Liu W, Jiang H, et al. 2011. Separation of phthalate esters from bio-oil derived from rice husk by a basification-acidification process and column chromatography[J]. Bioresource Technology, 102(2): 1982–1987.
DOI:10.1016/j.biortech.2010.09.024
|
Zhang W, Mao S, Chen H, et al. 2013. Pb(Ⅱ) and Cr(Ⅵ) sorption by biochars pyrolyzed from the municipal wastewater sludge under different heating conditions[J]. Bioresource Technology, 147: 545–552.
DOI:10.1016/j.biortech.2013.08.082
|
张越, 林珈羽, 刘沅, 等. 2015. 生物炭对铅离子的吸附性能[J]. 化工环保, 2015, 35(2): 177–181.
|
郑惠, 林文璇, 黄健红, 等. 2008. 环境铅污染对婴幼儿智能发育的影响[J]. 中国预防医学杂志, 2008, 9(6): 460–463.
|
朱惠霞, 胡立敏, 陶兴林. 2011. 花椰菜再生体系的优化[J]. 甘肃农业科技, 2011(6): 16–18.
|
 2017, Vol. 37
2017, Vol. 37