近年来,随着各国核工业的迅速发展和放射性同位素技术在航空航天、机械、医疗、辐射育种等领域的广泛应用,随之产生的一个严峻问题就是放射性污染.铀是核工业中运用最广的一种重金属,它具有的高毒性和长半衰期,对生态系统的危害极大,并能通过食物链进入生物体,破坏机体正常代谢活动,危害人体及其他生物健康(周书葵等,2011).自1949年Ruchhoft首次提出生物吸附概念后,生物吸附法在含铀废水处理中得到广泛研究.它具有成本低、吸附效率高、耗能少、不产生二次污染等优点,特别是在处理浓度低于100 mg·L-1的含铀放废水方面呈现出独特的优势(Wang et al., 2006;Zhang et al., 2014).国内外学者对这一领域都进行了深入的研究,选用的吸附剂主要有黑曲霉(Aspergillus niger) (Mukhopadhyay et al., 2007)、根霉((Rhizopus arrihizus)(Wang et al., 2010)和酿酒酵母(Saccharomyces cerevisiae)(Lu et al., 2013)等菌类和小球藻(Chlorella vulgaris)(Vogel et al., 2010)等藻类.
酿酒酵母作为一种重要的工业微生物,广泛应用于发酵工业与食品生产,它所具有的廉价、易于获得、安全无毒性以及理想模型生物等优点,使其成为研究重金属生物吸附的良好生物材料(陈灿等,2006;Sarri et al., 2009).目前,生物吸附的一个重要研究方向在于采用不同的预处理手段改善生物吸附剂的吸附性能,例如,Göksungur等(2005)利用乙醇处理的酵母进行Cd和Pb的吸附,发现吸附量有显著的改善. Mukhopadhyay等(2007)运用甲醛处理的黑曲霉对Cu进行吸附,也发现甲醛处理的菌体能吸附更多重金属.此外,就是通过化学试剂对细胞表面官能团进行改性以研究吸附机理,例如,Bai等(2010)分别采用甲醇和甲醛处理的粘红酵母对U(Ⅵ)进行吸附,发现两种试剂对于改善吸附量上存在很大的差异并提出了不同的吸附机理.但对于甲醛修饰的酿酒酵母对U(Ⅵ)的吸附机理却鲜有报道.
本研究采用甲醛修饰的酿酒酵母作为吸附剂,对铀的吸附过程中溶液酸碱度的影响、吸附动力学、吸附热力学进行分析,并结合扫描电镜(Scanning electron microscopy)以及傅里叶变换红外光谱(Fourier transform infrared spectroscopy)深入研究生物吸附机理,为工业化应用以及后续研究提供依据.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 铀溶液的配制与化学试剂称量2.1095 g硝酸铀酰(UO2(NO3)2·6H2O),先加入少量去离子水,再加入10 mL浓硝酸定容到1000 mL,得到1 mg·mL-1的铀储备液,实验所需铀溶液用pH为2的硝酸逐级稀释到所需的浓度.硝酸和氢氧化钠用于调节pH,实验用的所有试剂均为分析纯.
2.1.2 生物吸附剂的制备研究采用的酿酒酵母购自安琪酵母股份有限公司.实验前先将高活性干酵母活化选种,所选取的细胞保存在斜面试管中,实验时将斜面保存的酵母菌,用接种针接入液体培养基中活化16 h,取5 mL培养液接种到100 mL YPD液体培养基(成分:1%酵母提取物,2%蛋白胨,2%葡萄糖)中二次培养30 h,得到的菌体悬浊液离心(5000 r·min-1) 5 min并用去离子水清洗3遍,得到活性酵母悬浊液,并采用烘干法称重,配置成所需浓度的细胞悬浊液.
将部分活体酵母菌体悬浊液取出,加入30%甲醛溶液(菌液体积与甲醛体积1:1),置于恒温摇床中振荡6 h (30 ℃,200 r·min-1),体系离心(5000 r·min-1) 5 min并用去离子水清洗3遍,得到甲醛修饰酵母悬浊液,并采用烘干法称重,配置成所需浓度的甲醛修饰细胞悬浊液,悬浊液均置于4 ℃冰箱内备用.
2.1.3 实验仪器WGJ-Ⅲ型微量铀分析仪(杭州大吉光电仪器);JSM-6701F冷场发射型扫描电镜(日本电子株式会社);NEXUS670-傅里叶红外变换光谱仪(美国Thermo Nicolet公司).
2.2 吸附实验方法根据不同实验,在40 mL的聚乙烯试管内加入一定体积的菌体悬浮液和灭菌去离子水于摇床上恒温振荡混合(200 r·min-1,30 min)后,加入一定量铀储备液并调节溶液到适宜的pH值,在摇床上恒温振荡吸附(200 r·min-1),振荡一定时间后取下离心(10000 r·min-1,15 min),取50 μL上层清液测定其中铀离子浓度.
铀浓度利用微量铀分析仪工作曲线法测定,铀的吸附量及吸附率用分别式(1) 和式(2) 表示.
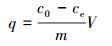
|
(1) |
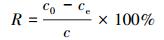
|
(2) |
式中,q为每克干菌吸附铀的质量(mg·g-1),c0为吸附前铀初始质量浓度(mg·L-1),ce为吸附后铀质量浓度(mg·L-1),V为溶液体积(L),m为菌体干重(g),R为铀吸附率.
2.3 光谱分析测试 2.3.1 扫描电镜样品制备实验离心收集所得的吸附前后的菌体,用0.1 mol·L-1的NaCl溶液清洗2次,以保持菌体的渗透压,加入2.5%戊二醛,置于4 ℃中固定1 h后,除去戊二醛,依次使用20%、50%、80%的乙醇溶液进行梯度脱水处理,再将菌体转移到洁净的铝箔纸上,用100%乙醇脱水,自然风干后,表面喷上粒径为4 nm的金颗粒,置于JSM-6701F冷场发射性扫描电镜下观测.
2.3.2 红外光谱样品制备实验离心收集所得的吸附前后的菌体,置于30 ℃恒温干燥箱中干燥成粉末,红外测试采用KBr压片法进行测定,测量的波数精度≤ ±0.01 cm-1.
3 结果与讨论(Results and discussion) 3.1 吸附量与吸附动力学如图 1所示是未经处理的活酵母与甲醛修饰酿酒酵母的吸附量差异图,在达到吸附平衡时,活菌与甲醛修饰细胞在吸附量上存在巨大的差异,在pH为3~6的范围内时,活体酵母与甲醛修饰酿酒酵母的吸附量和吸附率均随着pH的上升而升高,在pH为5时,甲醛修饰酿酒酵母的U(Ⅵ)吸附量达到了(17.89±0.45) mg·g-1,是活菌吸附量的近6倍,如此大的吸附差异可以归结为细胞表面的结构变化或结合位点活性的变化(Wang et al., 2017;Bai et al., 2010).
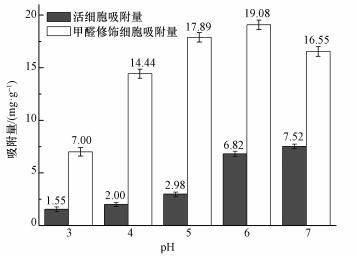 |
| 图 1 活菌与甲醛修饰酿酒酵母的U(Ⅵ)吸附量(T=30 ℃, 菌浓度为0.05 g·L-1, U(Ⅵ)为1 mg·L-1 t=4 h) Fig. 1 Uranium accumulation by raw and methanal modified S. cerevisiae biomass |
甲醛修饰酿酒酵母对铀的吸附率和吸附量随时间的变化如图 2所示.在实验条件下,仅需要15 min U(Ⅵ)的吸附量就可以达到(11.61±0.44) mg·g-1,90 min后基本达到吸附平衡,此时,铀酰离子的平衡吸附率为72.22%.如此快速的过程表明铀酰离子与甲醛修饰酿酒酵母的吸附机理主要是表面吸附(Göksungur et al., 2005).
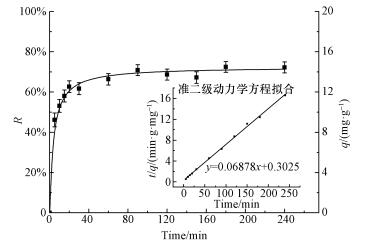 |
| 图 2 甲醛修饰酿酒酵母吸附U(Ⅵ)的动力学曲线(T为30 ℃,U(Ⅵ)为1 mg·L-1,菌浓度为0.05 g·L-1,t为4 h,pH为4.0) Fig. 2 Kinetic study of UO22+ adsorption in methanal modified Saccharomyce cerevisiae biomass |
为了进一步探讨甲醛修饰酿酒酵母对铀酰离子的吸附机理,采用准一级吸附动力学方程与准二级吸附动力学方程对吸附过程进行分析.准一级吸附动力学方程表达式如式(3) 所示.
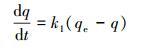
|
(3) |
带入边界条件t=0;q=0积分可得:
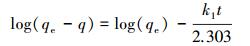
|
(4) |
式中,qe为平衡时的理论吸附量(mg·g-1), q为t时刻的吸附量(mg·g-1), k1为准一级吸附速率常数(min-1).
准二级吸附动力学方程是建立在假设吸附速率受化学吸附机理控制的基础上,其表达式如式(5) 所示.
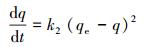
|
(5) |
带入边界条件t=0;q=0;t=t; q=qe可得式(6).
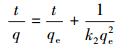
|
(6) |
式中,qe为平衡时的理论吸附量(mg·g-1);q为t时刻的吸附量(mg·g-1);k2为准二级吸附速率常数(g·mg-1·min-1).
利用式(4) 与式(6) 分别对吸附动力学过程进行研究,得到拟合参数如表 1所示.
| 表 1 甲醛修饰酿酒酵母对铀吸附的动力学拟合参数 Table 1 Kinetic constants of uranium adsorption onto methanal modified Scharromyces cerevisiae |
从表 1可以看出,对于甲醛修饰酵母的铀吸附过程来说,准二级吸附动力学方程拟合结果较好,R2达到0.998,这个结果远远高于准一级吸附动力学方程的拟合结果(0.728),因此,准二级动力模型适用于描述甲醛修饰酵母对铀酰离子的吸附过程,吸附过程是一个限速的化学吸附过程,吸附过程存在着电子共用和转移(Mukhopadhyay et al., 2007).
3.2 pH对吸附的影响金属离子与吸附剂在水溶液中的反应可表示为式(7):
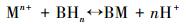
|
(7) |
式中,M为金属离子,n为金属所带电荷,B为官能团的结合位点(Iqbal et al., 2009).之前的研究表明,由于金属离子和溶液中的H+或者H3O+对结合位点的竞争关系,导致pH值对生物吸附的影响远超过其他的环境因素,为了探究pH在活性酵母与甲醛修饰酵母对铀酰离子吸附行为的影响,选择3.0~7.0的pH进行实验.
图 3是甲醛修饰酿酒酵母的吸附量(率)随pH变化的关系图,这条抛物线状曲线表明了吸附量对pH有强烈的依赖关系,在pH为3.5~5.5时,铀的吸附量迅速上升,峰值位于5.8左右,与此同时,约97.30%±2.08%的U(Ⅵ)被吸附,而在此之后,曲线迅速下降.Lu等(2013)也发现,高温高压灭活的酵母吸附量最高时的最佳pH为5.8.这可能与细胞壁表面的氨基酸提供了大量的带负电的基团或离子状配体有关,例如:—COOH、—NH2等(Tsezos, 1983).在pH 3.0~7.0的范围内,pH为3.0时,吸附率最低,同时吸附平衡往往需要更长的时间,可能是由于H+与酿酒酵母表面活性基团的结合性强于UO22+.随着pH的增加,这些活性基团逐渐去质子化并与U(Ⅵ)结合,而当pH约等于氨基酸的等电点时,吸附量最高.当pH>7时,铀酰离子逐渐转化为沉淀而阻碍铀离子与酵母表面的结合.表 2是常见氨基酸等电点,可以看出,最佳吸附pH与多数氨基酸的等电点是吻合的.
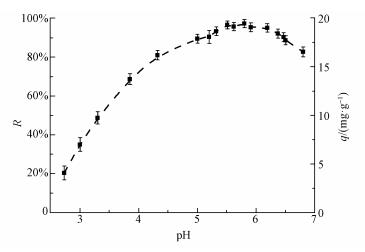 |
| 图 3 pH对甲醛修饰酿酒酵母吸附UO22+的影响(T为30 ℃,菌浓度为0.05 g·L-1,U(Ⅵ)为1 mg·L-1,t为7 h) Fig. 3 Effect of pH on UO22+ sorption in methanal modified Saccharomyces cerevisiae biomass |
| 表 2 常见氨基酸等电点(王镜岩等, 2002) Table 2 Isoelectric point associated with the common amino acid in proteins |
描述微生物对铀酰离子吸附的经典等温模型主要有Langmuir和Freundlich方程,L模型是假定吸附剂表面均一,各处吸附能相同,是一种单分子层的吸附,其表达式与线性表达式分别如式(8) 和式(9) 所示.
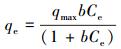
|
(8) |
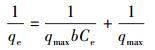
|
(9) |
式中,qe为吸附量(mg·g-1);Ce为平衡时铀浓度(mg·g-1);qmax为最大吸附量(mg·g-1).b是L模型常数,b值越小,表明铀酰离子与细胞的结合越紧密.
F模型是用于描述多分子层吸附的经验公式,其表达式与线性表达式分别如式(10) 和式(11) 所示.
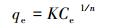
|
(10) |
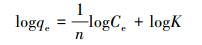
|
(11) |
式中,K和n为吸附等温常数(Faghihian et al., 2012).
铀离子浓度对生物吸附的影响如图 4所示,Langmuir和Freundlich等温模型的拟合结果如图 5所示,L模型和F模型的R2分别为0.997与0.845,L模型显著高于F模型,这表明甲醛修饰酿酒酵母对铀酰离子的吸附与L模型吻合较好,是一种单分子层的吸附,UO22+主要被吸附到酿酒酵母的表面,两种模型计算所得的拟合度与等温常数见表 3,在实验条件下,铀酰离子的最大吸附量可达到280.11 mg·g-1,表明甲醛修饰的酿酒酵母是一种具有高吸附量的生物吸附剂.
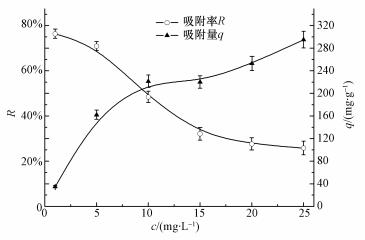 |
| 图 4 铀浓度对甲醛修饰酵母吸附过程的影响(T为30 ℃,pH为6.0,菌浓度为0.025 g·L-1,t为6 h) Fig. 4 Effect of uranium concentration on adsorption by methanal modified Saccharomyces cerevisiae |
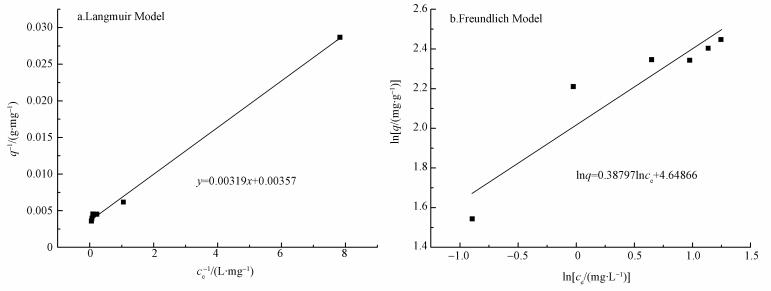 |
| 图 5 甲醛修饰酿酒酵母吸附铀酰离子的Langmuir (a)与Freundlich(b)模型拟合曲线 Fig. 5 Langmuir (a) and Freundlich (b) model fitting for biosorption of uranyl ions |
| 表 3 甲醛修饰酿酒酵母吸附铀的Langmuir与Freundlich模型拟合参数(T=30 ℃, pH为6.0, 菌浓度0.025 g·L-1, t为6 h) Table 3 Langmuir and Freundlich constants for biosorption of uranyl ions |
图 6所示是甲醛修饰前后以及铀酰离子吸附前后酿酒酵母扫描电镜图,从图中可以看出修饰前后以及吸附前后,酵母菌菌体表面的形貌差异.
 |
| 图 6 吸附铀前后的扫描电镜图(t为6 h,菌浓度:1.6 g·L-1, U(Ⅵ)为100 mg·L-1, pH为5.0,T为30 ℃) (a.吸附前活性酵母; b.吸附前甲醛修饰酵母; c.吸附后甲醛修饰酵母; d.为(c)的局部放大图) Fig. 6 Scanning electron micrographs of S. cerevisiae cells of (a) raw biomass; (b) methanal modified S. cerevisiae; (c) uranium-loaded of methanal modified S. cerevisiae and (d) The enlarged region denoted by rectangle in (c) |
扫描电镜图像显示,活体酵母表面光滑平整,细胞饱满(图 6a),经过甲醛修饰,细胞表面变得粗糙,凹凸不平,边缘产生皱褶.在吸附铀酰离子后,细胞表面被直径约为1 μm的鳞片状铀沉淀所覆盖.
3.5 傅里叶变换红外光谱分析研究表明,酵母细胞壁的主要成分(干重质量百分比)是β-葡聚糖和甘露蛋白(85%~90%),少量的几丁质(1%~3%)和脂类(2%~5%)(Galichet et al., 2001).这些成分提供了大量的活性基团,例如:氨基(-NH2)、羟基(—OH)、羧基(—COOH)和磷酸类物质.这些基团产生的伸缩、弯曲和变形振动均可以在红外光谱中产生明显的吸收峰.按文献可以将谱带进行归属,如表 4所示.
| 表 4 吸附铀前后酵母细胞的主要红外峰位 Table 4 Assignment of the FTIR spectra for raw and treated biomass before and after uranium sorption |
在3500~3200 cm-1范围内可以观察到一个较宽的峰,这是由于—OH和—NH基团的变形振动引起的,其中,位于3418 cm-1左右的峰位是由于分子间、分子内氢键或者KBr吸收水产生的—OH振动(Iqbal et al., 2009).在2927 cm-1处的吸收峰是由于脂肪酸中—CH基团的反对称振动引起的(Iqbal et al., 2009).表征蛋白质最重要的谱带是酰胺带,位于1650 cm-1处的酰胺Ⅰ带是由═CO的伸缩振动、N—H的弯曲振动形成的,它表明了酿酒酵母中蛋白质的二级结构以α螺旋为主(翁诗甫,2010).1540 cm-1处的酰胺Ⅱ带则是由N—H的弯曲振动和的反对称振动引起的,1400~1398 cm-1处的峰位由羧酸根COO的对称振动引起,位于1070 cm-1处的强峰是由于HPO42-中的P—O或P═O振动产生的.位于1237 cm-1处的酰胺Ⅲ带可能是由C—N弯曲振动、—COOH中C—O的伸缩振动和P═O的变形振动导致的,1452 cm-1处的特征峰是由于CH2的剪式振动、CH3的非对称弯曲振动以及羧酸根COO的反对称振动引起的(白静等,2009).位于1070 cm-1的峰是由于酿酒酵母细胞表面的多糖羟基骨架或HPO42-中的P═O,P—O伸缩振动引起的.在指纹区(1350~650cm-1),位于810 cm-1处的峰位是酿酒酵母表面醛糖酸的特征峰(Galichet et al., 2001).位于540~580 cm-1处的峰位是—PO4的剪式振动所产生的(翁诗甫,2010).
图 7为活性酿酒酵母和甲醛修饰酵母的红外光谱图.对比曲线a和b,—OH的峰位红移了约13个波数,表明甲醛修饰的过程导致—OH的键长增长和分子内(间)氢键的增加,可能是—CHO与—OH反应并产生共价配位键,基本原理如下(Chen et al., 2006):
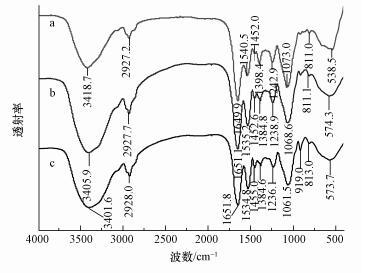 |
| 图 7 酵母细胞红外光谱图(a.吸附前活性酵母, b.吸附前甲醛修饰酵母, c.吸附后甲醛修饰酵母)(t为6 h,菌浓度1.6 g·L-1, U(Ⅵ)为100 mg·L-1, pH为5.0,T为30 ℃) Fig. 7 Fourier transform infrared spectrum of (a) raw yeast; (b) methanal modified yeast and (c) uranium-loaded of (b) |
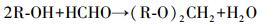
|
(12) |
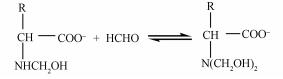
酰胺Ⅰ带的蓝移(1649.9/1651.1 cm-1)和酰胺Ⅱ带的红移(1540.5/1535.2 cm-1)表明可蛋白质肽链上O原子和N原子发生了变化,羧酸根COO的对称振动产生了15个波数的红移(1398.4/1384.8 cm-1),说明COO的键长增长了.另外,CH3峰位峰强明显增加,表明了官能团发生了甲基化.实际上,甲醛与α氨基酸中含N的氨基能发生加成反应,其反应机理如下:
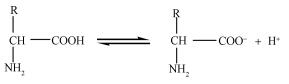
|
(13) |
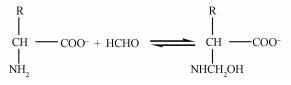
|
(14) |
|
(15) |
式中,R代表α氨基酸的支链,氨基酸的电离使COO-增多,在适宜的pH值下,可逆反应朝正向进行,甲醛与氨基发生作用生成羟甲基衍生物,从而使—OH、—NH、—CH2以及C═O的结构发生变化,并导致氨基甲基化(原来的—NH2被—CH2OH取代)和蛋白质变性(Bai et al. 2010;翁诗甫,2010).而甲醛修饰的酿酒酵母吸附量明显优于活性酿酒酵母,可能正是因为氨基甲基化的过程减少了菌体细胞壁上正电位的数目,增大了铀酰离子与酵母相互作用的几率,从而使吸附能力增加.另外,—COOH(1242.9/1238.9 cm-1),HPO42-(1073.0/1068.6 cm-1),PO43-(538.5/574.3 cm-1)峰位均产生了红移,可能是细胞修饰之后,细胞膜的通透性发生了改变并释放了一些胞内物质,糖醛酸等物质没有发生较大的峰移,表明细胞表面的物质没有发生很大的化学变化(Wang et al., 2017).
图 7b和7c为吸附铀前后,甲醛修饰酵母的红外光谱对比图.在指纹区可以观察到一个位于919~915 cm-1范围内的新吸收峰,这是铀酰基团非对称伸缩振动和其他铀酰络合物的特征峰位.先前的研究表明,pH=2时,UO22+的吸收峰位在961 cm-1,而42~46 cm-1的红移表明铀酰离子与其他离子产生了结合而使UO22+离子的键长增长,同时,胞内释放的HPO42-等离子均会与铀酰离子生成沉淀或络合物(Müller et al., 2008),因此,这个峰位是由多种沉淀或络合物导致的.
羧酸根COO的对称振动与非对称振动的峰移表明羧酸根COO与铀酰离子产生了络合,金属与羧酸盐的络合物通常有3种(图 8):(a)单齿配位化合物,(b)双齿配位化合物,(c)桥式配位化合物.配体类型取决于羧酸盐反对称振动与对称振动峰位之间的差值[Δν=νas(COO)-νs(COO)],当Δν>200 cm-1时,形成单齿配位化合物;当Δν < 100 cm-1时,形成双齿配位化合物;当Δν≈150 cm-1时,形成桥式配位化合物(翁诗甫,2010).甲醛修饰酵母菌在吸附铀前后,羧酸根的反对称振动与对称振动之间的差值约为70 cm-1,依据以上所述的准则,可以判断出铀酰与羧酸根主要络合为双齿配位化合物(图 8b).
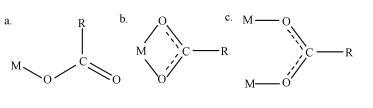 |
| 图 8 金属与羧酸盐络合物示意图 Fig. 8 Different types of metal-carboxylate coordination |
另外,—OH的峰位进一步红移(3405.9/3401.6 cm-1),UO22+离子对O—H键上电子云的诱导作用增强,O原子与铀酰离子产生配位,表明—OH在于酵母与铀酰离子的结合中发挥了重要的作用.酰胺Ⅰ、Ⅱ带和—CH产生了微弱的峰移,表明了CO,C—H和N—H均参与了铀的吸附过程,糖醛酸等结构未发生明显的改变.
4 结论(Conclusions)通过上述的研究发现,甲醛修饰酿酒酵母对铀酰离子具有显著的吸附作用,并能有效地回收低浓度废水中的铀离子,吸附动力学研究表明铀酰离子的吸附是一个快速的过程,大约90 min可以达到吸附动态平衡,吸附过程存在着电子共用和转移.吸附的最佳pH位于5.8,它与细胞表面的离子状配体、氨基酸等电点以及铀酰离子的水解息息相关.Langmuir和Freundlich等温模型的拟合结果表明,甲醛修饰酿酒酵母对铀酰离子的吸附是一种单分子层吸附,扫描电镜和红外光谱分析表明,甲醛修饰改变了酵母细胞的表面形貌,使蛋白结构发生了变化并形成了羟甲基衍生物,在吸附铀酰之后,细胞表面覆盖了一层鳞片状的铀沉淀,铀的沉淀与络合物形式复杂,主要与—OH、—PO43-、—COO、C═O等基团相互作用,铀酰与羧酸根主要络合为双齿配位化合物.甲醛修饰酿酒酵母与铀酰离子的相互作用主要存在着络合、沉淀、静电吸附以及电子交换等多种机理.
Bai J, Yao H J, Fan F L, et al. 2010. Biosorption of uranium by chemically modified Rhodotorula glutinis[J]. Journal of Environmental Radioactivity, 101(11): 969–973.
DOI:10.1016/j.jenvrad.2010.07.003
|
白静, 秦芝, 王菊芳, 等. 2009. 粘红酵母对铀的吸附研究[J]. 光谱学与光谱分析, 2009, 29(5): 1218–1221.
|
Chen J P, Yang L. 2006. Study of a heavy metal biosorption onto raw and chemically modified Sargassum sp. via spectroscopic and modeling analysis[J]. Langmuir, 22(21): 8906–8914.
DOI:10.1021/la060770+
|
陈灿, 王建龙. 2006. 酿酒酵母吸附重金属离子的研究进展[J]. 中国生物工程杂志, 2006, 26(1): 69–76.
|
Faghihian H, Peyvandi S. 2012. Adsorption isotherm for uranyl biosorption by Saccharomyces cerevisiae, biomass[J]. Journal of Radioanalytical and Nuclear Chemistry, 293(2): 463–468.
DOI:10.1007/s10967-012-1814-y
|
Galichet A, Sockalingum G D, Belarbi A, et al. 2001. FTIR spectroscopic analysis of Saccharomyces cerevisiae cell walls:study of an anomalous strain exhibiting a pink-colored cell phenotype[J]. FEMS Microbiology Letters, 197(2): 179–186.
DOI:10.1111/fml.2001.197.issue-2
|
Göksungur Y, Uren S, Güvenç U. 2005. Biosorption of cadmium and lead ions by ethanol treated waste baker's yeast biomass[J]. Bioresource Technology, 96(1): 103–109.
DOI:10.1016/j.biortech.2003.04.002
|
Iqbal M, Saeed A, Zafar S I. 2009. FTIR spectrophotometry, kinetics and adsorption isotherms modeling, ion exchange, and EDX analysis for understanding the mechanism of Cd2+ and Pb2+ removal by mango peel waste[J]. Journal of Hazardous Materials, 164(1): 161–171.
DOI:10.1016/j.jhazmat.2008.07.141
|
Lu X, Zhou X J, Wang T S. 2013. Mechanism of uranium(Ⅵ) uptake by Saccharomyces cerevisiae, under environmentally relevant conditions:Batch, HRTEM, and FTIR studies[J]. Journal of Hazardous Materials, 262(8): 297–303.
|
Mukhopadhyay M, Noronha S B, Suraishkumar G K. 2007. Kinetic modeling for the biosorption of copper by pretreated Aspergillus niger biomass[J]. Bioresource Technology, 98(9): 1781–1787.
DOI:10.1016/j.biortech.2006.06.025
|
Müller K, Brendler V, Foerstendorf H. 2008. Aqueous uranium(Ⅵ) hydrolysis species characterized by attenuated total reflection Fourier-transform infrared spectroscopy[J]. Inorganic Chemistry, 47(21): 10127–10134.
DOI:10.1021/ic8005103
|
Ruchhoft C C. 1949. The possibilities of disposal of radioactive wastes by biological treatment methods[J]. Sewage Works Journal, 21(5): 877–883.
|
Sarri S, Misaelides P, Papanikolaou M, et al. 2009. Uranium removal from acidic aqueous solutions by Saccharomyces cerevisiae, Debaryomyces hansenii, Kluyveromyces marxianus and Candida colliculosa[J]. Journal of Radioanalytical and Nuclear Chemistry, 279(3): 709–711.
DOI:10.1007/s10967-008-7274-8
|
Tsezos M. 1983. The role of chitin in uranium adsorption by R. arrhizus[J]. Biotechnology and Bioengineering, 25(8): 2025–2040.
DOI:10.1002/(ISSN)1097-0290
|
Vogel M, Günther A, Rossberg A, et al. 2010. Biosorption of U(Ⅵ) by the green algae Chlorella vulgaris in dependence of pH value and cell activity[J]. Science of the Total Environment, 409(2): 384–395.
DOI:10.1016/j.scitotenv.2010.10.011
|
Wang J S, Hu X J, Wang J, et al. 2010. The tolerance of Rhizopus arrihizus to U(Ⅵ) and biosorption behavior of U(Ⅵ) onto R. arrihizus[J]. Biochemical Engineering Journal, 51(1): 19–23.
|
Wang J L, Chen C. 2006. Biosorption of heavy metals by Saccharomyces cerevisiae:a review[J]. Biotechnology Advances, 24(5): 427–451.
DOI:10.1016/j.biotechadv.2006.03.001
|
Wang T S, Zheng X Y, Wang X Y, et al. 2017. Different biosorption mechanisms of Uranium(Ⅵ) by live and heat-killed Saccharomyces cerevisiae under environmentally relevant conditions[J]. Journal of Environmental Radioactivity, 167: 92–99.
DOI:10.1016/j.jenvrad.2016.11.018
|
翁诗甫. 2010. 傅里叶变换红外光谱分析[M]. 北京: 化学工业出版社: 377–388.
|
王镜岩, 朱圣庚, 徐长法. 2002. 生物化学(第3版)(上册)[M]. 北京: 高等教育出版社: 133–135.
|
Zhang C, Malhotra S V, Francis A J. 2014. Zhang C, Malhotra S V, Francis A J. 2014. Toxicity of ionic liquids to Clostridium, sp. and effects on uranium biosorption[J]. Journal of Hazardous Materials, 264(2): 246–253.
|
周书葵, 娄涛, 庞朝辉, 等. 2011. 放射性废水处理技术[M]. 北京: 化学工业出版社: 7–8.
|
 2017, Vol. 37
2017, Vol. 37


