2. 山西大学资源与环境工程研究所, 太原 030006;
3. 江西师范大学鄱阳湖湿地与流域研究教育部重点实验室, 南昌 330022;
4. 中国科学院遗传所农业资源研究中心, 石家庄 050021
2. Institute of Resources and Environment Engineering, Shanxi University, Taiyuan 030006;
3. Key Laboratory of Poyang Lake Wetland and Watershed Research, Ministry of Education, Jiangxi Normal University, Nanchang 330022;
4. Center for Agricultural Resources Research, Institute of Genetics and Developmental Biology, CAS, Shijiazhuang 050021
通过理解胶体在多孔介质中的迁移机理来模拟胶体在多孔介质中的迁移行为具有重要的意义,如在河堤过滤(Weiss et al., 2005)、环境修复(Zhang, 2003)、污染物迁移(张文静等, 2016)等方面.近二、三十年来,人们对胶体在饱和多孔介质中的迁移已经进行了广泛的研究.胶体过滤理论(Colloid Filtration Theory, CFT)常被用来描述胶体的迁移行为;DLVO(Derjaguin-Landau-Verwey-Overbeek)理论被用来描述胶体与多孔介质间的相互作用力,但实验结果仍然有许多地方与理论相违背.例如,在有利环境下,并不是所有的胶体均被滞留下来形成不可逆吸附,而是仅仅有少量的吸附位点被认为是有利的(Einat et al., 2011),并且通过降低离子强度仍然有部分胶体被解吸下来(Shen et al., 2012a);在不利环境下,大量的胶体被滞留在多孔介质中,通过降低离子强度却只有少量的胶体被解吸下来,而且不利环境下土柱滞留剖面常显示一种超指数分布(Tufenkji et al., 2004),与理论上的指数分布并不相符.介质表面化学异质性被认为是造成上述矛盾的主要原因之一.
介质表面化学异质性指的是由于多孔介质表面存在一些化学杂质,如金属氧化物、有机物等,造成多孔介质表面电荷不均匀的一种状态,这种电荷的不均匀分布直接导致了胶体与多孔介质之间相互作用力的差异.近年来,有学者针对化学异质性进行了大量的研究(Tufenkji et al., 2005; Shen et al., 2013).Tufenkji等(2004)认为多孔介质表面电荷分布的差异导致胶体吸附到多孔介质表面速率的差异,从而形成一种“快”吸附和一种“慢”吸附,即所谓的双速率吸附模型,这可以很好地解释土柱剖分产生的超指数曲线.但随后Foppen等(2007)否定了上述说法,排除了化学异质性是产生超指数分布的原因,而认为这是由种群之间吸附的特异性差异造成的.此外,Duffadar等(2007)基于表面元素集成技术,从理论上阐述了电荷的异质性会降低排斥势垒从而有利于胶体在初级势阱中的滞留.Foppen等(2005)则通过实验验证了随着化学杂质含量的增加,石英砂对大肠杆菌的吸附能力逐渐增强,但增加的速度随着杂质含量增加而降低.
近年来,不论从理论上还是实验上,学者们对化学异质性对胶体迁移的影响已进行深入研究,但仍然存在很多的问题.例如,化学异质性对可逆吸附和不可逆吸附的影响,对胶体解吸的影响,以及这种影响在有利和不利环境下是否同样显著等.一些学者认为化学异质性对胶体产生的吸附是不可逆的(Shen et al., 2013),而另一些学者认为这种吸附是可以随着溶液化学环境的变化而释放出来,即为可逆的(Kozlova et al., 2006).本文通过比较胶体在不同玻璃微珠中的迁移行为来探究多孔介质表面化学异质性对胶体迁移的影响,以期为研究胶体在多孔介质中的迁移提供依据.
2 材料和方法(Materials and methods) 2.1 胶体和多孔介质本实验采用的是羧基化聚苯乙烯乳胶颗粒,具有良好的稳定性,平均粒径为1 μm.胶体浓度用紫外-可见分光光度计来测量,波长为423 nm.
为了减小表面粗糙度对实验的影响,多孔介质用玻璃微珠来代替.用筛网筛出的粒径为0.45~0.6 mm的玻璃微珠,将筛选过的玻璃微珠分为2组,一组先用自来水漂洗数次,然后超声处理15 min,再用超纯水漂洗至上清液吸光度为0;而另一组需在自来水漂洗、超声处理后进行酸洗,酸洗的办法采用Li等(2004)的方法:先用丙酮和正己烷润洗,然后浸泡在浓盐酸中24 h,最后用超纯水漂洗至上清液pH接近中性且电导率接近超纯水.
2.2 土柱实验实验柱子采用PVC管组装而成,柱子两侧分别用盖子封口,在盖子和多孔介质之间铺层孔径为25 μm的尼龙网.柱子内径为4.6 cm,有效高度为12 cm.测得玻璃珠的孔隙度为0.38.实验前应先将玻璃珠均匀地填装在柱子中,采用湿法填装可以有效地排出柱子中的气泡.
实验过程中需配制背景液、胶体悬液及不同pH条件下的超纯水(加氢氧化钠调节),背景液为浓度分别为0.001、0.01、0.05 mol·L-1的氯化钠溶液,在背景液中添加胶体使得胶体的浓度为10 mg·L-1,即得对应的胶体悬液.
土柱实验采用从下至上的输入方式,用蠕动泵调节水流速率为2.5 mL·min-1,即达西流速为5.76 m·d-1.土柱实验包括3个阶段:在第1阶段先通入20 PV(多孔介质的孔隙体积)的背景液来平衡土柱的物理化学环境,然后依次加入3 PV的胶体悬液,5 PV的背景液;第2阶段通入6 PV的超纯水;第3阶段再通入11 PV pH为10的超纯水.实验期间用部分收集器每5 min收集一次流出液并测量流出液中胶体的含量,绘制穿透曲线.实验结束后反向收集土柱中残留的液体,并测量胶体的含量.土柱实验按照玻璃珠酸洗和未酸洗、背景液(氯化钠溶液)离子强度分别为0.001、0.01、0.05 mol·L-1共设6组,每组设置2个平行.之后将每一阶段胶体流出液的浓度进行积分,除去总的胶体输入量即得每一阶段的胶体恢复率R1、R2、R3,总的恢复率用RT表示,则RT=R1+R2+R3.另外,将反向流出液中胶体的量除以总的胶体输入量,记作RS.
2.3 扩展DLVO计算用马尔文Zetasizer Nano ZS90仪器测量不同离子强度下胶体和玻璃珠表面的Zeta电位,玻璃珠表面Zeta电位的测定方法采用相关文献中的方法(Shen et al., 2012; Tufenkji et al., 2004),并计算胶体与玻璃珠之间的相互作用能.由于DLVO理论存在一定的局限性,本文采用扩展DLVO理论,即考虑双电层力、范德华力及生斥力3个作用力.双电层力采用Hogg等(1966)提出的球-平面模型:
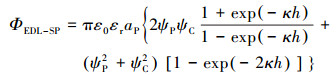
|
(1) |
式中,ε0表示真空下的介电常数,取值为8.845×10-12 C·V-1·m-1;εr表示水的相对电容率,25 ℃时为78.55;aP表示胶体的平均半径(m);h表示胶体-介质之间间隔的距离(m);ΨPΨC表示生物胶体和土壤基质的电势(V),常用Zeta电位来表示;k表示德拜休克尔长度倒数(Debye-Huckel Reciprocal Length),表达式如式(2) 所示.
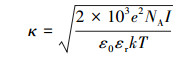
|
(2) |
式中,k表示玻尔兹曼常数,取值为1.38×10-23J·K-1;T表示绝对温度(K);NA表示阿伏伽德罗常数,取值为6.022×1023·mol-1;e表示电子的电荷,取值为1.6×10-19 C;I为离子强度(mol·L-1).
范德华力采用Gregory等(1981)提出的方程,具体见式(3);生斥力的表达式见式(4)(Ruckenstein et al., 1976).
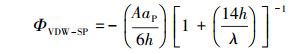
|
(3) |
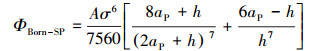
|
(4) |
式中,A表示哈梅克常数,取值为1×10-20 J;λ表示特征波长(通常采用100 nm);σ表示碰撞参数,取0.5 nm.
胶体与多孔介质间的相互作用力即为上述3个力之和,根据扩展DLVO作用力计算出每一组的初级势阱深度、排斥势垒高度和次级势阱深度.
3 结果与讨论(Results and discussion) 3.1 Zeta电位及胶体与玻璃珠之间的相互作用能不同环境下胶体与玻璃珠表面的Zeta电位见表 1.发现在不同环境下,胶体与玻璃珠表面的Zeta电位均为负值,这是由于胶体和玻璃珠的等电点较低,当环境pH大于其等电点时,胶体和玻璃珠表面便会携带负电荷.而随着溶液离子强度的增加,胶体和玻璃珠表面的Zeta电位也逐渐增加,这是由于离子强度的增加导致胶体和玻璃珠表面双电层的厚度降低造成的(马雪姣等,2007).而通过对比酸洗组和未酸洗组中玻璃珠表面Zeta电位发现,在相同离子强度下,经过酸洗的玻璃珠表面Zeta电位均有了一定程度的下降,即表面的负电荷更多了.说明经过酸洗处理后,玻璃珠表面一些带正电荷的化学物质被去除掉,从而降低了Zeta电位.
| 表 1 胶体与玻璃珠的Zeta电位及相互作用能 Table 1 Electrokinetic properties of colloids and glass beads as well as the calculated DLVO interaction energy |
根据扩展DLVO理论,用测得的Zeta电位计算不同环境下玻璃珠与胶体的相互作用能,结果如图 1所示.图中横坐标表示胶体与玻璃珠之间的距离,纵坐标表示胶体与玻璃珠之间的相互作用能,当作用能为正值时表示排斥力,而当作用能为负值时表示引力.从图 1可以发现,当溶液的离子强度(IS)为0.001和0.01 mol·L-1时,玻璃珠与胶体之间存在明显的排斥势垒,此时吸附环境为不利吸附;而当溶液离子强度为0.05 mol·L-1时,并不存在排斥势垒,而仅仅存在初级势阱,此时的溶液环境称之为有利吸附.为了便于精确地比较不同环境下的相互作用,将不同环境下的初级势阱、排斥势垒和次级势阱计算出并统计于表 1.发现不利环境下,离子强度越高,排斥势垒越高,次级势阱越深.而通过比较酸洗组和未酸洗组发现,相同离子强度下,酸洗组的排斥势垒更高,显然胶体的吸附环境更加不利.
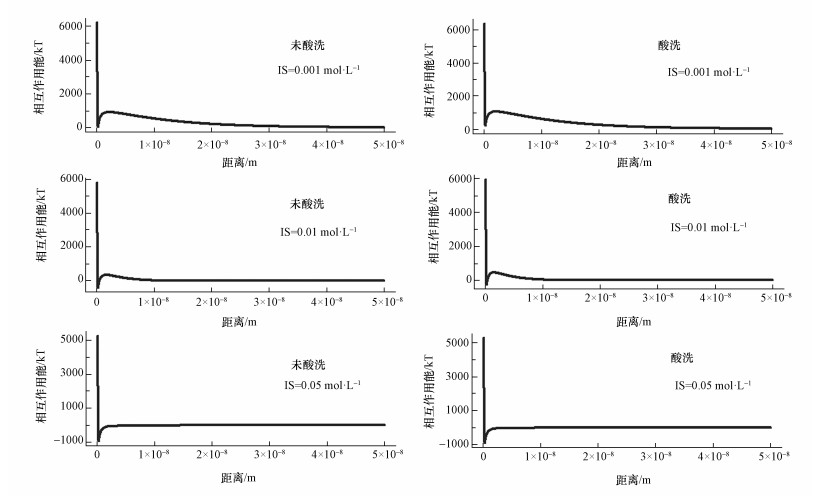 |
| 图 1 不同环境下胶体与玻璃珠的相互作用能 Fig. 1 Interaction energy between colloid and glass beads under different conditions |
按照玻璃珠的酸洗与否,将实验的6组数据分2组展示于图 2中,并将每一阶段胶体的恢复率统计于表 2中.从未酸洗组和酸洗组的实验结果中可以发现一些相似的规律.在第1阶段,溶液的离子强度越低,流出液的浓度越高,即表明胶体的吸附能力越差,这与表 1中排斥势垒大是相符的;并且在第1阶段的平衡阶段,仍然有一个非常明显的增加趋势,通常认为这是由blocking现象造成的,即吸附位点是有限的,因此,吸附速率会随着吸附过程逐渐降低(Molnar et al., 2015).在第2阶段,加了超纯水以后,由于离子强度进一步降低,胶体与多孔介质之间的排斥势垒更大,且次级势阱几乎消失,因此,可以使吸附在次级势阱中的胶体解吸下来(Bradford et al., 2015).由图 2可知,溶液离子强度为0.01 mol·L-1时流出液中胶体浓度最高,而离子强度为0.05 mol·L-1时几乎没有胶体.从表 2中可以更清楚地发现,离子强度为0.01 mol·L-1时两组实验在第2阶段恢复率分别达到了0.07、0.08,而离子强度为0.05 mmol·L-1时流出液中胶体浓度几乎为0.这是由于0.01 mol·L-1环境下的次级势阱较深,次级势阱中吸附了较多的胶体,而0.05 mol·L-1环境下并不存在次级势阱,因而也不会有胶体解吸下来.在第3阶段,仍然有大量的胶体释放出来,这很显然是受到水环境pH的影响造成的.从表 2中发现,这一阶段流出液中胶体的浓度与离子强度并未有明显的关系.从总恢复率的统计结果来看,离子强度越低恢复率则越大.
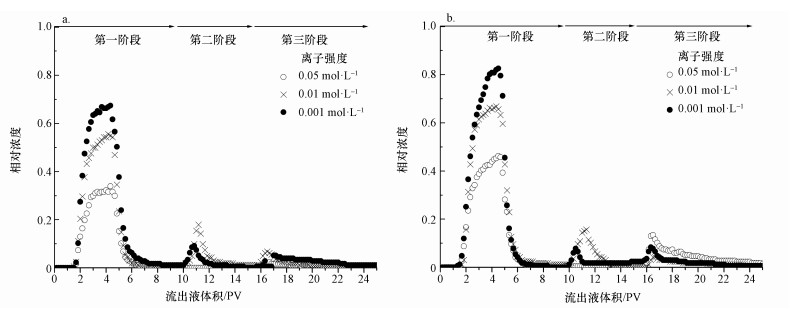 |
| 图 2 胶体在酸洗(a)和未酸洗(b)玻璃珠中的穿透曲线 Fig. 2 Breakthrough curves for colloids in acid treated(a) and untreated(b) glass beads |
| 表 2 不同环境下穿透曲线的胶体恢复率 Table 2 Recovery of colloids under different conditions |
通过横向对比酸洗组和未酸洗组的穿透曲线可以发现,在3种不同离子强度下,酸洗组在第1阶段的流出液浓度均明显大于未酸洗组,而且在不利环境下这种区别尤其明显.这是由于玻璃珠表面存在一些化学杂质,如金属氧化物、有机物等,这些杂质的表面会产生正电荷,导致不利环境下产生有利的吸附位点,大大地提高了胶体的吸附能力.酸洗去除化学杂质,从而降低了玻璃珠的吸附能力.而在有利环境下,这些化学杂质的存在与否并不会对胶体的吸附环境产生质的变化,但依然提高了胶体的吸附能力.根据胶体过滤理论,描述胶体吸附能力有2个变量:η0和α,前者为单一拦截效率,即表示胶体与多孔介质表面发生接触的可能性大小;后者表示碰撞效率,表示胶体与多孔介质表面接触后发生吸附的可能性大小.显然,在有利环境下,α=1.因此,当化学杂质吸附在多孔介质表面后,可能产生了更大的引力,从而提高了单一拦截效率(即η0),滞留了更多的胶体.但总的来说不论有利环境还是不利环境,酸洗均会降低胶体在多孔介质表面的吸附能力.
从表 2中可以发现,在第2阶段化学杂质并没有对流出液中胶体浓度有太大的影响,也就是说化学杂质对胶体在次级势阱中的吸附几乎没有影响.然而根据表 1的计算结果酸洗会使次级势阱变得更浅,与实验结果并不相符.这可能是由以下2个原因造成的:① 次级势阱非常浅,酸洗组与未酸洗组差异不大,因而实验结果并不明显;② 在计算DLVO作用能的过程中,通常带入的是表面的平均Zeta电位,而事实上多孔介质表面的Zeta电位是存在差异的,多孔介质表面携带带正电荷的化学杂质后,尽管会提高多孔介质的表面电荷,其作用是会提供有利的吸附位点,对其他不利吸附位点并不会产生影响.这与Duffadar等(2007)的计算结果相一致,Duffadar等通过计算考虑了化学异质性在内的DLVO作用能发现,化学杂质的存在有利于降低排斥势垒从而有利于胶体在初级势阱中的吸附.对于未酸洗组和酸洗组,胶体在次级势阱中的吸附并无明显差异,因此, 可以认为这种吸附的差异主要体现在胶体在初级势阱中的吸附.酸洗过的多孔介质会明显降低胶体的吸附能力,而且主要是降低了胶体在初级势阱中的吸附能力.
3.3 pH和化学异质性的关系为了消除表面化学杂质对胶体迁移的影响,研究人员常常采用提高背景液的pH来削弱化学异质性的影响(Shen et al., 2011; Tufenkji et al., 2005).这是由于在高pH环境下,这些化学杂质的表面电荷会由正电荷转变为负电荷,可以削弱化学杂质的影响.从图 2中可以发现,当用pH=10的超纯水来进行洗脱实验时,未酸洗组和酸洗组均有大量的胶体释放出来.对于未酸洗组,可以认为这部分胶体是吸附在多孔介质表面的化学杂质上,但这却并不能解释酸洗组中依然有大量的胶体解吸出来.从表 2中的恢复率来看,在不利环境下,酸洗与否没有产生明显的差异,但在有利环境下,酸洗组的R1要远高于未酸洗组.Johnson等(2010)曾指出经过酸洗过的多孔介质并不能完全去除化学杂质,这就意味着即使是酸洗组也可能有部分胶体释放出来,但酸洗组与未酸洗组并没有明显的差别说明仍存在其他机理使胶体解吸下来.例如,有可能高pH环境会导致胶体从初级势阱中解吸下来.有学者也曾多次研究过溶液化学环境变化后胶体的解吸行为,但几乎都是基于溶液离子强度(Torkzaban et al., 2015)和离子种类(Shen et al., 2012b)的改变,很少用高pH溶液来研究胶体的解吸行为.Torkzaban等(2016)也曾做过类似的实验,他采用超纯石英砂作为多孔介质,将pH=10的超纯水替换为pH=5.8的超纯水后,也有大量的胶体释放出来,但也不存在明显规律.当溶液的pH始终维持在较高的环境下时,虽然可以削弱化学异质性的影响,但当采用高pH的溶液代替低pH溶液对土柱进行洗脱时,这时候化学杂质对实验结果的影响却并不像所认为的那样.因此,关于高pH环境与化学异质性的关系需要进一步研究.
3.4 沥滤的重要性当依靠重力收集反向流出液后,测量胶体浓度后计算得出的恢复率(用RS表示)也统计于表 2中.可以看出,不管是酸洗还是未酸洗及在各种离子强度下,反向流出液中胶体的浓度差异并不大,但却均有明显的胶体流出.RS在0.08~0.1的范围内,这部分滞留在土柱中的胶体是由沥滤作用造成的,由此可以看出,沥滤在整个实验过程中具有重要的作用.
沥滤被认为是由于胶体颗粒太大而被卡在孔隙喉道中的一种现象.长期以来,人们一直通过研究胶体平均粒径与多孔介质平均粒径之比(dp/dm)来判断沥滤作用何时显著,从早期的单纯计算到后来的实验结果表明,人们大大低估了沥滤在胶体迁移过程中所起到的重要作用.例如,Herzig等(1970)通过计算认为当dp/dm>0.05时沥滤作用显著,而后来Bradford等(2005)通过实验发现当dp/dm>0.005时,沥滤作用效果显著.然而本实验中的dp/dm约为0.002,远低于Bradford的实验值,可见沥滤作用依然被低估.由于沥滤有其特殊性,很难对沥滤作用进行定量的计算.而目前对沥滤过程进行的研究均是建立在很多假设的基础上,例如,将实验环境设定成不利环境,从而排除掉胶体在初级势阱中的吸附(Shen et al., 2008),而这些假设在很多实验中被证明是不成立的.实验反向洗脱胶体也是研究沥滤中常用的一种手段,实验过程中水化学环境并没有发生改变,因此,不可能造成吸附在初级势阱中的胶体解吸下来.但反向流也有其缺点,那就是因沥滤作用而滞留的胶体有可能再次被滞留在多孔介质中.因此,如何定量的计算沥滤作用依旧是困扰研究人员的一个问题,但很明显的是沥滤作用至今依旧被人们所低估(Díaz et al., 2010).
4 结论(Conclusions)本实验通过对比胶体在酸洗过和未酸洗过的玻璃珠中的迁移行为来判断化学异质性对胶体在饱和多孔介质中迁移行为的影响,并且结合扩展DLVO理论来进行阐述.实验结果表明,不论在有利条件还是不利条件下,多孔介质表面的化学杂质均会提高胶体在初级势阱中的吸附能力,而在不利环境下,这种现象更加明显.高pH溶液依然可以进一步解析下吸附在多孔介质表面的胶体,这部分胶体很可能来源于初级势阱.尽管本实验中的dp/dm已经小于其他参考文献中认为沥滤发生的临界值,但沥滤作用依然在本实验中扮演着不可忽略的角色,因此,沥滤作用依旧是亟待解决的问题.本研究对化学杂质对胶体迁移的影响有了进一步的认识,可为研究胶体的迁移研究提供实验依据.
Bradford S A, Simunek J, Bettahar M, et al. 2005. Straining of colloids at textural interfaces[J]. Water Resources Research, 41(10): 3053–3057.
|
Bradford S A, Wang Y, Torkzaban S, et al. 2015. Modeling the release of E.coli D21g with transients in water content[J]. Water Resources Research, 51(5): 3303–3316.
DOI:10.1002/2014WR016566
|
Díaz J, Manuel R, Díaz M. 2010. Straining phenomena in bacteria transport through natural porous media[J]. Environmental Science and Pollution Research, 17(2): 400–409.
DOI:10.1007/s11356-009-0160-2
|
Duffadar R D, Davis J M. 2007. Interaction of micrometer-scale particles with nanotextured surfaces in shear flow[J]. Journal of Colloid And Interface Science, 308(1): 20–29.
DOI:10.1016/j.jcis.2006.12.068
|
Einat M, Noam W, Yoseph Y, et al. 2011. Colloid transport in porous media:impact of hyper-saline solutions[J]. Water Research, 45(11): 3521–3532.
DOI:10.1016/j.watres.2011.04.021
|
Foppen J W, Manon H, Schijven J. 2007. Transport of Escherichia coli in saturated porous media:Dual mode deposition and intra-population heterogeneity[J]. Water Research, 41(8): 1743–1753.
DOI:10.1016/j.watres.2006.12.041
|
Foppen J W, Schijven J. 2005. Transport of E.coli in columns of geochemically heterogeneous sediment[J]. Water Research, 39(13): 3082–3088.
DOI:10.1016/j.watres.2005.05.023
|
Gregory J. 1981. Approximate expressions for retarded van der Waals interaction[J]. Journal of Colloid and Interface Science, 83(1): 138–145.
DOI:10.1016/0021-9797(81)90018-7
|
Herzig J P, Leclerc D M, Goff P L. 1970. Flow of suspensions through porous media-application to deep filtration[J]. Industrial & Engineering Chemistry, 62(5): 8–35.
|
Hogg R, Healy T W, Fuerstenau D W. 1966. Mutual coagulation of colloidal dispersions[J]. Transactions of the Faraday Society, 62: 1638–1651.
DOI:10.1039/tf9666201638
|
Johnson W P, Pazmino E, Ma H. 2010. Direct observations of colloid retention in granular media in the presence of energy barriers, and implications for inferred mechanisms from indirect observations[J]. Water Research, 44(4): 1158–1169.
DOI:10.1016/j.watres.2009.12.014
|
Kozlova N, Santore M M. 2006. Manipulation of micrometer-scale adhesion by tuning nanometer-scale surface features[J]. Langmuir, 22(3): 1135–1142.
DOI:10.1021/la0515221
|
Li X, Scheibe T D, Johnson W P. 2004. Apparent decreases in colloid deposition rate coefficients with distance of transport under unfavorable deposition conditions:A general phenomenon[J]. Environmental Science & Technology, 38(21): 5616–5625.
|
马雪姣, 金妍, 黄元仿, 等. 2007. 冠状病毒IBV和噬菌体MS2在饱和多孔介质中的运移规律[J]. 中国环境科学, 2007, 27(2): 255–259.
|
Molnar I L, Johnson W P, Gerhard J I, et al. 2015. Predicting colloid transport through saturated porous media:A critical review[J]. Water Resources Research, 51(9): 6804–6845.
DOI:10.1002/2015WR017318
|
Ruckenstein E, Prieve D C. 1976. Adsorption and desorption of particles and their chromatographic separation[J]. Aiche Journal, 22(2): 276–283.
DOI:10.1002/(ISSN)1547-5905
|
Shen C, Huang Y, Li B, et al. 2008. Effects of solution chemistry on straining of colloids in porous media under unfavorable conditions[J]. Water Resources Research, 44(5): 335–342.
|
Shen C, Lazouskaya V, Zhang H, et al. 2013. Influence of surface chemical heterogeneity on attachment and detachment of microparticles[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 433: 14–29.
DOI:10.1016/j.colsurfa.2013.04.048
|
Shen C, Li B, Wang C, et al. 2011. Surface roughness effect on deposition of nano-and micro-sized colloids in saturated columns at different solution ionic strengths[J]. Vadose Zone Journal, 10(3): 1071–1081.
DOI:10.2136/vzj2011.0011
|
Shen C, Wang L, Li B, et al. 2012a. Role of surface roughness in chemical detachment of colloids deposited at primary energy minima[J]. Vadose Zone Journal, 11(1): 59–75.
|
Shen C, Lazouskaya V, Jin Y, et al. 2012b. Coupled factors influencing detachment of nano-and micro-sized particles from primary minima[J]. Journal of Contaminant Hydrology, 134: 1–11.
|
Torkzaban S, Bradford S A. 2016. Critical role of surface roughness on colloid retention and release in porous media[J]. Water Research, 88: 274–284.
DOI:10.1016/j.watres.2015.10.022
|
Torkzaban S, Bradford S A, Vanderzalm J L, et al. 2015. Colloid release and clogging in porous media:Effects of solution ionic strength and flow velocity[J]. Journal of Contaminant Hydrology, 181: 161–171.
DOI:10.1016/j.jconhyd.2015.06.005
|
Tufenkji N, Elimelech M. 2004. Deviation from the classical colloid filtration theory in the presence of repulsive DLVO interactions[J]. Langmuir, 20(25): 10818–10828.
DOI:10.1021/la0486638
|
Tufenkji N, Elimelech M. 2005. Breakdown of colloid filtration theory:Role of the secondary energy minimum and surface charge heterogeneities[J]. Langmuir, 21(3): 841–852.
DOI:10.1021/la048102g
|
Weiss W J, Bouwer E J, Aboytes R, et al. 2005. Riverbank filtration for control of microorganisms:results from field monitoring[J]. Water Research, 39(10): 1990–2001.
DOI:10.1016/j.watres.2005.03.018
|
张文静, 周晶晶, 刘丹, 等. 2016. 胶体在地下水中的环境行为特征及其研究方法探讨[J]. 水科学进展, 2016, 27(4): 629–638.
|
Zhang W X. 2003. Nanoscale iron particles for environmental remediation:An overview[J]. Journal of Nanoparticle Research, 5(3/4): 323–332.
DOI:10.1023/A:1025520116015
|
 2017, Vol. 37
2017, Vol. 37


