2. 华南理工大学生物科学与工程学院, 广州 510006;
3. 广东药科大学生命科学与生物制药学院, 广州 510006
2. School of Bioscience and Bioengineering, South China University of Technology, Guangzhou 510006;
3. School of Biosciences and Biopharmaceutics, Guangdong Pharmaceutical University, Guangzhou 510006
焦化废水是煤制焦炭、煤气净化及焦化产品回收过程中产生的高浓度有机废水.不同地区、规模、工艺的焦化厂所产生的焦化废水水量及污染物组成含量有着一定的差异,同时受到炼焦煤的质量、炼焦工艺及操作条件、化工生产车间设备构造、焦化废水处理厂的工艺与运行管理等因素影响.我国焦化废水不仅排放量大,成分也极其复杂,而且污染物浓度变化范围大.废水中除有氨氮、氰化物、硫化物、硫氰化物等高毒性无机污染物外,还有大量的有机污染物,主要为苯酚类物质及其衍生物、喹啉类及其衍生物(Lu et al., 2009),还含有油、胺、萘、吡啶、蒽等含氮、氧、硫杂环化合物及多环芳烃(PAHs)等多种有机组分(Wang et al., 2002; Zhang et al., 2012).韦朝海等(2011)统计了国内38家典型焦化企业废水的主要水质指标,指出全国各地焦化废水COD普遍在4000~8000 mg·L-1的范围内,其中,苯酚、硫化物、氰化物的普遍浓度范围及pH分别为500~1300 mg·L-1、50~200 mg·L-1、5~50 mg·L-1、9.5~10.5,个别地区的企业产生的焦化废水水质变化相对较大.
目前,国内外钢铁企业产生的焦化废水所采用的处理工艺一般为A/O、A2/O及其变型工艺等(Min et al., 1998; Yang et al., 2001; Wang et al., 2002; Park et al., 2008; Kim et al., 2008)生物处理工艺,其中,国内52家典型的焦化废水处理站的生物工艺主要分为6种:AO(7个)、AOO(6个)、AAO(17个)、AAOO(8个)、OAO(11个)、OHO(3个)(范丹, 2016),工艺设计主要围绕COD的去除及氨氮的硝化-反硝化过程.因厌氧生物技术具有低污泥产量、低能耗和能源可回收等优点(Mccarty et al., 1986),国内外大部分钢铁企业的焦化废水处理工艺都包含厌氧A单元技术.然而,大量工程实践和研究报道显示,厌氧A单元技术对焦化废水的处理效果甚微,均无法实现产甲烷的目标.Zhao等(2014)对韶钢二期工程A/O/H/O焦化废水处理工艺进行研究,指出在第一个厌氧单元A进水COD为1530 mg·L-1,A出水COD为1390 mg·L-1;Sahariah等(2015)采用A1/A2/O生物流化床对焦化废水进行降解,其A1厌氧反应器对苯酚和COD的去除率分别仅为3%和2%左右;Wei等(2012)的研究指出,焦化废水厌氧进水COD为1676 mg·L-1,经过12 h的水力停留时间后COD的去除率只有6.92%.另外,有研究对焦化废水进行厌氧条件下产甲烷活性抑制实验时发现,产酸阶段已被抑制(任源等, 2007),即使一些工程中厌氧段COD有20%~30%的去除率,现有工程所暴露的厌氧段COD去除率有相当一部分是由清水稀释作用及污泥对有机物的吸附作用所致.Zhu等(2016)对工程上在厌氧处理单元中微生物的分析研究发现,污泥中没有产甲烷菌存在.此外,硫氰化物、苯酚、硫化物和氰化物被报道为焦化废水的特征污染物(张万辉等, 2015),占总COD的70%~80%,其中,苯酚为贡献最大的有机污染物,约占焦化废水总COD的60%~70%.目前,虽然有较多研究报道了关于氨氮、硫化物、氰化物和金属离子等污染物对诸如葡萄糖、VFAs等有机物厌氧消化的影响(Hilton et al., 1988; Chen et al., 2008; Yenigün et al., 2013; Gupta et al., 2016).但对于含有大量毒性物质的焦化废水而言,其抑制厌氧生物降解的因素尚不明确.
针对厌氧降解焦化废水中有机物效果甚微,抑制因素及其机制不明确的问题,本研究以浓度梯度稀释的焦化废水为研究对象,以苯酚、COD和TOC的浓度变化为表征,考察焦化废水抑制厌氧生物降解的浓度阈值;通过COD和苯酚的去除率探讨硫氰化物、苯酚、硫化物和氰化物的浓度对焦化废水厌氧降解效率的影响,并尝试采用分级的评价方法间接表达焦化废水的复合毒性作用;另外,通过外加碳源的方法改变焦化废水的碳源结构,从微生物对基质利用的角度分析焦化废水抑制厌氧生物降解的因素;反应过程中还通过测定气体产量及组成的变化,从不同产气结构推断受抑制的微生物群体.
2 材料与方法(Materials and methods) 2.1 焦化废水原水水质及污泥来源焦化废水原水水样取自于广东韶钢焦化废水处理工程,其主要水质指标如表 1所示.已有大量的工程实践证明,厌氧焦化污泥的产甲烷活性已受到严重抑制,不便于观察焦化废水中毒性物质对厌氧污泥的抑制现象.因此,本研究为探究在焦化废水中各毒性物质浓度对厌氧污泥产甲烷的影响,实验选用的污泥取自广州市沥滘污水处理厂水处理系统的二沉池,并接种到本实验室的厌氧双层玻璃反应釜(5 L改进型)中,利用甲醇为有机碳源进行活化,并利用纯苯酚作为有机碳源对污泥进行驯化.通过低温恒温槽控制反应体系温度为(35.0±0.5) ℃,厌氧反应器的搅拌速度为60 r·min-1,控制pH为6.8~7.2.实验前,厌氧反应釜中以苯酚作为碳源已经稳定运行270 d,污泥负荷(Q)和产甲烷活性(SMA)分别为30.17 mg·g-1·d-1(以每g MLSS中的苯酚量(mg)计)和4.01 mL·g-1·d-1 (以每g VSS产生的CH4量(mL)计).以反应体系容积计算,每升分别加入10 mL维生素和无机盐营养液(胡纪萃等, 2003).
| 表 1 广东韶钢焦化废水原水的主要水质指标 Table 1 The major parameters of raw coking wastewater from Shaogang in Guangdong |
间歇式厌氧反应装置如图 1所示.厌氧活性污泥由本实验室长期运行的厌氧生物反应器中驯化得到,反应器有效容积为500 mL,反应体系中污泥含量(MLSS)约为5000 mg·L-1.反应前采用高纯氮气(99.99%)进行曝气,使整个装置充满氮气以保证厌氧环境.实验在(35.0±0.5) ℃恒温水浴锅和转子转速为60 r·min-1的条件下进行;三通阀用于取样时保持反应装置整体气压平衡;橡胶塞上附加硅酮垫片对厌氧盐水瓶加强密封;体系中产生的气体通过导管于装满饱和NaCl溶液的上嘴滤瓶进行收集,排出的液体收集于戴塞量筒中,液体体积即为收集到的气体总产量(CO2、H2和CH4),组分占比采用气相色谱定量分析.
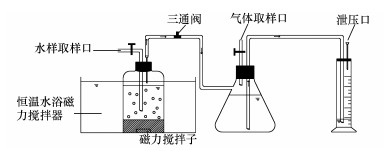 |
| 图 1 实验室规模间歇式厌氧反应装置示意图 Fig. 1 The laboratory-scale batch anaerobic reactor |
分析样品预处理:先取一定量的水样,在转速为5000 r·min-1下离心10 min后,从上清液中取5 mL水样稀释成50 mL,再经过0.45 μm的水系滤头进行过滤.
COD按照标准《水质化学需氧量的测定快速消解分光光度法》(HJ/T 399-2007),采用哈希DRB200快速消解仪进行消解后测定;TOC采用总有机碳检测仪(日本岛津TOC-V CPN)测定.
水样中的苯酚浓度用高效液相色谱(日本岛津HPLC-20A,紫外检测器,Eclipse PAH C18色谱柱,4.6 mm×250 mm, 5 μm)进行定量分析.预处理后的样品再采用0.22 μm的水系滤头进行过滤.检测条件:柱箱温度35 ℃;流动相A为甲醇(色谱纯),流动相B为超纯水,流动相A与B体积比为55:45;流速1.0 mL·min-1,进样体积20 μL;检测波长为270 nm.
反应体系的顶空气体,如CO2、H2和CH4等气体,用注射器从上嘴滤瓶收集的顶空气体中抽取,然后用气相色谱分析仪(Agilent-7820A)测定,采用热导检测器(TCD),柱子为TDX-01填充柱(2.4 m×3.2 mm),气体进样体积为1 mL,载气(N2)流速为25 mL·min-1,尾吹气(N2)流速为3 mL·min-1.柱温、检测器和进样口温度分别为100、200和100 ℃.
2.4 梯度稀释焦化废水的厌氧降解先量取一定量的焦化废水原水对其进行预处理,具体操作为:采用2 mol·L-1的盐酸将水样的pH调节为7左右,对水样采用高纯氮气(99.99%)进行曝气排氧10 min.以宏观指标COD为稀释对象设置6个稀释梯度,将焦化废水原水分别稀释至(1200±100)、(1500±100)、(1800±100)、(2100±100)、(2400±100)、(2700±100) mg·L-1.加入2.1节中的污泥,控制污泥浓度MLSS为5000 mg·L-1左右,反应体系稀释为500 mL,反应周期为30 d.根据2.3节中的方法分析各实验组中COD、TOC和苯酚浓度的变化,用以得出解除抑制厌氧生物降解的焦化废水浓度阈值.实验设置3个平行样,实验结果取平均值.
2.5 毒性物质的单抑制浓度分析根据2.4节的实验结果,选取可对焦化废水进行厌氧生物降解的浓度阈值来稀释焦化废水(即解除抑制的拐点浓度),水样预处理同2.4节,稀释成500 mL后分别加入焦化废水中毒性物质占比较大的几类代表性物质(硫氰化物、苯酚、硫化物、氰化物)进行批量间歇实验,反应周期为18 d.通过2.3节的分析方法测定各实验组中COD和苯酚的浓度变化,以分别探究这些毒性物质的浓度对厌氧生物降解焦化废水的影响.据统计(潘霞霞等, 2009;韦朝海等, 2011),焦化废水中硫氰化物、苯酚、硫化物、氰化物的浓度分别为200~1000、90~1300、17.5~200、5~50 mg·L-1,实验设计毒性物质浓度将根据其在实际焦化废水中出现频率较高的浓度范围进行选取,设置24个反应器(其中4个为对照组,对照组只稀释不添加任何毒性物质,实验结果取平均值),毒性物质投加量如表 2所示.
| 表 2 各反应器中毒性物质的设计浓度 Table 2 The design concentration of toxicant in each reactor |
根据2.4节的实验结果,选取无法对焦化废水进行厌氧生物降解的浓度阈值来稀释焦化废水(即无法解除抑制的拐点浓度),其水样预处理同2.4节,稀释成500 mL后加入与稀释后焦化废水等COD的不同有机碳源.实验设计选用工业上较为常用的3种有机碳源:葡萄糖、乙酸钠和甲醇,将其分别加至各反应器中,反应周期为18 d,根据2.3节中的方法分析各实验组中COD值和苯酚浓度的变化及气体的产量变化,以此对比不同简单有机物在焦化废水中厌氧生物降解的性能,以推断焦化废水不能厌氧生物降解的微生物因素.实验设置3个平行样,实验结果取平均值.
3 实验结果与讨论(Results and discussion) 3.1 不同浓度焦化废水的厌氧降解效率对比焦化废水属于高浓度有机废水,理论上应该先进行厌氧生物处理降低负荷,再进行好氧生物处理.然而,由于焦化废水原水对微生物的毒性抑制作用,高浓度的焦化废水难以实现厌氧生物降解.厌氧单元效率低将导致回流比的增大和水力停留时间的延长(Li et al., 2005),因而工程上通常采用大量的清水进行稀释以降低毒性物质的负荷,但仍然没有高效厌氧产CH4的效果.针对这个实际问题,为确定焦化废水抑制厌氧生物降解的浓度阈值,根据2.4节中的实验设计参数对焦化废水原水进行梯度稀释,以COD、TOC和苯酚浓度的变化直接表达焦化废水中毒性物质的复合抑制效应,实验结果如图 2所示.
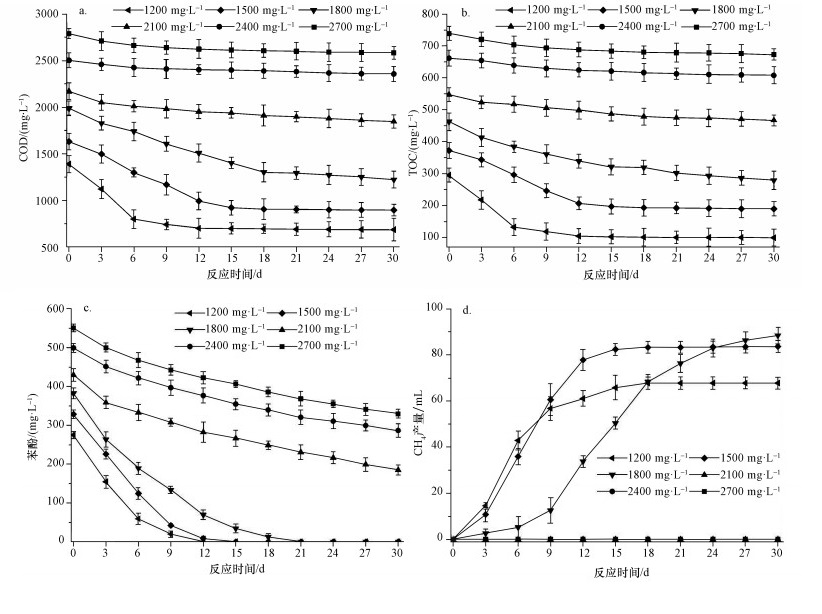 |
| 图 2 不同浓度焦化废水的厌氧降解效率及甲烷产量(a.COD,b.TOC,c.苯酚,d.甲烷产量) Fig. 2 The performance and methane production of coking wastewater at various concentrations by anaerobic biodegradation(a.COD, b.TOC, c.phenol, d.CH4 yield) |
从图 2中可以看出,当焦化废水被稀释到COD为1200和1500 mg·L-1时,反应体系中的苯酚在12 d以内被完全降解并生成大量CH4气体,且COD去除率分别为49.49%和39.15%,污泥负荷分别为5.33和6.09 mg·g-1·d-1.当焦化废水浓度提升到1800 mg·L-1时,厌氧污泥的活性开始出现抑制现象,且在30 d内COD去除率和苯酚负荷分别下降至31.49%和4.11 mg·g-1·d-1,产甲烷的速率下降.当焦化废水浓度为2100 mg·L-1时,其COD和TOC的浓度只有少许下降,可能部分有机物被微生物同化利用或降解成CO2气体,但由于产气量低于仪器检测限,且没有产生体积差,故认为此浓度水平属于抑制性浓度拐点.当焦化废水浓度大于2400 mg·L-1时,体系中苯酚浓度的下降却并没有伴随COD和TOC浓度的明显变化,说明苯酚被水解为中间产物且无法被进一步降解,体系中产甲烷菌等微生物的活性受到抑制且无CH4气体产生.由此可得,焦化废水原水一般需要2倍或以上的清水稀释,才能达到可对其进行厌氧生物降解的浓度水平.
高浓度的焦化废水无法厌氧生物降解,虽然可以通过稀释作用降低焦化废水的毒性负荷,但这将导致处理后的出水量增大.由于焦化行业的特殊性,其产生的废水需要按照零排放的要求,导致处理后的出水无法排放,且该行业用水量较少,外排水无法重复利用.同时,其外排水的风险性较大,不能作为其他行业的回用水,产生的水无处消耗,成为了焦化行业、钢铁企业的一大难题.因此,需要识别抑制焦化废水厌氧降解的关键毒性物质及浓度,分析其对厌氧微生物的抑制因素,以减少稀释水的用量.
3.2 毒性物质的单一抑制效应分析为探究焦化废水中硫氰化物、苯酚、硫化物和氰化物等物质浓度各自对厌氧降解性能的影响,根据2.4节的实验方案和3.1节的实验结果可得,选取可进行厌氧降解产CH4的焦化废水稀释浓度(1800 mg·L-1),并根据表 2中所设计的毒性物质的量投加到各反应器中,实验结果如图 3所示.
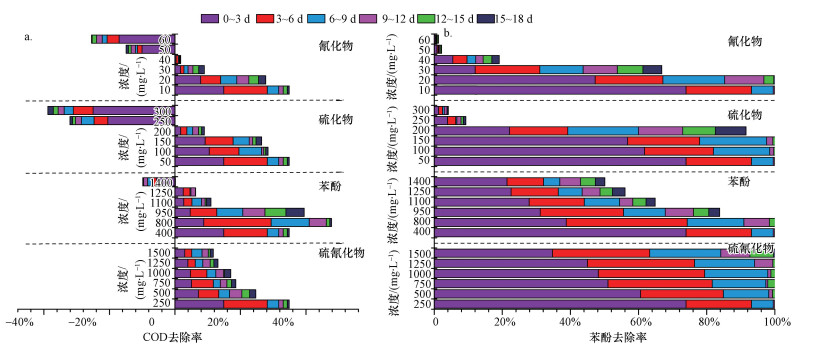 |
| 图 3 不同浓度硫氰化物、苯酚、硫化物和氰化物条件下各反应器的COD(a)和苯酚(b)厌氧降解效率 Fig. 3 The respective performance of anaerobic biodegradation in COD(a) and phenol(b) of diluted raw coking wastewater at various concentrations of SCN-, phenol, S2- and CN- |
图 3表明,随着反应体系中硫氰化物浓度的升高,其对厌氧微生物的抑制作用越来越明显.当硫氰化物浓度达到1500 mg·L-1,COD的去除率从34.89%下降至11.67%,污泥负荷由对照的8.49 mg·g-1·d-1降至5.23 mg·g-1·d-1,SMA从1.07 mL·g-1·d-1降至0.24 mL·g-1·d-1.此时,其对厌氧微生物活性的影响只起到减缓作用,但只要经过足够长的停留时间仍能保持厌氧污泥对焦化废水中COD和苯酚的去除率.由此表明,在当前硫氰化物浓度水平的焦化废水中,硫氰化物只作为一种抑菌性有毒物质而非杀菌性有毒物质.在低复合毒性的基础上,硫氰化物的单一抑制效应并不作为抑制焦化废水厌氧生物降解的主要毒性抑制因素,其在焦化废水处理过程中受到的重视程度远不如挥发酚和氰化物等.然而,硫氰化物是焦化废水中COD占比最大的无机物,不仅对水生生态环境和人类健康十分有害(Bhunia, 2000),而且对焦化废水COD、NH4+-N及色度等指标均有直接或间接的贡献(韦朝海等, 2007;潘霞霞等, 2009).
3.2.2 苯酚的抑制由于作为毒性物质的苯酚同时也作为营养物质而表现为COD,投加苯酚的实验组厌氧降解COD的规律不同于另外3种毒性物质.根据化学动力学,在没有受到抑制的时候,苯酚作为基质的浓度越高,相同时间内其去除率越高.从图 3可知,苯酚初始浓度为800 mg·L-1时,厌氧污泥没有受到明显抑制,18 d的COD去除率达到47.77%,SMA值为1.48 mL·g-1·d-1,苯酚被完全降解.虽然苯酚初始浓度为950 mg·L-1时的COD去除率比对照组高,但SMA值从1.48 mL·g-1·d-1下降至1.21 mL·g-1·d-1,此浓度水平的苯酚对厌氧污泥有轻微抑制作用.当苯酚初始浓度达到1100 mg·L-1和1250 mg·L-1,体系中COD去除率明显下降,这是由于体系中的产甲烷菌受到完全抑制,无法对苯酚的水解产物进行矿化作用,由于苯酚水解菌在高浓度苯酚的环境下仍然具有一定的活性,体系中的苯酚浓度仍然下降.然而,由于苯酚浓度高达1400 mg·L-1,超过部分厌氧微生物的耐受程度,导致该部分微生物死亡,微生物死亡后体内的有机物质溶出,从而使得水中的COD升高.随着反应时间增长,仍然具有一定活性的苯酚水解菌将苯酚的浓度降至非杀菌性水平,部分未死亡的微生物停止自溶现象,从而COD去除率的负增长趋势逐渐变得缓慢.
虽然低浓度的苯酚是一种较好的有机碳源,但其本身会引起生物体内蛋白质的变性和凝固,是一种原生质毒性物质,对厌氧微生物有着一定程度的抑制作用(Fang et al., 1997).高浓度苯酚可以使得厌氧污泥中产甲烷菌特有的辅酶F420和胞外聚合物(EPS)的含量大幅下降(马小云等, 2011).可用于保护污泥中微生物细胞的EPS含量减少,会导致污泥对毒性物质的耐受能力下降(Sheng et al., 2010),甚至死亡.虽然在实际工程的焦化废水中苯酚的浓度水平一般为600~1000 mg·L-1,处于厌氧污泥的抑菌性水平,但厌氧微生物对苯酚的适应能力较强(Fang et al., 1997),尤其是苯酚水解菌在高浓度苯酚的环境下仍然具有一定的活性.
3.2.3 硫化物的抑制图 3的实验结果表明,当硫化物浓度达到200 mg·L-1,反应器中的厌氧污泥受到明显的抑制作用,COD的去除率从34.89%下降至11.54%,SMA值从1.07 mL·g-1·d-1降至0.18 mL·g-1·d-1.当硫化物浓度达到250~300 mg·L-1时,硫化物的毒性作用从抑菌性转变为杀菌性,体系中的微生物由于受到高浓度硫化物的毒性作用而死亡,细胞体内有机质溶出导致体系中COD去除率呈负增长,苯酚水解菌的活性明显下降.
硫化物是一种对细菌生长有强抑制作用的物质,其毒性是由非离子形式即游离态(H2S)引起的,主要原因有2个:① 微生物自身带负电荷,中性的H2S分子比S2-和HS-更容易接近并穿透细菌的细胞壁,进而在细菌体内产生毒害作用(Nielsen, 1987);② S2-、HS-和H2S可使溶液中非碱性金属沉淀,影响微生物对该金属的可利用性,从而影响厌氧微生物的生长(胡纪萃等, 2003).由于体系中的温度和pH分别在35 ℃和7左右,根据硫化物在液相内的电离平衡,体系中硫化物的形态分布以H2S和HS-为主;且在35 ℃和气相分压为105 Pa的条件下,H2S在水溶液中的溶解度为0.2661 g/100 g水,可认为在适合厌氧微生物生存的水相环境中硫化物对厌氧污泥的抑制作用主要由H2S造成.适合厌氧消化体系的pH在6.5~7.5的范围内,在含有大量硫化物的焦化废水中,若需要对其进行厌氧生物降解,不仅需要投加大量的酸以调节焦化废水原水的pH,还会使其中含有的硫化物转化为H2S,进而加强了焦化废水的毒性作用.
3.2.4 氰化物的抑制图 3结果显示,当水相中氰化物浓度达到30 mg·L-1时,反应器中的污泥出现明显抑制,在反应周期内COD的去除率从对照组的34.89%下降至8.96%,苯酚的水解率下降至66.81%.当氰化物浓度提高至40 mg·L-1的浓度水平,反应器中仅有苯酚水解菌仍具有一定的活性,产甲烷菌的活性完全受到抑制,体系中COD去除率几乎为0.当氰化物浓度达到50~60 mg·L-1时,其毒性从抑菌性转变为杀菌性,该反应器中的COD去除率为负,部分微生物被杀死,其体内的有机质溶出进而导致COD升高.
焦化废水中含有的氰化物(CN-)是一类剧毒物质,CN-是典型的类卤素离子,具有很强的还原性和配合性,在焦化废水处理工程中通常表现出多重效应.氢氰酸属于一元弱酸型简单化合物,其在水溶液中仅以HCN、CN-的形式存在.氰化物与硫化物的毒性机制相似,其对微生物的毒性作用主要是由游离的HCN造成,且CN-容易与金属离子结合,进而影响微生物对金属的利用效率(Dash et al., 2009).在35 ℃和气相分压为105 Pa的条件下,根据氢氰酸与氰根离子在不同pH值时的质量分数分布规律,当pH在7左右时,水溶液中的氰化物基本以HCN的形态存在.为调节焦化废水酸度而加酸至最适合厌氧污泥生长繁殖的pH(6.5~7.5),水相中主要毒性成分将从毒性相对小的CN-转变为毒性更大的HCN,从而提升了废水的毒性作用,对微生物的活性造成更严重的影响.
3.3 复合毒性抑制作用的探讨在实际废水中,不同污染物对微生物的抑制效应体现为复合毒性作用,为了直观地表达复合抑制效应,将3.1节和3.2节的实验结果以抑制等级的形式间接表达.参考《美国药典》中细胞毒性分级标准(USP, 1990),建立了一套用于评价焦化废水复合毒性作用的分级方法,具体如下:以解除抑制的焦化废水(COD为1800 mg·L-1)18 d时的COD去除率(η1=34.89%)为基准,按式(1) 计算相对去除率(η).
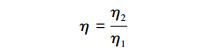
|
(1) |
式中,η2为实验组18 d时的COD去除率.根据式(1) 得出相对去除率η,各实验组的毒性抑制分级按照表 3分级标准判定,其中,无抑制定义为0级,杀菌性抑制定义为6级,抑制等级越高,抑制程度越大.将焦化废水原水的复合抑制性浓度和硫氰化物、苯酚、硫化物和氰化物等毒性物质各自的抑制效应分级列于表 4中.
| 表 3 毒性作用的分级标准 Table 3 Graded standard of toxicity effect |
| 表 4 毒性作用的抑制分级 Table 4 Inhibiting level of toxicity effect |
由3.1节和3.2节的实验结果和表 4的规律可以看出,焦化废水稀释到解除厌氧抑制的浓度水平时(1800 mg·L-1),再向其分别投加1250~1500 mg·L-1的硫氰化物、1250~1400 mg·L-1的苯酚、200~250 mg·L-1的硫化物和30~40 mg·L-1的氰化物,其单组分物质抑制要达到与复合抑制相同的抑制等级时,该物质浓度比复合抑制(以COD为2400 mg·L-1为例)时相对应的毒性物质浓度要高2~3倍.当底物浓度一定时,SMA值与相对去除率呈正相关关系;而投加苯酚的实验组基质浓度不一样,其SMA值不符合上述规律.苯酚的Ka=1.28×10-10,其与硫化氢和氢氰酸相似,都属于弱酸类物质,在适合厌氧的pH(6.5~7.5) 条件下,大部分都以分子形式存在于水相当中.根据基本的化学知识,在pH为7的厌氧条件下,它们三者相互之间并没有相互反应的趋势.由此推测,苯酚、硫化物和氰化物在该条件下的毒性作用属于加成作用.虽然硫氰化物属于低毒性物质,当其浓度高达1500 mg·L-1时,体系却仍未达到完全抑制效应.但硫氰化物为焦化废水COD值贡献最大的无机污染物,约占焦化废水原水总COD的10%~15%,硫氰化物与其他组分相互影响,在一定程度上影响着厌氧生物系统对污染物的承受能力.焦化废水中4种特征污染物在水体中体现的毒性相互加成,但硫氰化物毒性相对较低,且在焦化废水浓度水平中的苯酚可作为有机营养物质被微生物利用.故认为硫化物和氰化物是焦化废水中复合毒性的主导因素,在考虑降低焦化废水复合毒性时可优先考虑去除这两种物质,或许能够达到高浓度焦化废水厌氧降解产CH4的目标.
现阶段普遍模糊地认为前置厌氧A单元技术可用于促进废水中有机物的水解并具有降低有毒物质的毒性作用(Chakraborty et al., 2002; Wei et al., 2012).然而,本课题组调研考察的30余家焦化废水处理工程中,并没有发现一个成功厌氧产CH4的案例,甚至厌氧单元的水解效果也不明显.对于含氰含硫的焦化废水而言,厌氧水解或者厌氧消化的过程并不一定降低体系中污染物的毒性.根据3.2.3节和3.2.4节的讨论可知,在适合厌氧的pH条件下,硫化物和氰化物多以分子形式存在;再则,虽然韦朝海等(2011)研究统计中得出焦化废水中硫化物和氰化物浓度水平一般分别在50~200 mg·L-1和5~50 mg·L-1的范围内,但实际废水中仍含有大量的含硫杂环化合物及腈类化合物(张万辉等, 2012),厌氧水解作用必然导致部分含硫杂环化合物和腈类化合物发生水解反应进而使S2-和CN-被游离释放,增加水相中游离的硫化物和氰化物的含量及毒性,从而导致厌氧污泥受到的复合毒性抑制效应更加明显.因此,可认为降低焦化废水的毒性作用并不一定要采用传统的厌氧工艺,若能将焦化废水水相中的硫化物、氰化物等毒性物质作为靶向物质以分离的方式定向去除,则可大大降低焦化废水的复合毒性作用.本课题组的研究发现,可以通过FeSO4来使焦化废水中的氰化物以普鲁士蓝与滕氏蓝的化合物沉淀,降低水相中CN-的浓度(Yu et al., 2016).同时,亚铁盐也可以使硫化物形成FeS沉淀,降低焦化废水的毒性.
3.4 碳源结构改变的厌氧生物降解特性根据3.1节的实验结果,当焦化废水浓度高于2100 mg·L-1时,体系中的厌氧污泥受到抑制,无法进行厌氧产CH4反应.由于焦化废水毒性较大,导致体系中微生物活性降低,即使稀释过后也无法利用焦化废水自有的大量苯酚等有机碳源,从而无法进行厌氧降解.针对这个现象,为了更好地观察厌氧污泥中受抑制与不受抑制的菌群,且当前工程上生物进水的浓度一般被稀释到2000~2500 mg·L-1的水平,本实验选取无法对焦化废水进行厌氧产CH4的浓度水平(COD为2100 mg·L-1),根据2.6节的实验方案尝试改变焦化废水原有的碳源结构,通过对混合体系中厌氧污泥对不同碳源利用特征的研究,从微生物对碳源利用的方面来探讨高浓度焦化废水难以实现厌氧生物降解的原因.实验结果如图 4和图 5所示.
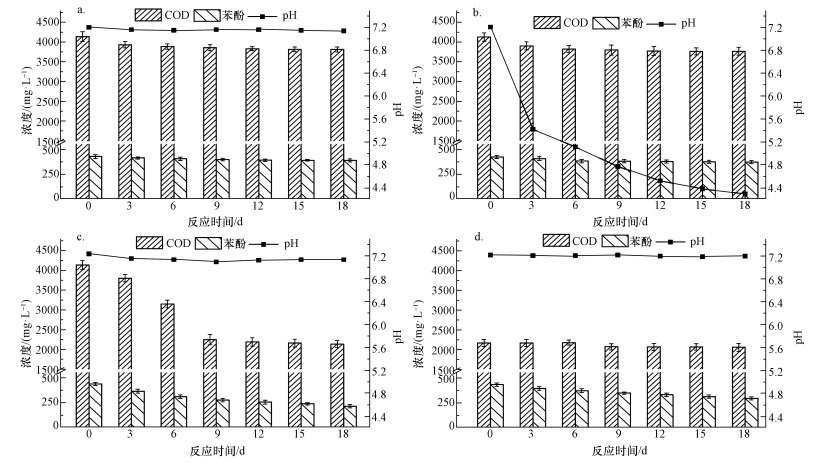 |
| 图 4 不同碳源结构的焦化废水厌氧降解特征(a.乙酸钠,b.葡萄糖,c.甲醇,d.无外加碳源) Fig. 4 The anaerobic biodegradation of coking wastewater under different external carbon sources(a.sodium acetate, b.glucose, c.methanol, d.without external carbon addition) |
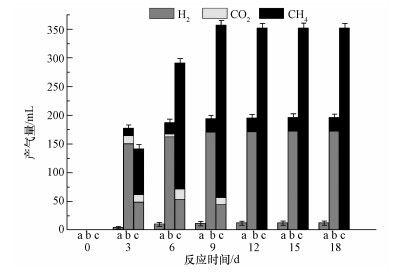 |
| 图 5 不同碳源结构的焦化废水中气体产物及产量变化规律(a.乙酸钠,b.葡萄糖,c.甲醇) Fig. 5 The variation pattern of bio-gas product and production in different carbon source structure of coking wastewater(a.sodium acetate, b.glucose, c.methanol) |
根据图 4a和图 5可知,在反应周期内,体系中的COD略有下降,外加的乙酸根无法被降解,体系中的顶空气体可以检测到少量H2且无CH4产生.COD值小幅度下降是因为污泥中乙酸互营菌(吴伟等, 2016)对乙酸的降解作用使其产生H2,但乙酸营养型产甲烷菌(Liu, 2010)的活性受到抑制,无法降解溶液中的大部分乙酸使其生成CH4.由图 4b和图 5可知,外加葡萄糖的反应器中,葡萄糖被大量水解,反应初期COD有所下降,且3 d内体系产生大量H2和少量CO2和CH4,这是因为葡萄糖自身需要先经过水解酸化产生大量的VFAs,进而降解为CO2和CH4(胡纪萃等, 2003).在这个过程中,随着葡萄糖的厌氧水解产生大量的VFAs和H2,乙酸营养型产甲烷菌受到抑制无法消耗产生的乙酸,导致VFAs大量累积且体系的pH下降至5以下,反应器中有明显的酸臭味且反应停止.在顶空气体中收集到少量的CH4气体是因为反应初期氢营养型产甲烷菌(Liu, 2010)利用CO2和H2生成CH4,体系酸败后其活性受到抑制,导致H2大量累积.由于甲醇属于极易生物降解的简单有机物,从图 4c中不难看出,外加的甲醇在9 d内被完全降解,并产生大量CH4,此后COD与对照组持平,苯酚表征的COD仍然无法被降解.图 5显示,甲醇被降解的反应过程中,不断有H2和CO2产生,但周期结束后,顶空气体只检测到大量CH4.而甲醇在厌氧条件下被降解为CH4的主要途径有2种:一是先水解为H2和CO2再被氢营养型产甲烷菌利用生成CH4;二是被甲基营养型产甲烷菌直接利用生成CH4(Lomans et al., 2002).由此推断,氢营养型产甲烷菌高效利用了甲醇水解成的H2和CO2生产CH4,其活性没有受到明显抑制.虽然向焦化废水中外加甲醇后可以得到CH4,但焦化废水自有的有机污染物并没有得到高效降解.
此外,对比图 4a、图 4c与图 4d的结果发现,由于投加了合适的碳源(甲醇)通过共基质作用(Veeresh et al., 2005),在18 d的反应时间里,外加甲醇的反应器中苯酚水解速率比对照组快18.95%.投加不合适的碳源(乙酸钠)作为共基质,反应器中苯酚浓度反而没有下降,这是因为乙酸是苯酚厌氧消化过程中的重要代谢产物(Evans et al., 1988; Karlsson et al., 1999);从化学动力学角度可以看出,外加乙酸钠导致体系中乙酸根大量增加,累积的乙酸根造成基质抑制作用,限制了苯酚的水解.当向焦化废水中投加葡萄糖作为共基质,则发现得到大量的H2和少量CH4,且累积了大量的VFAs.假若调节葡萄糖的量可以适当改善焦化废水中的碳源结构,为后续生物系统提供适量的简单碳源且避免VFAs的累积,通过共基质作用提高难降解化合物的降解效率,并且能回收大量较为纯净的H2气体,可为提高焦化废水处理效率和能源回收开发利用提供一种新的途径.
在一个厌氧消化体系里面,乙酸营养型产甲烷菌和氢营养型产甲烷菌在总产甲烷菌群中的占比约为72:28(Mccarty et al., 1986).由于焦化废水中苯酚等有机物的最终水解产物为乙酸,且焦化废水中缺乏产氢的有机物质,假如能对焦化废水中的有机物进行厌氧生物降解产CH4,乙酸营养型产甲烷菌必然是优势菌种.然而,上述实验结果表明,乙酸营养型产甲烷菌受到焦化废水中毒性物质明显的抑制作用,导致其无法降解体系中的乙酸生成CH4,且未受明显抑制的氢营养型产甲烷菌也无基质利用以产生CH4.因此,从厌氧微生物的基质利用特性方面分析可得,高浓度的焦化废水难以实现厌氧产CH4的目标.
4 结论(Conclusions)由于高浓度焦化废水中存在大量的毒性物质,难以对其实现厌氧生物降解产甲烷的过程,造成目前国内占主导地位的A2/O工艺的工程单元浪费并需要大量稀释水.通过对抑制性污染物质的识别,发现在焦化废水复合污染的条件下,硫氰化物、苯酚、硫化物和氰化物浓度分别在500~1500、1100~1250、200~250和30~40 mg·L-1范围内,对厌氧微生物的活性产生了明显的抑制作用.在pH为7左右的厌氧条件下,这4种特征污染物的毒性作用表现为协同加成作用.在改变焦化废水中的碳源结构后,从微生物对碳源利用和产物变化的规律中发现,乙酸营养型产甲烷菌对毒性物质的敏感程度比氢营养型产甲烷菌高;从共代谢的角度发现,合适的碳源结构不仅可产生正面的共基质作用从而提高焦化废水的处理效率,还能得到不同的能源产物.
Bhunia F, Saha N C, Kaviraj A. 2000. Toxicity of thiocyanate to fish, plankton, worm, and aquatic ecosystem[J]. Bulletin of Environmental Contamination and Toxicology, 64(2): 197–204.
DOI:10.1007/s001289910030
|
Chakraborty S, Veeramani H. 2002. Anaerobic-anoxic-aerobic sequential degradation of synthetic wastewaters[J]. Applied Biochemistry and Biotechnology, 102(1): 443–451.
|
Chen Y, Cheng J J, Creamer K S. 2008. Inhibition of anaerobic digestion process:a review[J]. Bioresource Technology, 99(10): 4044–4064.
DOI:10.1016/j.biortech.2007.01.057
|
Dash R R, Gaur A, Balomajumder C. 2009. Cyanide in industrial wastewaters and its removal:a review on biotreatment[J]. Journal of Hazardous Materials, 163(1): 1–11.
DOI:10.1016/j.jhazmat.2008.06.051
|
Evans W C, Fuchs G. 1988. Anaerobic degradation of aromatic compounds[J]. Annual Review of Microbiology, 1(42): 289–317.
|
Fang H H P, Chan O C. 1997. Toxicity of phenol towards anaerobic biogranules[J]. Water Research, 31(9): 2229–2242.
DOI:10.1016/S0043-1354(97)00069-9
|
范丹. 2016. 焦化废水生化处理工艺的比选及工程运行能耗的研究[D]. 广州: 华南理工大学
http://kns.cnki.net/KCMS/detail/detail.aspx?filename=hjxx201610026&dbname=CJFD&dbcode=CJFQ |
Gupta P, Ahammad S Z, Sreekrishnan T R. 2016. Improving the cyanide toxicity tolerance of anaerobic reactor:Microbial interactions and toxin reduction[J]. Journal of Hazardous Materials, 315: 52–60.
DOI:10.1016/j.jhazmat.2016.04.028
|
Hilton B L, Oleszkiewicz J A. 1988. Sulfide-induced inhibition of anaerobic digestion[J]. Journal of Environmental Engineering, 114(6): 1377–1391.
DOI:10.1061/(ASCE)0733-9372(1988)114:6(1377)
|
胡纪萃, 周孟津, 左剑恶. 2003. 废水厌氧生物处理理论与技术[M]. 北京: 中国建筑工业出版社: 36–274.
|
Karlsson A, Ejlertsson J, Nezirevic D, et al. 1999. Degradation of phenol under meso-and thermophilic, anaerobic conditions[J]. Anaerobe, 5(1): 25–35.
DOI:10.1006/anae.1998.0187
|
Kim Y M, Park D, Lee D S, et al. 2008. Inhibitory effects of toxic compounds on nitrification process for cokes wastewater treatment[J]. Journal of Hazardous Materials, 152(3): 915–921.
DOI:10.1016/j.jhazmat.2007.07.065
|
Li B, Sun Y L, Li Y Y. 2005. Pretreatment of coking wastewater using anaerobic sequencing batch reactor (ASBR)[J]. Journal of Zhejiang University Science B, 6(11): 1115–1123.
|
Liu Y. 2010. Taxonomy of methanogens[M]. Berlin, Heidelberg: Springer: 550–555.
|
Lomans B P, Van der Drift C, Pol A, et al. 2002. Microbial cycling of volatile organic sulfur compounds[J]. Cellular and Molecular Life Sciences (CMLS), 59(4): 575–588.
DOI:10.1007/s00018-002-8450-6
|
Lu Y, Yan L, Wang Y, et al. 2009. Biodegradation of phenolic compounds from coking wastewater by immobilized white rot fungus Phanerochaete chrysosporium[J]. Journal of Hazardous Materials, 165(1): 1091–1097.
|
Mccarty P L, Smith D P. 1986. Anaerobic wastewater treatment[J]. Environmental Science & Technology, 20(12): 1200–1206.
|
马小云, 万金泉. 2011. 苯酚对厌氧颗粒污泥的毒性研究[J]. 环境科学, 2011, 32(5): 1402–1406.
|
Min Z, Tay J H, Yi Q, et al. 1998. Coke plant wastewater treatment by fixed biofilm system for COD and NH3-N removal[J]. Water Research, 32(2): 519–527.
DOI:10.1016/S0043-1354(97)00231-5
|
Nielsen P H. 1987. Biofilm dynamics and kinetics during high-rate sulfate reduction under anaerobic conditions[J]. Applied & Environmental Microbiology, 53(1): 27–32.
|
潘霞霞, 李媛媛, 黄会静, 等. 2009. 焦化废水中硫氰化物的生物降解及其与苯酚、氨氮的交互影响[J]. 化工学报, 2009, 60(12): 3089–3096.
|
Park D, Lee D S, Kim Y M, et al. 2008. Bioaugmentation of cyanide-degrading microorganisms in a full-scale cokes wastewater treatment facility[J]. Bioresource Technology, 99(6): 2092–2096.
DOI:10.1016/j.biortech.2007.03.027
|
任源, 韦朝海, 吴超飞, 等. 2007. 焦化废水水质组成及其环境学与生物学特性分析[J]. 环境科学学报, 2007, 27(7): 1094–1100.
|
Sahariah B P, Anandkumar J, Chakraborty S.2015.[J].Desalination & Water Treatment, 57(31):1-7
|
Sheng G P, Yu H Q, Li X Y. 2010. Extracellular polymeric substances (EPS) of microbial aggregates in biological wastewater treatment systems:a review[J]. Biotechnology Advances, 28(6): 882–894.
DOI:10.1016/j.biotechadv.2010.08.001
|
USP XXⅡ, NF XVⅡ.1990.Toxicity Calssification in US Pharmacopeia.I[S] United States Pharmacopeial Convection.2069
|
Veeresh G S, Kumar P, Mehrotra I. 2005. Treatment of phenol and cresols in upflow anaerobic sludge blanket (UASB) process:a review[J]. Water Research, 39(1): 154–170.
DOI:10.1016/j.watres.2004.07.028
|
Wang J, Quan X, Wu L, et al. 2002. Bioaugmentation as a tool to enhance the removal of refractory compound in coke plant wastewater[J]. Process Biochemistry, 38(5): 777–781.
DOI:10.1016/S0032-9592(02)00227-3
|
Wei X X, Zhang Z Y, Fan Q L, et al. 2012. The effect of treatment stages on the coking wastewater hazardous compounds and their toxicity[J]. Journal of Hazardous Materials, 239: 135–141.
|
韦朝海, 贺明和, 任源, 等. 2007. 焦化废水污染特征及其控制过程与策略分析[J]. 环境科学学报, 2007, 27(7): 1083–1093.
|
韦朝海, 朱家亮, 吴超飞, 等. 2011. 焦化行业废水水质变化影响因素及污染控制[J]. 化工进展, 2011, 30(1): 225–232.
|
吴伟, 郑珍珍, 麻婷婷, 等. 2016. 互营乙酸氧化菌研究进展[J]. 中国沼气, 2016, 34(2): 3–8.
|
Yang P, Wang B. 2001. Review of treatment of coking wastewater by biological methods[J]. Environmental Protection of Chemical Industry, 3: 004.
|
Yenigün O, Demirel B. 2013. Ammonia inhibition in anaerobic digestion:A review[J]. Process Biochemistry, 48(5/6): 901–911.
|
Yu X, Xu R, Wei C, et al. 2016. Removal of cyanide compounds from coking wastewater by ferrous sulfate:Improvement of biodegradability[J]. Journal of Hazardous Materials, 302: 468–474.
DOI:10.1016/j.jhazmat.2015.10.013
|
Zhang W, Wei C, Chai X, et al. 2012. The behaviors and fate of polycyclic aromatic hydrocarbons (PAHs) in a coking wastewater treatment plant[J]. Chemosphere, 88(2): 174–182.
DOI:10.1016/j.chemosphere.2012.02.076
|
Zhao J, Jiang Y, Yan B, et al. 2014. Multispecies acute toxicity evaluation of wastewaters from different treatment stages in a coking wastewater-treatment plant[J]. Environmental Toxicology and Chemistry, 33(9): 1967–1975.
DOI:10.1002/etc.v33.9
|
Zhu S, Wu H, Wei C, et al. 2016. Contrasting microbial community composition and function perspective in sections of a full-scale coking wastewater treatment system[J]. Applied Microbiology and Biotechnology, 100(2): 949–960.
DOI:10.1007/s00253-015-7009-z
|
张万辉, 韦朝海. 2015. 焦化废水的污染物特征及处理技术的分析[J]. 化工环保, 2015, 35(3): 272–278.
|
张万辉, 韦朝海, 晏波, 等. 2012. 焦化废水中溶解性有机物组分的特征分析[J]. 环境化学, 2012, 31(5): 702–707.
|
 2017, Vol. 37
2017, Vol. 37


