中国作为一个农业大国, 秸秆废弃物产生量非常大.据《“十二五”农作物秸秆综合利用实施方案》公布的数据显示, 2010年全国秸秆理论产量为8.4亿t, 可收集量约为7.0亿t, 其中, 稻秸、麦秸、玉米秸这3种主要秸秆的产量分别约为2.11、1.54、2.73亿t(国家发展改革委等, 2011).在中国, 为了节省收集、处理的空间和便于下次耕作, 直接焚烧是一种较为普遍的处理方式.然而其燃烧过程释放出70%的CO2、7%的CO、0.66%的CH4、2.09%的N2O和大量的PM2.5, 释放出大量的温室气体并对空气环境造成严重污染(Li et al., 2007).随着国家近几年出台了一系列政策以禁止秸秆直接焚烧, 直接燃烧的比例已得到有效控制.但要从根本上解决这个问题需要寻找一种集经济、社会、环境效益于一体的处理方式对秸秆废物进行资源化利用.近年来, 将秸秆废弃物转化为乙醇等生物液体燃料的技术发展迅速, 因为其不仅能够有效降低碳排放量, 并且在一定程度上取代石油和煤炭等化石燃料的使用, 提高环境质量.生物质能“十三五”规划中提出, 到2020年生物液体燃料年利用量为600万t, 其中, 生物乙醇占400万t(国家能源局, 2016).因此, 以秸秆废弃物为原料制备生物乙醇是生物质能源化利用的热门技术.
秸秆作为一种天然的木质纤维素, 其致密的稳定结构阻碍了与微生物、酶的接触, 抑制了高分子糖类的分解和利用, 进而降低处理效率, 极大地增加了乙醇的生产成本.为打破木质纤维素的天然屏障, 需要对其进行预处理.离子液体作为一种“绿色”溶剂具有能够溶解纤维素的特性, 其溶解-析出过程能够破坏木质纤维素的致密结构和纤维素的结晶结构, 增大与酶和微生物的接触面积, 提高木质纤维素的可利用性(Sun et al., 2009).水分对大多数的离子液体具有很大的影响, 因为其存在会抑制离子液体对纤维素的溶解进而降低处理效果(Swatloski et al., 2002).但水分在木质纤维素处理过程中却无法避免, 因为离子液体会吸收环境中的水分, 而木质纤维素也含有一定的水分.已有研究表明, 通过添加一定量的盐酸能够有效提高离子液体水溶液的预处理效果(Qing et al., 2015; Zhang et al., 2012; Wang et al., 2015).这种新型的预处理方法能够有效解决水分存在的问题, 在较高的含水率下依然具有良好的木质纤维素处理效果.而含水率的提高能够降低离子液体的粘度, 促进物质运输, 提高生物质负载量, 并且减少离子液体的用量及后续回收耗费的时间和能量, 节省成本(Pang et al., 2016).
超声波作为一种机械声波在介质的传播过程所产生的空化效应对介质起到了很好的搅拌作用, 可以使两种不相溶的液体发生乳化, 加速溶质的溶解和加快化学反应(Luo et al., 2014).已有研究表明, 利用超声波辅助离子液体可以加快预处理过程, 并对结晶纤维素和木质素具有更强的破坏作用(Yang et al., 2015; Ninomiya et al., 2015).但到目前为止, 还未见利用超声波辅助离子液体-盐酸溶液预处理木质纤维素的报道.离子液体水溶液中由于水分子更倾向于与离子液体中的离子进行结合, 进而破坏阴阳离子间的作用力, 降低体系的粘度(Pang et al., 2016).通常认为, 介质的粘度下降, 有利于降低超声波的空化阀, 促进超声波的传质(Karimi et al., 2014).因此, 本试验在中低温度下, 采用超声波辅助离子液体-盐酸溶液对稻秆废弃物进行处理, 对预处理后的稻秆酶解产糖及其微观结构的变化进行研究.
2 试验材料与方法(Materials and methods) 2.1 材料试验所用木质纤维素材料为水稻秸秆, 由中国科学院城市环境研究所提供.将材料进行破碎后过40目筛, 于60 ℃烘干24 h后密封保存.
2.2 实验药品与仪器试剂:氯化-1-烯丙基-3-甲基咪唑([AMIM]Cl)、氯化-1-丁基-3-甲基咪唑([BMIM]Cl)购自上海默尼化工有限公司;盐酸(36%)购自广州化学试剂厂;3, 5-二硝基水杨酸(纯度98%)购自Sigama-Aldrich;酶(纤维素复合酶NS22086, 250 FPU·g-1;β-葡萄糖苷酶NS22118, 320 CBU·g-1)购自Novozymes公司;
仪器:FW100高速万能粉碎机(天津泰斯特仪器有限公司);HC-3018高速离心机(安徽中科中佳科学仪器有限公司);SB-800DT超声波清洗机(宁波新芝生物科技股份公司),频率为40 kHz;UV756CRT型紫外可见分光光度计(上海佑科仪器仪表有限公司);Nicolet6700傅里叶红外光谱仪(美国赛默飞世尔科技公司);Ultima X-射线衍射仪(日本理学);扫描电镜JSM-7001F(日本电子株式会社)
2.3 生物质预处理与回收取0.27 g稻杆(干重0.25 g)置于含离子液体的20 mL瓶子中, 加入一定量HCl溶液和去离子水配制成含水率20%(质量分数)、盐酸质量分数为0~3.6%的混合悬浊液, 固液比为1:20, 置于温度控制在(30±3)~(70±3) ℃的超声波清洗机水浴槽(声能密度0.0267 W·cm-3)中恒温超声反应30~240 min.反应结束并冷却后, 加入一定量去离子水搅拌15 min, 然后移至50 mL离心管中再添加去离子水至50 mL, 于8000 g下离心10 min移除上清液, 重复上述操作5次直至水洗液呈无色.真空抽滤后将滤渣于60 ℃下烘干24 h, 称重后密封保存.
2.4 酶解糖化取2.5% (m/V, g·mL-1)预处理后的稻秆加入至含有0.01 mol·L-1柠檬酸缓冲溶液(pH=4.8)和0.02%叠氮化钠的25 mL锥形瓶中, 加入生物酶(纤维素复合酶50 FPU·g-1和β-葡萄糖苷酶40 CBU·g-1), 置于50 ℃水浴摇床中在150 r·min-1条件下反应, 分别在0 h和48 h取样.采用DNS法测定反应液中的总还原糖含量(Miller, 1959).纤维转化率η采用公式(1)进行计算(张耿崚等, 2017).试验重复3次, 结果以平均值±标准偏差(SD)表示.
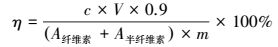
|
(1) |
式中, c为酶解48 h产生的还原糖浓度(mg·mL-1), V为反应液总体积(mL), A为纤维素、半纤维素组分含量, m为稻秆添加量(mg).
2.5 木质纤维素样品的成分分析采用硝酸-乙醇法、亚氯酸钠法和72%浓硫酸法分别对样品的纤维素、半纤维素及木质素含量进行测定(石淑兰, 2006).预处理后脱木质素率D采用公式(2)进行计算(Xu et al., 2016).试验重复3次, 结果以平均值±标准偏差(SD)表示.
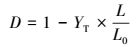
|
(2) |
式中, L0、L分别为预处理前后稻秆的木质素含量, 而YT是预处理后样品回收率.
2.6 木质纤维素样品的表征分析 2.6.1 X射线衍射分析(XRD)采用Cu靶产生X射线, 管压40 kV, 管流40 mA, 扫描步长为0.02 °·s-1, 2θ为5°~50 °.样品的结晶度(CrI)采用Segal公式(3)计算(Segal et al., 1959).
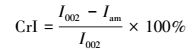
|
(3) |
式中, I002为(002)晶格面衍射强度, Iam为(001)与(002)晶格面间无定形区的衍射强度.
2.6.2 红外光谱分析(FTIR)采用KBr压片方式制备样品, 以KBr空白片作为参比扫描红外光谱, 扫描范围为4000~600 cm-1.
2.6.3 扫描电镜分析(SEM)将预处理前后的稻秆用导电胶带固定在铜台, 喷金后对样品的表面形貌进行观察.
3 结果与讨论(Results and discussion) 3.1 预处理条件对稻秆产糖影响 3.1.1 预处理温度对稻杆产糖量的影响采用超声波辅助含20%(质量分数)水分的离子液体-盐酸(1.2%, 质量分数)(US-IL-HCl)溶液于30~70 ℃下对稻秆预处理120 min, 酶解糖化结果如图 1a所示.由图可知, 温度对预处理效果具有显著性影响, 随着温度的升高, 酶解产糖量不断上升.在70 ℃时, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl处理的还原糖产量分别为8.423 mg·mL-1和9.717 mg·mL-1, 前者相比在30 ℃和50 ℃时分别提高了93.45%和44.77%, 而后者分别提高了74.20%和24.13%.更高的温度能够降低离子液体的粘度, 加速纤维素的润胀和溶解, 这是因为在较高温度下纤维素间氢键网络得到有效破坏(Badgujar et al., 2015).[BMIM]Cl相比[AMIM]Cl熔点更高, 在中低温度下前者的物质运输能力低于后者(Badgujar et al., 2015), 所以酶解的结果显示, US-[BMIM]Cl-HCl预处理能力显著低于US-[AMIM]Cl-HCl, 但从温度的升高对产糖量的提高而言, US-[BMIM]Cl-HCl受温度影响更大.
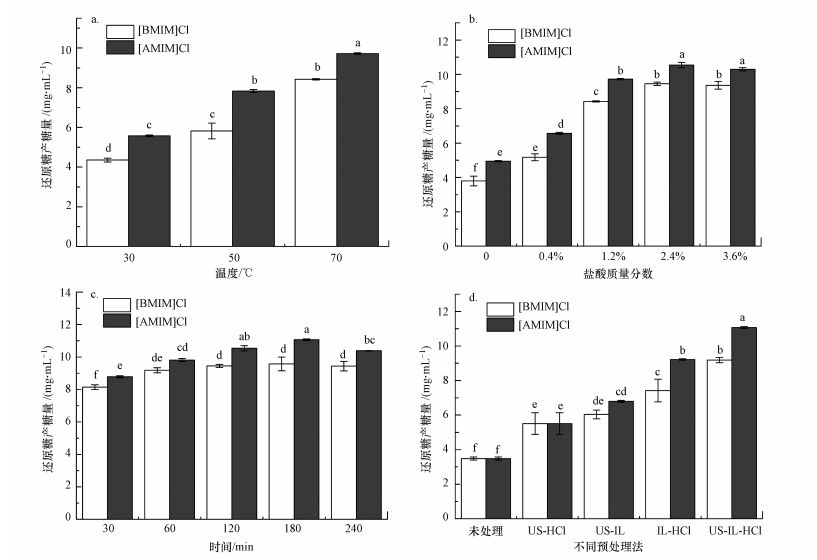 |
| 图 1 不同处理温度(a)、盐酸质量分数(b)、时间(c)和方法(d)下预处理后稻秆酶解效果(不同字母代表各组间在Duncan′s Multiple Range Test下具有显著性差异(p<0.05, n=3)) 注:US-HCl(超声辅助2.4%盐酸预处理), US-IL(超声辅助无水IL预处理), IL-HCl(离子液体-2.4%盐酸预处理), US-IL-HCl(超声辅助离子液体-2.4%盐酸预处理), [BMIM]Cl(70 ℃, 60 min), [AMIM]Cl(70 ℃, 180 min) Fig. 1 The enzymatic hydrolysis of rice straw pretreated with different temperature(a), concentration of acid(b), time(c) and method(d)(The different letters indicate significant difference between each group according to the Duncan′s Multiple Range Test (p < 0.05, n=3)) |
采用超声波辅助含20%水分的离子液体-盐酸(0~3.6%)(US-IL-HCl)溶液于70 ℃下对稻秆预处理120 min, 酶解糖化结果如图 1b所示.两种类型的离子液体水溶液预处理稻秆的酶解产糖量呈现一致的趋势, 随着盐酸质量分数的增加, 产糖量也随着增加, 在2.4%下达到最高, 相比不添加盐酸下US-[BMIM]Cl和US-[AMIM]Cl处理的稻秆产糖量分别提高了149.10%和113.34%.继续提高盐酸质量分数, 产糖量无明显提高.加入一定量盐酸, 能够提高体系中氢离子和氯离子的浓度.氯离子作为一种强电负性的离子能够与纤维素中的羟基自由基竞争质子, 而氢离子浓度的提高有利于对纤维素间糖苷键的氧原子进行攻击(Zhao et al., 2009; Li et al., 2008).因此, 添加一定量的盐酸能够显著地促进US-IL对纤维素的溶解和破坏进而促进酶解产糖效果.酸度的提升, 有利于提高离子液体对水的耐受性.在节省1/5离子液体用量和后续回收利用所耗费的时间和能量之余, 进一步提高了酶解产糖效率, 极大地节省了处理成本.
3.1.3 不同处理时间下的处理效果采用超声波辅助含20%水分的离子液体-盐酸(2.4%)(US-IL-HCl)溶液于70 ℃下对稻秆预处理30~240 min, 酶解糖化结果如图 1c所示.US-[BMIM]Cl-HCl处理在60 min后产糖量基本保持不变, US-[AMIM]Cl-HCl处理在180 min时产糖量达到最高.而其他文献曾报道离子液体-盐酸溶液(IL-HCl)在高温下(≥120 ℃)最佳预处理时间为30~45 min(Zhang et al., 2012; Wang et al., 2015), 本试验在降低预处理温度的同时通过超声进行辅助处理, 最佳预处理时间为60~180 min.预处理时间是直接影响处理效果的重要因素之一, 尽管延长反应时间能够促进木质纤维素结构的破坏, 但这也会导致糖类过度分解成糠醛、羟甲基糠醛及其他酶解抑制物(Zhou et al., 2012).
3.1.4 不同预处理方法下的处理效果为了确认超声在IL-HCl中的促进作用, 在试验中比较了不同预处理法的效果.如图 1d所示, 未处理稻秆酶解产糖量只有3.483 mg·mL-1, 而通过超声辅助2.4%盐酸溶液(US-HCl)预处理后, 稻秆的产糖量相比未处理提高了36.80%, 而超声辅助纯离子液体(无水)(US-IL)预处理稻秆中, US-BMICMCl和US-[AMIM]Cl处理的产糖量则分别提高了73.39%和95.06%.这说明超声与盐酸溶液或者超声与离子液体的结合对秸秆进行预处理对酶解产糖具有一定的提高效果, 但提高效果低于IL-HCl和US-IL-HCl.从图中也可以发现, 在IL-HCl中虽然含水量达20%, 但在HCl的存在下其产糖量相对于未处理稻秆仍分别提高113.06%和164.63%.为了进一步提高预处理效果, 采用超声波辅助IL-HCl.酶解试验结果表明, 超声辅助能够进一步提高还原糖总产量, 相比未超声, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl在较低超声能耗下(声能密度0.0267 W·cm-3)产糖量分别提高了28.96%和20.13%.发酵对糖的浓度有一定要求, 较高的含糖量节省了糖分浓缩的步骤, 减少生产成本.
3.2 木质纤维素成分分析与计算预处理前后稻秆的木质纤维素成分如表 1所示.经过预处理后, 稻秆的纤维素含量从38.10%上升至52.54%~56.09%, 这是因为在预处理和水洗过程中可溶性物质得到去除.对比有无超声辅助下IL-HCl预处理后稻秆的成分变化, 可以发现在超声的辅助下, 半纤维素、木质素含量均下降.半纤维素的下降主要是由于其与木质素间β-醚键的断裂, 在IL-HCl预处理中β-醚键断裂的速度和数量主要取决于酸度、可利用的质子数及温度(Zhang et al., 2012).在本试验中采用IL-HCl预处理稻杆, 最高温度为70 ℃, 半纤维素含量(18.18%和18.86%)与未处理稻秆(19.95%)相比下降不明显.但在超声的辅助下, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl预处理后稻秆的半纤维素含量相比未超声分别下降了37.52%和34.52%.这可能是因为在未超声、70 ℃下不足以达到β-醚键断裂的最佳条件, 但超声波的空化效应所造成的瞬间高温高压条件促使了β-醚键断裂的进行(Luo et al., 2014).另外, [BMIM]Cl-HCl、[AMIM]Cl-HCl、US-[BMIM]Cl-HCl及US-[AMIM]Cl-HCl处理的脱木质素率依次为46.24%、45.08%、55.18%及53.22%, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl处理相比未超声脱木质素率分别提高了19.33%和18.06%, 这说明超声辅助处理能够进一步提高木质素的去除.这是由于超声波能够将破坏后的木质素进行移除, 减少依附在样品中的木质素(Montalbo-Lomboy et al., 2015).为了进一步从成分变化和产糖量上对比IL-HCl和US-IL-HCl间的处理效果, 采用纤维转化率进行比较.计算结果显示, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl相比未超声处理的纤维转化率分别提高了35.23%和31.69%.所以, 超声辅助能够提高预处理稻秆的产糖率.
| 表 1 预处理前后稻秆的成分分析与计算 Table 1 The composition and cellulose conversion of untreated and treated rice straw |
木质纤维素的表面形貌、化学官能团及纤维素的结晶度的变化也可以作为考察预处理效果的依据.预处理前后稻秆的扫描电子显微镜(SEM)图谱(放大2000倍)如图 2所示.图 2a为未处理的稻秆, 从图中可发现, 稻秆表面结构均匀而完整.而经过IL-HCl或US-IL-HCl预处理后的稻秆表面结构变得无序和不规则, 而且疏松多孔.而对比有无超声的稻秆图片(图 2b和2c及2d和2e), 可以发现, 无超声下稻秆溶解后的纤维素再次析出堆积在表面, 呈现凹凸不平的结构, 而在超声辅助处理下的稻秆表面纤维束出现剥落和断裂的现象.这解释了超声辅助预处理稻秆酶解效率提高的原因, 微观结构的变化提高了酶对物料的可及度, 破坏了木质纤维素天然屏障, 提高了酶解产糖率.
 |
| 图 2 预处理前后稻秆SEM图谱(a.未处理, b.[BMIM]Cl-HCl处理, c.US-[BMIM]Cl-HCl处理, d.[AMIM]Cl-HCl处理, e.US-[AMIM]Cl-HCl处理) Fig. 2 The SEM figures of rice straw before and after pretreatment(a.Untreated, b. [BMIM]Cl-HCl treated, c. US-[BMIM]Cl-HCl treated, d.[AMIM]Cl-HCl treated, e.US-[AMIM]Cl-HCl treated) |
通过对预处理前后的稻秆进行X射线衍射(XRD)分析, 并按照公式(3)计算其结晶度(CrI), 结果如表 2所示.未处理的稻秆CrI为48.57%, 而经过US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl处理后结晶度分别提高至52.12%和51.06%.通过XRD分析计算的CrI值是样品中结晶区域与无定型区域的比值(Li et al., 2014).CrI值上升的原因主要是无定型物质如木质素和半纤维素的移除及无定型区域的坍塌和剥落, 导致结晶纤维素的相对含量提高.在超声的辅助下, US-[BMIM]Cl-HCl和US-[AMIM]Cl-HCl处理的稻秆结晶度分别下降至47.77%和46.19%.此时, 尽管半纤维素和木质素的含量相比未超声有进一步的下降, 但结晶度也下降, 这说明超声辅助处理对结晶纤维素具有一定破坏效果.纤维素结晶度的降低有助于减少其与水解酶之间的位阻, 提高反应速度.
| 表 2 预处理前后稻秆的XRD结晶指数和红外比率 Table 2 The crystallinity index of XRD and the infrared ratios of Fourier transform spectroscopy for untreated and treated rice straw |
样品的化学结构变化可以通过傅里叶变换红外光谱分析(FTIR)观察, 结果如图 3所示.纤维素和半纤维素中的特征峰如2920 cm-1(C—H和CH2伸缩峰)、1372 cm-1(纤维素和半纤维素中C—H的弯曲振动峰)、1160 cm-1(C—O—C反对称伸缩振动峰)、1105 cm-1(纤维素与半纤维素产生结合作用的O—H变化)、1063 cm-1(纤维素和半纤维素中C—O的伸缩振动峰)、897 cm-1(纤维素中C—H的弯曲振动峰).木质素中的特征峰有1514 cm-1(芳香骨架C—C振动峰)、1320 cm-1和1246 cm-1(紫丁香基中的C—O振动峰)(Ninorniya et al., 2012).另外, 1424 cm-1(木质素和碳水化合物的C—H弯曲振动峰)特征峰的变化通常代表无定型区的破坏情况(刘黎阳等, 2013).从FTIR结果发现, 经过预处理后, 稻秆中纤维素、半纤维素及木质素的特征峰均有明显变化(比较图 3a与3b~3e).值得注意的是, 通过比较IL-HCl和US-IL-HCl预处理稻秆的红外光谱图发现(即比较图 3b和3c及3d和3e), 在超声的辅助下, 纤维素、半纤维素特征峰(1372、1160、1105、1063 cm-1)变宽, 说明超声辅助能够进一步破坏纤维素和半纤维的结构, 改变其结合键位的吸收强度.另外, 897 cm-1处强度变化可反映结晶纤维素结构变化情况, 从图中也可以发现, 在超声辅助处理下其峰型变缓, 峰宽变大, 这说明结晶纤维素的特征官能团受到破坏导致吸收强度的下降.木质素的特征峰(1514、1320及1246 cm-1)经过超声辅助处理后强度相比未超声均有所下降, 这与表 1中的木质素含量变化情况一致.
 |
| 图 3 预处理前后稻秆的FTIR图谱(a.未处理, b.[BMIM]Cl-HCl处理, c.US-[BMIM]Cl-HCl处理, d.[AMIM]Cl-HCl处理, e.US-[AMIM]Cl-HCl处理) Fig. 3 The FTIR spectrum of rice straw before or after pretreatment(a.Untreated, b. [BMIM]Cl-HCl treated, c.US-[BMIM]Cl-HCl treated, d.[AMIM]Cl-HCl treated, e.US-[AMIM]Cl-HCl treated) |
1424 cm-1与897 cm-1处吸收强度的比值LOI(结晶指数或侧枝指数)和1372 cm-1与2920 cm-1处吸收强度的比值TCI(总结晶指数)通常作为判断纤维素结晶度的依据, 较高的指数说明样品具有较高的结晶度和结构指数(Ninorniya et al., 2012), 预处理前后稻秆的LOI和TCI指数如表 2所示.未处理、[BMIM]Cl-HCl、US-[BMIM]Cl-HCl、[AMIM]Cl-HCl及US-[AMIM]Cl-HCl处理稻秆的LOI值依次为1.5955、1.8159、1.5123、1.8029及1.4167, 其结果与由XRD计算的CrI值相吻合.而TCI值随着处理强度变大呈降低的趋势, 由1.2399下降至0.8639~1.0562, 与纤维转化率的趋势一致.
4 结论(Conclusions)1) 温度、酸度及处理时间对US-IL-HCl预处理稻秆的产糖量具有显著影响.
2) 超声波辅助IL-HCl预处理稻秆相比未超声, 产糖量、纤维转化率和脱木质素率分别提高20.13%~28.96%、31.69%~35.23%和18.06%~19.33%.
3) 利用SEM、XRD及FTIR对处理前后的稻秆的微观形貌、结晶度及化学结构进行分析, 发现超声波的辅助能够进一步提高IL-HCl预处理对稻秆表面形貌和化学结构的破坏, 并降低纤维素的结晶度, 提高酶解效果.
Badgujar K C, Bhanage B M. 2015. Factors governing dissolution process of lignocellulosic biomass in ionic liquid:Current status, overview and challenges[J]. Bioresource Technology, 178: 2–18.
|
国家发展改革委、农业部、财政部. 2011. 关于印发"十二五"农作物秸秆综合利用实施方案的通知[Z]. 北京
|
国家能源局. 2016. 生物质能"十三五"规划[Z]. 北京
|
Karimi M, Jenkins B, Stroeve P. 2014. Ultrasound irradiation in the production of ethanol from biomass[J]. Renewable and Sustainable Energy Reviews, 40(40): 400–421.
|
Li C, Wang Q, Zhao Z K. 2008. Acid in ionic liquid:An efficient system for hydrolysis of lignocellulose[J]. Green Chemistry, 10(2): 177–182.
DOI:10.1039/B711512A
|
刘黎阳, 牛坤, 刘晨光, 等. 2013. 离子液体预处理油料作物木质纤维素[J]. 化工学报, 2013, 64(S1): 104–111.
|
Li L, Yang D R, Liu D T, et al. 2014. Influence of combined pretreatment of quadrol and anhydrous ionic liquid microemulsion on the physicochemical property of masson pine[J]. Journal of Applied Polymer Science, 131(2): 1–9.
|
Li X, Wang S, Duan L, et al. 2007. Particulate and trace gas emissions from open burning of wheat straw and corn stover in China[J]. Enviromental Science and Technology, 41(17): 6052–6058.
|
Luo J, Fang Z, Smith R L. 2014. Ultrasound-enhanced conversion of biomass to biofuels[J]. Progress in Energy and Combustion Science, 41: 56–93.
DOI:10.1016/j.pecs.2013.11.001
|
Luo J, Fang Z, Smith R L. 2014. Ultrasound-enhanced conversion of biomass to biofuels[J]. Progress in Energy and Comnustion Science, 41: 56–93.
|
Miller G L. 1959. Use of dinitrosalicylic acid reagent for determination of reducing sugar[J]. Analytical Chemistry, 31(3): 426–428.
DOI:10.1021/ac60147a030
|
Montalbo-Lomboy M, Grewell D. 2015. Rapid dissolution of switchgrass in 1-butyl-3-methylimidazolium chloride by ultrasonication[J]. Ultrasonics Sonochemistry, 22: 588–599.
|
Ninomiya K, Kamide K, Takahashi K, et al. 2012. Enhanced enzymatic saccharification of kenaf power after ultrasonic pretreatment in ionic liquid at room temperature[J]. Bioresource Technology, 103: 259–265.
|
Ninomiya K, Kohori A, Osawa K, et al. 2015. Ionic liquid/ultrasound pretreatment and in situ enzymatic saccharification of bagasse using biocompatible cholinium ionic liquid[J]. Bioresource Technology, 176: 169–174.
|
Pang Z Q, Dong C H, Pan X J. 2016. Enhanced deconstruction and dissolution of lignocellulosic biomass in ionic liquid at high water content by lithium chloride[J]. Cellulose, 23: 323–338.
DOI:10.1007/s10570-015-0832-7
|
Qing Q, Hu R, Zhang Y, et al. 2014. Investigation of a novel acid-catalyzed ionic liquid pretreatment method to improve biomass enzymatic hydrolysis conversion[J]. Applied Microbiology and Biotechnology, 98(11): 5275–5286.
DOI:10.1007/s00253-014-5664-0
|
Segal L, Creely J J, Martin J A, et al. 1959. An empirical method for estimating the degree of crystallinity of native cellulose using the X-Ray diffractometer[J]. Textile Research Journal, 29(10): 786–794.
DOI:10.1177/004051755902901003
|
Sun N, Rahman M, Qin Y, et al. 2009. Complete dissolution and partial delignification of wood in the ionic liquid 1-ethyl-3-methylimidazolium acetate[J]. Green Chemistry, 11(11): 646–655.
|
Swatloski R P, Spear S K, Hobrey J D, et al. 2002. Dissolution of cellulose with ionic liquids[J]. Journal of the American Chemical Society, 124(18): 4974–4975.
DOI:10.1021/ja025790m
|
石淑兰. 2006. 纸浆造纸分析与检测[M]. 北京: 中国轻工业出版社: 1–380.
|
Wang G, Zhang S P, Xu W J, et al. 2015. Efficient saccharification by pretreatment of bagasse pith with ionic liquid and acid solutions simultaneously[J]. Energy Conversion and Management, 89: 120–126.
DOI:10.1016/j.enconman.2014.09.029
|
Xu F, Chen L, Wang A L, et al. 2016. Influence of surfactant-free ionic liquid microemulsions pretreatment on the composition, structure and enzymatic hydrolysis of the water hyacinth[J]. Bioresource Technology, 208: 19–23.
DOI:10.1016/j.biortech.2016.02.027
|
Yang C Y, Fang T J. 2015. Kinetics for enzymatic hydrolysis of rice hulls by the ultrasonic pretreatment with a bio-based basic ionic liquid[J]. Biochemical Engineering Journal, 100: 23–29.
|
Zhang Z Y, O'Hara I M, Doherty W O S. 2012. Pretreatment of sugarcane bagasse by acid-catalysed process in aqueous ionic liquid solutions[J]. Bioresource Technology, 120: 149–156.
DOI:10.1016/j.biortech.2012.06.035
|
Zhao H, Jones C L, Baker G A, et al. 2009. Regenerating cellulose from ionic liquids for an accelerated enzymatic hydrolysis[J]. Journal of Biotechnology, 139(1): 47–54.
DOI:10.1016/j.jbiotec.2008.08.009
|
Zhou N, Zhang Y M, Gong X W, et al. 2012. Ionic liquids-based hydrolysis of Chlorella biomass fermentable sugars[J]. Bioresource Technology, 118: 512–517.
|
张耿崚, 陈细妹, 韩业钜, 等. 2017. 表面活性剂辅助离子液体预处理稻秆的酶解动力学与结构变化分析[J]. 环境科学学报, 2017, 37(2): 686–693.
|
 2018, Vol. 38
2018, Vol. 38


