生物炭(Biochar, BC)作为一种由生物质在缺氧条件下经过热解而形成的含非芳香烃和芳香烃组分的混合炭质, 在土壤中降解缓慢, 具有作为长期碳汇、缓解气候变化的潜力(Lehmann, 2007; Marris, 2006; Woolf et al., 2010).生物炭包括易降解碳、相对难降解碳和灰分, 易降解碳部分在土壤中较易矿化和淋洗, 而且容易被微生物利用(Lehmann et al., 2009);相对难降解碳部分比较稳定, 但仍然能够被微生物(Hamer et al., 2004; Mun et al., 2009)和非生物氧化(Cheng et al., 2006; Liang et al., 2008)降解.研究表明, 生物炭只有一小部分(0.4%~1.1%)能被降解, 添加到土壤中的生物炭的大部分可作为相对难降解碳维持数百年甚至上千年(Glaser et al., 2001; Keith et al., 2014).
与未加生物炭的土壤相比, 添加生物炭的土壤中类腐殖质成分增加(Hernandez-Soriano et al., 2016).不同的热解温度导致生物炭的化学结构和成分有很大的不同(Asadullah et al., 2010; Li et al., 2006; Scott et al., 2007), 从而导致生物炭稳定性和矿化率的不同(Baldock et al., 2002).Jones等(2011)的研究表明, 添加水洗生物炭的土壤比添加原炭的土壤矿化速率低.也有研究表明, 生物炭的添加可能会促进土壤本体有机质的矿化作用, 同样易降解有机质的添加也会促进生物炭在土壤中的矿化作用(Liang et al., 2010; Barker, 2011).Liang等(2008)研究表明, 72%~90%的土壤有机碳存在于有机矿物质中.也有研究报道生物炭添加进土壤, 会嵌入微团聚体中(Lehmann et al., 2008), 从而增加了生物炭的稳定性.Brodowski(2005)研究还发现, 生物炭在沙土中的降解速率比在普通土壤中快.在自然界, 大量的有机残留物被添加进土壤中, 促进了微生物快速生长并能保持高活性, 且随着易降解有机质添加量的增加, 生物炭的矿化作用会增强(Keith et al., 2014).Hernandez-Soriano等(2016)的研究结果也说明了土壤中碳分布的情况对生物炭的矿化作用会产生一定的影响.综上可知, 生物炭不仅能够影响土壤的矿化作用, 同时其本身的矿化作用也受到土壤中其他物质的影响.但由于土壤环境比较复杂、影响因素众多, 难于清晰地认识生物炭本身在土壤中的矿化作用.
为探究不同热解温度的生物炭不同组分(包括易降解和相对难降解碳)对其在土壤中矿化作用的影响及机理, 本研究通过将代表不同降解碳库的原材料、不同热解温度的生物炭及其碳骨架加入到石英砂和土壤菌液(模拟不含有机质的土壤)中, 研究不同培养温度条件下具有不同难降解碳库的生物炭在土壤中的矿化作用, 以期为分析生物炭在土壤中的矿化作用和碳汇作用的潜在机制提供依据.
2 材料和方法(Materials and methods) 2.1 模拟土壤为了能较清晰地研究生物炭本身在土壤中的矿化作用, 课题组利用石英砂制作了一种不含有机质的“土壤”, 即“模拟土壤”.土壤样本采自广东省肇庆市鼎湖山(23°10′N, 112°31′E)地表层(0~10 cm).自然风干后, 去除可见根和石头, 过2 mm筛, 放入冰箱(4 ℃)保存.石英砂选用颗粒状和粉末状(SiO2含量≥99%), 按照质量比1:4(颗粒状:粉末状)的比例混合均匀, 放在干燥条件下保存.
取土壤25 g, 加500 mL去离子水, 振荡30 min, 过滤(Whatman No.1滤膜), 浸提液即为菌剂(Fang et al., 2014;Zimmerman, 2010).营养液组成如下:2 g葡萄糖, 4 mmol·L-1 NH4NO3, 4 mmol·L-1 CaCl2, 2 mmol·L-1 KH2PO4, 1 mmol·L-1 K2SO4, 1 mmol·L-1 MgSO4, 25 μmol·L-1 MnSO4, 2 μmol·L-1 ZnSO4, 0.5 μmol·L-1 CuSO4和0.5 μmol·L-1 Na2MoO4 (Cheng et al., 2006).营养液与菌种预培养数天, 使微生物达到较高的活性.将菌种过滤到0.22 μm的滤膜上并用去离子水反复冲洗以去除土壤有机碳, 再冲洗到营养液中, 混合均匀.然后将土壤菌悬液与石英砂混合均匀从而制备成“模拟土壤”, 以下简称为“土壤”.
2.2 生物炭及其碳骨架的制备生物炭原材料为甘蔗渣(GZ), 选自广东省广州市甘蔗研究所.甘蔗渣放入烘箱(105 ℃)中干燥至恒重, 经破碎机破碎后放入管式炉中, 程序设置为:40 min内升至250 ℃, 再以10 ℃·min-1的速度升至设定温度(分别为300、500、800 ℃), 停留2 h, 降温至50 ℃.整个烧制过程保持氩气(保护气)流通, 制成的3种生物炭分别表示为BC300、BC500、BC800.生物炭样品过60目筛(0.3 μm), 放入干燥器保存.
取甘蔗渣和每种温度的生物炭各12 g于1000 mL烧杯中, 加入480 mL去离子水, 100 ℃下加热搅拌3 h(Jones et al., 2011; Lou et al., 2015), 过0.45 μm滤膜得到浸提液和碳骨架, 并用数显电导率仪(雷磁DDS-11A)测定浸提液电导率(EC).重复上述操作数次, 直至浸提液的电导率<50 μS·cm-1.保留第一次的浸提液, 放入冰箱(4 ℃)保存;滤渣(即碳骨架)在105 ℃烘干24 h, 放入干燥器保存, 制成的4种碳骨架分别用WGZ、W300、W500、W800表示.
2.3 实验设计将40 g“土壤”加入到100 mL培养瓶中, 按“土壤”质量5%的比例分别加入原材料、3种生物炭和4种碳骨架, 加上“土壤”本身作为控制处理(CK), 共9种处理.向每个培养瓶中添加2 mL土壤菌剂和营养液的混合液, 混合均匀, 最后分别在(35.0±0.2) ℃和(25.0±0.2) ℃条件下进行为期50 d的培养实验.除气体采集外, 培养期间所有的培养瓶敞口.实验过程中持水率设定为60%, 每2 d调节含水率.每种处理和温度设置3个重复.
用密封注射器分别在第1、2、4、8、20、32、50 d采集培养瓶中的气体.采气时, 盖上橡胶塞, 并使用铝盖以保证气密性.用注射器分别在封盖后的第0 h和4 h抽取气体(≥4 mL), 所有气样在8 h内测完.
2.4 分析和计算方法溶解性有机碳(DOC)浓度用TOC仪测定.生物炭与去离子水按照1:20(g/mL)的比例混合, 放入恒温振荡器中振荡1 h, 过0.45 μm滤膜, 用数显电导率仪和pH计(Mettler-Toledo)分别测定电导率(EC)和pH.参照Cao等(2010)的方法, 称取(1.00±0.02) g样品, 在1000 ℃下加热2 h, 计算灰分.碳(C)、氢(H)、氮(N)含量用元素分析仪(Vario EL)测定.利用气相色谱仪(Shimadzu GC 2014, Japan)测定培养瓶中的CO2浓度, 通过以下公式来计算CO2的产生速率(Lim et al., 2014):

|
(1) |
式中, F为CO2的气体通量(mg·kg-1·h-1), ρ为标准状态下CO2气体的密度(1.977 g·m-3), V为培养瓶顶空体积(L), W为生物炭的质量(kg), ΔC/Δt是气体在培养期间内浓度随时间变化的直线斜率(ppm·h-1), T1为标准状态下气体的绝对温度(273 K), T2为培养瓶内气体的实际绝对温度(K).为了区分生物炭中易降解与相对难降解碳的不同矿化特性, 采用以下双指数模型对不同处理的生物炭中总碳的累积矿化率进行拟合:
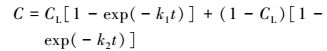
|
(2) |
式中, C为不同时间段生物炭的标准化的累积矿化率, CL和(1-CL)分别为易降解和相对难降解碳的比例, k1和k2分别为易降解和相对难降解碳的速率常数(d-1), t为培养时间(d), 1/k1和1/k2分别表示易降解和相对难降解碳的平均停留时间(d).
分别用Microsoft Excel 2007和Origin 9.1进行数据处理、数据图制作和非线性曲线拟合.采用SPSS19.0进行方差分析检验处理间的差异显著性.
3 结果(Results) 3.1 原材料和生物炭及其碳骨架的基本理化性质如表 1所示, 原材料和BC300、BC500、BC800的DOC含量随着生物炭热解温度升高而降低.生物炭的pH、电导率、总C含量和C/H值(物质的量比)随着热解温度的升高而增大, 但H含量降低.
| 表 1 原材料、生物炭及其碳骨架的基本理化性质 Table 1 Physical and chemical properties of the raw material, biochars and their carbon skeletons |
如图 1所示, 在25 ℃和35 ℃培养条件下, 各处理的矿化速率随时间的增加均降低, 培养4 d后渐趋平缓.在培养的前4 d各处理的矿化速率下降幅度分别为42.8%~93.6%(25 ℃)、36.2%~80.4%(35 ℃).第32 d时, 矿化速率接近为零, 且之后变化不明显.各处理的矿化速率大小关系基本为GZ>WGZ>BC300>W300>BC500>W500>BC800>W800.在同一培养温度下, GZ及WGZ的矿化速率显著高于生物炭及其碳骨架的矿化速率(p<0.05), 且随着生物炭热解温度升高, 矿化速率显著降低(p<0.05).生物炭碳骨架部分的矿化速率明显比生物炭低.与25 ℃培养温度相比, 35 ℃培养温度下明显促进了各处理的矿化速率.
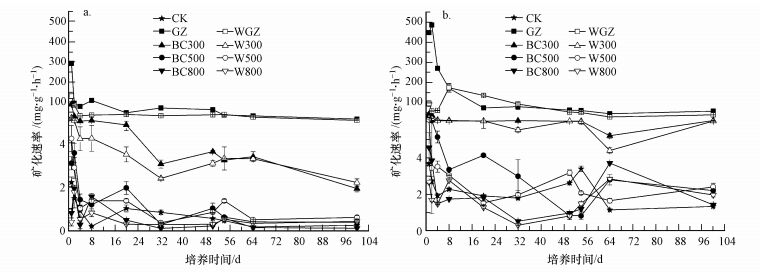 |
| 图 1 原材料、生物炭及其碳骨架在环境温度25 ℃(a)和35 ℃(b)下的矿化速率 Fig. 1 Mineralization rates of the raw material, biochars and their carbon skeletons under the ambient temperatures of 25 ℃(a) and 35 ℃(b) |
在两个培养温度下, 各处理的累积CO2矿化量大小关系基本为GZ>WGZ>BC300>W300>BC500>W500>BC800>W800(图 2).同一培养温度下, GZ及WGZ的累积CO2矿化量显著高于生物炭及其碳骨架(p<0.05), 随着生物炭热解温度升高, 累积CO2矿化量显著降低(p<0.05).生物炭碳骨架的累积CO2矿化量明显低于生物炭.35 ℃条件下各处理的累积CO2矿化量(1169.15~129068 mg·kg-1)显著高于在25 ℃条件下相应处理的累积CO2矿化量(346.95~89180 mg·kg-1).
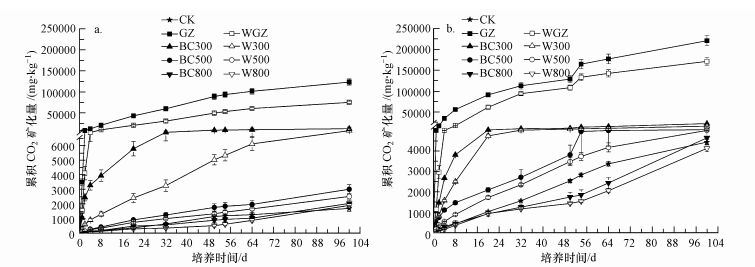 |
| 图 2 原材料、生物炭及其碳骨架在环境温度25 ℃(a)和35 ℃(b)下的累积CO2矿化量 Fig. 2 Cumulative CO2 released of the raw material, biochars and their carbon skeletons under the ambient temperatures of 25 ℃(a) and 35 ℃(b) |
如表 2和表 3所示, WGZ中仍然含有高含量的易降解碳, GZ及WGZ的易降解碳含量显著高于生物炭及其碳骨架(p<0.05).在25 ℃培养温度下, 生物炭及其碳骨架的易降解碳库含量分别减少78.3%和86.3%;在35 ℃培养温度下, 分别减少94.7%和91.3%.随着生物炭热解温度的升高, 其易降解碳含量逐渐降低, 相对难降解碳含量增多, 且两种碳的平均停留时间都增加, 易降解碳的平均停留时间从2 d增加到38 d, 相对难降解碳平均停留时间从14年增加到700多年.生物炭的易降解碳含量(0.12%~0.81%)远小于相对难降解碳含量(99.4%~99.9%).在25 ℃培养条件下, 生物炭碳骨架的易降解碳含量明显小于其对应的生物炭.但在35 ℃培养条件下, 300 ℃和500 ℃碳骨架与对应的生物炭相比, 易降解碳部分增加, 停留时间较长, 而W800保持所有处理中最低的可矿化含量(0.01%).将培养温度从25 ℃升高至35 ℃, 甘蔗渣及其碳骨架的易降解碳明显增加, 与其矿化速率和累积CO2矿化量显著增加相对应.但培养温度升高, 除W300和W500外, 其他生物炭及其碳骨架的易降解碳含量没有明显增加.并且值得注意的是, 相比25、35 ℃培养条件下, 生物炭及其碳骨架的相对难降解碳平均停留时间分别减少43%~87%和43%~80%.
| 表 2 利用双指数模型对25 ℃培养下生物炭累积矿化率拟合得到的模型参数 Table 2 Parameters from fitting cumulative mineralization proportion of biochar under 25 ℃ using the double-exponential model |
| 表 3 利用双指数模型对35 ℃条件下生物炭累积矿化率拟合得到的模型参数 Table 3 Parameters from fitting cumulative mineralization proportion of biochar under 35 ℃ using the double-exponential model |
原材料甘蔗渣及其碳骨架的矿化速率和累积矿化量较其热解产物生物炭显著增加, 双指数模型拟合结果表明, 与生物炭相比, 原材料甘蔗渣及其碳骨架中易降解碳含量显著增加.甘蔗渣热解为生物碳后, 相对难降解碳含量增加, 其平均停留时间明显变长, 产生碳汇效果.尽管生物炭被认为是较稳定的富碳物质, 但其仍含有少量可被微生物利用的有机碳, 能提高微生物新陈代谢活性, 进而增强土壤呼吸作用(Wang et al., 2016).各处理的矿化速率在前4 d显著降低, 后趋于平缓, 证实了生物炭在培养前期以易降解碳的矿化为主, 降解速率较快, 而后期以相对难降解碳的矿化为主, 降解速率较低.与其它研究结果相比, 在本实验中, 生物炭整体的矿化速率较快, 这可能是因为与复杂的土壤环境相比, “模拟土壤”环境比较单一, 降低了土壤的理化特性对生物炭矿化作用的影响.
由傅里叶变换红外光谱图(FT-IR)(图 3)可以看出, BC300含芳香化C—O—C基团(1061~1160 cm-1)、羧基(1715 cm-1)、CC键(1420~1600 cm-1)及酚基—OH基团(1380 cm-1)等多种有机官能团.随着热解温度升高, 羟基O—H(3427 cm-1)和脂肪族C—H(2850~2920 cm-1)逐渐减少.热解温度为500 ℃时, 主要官能团为CC键(1420~1600 cm-1)和C—O—C基团(1061~1160 cm-1).热解温度升高至800 ℃时, 官能团只剩下C—O—C基团(1061~1160 cm-1)有弱吸收峰.FT-IR图谱和元素含量变化结果表明, 随着制备热解温度的升高, 生物炭官能团种类减少, C/H值升高(表 1).这说明热解温度越高脱氢反应进行得越彻底, 在炭化过程中能得到稳定的高聚合芳香烃结构.因此, BC的矿化速率和易降解碳含量随着热解温度升高而降低, 相对难降解碳含量增多.X射线衍射图谱(XRD)结果表明, 随着生物炭热解温度增加, 衍射峰渐渐宽化, 说明无定形碳成分增加.如图 4所示, 在2θ=21.983°和22.490°两处, GZ和BC300分别出现了较为明显的衍射峰.随着BC热解温度升高, (002)峰2θ角由低角度向高角度转变.800 ℃热解制备的生物炭出现了(101)峰;500 ℃热解制备的生物炭(碳骨架), 无定型碳成分增加;在BC800和W800中, 有序的石墨层开始出现, 晶体碳增加, 而且石墨层结构比无定形结构更加稳定(Cohenofri et al., 2007).经过高温裂解的生物炭, 芳香化和聚合程度提高, 使其抗分解能力变强, 易降解碳和相对难降解碳的平均停留时间因而都变长(Hammes et al., 2007; Goldberg et al., 1985).
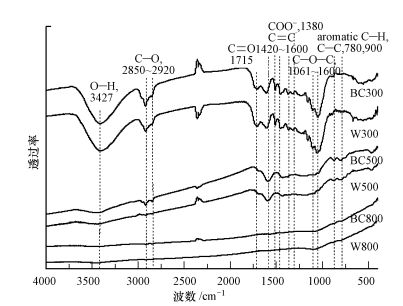 |
| 图 3 生物炭及其碳骨架的FT-IR图谱分析 Fig. 3 FTIR spectra of the raw material, biochar and their skeleton |
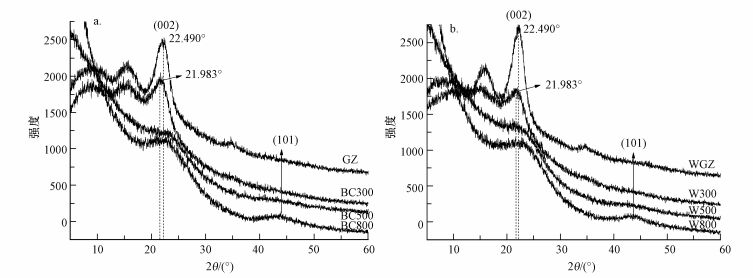 |
| 图 4 原材料、生物炭(a)及其碳骨架(b)的XRD图谱 Fig. 4 XRD spectra of the raw material, biochars and their carbon skeletons |
从生物炭中分离出的碳骨架, 比生物炭的矿化速率更低, 累积矿化量更少.根据双指数模型拟合结果, 25 ℃培养温度下, 碳骨架相对于生物炭的易降解碳含量减少, 而相对难降解碳含量增大.因为碳骨架缺少生物炭中可被微生物利用的溶解性有机碳, 芳香烃碳聚合程度升高, 能够有效地固持生物炭自身所含有的化学物质, 可生化性差(唐倩等, 2014).当培养温度升高至35 ℃时, W300和W500的易降解碳含量高于相应生物炭.从FT-IR和XRD谱图可看出, 热解温度较低的碳骨架主要为无定形碳, 碳骨架上依然存在有机官能团, 培养温度升高提高了微生物活性, 从而增加了碳骨架上的可利用部分.对于BC800及W800, H/C值皆小于0.35, 表明有机官能团裂解更完全, 且晶体碳部分占主导(Sun et al., 2017).实验空白产生了少量的CO2, 这可能是因为缺少有机物, 使得微生物进行内源呼吸.BC800及W800累积矿化量比空白低, 即使环境温度升高, W800的相对难降解碳含量仍然保持最高.根据酶反应动力学, 相对难降解碳的分子结构较易降解碳复杂, 其含量升高, 被微生物降解便需要更多的活化能和反应步骤, 所以具有更好的固碳效果.
本文的研究目标为探究不同热解温度的生物炭的易降解和相对难降解碳在土壤中的矿化作用及其机理, 为了减少土壤其他因素(如有机质)的干扰, 实验中采用了模拟的不含有机质土壤, 但实际土壤更为复杂, 后期将使用实际土壤开展进一步的研究.
5 结论(Conclusions)1) 与原材料相比, 生物炭的矿化速率和易降解碳含量显著降低(p<0.05), 且随热解温度升高, 易降解碳含量降低, 易降解碳和相对难降解碳的平均停留时间变长.
2) 当环境温度为25 ℃时, 碳骨架的累积矿化量和易降解碳含量皆低于生物炭, 说明碳骨架缺少生物炭中可被微生物利用的溶解性有机碳, 芳香烃碳聚合程度提高, 在土壤中的稳定性更强.
3) 当环境温度为35 ℃时, 300 ℃和500 ℃碳骨架的易降解碳含量高于相应生物炭, 说明热解温度较低的碳骨架在环境温度升高时其微生物可利用性增加.
4) 当环境温度升至35 ℃时, 800 ℃制备的生物炭及其碳骨架的累积矿化量依然比空白低, 且碳骨架的相对难降解碳含量也一直保持最高, 表明800 ℃制备的生物炭具有更好的碳汇作用.
Asadullah M, Zhang S, Li C Z. 2010. Evaluation of structural features of chars from pyrolysis of biomass of different particle sizes[J]. Fuel Processing Technology, 91(8): 877–881.
DOI:10.1016/j.fuproc.2009.08.008
|
Barker G. 2011. Positive and negative carbon mineralization priming effects among a variety of biochar-amended soils[J]. Soil Biology & Biochemistry, 43(6): 1169–1179.
|
Baldock J A, Smernik R J. 2002. Chemical composition and bioavailability of thermally altered Pinus resinosa (Red pine) wood[J]. Organic Geochemistry, 33(9): 1093–1109.
DOI:10.1016/S0146-6380(02)00062-1
|
Brodowski S B.2005.Origin, function, and reactivity of black carbon in the arable soil environment[D].Bonn, Germany:Institute of Crop Science and Resource Conservation-Division of Soil Science, Univ of Bonn
|
Cao X, Harris W. 2010. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation[J]. Bioresource Technology, 101(14): 5222–5228.
DOI:10.1016/j.biortech.2010.02.052
|
Cheng C H, Lehmann J, Thies J E, et al. 2006. Oxidation of black carbon by biotic and abiotic processes[J]. Organic Geochemistry, 37(11): 1477–1488.
DOI:10.1016/j.orggeochem.2006.06.022
|
Cohenofri I, Popovitzbiro R, Weiner S. 2007. Structural characterization of modern and fossilized charcoal produced in natural fires as determined by using electron energy loss spectroscopy[J]. Chemistry, 13(8): 2306–2310.
DOI:10.1002/(ISSN)1521-3765
|
Fang Y, Singh B, Singh B P, et al. 2014. Biochar carbon stability in four contrasting soils[J]. European Journal of Soil Science, 65(1): 60–71.
|
Glaser B, Haumaier L, Guggenberger G, et al. 2001. The 'Terra Preta' phenomenon:a model for sustainable agriculture in the humid tropics[J]. The Science of Nature, 88(1): 37–41.
DOI:10.1007/s001140000193
|
Goldberg E D.1985.Black Carbon in the Environment:Properties and Distribution[M]. New York:John Wiley
|
Hammes K, Schmidt M W I, Smernik R J, et al. 2007. Comparison of quantification methods to measure fire-derived (black/elemental) carbon in soils and sediments using reference materials from soil, water, sediment and the atmosphere[J]. Global Biogeochemical Cycles, 21(3): B3016.
|
Hamer U, Marschner B, Brodowski S, et al. 2004. Interactive priming of black carbon and glucose mineralisation[J]. Organic Geochemistry, 35(7): 823–830.
DOI:10.1016/j.orggeochem.2004.03.003
|
Hernandez-Soriano M C, Bart K, Kopittke P M, et al. 2016. Biochar affects carbon composition and stability in soil:a combined spectroscopy-microscopy study[J]. Scientific Reports, 6: 25127.
DOI:10.1038/srep25127
|
Jones D L, Murphy D V, Khalid M, et al. 2011. Short-term biocharinduced increase in soil CO2 release is both biotically and abiotically mediated[J]. Soil Biology & Biochemistry, 43(8): 1723–1731.
|
Keith A, Singh B, Singh B P. 2014. Interactive priming of biochar and labile organic matter mineralization in a smectite-rich soil[J]. Environmental Science & Technology, 45(22): 9611–9618.
|
Lehmann J. 2007. A handful of carbon[J]. Nature, 447(7141): 143.
DOI:10.1038/447143a
|
Lehmann J, Solomon D, Kinyangi J, et al. 2008. Spatial complexity of soil organic matter forms at nanometre scales[J]. Nature Geoscience, 1(4): 238–242.
DOI:10.1038/ngeo155
|
Lehmann J D, Joseph S. 2009. Biochar for environmental management:science and technology[J]. Science and Technology, Earthscan, 25(1): 15801–15811.
|
Liang B, Lehmann J, Solomon D, et al. 2008. Stability of biomass-derived black carbon in soils[J]. Geochimica et Cosmochimica Acta, 72(24): 6069–6078.
DOI:10.1016/j.gca.2008.09.028
|
Liang B Q, Lehmann J, Sohi S P, et al. 2010. Black carbon affects the cycling of non-black carbon in soil[J]. Organic Geochemistry, 41(2): 206–213.
DOI:10.1016/j.orggeochem.2009.09.007
|
Li X, Hayashi J, Li C. 2006. FT-Raman spectroscopic study of the evolution of char structure during the pyrolysis of a Victorian brown coal[J]. Fuel, 85: 1700–1707.
DOI:10.1016/j.fuel.2006.03.008
|
Lim S S, Choi W J. 2014. Changes in microbial biomass, CH4 and CO2 emissions, and soil carbon content by fly ash co-applied with organic inputs with contrasting substrate quality under changing water regimes[J]. Soil Biology & Biochemistry, 68(1): 494–502.
|
Lou Y M, Joseph S, Li L Q, et al. 2015. Water extract from straw biochar used for plant growth promotion:an initial test[J]. Bioresources, 11(1): 249–266.
|
Marris E. 2006. Putting the carbon back black is the new green[J]. Nature, 442(7103): 624–626.
DOI:10.1038/442624a
|
Mun G J, Kim Y M, Kim D K, et al. 2009. Black carbon decomposition and incorporation into soil microbial biomass estimated by 14C labeling[J]. Soil Biology & Biochemistry, 41(2): 210–219.
|
Scott A, Glasspool I. 2007. Observations and experiments on the origin and formation of inertinite group macerals[J]. International Journal of Coal Geology, 70: 53–66.
DOI:10.1016/j.coal.2006.02.009
|
Sun T, Levin B D, Guzman J J, et al. 2017. Rapid electron transfer by the carbon matrix in natural pyrogenic carbon[J]. Nature Communications, 8: 14873.
DOI:10.1038/ncomms14873
|
唐倩, 梁卓良, 欧阳磊, 等. 2014. 生物碳的物理结构与化学成分对土壤氧化亚氮排放的影响[J]. 环境科学学报, 2014, 34(11): 2839–2845.
|
Wang J, Xiong Z, Kuzyakov Y. 2016. Biochar stability in soil:meta-analysis of decomposition and priming effects[J]. Global Change Biology Bioenergy, 8(3): 512–523.
DOI:10.1111/gcbb.2016.8.issue-3
|
Woolf D, Amonette J E, Street-Perrott F A, et al. 2010. Sustainable biochar to mitigate global climate change[J]. Nature Communications, 1(5): 1–9.
|
Zimmerman A R. 2010. Abiotic and microbial oxidation of laboratory-produced black carbon (biochar)[J]. Environmental Science & Technology, 44(4): 1295–1301.
|
 2018, Vol. 38
2018, Vol. 38


