2. 中国海洋大学海洋环境与生态教育部重点实验室, 青岛 266100
2. Key Laboratory of Marine Environment and Ecological Education, Ocean University of China, Qingdao 266100
地下水是人们生活和社会发展必须的重要资源, 广泛应用于居民生活、农业灌溉、工业生产等领域(Menció et al., 2016; Rodriguez-Galiano et al., 2018).但随着工农业迅速发展、人口增加、城市化进程加快, 地下水的污染问题也愈发严峻(Huan et al., 2018).其中, 地下水硝酸盐污染已成为国际上普遍关注的环境问题(Chen et al., 2005; Chen et al., 2007).地下水硝酸盐污染来源广泛, 有农业施用的化肥、生活污水和工业废水、固体废弃物的渗滤液、污水回灌及大气干湿沉降等(Zhang et al., 2018).其中, 固体废弃物渗滤液造成的污染可分为两类:①垃圾渗滤液下渗造成的地下水污染;②畜禽养殖粪污渗滤液造成的地下水污染(毕晶晶等, 2010).我国畜牧业快速发展, 粪污的产生量不断增加.据2007年全国污染源普查结果显示, 畜禽养殖业的粪便总产生量高达2.43×108 t.其中含氮量为102.48×108 t, 占农业污染源氮素总排放量的38%(仇焕广等, 2013; 刘明等, 2017).同时, 我国规模化养殖较为落后, 多数养殖场为中小规模(吴昊等, 2014; 赵兴征等, 2015), 缺乏防雨、防渗设施和基本的污染治理设备, 通常采用自然堆肥技术对粪污熟化处理(Li et al., 2016).但在降雨淋溶作用下粪肥中的有机氮组分会渗入土壤, 并通过氨化作用转化为氨氮(Dong et al., 2018).其中一部分氨氮被土壤吸附或被植物吸收, 另外一部分在微生物的作用下发生硝化反应, 生成亚硝态氮和硝态氮.亚硝态氮很不稳定, 而硝态氮会通过淋溶进入地下水, 造成地下水硝酸盐污染(胡敏杰等, 2016).
地下水污染治理技术可分为原位处理和抽出处理两大类(姜烈等, 2014).抽出处理是较为常用的技术, 短期处理效率高, 但长期普遍存在拖尾、反弹等现象, 且成本高昂.地下水原位修复技术是通过人为干预, 在污染发生处将受污染地下水体修复的方法, 具备污染修复效果良好、环境扰动小, 成本低廉等优势(董慧峪等, 2010).但地下水中硝酸盐迁移能力强, 原位修复具有局限性.因此, 对地下水的硝酸盐污染问题应更加注重防控(冯锦霞等, 2006).粪污中污染物浓度较高(Girotto and Cossu, 2017; Ren et al., 2010), 而土壤非饱和带中的有机碳含量较低, 反硝化反应会受限, 因此需要外加碳源.反硝化层是通过人工添加固体有机物强化反硝化作用来实现硝酸盐去除的修复技术.微生物将固体有机物水解产生的小分子有机物作为碳源, 在4种金属酶(硝酸盐还原酶、亚硝酸盐还原酶、一氧化氮还原酶和氧化亚氮还原酶)催化作用下, 将硝酸盐最终还原为氮气(Wang and Chu, 2016).日本学者高畑等(2013)曾使用工业用硬脂酸作为持续性碳源, 设计了在农耕地下铺设水平脱氮层以阻控硝酸盐污染渗入地下水的试验, 取得了较好的硝酸盐去除效果.但其碳源造价较高, 且试验中设计的脱氮反应层厚度较薄(20 cm), 对于高浓度含氮废水的持续处理能力未知.相比之下, 木质生物质作为碳源具有廉价易获取、使用寿命长、副产物少(亚硝酸盐、氧化亚氮、溶解性有机物)等优点(李同燕等, 2015; 陆松柳等, 2011; 宋宇杰等, 2013).Hu等(2017)采用熟石灰对木屑进行预处理, 提高了木屑释碳能力, 强化了脱氮效能.
本文针对典型的养殖场粪污堆肥污染, 在土壤非饱和带中构建强化脱氮反应层, 揭示反应层内部环境特征以及非饱和带中硝酸盐的浓度变化规律, 计算出反应层的脱氮能力, 从而阻控硝酸盐污染物渗入地下水.本研究对防控地下水硝酸盐污染具有重要的科学意义和应用价值.
2 材料和方法(Materials and methods) 2.1 供试材料 2.1.1 碳源材料采用处理木屑作为碳源材料.木屑原料为山东省产白杨木, 粒径0.18~0.7 mm, 总有机碳(TOC)为480 g·kg-1, 总氮(TN)为1400 mg·kg-1.木屑在熟石灰投加量为100 mg·kg-1和95 ℃条件下处理24 h, 然后进行抽滤, 至滤液的pH为7后烘干备用(Hu et al., 2017).
2.1.2 土样原位试验场布置于山东省青岛莱西市店埠镇东庄头村(36°43′ N, 120°20′E)某畜禽养殖厂的堆肥场.供试土样包括壤土和砂土.壤土样取自试验场地地表 10~30 cm深度原位壤土, 其pH为6.7, 硝态氮、TN和TOC的含量分别为60.5、500、3300 mg·kg-1;砂土样取自附近河砂, 其粒径小于2.0 mm, 中值粒径为0.45 mm, 属于中砂.
2.1.3 粪肥采用猪粪及其渗滤液模拟粪肥污染源.猪粪取至山东省店埠镇养猪场, 硝酸盐氮为63 mg·kg-1, TOC和TN分别为401 g·kg-1和22 g·kg-1.
2.1.4 水样试验水样由自来水与猪粪渗滤液按照体积比5:2混合配置.各批次配水中化学物质浓度存在一定差异, 取其平均值, 硝态氮浓度为170.00 mg·L-1, 亚硝态氮浓度为0.25 mg·L-1, 铵态氮浓度为3.15 mg·L-1, pH为7.1, 化学需氧量(COD)为483 mg·L-1.
2.2 试验装置现场试验装置主要由圆形土柱、采样装置、含水量测试系统等组成(图 1).土柱为PVC管材, 分上下两个部分:上部为等直径管(φ40 cm×150 cm), 为试验的渗流区;下部为变径管, 底部进行了密封, 高度为20 cm, 为试验的集水区.
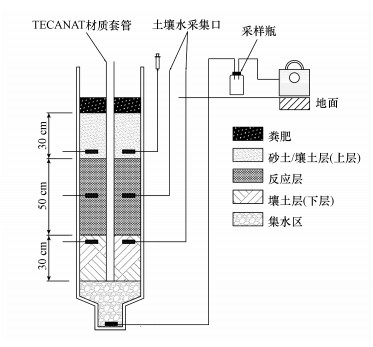 |
| 图 1 脱氮试验装置示意图 Fig. 1 A schematic diagram of the denitrification test device |
在距装置顶部55、85和115 cm处两侧的对称部位埋设6个取样陶土头, 其直径为2.5 mm, 而微孔的平均孔径为0.15 μm, 用透明延长管与取样陶土头相连接, 通过土壤水分采样器(Rhizon, 荷兰)采集不同深度的水样.另外, 在集水区的底端设置一个出水口, 使用真空泵抽取底部出水至采样瓶, 用于出水体积测量和水质分析.从土柱渗流区的顶部开始埋设一根直径为5 cm的专用TECANAT材质套管, 采用水分传感器(TRIME-PICO-IPH, 德国)测定不同深度上含水介质的温度和体积含水量.
2.3 试验方法 2.3.1 装置构建现场试验设置为对照组、壤土组和砂土组, 并依次标记为CK、1#和2#处理, CK处理从下至上分为5层, 依次填充砾石、壤土(下层)、壤土、壤土(上层)、粪肥, 其厚度分别为30、30、50、30和10 cm;1#和2#处理从下至上也分为5层, 厚度与CK相同, 依次填充砾石、壤土(下层)、反应层、壤土(1#)或砂土(2#)(上层)、粪肥.反应层的具体构建方法为:①分层挖掘深度为150.0 cm的基坑, 取地表下0~30 cm的土样, 并筛分去除大于4.0 mm颗粒杂物;②将实验装置放入基坑, 在各处理底部分别铺设砾石层, 并将含水率观测孔底端设置在砾石层顶部, 顶端至地表以上30.0 cm;③各处理下层按等容重(1.5 g·cm-3)法分层(5 cm)将壤土装入土柱;④在埋设反应层时, 按土样与木屑的质量比(9:1)进行混合后, 将混合材料按等容重(1.2 g·cm-3)分层填入土柱;⑤对于1#和2#处理, 上层分别按等容重的壤土(1.5 g·cm-3)和砂土(1.65 g·cm-3)分层填充;⑥各处理土柱的顶部铺设10.0 cm的粪肥层.具体情况参考图 1.
2.3.2 试验运行从9月13日开始, 每15 d灌水1次.灌水前配置水样并静置, 待稳定后分别向CK、1#、2#处理中一次性灌水12 L(100 mm).试验期间总共灌水6次, 至12月10日结束试验.在各批次灌水试验中第1、3、5、7、10和14 d, 用套管式TDR水分传感器分别测定CK、1#、2#处理的剖面温度和体积含水率.套管式TDR水分传感器可通过测定电磁波的传播速度差异确定介质的介电常数, 并由介电常数与体积含水率的数学关系计算出介质的体积含水率(张瑞国等, 2016);第3、7 d, 使用土壤水分采样器采集土壤水样带回实验室分析;第7、15 d, 用真空泵抽取集水区出水, 记录处理水量.
2.3.3 分析方法土壤水和出水水样经过滤后, 分别测定水样的NO3--N、NO2--N、NH4+-N的浓度及COD值和pH值.其中, NO3--N、NO2--N和NH4+-N浓度分别用N-(1-萘基)-乙二胺光度法、紫外分光光度法和纳氏试剂光度法进行测定;COD用重铬酸钾氧化法测定;pH值用电极探头(哈希HQ40D, 美国)进行测定.
3 结果与讨论(Results and discussion) 3.1 非饱和带反硝化系统的环境特征从9月开始试验, 气温持续降低, 1#处理反应层剖面温度和地表温度均呈下降趋势(图 2a).后者变化幅度较为平缓, 由25 ℃逐渐降低至10 ℃.因反应层位于地面以下75 cm, 对地表温度变化具有一定的缓冲作用.所以当地表温度降至0 ℃时, 反应层内温度维持在10 ℃以上, 保持了反硝化微生物的活性.
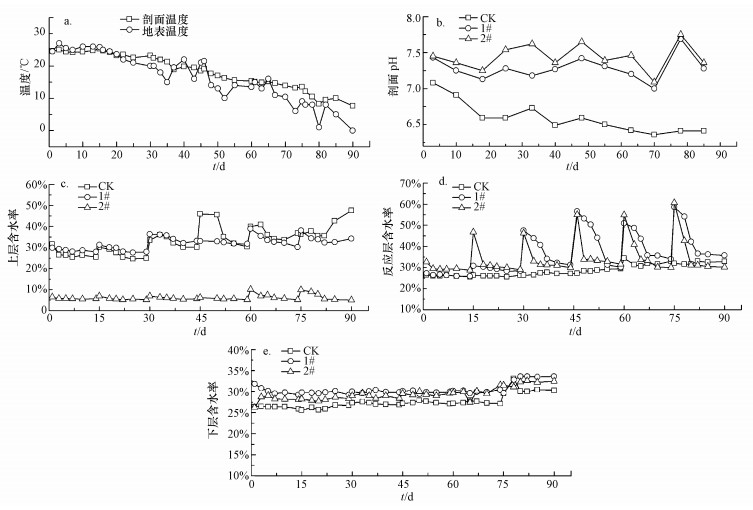 |
| 图 2 3种处理(CK、1#、2#)的温度(a)、剖面pH(b)、上层含水率(c)、反应层含水率(d)、下层含水率(e)随时间变化曲线 Fig. 2 The temperature (a), profile pH (b), moisture content of upper soil (c), moisture content of reaction layer (d), moisture content of lower soil (e) of 3 kinds of treatments (CK, 1#, 2#) over time |
1#、2#处理反应层及CK的相应层位pH动态变化如图 2b所示.CK处理pH随时间降低, 这主要是发生了硝化作用, 氨氮向硝态氮转化的同时会产生酸, 使土壤环境酸化;1#和2#处理的pH同步波动且高于进水, 均值分别为7.28、7.32.反硝化过程会产生一定量的碱从而使pH升高.另外, 由于2#处理上层为砂土, 渗透性较强.灌水后水分快速入渗反应层, 减少了上层水分蒸发量, 增加了处理水量, 使得2#处理的脱氮总量更多, 发生了较强的反硝化作用, 所以pH高于1#处理.
在间歇灌水条件下, CK和1#处理在灌水后5 d内水分完全渗入表层以下, 2#处理灌水后30 min内水分完全渗入表层以下.由于2#处理上层砂土的渗透性较强, 使其入渗速度明显快于CK和1#处理.CK、1#、2#处理的上层含水量随灌水呈现周期性波动(图 2c), CK和1#处理波形明显, 含水量明显高于2#处理.这是由于其上层为壤土, 灌水呈均匀稳定下渗状态, 地表积水不断补充上层水分, 使含水量维持在相对高位.同时, CK和1#处理的含水量随灌水批次升高, 可能是因为试验过程中气温逐渐降低, 土壤水分蒸发速率变缓, 导致含水量上升.
1#、2#处理反应层和CK处理相同层位的含水量随灌水周期同步变化(图 2d).CK处理含水量波动平缓, 1#、2#处理的含水量波动剧烈.这是因为木屑具有较强的吸水性, 灌水后吸水膨胀, 填充反应层内部空隙并吸附更多水分, 使反应层含水量短时间内迅速升高.1#处理的含水量缓慢降低, 2#处理的含水量迅速下降.这是因为2#处理上层渗透性强, 灌水后水分集中且快速入渗反应层, 并在处理后流出.而1#处理上层渗透性弱, 灌水后呈连续稳定的下渗状态, 一段时间内反应层可得到上层的水量补给, 所以含水量降低缓慢.同时, 2#处理上层含水量较低, 有利于反应层水分蒸发, 加快了其含水量降低速率.试验前期1#和2#处理的反应层含水量逐次升高, 这是因为试验初始阶段土柱内部较为干燥, 灌入的一部分水分被土壤吸收, 随着试验进行, 土柱含水率变化范围趋于稳定.
CK、1#、2#处理的下层含水量总体呈平稳状态(图 2e).随灌水周期, CK处理波动平缓, 1#和2#处理则未出现明显的波形, 且含水量略高于CK处理.由于下层均为壤土, 而底部集水区可视为自由排泄边界, 所以反应层出水量差异是造成3种处理下层含水量差异的主要原因.CK处理中, 上方壤土对灌水形成滤波, 下层含水量波动在时间上滞后于灌水周期, 波幅上较为平缓.1#和2#处理未产生明显的波形, 通过测定其反应层和下层界面处的含水量, 发现界面上方含水量始终保持在60%以上, 下方骤降至30%附近.据此可推测在反应层底部界面处产生了积水, 从而为下层提供了稳定流量的上边界.所以试验中1#和2#处理的下层含水量基本保持恒定, 与灌水周期无明显关联.
3.2 现场强化反应层的脱氮行为 3.2.1 COD垂向分布间歇性淋溶粪肥, 取3种处理中不同剖面上COD平均值, 见图 3a.由图可知, 上层中CK、1#和2#处理的COD随深度增加而降低.反应层中1#和2#处理COD明显升高, CK处理相同层位COD继续降低.下层中, 各处理COD均随深度增加缓慢降低.上层COD降低是因为壤土或砂土通过截留作用去除了淋溶出的部分有机物.CK和1#处理比2#处理浓度下降更多是因为壤土截留效果好于砂土.1#和2#处理反应层中COD升高是因为木屑在微生物作用下水解释放出大量的溶解性有机碳, 供给反硝化微生物进行脱氮.2#处理的COD高于1#处理, 因为其处理水量大, 含NO3--N总量多, 而氮源是制约木屑水解的关键因素之一, 丰富的氮源有利于木屑的水解(宋宇杰等, 2013), 所以2#反应层中释放出了更多的有机碳.但1#和2#处理出水COD较高, 这主要是由于反应层木屑水解释放碳源过多导致的, 在实际应用中应适量减少木屑配比.
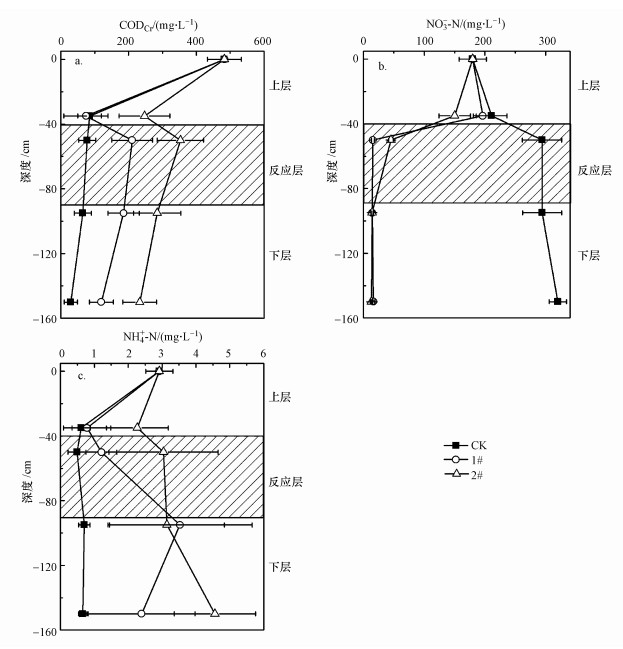 |
| 图 3 间歇性灌水条件下3种处理(CK、1#、2#)COD(a)、NO3--N(b)和NH4+-N(c)浓度的垂向分布 Fig. 3 The vertical distribution of COD(a)、NO3--N(b) and NH4+-N(c) concentration in 3 kinds of treatments (CK, 1# and 2#) in intermittent irrigation |
各处理中NO3--N浓度的变化如图 3b所示.CK处理中NO3--N浓度随深度增加持续升高, 这是因为从粪肥中淋溶出的有机氮在非饱和带中经过氨化作用转化为氨氮, 一部分氨氮被壤土吸附, 另一部分则通过硝化作用转化为NO3--N随渗流垂向迁移, 使CK处理中NO3--N浓度不断上升.1#处理上层NO3--N浓度随深度增加而增加, 2#处理上层NO3--N浓度随深度增加小幅降低, 渗入反应层后两者NO3--N浓度均迅速降低.当进水NO3--N浓度为170 mg·L-1时, CK、1#和2#处理的出水NO3--N浓度分别为310.27、6.29和2.95 mg·L-1.1#和2#处理的反应层对NO3--N去除率分别达到97.63%和96.98%.反应层可以高效脱氮的原因在于它同时提供了有利于反硝化进行的缺氧环境和有效碳源.灌水后由于木屑的强吸水特性, 反应层含水量迅速升高, 气体(O2)向反应层内部的扩散速率随之降低(Mekala and Nambi, 2017), 从而使反应层内形成厌氧环境.较高的含水量也增加了底物的迁移扩散能力并且对微生物的繁殖代谢产生积极影响(Rubol et al., 2013).更为重要的是, 反应层中的木屑在水解类微生物作用下释放出溶解性有机碳, 它们被直接提供给反硝化微生物进行脱氮.因为有效碳含量是限制生物反硝化最为关键的因素, 所以在碳源充足的条件下, 反应层中的NO3--N被充分去除.
3.2.3 亚硝酸盐氮的去除效果CK、1#、2#处理的出水NO2--N浓度均低于0.5 mg·L-1, 可忽略不计.土壤中的硝化和反硝化作用均会生成中间产物NO2--N, 且土壤含水率大于田间持水量的80%时主要发生反硝化作用(杜晓娜, 2016).强化反应层具有较高的含水量和有机物浓度, 容易形成缺氧环境, 这说明亚硝酸盐主要来源于反硝化作用.亚硝酸盐作为反硝化的中间产物, 可以被亚硝酸盐还原酶和氧化亚氮还原酶最终还原为氮气, 而发生完全反硝化过程.由于反应层中木屑提供了充足的碳源, 使得反硝化过程完全进行, 生成的NO2--N很快被进一步还原, 所以几乎不发生累积.
3.2.4 氨氮浓度的垂向分布NH4+-N在3种处理不同剖面的分布情况如图 3c所示.上层中, CK、1#和2#的NH4+-N浓度随深度增加而降低, 且2#处理的NH4+-N浓度降低幅度比CK和1#处理小.反应层中, 1#和2#处理的NH4+-N浓度随深度增加呈上升趋势, 而CK处理相同层位NH4+-N浓度则相对较低.下层中, CK和1#处理的NH4+-N浓度随深度增加降低, 而2#处理的NH4+-N浓度随深度增加而升高.CK、1#和2#处理的出水NH4+-N平均浓度分别为0.32、2.50和5.20 mg·L-1.造成NH4+-N浓度变化的主要原因是土壤吸附作用和DNRA(Dissimilatory nitrate reduction to ammonium)过程.铵态氮在土壤中发生的吸附机制与土壤界面性质有关, 试验中壤土表面带有负电荷, 其对于铵态氮吸附作用主要为离子交换作用(杜青青等, 2017).随着下渗深度增加, 土壤对铵态氮的吸附量增大, 所以上层中各处理NH4+-N浓度呈降低趋势.基于不同类型介质吸附试验和Langmuir模型, 砂质土对铵态氮的吸附能力低于壤土(陈坚, 2011), 所以2#处理上层氨氮的降低幅度小于CK和1#处理.反应层中NH4+-N浓度上升主要是因为发生了DNRA作用.一般认为, DNRA强度受缺氧环境和有机质含量的影响(Salk et al., 2017; Zhang et al., 2015), 反应层内部兼具缺氧环境条件和充足碳源, 使得部分硝态氮在微生物作用下经由DNRA途径异化还原为铵, 而1#处理反应层中NH4+-N浓度增加幅度大于2#处理, 这可能是因为灌水后1#处理反应层较长时间保持了较高的含水量, 延长了缺氧环境持续时间, 从而增加了DNRA的反应时间, 产生更多的NH4+-N.在下层中, 处理水量较小的CK和1#处理渗流中的NH4+被壤土充分吸附而得以去除.2#处理的出水流量较大, NH4+离子得不到充分吸附而随水流出, 所以出水中NH4+-N浓度略有升高.
3.3 强化反应层的脱氮量采用各批次灌水试验反应层进水和出水NO3--N浓度差平均值与处理水量的乘积计算反应层的总脱氮量, 用总脱氮量除以反应层体积计算出单位体积反应层脱氮量, 结果如图 4所示.前3批次试验脱氮量较少是因为启动阶段处理水量较少.后3次试验处理水量趋于稳定, 在灌水量为100 mm条件下, CK、1#和2#处理反应层的平均处理水量分别为31.85、30.7和70.6 mm.CK处理的脱氮量没有在图中展示, 是因为其NO3--N浓度随深度增加而升高, 使得计算脱氮量为负值.1#和2#处理中平均脱氮量分别为9.56 g·m-3和24.61 g·m-3, 2#处理脱氮量明显高于1#处理.这是因为在进水NO3--N浓度为170 mg·L-1条件下, 装置的处理能力尚未达到饱和, 所以尽管处理水量差异较大, 对NO3--N去除率却十分接近.此时造成脱氮量差异的主要因素在于处理水量的多少, 2#处理的处理水量较大, 因此脱氮量更高.
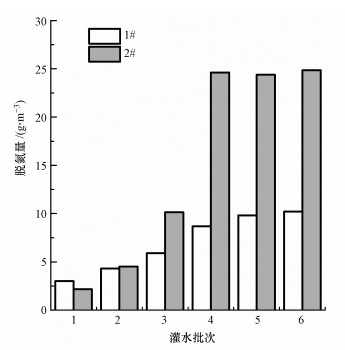 |
| 图 4 1#和2#处理反应层脱氮量的批次变化 Fig. 4 The batch change of the removal amount of nitrogen in the enhanced reaction layer of 1# and 2# treatments |
1) 反应层中的木屑材料具有强吸水特性, 灌水后短时间内使反应层含水量大幅提升, 形成有利于反硝化反应进行的厌氧环境.木屑在水解类微生物作用下释放出溶解性有机碳, 供给反硝化微生物进行脱氮.
2) 在入渗硝态氮浓度为170.00 mg·L-1条件下, 1#和2#处理反应层NO3--N的去除率分别为97.63%和96.98%.上层选用渗透性较强的砂土可以提升反应层处理水量, 进而使脱氮量显著提高.在灌水量为100 mm条件下, 1#和2#处理的平均处理水量分别为30.7 mm和70.6 mm, 脱氮量分别为9.56 g·m-3和24.61 g·m-3.
3) 反应层内碳源充足, NO3--N发生了完全反硝化, 出水NO2--N浓度低于0.5 mg·L-1, 几乎不发生积累.反应层中发生的DNRA过程使其内部NH4+-N浓度小幅升高.
毕晶晶, 彭昌盛, 胥慧真. 2010. 地下水硝酸盐污染与治理研究进展综述[J]. 地下水, 2010, 32(1): 97–102.
|
陈坚. 2011.铵态氮在包气带介质中的吸附机制及转化去除研究[D].北京: 中国地质大学(北京). 166
http://cdmd.cnki.com.cn/Article/CDMD-11415-1011077662.htm |
Chen J, Tang C, Sakura Y, et al. 2005. Nitrate pollution from agriculture in different hydrogeological zones of the regional groundwater flow system in the North China Plain[J]. Hydrogeology Journal, 13(3): 481–492.
DOI:10.1007/s10040-004-0321-9
|
Chen J, Taniguchi M, Liu G, et al. 2007. Nitrate pollution of groundwater in the Yellow River delta, China[J]. Hydrogeology Journal, 15(8): 1605–1614.
DOI:10.1007/s10040-007-0196-7
|
Dong L, Lin L, Li Q, et al. 2018. Enhanced nitrate-nitrogen removal by modified attapulgite-supported nanoscale zero-valent iron treating simulated groundwater[J]. Journal of Environmental Management, 213: 151–158.
|
董慧峪, 强志民, 李庭刚, 等. 2010. 污染河流原位生物修复技术进展[J]. 环境科学学报, 2010, 30(8): 1577–1582.
|
杜青青, 尹芝华, 左锐, 等. 2017. 某污染场地氨氮迁移过程模拟研究[J]. 中国环境科学, 2017, 37(12): 4585–4595.
|
杜晓娜. 2016.反硝化过程中亚硝酸盐积累影响因素与稳定运行[D].天津: 天津大学. 66
|
冯锦霞, 朱建军, 陈立. 2006. 我国地下水硝酸盐污染防治及评估预测方法[J]. 地下水, 2006, 28(4): 58–62.
|
Girotto F, Cossu C A. 2017. Animal waste and waste animal by-products generated along the livestock breeding and meat food chain[J]. Waste Management, 70: 1–2.
DOI:10.1016/j.wasman.2017.11.028
|
Hu R, Zheng X, Xin J, et al. 2017. Selective enhancement and verification of woody biomass digestibility as a denitrification carbon source[J]. Bioresource Technology, 244: 313–319.
DOI:10.1016/j.biortech.2017.07.162
|
Huan H, Zhang B, Kong H, et al. 2018. Comprehensive assessment of groundwater pollution risk based on HVF model:A case study in Jilin City of northeast China[J]. Science of The Total Environment, 628-629: 1518–1530.
DOI:10.1016/j.scitotenv.2018.02.130
|
胡敏杰, 邹芳芳, 仝川, 等. 2016. 氮、硫输入对河口湿地土壤有机碳矿化的实验研究[J]. 环境科学学报, 2016, 36(11): 4184–4192.
|
姜烈, 何江涛, 姜永海, 等. 2014. 地下水硝酸盐污染抽出处理优化方法模拟研究[J]. 环境科学, 2014, 35(7): 2572–2578.
|
Li F, Cheng S, Yu H, et al. 2016. Waste from livestock and poultry breeding and its potential assessment of biogas energy in rural China[J]. Journal of Cleaner Production, 126: 451–460.
DOI:10.1016/j.jclepro.2016.02.104
|
李同燕, 李文奇, 胡伟武, 等. 2015. 玉米秆碳源去除地下水硝酸盐[J]. 环境工程学报, 2015, 9(9): 4245–4251.
|
刘明, 黄荣, 李明, 等. 2017. 畜禽粪污处理技术标准现状研究[J]. 中国标准化, 2017(24): 40–42.
|
陆松柳, 张辰, 王国华. 2011. 碳源强化对人工湿地反硝化过程的影响研究[J]. 环境科学学报, 2011, 31(9): 1949–1954.
|
Mekala C, Nambi I M. 2017. Understanding the hydrologic control of N cycle:Effect of water filled pore space on heterotrophic nitrification, denitrification and dissimilatory nitrate reduction to ammonium mechanisms in unsaturated soils[J]. Journal of Contaminant Hydrology, 202: 11–22.
DOI:10.1016/j.jconhyd.2017.04.005
|
Menció A, Mas-Pla J, Otero N, et al. 2016. Nitrate pollution of groundwater; all right…, but nothing else?[J]. Science of The Total Environment, 539: 241–251.
DOI:10.1016/j.scitotenv.2015.08.151
|
仇焕广, 廖绍攀, 井月, 等. 2013. 我国畜禽粪便污染的区域差异与发展趋势分析[J]. 环境科学, 2013, 34(7): 2766–2774.
|
Ren L, Wu Y, Ren N, et al. 2010. Microbial community structure in an integrated A/O reactor treating diluted livestock wastewater during start-up period[J]. Journal of Environmental Sciences, 22(5): 656–662.
DOI:10.1016/S1001-0742(09)60159-5
|
Rodriguez-Galiano V F, Luque-Espinar J A, Chica-Olmo M, et al. 2018. Feature selection approaches for predictive modelling of groundwater nitrate pollution:An evaluation of filters, embedded and wrapper methods[J]. Science of The Total Environment, 624: 661–672.
DOI:10.1016/j.scitotenv.2017.12.152
|
Rubol S, Manzoni S, Bellin A, et al. 2013. Modeling soil moisture and oxygen effects on soil biogeochemical cycles including dissimilatory nitrate reduction to ammonium (DNRA)[J]. Advances in Water Resources, 62: 106–124.
DOI:10.1016/j.advwatres.2013.09.016
|
Salk K R, Erler D V, Eyre B D, et al. 2017. Unexpectedly high degree of anammox and DNRA in seagrass sediments:Description and application of a revised isotope pairing technique[J]. Geochimica et Cosmochimica Acta, 211: 64–78.
DOI:10.1016/j.gca.2017.05.012
|
宋宇杰, 李屹, 刘玉香, 等. 2013. 碳源和氮源对异养硝化好氧反硝化菌株Y1脱氮性能的影响[J]. 环境科学学报, 2013, 33(9): 2491–2497.
|
Wang J, Chu L. 2016. Biological nitrate removal from water and wastewater by solid-phase denitrification process[J]. Biotechnology Advances, 34(6): 1103–1112.
DOI:10.1016/j.biotechadv.2016.07.001
|
吴昊, 管永祥, 梁永红, 等. 2014. 江苏省太湖流域畜禽养殖污染治理现状及政策建议[J]. 江苏农业科学, 2014, 42(12): 401–403.
|
陽高畑, 雅子伊藤, 健太郎増岡, 等. 2013. 水平透過性浄化壁を用いる地下水の硝酸性窒素汚染防止対策技術の検証[J]. 土木学会論文集G(環境), 2013, 2(69): 84–96.
|
Zhang J, Lan T, Müller C, et al. 2015. Dissimilatory nitrate reduction to ammonium (DNRA) plays an important role in soil nitrogen conservation in neutral and alkaline but not acidic rice soil[J]. Journal of Soils and Sediments, 15(3): 523–531.
DOI:10.1007/s11368-014-1037-7
|
Zhang W, Ruan X, Bai Y, et al. 2018. The characteristics and performance of sustainable-releasing compound carbon source material applied on groundwater nitrate in-situ remediation[J]. Chemosphere, 205: 635–642.
DOI:10.1016/j.chemosphere.2018.04.133
|
张瑞国, 罗强, 蒋良潍, 等. 2016. 套管式TDR水分传感器侧向感应范围试验分析[J]. 铁道科学与工程学报, 2016, 13(5): 827–835.
|
赵兴征, 刘晨峰, 郭黎卿, 等. 2015. _十二五_畜禽养殖污染减排问题及防治对策_刘晨峰[J]. 环境污染与防治, 2015, 37(3): 86–89.
|
 2018, Vol. 38
2018, Vol. 38


