2. 湿润亚热带生态-地理过程教育部重点实验室, 福州 350007;
3. 福建师范大学亚热带湿地研究中心, 福州 350007
2. Key Laboratory of Humid Sub-tropical Eco-geographical Process of Ministry of Education, Fuzhou 350007;
3. Research Centre of Wetlands in Subtropical Region, Fujian Normal University, Fuzhou 350007
作为一种重要的温室气体, N2O在100年时间尺度上增温效应约为CO2的298倍(IPCC, 2007).N2O在大气层中寿命达150年, 对全球环境具有潜在且长期的影响(Prinn et al., 1990).大气中N2O主要来自土壤反硝化和硝化过程, 其产生的N2O约占全球大气中N2O总量的90%(Bouwman, 1990).河口滨海湿地是天然湿地的一个重要组成部分.关于河口、滨海感潮沼泽湿地N2O通量的研究, 近年来国际逐渐开始给予关注, 一些研究表明河口感潮沼泽湿地和潮间带湿地基本为大气N2O的源(Dausse et al., 2012; Sun et al., 2017), 也有研究表明感潮淡水森林湿地(tidal freshwater forested wetlands, tidal swamps)为大气中N2O的汇(Krauss et al., 2012).但目前仍十分缺乏亚热带河口感潮湿地N2O通量的数据.作为一个区域性环境问题, 酸雨深刻影响着生态系统的结构与过程.目前关于SO42-沉降对于湿地温室气体排放的影响主要聚焦在对于泥炭湿地和水稻田甲烷气体排放的影响(Dise and Verry 2001; Granberg et al., 2001; Gauci et al., 2002; Gon, 2001; Liou et al., 2003; 柳铮铮等, 2010).然而关于S沉降对于不同生态系统N2O通量的影响却鲜见报道, 张彪(2010)通过模拟大气SO2干沉降研究S沉降对林地土壤N2O排放的影响, 发现SO2干沉降显著促进了森林土壤N2O排放, 且土壤水分含量较高的林地, SO2被土壤水分吸收较多, S沉降对N2O排放的刺激效应更明显;Cai等(2012)研究也发现氧化性硫(SO2)沉降激发了森林土壤NO和N2O的排放, 但关于S沉降对于河口感潮淡水湿地N2O通量的影响还未见报道.
福建是我国酸雨多发区之一(庄世坚, 2004), 硫酸型酸雨较明显(潘秀丽, 2001;赵卫红, 2008).本研究以福建闽江口塔礁洲分布的淡水感潮野慈姑(Sagittaria trifolia L.)湿地为研究对象, 探讨小潮日原位施加不同浓度K2SO4溶液对N2O通量及间隙水化学的影响, 并分析影响N2O通量的主要环境因子, 以期为酸沉降对于亚热带河口淡水感潮湿地N2O通量的影响提供基础数据, 并对河口湿地生态系统保护及区域生态安全提供理论依据.
2 材料与方法(Materials and methods) 2.1 研究样地塔礁洲(119°18'29"E~119°22'04"E, 25°58'03"N~25°57'37"N)位于闽江河口区中部, 面积约878 hm2, 是一个面积较小的淡水洲滩, 洲中心部分为当地居民住地, 洲四周主要由沙滩和泥滩组成(刘剑秋等, 2010), 分布的湿地植物主要有短叶茳芏(Cyperus malaccensis Lam. var. brevifolius)、芦苇(Phragmites australis)及野慈姑等.闽江河口区气候属于亚热带和南亚热带海洋性季风气候区的过渡区(曾从盛等, 2006), 气候暖热湿润, 年均降水日数153 d, 年均降水量1346 mm, 降水多发生在3—9月(郑彩红等, 2006).闽江口潮汐特征表现为口外正规半日潮, 口内非正规半日浅海潮(王纯等, 2011).在塔礁洲南侧的泥滩滩涂上, 从岸向河方向依次分布有野慈姑群落湿地和短叶茳芏湿地, 考虑到短叶茳芏湿地距河岸较近, 地形有一定的坡度, 此外, 其受潮水和径流的影响较大, 对于模拟施加的K2SO4溶液的稀释作用更明显, 故本研究选取离岸较近, 且地形和水文环境均一致的野慈姑湿地(盐度:(0.1±0.0) ‰)(图 1)为模拟硫酸根沉降实验样地, 样地土壤理化性质及野慈姑群落特征见表 1.
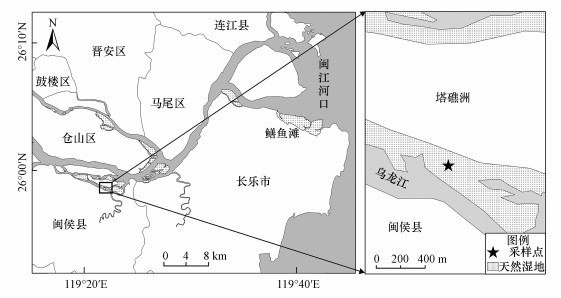 |
| 图 1 实验样地空间位置示意图 Fig. 1 Location of study site in the Tajiaozhou of the Min River estuary |
| 表 1 采样点土壤理化性质及野慈姑群落特征 Table 1 Soil physical and chemical properties and the feature of S. trifolia community of the sampling site |
在研究样地搭设木制栈桥便于顺利到达采样点和减少采样时的践踏和干扰.在野慈姑群落湿地, 选取长势良好、覆盖均匀, 且环境条件均一的地段随机布设2条与河岸平行、间距2 m的样带.每个样带共布设9个PVC底座(长×宽×高: 35 cm×35 cm×40 cm), 底座埋深30 cm, 顶部出露地表 10 cm, 各底座两两间距50 cm, 开展模拟SO42-沉降处理试验, 包括2个模拟SO42-沉降处理组和1个对照组, 每处理组3个重复.根据世界范围内酸雨影响区硫沉降负荷的一般区间(Gauci et al., 2002)及福建省酸雨影响区硫沉降的一般区间(赵卫红等, 2008; 李爱萍等, 2015), 按照模拟高沉降量的原则进行模拟处理. 2015年12月—2016年10月, 每月定期向底座内施加K2SO4溶液, 2个施加K2SO4溶液处理组为:S60(60 kg·hm-2·a-1), 和S120(120 kg·hm-2·a-1), 将各处理输入总量平分到12个月, 每月向S60处理组施加0.133 g K2SO4, S120处理组施加0.267 g K2SO4, 对照组未施加K2SO4溶液.每月选取2 d的小潮日退潮后施加K2SO4溶液, 该时段地表出露且无潮水水淹, 第1天只进行K2SO4溶液施加处理, 第2天施加K2SO4溶液后约2~3 h开始采集气样、间隙水样和土壤样.样带一用于采集气样和间隙水样, 样带二用于采集土样.
2.3 气样采集与测定采用静态暗箱-气相色谱法对N2O进行采集与测定.静态暗箱由底座和顶箱2个部分组成, 材料均为PVC板.野慈菇植株高度多小于0.5 m, 故顶箱长×宽×高分别为35 cm×35 cm×50 cm, 在顶箱侧面25 cm高度有气孔用于采集气样.1个通量测定共抽气4次, 每次抽气间隔10 min, 1次采样量为50 mL, 气样装入铝箔气样袋(大连德霖气体包装有限公司生产)带回实验室分析.
N2O浓度采用气相色谱仪(Shimadzu GC-2014, Japan)测定, 检测器为电子俘获检测器(ECD), 参数设置为进样口温度50 ℃, 柱箱温度60 ℃, 检测器温度320 ℃, 载气为高纯氦气, 流速30 mL·min-1.N2O气体通量的计算公式如下:
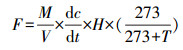
|
(1) |
式中, F为N2O通量(mg·m-2·h-1), M为N2O的摩尔质量(g·mol-1), V为标准状态下的气体摩尔体积(22.4 L·mol-1), dc/dt为N2O气体浓度单位时间的变化(μL·L-1·h-1), H为采样箱的箱高(m), T为采样箱内温度(℃).一组通量的N2O浓度数据在其与时间的线性函数回归系数R2>0.80时视为有效.
2.4 间隙水采集与测定在样带一底座内提前埋设土壤间隙水取样器(由外径为5 cm的PVC管制作而成), 采集10 cm深度的间隙水.采样器底部密封以便储水, 顶部为带有橡胶密封圈的螺旋盖.每月小潮日第1 d在施加K2SO4溶液前抽干间隙水采集器内的间隙水, 第2 d在采集完气样后立刻采集间隙水水样, 尽量保证为采集日进入到间隙水采样器中的间隙水.间隙水采集后立刻注入50 mL聚乙烯瓶, 带回实验室用定量滤纸过滤后冷藏保存测定各项指标.
水样中NH4+-N、NO3--N含量用流动注射分析仪(SKALAR San++, Netherlands)测定, 并转换为NH4+、NO3-浓度进行分析, SO42-采用离子色谱仪(Dionex ICS-2100, USA)测定, 电导率和pH值用便携式电导/温度计(2265FS, USA)和pH计(ST3100, USA)测定.
2.5 环境因子测定气样采集过程中同步用手持气象仪(Kestrel-3500, USA)测定地面1.5 m高度的气温、风速、湿度等气象因子, 气样采集完成后, 原位测定每个静态箱的箱温, 撤去静态箱顶箱立刻测定底座内10 cm深度的土温, 箱温和土温采用便携式电导/温度计(2265FS, USA)测定.在样带二底架内采集土样, 室内采用蒸馏水浸提法(水土质量比为2.5:1), 然后分别用便携式电导计(2265FS, USA)和pH计(ST3100, USA)测定.
2.6 统计分析统计分析使用Spss19.0软件进行, 制图在Origin8.0软件上完成.采用配对样本T检验(Paired-Samples T Test)检验两组变量之间的差异性, 不同处理间N2O通量、间隙水理化指标差异性采用重复测量方差分析在年尺度上进行统计分析, 采用皮尔逊相关系数(Pearson's correlation coefficient)分析两组变量之间的相关性, 并对数据进行线性回归拟合分析.文中数据为平均值±标准误差.
3 结果与分析(Results and analysis) 3.1 气象因子月动态研究样地气象因子月动态见图 2, 气温最低值和最高值分别是(16.77±0.17)和(33.50±0.21) ℃, 分别出现在12月和7月, 月平均气温为24.59 ℃.冬季、春季、夏季、秋季气温均值分别为20.68、24.32、30.19、22.47 ℃.
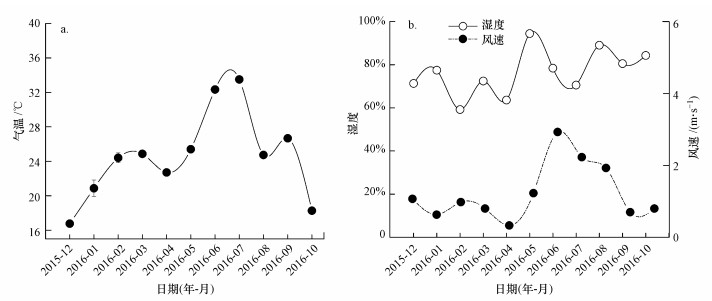 |
| 图 2 研究样地气象因子月动态 Fig. 2 Monthly varieties of meteorological factors in the study sites |
模拟SO42-沉降情景下野慈姑样地N2O通量的月动态和季节动态见图 3.CK处理N2O通量最低值和最高值分别在5月((7.63±26.80) μg·m-2·h-1)和2月((257.87±29.91) μg·m-2·h-1), 平均值为(58.06± 23.07) μg·m-2·h-1;S60处理N2O通量的最低值和最高值分别在8月((-58.92±24.62) μg·m-2·h-1)和1月((173.79±24.52) μg·m-2·h-1), 平均值为(23.50 ± 22.85) μg·m-2·h-1;S120处理N2O通量的最低值和最高值为(-32.64±65.37)和(40.95±19.14) μg·m-2·h-1, 分别出现在8月和2月, 平均值为(20.75 ± 7.83) μg·m-2·h-1.季节尺度上重复测量方差分析表明, S60处理与CK处理各季节N2O通量均无显著性差异(p>0.05);S120处理仅在冬季N2O通量显著低于CK处理(p<0.05);年尺度上重复测量方差分析表明, S120处理显著降低了野慈姑湿地N2O通量(p<0.05), S60处理与CK处理差异不显著(p>0.05), S60处理与S120处理差异也不显著(p>0.05).与CK处理相比, S60处理和S120处理组野慈姑湿地N2O通量年均值下降59.5%和64.3%.
 |
| 图 3 模拟硫沉降情景下野慈姑湿地N2O通量月动态和季节动态 (误差线为标准误, 不同大写字母表示同一季节不同处理的差异性显著;不同小写字母表示同一处理不同季节差异性显著) Fig. 3 Monthly and seasonal variations of N2O fluxes from S. trifolia wetland with different simulated SO42-deposition in the Tajiaozhou (Error line represents standard error, different lowercase letters mean different seasons exist significant differences in the same kind of treatment, different capital letters mean different treatments exist significant differences in the same season) |
模拟SO42-沉降情景下野慈姑样地10 cm深度土壤温度、电导率和pH值月动态见图 4.年尺度上重复测量方差分析表明, 不同处理间土温无差异(p>0.05).CK处理土温最低值和最高值分别为(14.80±0.10)和(31.23±0.13)℃, 平均值为(23.84±0.75) ℃;S60处理土温最低值和最高值分别为(15.03±0.23)和(31.33±0.09) ℃, 平均值(23.74±0.95) ℃;S120处理土温最低值和最高值分别为(14.90±0.17)和(31.43±0.09) ℃, 平均值(23.93±0.96) ℃.年尺度上重复测量方差分析表明, S120组显著提高了电导率(p<0.05).CK处理电导率最低值和最高值分别为(0.21±0.01)和(0.40±0.06) mS·cm-1, 平均值为(0.28±0.01) mS·cm-1;S60处理电导率最低值和最高值分别为(0.23±0.01)和(0.43±0.01)mS·cm-1, 平均值为(0.32±0.01) mS·cm-1;S120处理电导率最低值和最高值分别为(0.28±0.01)和(0.44±0.02) mS·cm-1, 平均值为(0.34±0.01) mS·cm-1.年尺度上重复测量方差分析表明, 不同处理间pH值无差异(p>0.05).CK处理pH值的最低值和最高值分别为(4.98±0.04)和(6.18±0.13), 平均值为(5.30±0.06);S60处理pH值的最低值和最高值分别为(5.00±0.04)和(5.95±0.08), 平均值为(5.39±0.07);S120处理pH值的最低值和最高值分别为(5.04±0.10)和(6.09±0.14), 平均值为(5.33±0.06).
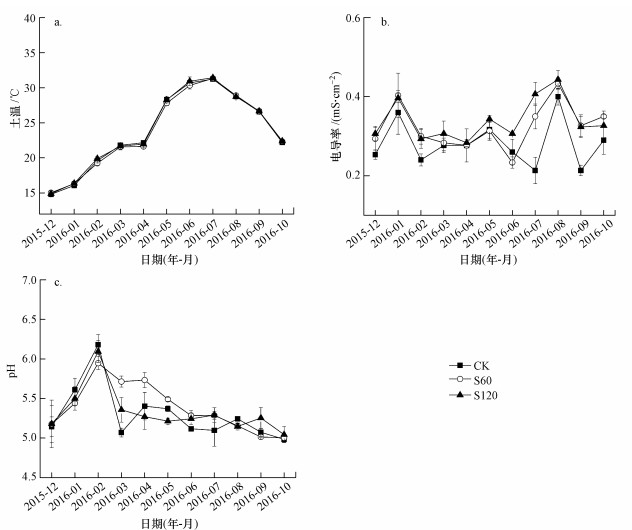 |
| 图 4 模拟硫沉降情景下野慈姑湿地土壤理化性质月动态 Fig. 4 Monthly variations of soil physical and chemical properties of S. trifolia wetland with different simulated SO42-deposition in the Tajiaozhou |
模拟SO42-沉降情景下野慈姑样地10 cm深土壤间隙水SO42-、NH4+、NO3-含量的月动态见图 5.CK组间隙水SO42-含量最低值和最高值为(3.85±0.49)和(13.34±0.83) mg·L-1, 分别出现在5月和12月, 平均值为(9.01±1.64) mg·L-1;S60组间隙水SO42-含量最低值和最高值分别为(10.28±0.08)和(21.53±2.94) mg·L-1, 分别出现在4月和12月, 平均值为(15.73±1.37) mg·L-1;S120组间隙水SO42-含量最低值和最高值分别为(4.94±1.31)和(26.71±11.17) mg·L-1, 分别出现在6月和12月, 平均值为(16.61±2.68) mg·L-1.年尺度上重复测量方差分析表明, S60处理及S120处理组间隙水SO42-含量显著高于CK组(p<0.05);S120处理与S60处理差异不显著(p>0.05).
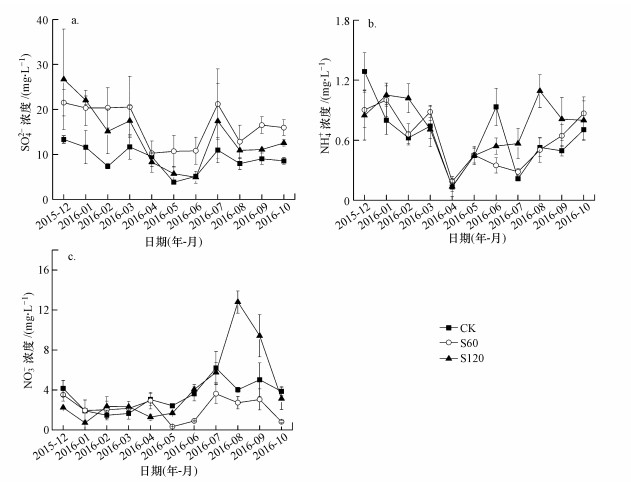 |
| 图 5 模拟硫沉降情景下野慈姑湿地间隙水SO42-、NH4+、NO3-含量月动态 Fig. 5 Monthly variations of pore water SO42-、NH4+ and NO3- concentration in S. trifolia wetland with different simulated SO42-deposition in the Tajiaozhou |
CK处理间隙水NH4+含量最低值和最高值为(0.13±0.04)和(1.29±0.49) mg·L-1, 平均值为(0.63±0.08) mg·L-1;S60处理间隙水NH4+含量最低值和最高值为(0.19±0.03)和(1.00±0.47) mg·L-1, 平均值为(0.61±0.07)mg·L-1;S120处理间隙水NH4+含量最低值和最高值为(0.14±0.10)和(1.09±0.56) mg·L-1, 平均值为(0.73±0.07) mg·L-1.年尺度上重复测量方差分析表明, 不同处理下野慈姑样地间隙水NH4+含量无差异(p>0.05).CK处理间隙水NO3-含量最低值和最高值为(1.49±0.49)和(6.20±1.67) mg·L-1, 平均值为(3.41±0.34) mg·L-1;S60处理间隙水NO3-含量最低值和最高值为(0.34±0.01)和(3.63±0.98) mg·L-1, 平均值为(2.19±0.26) mg·L-1;S120处理间隙水NO3-含量最低值和最高值为(0.73±0.04)和(16.80±12.11) mg·L-1, 平均值为(3.43±0.50) mg·L-1.年尺度上重复测量方差分析表明, 不同处理下野慈姑样地间隙水NO3-含量无差异(p>0.05).
3.4.2 对电导率与pH的影响模拟SO42-沉降情景下野慈姑样地间隙水电导率与pH值月动态见图 6.年尺度上重复测量方差分析表明, 2个处理组均显著提高了间隙水电导率(p<0.05).CK处理间隙水电导率最低值和最高值分别为(0.07±0.02)和(0.19±0.02) mS·cm-1, 平均值为(0.12±0.01) mS·cm-1;S60处理间隙水电导率最低值和最高值分别为(0.08±0.02)和(0.31±0.05) mS·cm-1, 平均值为(0.17±0.01) mS·cm-1;S120处理间隙水电导率最低值和最高值分别为(0.08±0.02)和(0.23±0.01) mS·cm-1, 平均值为(0.15±0.01) mS·cm-1.不同处理组间隙水pH值也无差异(p>0.05).CK处理间隙水pH值最低值和最高值分别为(6.86±0.16)和(8.36±0.37), 平均值为(7.54±0.08);S60处理间隙水pH值最低值和最高值分别为(7.08±0.06)和(8.62±0.31), 平均值为(7.71±0.08);S120处理间隙水pH值最低值和最高值分别为(7.15±0.03)和(8.64±0.31), 平均值为(7.64±0.09).
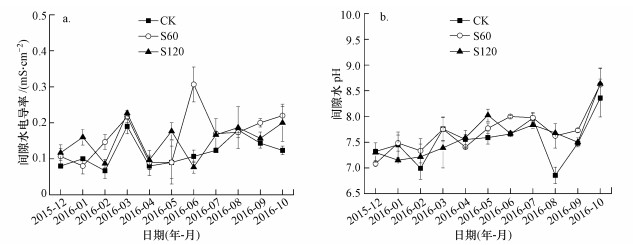 |
| 图 6 模拟硫沉降情景下野慈姑湿地间隙水电导率、pH月动态特征 Fig. 6 Monthly variations of pore water electric conductivity and pH in S. trifolia wetland with different simulated SO42-deposition in the Tajiaozhou |
S60处理、S120处理N2O通量均与间隙水电导率存在显著负相关关系(p<0.05), 与其余间隙水理化指标间无显著相关性(p>0.05), CK处理N2O通量与所有间隙水理化指标均无显著相关性(p>0.05);CK处理N2O通量与土壤pH值存在显著正相关关系(p<0.01).
| 表 2 N2O通量与环境因子的Pearson相关性分析结果 Table 2 Pearson's correlation coefficient between N2O fluxes and environmental factors |
为探讨各环境影响因子对3种处理N2O通量的贡献的大小, 利用多元回归分析中逐步回归法建立CK、S60和S120 N2O通量(分别为Yck、YS60与YS120)与气温(X1)、土温(X2)、土壤电导率(X3)、土壤pH值(X4)、间隙水NH4+含量(X5)、间隙水NO3-含量(X6)、间隙水SO42-含量(X7)、间隙水pH值(X8)、间隙水电导率(X9)之间的最优回归方程(表 3).
| 表 3 N2O通量与环境因子的多元回归线性拟合方程 Table 3 Multiple regression equations between N2O fluxes and environmental factors |
结果表明, 在所测定的自然环境因子中, CK处理N2O通量主要受土壤pH值影响, S60处理和S120处理N2O通量主要受到间隙水电导率影响.
4 讨论(Discussion) 4.1 SO42-沉降对河口湿地N2O通量的影响本研究中施加K2SO4溶液(120 kg·hm-2·a-1)在年尺度上显著降低闽江口淡水感潮野慈姑湿地N2O通量(p<0.05), 施加量为60 kg·hm-2·a-1的处理对N2O通量影响不显著.从N2O通量下降幅度看, 与对照相比夏季N2O通量下降率最大(表 4).目前国际上关于S沉降对于陆地生态系统(包括森林和湿地生态系统)N2O通量的影响鲜见报道, 张彪(2010)和Cai等(2012)研究均发现氧化性硫(SO2)沉降显著促进森林土壤N2O和NO的排放通量;章宪等(2014)也发现外源硫酸盐添加增加水稻田N2O排放通量, 以上结果与本研究中施氮对河口感潮淡水湿地N2O通量的影响正好相反, 可惜的是目前还未见关于S沉降对于河口感潮淡水湿地N2O通量影响的文献报道.
| 表 4 与对照比较, 模拟SO42-沉降情景下N2O通量下降的百分比 Table 4 Percentage of the decrease of N2O fluxes with different simulated SO42-deposition |
本研究中模拟SO42-沉降显著增加研究样地间隙水电导率以及SO42-浓度.已有的研究表明:盐度增加可提升湿地土壤硝酸盐异化还原为铵作用(DNRA)的强度, 进而抑制湿地土壤反硝化作用强度(Brunet and Garci, 1996; Larsen et al., 2010).施瑾欢(2009)对上海崇明东滩不同盐度光滩沉积物的培养实验表明:盐度越高反硝化速率越低, 反硝化菌在高盐度下呈现较低的活性;李佳霖(2009)对河口沉积物4 h的培养实验也表明:反硝化细菌数量与盐度显著负相关;Aelion and Warttinger (2010)研究发现, 河口沉积物硫酸盐还原过程产生的H2S对于反硝化作用具有抑制作用;汪旭明等(2015)研究也表明, SO42-是影响淡水和半咸水湿地N2O通量的重要因子, SO42-含量对N2O通量产生显著的抑制作用.考虑到反硝化作用是湿地土壤产生N2O、脱氮的优势途径(Howarth et al., 1996; Eyre et al., 2002; Seitzinger et al., 2006; Jordan et al., 2011; Ballantine et al., 2014), 认为模拟SO42-沉降提高间隙水电导率以及SO42-浓度是造成淡水感潮野慈姑湿地N2O排放通量降低的主要原因之一.关于施加硫酸铵对于针叶林和水稻田土壤N2O排放通量的激发效应, Cai等(1997)提出氧化性硫(SO2)沉降导致的土壤酸化是N2O排放通量增加的主要原因之一, 反硝化作用较喜好酸性土壤(Braker and Conrad, 2011).Cai等(2012)进一步提出氧化性硫(SO2)沉降显著促进森林土壤N2O排放通量的原因是其对反硝化作用、异养硝化作用或两者共同的激发效应, 而非来自于自养硝化作用, 因此, SO2沉降极有可能通过激发酸性土壤的异养硝化作用进而产生更多的N2O.
4.2 影响河口感潮湿地N2O通量的环境因子本研究中淡水感潮野慈姑湿地N2O通量主要受土壤pH值的影响, 两者存在显著的正相关关系, 这与前人研究结果相一致.朱兆良等(1992)研究分析了土壤硝化率与pH的相关性, 发现pH为5.8~8.0范围内硝化速率随土壤pH增加而增加, 两者呈显著相关;黄耀等(2002)研究也发现, pH在5.6~8.6范围内N2O排放与土壤pH呈显著正相关.本研究中模拟SO42-沉降对闽江口淡水感潮野慈姑湿地土壤pH值无影响, 这也可能是没有增加野慈姑湿地N2O排放通量的原因之一.
温度(包括气温和土温)是影响N2O通量时间动态的重要因素, 温度可通过影响土壤有机质分解和相关酶活性进而调节土壤N2O产生(郑偱华等, 1997; 郭宁等, 2013; 朱永官等, 2014).宋长春等(2005)通过对三江平原沼泽湿地的研究发现, 冬季三江平原沼泽湿地是N2O的汇, 随着土壤温度的升高而逐渐成为N2O的源(宋长春等, 2005).但本研究中闽江口淡水感潮野慈姑湿地N2O排放通量与土温和气温均无相关性, 分析原因可能是由于研究区地处亚热带季风气候区, 温度较高, 本研究采样日的气温最低为16.8 ℃, 这也许是N2O排放通量与温度相关性不好的原因之一.郑偱华等(1997)研究表明:5 cm深度土层日均温度高于15 ℃时, 土壤N2O排放对温度变化不敏感.N2O通量亦受到其他主要环境因子的影响.宋长春等(2006)研究也表明, N2O排放通量与土壤温度相关关系不明显, 而水分状况是影响N2O季节变化的主要因素(宋长春等, 2006).谢文霞等(2011)研究结果也表明:胶州湾河口芦苇湿地秋冬季N2O排放通量与5 cm和10 cm深度土层温度无相关性, 分析认为潮汐引起的干湿交替过程在一定程度上影响着N2O的排放和吸收.Hirota等(2007)对夏季日本Nakaumi滨海泻湖沙岸N2O排放放通量研究也发现:N2O通量时空变异在很大程度上受到天文潮引起的水位波动的控制.本研究中为了保证施加K2SO4溶液最大程度地下渗到野慈姑实验样地, 施氮处理和气样采集是于各月的小潮日开展, 故潮汐过程对于研究结果的影响降低到最小程度.
5 结论(Conclusions)1) 小潮日模拟施加K2SO4溶液(120 kg·hm-2·a-1), 在年尺度上显著降低闽江口淡水感潮野慈姑湿地N2O通量.
2) 闽江口淡水感潮野慈姑湿地整体上表现为大气中N2O源.模拟SO42-沉降情景下, 闽江口野慈姑湿地N2O排放通量与间隙水盐度呈显著负相关关系.
Aelion C M, Warttinger U. 2010. Sulfide inhibition of nitrate removal in coastal sediments[J]. Estuaries and Coasts, 33(3): 798–803.
DOI:10.1007/s12237-010-9275-4
|
Bouwman A F. 1990. Exchange of greenhouse gases between terrestrial ecosystems and the atmosphere[A]. In: Bouwan A F. Soils and the Greenhouse Effect. [C]. Chichester: Wiley and Dond, 1990: 60-66
|
Brunet R C, Garcia-Gil L J. 1996. Sulfide-induced dissimilatory nitrate reduction to ammonia in anaerobic freshwater sediments[J]. Fems Microbiology Ecology, 21(2): 131–138.
DOI:10.1111/fem.1996.21.issue-2
|
Ballantine K A, Groffman P M, Lehmann J, et al. 2014. Stimulating nitrate removal processes of restored wetlands[J]. Environmental Science and Technology, 48(13): 7365–7373.
DOI:10.1021/es500799v
|
Braker G, Conrad R. 2011. Diversity, structure, and size of N2O-producing microbial communities in soils-what matters for their functioning?[J]. Advances in Applied Microbiology, 75: 33–70.
DOI:10.1016/B978-0-12-387046-9.00002-5
|
Cai Z, Zhang J, Zhu T, et al. 2012. Stimulation of NO, and N2O, emissions from soils by SO2, deposition[J]. Global Change Biology, 18(7): 2280–2291.
DOI:10.1111/j.1365-2486.2012.02688.x
|
Cai Z, Xing G, Yan X, et al. 1997. Methane and nitrous oxide emissions from rice paddy fields as affected by nitrogen fertilisers and water management[J]. Plant and Soil, 196(1): 7–14.
DOI:10.1023/A:1004263405020
|
Dausse A, Garbutt A, Norman L, et al. 2012. Biogeochemical functioning of grazed estuarine tidal marshes along a salinity gradient[J]. Estuarine, Coastal and Shelf Science, 100: 83–92.
DOI:10.1016/j.ecss.2011.12.037
|
Dise N B, Verry E S. 2001. Suppression of peatland methane emission by cumulative sulfate deposition in simulated acid rain[J]. Biogeochemistry, 53(2): 143–160.
DOI:10.1023/A:1010774610050
|
Eyre B D, Rysgaard S, Dalsgaard T, et al. 2002. Comparison of isotope pairing and N2:Ar methods for measuring sediment denitrification-Assumption, modifications, and implications[J]. Estuaries, 25(6): 1077–1087.
DOI:10.1007/BF02692205
|
郭宁, 张建, 孔强, 等. 2013. 温度对亚硝化及氧化亚氮释放的影响[J]. 环境工程学报, 2013, 7(4): 1308–1312.
|
Granberg G, Sundh I, Svensson B H, et al. 2001. Effects of temperature, and nitrogen and sulfur deposition, on methane emission from a boreal mire[J]. Ecology, 82(7): 1982–1998.
DOI:10.1890/0012-9658(2001)082[1982:EOTANA]2.0.CO;2
|
Gauci V, Dise N, Fowler D. 2002. Controls on suppression of methane flux from a peat bog subjected to simulated acid rain sulfate deposition[J]. Global Biogeochemical Cycles, 16(1): 4–1.
|
Gon H A D V D. 2001. Sulfate-containing amendments to reduce methane emissions from rice fields:mechanisms, effectiveness and costs[J]. Mitigation and Adaptation Strategies for Global Change, 6(1): 71–89.
DOI:10.1023/A:1011380916490
|
黄耀, 焦燕, 宗良钢, 等. 2002. 土壤理化特性对麦田N2O排放影响的研究[J]. 环境科学学报, 2002, 22(5): 598–603.
|
Hirota M, Senga Y, Seike Y, et al. 2007. Fluxes of carbon dioxide, methane and nitrous oxide in two contrastive fringing zones of coastal lagoon, Lake Nakaumi, Japan[J]. Chemosphere, 68(3): 597–603.
DOI:10.1016/j.chemosphere.2007.01.002
|
Howarth R W, Billen G, Swaney D, et al. 1996. Regional nitrogen budgets and riverine N and P fluxes for the drainages to the North Atlantic Ocean:natural and human influences[J]. Biogeochemistry, 35: 75–139.
DOI:10.1007/BF02179825
|
Jordan S J, Nestlerode J A. 2011. Wetlands as sinks for reactive nitrogen at continental and global scales:A meta-analysis[J]. Ecosystems, 14(1): 144–155.
DOI:10.1007/s10021-010-9400-z
|
Krauss K W, Whitbeck J L. 2012. Soil greenhouse gas fluxes during wetland forest retreat along the lower Savannah River, Georgia (USA)[J]. Wetlands, 32(1): 73–81.
DOI:10.1007/s13157-011-0246-8
|
李爱萍, 黄广华, 高人, 等. 2015. 福州、建瓯和武夷山大气氮/硫湿沉降特征分析[J]. 亚热带资源与环境学报, 2015, 10(3): 33–40.
|
刘剑秋, 曾从盛. 2010. 福建湿地及其生物多样性[M]. 北京: 科学出版社.
|
李佳霖. 2009. 典型河口区沉积物的硝化和反硝化过程[D]. 青岛: 中国海洋大学
|
Liou R M, Huang S N, Lin C W. 2003. Methane emission from fields with differences in nitrogen fertilizers and rice varieties in Taiwan paddy soils[J]. Chemosphere, 50(2): 237–246.
DOI:10.1016/S0045-6535(02)00158-3
|
Larsen L, Moseman S, Santoro A E, et al. 2010. A complex-systems approach to predicting effects of sea level rise and nitrogen loading on nitrogen cycling in coastal wetland ecosystems[J]. Ecological Dissertations in the Aquatic Sciences Symposium Proceedings Ⅷ, 5: 67–92.
|
潘秀丽. 2001. 福建省酸雨成因分析及防治措施[J]. 水文, 2001, 21(1): 47–49.
|
Prinn R, Cunnold D, Rasmussen R, et al. 1990. Atmospheric emissions and trends of nitrous oxide deduced from 10 years of ALE-GAGE data[J]. Journal of Geophysical Research:Atmospheres, 95(D11): 18369–18385.
DOI:10.1029/JD095iD11p18369
|
宋长春, 王毅勇, 王跃思, 等. 2005. 季节性冻融期沼泽湿地CO2、CH4和N2O排放动态[J]. 环境科学, 2005, 26(4): 7–12.
|
宋长春, 张丽华, 王毅勇, 等. 2006. 淡水沼泽湿地CO2、CH4和N2O排放通量年际变化及其对氮输入的响应[J]. 环境科学, 2006, 27(12): 2369–2375.
DOI:10.3321/j.issn:0250-3301.2006.12.001 |
施瑾欢. 2009. 崇明东滩氨氧化、反硝化微生物群落初步研究[D]. 上海: 复旦大学
|
Seitzinger S, Harrison J A, Bohlke J K, et al. 2006. Denitrification across landscapes and waterscapes:a synthesis[J]. Ecological Application, 16(6): 2064–2090.
DOI:10.1890/1051-0761(2006)016[2064:DALAWA]2.0.CO;2
|
Solomon S. 2007. IPCC (2007):Climate Change The Physical Science Basis[J]. American Geophysical Union, 9(1): 123–124.
|
Sun W G, Sun Z G, Mou X J, et al. 2017. Nitrous oxide emissions from intertidal zone of the Yellow River Estuary in autumn and winter during 2011-2012[J]. Estuaries and Coasts, 40(1): 145–159.
DOI:10.1007/s12237-016-0140-y
|
仝川, 柳铮铮, 曾从盛, 等. 2010. 模拟SO42-沉降对河口潮汐湿地甲烷排放通量的影响[J]. 中国环境科学, 2010, 30(3): 302–308.
|
王纯, 王维奇, 曾从盛, 等. 2011. 闽江河口区盐-淡水梯度下湿地土壤氮形态及储量特征[J]. 水土保持学报, 2011, 25(5): 147–153.
|
汪旭明. 2015. 闽江口淡水和半咸水短叶茳芏潮汐湿地N2O通量研究[D]. 福州: 福建师范大学
|
谢文霞, 赵全升, 张芳, 等. 2011. 胶州湾河口湿地秋冬季N2O气体排放通量特征[J]. 地理科学, 2011, 31(4): 464–469.
|
张彪. 2010. 不同植被类型土壤氮氧化物排放及其对硫沉降的响应[D]. 福州: 福建师范大学
|
庄世坚. 2004. 福建省酸雨形势与污染损耗及其控制对策[J]. 应用海洋学学报, 2004, 23(1): 101–106.
|
赵卫红. 2008. 福建省主要城市降水离子特征及沉降量现状分析[J]. 亚热带资源与环境学报, 2008, 3(3): 19–24.
|
曾从盛. 2006. 福建典型区生态环境研究[M]. 北京: 中国环境科学出版社.
|
郑彩红, 曾从盛, 陈志强, 等. 2006. 闽江河口区湿地景观格局演变研究[J]. 湿地科学, 2006, 4(1): 29–35.
|
章宪, 马永跃, 王维奇. 2014. 外源硫酸盐添加对福州平原稻田甲烷与氧化亚氮排放的影响[J]. 福建师大学报(自然科学版), 2014, 30(4): 111–117.
|
朱兆良, 文孝启. 1992. 中国土壤氮素[M]. 南京: 江苏科学技术出版社: 97–160.
|
郑循华, 王明星. 1997. 温度对农田N2O产生与排放的影响[J]. 环境科学, 1997, 18(5): 1–5.
|
朱永官, 王晓辉, 杨小茹, 等. 2014. 农田土壤N2O产生的关键微生物过程及减排措施[J]. 环境科学, 2014, 35(2): 792–800.
|
 2018, Vol. 38
2018, Vol. 38


