2. 中国科学院生态环境研究中心环境水质学国家重点实验室, 北京 100085;
3. 北京林业大学环境科学与工程学院, 北京 100083;
4. 中国科学院大学, 北京 100049
2. State Key Laboratory of Environmental Aquatic Chemistry, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085;
3. College of Environmental Science and Engineering, Beijing Forestry University, Beijing 100083;
4. University of Chinese Academy of Sciences, Beijing 100049
含重金属废水排放到环境中会造成重金属污染, 破坏生态系统, 并可通过食物链富集危害人类的健康(Maity et al., 2017).重金属污染主要来源于矿石开采、化工制造、冶炼、电镀等工业生产过程.在我国, 铜污染问题相对比较普遍, 废水中的Cu2+含量很高, 铜污染问题亟需经济高效且可实现资源回收的解决方法(常春等, 2016).目前, 常用的Cu2+去除和回收工艺主要有化学沉淀、离子交换、膜分离、吸附法等(Hua et al., 2012).其中, 吸附法因相对经济、操作简便等特点而被广泛关注.目前研究和使用较多的吸附剂主要有纳米材料(Hua et al., 2012)、高岭土(Bhattacharyya et al., 2008)和生物大分子(Triki et al., 2017)等.
水凝胶是一种在水中能迅速溶胀但不溶解的、具有三维交联网络结构的功能性高分子材料.双网络水凝胶是由相互独立且相互贯穿的两个水凝胶体系构所成的, 较单网络水凝胶而言, 双网络水凝胶因大大提高了材料的机械性能而得到了较多关注(Gong et al., 2003).其中, 以生物高分子制备的水凝胶因含有丰富的羟基、羧基和氨基等官能团而具有良好的吸附重金属的性能.常用的生物高分子如壳聚糖(Haider et al., 2009)、明胶(Wang et al., 2013)、纤维素(Kono et al., 2013)、海藻酸钠(Wang et al., 2016)等, 具有成本低廉、可生物降解性的优点, 被广泛用于环境水处理领域.海藻酸钠是一种天然多糖, 含有大量的羧基和羟基, 具有良好的成凝胶性能, 能与二价盐离子(如Ca2+、Ba2+、Co2+等)交联而凝胶化.但该类凝胶硬而脆, 孔隙率低, 稳定性差(Thakur et al., 2016), 在一定程度上限制了其应用范围.聚乙烯醇是一种使用广泛且无毒无害的水溶性高分子聚合物, 可通过循环冷冻解冻的方式形成凝胶.与海藻酸钠凝胶相比, 聚乙烯醇凝胶具有良好的韧性和稳定性, 但硬度较低, 且官能团单一(Yang et al., 2016), 在环境方面应用较少.此外, 诸多纳米材料, 如磁性纳米粒子(Li et al., 2016)、碳纳米管(Karkeh-abadi et al., 2016)、石墨烯(Li et al., 2013)等被用于与水凝胶复合以进一步改善其吸附性能、机械性能和生物稳定性, 并获得更方便的固液分离能力.其中, 磁性纳米Fe3O4粒子因制备工艺简单、比表面积较高、具有超顺磁性和较好的吸附性能而备受关注(Mohammadi et al., 2014), 但磁性纳米Fe3O4粒子暴露在空气中易被氧化、易发生团聚且稳定性差, 降低了其应用性能.
为了构建拥有丰富官能团以能够高效吸附去除重金属离子且具有良好固液分离性能的磁性高分子复合水凝胶, 本研究拟在海藻酸钠凝胶基础上, 通过与聚乙烯醇凝胶和磁性纳米Fe3O4的复配, 以海藻酸钠与Ca2+交联形成第一网络, 得到磁性单网络水凝胶(简写为SAPFe); 磁性单网络水凝胶继续通过聚乙烯醇冷冻解冻循环形成第二网络, 获得双网络磁性水凝胶(简写为DAPFe).同时,利用扫描电镜、红外光谱、含水率变化、比表面积对SAPFe和DAPFe进行表征, 并通过对Cu2+的吸附实验探讨SAPFe和DAPFe的吸附性能.
2 材料与方法(Materials and methods) 2.1 主要材料海藻酸钠、聚乙烯醇、氯化钙、硫酸铜、六水合氯化铁、乙二胺、氢氧化钠、柠檬酸钠等药剂均为分析纯, 购自国药集团化学试剂有限公司.实验用水均为超纯水.
2.2 磁性纳米Fe3O4的制备水热法制备磁性纳米Fe3O4:取0.2 g六水合氯化铁溶解至15 mL超纯水中, 分别加入0.5 g柠檬酸钠、3 mL乙二胺、0.3 g氢氧化钠, 搅拌均匀后加入高温反应釜内, 加热200 ℃保持12 h.产物进行磁分离后用乙醇、超纯水水各清洗3次, 真空烘干后备用.
2.3 单网络磁性水凝胶(SAPFe)的制备将2 g海藻酸钠和2 g聚乙烯醇溶解到100 mL超纯水中, 取0.1、0.2、0.5、1.0 g制备好的磁性纳米Fe3O4加入上述溶液, 机械搅拌和超声获得均一溶液, 通过蠕动泵滴入100 mL 10%的CaCl2溶液里, 得到负载磁性纳米Fe3O4量为0、2.5%、5.0%、12.5%、25.0%的凝胶球.浸泡24 h后, 用超纯水清洗3次, 去除表面的杂质离子, 获得SAPFe.
2.4 双网络磁性水凝胶(DAPFe)的制备将2.3节制备的负载磁性纳米Fe3O4量分别为0、2.5%、5.0%、12.5%、25.0%的单网络水凝胶球装入培养皿中, 在-40 ℃下冷冻24 h, 再常温下完全解冻.上述操作进行3个循环, 所得凝胶球用超纯水清洗3次即得到DAPFe.
2.5 磁性高分子复合水凝胶的表征与分析方法所有样品都经过冷冻干燥后进行表征分析, 样品的表面形貌利用日本日立公司的场发射扫描电子显微镜(SEM, H-7500)获得; 样品孔结构利用美国麦克公司ASAP-2460全自动比表面积与孔隙度仪分析, 样品在80 ℃脱气4 h, 于液氮(77 K)温度下以高纯氮为吸附介质测定相对压力为0~1的吸脱附曲线; 傅里叶变换红外(FTIR)光谱由德国布鲁克公司的Vertex 70红外光谱仪获得, 谱图采集范围为4000~400 cm-1, 分辨率为4 cm-1.
2.6 磁性高分子复合水凝胶的吸附实验准确称取0.02 g SAPFe和DAPFe分别加入到40 mL的样品瓶中, 再加入20 mL一定浓度的硫酸铜溶液.将样品瓶置于恒温振荡箱内振荡吸附一定时间(25 ℃, 150 r·min-1).最后, 溶液通过0.45 μm滤膜, 用电感耦合等离子体发射光谱仪(ICP-OES, 岛津9800)分析滤液中剩余的Cu2+浓度.每组实验均设置1个空白样和3个平行样, 最后平衡浓度取平均值.根据吸附实验前后Cu2+浓度的差值计算凝胶材料的吸附量, 公式如下:
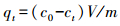
|
(1) |
式中, qt为吸附t时的吸附量(mg·g-1); c0、ct分别为吸附前后Cu2+浓度(mg·L-1); V为溶液体积(L); m为凝胶质量(g).
2.6.1 吸附动力学实验准确称取0.02 g SAPFe或DAPFe置于20 mL Cu2+初始浓度为200 mg·L-1的溶液中, 25 ℃、150 r·min-1下振荡反应, 在不同时间取样, 时间设置为0.5、1、2、3、5、7、9、12、20、24、36 h, 溶液通过0.45 μm滤膜后, 分析剩余Cu2+浓度, 计算吸附剂的吸附量.采用准一级动力学、准二级动力学和颗粒内扩散模型进行拟合, 其表达式分别如下:

|
(2) |
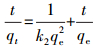
|
(3) |
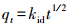
|
(4) |
式中, k1、k2和kid分别是准一级动力学(min-1)、准二级动力学(g·mg-1min-1)和颗粒内扩散模型(mg·g-1·min-0.5)的吸附速率常数; qe和qt分别为Cu2+的平衡吸附容量(mg·g-1)和在t时的吸附量(mg·g-1).
2.6.2 吸附等温线实验准确称取0.02 g SAPFe或DAPFe置于20 mL Cu2+初始浓度分别为10、20、50、100、150、200 mg·L-1的溶液中, 25 ℃、150 r·min-1下振荡反应24 h, 溶液通过0.45 μm滤膜后, 分析剩余Cu2+浓度, 计算吸附剂的吸附量.吸附等温线采用Langmuir、Freundlich、Temkin模型方程进行拟合, 其表达式分别如下:
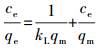
|
(5) |
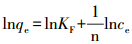
|
(6) |
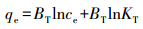
|
(7) |
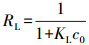
|
(8) |
式中, KL、KF、BT和KT分别为Langmuir、Freundlich和Temkin模型中与吸附有关的常数; n为Freundlich吸附指数, 与吸附剂的性质有关.
2.6.3 pH值对磁性水凝胶的影响准确称取0.02 g SAPFe或DAPFe置于20 mL Cu2+初始浓度为120 mg·L-1的溶液中, 调节Cu2+溶液的pH值为2~6, 并设置未添加水凝胶的空白对照实验考察Cu2+的沉淀现象.在25 ℃、150 r·min-1下振荡反应, 通过0.45 μm滤膜后, 分析剩余Cu2+浓度, 计算吸附剂的吸附量.
3 结果与分析(Results and analysis) 3.1 磁性高分子复合水凝胶的表征 3.1.1 形貌特征图 1a是SAPFe和DAPFe的实物照片, 可以观察到SAPFe表面光滑, DAPFe表面粗糙.SAPFe经过反复冷冻解冻的物理交联方式即可得到具有互穿网络结构的DAPFe, 冷冻时聚乙烯醇内部的水以冰晶的形态存在于非晶区内, 经过解冻后, 内部冰晶融化而形成互穿的孔(Mohammadi et al., 2014).图 1b是磁性纳米Fe3O4的SEM图像, 为大小均一的微球.图 1c、1d分别为SAPFe放大50和1000倍的SEM图像, 具有类似蜂窝煤的多孔网状结构, 内部结构放大后可看出凝胶已经成功均匀地负载了磁性纳米Fe3O4, 增加了内部的比表面积.三维多孔网络结构中相互交叉连通的孔隙可以使被吸附的溶质分子扩散通过, 有利于磁性水凝胶在水处理领域的应用.图 1e、1f分别为DAPFe放大50和1000倍的SEM图像, 发现DAPFe的网络结构变得致密, 这可能是由于聚乙烯醇经过冷冻解冻循环的物理交联使凝胶球内部物理缠结作用加强, 凝胶球的交联程度加大, 形成了更密集的网络结构.
 |
| 图 1 水凝胶及磁性纳米Fe3O4的表观形貌(a.磁性水凝胶球的光学照片, b.磁性纳米Fe3O4, c、d.SAPFe, e、f.DAPFe) Fig. 1 Photographic (a) and SEM images of Fe3O4 nanoparticles (b), SAPFe (c, d) and DAPFe (e, f) |
以氮气为吸附介质, 在77 K和相对压力10-6~1.0范围内进行氮气吸附脱附以测定比表面积和孔结构, 图 2是SAPFe和DAPFe的N2吸附脱附曲线和BJH孔径分布曲线(插图).结果表明, SAPFe和DAPFe的比表面积分别为64.54和89.01 m2·g-1, 相比较未负载磁性纳米Fe3O4的海藻酸钠/聚乙烯醇单、双网络复合水凝胶(14.68 m2·g-1、27.74 m2·g-1)比表面积大大增大.孔径主要分布在1.2~6.0 nm之间, 孔容积分别在2.958和2.924 nm处达到最大值.在25~60 nm区间出现弱峰, 说明材料具有双峰孔径分布的特点.SAPFe和DAPFe的平均孔径大小分别为3.797和3.443 nm, 孔容体积为0.061和0.034 cm3·g-1.
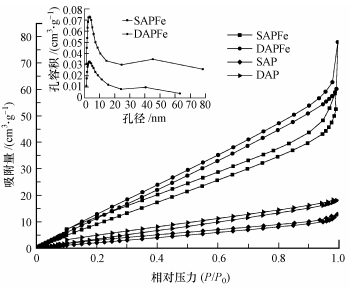 |
| 图 2 SAPFe、DAPFe、SAP和DAP的氮气吸附脱附曲线 Fig. 2 Nitrogen adsorption-desorption isotherms and pore size distribution curves of SAPFe, DAPFe, SAP and DAP |
图 3为纳米Fe3O4负载量对SAPFe和DAPFe平衡含水率的影响结果, 其中, R为Fe3O4与海藻酸钠、聚乙烯醇总量的质量比.由图可知, SAPFe的平衡含水率大于DAPFe; 随着Fe3O4负载量的增多, 两种凝胶材料的平衡含水率降低, 其中,Fe3O4负载量变化对DAPFe平衡含水率的影响更大.分析可知, 由单网络到双网络凝胶, 通过冷冻解冻循环, 使聚乙烯醇发生了交联反应, 不仅阻碍了水对高分子链的溶解, 而且形成了更多的交联点, 增大了交联程度, 使凝胶收缩程度增大, 形成更加致密结构, 因此, 凝胶的平衡含水率有所下降(郑丹, 2014).随着纳米Fe3O4负载量的增加, 纳米粒子的添加占据了原来水分子所占有的空间, 使凝胶更加致密, 同时阻碍了水分子向凝胶内部的扩散, 因此, 平衡含水率也随之降低.含水率低的水凝胶具有更好的稳定性和机械性能, 但其溶胀性能降低(Spinks et al., 2006).
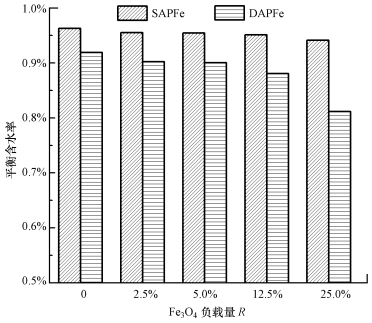 |
| 图 3 纳米Fe3O4的负载对SAPFe和DAPFe平衡含水率的影响 Fig. 3 The effect of Fe3O4 nanoparticles content on equilibrium water content of SAPFe and DAPFe |
图 4为外加磁场作用下负载0、2.5%、5%、12.5%、25%纳米Fe3O4的SAPFe和DAPFe的磁性效果图, 其中, 纳米Fe3O4占海藻酸钠和聚乙烯醇总量12.5%和25%的凝胶球均表现出了良好的磁性能.结合含水率结果确定纳米磁性Fe3O4的适宜负载量为12.5%, 并作为后续吸附试验中凝胶材料负载磁性纳米Fe3O4的用量.
 |
| 图 4 纳米Fe3O4的负载对SAPFe和DAPFe磁性能的影响(a.无外加磁场, b.加外加磁场) Fig. 4 The effect of Fe3O4 nanoparticles content on magnetic properties of SAPFe and DAPFe |
为了研究SAPFe和DAPFe对Cu2+的吸附速率, 对其进行吸附动力学试验, 吸附动力学模型拟合结果如图 5a所示.5 h内SAPFe和DAPFe对Cu2+的吸附量分别迅速增加到130.8和144.2 mg·g-1; SAPFe在6 h以后基本达到吸附平衡, DAPFe在9 h后达到吸附平衡; 最终, SAPFe和DAPFe对200 mg·L-1 Cu2+的平衡吸附量分别为141.8和162.5 mg·g-1; SAPFe对Cu2+的吸附速率大于DAPFe.DAPFe比表面积较大, 孔结构相对致密, 孔径较小, 因此, 吸附速率较慢.
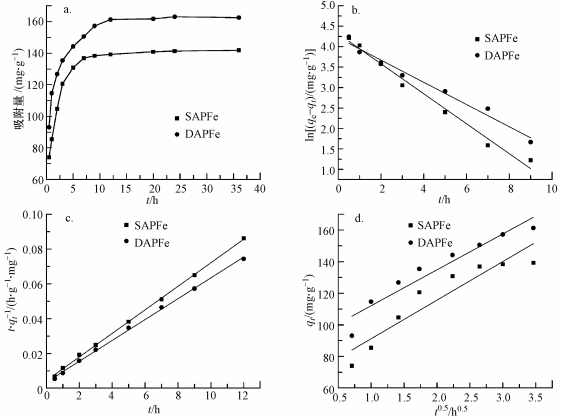 |
| 图 5 SAPFe和DAPFe对Cu2+的吸附动力学模型线性拟合(a.吸附量随时间的变化, b.准一级动力学拟合结果, c.准二级动力学拟合结果, d.颗粒内扩散模型拟合结果) Fig. 5 Adsorption kinetics(a) of Cu2+ on SAPFe and DAPFe (b.pseudo-first-order model, c.pseudo-second-order model, d.intra-particle diffusion model) |
SAPFe和DAPFe对Cu2+的吸附动力学模型如图 5b、5c、5d所示, 拟合参数如表 1所示.准一级动力学模型只反映吸附速率与一种反应物浓度的关系, 具有局限性, 而准二级动力学模型包含外部液膜扩散、颗粒内部扩散和表面吸附等过程, 能够更好地反映吸附过程和吸附机理(方敦等, 2016).分析3个模型拟合的可决系数, 发现SAPFe和DAPFe的准一级动力学模型的R2分别为0.90和0.97, 准二级动力学模型的R2均大于0.99, 拟合度高于一级动力学模型, 其计算出的平衡吸附容量qe也更接近实验数据, 即化学反应是主要的控速步骤.由颗粒内扩散模型拟合的结果可知, SAPFe和DAPFe对Cu2+的吸附分为2个阶段:第一个线性阶段(t < 15 h)为Cu2+在凝胶表面的扩散过程, 第2个阶段(t>15 h)为内部扩散.随着吸附的进行, SAPFe和DAPFe表面可利用的吸附位点逐渐减少, 吸附最终达到平衡(Li et al., 2013).qt与t-0.5拟合为线性关系, 但不过原点, 说明颗粒内扩散是单、双网络磁性水凝胶对Cu2+的主要控速因素, 但不是唯一的控速步骤.
| 表 1 SAPFe、DAPFe对Cu2+的吸附动力学参数 Table 1 Kinetics parameters of Cu2+ adsorption on SAPFe and DAPFe |
SAPFe和DAPFe对Cu2+的等温吸附分别用Langmuir、Freundlich和Temkin模型进行拟合, 结果如图 6所示, 拟合参数如表 2所示.结果表明, Langmuir和Freundlich方程得到了较好的可决系数, Temkin模型较差.其中, Langmuir吸附等温模型为单分子层吸附(孙德帅等, 2016), 可以更好地描述Cu2+在SAPFe和DAPFe上的吸附行为.此外, 通过拟合参数计算出SAPFe和DAPFe的RL均介于0~1, 表明易于吸附的进行.Freundlich模型拟合得到的n均大于1, 说明单、双网络凝胶均对Cu2+有较好的吸附效果(Kilic et al., 2011).由Langmuir模型可得出SAPFe和DAPFe的饱和吸附量分别为173.01和207.01 mg·g-1, 双网络凝胶较单网络凝胶的吸附效果有明显提高.
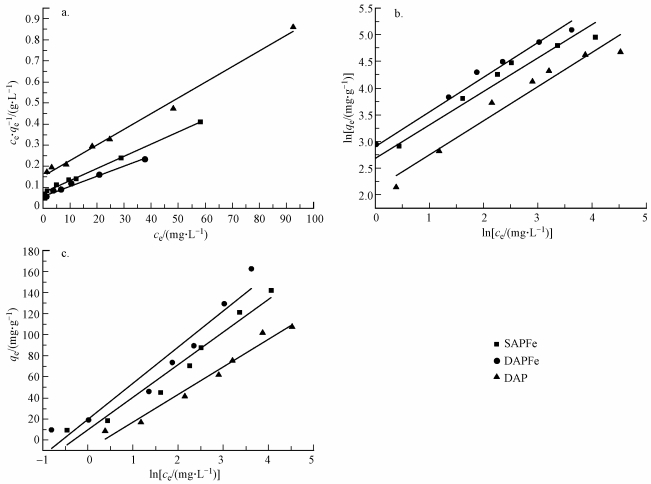 |
| 图 6 SAPFe、DAPFe和DAP对Cu2+的吸附等温线(a. Langmuir, b.Frendlich, c.Tempkin) Fig. 6 Adsorption isotherm model for Cu2+ on SAPFe, DAPFe, and DAP |
| 表 2 SAPFe、DAPFe和DAP对Cu2+的吸附等温线参数 Table 2 Isotherm parameters of Cu2+ adsorption on SAPFe, DAPFe, and DAP |
在pH为2~6范围内研究磁性高分子复合水凝胶的吸附性能, 结果如图 7所示.随着pH的增加, 吸附容量增大.在低pH值时, 溶液中的H+抑制了羧基和羟基的脱质子作用, 螯合作用减弱, SAPFe和DAPFe对Cu2+的吸附容量低; 当pH增大时, H+浓度降低, 羧基和羟基更容易发生脱质子作用, 因而促进了吸附.另外, 空白对照实验中发现pH在2~5之间无明显的Cu2+沉淀现象发生, 而在pH=6时, 有微弱的沉淀现象.因此, 在pH为2~5之间主要为材料对Cu2+的吸附, 而在pH=6时, 沉淀作用对吸附也可能有一定的贡献.
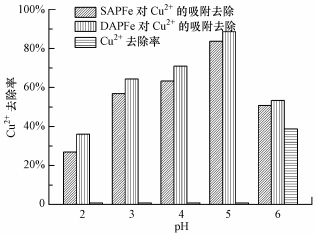 |
| 图 7 pH值对SAPFe和DAPFe吸附Cu2+的影响 Fig. 7 Effects of solution pH on the Cu2+ adsorption on SAPFe and DAPFe |
图 8给出了SAPFe和DAPFe吸附铜离子前后在4000~400 cm-1区间的光谱图.SAPFe谱图中3279、2921、1591、1412、1024 cm-1处分别为—OH、C—H、—COOH—(不对称)、COO—(对称)、C—O—C的伸缩振动(Chhatri et al., 2011), 563 cm-1处的吸收峰为磁性纳米Fe3O4的特征吸收峰(钟远红等, 2010; Cui et al., 2014).相比较而言, DAPFe水凝胶中由于聚乙烯醇交联后在3279、2921 cm-1处峰强减弱明显, 说明聚乙烯醇中的—OH参与了交联反应.就DAPFe而言, 吸附Cu2+后, —OH伸缩振动的吸收峰由吸附前的3280 cm-1移动到了3295 cm-1; C=O的对称伸缩振动峰由吸附前的1410 cm-1移动至1408 cm-1; C—O—C的伸缩振动的吸收峰由吸附前的1021 cm-1移动到了1029 cm-1(Kamoun et al., 2015).基团吸收峰在吸附后均有相应的减弱, 说明吸附过程中羟基上具有孤对电子的O与重金属离子发生了螯合作用, 海藻酸钠里的C=O及醚键中的—O—也参与了重金属的吸附(Kumar et al., 2017).
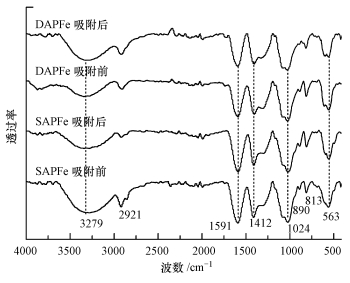 |
| 图 8 SAPFe和DAPFe吸附Cu2+前、后的FTIR图 Fig. 8 FTIR spectrum of SAPFe and DAPFe before and after adsorption of Cu2+ |
1) 以海藻酸钠和聚乙烯醇为骨架负载磁性纳米Fe3O4颗粒成功合成了磁性高分子复合水凝胶SAPFe和DAPFe.扫描电镜图呈现出类似蜂窝煤的三维多孔网状结构, SAPFe和DAPFe中的三维多孔网络结构中相互交叉连通的孔隙易于溶质分子扩散通过, 有利于磁性水凝胶吸附去除污染物.
2) DAPFe由于交联程度大, 含水率低于SAPFe, 但含水率仍然能达到80%.SAPFe和DAPFe的比表面积分别为64.54 m2·g-1和89.01 m2·g-1, 相比较未负载磁性纳米Fe3O4的复合水凝胶比表面积大大提高.赋磁后可快速分离出磁性高分子复合水凝胶.在pH值2~5范围内, 随着pH的增加, 两种材料对Cu2+的吸附容量逐渐增大.通过红外分析发现, 相比较SAPFe而言, DAPFe中的聚乙烯醇参加了交联反应形成了更稳定的磁性水凝胶.SAPFe和DAPFe具有丰富的与重金属产生螯合作用的羧基和羟基功能性官能团.
3) 磁性高分子复合水凝胶对Cu2+的吸附过程符合准二级动力学模型, SAPFe对Cu2+的吸附速率大于DAPFe.吸附过程能够很好地被Langmuir吸附等温模型描述, 说明磁性高分子复合水凝胶对Cu2+的吸附是单分子层吸附, DAPFe对Cu2+的最大吸附量可达207.01 mg·g-1, 吸附性能优于SAPFe(173.01 mg·g-1).
综上, 磁性双网络水凝胶球(DAPFe)是一种绿色环保无毒的吸附剂, 原料来源广泛, 具有独特的网络结构和丰富的官能团, 吸附性能优良, 固液分离方便, 有一定的开发潜力和应用前景.
Bhattacharyya K G, Gupta S S. 2008. Adsorption of a few heavy metals on natural and modified kaolinite and montmorillonite:A review[J]. Advances in Colloid and Interface Science, 140(2): 114–131.
DOI:10.1016/j.cis.2007.12.008
|
常春, 王胜利, 郭景阳, 等. 2016. 不同热解条件下合成生物炭对铜离子的吸附动力学研究[J]. 环境科学学报, 2016, 36(7): 2491–2502.
|
Chhatri A, Bajpai J, Bajpai A K, et al. 2011. Cryogenic fabrication of savlon loaded macroporous blends of alginate and polyvinyl alcohol (PVA).Swelling, deswelling and antibacterial behaviors[J]. Carbohydrate Polymers, 83(2): 876–882.
DOI:10.1016/j.carbpol.2010.08.077
|
Cui L, Hu L, Guo X, et al. 2014. Kinetic, isotherm and thermodynamic investigations of Cu2+ adsorption onto magnesium hydroxyapatite/ferroferriC=Oxide nano-composites with easy magnetic separation assistance[J]. Journal of Molecular Liquids, 198: 157–163.
DOI:10.1016/j.molliq.2014.06.016
|
方敦, 田华婧, 叶欣, 等. 2016. 富里酸-膨润土复合体对氟的吸附特性[J]. 环境科学, 2016, 37(3): 1023–1031.
|
高瀚文, 杨荣杰, 何吉宇, 等. 2010. 冷冻/解冻制备的聚乙烯醇水凝胶的结构和流变性研究[J]. 高分子学报, 2010(5): 542–549.
|
Gong J P, Katsuyama Y, Kurokawa T, et al. 2003. Double-network hydrogels with extremely high mechanical strength[J]. Advanced Materials, 15(14): 1155–1158.
DOI:10.1002/adma.200304907
|
Haider S, Park S. 2009. Preparation of the electrospun chitosan nanofibers and their applications to the adsorption of Cu(Ⅱ) and Pb(Ⅱ) ions from an aqueous solution[J]. Journal of Membrane Science, 328(1/2): 90–96.
|
Hua M, Zhang S, Pan B, et al. 2012. Heavy metal removal from water/wastewater by nanosized metal oxides:A review[J]. Journal of Hazardous Materials, 211-212: 317–331.
DOI:10.1016/j.jhazmat.2011.10.016
|
Kamoun E A, Kenawy E S, Tamer T M, et al. 2015. Poly (vinyl alcohol)-alginate physically crosslinked hydrogel membranes for wound dressing applications:Characterization and bio-evaluation[J]. Arabian Journal of Chemistry, 8(1): 38–47.
DOI:10.1016/j.arabjc.2013.12.003
|
Karkeh-Abadi F, Saber-Samandari S, Saber-Samandari S. 2016. The impact of functionalized CNT in the network of sodium alginate-based nanocomposite beads on the removal of Co(Ⅱ) ions from aqueous solutions[J]. Journal of Hazardous Materials, 312: 224–233.
DOI:10.1016/j.jhazmat.2016.03.074
|
Kilic M, Apaydin-Varol E, Pütün A E. 2011. Adsorptive removal of phenol from aqueous solutions on activated carbon prepared from tobacco residues:Equilibrium, kinetics and thermodynamics[J]. Journal of Hazardous Materials, 189(1/2): 397–403.
|
Kono H, Onishi K, Nakamura T. 2013. Characterization and bisphenol A adsorption capacity of β-cyclodextrin-carboxymethylcellulose-based hydrogels[J]. Carbohydrate Polymers, 98(1): 784–792.
DOI:10.1016/j.carbpol.2013.06.065
|
Kumar A, Lee Y, Kim D, et al. 2017. Effect of crosslinking functionality on microstructure, mechanical properties, and in vitro cytocompatibility of cellulose nanocrystals reinforced poly (vinyl alcohol)/sodium alginate hybrid scaffolds[J]. International Journal of Biological Macromolecules, 95: 962–973.
DOI:10.1016/j.ijbiomac.2016.10.085
|
Li X, Lu H, Zhang Y, et al. 2016. Fabrication of magnetic alginate beads with uniform dispersion of CoFe2O4 by the polydopamine surface functionalization for organic pollutants removal[J]. Applied Surface Science, 389: 567–577.
DOI:10.1016/j.apsusc.2016.07.162
|
Li Y, Du Q, Liu T, et al. 2013. Methylene blue adsorption on graphene oxide/calcium alginate composites[J]. Carbohydrate Polymers, 95(1): 501–507.
DOI:10.1016/j.carbpol.2013.01.094
|
Liu W, Wang T, Borthwick A G L, et al. 2013. Adsorption of Pb2+, Cd2+, Cu2+ and Cr3+ onto titanate nanotubes:Competition and effect of inorganic ions[J]. Science of The Total Environment, 456-457: 171–180.
DOI:10.1016/j.scitotenv.2013.03.082
|
Maity J, Ray S K. 2017. Removal of Cu (Ⅱ) ion from water using sugar cane bagasse cellulose and gelatin based composite hydrogels[J]. International Journal of Biological Macromolecules, 97: 238–248.
DOI:10.1016/j.ijbiomac.2017.01.011
|
Mohammadi A, Daemi H, Barikani M. 2014. Fast removal of malachite green dye using novel superparamagnetic sodium alginate-coated Fe3O4 nanoparticles[J]. International Journal of Biological Macromolecules, 69: 447–455.
DOI:10.1016/j.ijbiomac.2014.05.042
|
孙德帅, 刘亚丽, 张晓东, 等. 2016. 铁有机骨架材料的快速合成及对阴离子染料的吸附性能[J]. 环境科学, 2016, 37(3): 1016–1022.
|
Spinks G M, Lee C K, Wallace G G, et al. 2006. Swelling behavior of chitosan hydrogels in ionic liquid-water binary systems[J]. Langmuir, 22(22): 9375–9379.
DOI:10.1021/la061586r
|
Thakur S, Pandey S, Arotiba O A. 2016. Development of a sodium alginate-based organic/inorganic superabsorbent composite hydrogel for adsorption of methylene blue[J]. Carbohydrate Polymers, 153: 34–46.
DOI:10.1016/j.carbpol.2016.06.104
|
Triki M, Tanazefti H, Kochkar H. 2017. Design of β-cyclodextrin modified TiO2 nanotubes for the adsorption of Cu(Ⅱ):Isotherms and kinetics study[J]. Journal of Colloid and Interface Science, 493: 77–84.
DOI:10.1016/j.jcis.2017.01.028
|
Wang S, Vincent T, Faur C, et al. 2016. Alginate and algal-based beads for the sorption of metal cations:Cu(Ⅱ) and Pb(Ⅱ)[J]. International Journal of Molecular Sciences, 17(9): 1453.
|
Wang W, Huang D, Kang Y, et al. 2013. One-step in situ fabrication of a granular semi-IPN hydrogel based on chitosan and gelatin for fast and efficient adsorption of Cu2+ ion[J]. Colloids and Surfaces B:Biointerfaces, 106: 51–59.
DOI:10.1016/j.colsurfb.2013.01.030
|
Yang J M, Yang J H, Tsou S C, et al. 2016. Cell proliferation on PVA/sodium alginate and PVA/poly(γ-glutamic acid) electrospun fiber[J]. Materials Science and Engineering:C, 66: 170–177.
DOI:10.1016/j.msec.2016.04.068
|
郑丹. 2014. 用于细胞培养的聚乙烯醇/海藻酸钙水凝胶力学性能的模拟及定量控制[D]. 重庆: 重庆大学. 56
|
钟远红, 梁晓亮, 朱建喜, 等. 2010. 钒掺杂磁铁矿对亚甲基蓝的吸附性能研究[J]. 环境科学, 2010, 31(6): 1568–1574.
|
Zhuang Y, Yu F, Chen H, et al. 2016. Alginate/graphene double-network nanocomposite hydrogel beads with low-swelling, enhanced mechanical properties, and enhanced adsorption capacity[J]. Journal of Materials Chemistry A, 4(28): 10885–10892.
DOI:10.1039/C6TA02738E
|
 2018, Vol. 38
2018, Vol. 38


