2. 北京工业大学城镇污水深度处理与资源化利用技术国家工程实验室, 北京 100124
2. National Engineering Laboratory of Urban Sewage Advanced Treatment and Resource Utilization Technology, Beijing University of Technology, Beijing 100124
自养型厌氧氨氧化(ANAMMOX)菌以氨为电子供体, 以亚硝酸盐为电子受体可直接反应生成氮气, 反应过程无需外加碳源, 因此, 该工艺是一种高效、节能的新型脱氮工艺(闾刚等, 2017b; 陈重军等, 2014; 喻徐良, 2017).Strous等(1998)通过元素平衡确定厌氧氨氧化反应基质NO2--N/NH4+-N理论比为1.32, 但在实际工程运行中, 由于反应器运行条件和菌种结构的不同, 并不完全符合理论比值.Tsushima等(2007)研究发现, NO2--N/NH4+-N为0.80~0.87时, 反应器去除效率较高; Jin等(2013)研究表明, 最佳NO2--N/NH4+-N为1.2, 此时出水总氮最低; 陈永等(2006)发现NO2--N/NH4+-N为1.34时, TN的去除率为87.7%, 过高或过低的进水NO2--N/NH4+-N都会导致NO2--N、NH4+-N的不完全转化.
亚硝酸盐氮浓度过高会对厌氧氨氧化过程产生抑制, 据报道(Strous et al., 1999), 当NO2--N浓度大于100 mg·L-1时, 能完全抑制厌氧氨氧化反应; 而Jetten等(1999)认为, 当NO2--N浓度大于280 mg·L-1时, 厌氧氨氧化过程才会被抑制, 但当NO2--N浓度大于140 mg·L-1时, 就已经不是厌氧氨氧化反应的最理想浓度.康晶等(2005)采用EGSB反应器, 在进水氨氮、亚硝和COD分别为100、100和650 mg·L-1时, 反应器所去除的NO2--N/NH4+-N值为2.63, 比理论值1.32大很多, 这是由于进水中存在大量的COD所致.
目前, 多数研究者实现厌氧氨氧化都基于高浓度的NH4+-N和NO2--N, 对于低基质浓度条件下的研究较鲜见.因此, 本研究采用低基质浓度条件, 同时改变基质比, 实现厌氧氨氧化的高效脱氮, 以期为实际厌氧氨氧化工程提供一定的参考.
2 材料与方法(Materials and methods) 2.1 实验装置ASBR反应器采用圆柱形有机玻璃制成(图 1), 直径14 cm, 高45 cm, 有效容积5 L.在其侧壁的垂直方向设置取样口, 底部设有排泥口, 上部设有通气口, 反应产生的气体经水封瓶排出, 为防止光对厌氧氨氧化菌活性的影响, 反应器外侧用黑色塑料布覆盖.
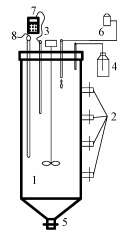 |
| 图 1 ASBR反应器示意图(1. ASBR反应器, 2.排水口, 3.搅拌器, 4.水封瓶, 5.排泥口, 6.缓冲瓶, 7. pH、ORP检测仪, 8.温控仪) Fig. 1 Schematic diagram of ASBR reactor |
试验污泥取自成功启动的厌氧氨氧化中的活性污泥, 具有良好的脱氮性能, 其MLSS为3500 mg·L-1, VSS为2550 mg·L-1.
2.3 试验用水水质及检测方法试验用水采用人工模拟污水, 其组成成分如下:NH4Cl(按需配), NaNO2 30 mg·L-1(以N计), 微量元素参照文献(Van der Star et al., 2007), KH2PO4 2 mg·L-1, KHCO3 110 mg·L-1, MgSO4·7H2O 20 mg·L-1, CaCl2·2H2O 20 mg·L-1.其中, 微量元素Ⅰ和微量元素Ⅱ各1.5 mL·L-1, 微量元素浓缩液Ⅰ组成为(mg·L-1):EDTA 5, FeSO4 5000;微量元素浓缩液Ⅱ组成为(mg·L-1):EDTA 5000, CoCl2·6H2O 240, ZnSO4·7H2O 430, MnCl2·4H2O 990, CuSO4·5H2O 250, NiCl2·6H2O 190, NaMoO4·2H2O 220, H3BO4 14, NaSeO4·10H2O 210, NO2--N与NH4+-N的浓度及比值见表 1.水样经过0.45 μm滤纸过滤后根据国家标准方法测定COD、NH4+-N、NO2--N、NO3--N(国家环境保护总局, 2002).
| 表 1 试验进水NO2--N、NH4+-N的浓度及比值 Table 1 Concentration and ratio of influent NO2--N and NH4+-N |
温度控制为30 ℃, 通过投加NaHCO3将进水的pH控制为(7.2±0.2).ASBR采用间歇运行, 瞬时进出水; 单周期运行4 h, 沉淀0.5 h后排水, 排水比为80%.每次改变NO2--N/NH4+-N的比值后, 运行7个周期.
3 结果与讨论(Results and discussion) 3.1 不同NO2--N/NH4+-N下氮素的变化图 2为进水基质比分别为0.9、1.1、1.3、1.4、1.5和1.6时, 氮素的变化.由图可知, NO2--N/NH4+-N为0.9时, 随着运行周期数的增加, 出水NO2--N、NH4+-N浓度均在逐渐降低, 但降低幅度较小; 至第7周期时, 出水NH4+-N、NO2--N及TN浓度分别为14.3、10.5和27.6 mg·L-1, 去除率分别为57.7%、64.2%和56.8%.NO2--N/NH4+-N为1.1时, 出水浓度随着运行周期数的增加均在降低; 运行至第14周期时, 出水NH4+-N、NO2--N及TN的去除率分别为70.6%、79.3%和70.2%.NO2--N/NH4+-N为1.3, 出水NO2--N、NH4+-N浓度略有波动, 但总体呈下降的趋势; 试验运行至第21周期时, 出水NH4+-N的浓度出现最小值3.6 mg·L-1, 去除率为84.7%;出水NO2--N浓度为4.5 mg·L-1, 去除率为85.2%;出水TN浓度为12.9 mg·L-1, 去除率为76.2%, 此阶段NO2--N、NH4+-N的去除率均比NO2--N/NH4+-N为0.9、1.1时高, 已很接近Strous等(1999)提出的理论值1.32, 说明ASBR反应器厌氧氨氧化功能较强.
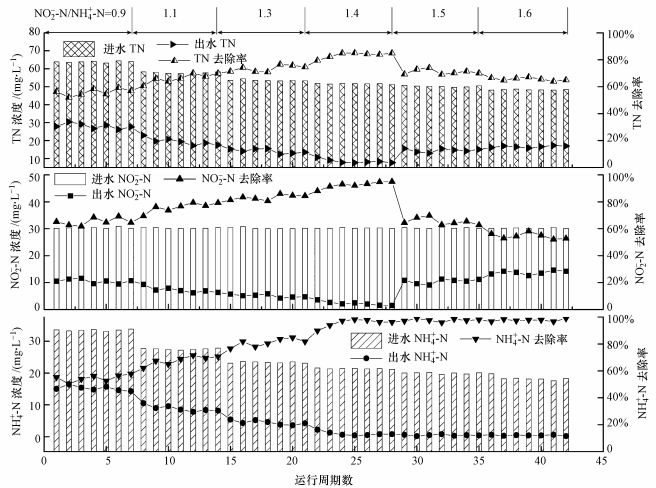 |
| 图 2 不同基质比下NH4+-N、NO2--N、TN的变化 Fig. 2 Variations of NH4+-N, NO2--N and TN under different NO2--N/NH4+-N |
当NO2--N/NH4+-N为1.4时, 反应运行至第28周期时达到稳定运行, 出水NH4+-N、NO2--N及TN浓度分别为0.8、1.5和7.7 mg·L-1, 去除率分别为96.2%、95.4%和85.3%.可见NO2--N/NH4+-N在0.9~1.4时, NO2--N、NH4+-N及TN的去除率均在增加.继续增大进水基质比达到1.5~1.6时, 出水NH4+-N浓度基本维持不变, 而出水NO2--N浓度却持续增加, 从第35周期时的11.4 mg·L-1增加至第42个周期时的14.2 mg·L-1, 去除率从62.8%下降至52.8%;相应的出水TN浓度从15.1 mg·L-1上升至17.3 mg·L-1, 去除率由70.1%下降至64.1%, 说明在此运行工况下, 低基质厌氧氨氧化反应不能完全进行, 使得出水水质严重恶化, 低基质厌氧氨氧化最适宜的NO2--N/NH4+-N比值应控制为1.4, 可以维持稳定且具有较高的脱氮性能.闾刚等(2017a)对厌氧折流板反应器(ABR)的厌氧氨氧化脱氮性能进行研究, 发现最佳基质比为1.34, 略大于理论值, 可能是由于反应体系中存在异养反硝化菌, 发生了反硝化.
3.2 不同NO2--N/NH4+-N下pH及NO3--N的变化图 3为在不同进水基质比及pH为(7.2±0.2)条件下, 出水pH与NO3--N的变化.可以看出, 在不同的NO2--N/NH4+-N条件下, 出水pH及NO3--N浓度有明显不同.当NO2--N/NH4+-N为0.9和1.1时, 出水pH值在7.9~8.1之间波动, 而出水NO3--N浓度由2.1 mg·L-1逐渐增大至3.9 mg·L-1; 当NO2--N/NH4+-N为1.3时, 出水pH值明显增加, 最后维持在8.21左右, 出水NO3--N浓度先增加至4.7 mg·L-1, 然后逐渐减小至4.4 mg·L-1; NO2--N/NH4+-N为1.4时, 出水pH值逐渐增大, 最后稳定在8.26~8.33之间, 与Strous等(1999)研究结果一致, 出水NO3--N浓度呈增大趋势.然而当NO2--N/NH4+-N为1.5和1.6时, 出水pH值出现小幅下降, 最小值为8.11, 本阶段出水NO3--N浓度呈降低的趋势.分析原因可能是由于内源反硝化作用所致, 这与闾刚等(2017a)的研究结果相符.田智勇等(2009)研究了上向流厌氧氨氧化生物滤池中pH的变化规律, 结果表明, 由于H+的消耗使厌氧氨氧化过程中pH上升.因此, 出水pH值和NO3--N浓度的下降说明厌氧氨氧化的过程出现异常, 说明这两个比值已不是最佳的进水基质条件, 同样说明可以根据pH值及NO3--N的浓度变化衡量厌氧氨氧化反应器脱氮性能是否良好(李亚峰等, 2013; 鲍林林等, 2012; 李伟刚, 2014).
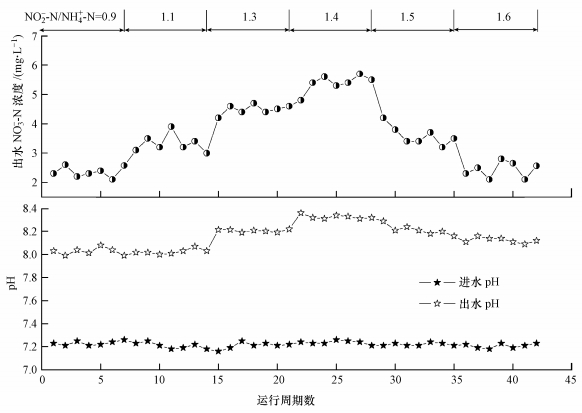 |
| 图 3 不同基质比下pH、NO3--N的变化 Fig. 3 Variations of pH and NO3--N under differnet NO2--N/NH4+-N |
在废水处理工程应用中, 反应化学计量比具有一定的指导意义.图 4为不同进水基质比时, 发生厌氧氨氧化的ΔNO2--N/ΔNH4+-N比值(反应掉的NO2--N量与反应掉的NH4+-N量的比).当进水NO2--N/NH4+-N为0.9时, 厌氧氨氧化的ΔNO2--N/ΔNH4+-N在1.03~1.14之间波动, ΔNO3--N/ΔNH4+-N(生成的NO3--N量与反应掉的NH4+-N的比)为0.11~0.15;当进水NO2--N/NH4+-N为1.1时, 厌氧氨氧化的ΔNO2--N/ΔNH4+-N值基本稳定在1.23, ΔNO3--N/ΔNH4+-N值为0.16~0.20.当进水NO2--N/NH4+-N为1.3时, 实际厌氧氨氧化的ΔNO2--N/ΔNH4+-N值为1.28~1.40, ΔNO3--N/ΔNH4+-N为0.23~0.26.当进水NO2--N/NH4+-N为1.4时, 厌氧氨氧化的计量关系更稳定, 实际发生厌氧氨氧化的ΔNO2--N/ΔNH4+-N值约为1.37, 比理论值1.32偏高, 可能是进水中的小部分NO2--N直接发生了反硝化.马斌(2012)发现, ΔNO2--N/ΔNH4+-N平均为1.19, 比理论值偏低, 可能是由于反应器内发生了反硝化, 使得厌氧氨氧化产生的NO3--N被还原为NO2--N.从图 4还发现, ΔNO3--N/ΔNH4+-N为0.25~0.28, 与理论值0.26一致.综上所述, 当进水NO2--N浓度不变而NH4+-N的浓度减小时, ΔNO2--N/ΔNH4+-N与ΔNO3--N/ΔNH4+-N均增大, 这与唐崇俭等(2010)的研究结果一致.但当进水NO2--N/NH4+-N继续增加为1.5和1.6, 实际发生厌氧氨氧化反应的计量比发生很大的变化, 导致ΔNO2--N/ΔNH4+-N及ΔNO3--N/ΔNH4+-N均下降, 分析原因主要是由于进水NO2--N/NH4+-N的值严重偏离理论值, 可能使菌群结构发生变化, 导致厌氧氨氧化反应恶化, 因此, NO2--N/NH4+-N的最佳值应为1.4.
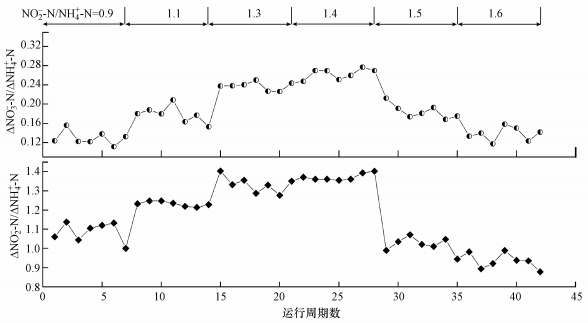 |
| 图 4 厌氧氨氧化反应的计量比变化 Fig. 4 Variations of nitrogen stoichiometric ratio for ANAMMOX |
图 5为典型周期内NO2--N、NH4+-N、pH及ORP的变化, 在进水NO2--N/NH4+-N为1.4时, 在前30 min内, NH4+-N、NO2--N浓度降低缓慢, 导致厌氧氨氧化反应的脱氮延迟, 这可能是由于ASBR反应器进水后, 微生物需要适应新环境, 这与李伟刚(2014)的研究相符.在30~100 min内, NO2--N、NH4+-N的下降速率都较大, 运行至100 min时, 出水NO2--N、NH4+-N浓度分别为6.8、5.2 mg·L-1.在100~240 min内, NO2--N、NH4+-N的下降速率逐渐减小, 这是由于厌氧氨氧化所需的底物浓度较低, 限制了反应速率.运行至240 min时, 出水NO2--N、NH4+-N浓度分别低至1.9、0.8 mg·L-1, 在整个周期内, 出水NO2--N、NH4+-N浓度逐渐减小.随着进水NH4+-N和NO2--N的逐渐降解, 反应器中pH值曲线不断攀升, 而ORP曲线呈下降趋势.ORP与pH值的线性拟合如图 6所示, 可决系数R2高达0.96, 这与有关文献(Lindsay et al., 2001; Kartal et al., 2008)的报道相吻合.因此, ORP可以作为厌氧氨氧化反应中重要的指示性参数.
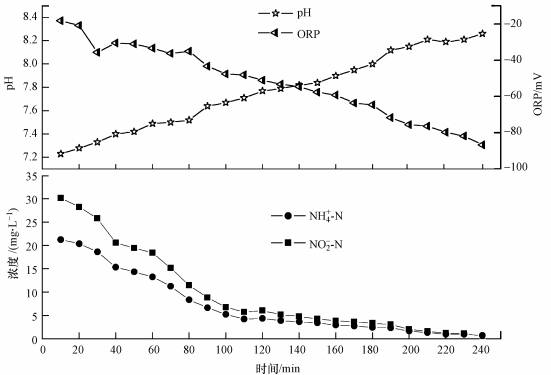 |
| 图 5 典型周期内NH4+-N、NO2--N、pH及ORP的变化 Fig. 5 Variations of NH4+-N、NO2--N、pH and ORP at typical cycle |
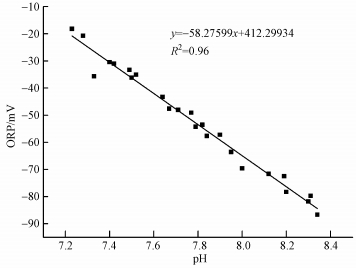 |
| 图 6 典型周期内ORP与pH的线性拟合 Fig. 6 Linear relationship between ORP and pH at typical cycle |
1) 在反应器进水NO2--N浓度为(30.0±0.2) mg·L-1, NO2--N/NH4+-N从0.9升高至1.6的过程中, NO2--N和NH4+-N的去除率先升高后降低, NO2--N/NH4+-N为1.4时, NO2--N、NH4+-N的去除率分别高达95.4%、96.2%, 且总氮的去除率达到85.3%.
2) 当进水的NO2--N/NH4+-N为1.4时, 厌氧氨氧化的ΔNO2--N/ΔNH4+-N约为1.37, ΔNO3--N/ΔNH4+-N为0.25~0.28, 表明发生厌氧氨氧化反应的比值关系更稳定.
3) 进水NO2--N/NH4+-N为1.4时, 周期内NO2--N、NH4+-N降解速率最大的时间段为30~100 min; 整个周期内, ORP与pH呈负向变化关系, 可决系数R2为0.96, ORP可以作为厌氧氨氧化反应过程的指示性参数.
鲍林林, 赵建国, 李晓凯, 等. 2012. 常温低基质下pH值和有机物对厌氧氨氧化的影响[J]. 中国给水排水, 2012, 28(13): 38–42.
DOI:10.3969/j.issn.1000-4602.2012.13.009 |
陈永, 张树德, 张杰, 等. 2006. 亚硝酸盐氮浓度对厌氧氨氧化反应的影响[J]. 中国给水排水, 2006, 22(17): 74–76.
DOI:10.3321/j.issn:1000-4602.2006.17.020 |
陈重军, 王建芳, 张海芹, 等. 2014. 厌氧氨氧化污水处理工艺及其实际应用研究进展[J]. 生态环境学报, 2014, 23(3): 521–527.
|
国家环境保护总局. 2002. 水和废水检测分析方法(第4版)[M]. 北京: 中国科学出版社: 1–10.
|
Jetten M S, Strous M, van de Pas Schoonen K T, et al. 1999. The anaerobic oxidation of ammonium[J]. FEMS Microbiology Reviews, 22(5): 421–437.
|
Jin R C, Xing B S, Yu J J, et al. 2013. The importance of the substrate ratio in the operation of the Anammox process in upflow biofilter[J]. Ecological Engineering, 53(3): 130–137.
|
Kartal B, van Niftrik L A, Rattray J, et al. 2008. Candidatus "Brocadia fulgida" an Autofluorescent anaerobic ammonium oxidizing bacterium[J]. FEMS Microbiology Ecology, 63(1): 46–55.
DOI:10.1111/fem.2008.63.issue-1
|
康晶, 王建龙. 2005. EGSB反应器中厌氧颗粒污泥的脱氮特性研究[J]. 环境科学学报, 2005, 25(2): 208–213.
|
李伟刚. 2014. ASBR反应器厌氧氨氧化的工艺特性与控制策略研究[D]. 青岛: 青岛大学. 18-24
|
李亚峰, 张文静, 马晨曦. 2013. pH值和DO对厌氧氨氧化脱氮性能的影响[J]. 沈阳建筑大学学报(自然科学版), 2013, 29(4): 715–720.
|
闾刚, 徐乐中, 沈耀良, 等. 2017a. 基质比对ABR厌氧氨氧化工艺脱氮性能的影响[J]. 环境科学, 2017a, 38(5): 2006–2011.
|
闾刚, 徐乐中, 沈耀良, 等. 2017b. 快速启动厌氧氨氧化工艺[J]. 环境科学, 2017b, 38(3): 1116–1121.
|
Lindsay M R, Webb R I, Strous M, et al. 2001. Cell compartmentalisation in planctomycetes:novel types of structural organisation for the bacterial cell[J]. Archives of Microbiology, 175(6): 413–429.
DOI:10.1007/s002030100280
|
马斌. 2012. 城市污水连续流短程硝化厌氧氨氧化脱氮工艺与技术[D]. 哈尔滨: 哈尔滨工业大学. 77-80
|
Strous M, Heijnen J J, Kuenuen J G, et al. 1998. The sequencing batch reactor as a powerful tool for the study of slowly growing anaerobic ammonium-oxidizing microorganisms[J]. Applied Microbiology and Biotechnology, 50(5): 589–596.
DOI:10.1007/s002530051340
|
Strous M K, uenen J G, Jetten M S M. 1999. Key physiology ofanaerobic ammonium oxidation[J]. Applied and Environmental Microbiology, 65(7): 3248–3250.
|
Tsushima I, Ogasawara Y, Kindaichi T, et al. 2007. Development of high-rate anaerobic ammonium-oxidizing (anammox) biofilm reactors[J]. Water Research, 41(8): 1623–1634.
DOI:10.1016/j.watres.2007.01.050
|
唐崇俭, 郑平. 2010. 厌氧氨氧化膨胀污泥床反应器的化学计量学特性[J]. 中国环境科学, 2010, 30(11): 1446–1452.
|
田智勇, 李冬, 张杰. 2009. 厌氧氨氧化过程中COD及pH与基质浓度之间的关系[J]. 环境科学, 2009, 30(11): 3342–3346.
DOI:10.3321/j.issn:0250-3301.2009.11.035 |
Van der Star W R L, Abma W R, Blommers D, et al. 2007. Start up of reactors for anoxic ammonium oxidation:Experiences from the first full-scale anammox reactor in Rotterdam[J]. Water Research, 41(18): 4149–4163.
DOI:10.1016/j.watres.2007.03.044
|
喻徐良. 2017. ABR厌氧氨氧化反硝化协同脱氮除碳及微生物特性研究[D]. 苏州: 苏州科技大学. 1-6
|
 2018, Vol. 38
2018, Vol. 38


