2. 中国科学院安徽光学精密机械研究所大气物理化学实验室, 合肥 230031
2. Laboratory of Atmospheric Physico-Chemistry, Anhui Institute of Optics and Fine Mechanics, Chinese Academy of Sciences, Hefei 230031
来自机动车尾气、牲畜排泄物、肥料和其他非农业源排放的氨(NH3)是大气中常见的主要碱性污染气体.外场测量结果表明, 偏远地区NH3的浓度低于500 ppt, 而集约化农作地大气中NH3的浓度则达到10~20 ppb(Sharma et al., 2014).同时, 机动车尾气是城市大气氨的一个重要来源(Sun et al., 2017), 随着城市机动车保有量的日益增多, 导致城市大气中NH3浓度逐渐增加.大气中NH3的主要汇机制是干湿沉降和酸性气体的中和反应(Zhu et al., 2015;Bash et al., 2013).研究表明, NH3在大气中与H2SO4和HNO3反应可以形成NH4HSO4、(NH4)2SO4和NH4NO3, 这些铵盐凝结形成的二次无机气溶胶(Secondary Inorganic Aerosol, SIA)能够散射太阳光, 降低大气能见度(Schiferl et al., 2014;Chen et al., 2016).
最近的研究显示, NH3还能够影响大气二次有机气溶胶(Secondary Organic Aerosol, SOA)的形成和化学组分.Na等(2006)在苯乙烯与O3的烟雾腔实验中加入NH3后, 探测到生成的SOA颗粒数量和体积浓度在短时间内明显降低.他们认为主要是加入的NH3能够与颗粒相中间产物发生反应, 如3, 5-二苯基-1, 2, 4-三恶烷和羟基取代酯反应, 产生挥发性的产物导致SOA数量减少.相较于Na等(2006)的研究结果, Na等(2007)和Babar等(2017)在烟雾腔和流动反应管的实验中则发现在NH3存在下, NH3同α-蒎烯臭氧化产生的气相有机酸产物发生酸碱中和反应, 形成可凝结的有机铵盐, 使SOA颗粒的数量和体积浓度显著增加.此外, NH3还能够与SOA中的羰基成分相互作用, 形成含氮有机物.这些产物能够有效吸收近紫外光(300~400 nm)和短波长的可见光辐射, 对辐射强迫有重要贡献(Laskin et al., 2015;Andreae et al., 2013).
Updyke等(2012)将人为源和生物源前体物与·OH和O3光反应形成的SOA颗粒收集在滤膜上, 并暴露在NH3环境下, 利用紫外可见吸收光谱测量得到的NH3存在时的柠檬烯和倍半萜烯SOA的质量吸收系数(MAC)与生物质燃烧颗粒的MAC值几乎相等.Flores等(2014)采用宽带腔增强光谱测量了NH3存在时生物源SOA颗粒的复折射率(RI).相比于生物源臭氧化产生的SOA, NH3存在时的生物源SOA的实部值(n)没有明显变化, 但NH3存在下的柠檬烯和α-草烯SOA, 其虚部值(k)从k = 0增加到了0.030.此外, Liu等(2015)还开展了间二甲苯和α-蒎烯SOA吸附NH3的非均相实验研究.该研究利用气溶胶质谱仪测量得到一系列含有有机氮碎片的离子峰, 这进一步验证了NH3能够同SOA中羰基成分发生反应形成含氮有机物.
上述实验主要侧重于NH3存在时生物源SOA的光学参数(MAC、RI)测量研究.然而, 这些研究没有考虑表征含氮有机产物的详细化学成分.来源于机动车尾气和溶剂挥发等人为活动排放的甲苯等挥发性有机物(VOCs)是SOA的重要前体物(陈文泰等, 2013; 谢绍东等, 2010).它们在大气中主要同·OH反应产生难挥发性和半挥发性产物, 这些产物通过自身凝结或气体相/微粒相均分形成SOA粒子(Li et al., 2016;Gentner et al., 2017), 成为大气PM2.5的重要组成部分.然而, NH3对苯系物SOA的形成和化学组分的影响研究却鲜见报道.最近Huang等(2016; 2017)利用扫描移动粒径谱仪和气溶胶激光飞行时间质谱仪测量了苯系物SOA在硫酸铵、氯化钙等无机细粒子存在下的质量浓度和化学组分.本文利用自制的烟雾腔系统开展NH3对甲苯SOA形成和化学组分的影响研究, 并采用扫描移动粒径谱仪、气溶胶激光飞行时间质谱仪、紫外-可见分光光度计、衰减全反射傅里叶变换红外光谱仪和荧光光谱仪测量产生的SOA粒子, 以期为人为源SOA的形成机制研究提供实验依据.
2 材料与方法(Materials and methods) 2.1 实验药品与器材甲苯购于汕头市达濠精细化学品有限公司, 氨水购于西陇化工股份有限公司, 甲醇购于Sigma Aldrich(St.Louis, MO), 以上药品均为分析纯.臭氧通过臭氧发生器(青岛新美净化设备有限公司)产生.
2.2 烟雾腔实验装置与表征甲苯SOA的形成在自制的烟雾腔装置内进行.该装置由零空气系统、进样系统、烟雾腔系统和检测系统组成.零空气系统所需的气源由空气压缩机提供, 产生的气体首先通过活性炭过滤器, 吸附除去空气中的痕量碳氢化合物;其次经过变色硅胶过滤器, 除去空气中含有的水蒸气;最后经过Balston DFU Grade BX过滤器, 除去悬浮颗粒物后得到零空气.进样系统由液体汽化瓶、流量控制器和配气管道组成.液体汽化瓶的体积为250 mL, 放在加热套中, 加热温度可在0~100 ℃范围内调节.用微量注射器抽取所需的液体样注射入汽化瓶中挥发成气体, 再用零空气将其吹入烟雾腔内.臭氧、氨等样品通过流量控制器控制一定流速注入配气管道一定时间后, 用零空气注入烟雾腔.烟雾腔系统的框架呈长方体形结构, 长1.5 m、宽0.5 m、高1.8 m, 由冷轧钢板组装制成, 左右两面各安装2只功率为40 W、辐射波长范围为200~400 nm的紫外灯.烟雾腔腔体是Teflon薄膜材料制成的不规则圆柱体, 表面积为3.6 m2, 体积为400 L, 表面积体积比为9 m-1, 腔体前段安装进样管口、采样管口.检测系统主要有配备离子火焰检测器的气相色谱(GC-FID, Agilent 7820A)、臭氧分析仪(TEI model 49i)、氨分析仪(TEI model 17i)、扫描电迁移率粒径谱仪(Scanning Mobility Particle Sizer, SMPS, TSI 3080L DMA, TSI 3775 CPC)和气溶胶激光飞行时间质谱仪(Aerosol Laser Time-of-flight Mass Spectrometer, ALTOFMS)来测量烟雾腔内甲苯、臭氧、氨、SOA的质量浓度、粒径分布和化学组分.
实验正式开始进行前, 需要对烟雾腔装置进行一系列的表征.首先向新搭建的烟雾腔内充入1000 ppm的臭氧气体, 并用4只紫外灯光照24 h, 清除Teflon薄膜内表面残留的有机物.参照课题组前期的表征方法(刘宪云等, 2009), 开展了4个表征实验:①向烟雾腔内充满纯的洁净空气, 4只紫外灯光照2 h;②向烟雾腔内注入10 ppm的甲苯/洁净空气混合气体, 4只紫外灯光照2 h;③向烟雾腔内注入60 ppm的臭氧/洁净空气混合气体, 4只紫外灯光照2 h;④向烟雾腔内注入甲苯/臭氧/洁净空气混合气体, 其浓度分别为甲苯10 ppm、臭氧60 ppm, 不开紫外灯暗反应2 h.然后利用SMPS测量反应过程中腔内颗粒物浓度.2 h后, 以4 L·min-1的流速将腔内的气体抽至装有10 mL 3%甲醇溶液的洗气瓶内, 再将收集在洗气瓶里的产物进行紫外离线测量.
2.3 实验方法每次实验开始前, 用零空气清洗气袋3次.清洗后向Teflon气袋充入一定体积的零空气, 然后根据实验需要, 利用进样系统依次注入甲苯、臭氧和NH3, 随后用零空气充至满体积状态.打开4只紫外灯光照, 臭氧在波长为254 nm的紫外光照射下产生·OH, 启动甲苯光氧化反应形成SOA粒子.并利用SMPS实时在线测量烟雾腔内形成的SOA粒子的质量浓度和粒径分布.在光照2 h后, 连接自制的ALTOFMS测量SOA的化学组分.随后以4 L·min-1的流速将腔内的剩余气体抽至装有10 mL 3%甲醇溶液的洗气瓶内, 将反应产物收集在3%甲醇溶液后进行紫外、红外和荧光等离线测量.
为了研究NH3对甲苯SOA形成和化学组分的影响, 在烟雾腔装置表征的基础上, 分别开展了无NH3和有NH3条件下的两组实验, 每组实验各平行重复3次.无NH3条件下的对照实验, 只往烟雾腔内注入10 ppm甲苯与60 ppm臭氧;有NH3条件下的实验则往腔内注入10 ppm甲苯、60 ppm臭氧和10 ppm氨.然后打开紫外灯进行光照反应, 并进行在线和离线的检测与分析.
2.4 甲苯SOA化学组分的在线检测利用扫描电迁移率粒径谱仪(SMPS)实时获得光反应过程中烟雾腔内颗粒物质量浓度和粒径的变化情况.SMPS主要由差分迁移分析仪DMA(Differential Mobility Analyzer, Model 3080L, 美国TSI公司)和凝结核计数器CPC(Condensation Particle Counter, Model 3775, 美国TSI公司)及相应的微机软件程序AIM(Aerosol Instrument Manager)三大部分组成.实验时DMA的扫描电压范围是-10~-9591 V, 扫描时间为135 s, 碰撞器为0.0457 cm, 粒径测量范围是14~673 nm.DMA鞘流与样流流量比为10:1, 其中, 鞘流为3.0 L·min-1, 样流为0.3 L·min-1.实验每次光照开始时同时运行SMPS, 仪器每隔3 min自动测量一次烟雾腔内的颗粒物数量、颗粒直径和质量浓度.
气溶胶激光飞行时间质谱仪(ALTOFMS)能够实时测量气溶胶粒子的粒径和化学组分.主要由进样系统、粒径测量系统和化学成分分析系统组成.光反应形成的气溶胶粒子通过空气动力学透镜后, 先后经过两个skimmer形成准直的气溶胶粒子束, 然后进入粒径测量系统.在该系统内, 有两个相距70 mm的532 nm二极管, 激光经过透镜聚焦后垂直照射到气溶胶粒子的飞行路径上.进入飞行路径的气溶胶粒子先后与这两个二极管激光相遇, 由光电倍增管接收产生的散射光, 再由计时电路计算出气溶胶粒子在这两束激光间的飞行速度, 由于粒子的飞行速度与粒径大小有确定性关系, 即可以用测出的气溶胶粒子的飞行速度计算得到该粒子的粒径大小.气溶胶粒子离开粒径测量系统后进入质谱仪真空腔中, 被248 nm的KrF激光解吸附电离, 产生的离子经飞行时间质谱仪测量得到激光电离产生的全部离子的质谱图, 由质谱图上的离子峰获得气溶胶粒子化学成分信息.
2.5 甲苯SOA化学组分的离线测量为了进一步验证甲苯SOA的化学组分, 将洗气瓶收集的样品溶液分别进行紫外、红外和荧光等离线测量.以3%甲醇溶液作为参比, 采用双光束紫外-可见分光光谱仪(UV-Visible spectrophotometer, UV-6100s, 上海Mapada公司)测量甲苯SOA样品溶液在200~600 nm范围内的吸光度, 获得产物分子对紫外可见光特征吸收.同时利用荧光光谱仪(Fluorescence Spectrometer, Cary Eclipse, 美国Varian Medical Systems公司)对产物样品进行测量, 得到产物的荧光谱图.传统的FTIR常采用液膜法测量液相产物样品, 操作繁琐、消耗时间长.本文采用衰减全反射傅里叶变换红外光谱仪(Attenuated Total Reflection Fourier Transform Infrared Spectrometer, NICOLET iS 10, 美国Thermo Fisher Scientific公司)直接测量液相样品溶液, 扫描光谱范围为450~4000 cm-1, 扫描速度为0.4747 cm·s-1.
3 结果与讨论(Results and discussion) 3.1 烟雾腔装置的表征结果SMPS测量结果表明, 在4个表征实验中, 2 h内腔内的颗粒物的数量浓度始终维持在1~5个·cm-3, 图 1所示的紫外可见吸收光谱也未见吸收峰存在, 这表明紫外辐照清洁空气、臭氧/清洁空气混合气体、甲苯/清洁空气混合气体和甲苯/臭氧/清洁空气暗反应均不会产生新的颗粒物.烟雾腔系统可以用于SOA的模拟实验研究.
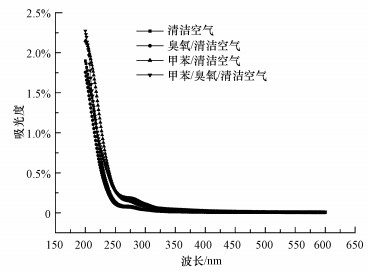 |
| 图 1 4种条件下暗反应2 h后产物的紫外可见吸收光谱 Fig. 1 UV-Vis absorption spectrum of the product after reacting for 2 hours under four conditions |
SMPS每隔3 min测量烟雾腔内颗粒物的质量浓度和粒径分布.图 2显示了反应时间在0~60 min范围内生成的SOA质量浓度和中心粒径分布情况.从图 2a可以看出, 在没有NH3存在下, 在光氧化反应前3 min内, 臭氧光解产生的·OH比较少, ·OH与甲苯反应产生少量的光氧化产物, 大部分产物不能达到其饱和蒸气压, 因此, 几乎没有SOA颗粒生成(Li et al., 2016;Gentner et al., 2017).在光照3 min后, 随着·OH浓度的增大, 氧化产物不断产生, 达到其饱和蒸气压后凝结形成SOA粒子.此后, 光氧化产物通过气体相/微粒相均分形成SOA粒子, 使得SOA粒子的浓度和粒径迅速增大.因此在3~30 min内, SOA浓度急剧增加, 从40 μg·m-3增加到580 μg·m-3.如图 2b所示, SOA粒子的中心粒径从3 min时的40 nm迅速增大至30 min时的120 nm.在随后的30~60 min内, 随着辐照时间的延长, 形成的SOA的质量浓度逐渐增大, 中心粒径也随之变大, 在60 min时, 烟雾腔内的甲苯SOA的质量浓度达到最大值800 μg·m-3, 中心粒径增至160 nm.随后腔内的SOA粒子由于湍流、布朗扩散等原因, 沉积在烟雾腔壁上, 造成SOA粒子浓度逐渐减小, 但SOA粒径分布基本保持不变.
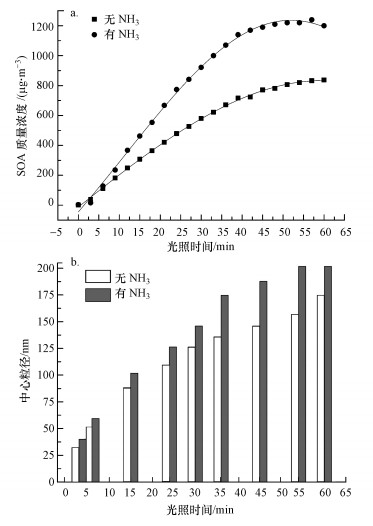 |
| 图 2 在无氨和有氨条件下甲苯SOA质量浓度(a)和甲苯SOA产物的中心粒径(b)随光照时间的变化规律 Fig. 2 The changes regulation of mass concentration of toluene SOA(a) and central particle size of toluene SOA(b) in the absence and presence of ammonia with illumination time |
将图 2综合起来可以看出, 在无NH3和有NH3条件下甲苯SOA的质量浓度和中心粒径随光照时间的变化规律基本相似.在光照3、15、30和60 min的过程中, 两种条件下甲苯SOA的质量浓度均有较为显著的增加, 并且中心粒径也都呈现出随光照时间的延长而逐渐增大的趋势, 只不过有NH3时形成的SOA粒子的质量浓度增加更为显著, 其中心粒径增长的速度也更快.在光照60 min的时间范围里, 有NH3时形成SOA的质量浓度和中心粒径分别可以达到最大值1200 μg·m-3和200 nm, 相比于无NH3时的最大质量浓度800 μg·m-3和最大中心粒径160 nm, 分别增加了50%和25%.这表明NH3能够改变甲苯与·OH光氧化产物的气体相/微粒相均分过程, 使更多的气相组分均分为微粒相, 导致SOA粒径增大, 从而显著促进甲苯SOA的形成.这些实验情况与Liu等(2015)的实验结果较为一致, 他们通过研究发现, ·OH启动间-二甲苯光氧化产生的SOA粒子能够吸收NH3发生非均相反应形成颗粒相含氮有机物, 使间-二甲苯SOA质量浓度显著增大.为了进一步表征产生的含氮有机产物, 开展了有NH3存在时甲苯SOA样品的紫外、红外、荧光和气溶胶激光飞行时间质谱测量.
3.2 甲苯SOA化学组分的紫外-可见吸收光谱和红外光谱研究甲苯SOA样品溶液的紫外-可见吸收光谱如图 3所示.无NH3时, 甲苯SOA样品溶液紫外吸收曲线在可见光400~600 nm范围内没有明显的吸收峰, 但在205 nm处有一个较强的吸收带.根据Carlton等(2007)的实验结果, 该吸收带是羧基(—COOH)的n→π*跃迁产生的特征吸收.这表明羧酸类化合物是无NH3条件下甲苯SOA主要的化学组分.图 4a所示的红外吸收图中3256 cm-1处有较强的宽吸收峰, 对应为O—H的伸缩振动;1643 cm-1的吸收峰为C=O伸缩振动特征吸收峰;1055 cm-1的吸收峰为C—O伸缩振动吸收峰, 这些红外吸收峰进一步证实羧酸产物的存在.
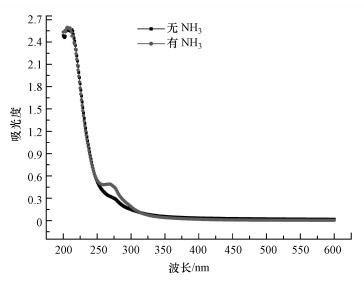 |
| 图 3 有氨和无氨条件下甲苯SOA样品溶液的紫外-可见吸收光谱图 Fig. 3 UV-Vis spectra of the sample solution of toluene SOA in the absence and presence of ammonia |
 |
| 图 4 无氨(a)和有氨(b)条件下甲苯SOA样品溶液的红外谱图 Fig. 4 Infrared spectra of the sample solution of toluene SOA in the absence (a) and presence (b) of ammonia |
前期烟雾腔实验已证实醛类化合物是甲苯与·OH光氧化反应的主要产物(Jang et al., 2001;Huang et al., 2011;张宇飞等, 2015), 根据Jang等(2001)提出的反应机理, 如图 5所示, ·OH与甲苯主要发生提取反应和加成反应. ·OH摘取甲苯甲基上的氢原子, 形成H2O和苯甲基自由基C6H5CH2·, 该自由基与O2和NO发生后续反应产生苯甲醛和苯甲酸. ·OH与苯环的加成反应是主要的反应通道, ·OH可加成到甲苯的邻位、间位和对位, 但形成的邻-OH-甲苯加合物是最稳定的.该加合物继续与O2和NO反应, 导致苯环裂解, 产生2-甲基-2, 4-己二烯二醛、环氧丁烯二醛和乙二醛等醛类产物.这些醛类产物在无NH3存在下, 与OH、HO2等自由基发生反应(图 5). ·OH与醛类化合物发生摘取醛基上氢原子的提取反应, 在O2分子存在的情况下又反应产生过氧自由基, 该过氧自由基与HO2自由基反应, 形成O3和2-甲基-2, 4-己二烯二酸、环氧丁烯二酸和乙二酸等羧酸产物.
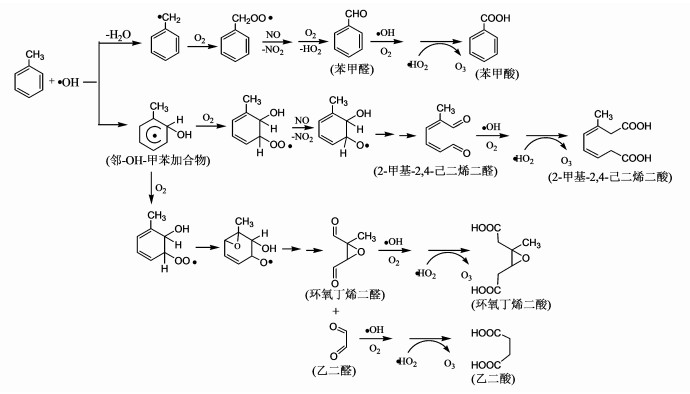 |
| 图 5 甲苯与·OH反应形成醛和羧酸产物的可能反应机理 Fig. 5 The possible reaction mechanism for the formation of aldehyde and carboxylic acids from toluene reaction with OH radical |
NH3存在时甲苯SOA样品溶液紫外吸收光谱除了在205 nm处有一个较强的吸收带外(图 3), 该曲线还在270 nm附近出现了一个新的吸收带, 这表明有新的产物形成.Lee等(2013)利用紫外可见吸收光谱表征了含有乙二醛和硫酸铵的液相气溶胶的化学组分, 也测量得到270 nm处的吸收带.他们认为是NH3与乙二醛反应产生的1H-咪唑、4-咪唑甲醛等咪唑类含氮化合物中C=N双键的n→π*电子跃迁产生的吸收. ·OH与甲苯光氧化产生的乙二醛是产率最大的醛类产物, 它通过自身凝结或气体相/微粒相均分形成SOA粒子, 在NH3存在的条件下, 我们推测这些乙二醛粒子吸收NH3发生类似的反应形成咪唑类产物.按照Lee等(2013)和Maxut等(2015)建议的反应机理, 如图 6所示, NH3会亲核进攻乙二醛羰基上的氧原子, 形成中间产物二亚胺(1), 同时凝结的乙二醛发生水合反应形成四醇产物(2), 二亚胺N上的氢会同四醇产物的OH发生脱水反应形成物质(3), 物质(3)的氮原子上的孤对电子会进攻碳原子, 脱水后形成物质(4), 物质(4)发生重排和断裂形成甲酸和1H-咪唑.此外, 物质(4)也会发生如图 6所示的重排形成物质(5), 脱水后产生4-咪唑甲醛(Lee et al., 2013).Teich等(2016)利用毛细管-质谱联用装置定量测量得到大气气溶胶含有咪唑甲醛等5种咪唑类化合物, 进一步验证了这一实验结果.
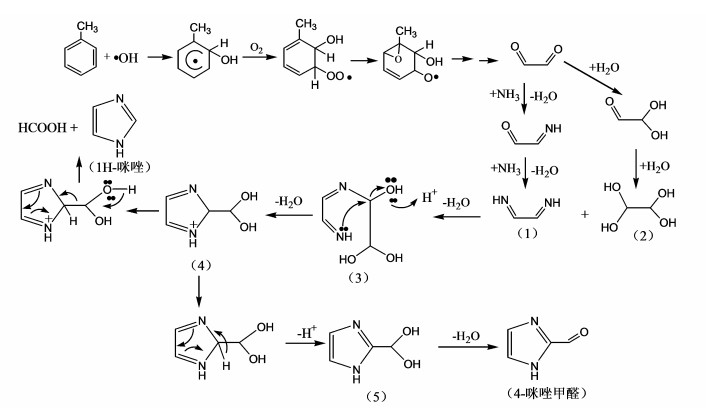 |
| 图 6 形成咪唑类产物的可能反应机理 Fig. 6 The possible reaction mechanism for the formation of imidazole products |
咪唑类产物也被图 4b所示的有NH3存在时的甲苯SOA样品的红外谱图进一步证实.除了在3600~4000 cm-1处有O—H的伸缩振动吸收峰, 在1600~1700 cm-1有C=O伸缩振动特征吸收峰, 1087 cm-1处存在C—O伸缩振动吸收峰外, 还在1800~1400 cm-1的范围内出现了数个新的吸收峰.图 4b中1698~1743 cm-1吸收峰对应为C=N伸缩振动特征吸收峰, 1518 cm-1处的红外吸收为N—H弯曲振动, 而1457 cm-1处的吸收峰对应为C—N伸缩振动.综合紫外可见吸收光谱和红外光谱及Lee等(2013)提出的反应机理, 可以判断NH3与甲苯SOA的二醛组分反应产生了咪唑类产物.该产物含有共轭双键体系和刚性平面结构, 是常见的荧光物种.甲苯SOA样品溶液的荧光测量结果也证实这一情况.无NH3条件下的甲苯SOA样品溶液经荧光光谱仪测量, 没有得到荧光谱图.这是因为其产物主要是乙二醛酸、2-甲基-2, 4-己二烯酸等羧酸化合物.这些羧酸虽然具有共轭双键体系, 能够吸收205 nm的紫外光, 但没有刚性的平面结构, 而不能发射荧光.图 7显示了NH3存在时甲苯SOA样品的荧光光谱图, 其最大的激发波长为268 nm, 与紫外吸收波长270 nm基本一致, 最大荧光发射波长为297 nm, 说明具有较强的荧光效率.
 |
| 图 7 氨存在时甲苯SOA样品溶液的荧光谱图 Fig. 7 Fluorescence spectra of the sample solution of toluene SOA in the presence of ammonia |
为了进一步确认甲苯SOA的化学组分, 采用自制的气溶胶激光飞行时间质谱仪在线测量SOA粒子.图 8a显示的是无NH3存在下, 100个甲苯SOA粒子的平均正离子质谱图.图中相对强度最大的质谱峰是m/z = 44.Sato等(2012)和Alfarra等(2006)通过实验证实m/z = 44的质谱峰是羧酸化合物的羧基失去氢后产生的COO+.此外, 该质谱图中还存在有m/z = 29和m/z = 57的碎片离子峰.参照有机质谱知识, m/z= 29可能对应的结构为醛基离子(HCO+)和乙基离子(C2H5+);而m/z= 57可能对应的结构为二醛基离子(HCOCO+)和丁基离子(C4H9+).根据图 5所示的甲苯与·OH反应机理, 不能产生含有乙基和丁基的产物.因此, m/z= 29和m/z= 57是苯甲醛、乙二醛等醛类产物激光解吸附电离产生的HCO+和HCOCO+离子.这些进一步表明由醛类化合物被·OH氧化形成的羧酸化合物是无NH3条件下甲苯SOA主要的化学组分.而图 8b所示的NH3存在时100个甲苯SOA粒子的平均正离子质谱图明显不同于无NH3情况下的质谱图, 但与Lee等(2013)实验测得的1H-咪唑的质谱较为相似.图中除了含有羧酸化合物的特征裂解峰m/z = 44(COO+)外, 还含有1H-咪唑的特征裂解峰m/z= 67 (C3H3N2+)、m/z = 41 (C2H2N+)和m/z= 28 (CH2N+), 这进一步验证了咪唑类化合物是NH3与甲苯SOA中二醛组分发生反应形成的新产物(Maxut et al., 2015).
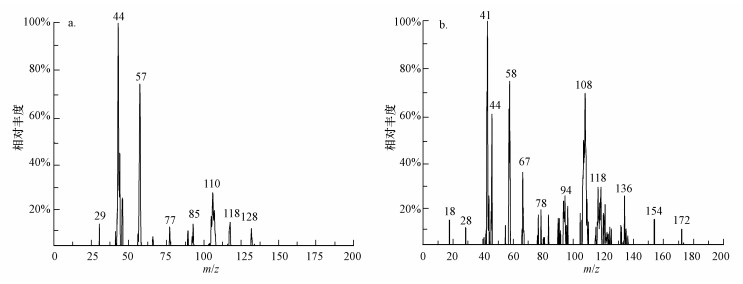 |
| 图 8 无氨(a)和有氨(b)存在时100个甲苯SOA粒子的平均正离子质谱图 Fig. 8 The positive mass spectra out of 100 raw spectra of toluene SOA particles in the absence (a) of and the presence (b) of ammonia |
利用自制的烟雾腔系统开展了NH3对甲苯SOA形成和化学组分影响的实验研究, 采用离线和在线仪器检测了甲苯SOA粒子的化学组分.UV-Vis、ATR-FTIR和ALTOFMS的测量结果综合表明, NH3能与甲苯SOA中的二醛组分发生非均相反应形成1H-咪唑、4-咪唑甲醛等咪唑类产物, 从而改变气体相/微粒相均分过程, 使更多的气相组分均分为微粒相, 让SOA粒子的粒径和质量浓度显著增大.SMPS表征结果显示, 光照60 min时, 有NH3条件下形成的SOA中心粒径和质量浓度比无NH3条件下分别增加了25%和50%.形成的咪唑类产物能够吸收270 nm的紫外光, 并具有较强的荧光特性, 是大气棕色碳的重要组成部分.然而, 参与反应的各组分浓度高于实际大气中的浓度, 后续应开展接近大气浓度的甲苯光氧化实验, 并考察光照强度、相对湿度、无机细粒子等环境因素对咪唑类产物形成的影响研究.
Alfarra M R, Paulsen D, Gysel M, et al. 2006. A mass spectrometric study of secondary organic aerosols formed from the photooxidation of anthropogenic and biogenic precursors in a reaction chamber[J]. Atmospheric Chemistry and Physics, 6(12): 5279–5293.
DOI:10.5194/acp-6-5279-2006
|
Andreae M O, Ramanathan V. 2013. Climate change.Climate's dark forcings[J]. Science, 6130(340): 280–281.
|
Bash J O, Cooter E J, Dennis R L, et al. 2013. Evaluation of a regional air-quality model with bidirectional NH3 exchange coupled to an agroecosystem model[J]. Biogeosciences, 10(3): 1635–1645.
DOI:10.5194/bg-10-1635-2013
|
Babar Z B, Park J H, Lim H J. 2017. Influence of NH3 on secondary organic aerosols from the ozonolysis and photooxidation of α-pinene in a flow reactor[J]. Atmospheric Environment, 164: 71–84.
DOI:10.1016/j.atmosenv.2017.05.034
|
Chen H H, Varner M E, Gerber R B, et al. 2016. Reactions of methanesulfonic acid with amines and ammonia as a source of new particles in air[J]. Journal of Physical Chemistry B, 120(8): 1526–1536.
DOI:10.1021/acs.jpcb.5b07433
|
陈文泰, 邵敏, 袁斌, 等. 2013. 大气中挥发性有机物(VOCs)对二次有机气溶胶(SOA)生成贡献的参数化估算[J]. 环境科学学报, 2013, 33(1): 163–172.
|
Carlton A G, Turpin B J, Altieri K E, et al. 2007. Atmospheric oxalic acid and SOA production from glyoxal:Results of aqueous photooxidation experiments[J]. Atmospheric Environment, 41(35): 7588–7602.
DOI:10.1016/j.atmosenv.2007.05.035
|
Flores J M, Washenfelder R A, Adler G, et al. 2014. Complex refractive indices in the near-ultraviolet spectral region of biogenic secondary organic aerosol aged with ammonia[J]. Physical Chemistry Chemical Physics, 16(22): 10629–10642.
DOI:10.1039/C4CP01009D
|
Gentner D R, Jathar S H, Gordon T D, et al. 2017. Review of urban secondary organic aerosol formation from gasoline and diesel motor vehicle emissions[J]. Environmental Science & Technology, 51(3): 1074–1093.
|
Huang M Q, Zhang J H, Cai S Y, et al. 2016. Characterization of particulate products for aging of ethylbenzene secondary organic aerosol in the presence of ammonium sulfate seed aerosol[J]. Journal of Environmental Sciences, 47(9): 219–229.
|
Huang M Q, Hao L Q, Cai S Y, et al. 2017. Effects of inorganic seed aerosols on the particulate products of aged 1, 3, 5-trimethylbenzene secondary organic aerosol[J]. Atmospheric Environment, 152: 490–502.
DOI:10.1016/j.atmosenv.2017.01.010
|
Huang M Q, Zhang W J, Wang Z Y, et al. 2011. Mass spectrometry study of OH-initiated photooxidation of toluene[J]. Chinese Journal of Chemical Physics, 24(6): 672–678.
DOI:10.1088/1674-0068/24/06/672-678
|
Jang M, Kamens R M. 2001. Characterization of secondary aerosol from the photooxidation of toluene in the presence of NOx and 1-propene[J]. Environmental Science & Technology, 35(18): 3626–3639.
|
Laskin A, Laskin J, Nizkorodov S A. 2015. Chemistry of atmospheric brown carbon[J]. Chemical Reviews, 115(10): 4335–82.
DOI:10.1021/cr5006167
|
Liu Y, Liggio J, Staebler R, et al. 2015. Reactive uptake of ammonia to secondary organic aerosols:kinetics of organonitrogen formation[J]. Atmospheric Chemistry and Physics, 15(23): 13569–13584.
DOI:10.5194/acp-15-13569-2015
|
Li L J, Tang P, Nakao S S, et al. 2016. Novel approach for evaluating secondary organic aerosol from aromatic hydrocarbons:unified method for predicting aerosol composition and formation[J]. Environmental Science & Technology, 50(12): 6249–6256.
|
刘宪云, 黄明强, 王振亚, 等. 2009. 用于模拟SOA形成的烟雾腔的构造和表征[J]. 环境科学与技术, 2009, 32(9): 105–109.
|
Lee A K, Zhao R, Li R, et al. 2013. Formation of light absorbing organo-nitrogen species from evaporation of droplets containing glyoxal and ammonium sulfate[J]. Environmental Science & Technology, 47(22): 12819–12826.
|
Maxut A, Nozière B, Fenet B, et al. 2015. Formation mechanism and yield of small imidazoles from reactions of glyoxal with NH4+ in water at neutral pH[J]. Physical Chemistry Chemical Physics, 17(31): 20416–20424.
DOI:10.1039/C5CP03113C
|
Na K, Song C, Cocker Ⅲ, et al. 2006. Formation of secondary organic aerosol from the reaction of styrene with ozone in the presence and absence of ammonia and water[J]. Atmospheric Environment, 40(10): 1889–1900.
DOI:10.1016/j.atmosenv.2005.10.063
|
Na K, Song C, Switzer C, et al. 2007. Effect of ammonia on secondary organic aerosol formation from a-Pinene ozonolysis in dry and humid conditions[J]. Environmental Science & Technology, 41(17): 6096–6102.
|
Sharma S K, Kumar M, Rohtash, et al. 2014. Characteristics of ambient ammonia over Delhi, India[J]. Meteorology and Atmospheric Physics, 124(1/2): 67–82.
|
Sun K, Tao L, Miller D J, et al. 2017. Vehicle emissions as an important urban ammonia source in the united states and China[J]. Environmental Science & Technology, 51(4): 2472–2481.
|
Schiferl L D, Heald C L, Nowak J B, et al. 2014. An investigation of ammonia and inorganic particulate matter in California during the CalNex campaign[J]. Journal of Geophysical.Research:Atmospheres, 119(4): 1883–1902.
DOI:10.1002/2013JD020765
|
Sato K, Takami A, Kato Y, et al. 2012. AMS and LC/MS analyses of SOA from the photooxidation of benzene and 1, 3, 5-trimethylbenzene in the presence of NOx:effects of chemical structure on SOA aging[J]. Atmospheric Chemistry and Physics, 12(10): 4667–4682.
DOI:10.5194/acp-12-4667-2012
|
Teich M, Van P D, Kecorius S, et al. 2016. First quantification of imidazoles in ambient aerosol particles:potential photosensitizers, brown carbon constituents, and hazardous components[J]. Environmental Science & Technology, 50(3): 1166–1173.
|
Updyke K M, Nguyen T B, Nizkorodov S A. 2012. Formation of brown carbon via reactions of ammonia with secondary organic aerosols from biogenic and anthropogenic precursors[J]. Atmospheric Environment, 63: 22–31.
DOI:10.1016/j.atmosenv.2012.09.012
|
谢绍东, 田晓雪. 2010. 挥发性和半挥发性有机物向二次有机气溶胶转化的机制[J]. 化学进展, 2010, 22(4): 727–733.
|
Zhu L, Henze D, Bash J, et al. 2015. Global evaluation of ammonia bidirectional exchange and livestock diurnal variation schemes[J]. Atmospheric Chemistry and Physics, 15(22): 12823–12843.
DOI:10.5194/acp-15-12823-2015
|
张宇飞, 朱燕群, 王树荣, 等. 2015. 甲苯的光氧化降解试验研究[J]. 环境科学学报, 2015, 35(9): 2759–2765.
|
 2018, Vol. 38
2018, Vol. 38


