溶解性有机质(DOM)是一类结构复杂且具有交互作用的有机混合物, 在水体中存在时间长, 且时刻处于变化之中, 并与水体中的污染物之间存在耦和作用, 对水体中污染物的转化和去除具有十分重要的作用(何伟等, 2016), 其主要作用机制分为参与微生物降解过程和光降解过程.在厌氧环境水体中, DOM可以作为微生物和污染物之间的电子穿梭体, 参与到微生物对污染物的降解过程中(Yu et al., 2016).研究表明, DOM作用下可以促进微生物还原三价砷(陈铮, 2016), 以及介导微生物降解类固醇雌激素(Gu et al., 2016)等.自然环境中DOM的光降解过程分为直接光降解和间接光降解两种, 其均可使DOM的分子量减少(刘婷婷, 2015)、氧化性提高.光降解主要存在过程为:①DOM会吸收部分入射光的光能造成能键的断裂, 然后降解成分子量较小的物质;②光照会产生活性中间物质, 这些活性物质会与DOM反应, 导致DOM的分解.由于光照下DOM产生自由基等原因, 因此, 可在一定程度上影响水体污染物的光降解.例如, 水中腐殖酸会抑制萘普生(NPX)的光解, 富里酸会促进低浓度萘普生的光解(吴波, 2014);DOM存在条件下会抑制甲硝唑的光降解(杨兰兰等, 2016).
水环境中的内分泌干扰物(EDCs)主要分为两类, 一类是环境浓度低, 但雌激素效应强的雌激素, 如17β-雌二醇(E2)和17α-乙炔基雌二醇(EE2);另一类是环境浓度高, 但雌激素效应弱的雌激素, 如壬基酚(NP)和双酚A(BPA)(Li et al., 2013).EE2由天然雌激素E2衍生合成(Aris et al., 2014), 具有强烈的雌激素效应, 对生物的生存发展造成了严重的威胁, 不仅会对生物的生殖造成影响, 还会影响下一代的生长发育.近几年来, 世界范围内的EE2消费量不断提高, 其自身的存在持久性特点使得污水处理厂不能完全将其去除(Ma et al., 2017).目前, EE2在全球环境中的浓度级别为ng·L-1, 我国也已将其列为最重要的有机污染物之一(杨烨, 2015).
自然水体DOM在光照和微生物存在条件下, 理化性质会发生一定程度的改变.经过改性后的DOM参与到水中EE2的光降解和微生物降解去除反应时, 所起到的介导作用会发生变化.为了探究经过微生物和光改性前后的DOM对EE2降解的介导作用差异, 了解自然界中存在的EE2去除过程和变化.本文选取从洱海沉积物中提取出来的两种DOM代表物质—胡敏酸(HA)和富里酸(FA), 分别经过光改性和微生物改性后, 加入到EE2的微生物降解和光降解体系中, 采用紫外-可见光谱技术、三维荧光光谱等技术对改性前后的DOM进行对比分析, 并研究改性前后DOM对EE2降解的影响, 以期揭示自然界中DOM成分的自然变化对类固醇类雌激素降解效果的影响机制.
2 材料与方法(Materials and methods) 2.1 试剂与仪器试剂:希瓦氏菌购于北京工业微生物菌种保藏管理中心(CICC);EE2(纯度>98%)标准品购于美国Sigma公司;HA和FA按照国际腐殖酸协会提供的标准方法从洱海沉积物中提取所得, 具体的元素分析详见之前的研究(He et al., 2016);FeCl3、邻二氮菲、醋酸钠等.
无机盐培养基(g·L-1):NaCl 1.00、NH4Cl 0.80、KH2PO4 0.50、K2HPO4 0.60、MgCl2·6H2O 0.20、CaCl2·2H2O 0.05、酵母提取物0.01.
仪器:紫外可见分光光度计(UV-2600);荧光分光光度计(RF-5301PC);高效液相色谱(Agilent Technologies, 1260);总有机碳检测仪(Elementar);高压蒸汽灭菌锅.
2.2 DOM改性过程 2.2.1 微生物改性DOM在500 mL锥形瓶中加入提取的DOM(HA或FA)、希瓦氏菌及无机盐培养基, 配制成含有100.0 mg·L-1 (以C计, 下同)DOM和1.0 g·L-1希瓦氏菌的250 mL培养液, 向溶液中通入氮气15 min, 在30 ℃、160 r·min-1摇床中避光培养72 h.经过微生物改性后DOM过0.2 μm滤膜去除微生物, 放入4 ℃冰箱中保存, 以备后续实验使用.
2.2.2 光改性DOM配置溶剂分别为超纯水和无机盐培养基的20 mg·L-1 DOM培养液, 于121 ℃条件下在高压蒸汽灭菌锅中灭菌20 min, 灭菌后分别取40 mL于50 mL石英管中并曝氮气15 min, 封口后置于光反应器中, 于>290 nm波长的300 W氙灯下模拟自然光光照48 h.Ren等(2016)研究表明, 经过50 h光照后的DOM对EE2微生物和光降解的介导作用趋于稳定, 故本试验选择光照48 h.将改性后的DOM置入4 ℃冰箱中保存, 以备后续实验使用.
2.3 实验方法 2.3.1 光改性前后DOM介导EE2微生物降解在500 mL锥形瓶中加入光改性前后的DOM(HA或FA), 于121 ℃条件下在高压蒸汽灭菌锅中灭菌20 min, 配制成含有20 mg·L -1 DOM和1 g·L -1希瓦氏菌的250 mL培养液, 向溶液中通入氮气15 min.在30 ℃、160 r·min-1摇床中避光振荡培养72 h, 取样间隔为12 h.样品经16000 r·min-1、4 ℃离心10 min, 取上清液, 用HPLC测溶液剩余EE2浓度.
2.3.2 微生物改性DOM介导EE2光降解在50 mL石英管中加入40 mL含有20 mg·L -1微生物改性前后的DOM溶液, 溶剂分别为超纯水和无机盐培养基, 置于光反应器中, 于>290 nm波长下模拟自然光进行光照20 h, 光照过程同时通入氮气, 以保持反应过程的缺氧条件.取样后经HPLC测溶液剩余EE2的浓度.
2.4 分析方法 2.4.1 DOM理化特性表征三维荧光分析:将改性前后的DOM用超纯水稀释至20 mg·L-1, 并将其pH调至7.0, 荧光分光光度计(RF-5301PC)设定激发波长(λEx)范围为200~600 nm, 发射波长(λEm)范围为280~600 nm, 波长扫描间隔为5 nm, 扫描速度为1200 nm·min -1.
UV-Vis分析:将改性前后的DOM用超纯水稀释至20 mg·L -1, 并将其pH调至7.0, 于UV-2600紫外可见分光光度计测定吸收特征光谱, 扫描范围200~700 nm, 扫描间距为0.50 nm.
电子供给能力:在500 mL锥形瓶中配制250 mL含有20 mg·L -1(以C计) HA或FA的无机盐培养基, 希瓦氏菌浓度为1 g·L -1, 甲酸钠作为碳源, 浓度为5 mmol·L -1.向溶液中通入氮气15 min, 在30 ℃、160 r·min-1摇床中培养24 h后, 在厌氧培养箱中过0.2 μm滤膜去除微生物, 按照国标测定二价铁方法, 加入50 μmol·L -1 FeCl3反应15 min, 测得最终二价铁浓度.
2.4.2 EE2定量分析降解过程中EE2的浓度用Agilent Technologies 1260高效液相色谱进行定量.测定条件:Waters C18反相柱(4.6 mm×250 mm, 5 μm), 荧光检测器(λEx/λEm=283 nm /346 nm), 进样量50 μL, 流动相为40%超纯水和60%的乙腈(含0.1%三氟乙酸), 流速为1 mL·min -1.
2.5 数据处理与统计本文中所有误差为3次平行取样的标准偏差.光降解数据选取一级反应动力学模型处理, 即:
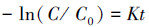
|
(1) |
式中, C0为EE2初始浓度(mg·L-1), C为t时EE2的浓度(mg·L-1), t为降解反应时间(min), K为反应速率常数(min-1).
3 结果与讨论(Results and discussion) 3.1 DOM改性结果表征 3.1.1 DOM改性前后紫外全波长扫描HA和FA的紫外吸收光谱均随着波长的增加呈指数下降, 在虚线处有较强的吸收特征峰, 该图谱与文献中(Mignone et al., 2012)已经报道的DOM紫外吸收图谱一致.由图 1可以看出, 同一波长下吸光度大小顺序均为:无机盐培养基中光改性>水中光改性>未改性前>微生物改性, 说明微生物改性和光改性前后HA和FA均发生了一定的变化.吸光度的产生主要与分子间羟基芳香电子供体基团与醌电子受体的直接电子转移有关, HA的吸光度比FA的吸光度高, 该结果也与DOM光改性后的电子供给能力结果相符.
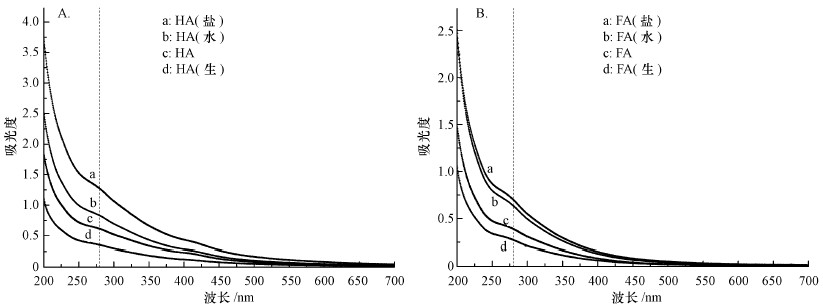 |
| 图 1 10 mg·L -1 DOM改性前后紫外吸收光谱(A.HA改性前后, B.FA改性前后;水-水溶剂中进行光改性;盐-无机盐溶剂中进行光改性;生-微生物改性;HA/FA -未改性HA/FA) Fig. 1 UV-Vis spectroscopy of 10 mg·L -1 DOM before and after modification |
SUV254代表 254 nm下的特定紫外吸光值, 其值是通过将在λ= 254 nm处测量的UV吸光度除以DOC浓度来确定的(Weishaar et al., 2003).SUV254值的大小代表着DOM样品的亲疏水性, 低SUV254值(<3)与亲水特性相关(Li et al., 2016).A280代表 280 nm下的吸光度, SUVA254、A280与DOM的芳香性成正比(Zhang et al., 2009; Nurmi et al., 2002).
改性前后DOM紫外分析结果见表 1.由表 1可以看出, 光改性DOM的芳香性要比微生物改性好;而溶剂为无机盐培养基时的光改性DOM的芳香性比溶剂为纯水时的芳香性好.经过微生物改性后, DOM芳香性降低, 这可能与微生物生命活动相关, 微生物会将大分子物质分解为小分子物质.这一结果也和E4/E6相对应, E4/E6表示DOM在紫外波长472 nm和664 nm下吸光度的比值(Wei et al., 2015), 与DOM的腐殖化程度成反比, 而经过微生物改性后, E4/E6的值相较原本值降低, 因此, 腐殖化程度升高.
| 表 1 DOM改性前后紫外组分分析 Table 1 UV-Vis spectrometric analysis of the component before and after DOM modification |
E2/E3表示DOM在紫外波长250 nm和365 nm下吸光度的比值, 可用来表征腐殖酸的腐殖化程度, 也可以用来指示有机物的来源.当E2/E3<3.5时, 主要成分是胡敏酸;E2/E3>3.5时, 主要成分是富里酸(钱锋等, 2016).微生物改性后DOM的E2/E3值有一定程度的提高, 即微生物改性过程使得DOM的腐殖化程度变高.光改性后DOM的E2/E3值提高代表着经过光改性后, DOM的可见区吸收结构更容易进行光氧化反应(刘雪石等, 2017).
经过微生物改性后, HA的TOC值变化很小, 这主要是因为HA相比FA是大分子物质, 可以被微生物利用的有机碳源很少, 因此, TOC值变化微小.光改性过程中, DOM中的有机碳发生矿化反应, 故TOC值减少.
色调系数值Δlgk是DOM在波长400 nm和600 nm吸光度对数的差值(王鑫等, 2014), 与不饱和程度成正比, 与氧化程度成反比.经过微生物改性后的DOM, Δlgk值减小, 也就是微生物改性后的DOM氧化程度增加, 而不饱和度降低.光改性后DOM的Δlgk值有一定程度的减小.光和微生物改性之后DOM的pH从中性变为弱酸性, 可能跟DOM自身变化产生了一些小分子有机酸有关.
3.1.2 DOM改性前后荧光对比发色DOM能够吸收光, 主要是因为共轭双键的存在, 当这些共轭双键环化后再吸收光, 一部分吸收的光会发射出荧光.天然环境中类腐殖酸荧光λEx/λEm=350~440 nm/430~510 nm, 类富里酸荧光λEx/λEm=310~360 nm/370~450 nm或λEx/λEm=240~270 nm/370~440 nm(傅平青等, 2004).如图 2所示, 经过不同处理HA和FA的三维荧光光谱图均发生了一定的变化, 对照组HA的λEx/λEm=360.0/494.0 nm, FA的λEx/λEm=270.0/460.0 nm.经过微生物改性后, HA的λEx/λEm=280.0 nm/470.0 nm, FA的λEx/λEm=270.0 nm/450.0 nm.溶剂为水时光改性后, HA的λEx/λEm=360.0 nm /492.0 nm和450.0 nm/530.0 nm, FA的λEx/λEm=270.0 nm/460.0 nm.溶剂为无机盐光改性后, HA的λEx/λEm= 370.0 nm/500.0 nm和440.0 nm/520.0 nm, FA的λEx/λEm=270.0 nm/458.0 nm和330.0 nm /452.0 nm.可以发现, 无论是HA还是FA, 经过光改性后均发生了λEx/λEm峰的红移现象, 而经过微生物改性后发生了λEx/λEm峰的蓝移.溶解性有机质的荧光可见吸收和发射特征来自于主链中的电子转移, 分子间电荷转移的增强会导致吸收和发射波长的红移(Mignone et al., 2012).HA相比FA分子量大, 共轭结构复杂, 腐殖化程度更高, 因此, 吸收光谱更加容易向长波方向发生红移(高洁等, 2015).
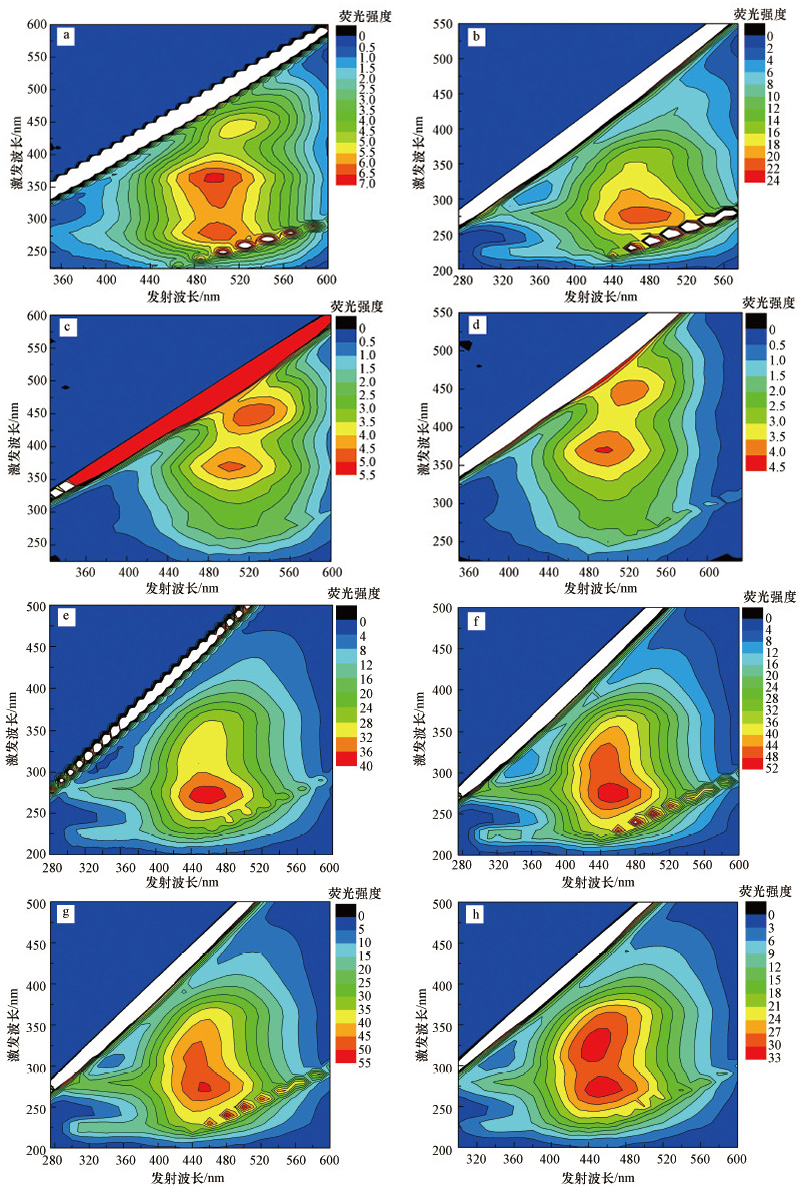 |
| 图 2 改性前后腐殖酸三维荧光图谱(a.改性前HA, b.微生物改性HA, c.去离子水光改性HA, d.无机盐培养基光改性HA, e.改性前FA, f.微生物改性FA, g.去离子水光改性FA, h.无机盐培养基光改性FA) Fig. 2 Three-dimensional fluorescence spectra of DOM before and after modification |
HA和FA改性前后荧光强度排序为:微生物改性>未改性>去离子水光改性>无机盐培养基光改性.光降解会引起类腐殖酸物质吸光度和荧光的减小, 而微生物降解会引起类腐殖酸物质吸光度和荧光的增加, 但会降低类蛋白物质的荧光.还原性醌基相较于氧化性醌基会增加荧光强度(Cory et al., 2005), 因此, 经过微生物改性后的DOM的荧光强度会比改性前强, 主要是在厌氧条件下, 微生物会产生电子将醌基还原导致.
3.1.3 DOM光改性前后电子供给能力变化三价金属离子, 尤其可溶性的常作为电子受体用来检测体系中的电子穿梭能力(Li et al., 2013), 因此, 本文中选择FeCl3作为电子受体.微生物对铁的还原能力随着醌基数量的增多而变强(陈铮, 2016), 在含有DOM的微生物氧化甲酸钠体系中加入Fe3+后, 会促使Fe3+还原产生Fe2+, 并可以通过Fe2+产量表征DOM的电子供给能力.图 3为光改性前后DOM的电子供给能力, 可以看出, 经过光改性后DOM的电子供给能力变弱, 溶剂为水时的光改性DOM的电子供给能力好于溶剂为无机盐时的光改性DOM, 并且HA的电子供给能力好于FA, 这也对应了荧光图谱分析中λEx/λEm峰的红移结果, 是由于电子转移的变化导致了荧光吸收和发射特征的变化.
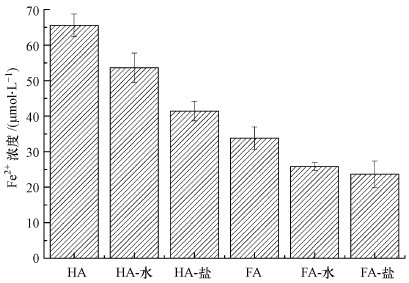 |
| 图 3 光改性前后DOM的电子供给能力 Fig. 3 Electron donating capacity of DOM before and after photo-modification |
采用在水和无机盐培养基两种溶剂中光改性的DOM与未经改性的DOM一同进行EE2的微生物降解实验, 结果如图 4所示.从图中可以看出, 微生物降解过程中HA介导下的EE2降解效果要明显好于FA介导下的效果, 并且未经光改性的DOM介导EE2微生物降解效果要好于光改性后的DOM.这可能是由于光照过程中DOM吸收能量, 键发生断裂, 并产生了一系列的自由基(Ren et al., 2017), 使得DOM性质发生一定程度的改变, DOM介导微生物降解EE2过程主要利用了DOM的电子穿梭体能力, 即通过DOM醌呼吸作用完成电子转移过程, 促使微生物完成对污染物的降解过程(陈蕾等, 2013).因此, 从DOM光改性后的电子供给能力分析结果可以看出, 光改性过程使得DOM的电子供给能力变弱, 并且无机盐溶剂中进行光改性的DOM电子供给能力弱于水溶剂中进行光改性的DOM.电子供给能力的变化在一定程度上影响了DOM介导微生物降解污染物过程, 因此, 光改性前后DOM电子供给能力结果与其介导微生物降解EE2结果相一致.
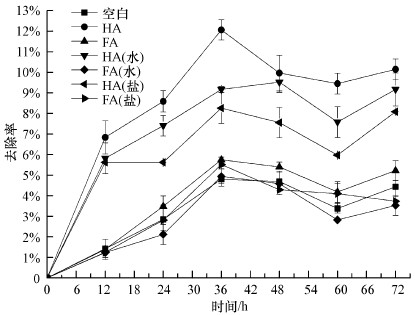 |
| 图 4 光改性DOM介导EE2微生物降解 Fig. 4 Biodegradation of EE2 mediated by photo-modified DOM |
经过微生物改性DOM与未经改性DOM一同介导EE2的光降解, 降解过程分别在水和无机盐培养基两种溶剂中进行, 结果如图 5所示.从图中可以看, 经过微生物改性后的DOM介导EE2的光解效果要好于未经改性的DOM和空白.有文献中提到微生物改性过程会使得腐殖酸的极性减小, 腐殖性增加, 同时其与污染物的结合能力也会增加(顾丽鹏等, 2016), 与本实验中由紫外组分分析得出的结果基本一致, 经过微生物改性后的DOM腐殖化程度增加, 芳香性减小, 氧化程度增加, 不饱和度降低.由此可以推断出微生物改性后DOM与EE2的结合能力变高并且芳香性减小, DOM光照是一个芳香性增加的过程, 因此, 较低芳香性的DOM在光照条件下可能更利于介导污染物降解的发生.HA介导EE2光降解效果要好于FA, 从之前的分析可以看出, 实验用HA的腐殖化程度要好于FA的腐殖化程度, 并且在无机盐溶剂中进行的EE2光降解效果要好于在水溶剂中, 这可能与不同溶剂中的DOM分子结构不同有关.
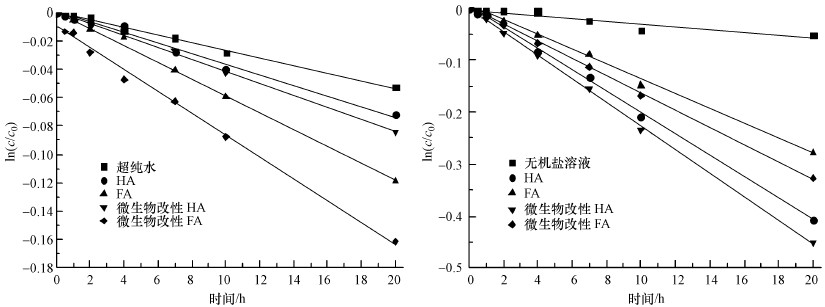 |
| 图 5 微生物改性DOM介导EE2光降解(a.水溶剂系列光照, b.无机盐溶剂系列光照) Fig. 5 Photodegradation of EE2 mediated by bio-modified DOM |
1) 通过紫外-可见全波长扫描和三维荧光分析可以得出, 光和微生物改性前后的DOM均发生了一定程度的变化, HA的紫外-可见吸收强度和荧光强度都要大于FA, 并且经过微生物改性的DOM荧光强度有所提高.紫外吸光度的产生主要与分子间羟基芳香电子供体基团与醌电子受体的直接电子转移有关, 在一定程度上DOM的紫外吸光强度与电子供给能力呈相关关系.紫外-可见组分分析可以得出, 光改性DOM的芳香性要比微生物改性好, 经过微生物改性后, DOM芳香性降低, 腐殖化程度升高.经过光改性后, DOM芳香性升高.
2) 经过微生物改性后的HA和FA与EE2的结合能力变强并且芳香性减小, HA和FA光照是一个芳香性增加的过程, 因此, 较低芳香性的DOM在光照条件下会更利于介导污染物降解的发生, 故微生物改性后HA和FA会促进EE2的光降解.微生物改性后HA介导下的EE2光降解效果要明显好于FA介导下的光降解效果.
3) 光照过程中HA和FA吸收能量, 键发生断裂, 并产生了一系列的自由基, 使得HA和FA性质发生一定程度的改变, HA和FA介导微生物降解EE2过程主要利用了HA和FA的电子穿梭体能力, 光改性过程使得HA和FA的电子供给能力变弱, 电子供给能力的变化在一定程度上影响了HA和FA介导微生物降解污染物过程, 使得光改性后HA和FA会抑制EE2的微生物降解.光改性后HA介导下的EE2微生物降解效果要好于FA介导下的降解效果.
4) 自然水体中污染物降解过程离不开光降解和微生物降解两种作用过程, DOM作为水体中普遍存在的物质, 其分别经过光和微生物的作用影响之后, 对污染物降解的影响也不同, 通过本实验可以说明, 在自然水体中相比光改性过程, 微生物改性过程对DOM介导EE2降解的影响要更好一些.
Aris A Z, Shamsuddin A S, Praveena S M. 2014. Occurrence of 17α-ethynylestradiol (EE2) in the environment and effect on exposed biota:a review[J]. Environment International, 69: 104–109.
DOI:10.1016/j.envint.2014.04.011
|
陈蕾, 超峰, 王郑, 等. 2013. 天然有机质对环境污染物的转化过程的介导作用[J]. 生态环境学报, 2013(7): 1244–1249.
DOI:10.3969/j.issn.1674-5906.2013.07.026 |
陈铮. 2016. 电子中介体介导高砷尾矿沉积物中砷/铁形态转化的微生物作用机制研究[D]. 厦门: 厦门大学. 30-31;33
|
Cory R M, McKnight D M. 2005. Fluorescence spectroscopy reveals ubiquitous presence of oxidized and reduced quinones in dissolved organic matter[J]. Environmental Science and Technology, 39(21): 8142–8149.
DOI:10.1021/es0506962
|
傅平青, 刘丛强, 尹祚莹, 等. 2004. 腐殖酸三维荧光光谱特性研究[J]. 地球化学, 2004, 33(3): 301–308.
DOI:10.3321/j.issn:0379-1726.2004.03.010 |
高洁, 江韬, 李璐璐, 等. 2015. 三峡库区消落带土壤中溶解性有机质(DOM)吸收及荧光光谱特征[J]. 环境科学, 2015, 36(1): 151–162.
DOI:10.3969/j.issn.1673-288X.2015.01.042 |
顾丽鹏, 何欢, 胥志祥, 等. 2016. 可溶性有机质生物改性介导17β-雌二醇生物降解作用[J]. 中国环境科学, 2016, 36(2): 468–475.
DOI:10.3969/j.issn.1000-6923.2016.02.024 |
Gu L, Huang B, Xu Z, et al. 2016. Dissolved organic matter as a terminal electron acceptor in the microbial oxidation of steroid estrogen[J]. Environmental Pollution, 218: 26–33.
DOI:10.1016/j.envpol.2016.08.028
|
何伟, 白泽琳, 李一龙, 等. 2016. 溶解性有机质特性分析与来源解析的研究进展[J]. 环境科学学报, 2016, 36(2): 359–372.
|
He H, Huang B, Gu L, et al. 2016. Stimulated dissolved organic matter by electrochemical route to produce activity substances for removing of 17 α-ethinylestradiol[J]. Journal of Electroanalytical Chemistry, 780: 233–240.
DOI:10.1016/j.jelechem.2016.09.033
|
刘婷婷. 2015. DOM的光降解及其对典型污染物环境行为的影响[D]. 长春: 吉林大学. 35-36
http://cdmd.cnki.com.cn/Article/CDMD-10183-1015597966.htm |
刘雪石, 乔显亮, 刘远. 2017. DOM的光化学活性及其对污染物光解的影响[J]. 环境科学与技术, 2017(1): 85–94.
|
Li J, Jiang L, Liu X, et al. 2013. Adsorption and aerobic biodegradation of four selected endocrine disrupting chemicals in soil-water system[J]. International Biodeterioration and Biodegradation, 76(1): 3–7.
|
Li X, Liu L, Liu T, et al. 2013. Electron transfer capacity dependence of quinone-mediated Fe(Ⅲ) reduction and current generation by Klebsiella pneumoniae L17[J]. Chemosphere, 92(2): 218–224.
DOI:10.1016/j.chemosphere.2013.01.098
|
Li Y, Harir M, Lucio M, et al. 2016. Comprehensive structure-selective characterization of dissolved organic matter by reducing molecular complexity and increasing analytical dimensions[J]. Water Research, 106: 477–487.
DOI:10.1016/j.watres.2016.10.034
|
Ma W, Sun J, Li Y, et al. 2018. 17α-Ethynylestradiol biodegradation in different river-based groundwater recharge modes with reclaimed water and degradation-associated community structure of bacteria and archaea[J]. Journal of Environmental Sciences, 64: 51–64.
DOI:10.1016/j.jes.2016.11.022
|
Mignone R A, Martin M V, Morán Vieyra F E, et al. 2012. Modulation of optical properties of dissolved humic substances by their molecular complexity[J]. Photochemistry and Photobiology, 88(4): 792–800.
DOI:10.1111/j.1751-1097.2012.01135.x
|
Nurmi J T, Tratnyek P G. 2002. Electrochemical properties of natural organic matter (NOM), fractions of NOM, and model biogeochemical electron shuttles[J]. Environmental Science and Technology, 36(4): 617–624.
DOI:10.1021/es0110731
|
钱锋, 吴婕赟, 于会彬, 等. 2016. 多元数理统计法研究太子河本溪城市段水体DOM紫外光谱特征[J]. 环境科学, 2016, 37(10): 3806–3812.
|
Ren D, Huang B, Yang B, et al. 2017. Photobleaching alters the photochemical and biological reactivity of humic acid towards 17α-ethynylestradiol[J]. Environmental Pollution, 220: 1386–1393.
DOI:10.1016/j.envpol.2016.10.096
|
Ren D, Huang B, Xiong D, et al. 2017. Photodegradation of 17α-ethynylestradiol in dissolved humic substances solution:Kinetics, mechanism and estrogenicity variation[J]. Journal of Environmental Sciences, 54: 196–205.
DOI:10.1016/j.jes.2016.03.002
|
王鑫, 王金成, 刘建新. 2014. 不同恢复阶段人工沙棘林土壤腐殖质组成及性质[J]. 水土保持通报, 2014, 34(5): 49–54.
|
吴波. 2014. 萘普生在水中光降解研究[D]. 武汉: 华中科技大学. 23-25
http://cdmd.cnki.com.cn/Article/CDMD-10487-1015014562.htm |
Weishaar J L, Aiken G R, Bergamaschi B A, et al. 2003. Evaluation of specific ultraviolet absorbance as an indicator of the chemical composition and reactivity of dissolved organic carbon[J]. Environmental Science and Technology, 37(20): 4702–4708.
DOI:10.1021/es030360x
|
Wei Z, Chenchen L I, Zhao Y, et al. 2015. Research on characteristics of UV-Vis absorbance of DOM in municipal solider waste with inoculation agent[J]. Journal of Northeast Agricultural University, 46(2): 83–88.
|
杨兰兰, 魏群山, 李宗宸, 等. 2016. 溶解性有机质DOM对甲硝唑光降解的影响研究[J]. 广东化工, 2016, 43(14): 13–15.
DOI:10.3969/j.issn.1007-1865.2016.14.006 |
杨烨. 2015. 石墨烯基二氧化钛复合光催化剂的制备及其对水中17α-乙炔基雌二醇的去除研究[D]. 昆明: 昆明理工大学. 3-4
http://cdmd.cnki.com.cn/Article/CDMD-10674-1015635795.htm |
Yu Z G, Orsetti S, Haderlein S B, et al. 2016. Electron transfer between sulfide and humic acid:electrochemical evaluation of the reactivity of sigma-aldrich humic acid toward sulfide[J]. Aquatic Geochemistry, 22(2): 117–130.
DOI:10.1007/s10498-015-9280-0
|
Zhang H, Weber E J. 2009. Elucidating the role of electron shuttles in reductive transformations in anaerobic sediments[J]. Environmental Science and Technology, 43(4): 1042–1048.
DOI:10.1021/es8017072
|
 2018, Vol. 38
2018, Vol. 38


