印染污泥是印染废水经处理后的二次产物, 成分复杂, 包含重金属、染料、助剂等, 是各种污染物的最终富集体(Khandegar et al., 2013), 其中多环芳烃(PAHs)是典型的特征污染物(Ning et al., 2014).据2016年中国环境统计年鉴数据, 中国印染废水排放量为18.42×108 t, 据此计算印染污泥的年产量为2.76×106 m3(含水率80%), 处工业污泥之首.然而, 现有的处理技术很难将印染污泥做到无害化处理, 并且当前的处理成本高, 处理能力严重不足, 导致印染污泥长期以来处于无序处置的状态(吴浩亮等, 2015).印染污泥进入环境后其中的污染物会对生态环境造成风险, 国内外的研究侧重于印染污泥的干化脱水(Ning et al., 2015;Feng et al., 2017)、混烧热解(Xie et al., 2018;Zhang et al., 2017)、成分分析(Liang et al., 2013)与有机物降解(Man et al., 2018;Liang et al., 2016)等, 而有关印染污泥对环境的生态毒性研究少见报道.
蚯蚓在土壤中的生物量大, 在地球物质循环和陆地生态系统食物链的物质传递中担负着重要功能(Blouin et al., 2013), 是最易受到环境有毒有害物质伤害的土壤生物之一, 因而也成为开展土壤污染生态风险评价的重要指示生物(颜增光等, 2007).蚯蚓毒理实验标准成熟可靠, 已广泛应用于各种土壤污染的评价和监测(Shi et al., 2017; Velki et al., 2017).
本研究选取珠三角地区广州、中山、东莞4家典型的印染废水处理厂, 以印染废水经处理后产生的印染污泥为研究对象, 首先采用化学方法评价印染污泥中PAHs的生态风险, 进一步以蚯蚓作为受试生物, 研究印染污泥对蚯蚓个体水平的急性毒性、亚细胞水平的生物标志物毒性和对蚯蚓的行为回避影响, 并对印染污泥对蚯蚓产生毒性的原因进行分析, 以期获得印染污泥潜在的生态环境风险信息, 为印染污泥的安全处理处置提供科学依据和实践指导.
2 材料与方法(Materials and methods) 2.1 主要仪器与试剂仪器:冷冻干燥机(LGJ-10C北京四环);马弗炉(KQH-60东莞科昶);气相色谱-质谱联用仪(7890B GC-5977B MS);pH计(pHS-3C雷磁);超纯水设备(Mil-Q法国Milipore);显微镜(CSW-52科视威);离心机(H1850R湘仪);生化培养箱(250B金坛新航);恒温振荡器(JBZL-08金坛晶玻).
试剂:苔藓泥炭土(德国Base Substrate 413);高岭土、碳酸钙(AR天津市大茂化学试剂厂);二氧化硅、二甲基亚砜、氯化钠、EDTA、中性红、Guaifenesin(AR阿拉丁);硫酸亚铁(AR麦克林);30%过氧化氢, 硫酸(AR广州化学试剂厂);甲醇、丙酮、二氯甲烷和正己烷(GC阿拉丁);16种PAHs混标(GC安谱).
2.2 供试污泥和蚯蚓人工土壤采用OECD的方法:10%泥炭土, 20%高岭土, 70%石英砂(50~200 μm粒径的细砂质量分数大于50%), 用碳酸钙调节pH为6.5±0.5;印染污泥采自广州、中山、东莞4家印染厂的污水处理厂, 分别记为TDS1、TDS2、TDS3、TDS4;用于毒性试验的污泥室外风干后磨细, 用于有机物分析的污泥冷冻干燥处理, 处理后的污泥置于4 ℃的冰箱中保存.
蚯蚓:赤子爱胜蚓(Eisenia fetida)购自广州蚌湖蚯蚓养殖厂, 在实验室用牛粪作为饲养基质, 于室温下长期培养.试验时选取体重0.3~0.5 g, 生殖环带明显的性成熟蚯蚓.
2.3 试验方法 2.3.1 印染污泥基本性质的分析方法印染污泥的最大持水率按ISO的标准测定;有机质的测定依据《HJ 761-2015固体废物有机质的测定灼烧减量法》, 含量视为烘干样在(600±20) ℃灼烧的失重量;依据《HJ 557-2010固体废物浸出毒性浸出方法水平振荡法》, 按液固比10:1制取浸出液测定总有机碳(TOC)并测定浸出液pH;用气相色谱-质谱联用仪(GC-MS)测定印染污泥中美国环保局(EPA)优先控制的16种PAHs总量, 分别为:萘、苊烯、苊、菲、蒽、荧蒽、芘苯并(a)蒽、、苯并(b)荧蒽、苯并(k)荧蒽、苯并(a)芘、茚(1, 2, 3-cd)并芘、二苯并(a, h)蒽、苯并(g, h, i)芘、印染污泥的基本性质见表 1.
| 表 1 印染污泥的基本信息 Table 1 Basic information of the TDS |
测定印染污泥中PAHs含量的样品制备:污泥冷冻干燥后, 用超声萃取法对污泥进行前处理, 具体步骤如下:称取1 g污泥和1 g无水硫酸钠置于100 mL带磨口锥形瓶中, 再加入20 mL体积比为1:1的正己烷与丙酮混合溶剂, 密封;在功率为400 W, 频率为40 kHz的超声清洗机中超声5 min, 倒入离心管在4000 r·min-1下离心5 min, 保留上清液于500 mL圆底烧瓶中, 污泥等几分钟后转入锥形瓶中, 重复共3次
GC-MS分析条件:进样口温度290 ℃, 载气为高纯氦气, 载气流速为54 mL·min-1, 1 μL无分流进样.GC-MS升温程序:初始温度80 ℃, 保持1 min;以3 ℃·min-1的速度上升到161 ℃后以5 ℃·min-1的速度上升到220 ℃;最后以10 ℃·min-1的速度上升到310 ℃, 保留5 min.
质量保证与质量控制(QA/QC):设置方法空白、加标空白和基质加标, 分析流程与实际样品相同, 回收率指示标准物质为芴-D10, 芘-D10, 在本试验中, 芴-D10的回收率为73%±9%, 芘-D10的回收率为93%±13%.
2.3.2 蚯蚓急性毒性试验急性毒性试验按照OECD方法进行.将人工土壤(最大持水率为86%)与印染污泥混合, 制得含印染污泥浓度从0~1000 g·kg-1(w/w, 干重)的混合污泥.将200 g(干重)混合污泥置于500 mL玻璃烧杯中, 用去离子水根据人工土壤与相应印染污泥的组成比例将各组分的含水率调整为对应组分最大持水率的60%.选取已在人工土壤中驯化24 h的蚯蚓10条放入污泥表面, 任其自行钻探, 烧杯用纱布封口, 橡皮筋捆扎, 防止蚯蚓逃逸, 称重记录.将烧杯置于生化培养箱内培养, 设置温度(20±2) ℃, 湿度80%, 提供连续光照, 适时补充水分.整个试验期为14 d, 分别在第7 d和第14 d评估蚯蚓死亡率.每个处理设4个重复.
2.3.3 蚯蚓体腔细胞溶酶体中性红保留时间(NRRT)蚯蚓体腔细胞的提取和染色参考马静静(2015)的方法.蚯蚓清肠48 h后, 取3~5条放入盛有2 mL体腔细胞提取液的离心管中, 5 min后用镊子取出蚯蚓, 离心弃上清液, 沉淀细胞加入1 mL复方氯化钠溶液摇匀, 取10 μL蚯蚓体腔细胞液滴到载玻片上, 等待30 s让细胞吸附, 加10 μL中性红工作液, 盖上盖玻片, 于400倍显微镜下每2 min观察1次, 直至视野中超过50%的体腔细胞被染色, 记录NRRT.
2.3.4 蚯蚓回避行为试验蚯蚓回避试验能够很好地模拟印染污泥进入自然环境中后, 土壤中蚯蚓的行为反应, 测定蚯蚓对印染污泥的回避行为阈值.整个试验周期为48 h, 根据ISO标准选择六室行为观测仪, 观测仪由有机玻璃材料做成, 分为内圆筒与外圆筒, 中间平均分隔为6个区, 各区分隔板底部钻置3个直径1 cm半圆孔, 内圆筒区对应每个分区底部钻有2个直径1 cm半圆孔, 供蚯蚓选择进出, 结构见图 1.不同浓度的混合污泥随机放置于各分室中.取10条在人工土壤中驯化好的蚯蚓, 逐条释放于内圆筒区, 记录蚯蚓选择进入的浓度, 记为反应开始时刻(t0)蚯蚓的选择, 蚯蚓全部进入土壤后置于生化培养箱内培养48 h, 培养条件同蚯蚓急性毒性试验.检查结果时将各分室的污泥取出, 记录各浓度中蚯蚓的数量, 记为测试终点(t48)时刻蚯蚓的选择, 计算每一浓度中的蚯蚓数占总数的百分比, 每个处理设3个重复.
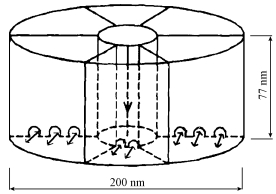 |
| 图 1 六室行为观测仪示意图 Fig. 1 Six-chamber test system for the avoidance response |
采用Excel和origin8.0进行数据分析与作图, 数据表示为平均数±标准偏差(AV±SD);印染污泥对蚯蚓的半数致死浓度(LC50)通过线性回归算法求出.
3 结果与分析(Results and analysis) 3.1 印染污泥中PAHs的含量采用风险评价低值(effects range-low, ERL, 生物有害效应概率小于10%, ∑16PAHs ERL为4022 ng·g-1)、风险评价中值(effects range-median, ERM, 生物有害效应概率大于50%, ∑16PAHs ERM为44792 ng·g-1)(Long et al., 1995)和不设最低安全值, 只要在环境中存在就会对生物产生毒性作用的4种高环PAHs(苯并(b)荧蒽、苯并(k)荧蒽、茚(1, 2, 3-cd)并芘、苯并(g, h, i)芘, 记为∑4PAHs)3个指标对印染污泥中的PAHs进行生态风险评价(王靖宇等, 2015).如图 2所示, 4种印染污泥中∑16PAHs总量最高的是TDS3, 为(5465±283) ng·g-1, 其次是TDS4:(1264±89) ng·g-1, TDS1:(1199±145) ng·g-1和TDS2:(1005±51) ng·g-1.对比发现, 4种印染污泥的∑16PAHs总量均低于∑16PAHs ERM值, 只有TDS3的∑16PAHs总量超过∑16PAHs ERL值, 同时不设最低安全值的4种高环PAH在4种印染污泥中都有检出, 相应含量为TDS1∑4PAHs:267 ng·g-1、TDS2∑4PAHs:19 ng·g-1、TDS3∑4PAHs:943 ng·g-1、TDS4∑4PAHs:27 ng·g-1, 说明印染污泥进入环境后具有一定的生态风险.
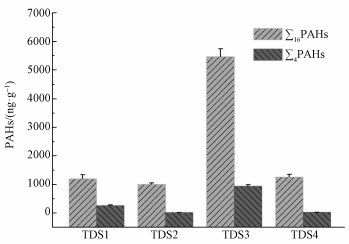 |
| 图 2 4种印染污泥中∑16PAHs总量和不设最低安全值的∑4PAHs总量 Fig. 2 The total amount of 16 kinds of PAHs and the total amount of 4 kinds of PAHs without minimum safety value in 4 kinds of textile dyeing sludge |
在前期试验中, 设置0、200、400、500、600、800、1000 g·kg-1 7个浓度的混合污泥进行测试, 发现浓度在500 g·kg-1时, 蚯蚓已全部死亡, 依据OECD测试标准, 急性毒性试验测定某物质的半数致死浓度应包含死亡率为0的最高浓度组和死亡率为100%的最低浓度组, 因此最终选取0、100、200、300、400 g·kg-1这5个浓度用于蚯蚓急性毒性测试.急性毒性试验结束时, 对照组(人工土壤)无蚯蚓死亡, 除TDS2浓度为100 g·kg-1处理组无蚯蚓死亡外, 各处理组均有蚯蚓死亡, 试验结果见表 2.试验过程中观察到蚯蚓在加入4种类型的印染污泥后,在600、800、1000 g·kg-13个浓度表现出剧烈爬行,试图爬上烧杯壁的实验现象;在24 h内观察到中毒症状:躯体萎缩、局部溃烂、渗液, 最终在72 h内全部死亡;在其他各浓度处理组中均观察到部分蚯蚓团聚在污泥表层, 不钻探.蚯蚓的中毒现象与崔春燕等(2015)在铬(Ⅵ)和菲单一及复合暴露对赤子爱胜蚓的急性毒性效应研究以及申荣艳等(2008)在长江三角洲地区城市污泥对蚯蚓的急性毒性效应研究中观察到的现象一致.
| 表 2 4种印染污泥对蚯蚓的14 d半数致死浓度 Table 2 50% lethal concentrations (14 d LC50) of 4 kinds of TDS to earthworm |
由表 2可知4种印染污泥中毒性最大的是TDS3, 半数致死浓度为177.6 g·kg-1, 相应的TDS3 PAHs的含量最高, 达到5465 ng·g-1, 其中芘的含量达到1515 ng·g-1, 说明印染污泥的生态毒性与PAHs有关.林康丽等(2013)在研究中也发现, 土壤中1 mg·kg-1的芘就能显著诱导蚯蚓体内过氧化物还原蛋白, 表明蚯蚓受到了芘污染的胁迫;同时吴尔苗(2011)在研究中也发现, 芘能显著影响蚯蚓体内超氧化物歧化酶和丙二醛的含量(这两种物质是动植物在逆境胁迫下非常重要的生理指标).试验结果说明印染污泥对蚯蚓具有一定的毒性作用, 蚯蚓死亡率随着印染污泥浓度的提高而上升.在试验中还观察到各处理组存活蚯蚓的体重显著减轻, 因此本研究进一步探究蚯蚓个体在受到印染污泥胁迫发生死亡之前, 蚯蚓生理水平的反应.
3.3 蚯蚓体腔细胞溶酶体NRRT的变化试验选取TDS3各处理组在14 d急性毒性试验中存活的蚯蚓用于测定NRRT, 试验中观察到的蚯蚓健康体细胞及曝露于TDS3 200 g·kg-1处理组体细胞在不同时间的染色情况细胞形态见图 3.将蚯蚓曝露于印染污泥污染的土壤中, 蚯蚓体细胞溶酶体膜受到污染物的毒害作用而损伤, 膜的稳定性降低, 通透性增加, 细胞被染色的历时缩短.通过判断溶酶体中中性红染料停留时间的长短来指示蚯蚓受到的污染胁迫, NRRT长, 毒害作用小, NRRT短, 毒害作用强(Weeks et al., 1996).
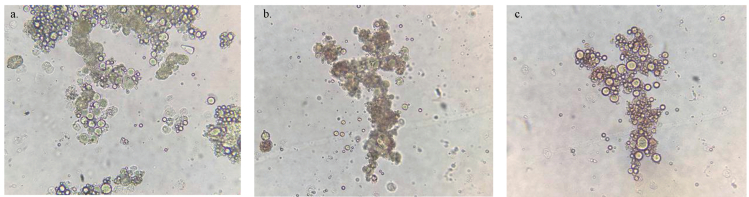 |
| 图 3 蚯蚓健康体细胞及曝露于TDS3 200 g·kg-1印染污泥中的体细胞在不同时间的染色情况(a.健康体细胞, b.染色5 min, c.染色21 min) Fig. 3 Health coelomocytes of earthworm and the dyeing condition of coelomocytes in different times exposed to TDS3 200 g·kg-1 |
图 4展示了在TDS3各处理组下蚯蚓体腔细胞中性红的停留时间.随着混合土壤中印染污泥浓度的增加, 蚯蚓体腔细胞溶酶体NRRT不断变短.根据抑制率NRRT=(NRRT对照组-NRRT处理组)/NRRT对照组计算, TDS3各处理组中蚯蚓NRRT抑制率分别为25.4%、58.7%、82.5%、96.8%.在急性毒性试验中得出TDS3的半数致死浓度为177.6 g·kg-1, 对比之下, 在浓度为100 g·kg-1时, NTTR抑制率达到25.4%, 说明在蚯蚓个体发生死亡之前, 蚯蚓体腔细胞溶酶体膜已经受到损伤.张伟等(2014)在土壤苯并(a)芘多次叠加污染的生物有效性及对蚯蚓体腔细胞染色体和溶酶体的毒性效应研究中发现, 苯并(a)芘对蚯蚓产生一定毒性, 体腔溶酶体膜受到一定程度的损伤, 中性红保留时间缩短.试验结果说明蚯蚓在低浓度印染污泥污染土壤中虽然能够存活, 但在生理上已经受到污染物的胁迫.本文在此基础上, 进一步模拟在自然条件下, 蚯蚓对于印染污泥污染土壤的响应.
 |
| 图 4 TDS3不同浓度印染污泥下蚯蚓体腔细胞中性红停留时间 Fig. 4 Neutral Red Retention Time of earthworm in different concentration of textile dyeing sludge of TDS3 |
在前期试验中, 设置混合污泥的浓度为0、200、400、600、800、1000 g·kg-1, 发现浓度在200 g·kg-1时, 蚯蚓已表现出完全的回避反应, 因此最终选取0、40、80、120、160、200 g·kg-1这6个浓度用于测试.试验结束时, 没有蚯蚓死亡, 试验结果见图 5.试验中观察到部分蚯蚓在接触到高浓度混合污泥(120、160、200 g·kg-1)时, 立即退回, 并且在整个选择过程中避开这一区域, 同时也观察到部分进入高浓度组的蚯蚓在短时间内(30 min)退出到内圆筒释放区, 重新选择进入低浓度组, 与Safwat等(2002)和何巧力等(2007)在研究中观察到的现象一致.
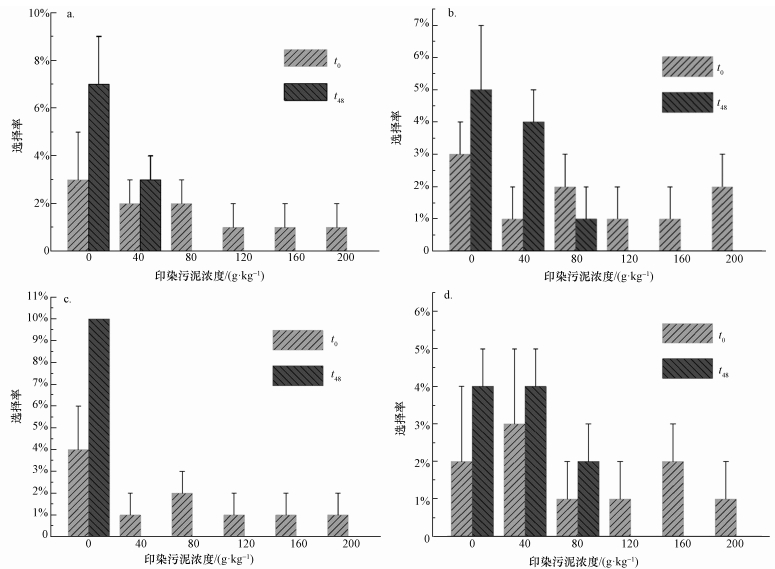 |
| 图 5 曝露于印染污泥中的蚯蚓的选择率(a.TDS1, b.TDS2, c.TDS3, d.TDS4) Fig. 5 Selection rate of earthworms exposed to TDS(a. TDS1, b. TDS2, c. TDS3, d. TDS4) |
随着土壤中印染污泥浓度的升高, 选择进入的蚯蚓趋于减少, 表现出明显的剂量-效应关系, 蚯蚓对于TDS3印染污泥的回避阈值为40 g·kg-1, TDS1为80 g·kg-1, TDS2和TDS4为120 g·kg-1, 分别只有蚯蚓14 d急性毒性试验中LC50值的22.5%、43.1%、48.4%和40.3%, 表明土壤即使被少量印染污泥污染, 其质量与生态功能已经削弱, 不适宜蚯蚓的栖息, 同时也证明蚯蚓能够快速感知土壤中污染物的存在, 类似的研究结论在黄盼盼等(2012)的研究中也有报道.将印染污泥中不设最低安全值的∑4PAHs总量与蚯蚓对4种印染污泥的响应浓度进行分析, 得到回归方程为y=-11x+1304.8, R2=0.94, 发现二者之间具有很强的线性关系, 说明印染污泥中的PAHs是引起蚯蚓产生回避行为的原因之一.
4 结论(Conclusions)1) 4种印染污泥中∑16PAHs总量不高, 只有TDS3的∑16PAHs总量超过∑16PAHs ERL值, 但都存在不设最低安全值的高环PAHs, 印染污泥进入环境后具有一定的生态风险.
2) 蚯蚓急性毒性试验、体腔细胞溶酶体NRRT抑制率试验以及蚯蚓回避试验结果说明, 印染污泥对蚯蚓具有一定的毒性作用, 其中蚯蚓回避试验对印染污泥的响应最为敏感, 响应值不到LC50的50%, 土壤中少量印染污泥的存在即可引起蚯蚓的回避行为, 可以应用于污染场地的快速毒性评价.
3) 蚯蚓急性毒性试验结果与蚯蚓回避试验结果与印染污泥中∑16PAHs的总量及不设最低安全值的∑4PAHs总量表现出较强的相关性, 印染污泥对蚯蚓的毒性效应与PAHs含量有关.
Blouin M, Hodson M E, Delgado E A, et al. 2013. A review of earthworm impact on soil function and ecosystem services[J]. European Journal of Soil Science, 64(2): 161–182.
DOI:10.1111/ejss.12025
|
崔春燕, 沈根祥, 胡双庆, 等. 2015. 铬(Ⅵ)和菲单一及复合暴露对赤子爱胜蚓的急性毒性效应研究[J]. 农业环境科学学报, 2015, 34(11): 2070–2075.
DOI:10.11654/jaes.2015.11.005 |
Feng L, Zheng H L, Gao B Y, et al. 2017. Enhancement of textile-dyeing sludge dewaterability using a novel cationic polyacrylamide:role of cationic block structures[J]. RSC Adcances, 8(19): 11626–11635.
|
黄盼盼, 周启星. 2012. 石油污染土壤对蚯蚓的致死效应及回避行为的影响[J]. 生态毒理学报, 2012, 7(3): 312–316.
|
何巧力, 颜增光, 汪群慧, 等. 2007. 利用蚯蚓回避试验方法评价萘污染土壤的生态风险[J]. 农业环境科学学报, 2007, 26(2): 538–543.
DOI:10.3321/j.issn:1672-2043.2007.02.025 |
Khandegar V, Saroha A K. 2013. Electrocoagulation for the treatment of textile industry effluent-A review[J]. Journal of Environmental Management, 128: 949–963.
DOI:10.1016/j.jenvman.2013.06.043
|
Long E R, Macdonald D D, Smith S L, et al. 1995. Incidence of adverse biological effects within ranges of chemical concentrations in marine and estuarine sediments[J]. Environmental Management, 19(1): 81–97.
DOI:10.1007/BF02472006
|
Liang J Y, Ning X A, An T C, et al. 2016. Degradation of aromatic amines in textile-dyeing sludge by combining the ultrasound technique with potassium permanganate treatment[J]. Journal of Hazardous Materials, 314: 1–10.
DOI:10.1016/j.jhazmat.2016.04.018
|
林康丽, 郑森林, 宋玉芳, 等. 2013. 蚯蚓体内过氧化物还原蛋白PRDX基因对土壤PAHs污染胁迫的转录响应[J]. 环境科学, 2013, 34(3): 1204–1210.
|
Liang X, Ning X A, Chen G X, et al. 2013. Concentrations and speciation of heavy metals in sludge from nine textile dyeing plants[J]. Ecotoxicology and Environmental Safety, 98: 128–134.
DOI:10.1016/j.ecoenv.2013.09.012
|
马静静, 钱新春, 张伟, 等. 2015. 土壤菲多次叠加污染对蚯蚓的毒性效应[J]. 土壤学报, 2015, 52(6): 1374–1382.
|
Man X Y, Ning X A, Zou H Y, et al. 2018. Removal of polycyclic aromatic hydrocarbons (PAHs) from textile dyeing sludge by ultrasound combined zero-valent iron/EDTA/Air system[J]. Chemosphere, 191: 839–847.
|
Ning X A, Feng Y F, Wu J J, et al. 2015. Effect of K2FeO4/US treatment on textile dyeing sludge disintegration and dewaterability[J]. Journal of Environmental Management, 162: 81–86.
|
Ning X A, Lin M Q, Shen L Z, et al. 2014. Levels, composition profiles and risk assessment of polycyclic aromatic hydrocarbons (PAHs) in sludge from ten textile dyeing plants[J]. Environmental Research, 132: 112–118.
DOI:10.1016/j.envres.2014.03.041
|
Safwat H, Shakir H, Weaver R W. 2002. Earthworm survival in oil contaminated soil[J]. Plant and Soil, 240: 127–132.
DOI:10.1023/A:1015816315477
|
申荣艳, 骆永明, 李振高, 等. 2008. 长江三角洲地区城市污泥对蚯蚓的急性毒性效应[J]. 土壤, 2008, 40(5): 738–743.
DOI:10.3321/j.issn:0253-9829.2008.05.010 |
Shi Z M, Tang Z W, Wang C Y. 2017. A brief review and evaluation of earthworm biomarkers in soil pollution assessment[J]. Environmental Science and Pollution Research, 24(15): 13284–13294.
DOI:10.1007/s11356-017-8784-0
|
Velki M, Ecimovic S. 2017. Important issues in ecotoxicological investigations using earthworms[J]. Reviews of Environmental Contamination and Toxicology, 239: 157–184.
|
吴尔苗. 2011. 菲、芘对蚯蚓(Eisenia foetida)的毒性机理研究[D]. 杭州: 浙江工业大学
|
吴浩亮, 杜伟志, 陈繁, 等. 2015. 关于佛山市印染污泥现状分析及焚烧处理的研究[J]. 化纤与纺织技术, 2015, 44(1): 23–30.
DOI:10.3969/j.issn.1672-500x.2015.01.09 |
王靖宇, 宁寻安, 李锐敬, 等. 2015. 典型印染废水处理过程中芳香烃化合物的污染特征及污泥生态风险评价[J]. 环境化学, 2015, 34(6): 1201–1208.
|
Weeks J M, Svendsen C. 1996. Neutral red retention by lysosomes from earthworm (Lumbricus rubellus) coelomocytes:a simple biomarker of exposure to soil copper[J]. Environmental Toxicology and Chemistry, 15(10): 1801–1805.
DOI:10.1897/1551-5028(1996)015<1801:NRRBLF>2.3.CO;2
|
Xie W H, Wen S T, Liu J Y, et al. 2018. Comparative thermogravimetric analyses of co-combustion of textile dyeing sludge and sugarcane bagasse in carbon dioxide/oxygen and nitrogen/oxygen atmospheres:Thermal conversion characteristics, kinetics, and thermodynamics[J]. Bioresource Technology, 255: 88–95.
DOI:10.1016/j.biortech.2018.01.110
|
颜增光, 何巧力, 李发生. 2007. 蚯蚓生态毒理试验在土壤污染风险评价中的应用[J]. 环境科学研究, 2007(1): 134–142.
DOI:10.3321/j.issn:1001-6929.2007.01.026 |
Zhang H D, Gao Z P, Ao W Y, et al. 2017. Microwave pyrolysis of textile dyeing sludge in a continuously operated auger reactor[J]. Fuel Processing Technology, 166: 174–185.
DOI:10.1016/j.fuproc.2017.05.031
|
张伟, 郑彬, 马静静, 等. 2014. 土壤B[a]P多次叠加污染的生物有效性及对蚯蚓体腔细胞染色体和溶酶体的毒性效应[J]. 应用与环境生物学报, 20(6): 1020-1026
|
 2018, Vol. 38
2018, Vol. 38


