2. 中国人民大学环境学院, 北京 100872;
3. 大连科技学院 图书馆, 大连 116052
2. School of Environment and Natural Resources, Renmin University of China, Beijing 100872;
3. Library, Dalian Institute of Science and Technology, Dalian 116052
CHENG Rong, E-mail: chengrong@ruc.edu.cn
水中的微生物致病性强、易传染, 会打破自然生态平衡, 人畜直接或间接接触受污染的水体, 会导致疾病的发生甚至流行, 危害人类健康.致病E.coli进入人体后会引发人体肠道疾病, 如腹泻、出血性肠炎等并发症, 所以是水处理消毒的必要指标.噬菌体是细菌病毒, 其行为可用于类比分析人类病毒对人体健康的危害.研究表明, 饮用水和污水中都有肠道病毒的存在, 会引起麻痹性疾病、无菌脑膜炎、心肌损伤等病症(Wingender et al., 2004).二者同时存在时, 大肠杆菌作为MS2和F2噬菌体宿主, 可影响噬菌体的繁殖, 提高噬菌体的存活时间, 因此二者同时存在, 危害更大.因此消毒是水处理工艺的必备环节.与传统的液氯或臭氧消毒技术相比, 紫外线消毒不使用化学药剂, 无副产物, 广谱灭菌, 管理方便(Oparaku et al., 2011;Sobhani et al., 2017), 因此, 在废水(Loge et al., 1996;Hassen et al., 2000)和饮用水(Dotson et al., 2012;Plewa et al., 2012;Hijnen et al., 2006)处理中得到广泛应用.
紫外线可透过致病菌的细胞壁和细胞膜, 破坏胞内遗传物质中的碱基对, 生成嘧啶二聚体, 阻碍微生物繁殖(Wojtenko et al., 2001;Kim et al., 2002).然而, 紫外线处理后的细菌在光复活酶的作用下能够修复紫外损伤, 恢复遗传物质的复制能力(Guo et al., 2012).这种“光复活”现象(Kim et al., 2013)使紫外消毒后的水仍具有健康风险.
光催化产生的羟基自由基(·OH)(Maness et al., 1999)具有强氧化能力, 不但能破坏细胞壁和细胞膜, 还能分解胞内物质, 彻底杀死致病菌(Sadek et al., 2015), 抑制微生物复活.报道的光催化消毒反应器一般为序批式(Rizzo et al., 2014;Rafael et al., 2009;Rizzoa et al., 2014;Wols et al., 2011), 难以满足水量较大的处理要求.市售连续流动式紫外线消毒器处理能力可满足实际废水消毒要求, 如果在紫外消毒器中安装光催化组件, 可以方便地实现连续流动式光催化消毒.以前的研究表明连续流动光催化消毒器的灭菌速度和抑制复活性能都优于商品紫外消毒器(Yu et al., 2016).但没有评价光催化过程对病毒的去除能力.本文采用性质与病毒类似的噬菌体F2和MS2为目标物, 考察连续流动式光催化消毒器对病毒的灭活能力.
2 实验部分(Experiment) 2.1 催化剂制备把钛片切割成特殊形状的小片并打孔(图 1a), 砂纸打磨后依次置于丙酮、无水乙醇中超声清洗5 min, 然后混合酸液(V(HF): V(HNO3): V(H2O)=1: 4: 5)刻蚀30 s, 超纯水冲洗后于空气中自然风干.采用如下3种方法在Ti片上负载TiO2层.
 |
| 图 1 光催化反应器构件和结构(a.切割并打孔的Ti片, b.光催化组件, 由4根长螺丝把15片Ti-TiO2组装到一起, Ti圆环的缺口形成折流通道, 增加水流的湍动, c.光催化组件的俯视图, d.光催化组件安装到市售紫外消毒器中, e.反应器结构示意图, f.反应器照片) Fig. 1 Component and structure of photocatalytic reactor |
① 溶胶凝胶法:量取7.5 mL钛酸四丁酯和1 mL TiCl4缓慢加入75 mL无水乙醇中, 常温搅拌2 h后向溶液中缓慢滴加3.75 mL的高纯水, 继续强烈搅拌2 h, 最终形成均匀、澄清、透明的淡黄色溶胶.将经过预处理的钛片浸入溶胶中, 浸渍120 s, 用提拉机将钛片拉出溶胶液面(0.2 mm·s-1).自然风干后, 放入烘箱中, 60 ℃水解反应12 h.然后高温煅烧, 升温速率为2 ℃·min-1;升至预设温度(450、500、550 ℃);保温时间为2 h.重复上述提拉、水解、煅烧过程即得二氧化钛薄膜样品.
② 阳极氧化法:配制0.2%(质量分数) HF溶液作为电解质, 以钛片为工作电极, 铂片为对电极, 20 V氧化20 min.阳极氧化后的样品放入马弗炉, 2 ℃·min-1从室温升到预定温度(450、500、550 ℃), 然后保温2 h后再自然冷却到室温即得TiO2纳米管(Quan et al., 2005).
③ 热氧化法:将预处理后的钛片直接置于马弗炉中, 从室温开始, 以2 ℃·min-1升至500 ℃, 然后在此温度下保温2 h, 冷却至室温即得氧化钛薄膜样品TC.
2.2 催化剂表征采用扫描电镜(SEM, S4800型)表征样品的表面形貌.测试条件如下:加速电压10 kV, 电流10 μA, 工作距离为8.0 mm.采用X射线衍射仪(XRD-7000)测试样品晶体结构.以Cu Kα辐射照射, 加速电压和应用的电流分别是40 kV和30 mA, 扫描速率为4 o·min-1.
2.3 反应器搭建通过在市售紫外消毒器中安装光催化组件搭建连续流动式光催化反应器.光催化组件由隔板式光载体和负载的TiO2组成.市售紫外消毒器反应腔体材质为不锈钢304, 直径63.5 mm, 长度为310 mm, 如图 1所示.该光催化消毒器处理量为75 L·h-1, 紫外灯为低压汞灯, 功率为11 W.
2.4 灭菌实验① 微生物的培养和计数:噬菌体F2和其宿主E.coli285以及噬菌体MS2和其宿主E.coliATCC15597均由中国人民大学环境学院提供.培养基为营养肉汤, 用NaOH溶液调节pH至7.2, 用灭菌锅121 ℃灭菌30 min.采用平板计数法获得E.coli浓度, 采用双层琼脂平板法检测噬菌体, 计算噬菌斑数量表示噬菌体浓度(PFU·mL-1).
② 灭活实验:用经灭菌处理过的去离子水接种E.coli后配制成细菌数约106 CFU·mL-1的原水.分别评估光催化组件的吸附性质、UV消毒性能和光催化消毒性能.配制噬菌体初始浓度为106~107 PFU·mL-1的原水, 在1.25 L·min-1和0.75 L·min-1两组流量下(紫外剂量分别为30 mJ·cm-2和50 mJ·cm-2)分别进行吸附, UV和光催化对F2/MS2噬菌体的去除性能.
测定处理前后菌液中活菌数, 通过公式(1)计算灭菌效果:

|
(1) |
式中, N0为处理前水样中活菌数(CFU·mL-1 (PFU·mL-1));Nt为处理后水样中剩余活菌数(CFU·mL-1 (PFU·mL-1)).
③ 复活实验:收集UV和光催化出水水样, 放入生化培养箱中, 25 ℃、光强3000 lx, 培养8 h, 每隔2 h采集水样, 采用平板计数法测定水样中活菌数目, 分析水质中细菌光复活情况.F2/MS2噬菌体水样的培养时间为24 h, 其他条件同上.复活率计算公式见式(2)(Kelner et al., 1951).
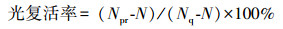
|
(2) |
式中, Nq为紫外线照射前的微生物数;N为紫外线照射后存活的微生物数;Npr为光复活后的微生物数.
3 结果与讨论(Results and discussion) 3.1 光催化材料表征扫描电镜图片(图 2a~2c)显示, 热氧化法制备的Ti-TiO2表面分布着零散的颗粒, 相对于Ti基底的形貌没有明显变化, 阳极氧化法制备样品的表面密集分布着小孔, 溶胶凝胶法的样品表面有很多龟裂的纹路.热处理温度影响样品的结晶度, 如图 2d和2e所示, 溶胶凝胶和阳极氧化法制备的样品的结晶度都随煅烧温度提高, 450 ℃和500 ℃制备的样品都是金红石和锐钛矿的混晶, 550 ℃的样品只有金红石相, 同样温度下溶胶凝胶样品的结晶度更高.综合XRD和SEM结果, 以及前期工作已证明光催化组件在连续运行40 h之后仍具有较强的稳定性(Yu et al., 2016), 所以选择溶胶凝胶结合500 ℃煅烧条件的样品进行后续实验.采用电子顺磁共振谱仪EPR检测单独紫外和光催化两个体系的· OH, 结果如图 2所示.由图可知, UV体系没有· OH的产生而光催化体系中产生了· OH, 说明光催化消毒过程中· OH是主要的氧化物种.
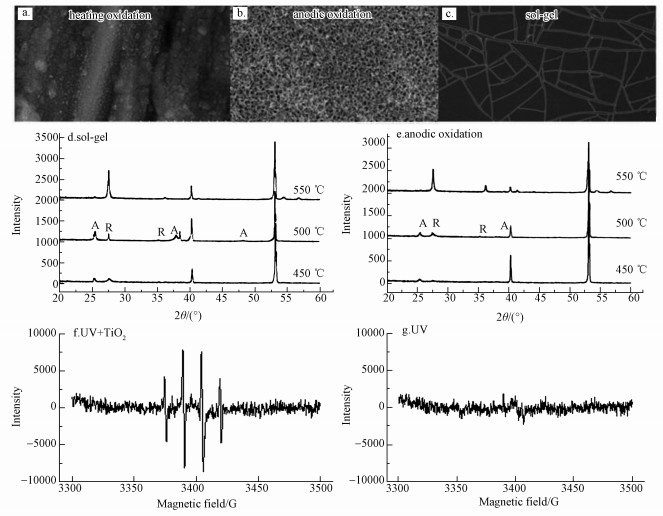 |
| 图 2 扫描电镜图(a.热氧化Ti-TiO2, b.阳极氧化Ti-TiO2, c.溶胶凝胶法Ti-TiO2和XRD图, d.阳极氧化样品经不同温度煅烧, e.溶胶凝胶样品经不同温度煅烧, f.光催化消毒过程的EPR检测结果, g.紫外消毒过程的EPR检测结果) Fig. 2 SEM images of Ti-TiO2 fabricated by ((a) heating oxidation, (b) anodic oxidation, (c) sol-gel, and XRD (d) patterns of samples under different heating temperatures, EPR spectra of DMPO-OH in the presence(f) or absence(g) of TiO2 under UV) |
图 3是溶胶凝胶法Ti-TiO2的高倍SEM, 其中图 3a是提拉1次的样品, 图 3b是提拉4次的样品.提拉4次的样品对基底的覆盖度好于提拉1次的样品, 增强了光吸收和接触细菌的面积, 而且抗冲刷性能较好.继续增加提拉次数得到的TiO2层过厚, 反复浸入水中TiO2层易剥落.
 |
| 图 3 提拉1次(a)和4次(b)制备的溶胶凝胶Ti-TiO2的SEM图 Fig. 3 SEM images of sol-gel Ti-TiO2(a) Pulling once (b) Pulling four times |
灭活结果如图 4a所示.原水中E.coli浓度为3.4×106 CFU·mL-1, 吸附过程(无光照有TiO2)出水E.coli浓度为2.8×106 CFU·mL-1.出水浓度略低于原水的原因是光催化剂吸附了少量的E.coli.UV过程的出水E.coli浓度为2.57×102 CFU·mL-1, 灭活4.12log10.光催化过程的E.coli浓度为5.5×101 CFU·mL-1, 灭活4.79 log10.这是因为光催化过程中, 除了UV可以灭活, 光催化产生的强氧化性· OH也能够杀死E.coli, 因此灭活速度在UV消毒的基础上明显提高..
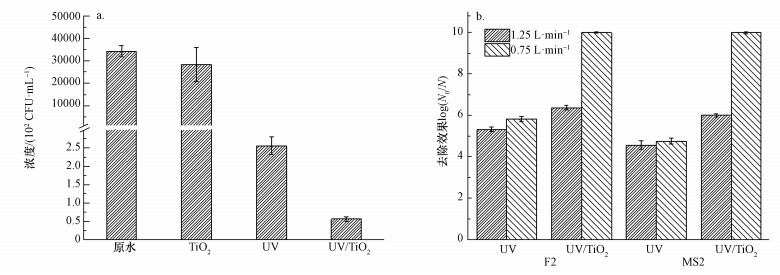 |
| 图 4 光催化灭菌效率(a.E.coli, b.噬菌体F2/MS2) Fig. 4 Sterilization efficiency of photocatalytic (a.E.coli, b.phage F2/MS2) |
图 4b为不同流量下光催化消毒设备和紫外消毒设备对噬菌体F2和MS2的去除效果.《城市给排水紫外线消毒设备GB/T-19837-2005》中提出污水排放达污染物排放标准一级A时, 紫外剂量不低于20 mJ·cm-2, 达饮用水水质标准时不低于40 mJ·cm-2.本实验在1.25 L·min-1和0.75 L·min-1流量下(对应的紫外剂量分别为30 mJ·cm-2和50 mJ·cm-2, 均满足标准要求), UV过程对噬菌体F2的去除分别为5.33log10和5.83log10, 光催化对F2的去除分别为6.37log10和几乎无检出.1.25 L·min-1的高流量下, 紫外消毒对噬菌体MS2的去除效果达4.56log10, 而0.75 L·min-1时提高到4.75log10.而在光催化设备中, MS2在1.25 L·min-1条件下的灭活达6log10, 0.75 L·min-1流量下几乎无检出.上述结果表明, 光催化对病毒的灭活速度也高于紫外过程, 且低紫外剂量下, 光催化的优势更明显.
3.3 抑制光复活性能取出水水样置于生化培养箱, 模拟自然条件下连续光照培养8 h, 每隔2 h采集水样, 用平板计数法统计水体中活菌数目.E.coli的光复活情况如图 5a所示.原水中E.coli浓度为3.42×106 CFU·mL-1.经过单独UV辐照消毒的出水浓度为2.54×102 CFU·mL-1, 8 h后E.coli浓度为5.48×102 CFU·mL-1.根据公式计算得到复活率为0.0086%.光催化出水中E.coli浓度为59 CFU·mL-1, 光照8 h后, E.coli浓度为110 CFU·mL-1, 复活率0.0015%, 不到UV过程的1/5.
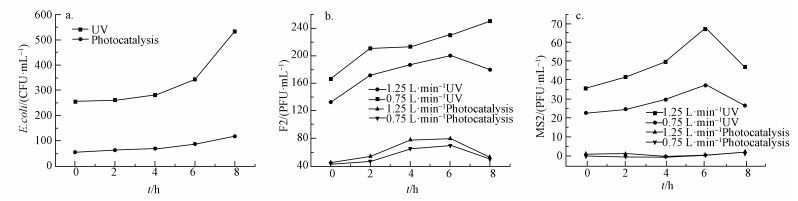 |
| 图 5 光复活实验:(a.E.coli; b.噬菌体F2; c.噬菌体MS2) Fig. 5 Reactivation evaluation: (a.E.coli; b.phage F2; c.phage MS2) |
类似的, 含噬菌体原水经紫外或光催化处理出水置于生化培养箱中模拟自然条件光照培养8 h, 每隔2 h采集水样并利用双层琼脂法统计水样中噬菌体F2和MS2的浓度.图 5b中, 1.25 L·min-1流量下, 单独紫外线辐照出水中噬菌体浓度为1.66×103 PFU·mL-1, 8 h后, 噬菌体F2浓度增长到2.50×103 PFU·mL-1, 其复活率为0.034%.而光催化作用出水中, 噬菌体浓度为4.5×102 PFU·mL-1, 6 h自然光照后浓度为8.0×102 PFU·mL-1, 复活率是0.014%.在0.75 L·min-1流量下, 单独UV辐照消毒的出水浓度为1.32×103 PFU·mL-1, 6 h后浓度为2.0×103 PFU·mL-1, 光催化6 h噬菌体F2浓度为7.0×102 PFU·mL-1, 光复活率是单独紫外的1/2.
如图 5c所示, 1.25 L·min-1流量下, 单独紫外线辐照出水中噬菌体初始浓度为3.6×101 PFU·mL-1, 8 h后, 噬菌体MS2浓度增长到4.7×101 PFU·mL-1.MS2浓度最大的时刻出现在光照6 h, 光复活率为0.00084%.光催化和紫外线联用的出水中, 噬菌体初始浓度为0.13×101 PFU·mL-1, 8 h自然光照后浓度为0.23×101 PFU·mL-1, 光复活率是0.000076%, 仅为紫外光复活率的9%.在0.75 L·min-1流量下, 单独UV辐照消毒的出水初始浓度为2.3×101 PFU·mL-1, 8 h后浓度为3.8×101 PFU·mL-1, 其光复活率为0.0011%, UV/TiO2联用系统8 h噬菌体MS2浓度为0.2×101 PFU·mL-1复活率是0.00015%, 仅为UV过程的14%.光复活实验进行6 h后, 噬菌体浓度开始下降, 这是由于噬菌体的繁殖需要最适浓度的E.coli, 而水样中的E.coli已经不能满足需求.
3.4 光催化消毒器稳定性为了考查设备运行稳定性, 连续做了5次重复实验, 共运行40 h, 结果如图 6所示.E.coli原液浓度为1.61×109 CFU·mL-1, 紫外消毒出水中E.coli浓度分别为3.06×102、3.20×102、3.10×102、3.30×102、3.60×102 CFU·mL-1, 平均浓度为3.25×102 CFU·mL-1;相比而言, 光催化作用的出水中, E.coli浓度分别为4.8×101、5.0×102、5.1×101、5.0×101、4.2×101 CFU·mL-1, 平均浓度为4.8×101 CFU·mL-1.实验结果表明, 光催化水处理消毒设备处理后的出水中E.coli浓度为紫外线消毒出水的14.8%, 消毒效率得到大幅度提高.此外, 连续运行过程中, 流经光催化水处理消毒设备的出水中E.coli的浓度稳定在4.2×101~5.1×101 CFU·mL-1之间.这表明光催化水处理消毒设备运行过程中消毒性能较为稳定.
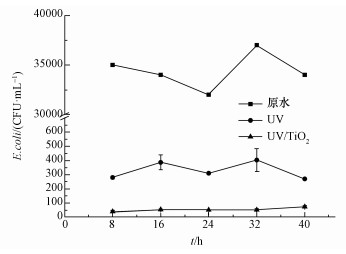 |
| 图 6 设备运行40 h的灭菌性能 Fig. 6 Disinfection performance of device in 40 h of operation |
本文设计并制造挡板式负载型光催化消毒设备, 用E.coli和噬菌体为指标考察光催化消毒设备灭菌性能.结果显示, 流动式光催化消毒器对E.coli及噬菌体的灭活能力和抑制复活能力均明显优于紫外线消毒器.这一成果有助于推动光催化技术在水处理消毒中的应用.
Dotson A D, Rodriguez C E, Linden K G. 2012. UV disinfection implementation status in US water treatment plants[J]. J Am Water Works Assoc, 104(5): 77–78.
|
Guo M T, Huang J J, Hu H Y, et al. 2012. UV inactivation and characteristics after photoreactivation of Escherichia coli with plasmid:health safety concern about UV disinfection[J]. Water Research, 46(13): 4031–4036.
DOI:10.1016/j.watres.2012.05.005
|
Hassen A, Mahrouk M, Ouzari H. 2000. UV disinfection of treated wastewater in a large-scale pilot plant and inactivation of selected bacteria in a laboratory UV device[J]. Bioresource Technology, 74(2): 141–150.
DOI:10.1016/S0960-8524(99)00179-0
|
Hijnen W A M, Beerendonk E F, Medema G J. 2006. Inactivation credit of UV radiation for viruses, bacteria and protozoan(oo)cysts in water:a review[J]. Water Research, 40(1): 3–22.
DOI:10.1016/j.watres.2005.10.030
|
Kelner A. 1951. Action spectra for photoreactivation of ultraviolet-irradiated Escherichia coli and Streptomyces griseus[J]. The Journal of General Physiology, 34(6): 835–852.
DOI:10.1085/jgp.34.6.835
|
Kim B R, Anderson J E, Mueller S A, et al. 2002. Literature review-efficacy of various disinfectants against Legionella in water systems[J]. Water Research, 36(18): 4433–4444.
DOI:10.1016/S0043-1354(02)00188-4
|
Kim S, Ghafoor K, Lee J, et al. 2013. Bacterial inactivation in water, DNA strand breaking, and membrane damage induced by ultraviolet-assisted titanium dioxide photocatalysis[J]. Water Research, 47(13): 4403–4411.
DOI:10.1016/j.watres.2013.05.009
|
Loge F J, Emerick R W, Health M, et al. 1966. Ultraviolet disinfection of secondary wastewater effluents:prediction of performance and design[J]. Water Environmental Research, 68(5): 901–916.
|
Maness P, Smolnski S, Blake D M. 1999. Bactericidal activity of photocatalytic TiO2 reaction:toward an understanding of its killing mechanism[J]. Applied and Environmental Microbiology, 65(9): 4094–4098.
|
Oparaku N F, Mgbenka B O, Ibeto C N. 2011. Waste water disinfection utilizing ultraviolet light[J]. Journal of Environmental Science and Technology, 4(1): 73–78.
DOI:10.3923/jest.2011.73.78
|
Plewa M J, Wagner E D, Merz D H. 2012. Differential toxicity of drinking water disinfected with combinations of ultraviolet radiation and chlorine[J]. Environtenal Science & Technology, 46(14): 7811–7817.
|
Quan X, Yang S, Ruan X, et al. 2005. Preparation of titania nanotubes and their environmental applications as electrode[J]. Environmental Science & Technology, 39(10): 3770–3775.
|
Rafael V G, Javier M, Carlos S, et al. 2009. Comparison of the photocatalytic disinfection of E. coli suspensions in slurry, wall and fixed-bed reactors[J]. Journal of Catalysis, 144(1/2): 48–54.
|
Rizzo L, Sala A D, Fiorentino A, et al. 2014. Disinfection of urban wastewater by solar driven and UV lamp-TiO2 photocatalysis:effect on a multi drug resistant Escherichia coli strain[J]. Water Research, 53: 145–152.
DOI:10.1016/j.watres.2014.01.020
|
Rizzoa L, Sanninob D, Vaiana V, et al. 2014. Effect of solar simulated N-doped TiO2 photocatalysis on the inactivation and antibiotic resistance of an E. coli strain in biologically treated urban wastewater[J]. Applied Catalysi B: Environmental, 144: 369-378
|
Sadek I, Fatiha S, Chems E C, et al. 2015. Efficiency evaluation of solar photolysis and solar photocatalysis processes used for the wastewater disinfection[J]. Desalination and Water Treatment, 53(8): 2049–2058.
DOI:10.1080/19443994.2013.862866
|
Sobhani H, Shokouhmand H. 2017. Effects of number of low-pressure ultraviolet lamps on disinfection performance of a water reactor[J]. Journal of Water Process Engineering, 20: 97–105.
DOI:10.1016/j.jwpe.2017.08.021
|
Wingender J, Flemming H C. 2004. Contamination potential of drinking water distribution network biofilms[J]. Water Science and Technology, 49(11/12): 277–286.
|
Wojtenko I, Stinson M K, Field R. 2001. Challenges of combined sewer overflow disinfection by ultraviolet light irradiation[J]. Critical Reviews in Environmental Science and Technology, 31(3): 223–239.
DOI:10.1080/20016491089217
|
Wols B A, Hofman J A M H, Beerendon E F, et al. 2011. A systematic approach for the design of UV reactors using computational fluid dynamics[J]. Alche Journal, 57(1): 193–207.
DOI:10.1002/aic.12255
|
Yu H T, Song L, Hao Y, et al. 2016. Fabrication of pilot-scale photocatalytic disinfection device by installing TiO2 coated helical support into UV annular reactor for strengthening sterilization[J]. Chemical Engineering Journal, 283: 1506–1513.
DOI:10.1016/j.cej.2015.08.042
|
 2018, Vol. 38
2018, Vol. 38


