随着中国经济的快速增长, 城市化进程的加快, 大气细颗粒物污染已经成为我国重大的环境问题之一.硝酸盐、硫酸盐等水溶性无机盐是大气PM2.5(空气动力学直径小于2.5 μm的颗粒物)的重要组成部分, 贡献了大气PM2.5质量浓度的62%~77%(Liang et al., 2015), 大气PM2.5中的二次无机盐会影响大气颗粒物的化学性质、光学性能和吸湿性, 对大气能见度和气候环境有重大的潜在影响(Wang et al., 2014).Tang等(2016)研究发现, 高湿条件下非均相化学过程促发的二次粒子快速生成及吸湿增长是北京地区大气重污染形成的重要原因.重霾期间硝酸盐等二次无机气溶胶对细颗粒物质量的贡献显著大于清洁期(Wang et al., 2014).
颗粒物及对应化学组分的粒径分布是颗粒物的重要性质, 可以有效反映颗粒物的来源和形成机制.亚微米的颗粒物(粒径小于1 μm)主要来源于燃烧过程及多相反应过程(Lanz et al., 2010; Wang et al., 2013; Calvo et al., 2013), 而粗模态颗粒及组分主要来源于海盐、矿物尘及粗颗粒表面的非均相反应(Cabada et al., 2004; Anlauf et al., 2006).在亚微米的颗粒物中, 蒸气的凝结和极细颗粒的凝结一般会形成凝结态颗粒, 而云过程的液相反应形成液滴模态颗粒(Seinfeld et al., 2006; Han et al., 2013).国内也已有不少关于颗粒物及其典型组分的粒径分布的研究, 如Yao等(2003)于2001年夏季和2002年春季研究了北京大气颗粒物中水溶性离子的粒径分布, 发现夏季SO42-主要以液滴模态存在, 而春季主要以凝结模态存在;刘臻等(2012)分析了青岛大气颗粒物中水溶性离子的粒径分布, 发现SO42-和NH4+以细粒子为主呈单峰分布, 而NO3-呈双峰型分布, 且粗、细粒子中SO42-和NH4+均具有很好的相关性;于丽敏等(2007)在2005年5月的一次航测中采集并分析了南、黄海的大气颗粒物, 结果表明, 近海大气颗粒物中含氮无机离子的粒径分布与陆地(青岛)颗粒物有较好的相似性.Tian等(2014)分析了北京2013年1—2月严重雾霾期间颗粒物及主要组分的粒径分布, 发现随着霾污染的加重, 峰值粒径有增加的趋势, 说明颗粒物的吸湿增长对霾污染的形成有重要作用.Xiu等(2004)利用8级采样器分析了上海市主要离子的粒径分布, 发现硫酸根的峰值粒径为0.7 μm, 而硝酸根存在较明显的双峰分布;Tao等(2014)于2012年4—5月分析了上海大气颗粒物的粒径分布, 发现硫酸根、硝酸根和铵根主要存在于亚微米颗粒物中, 而Ca2+、Mg2+和Cl-呈双峰分布.总体而言, 对颗粒物组成的粒径分布的研究仍较有限, 且已有研究的采样期都较短, 因而相关研究仍有待加强.
上海是中国最重要的城市之一, 作为一个国际化大都市, 上海的大气细颗粒物污染广受关注.随着常规污染物治理的不断推进, 以细颗粒物和臭氧为特征的复合污染日益突出, 但目前人们对上海大气颗粒物组成及来源的认识仍有较大不足.因此, 本研究通过采集上海4个季节的大气颗粒物分粒径样品, 分析水溶性离子组分的粒径分布, 以期更好地理解上海大气颗粒物的组成特征、来源及形成机制.
2 实验与方法(Experiments and methods) 2.1 样品采集本研究选择的采样点位于上海大学宝山校区一座教学楼的楼顶, 距地高度约25 m.采样点地处快速城市化的上海市近郊地区, 周边以居住、办公区为主, 但东北方向离宝钢及石洞口电厂的距离仅为10 km左右, 采样点的东部约600 m处有一条车流量较高的公路, 北部约300 m处是一条中等车流量的公路, 经常有重型柴油车通过, 可以作为受工业、交通影响的近郊环境的代表.
选用微孔均匀沉积式多级碰撞采样器(MOUDI), 采样流量为30 L · min-1.采样器共11级, 切割粒径分别为0.056、0.10、0.18、0.32、0.56、1.0、1.8、3.2、5.6、10、18 μm.样品采集时间为每天中午12:00至第3 d中午12:00, 每套样品的采样时间为48 h.采样时期为2016年7月—2017年4月, 共采集44套分粒径样品(每个季节11套, 共484个样品).使用石英滤膜进行样品采集, 石英膜使用前于450 ℃灼烧4 h以去除残留有机物.采集后的样品装入铝箔包裹的膜盒, 密实袋密封后放入-20 ℃的冰箱保存, 以待分析.
2.2 水溶性离子组分分析将采样膜放入10 mL超纯水(Milli-Q)中, 冰水浴超声抽提30 min, 用0.45 μm亲水性聚四氟乙烯过滤头过滤.无机离子采用双通道离子色谱(Metrohm IC, 瑞士万通公司)测定.阴离子分离柱为Metrosep A-SUPP5-250(长度250 mm, 内径4 mm), 流动相为3.2 mmol · L-1 Na2CO3/1.0 mmol · L-1 NaHCO3混合溶液, 流速为0.7 mL · min-1;阳离子分离柱为Metrosep C2-250 (长度250 mm, 内径4 mm), 流动相为4 mmol · L-1酒石酸/0.75 mmol · L-1吡啶二羧酸混合溶液, 流速为1.0 mL · min-1.
2.3 质量保证和质量控制每次采样结束后用超纯水清洗MOUDI多孔板, 防止微孔被颗粒物堵塞.抽提所用聚丙烯瓶使用前分别用蒸馏水和超纯水超声清洗各6遍以上以消除本底;每个季节采集一套野外空白样品, 对野外空白和实验室空白的分析结果表明, 空白中检测到的离子组分的浓度小于实际样品中浓度的10%, 不影响目标化合物的定量分析.每10个样品分析一个平行样, 分析结果的重复性良好, 偏差小于5%.
3 结果与讨论(Results and discussion) 3.1 上海市大气颗粒物中水溶性离子浓度、组成及其季节分布本研究将 < 1.8 μm的颗粒物定为细颗粒, 将>1.8 μm的颗粒物定为粗颗粒.表 1列举了上海不同季节大气颗粒物中无机离子的浓度, 细颗粒物中离子总浓度在春、夏、秋、冬季分别为13.46、4.97、6.72、16.54 μg · m-3, 存在显著的季节变化, 冬季>春季>秋季>夏季, 其中尤以NO3-的季节变化最为显著;而粗颗粒中春、夏、秋、冬季的总离子浓度分别为4.65、3.78、5.90、4.14 μg · m-3, 季节变化不明显.根据已发表的研究结果, 2000年和2004年上海PM2.5中的总离子平均浓度分别为33.7和26.1 μg · m-3, 2012年春季上海PM2.1中的总离子平均浓度为32.6 μg · m-3(Ye et al., 2003; Wang et al., 2006; Tao et al., 2014).本次采样期间大气颗粒物中水溶性离子的浓度明显较低, 与近几年上海空气质量已有显著改善的实际情况一致.
| 表 1 四季采样期间颗粒物中离子浓度分布特征 Table 1 Averaged seasonal concentrations of ions in aerosols inShanghai |
从不同季节粗、细颗粒中离子总浓度的分布可以看出, 冬、春季上海颗粒物中的水溶性离子主要集中在细颗粒物中, 而夏、秋季粗颗粒态离子占比较高(~45%).NO3-、SO42-和NH4+是主要的水溶性离子, 除NO3-外主要存在于细颗粒物中, 三者浓度之和占细颗粒物中离子总浓度的比例在春、夏、秋、冬季分别为84%、71%、78%和87%.K+主要存在于细颗粒物中, 而Na+、Ca2+、Mg2+和Cl-(除冬季外)主要存在于粗颗粒物中.
3.2 上海市大气颗粒物中水溶性离子的粒径分布特征图 1是上海市大气颗粒物中主要离子NO3-、SO42-、NH4+、Cl-、K+、Ca2+在不同季节的粒径分布, 以下将分别加以讨论.
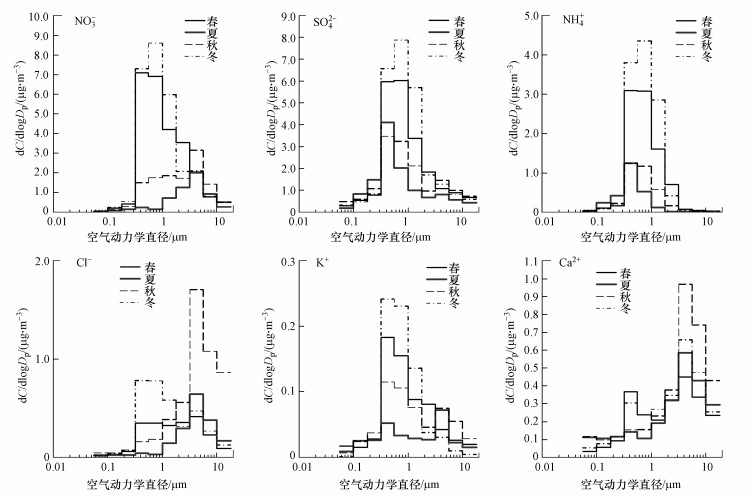 |
| 图 1 不同季节颗粒物中主要离子浓度粒径分布 Fig. 1 Size distributions of major ions in aerosols in Shanghai during different seasons |
由图 1可知, NO3-的粒径分布具有显著的季节变化, 冬、春季浓度较高且以细颗粒态为主, 峰值粒径分别为0.56~1.0 μm和0.32~0.56 μm, 亚微米颗粒物中的NO3-浓度占总硝酸根的78%±10%;而夏、秋季NO3-的浓度较低且主要存在于粗颗粒中, 峰值粒径为3.2~5.6 μm, 占总硝酸根浓度的25%~32%.
NO3-主要来源于氮氧化物气体的二次氧化, 其模态分布主要受硝酸铵分解的热力学平衡控制, 受大气温度、湿度的影响较大, 当热力学平衡有利于颗粒态硝酸铵形成时, NO3-主要以细颗粒形式存在, 而当气象条件不利于颗粒态硝酸铵形成时, 气态HNO3与海盐、矿物质等反应形成的粗颗粒态不挥发硝酸盐的占比较高(Zhuang et al., 1999; Yao et al., 2003).上海大气中细颗粒态NO3-在总浓度中的占比由夏季到秋季再到春季和冬季不断增加的趋势体现了大气温度对细颗粒态硝酸铵气-粒转换的影响, 夏、秋季较高的大气温度使得硝酸铵的气-粒平衡更偏向于气态, 细颗粒态硝酸铵的浓度较低, 与此同时, 硝酸气体与碳酸岩盐或海盐的反应更易发生, 因此, 粗颗粒态硝酸盐的比例大幅增加, 而冬季和春季时的低温有利于细颗粒态硝酸铵的形成.夏季细颗粒态NO3-含量非常低的另一个可能原因是采样过程中一定的真空度会导致已采集颗粒物中硝酸盐的挥发, 但硝酸根从细粒径段到粗粒径段的质量迁移可以忽略不计(Kang et al., 2013).从图 1还可以看到, 0.18 μm以下的颗粒中NO3-的含量在所有季节都非常低, 可能说明由于其半挥发特性及颗粒曲率对蒸气压的影响使得NO3-难于在超细颗粒物中存在.
3.2.2 SO42-的粒径分布及季节变化SO42-主要存在于细颗粒物中, 细颗粒态SO42-在总浓度中的占比在春、夏、秋、冬季分别为79%、79%、72%和83%.春、冬季时SO42-的粒径分布呈单峰型, 峰值粒径分别为0.32~0.56 μm和0.56~1.0 μm;夏、秋季时呈双峰型分布, 在3.2~5.6 μm粒径段出现较弱的次峰(图 1).SO42-在粗颗粒段出现次峰的现象在其他研究中也有发现, 并被认为主要源于海盐的贡献及SO2在粗颗粒表面的非均相氧化(Yao et al., 2003; Xiu et al., 2004; Tao et al., 2014).
由图 1可以看到, 与0.32~0.56 μm粒径段的SO42-浓度相比, 0.56~1.0 μm粒径段的浓度存在冬季>春季>秋季>夏季的趋势, 0.32~0.56 μm粒径段与0.56~1.0 μm粒径段SO42-浓度的比值在春、夏、秋、冬季分别为0.99、2.04、1.07、0.83, 即SO42-的峰值粒径由夏季的0.32~0.56 μm逐渐转变为冬季的0.56~1.0 μm.已有研究表明, 0.32~0.56 μm粒径的凝结态SO42-源于SO2气体氧化、凝结后的吸湿增长(Ondov et al., 1998), 而0.56~1.0 μm粒径的液滴态SO42-来源于云过程液相反应(Meng et al., 1994).因此, 上海颗粒物中液滴模态SO42-相对贡献的季节变化表明, 气相/非均相氧化过程是夏季SO42-的主要形成方式, 云过程次之, 而冬季SO42-的主要形成方式为云过程, 其次是气相/非均相反应;云过程属于快速反应, 且反应速率与温度无关, 而气相/非均相反应的速率与大气温度密切相关, 夏季高温下的反应速率会显著高于冬季.Yao等(2003)对北京大气颗粒物的研究发现, 春季时SO42-的峰值粒径为0.32~0.56 μm, 而夏季为0.56~1.0 μm.这与本次研究的结果有明显的差别, 造成这种差别的主要原因是北京春季的大气相对湿度较低, 发生云过程反应的概率较低, 而上海四季的相对湿度均较高(春、夏、秋、冬季采样期间的平均湿度分别为76%、72%、77%和75%), 易于发生云过程反应, 因此, 云过程液相氧化是上海亚微米颗粒物中SO42-的重要形成机制, 但气相/非均相反应也是重要的形成方式, 其贡献率与大气温度相关, 夏季时其贡献超过云过程.夏季0.56~1.0 μm粒径段SO42-浓度较低的另一个可能原因是夏季降雨频率较高, 云过程生成的硫酸盐可能以湿沉降的方式被从大气中清除而未转化为亚微米颗粒物.
3.2.3 NH4+的粒径分布及季节变化NH4+的粒径分布在不同季节均呈单峰形, 与SO42-在细颗粒范围的粒径分布非常相似, 表明细颗粒态的SO42-主要与NH4+结合.NH4+是细颗粒物中最主要的阳离子, 是中和SO42-、NO3-和Cl-等酸性组分的主要物质, NH4+的粒径分布与多种阴离子的粒径分布有关.>3.2 μm的粗颗粒中基本检测不到NH4+的存在, 这与SO42-和NO3-有明显差别, 证实了粗颗粒态的SO42-和NO3-主要与Na+、Ca2+等金属离子相结合.
3.2.4 Cl-的粒径分布及季节变化Cl-的粒径分布除夏季外均呈双峰形, 粗颗粒态Cl-的占比在春、夏、秋、冬季分别为48%、84%、82%和34%.粗颗粒中的峰值粒径在不同季节都出现在3.2~5.6 μm粒径段, 主要来自海盐的贡献及HCl气体与矿物尘的非均相反应(Zhuang et al., 1999; Yao et al., 2003), 因此, 海盐是上海大气颗粒物中Cl-的主要贡献者, 尤其是秋季和夏季, 这与上海是沿海城市、夏秋季海风频率较高的实际情况一致.细颗粒态Cl-主要来自燃煤及生物质燃烧(Yao et al., 2002), 由于K+的浓度较低(表 1), 燃煤应是上海大气细颗粒物中Cl-的主要来源.Cl-在亚微米段的粒径分布及其季节变化与NO3-较为相似, 峰值粒径分别为0.32~0.56 μm和0.56~1.0 μm, 说明细颗粒态Cl-的形成方式主要是燃煤产生的HCl气体的凝结、中和及吸湿增长.Cl-粒径分布与NO3-的相似性说明细颗粒态Cl-可能主要以氯化铵的形式存在, 氯化铵的半挥发性对Cl-浓度及粒径分布的季节变化有重要的控制作用.
3.2.5 K+的粒径分布及季节变化K+已被广泛用作生物质燃烧源的示踪物, 但也可能来源于农业施肥、扬尘及海盐.由图 1可知, 冬、春季时K+为单峰型粒径分布, 主要存在于细颗粒物中(占比分别为89%和75%), 峰值粒径为0.32~0.56 μm;夏、秋季时K+的粒径分布呈双峰型, 峰值粒径分别为0.32~0.56 μm和3.2~5.6 μm, 粗颗粒态K+分别占总浓度的43%和36%.K+主要赋存于亚微米颗粒中说明生物质燃烧是上海大气颗粒物中K+的主要来源, 夏、秋季粗颗粒态K+可能来源于海盐及矿物质.与此同时, K+的浓度显著低于文献报道值(Ye et al., 2003; Tao et al., 2014), 说明近年来对秸杆焚烧的控制取得了较好的成效.
3.2.6 Ca2+的粒径分布及季节变化Ca2+被广泛用作扬尘及建筑尘的示踪物, 粒径分析的结果也表明Ca2+主要存在于粗颗粒中, 峰值粒径为3.2~5.6 μm.计算表明, 粗颗粒态Ca2+在总浓度中的占比在春、夏、秋、冬季分别为56%、68%、74%、60%, 说明细颗粒态Ca2+也有一定的占比, 冬、春季时Ca2+呈明显的双峰分布, 次级峰值粒径为0.32~0.56 μm, 因此, 细颗粒态Ca2+可能部分来源于燃烧过程, 而并非全部源于扬尘.Tao等(2014)对上海春季颗粒物的研究也发现Ca2+存在双峰型粒径分布, 燃煤及生物质燃烧可能是细颗粒态Ca2+的主要来源, 但对细颗粒态Ca2+来源的研究较少.Na+和Mg2+的粒径分布与Ca2+基本一致.
3.3 上海市大气颗粒物的阴阳离子平衡大气颗粒物中阴阳离子的电荷平衡常被用于指示颗粒物的酸碱度, 所有阴离子的总当量浓度与所有阳离子的总当量浓度之比(AI/CI)大于1.0时表示颗粒物呈酸性(Kim et al., 2000).上海2016—2017年18 μm以下颗粒物的AI/CI比值在春、夏、秋、冬季的平均值分别为1.04、0.73、1.01和1.06, 说明颗粒物整体呈微弱酸性或中性, 但在夏季偏碱性, 这可能与夏季高温导致硝酸铵及半挥发有机酸的挥发因而粗颗粒矿物质的占比较高有关.分析结果与一般认为上海的细颗粒物呈微弱酸性的认识相符(Xiu et al., 2004; Wang et al., 2006).
图 2展示了不同季节、不同粒径颗粒物的AI/CI比值, 3.2 μm以上的粗颗粒都呈碱性, 这与通常的认识一致, 与粗颗粒中源于扬尘的Ca2+、Mg2+等碱性离子的富集有关;除夏季外, 0.32~3.2 μm的颗粒中AI/CI明显大于1.0, 说明这些颗粒物可能有较强的酸性;但0.056~0.32 μm颗粒物的AI/CI比值在所有季节都小于1.0, 且粒径越小, 比值越低, 按现有的认识则这些细颗粒物均呈碱性, 明显与我们对核模态及凝结模态细颗粒物的认识不符.半挥发组分的饱和蒸汽压与颗粒物的粒径有关, 粒径越小蒸汽压越高(Huebert et al., 1988), 因此, Cl-、NO3-和NH4+在0.32 μm以下细颗粒物中的浓度非常低, 浓度过低时离子色谱响应的非线性和较大的实验误差可能导致0.056~0.32 μm粒径段颗粒物AI/CI比值的失真.已有证据表明, 生物源和人为源排放的挥发性有机物经光化学反应会生成众多的有机酸, 并在气态硫酸的成核过程及新粒子生成过程中起重要作用(Fan et al., 2004; Fan et al., 2006).因此, 定量过程中有机酸的缺失可能是0.056~0.32 μm粒径段颗粒物呈“碱性”的重要原因之一, 后续需要加强对核模态及凝结态细颗粒中有机酸的研究, 同时也说明通过阴阳离子平衡判断颗粒物酸碱性的方法可能不适用于核模态及凝结态细颗粒物.
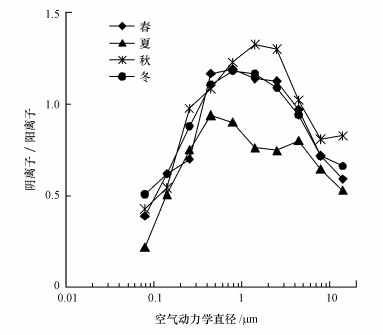 |
| 图 2 不同季节上海大气颗粒物中阴/阳离子比值的粒径分布 Fig. 2 Size distributions of anion tocation ratio in seasonal aerosols in Shanghai |
SO42-/NO3-质量比值常被用于识别大气颗粒中硝酸盐和硫酸盐的来源, SO42-/NO3-比值大于1.0说明燃煤电厂等固定源是主要的大气污染源, 比值小于0.5则机动车尾气是主要的污染源(Arimoto et al., 1996; Yao et al., 2002).上海小于1.8 μm的细颗粒物中SO42-/NO3-的平均比值在春、夏、秋、冬季分别为0.90、6.83、1.96和0.96, 如3.2.1节所述, 夏、秋季的高比值主要缘于硝酸铵的气-粒平衡转换, 冬、春季小于1.0的SO42-/NO3-比值明显小于21世纪初的结果(Yao et al., 2002; Xiu et al., 2004), 说明随着各项烟气脱硫措施的实施, 机动车排放的贡献显著增加, 已成为上海非常重要的大气污染源.
如图 3所示, SO42-/NO3-最小比值(0.4~0.6)出现于3.2~5.6 μm粒径段, 该粒径段是海盐及矿物质的峰值粒径, 最小比值的出现是由于气态HNO3在粗颗粒表面通过非均相反应形成NO3-浓度的次级峰(3.2节粒径分布).春、秋、冬季的SO42-/NO3-比值在5.6 μm以下的颗粒中都呈现随粒径变小而增大的趋势, 但秋季亚微米颗粒中的SO42-/NO3-比值明显高于冬、春季, 这主要与NH4NO3的挥发/热分解有关, NH4NO3的蒸汽压除与温度有关外和颗粒的直径也密切相关, 细颗粒物表面NH4NO3的蒸汽压较高、热分解作用更显著(Arimoto et al., 1996; Huebert et al., 1988; Yao et al., 2002), 而硫酸盐的挥发性非常小, 因此, NO3-的挥发导致SO42-/NO3-比值随粒径变小而增大.
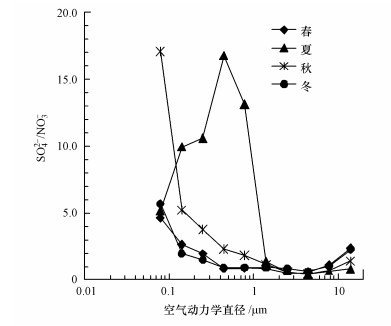 |
| 图 3 不同季节颗粒物中SO42-/NO3-比值的粒径分布 Fig. 3 Size distributions of the SO42-/NO3- ratio in different seasons in Shanghai |
夏季SO42-/NO3-比值的粒径分布显示出与其他季节不同的特征, 在0.32~0.56 μm粒径段出现最高值, 而在更细的颗粒中SO42-/NO3-比值随粒径变小而下降.夏季大气温度高, NH4NO3容易分解而难以以细颗粒态存在, 亚微米颗粒中的NO3-浓度很低, 因而SO42-/NO3-比值显著高于其他季节(图 3), 随着粒径进一步变小, NO3-浓度下降的幅度很小且与其他季节接近(图 1), 表明在浓度很低时蒸汽压随曲率而变化的规律可能不再适用, 或者硝酸盐的赋存形态发生了变化, 但具体原因有待进一步研究.
4 结论(Conclusions)1) 冬、春季上海大气颗粒物中的水溶性离子主要集中在细颗粒物中, 而夏、秋季粗颗粒态离子的占比较高(~45%).
2) SO42-、NH4+和K+主要存在于细颗粒物中, Na+、Ca2+和Mg2+主要存在于粗颗粒物中.而NO3-和Cl-在冬、春季以细颗粒态为主, 夏、秋季以粗颗粒态为主, 细颗粒态NO3-和Cl-的半挥发特性是导致不同季节的粒径分布发生变化的主要原因.
3) 上海大气颗粒物中SO42-的峰值粒径由夏季的0.32~0.56 μm逐渐转变为冬季的0.56~1.0 μm, 说明夏季SO42-的形成机制以气相/非均相反应为主, 冬季以云过程为主;气相/非均相反应相对云过程的贡献为:夏季>秋季>春季>冬季, 与大气温度的季节变化一致.
4) 上海大气颗粒物除夏季外整体呈微弱酸性或中性, 其中, 0.32~3.2 μm粒径段的颗粒呈明显的酸性;0.056~0.32 μm粒径段的细颗粒阴离子/阳离子比值明显小于1.0, 且粒径越小, 比值越低, 未被测定的有机酸的存在可能是原因之一.
5) 冬、春季时 < 1.8 μm的细颗粒物中SO42-/NO3-比值小于1, 说明移动源排放对上海大气细颗粒物的贡献可能已超过固定源;但不同粒径、不同季节的SO42-/NO3-比值受NO3-挥发性的影响显著, 利用SO42-/NO3-比值判断大气颗粒物来源时需要充分考虑NO3-挥发性的影响.
Anlauf K, Li S, Leaitch R, et al. 2006. Ionic composition and size characteristics of particles in the Lower Fraser Valley: Pacific 2001 field study[J]. Atmospheric Environment, 40(15): 2662–2675.
DOI:10.1016/j.atmosenv.2005.12.027
|
Arimoto R. 1996. Relationships among aerosol constituents from Asia and the North Pacific during Pem-West area[J]. Journal of Geophysical Research, 101(D1): 2011–2023.
DOI:10.1029/95JD01071
|
Cabada J C, Rees S, Takahama S, et al. 2004. Mass size distributions and size resolved chemical composition of fine particulate matter at the Pittsburgh supersite[J]. Atmospheric Environment, 38(20): 3127–3141.
DOI:10.1016/j.atmosenv.2004.03.004
|
Calvo A I, Alves C, Castro A, et al. 2013. Research on aerosol sources and chemical composition:past, current and emerging issues[J]. Atmospheric Research, 120-121: 1–28.
DOI:10.1016/j.atmosres.2012.09.021
|
Fan J, Zhang R. 2004. Atmospheric oxidation mechanism of isoprene[J]. Environmental Chemistry, 1(3): 140–149.
DOI:10.1071/EN04045
|
Fan J, Zhang R, Collins D, et al. 2006. Contribution of secondary condensable organics to new particle formation:A case study in Houston, Texas[J]. Geophysical Research Letters, 33(15): 483–507.
|
Han Y M, Cao J J, Lee S C, et al. 2013. Different characteristics of char and soot in the atmosphere and their ratio as an indicator for source identification in Xi′an, China[J]. Atmospheric Chemistry & Physics, 10(2): 595–607.
|
Huebert B J, Wang M X, Lü W X, et al. 1988. Atmospheric nitrate, sulfate, ammonium and calcium concentrations in China[J]. Tellus, 40(B): 260–269.
|
Kang E, Han J, Lee M, et al. 2013. Chemical characteristics of size-resolved aerosols from Asian dust and haze episode in Seoul Metropolitan City[J]. Atmospheric Research, 127: 34–46.
DOI:10.1016/j.atmosres.2013.02.002
|
Kim B M, Teffera S, Zeldin D, et al. 2000. Characterization of PM2.5 and PM10 in the south coast Air Basin of Southern California:Part 1-spatial variations[J]. Journal of the Air and Waste Management Association, 50(12): 2034–2044.
DOI:10.1080/10473289.2000.10464242
|
刘臻, 祁建华, 王琳, 等. 2012. 青岛大气气溶胶水溶性无机离子的粒径分布特征[J]. 中国环境科学, 2012, 32(8): 1422–1432.
DOI:10.3969/j.issn.1000-6923.2012.08.012 |
Lanz V A, Prévôt A S H, Alfarra M R, et al. 2010. Characterization of aerosol chemical composition with aerosol mass spectrometry in Central Europe:an overview[J]. Atmospheric Chemistry & Physics, 10(21): 10453–10471.
|
Liang X, Zou T, Guo B, et al. 2015. Assessing Beijing′s PM2.5 pollution:severity, weather impact, APEC and winter heating[J]. Proceedings of the Royal Society A Mathematical Physical & Engineering Sciences, 471(2182): 2182–2187.
|
Meng Z, Seinfeld J H. 1994. On the source of the submicrometer droplet mode of urban and regional aerosols[J]. Aerosol Science and Technology, 20(3): 253–265.
DOI:10.1080/02786829408959681
|
Ondov J M, Wexler A S. 1998. Where do particulate toxins reside? An improved paradigm for the structure and dynamics of the urban mid-Atlantic aerosol[J]. Environmental Science and Technology, 32(17): 2547–2555.
DOI:10.1021/es971067y
|
Seinfeld J H, Pandis S N. 2006. Atmospheric Chemistry and Physics, from Air Pollution to Climate Change(2nd edition)[M]. New Jersey: John Wiley and Sons, Inc: 211–219.
|
Tang G, Zhang J, Zhu X, et al. 2016. Mixing layer height and its implications for air pollution over Beijing, China[J]. Atmospheric Chemistry & Physics, 16(4): 2459–2475.
|
Tao Y, Yin Z, Ye X N, et al. 2014. Size distribution of water-soluble inorganic ions in urban aerosols in Shanghai[J]. Atmospheric Pollution Research, 5(4): 639–647.
DOI:10.5094/APR.2014.073
|
Tian S L, Pan Y P, Liu Z R, et al. 2014. Size-resolved aerosol chemical analysis of extreme haze pollution events during early 2013 in urban Beijing, China[J]. Journal of Hazardous Materials, 279: 452–460.
DOI:10.1016/j.jhazmat.2014.07.023
|
Wang G H, Zhou B H, Cheng C L, et al. 2013. Impact of Gobi desert dust on aerosol chemistry of Xi′an, inland China during spring 2009:differences in composition and size distribution between the urban ground surface and the mountain atmosphere[J]. Atmospheric Chemistry & Physics, 13(2): 819–835.
|
Wang H, An J, Shen L, et al. 2014. Mechanism for the formation and microphysical characteristics of submicron aerosol during heavy haze pollution episode in the Yangtze River Delta, China[J]. Science of the Total Environment, 490: 501–508.
DOI:10.1016/j.scitotenv.2014.05.009
|
Wang Y, Zhuang G S, Zhang X Y, et al. 2006. The ion chemistry, seasonal cycle, and sources of PM2.5 and TSP aerosol in Shanghai[J]. Atmospheric Environment, 40(16): 2935–2952.
DOI:10.1016/j.atmosenv.2005.12.051
|
Xiu G L, Zhang D N, Chen J Z, et al. 2004. Characterization of major water-soluble inorganic ions in size-fractionated particulate matters in Shanghai campus ambient air[J]. Atmospheric Environment, 38(2): 227–236.
DOI:10.1016/j.atmosenv.2003.09.053
|
Yao X H, Chan C K, Fang M, et al. 2002. The water-soluble ionic composition of PM2.5 in Shanghai and Beijing, China[J]. Atmospheric Environment, 36(26): 4223–4234.
DOI:10.1016/S1352-2310(02)00342-4
|
Yao X H, Lau A P S, Fang M, et al. 2003. Size distributions and formation of ionic species in atmospheric particulate pollutants in Beijing, China:1-inorganic ions[J]. Atmospheric Environment, 37(21): 2991–3000.
DOI:10.1016/S1352-2310(03)00255-3
|
Ye B M, Ji X L, Yang H Z, et al. 2003. Concentration and chemical composition of PM2.5 in Shanghai for a 1-year period[J]. Atmospheric Environment, 37(4): 499–510.
DOI:10.1016/S1352-2310(02)00918-4
|
于丽敏, 祁建华, 孙娜娜, 等. 2007. 南、黄海及青岛地区大气气溶胶中无机氮组分的研究[J]. 环境科学学报, 2007, 27(2): 319–325.
DOI:10.3321/j.issn:0253-2468.2007.02.023 |
Zhuang H, Chan C K, Fang M, et al. 1999. Formation of nitrate and non-sea-salt sulfate on coarse particles[J]. Atmospheric Environment, 33(26): 4223–4233.
DOI:10.1016/S1352-2310(99)00186-7
|
 2019, Vol. 39
2019, Vol. 39


