2. 中国地质大学(北京)水资源与环境学院, 北京 100083
2. School of Water Resources and Environment, China University of Geosciences(Beijing), Beijing 100083
金属铬(Cr)主要来自制革、电镀等工业生产过程, 是工业废料场地中的一种常见污染物, 其污染范围可涉及地表水、土壤及地下水(Fu et al., 2015; Jia et al., 2018; Su et al., 2016).环境中存在六价铬(Cr(Ⅵ))和三价铬(Cr(Ⅲ))两种稳定的氧化状态, 且前者比后者毒性更大, 致畸、致癌、致突变能力和流动性更强(Hu et al., 2010; Zou et al., 2019).因此, 世界卫生组织对饮用水中Cr(Ⅵ)水平进行了限制, 最大允许浓度为0.05 mg·L-1 (Veerakumar et al., 2017).将Cr(Ⅵ)转化为Cr(Ⅲ)是最常用的铬污染治理手段, 对含铬废水的处理主要有化学沉淀、吸附、电解、膜分离、光催化等方法(辛梓弘等, 2017).
纳米零价铁(nZVI)对多种污染物有较强的去除效率, 相关研究也日益受到人们的广泛关注.作为纳米材料, nZVI巨大的比表面积及表面能可以促使污染物吸附到其表面, 同时基于铁自身极高的氧化还原活性可使有机污染物分解或者无机污染物发生价态转换(Xin et al., 2018; Zhang et al., 2018c).目前, 文献已报道过多种基于nZVI的铬去除方法(Zou et al., 2019), 发现nZVI对Cr(Ⅵ)的去除通常通过吸附、还原及共沉淀几个步骤来进行(Li et al., 2008).零价铁极强的反应活性在提供高去除效率的同时也给其实际应用带来了诸多问题, 如极易氧化和团聚等(Tian et al., 2018; Zhang et al., 2018a).
表面活性剂可以对水中的固体颗粒起到分散作用(Mao et al., 2015), 基于其亲水基离子电荷的不同分为非离子型、阳离子型、阴离子型及两亲型表面活性剂(Lamichhane et al., 2017).聚乙烯吡咯烷酮(PVP)是一种常用的非离子型表面活性剂, 有报道称PVP可以增强nZVI的分散性, 提高反应活性(Chen et al., 2011).油酸钠(NaOA)是一种阴离子型表面活性剂, 李铁龙等(2008)研究了NaOA对nZVI的修饰作用, 结果表明, 油酸钠的修饰便于隔绝空气, 可以使材料有更好的稳定性.
本研究旨在通过PVP和NaOA的共同修饰, 制备稳定性及活性更高的纳米零价铁, 并用于水中Cr(Ⅵ)的去除.同时, 在不同pH值、材料的干湿状态、初始浓度及共存离子条件下进行反应, 研究反应动力学及25 ℃等温线的模型拟合效果, 并结合反应前后XRD、XPS等表征手段揭示反应机理.以期为分析nZVI系列材料原位处理含铬污水的可行性提供理论支持.
2 实验部分(Experiment) 2.1 主要试剂PVP-K30、NaOA、NaBH4购于上海阿拉丁生化科技股份有限公司, FeSO4·7H2O、K2Cr2O8购于国药集团化学试剂有限公司, 无水乙醇、NaOH、37%HCl、NaCl、NaHCO3、Na2SO4、NaNO3、CaCl2、MgCl2等购于北京化工厂.实验用水使用实验室自制去离子水.
2.2 实验设备实验过程中所用到的仪器设备主要有机械搅拌器(J-J1, 江苏科析仪器有限公司)、冷冻干燥机(FDU-1200, 东京理化器械株式会社)、恒温水浴振荡器(THZ-82A, 江苏科析仪器有限公司)、紫外可见分光光度计(DR6000, 哈希水质分析仪器(上海)有限公司)、扫描电子显微镜(Merlin Compact, 德国卡尔·蔡司股份公司)、透射电子显微镜(JEM-2100 LaB6, 日本电子株式会社)、能谱检测器(Trident XM4, 美国伊达克斯有限公司)、X射线衍射仪(D/max-2550, 德国布鲁克公司)、X射线光电子能谱(250XL, 美国赛默飞世尔科技公司)、电感耦合等离子体发射光谱仪(Optima8000, 美国铂金埃尔默股份有限公司)等.
2.3 材料合成及表征本实验选择硼氢化钠液相还原法作为纳米零价铁的基本合成方法(Mukherjee et al., 2016), 并对传统的合成方法做了修改.具体操作如下:①配置反应溶液, A液:0.1 mol·L-1 FeSO4溶液(水:乙醇=7:3, V/V) 40 mL, 超声溶解5 min;B液:0.5 mol·L-1 NaBH4溶液(水:乙醇=7:3, V/V)20 mL, 搅拌溶解;②将A液盛于250 mL三口圆底烧瓶中, B液盛于25 mL恒压滴液漏斗中, 机械搅拌转速400 r·min-1, A液通氮气, 将B液以1滴·s-1的速度滴加于A液中, 待滴加完毕后继续搅拌20 min;③在氮气保护下, 对材料磁分离并进行清洗, 采用无水乙醇及除氧去离子水分别清洗2遍, 最后置于冷冻干燥机中进行干燥, 如此合成的零价铁记为nZVI.同时应用相同的方法制备有表面活性剂修饰的nZVI(PVP及NaOA共同修饰), 分别在A、B液中添加0.1 g PVP和0.1 g NaOA, 由此制备出的材料记为nZVI-PN.为对比干湿材料的不同, 将一部分nZVI及nZVI-PN未经干燥保存在除氧水中配置成10 mg·mL-1的悬液, 在4 ℃冰箱保存.干燥后的材料分别记为D-nZVI和D-nZVI-PN, 湿样分别记为W-nZVI和W-nZVI-PN.文中未特别说明的均为干燥后样品.
材料通过扫描电子显微镜(SEM)进行形貌分析, 并利用XRD及XPS进行反应前后材料成分的确定和对比.
2.4 去除铬实验去除反应在100 mL带盖螺口玻璃瓶中进行, 盖内覆锡纸.在50 mL 80 mg·L-1 Cr(Ⅵ)溶液中加入20 mg材料, 在150 r·min-1、25 ℃的恒温水浴振荡器中振荡4 h, 磁分离或者过0.2 μm滤膜后取上清液用分光光度计进行测定.根据反应前后目标物浓度的变化由方程(1)计算单位去除量(Qt)及去除效率(η).
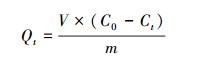
|
(1) |
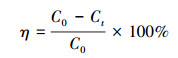
|
(2) |
式中, Qt为材料在t时间内对Cr(Ⅵ)的单位去除量(mg·g-1), C0为Cr(Ⅵ)初始浓度(mg·L-1), Ct为t时刻溶液中Cr(Ⅵ)的浓度(mg L-1), V为溶液体积(mL), m为材料的质量(g).
检测条件如下:Cr(Ⅵ)采用二苯碳酰二肼分光光度法, 在540 nm处进行测定;测定反应后的总铬时, 将溶液静置沉淀2 h, 取上清液采用电感耦合等离子体光谱仪进行测定.
3 结果与讨论(Results and discussion) 3.1 材料的表征 3.1.1 SEM分析纳米材料的表面形貌可以一定程度上反映材料颗粒的大小、形状、分散程度等信息.图 1a所示为nZVI的SEM图像, 图 1b为表面活性剂修饰后nZVI-PN的SEM图像.可以看出, 材料粒径基本在100 nm以内, 平均约为50~60 nm.经表面活性剂PVP和油酸钠修饰后的零价铁外形表现出较大改变:纯nZVI颗粒呈球状, 表现出典型的链状团聚;添加PVP及NaOA后的材料形貌有了较大变化, 不再呈现链状团聚, 分散性增强, 且颗粒表现为很多小颗粒的团簇状聚集体, 或许此结构能增强反应活性.
 |
| 图 1 nZVI(a)和nZVI-PN(b)的SEM图 Fig. 1 SEM images of nZVI(a) and nZVI-PN(b) |
图 2a显示了nZVI、nZVI-PN及nZVI-PN反应后样品的XRD谱图.从图中可以看出, nZVI在44.5°、65°、82.3°处表现出明显的零价铁特征峰, 35°处存在一个不明显的Fe3O4特征峰.nZVI-PN及其去除铬反应后的材料峰位置及强度极为相似, 均有弱的零价铁特征峰(44.5°)及铁氧化物特征峰(62°), 证明样品均有一定程度的氧化, 但仍未氧化完全(Li et al., 2013a).或许由于反应生成的产物不具有明显的晶型结构或者最终附着在材料表面上的量很少, 故而在反应前后看不到明显的谱峰变化.
 |
| 图 2 反应前后材料的XRD(a)和XPS(b、c)谱图 Fig. 2 XRD patterns (a) and XPS spectra (b, c) of nZVI before and after Cr reaction |
对反应前后的材料进行XPS分析, 从图 2b可以看出, 反应后的材料表面出现了铬的特征峰(结合能在577 eV附近), 证明反应后会有一部分铬吸附或者沉淀附着于材料表面.结合图 2c铬的XPS高分辨谱图, 对比反应前后Cr特征峰的明显差异, 更证明了反应后铬在材料表面的存在, 并拟合出铬均处于三价状态(577.6 eV处的Cr 2p3/2特征峰及587.3 eV处的Cr 2p1/2特征峰), 此时溶液中Cr(Ⅵ)的去除率在95%以上, 因此可以推断Cr(Ⅵ)几乎全部转化为Cr(Ⅲ)(Xu et al., 2018).对材料表面铁的含量进行对比分析, 发现反应后铁的原子百分比由22.28%降到了16.21%, 这可能与铬的附着和铁反应后的溶出有关, 在一定程度上证明了去除Cr(Ⅵ)过程中零价铁参与了氧化还原反应(Olea-Mejía et al., 2017; Xu et al., 2018; Zhang et al., 2018b).
3.2 去除Cr(Ⅵ)效果研究 3.2.1 不同pH值的影响分析如图 3所示, 酸性条件大大提高了铬的去除率, 尤其在pH=2条件下去除效率达到了95.35%.首先, 从表面电荷的角度考虑, 有研究表明, 在pH=1~6范围内Cr(Ⅵ)的主要存在状态是HCrO4-, 随着pH值的升高, 该物种逐渐被CrO42-取代, 但电荷仍为负电, 且HCrO4-由于具有更低的吸附自由能, 与CrO42-相比更利于吸附去除(Pang et al., 2011; Xu et al., 2018).有研究表明, 零价铁类材料的等电点约为pH=7.1(Li et al., 2016).等电点以下材料表面带正电荷, 这与同pH值下Cr(Ⅵ)的离子状态刚好相反, 利于材料与污染物的接触, 从而可实现进一步的去除反应.随着pH的升高, CrO42-与带负电荷的材料表面之间的静电斥力越来越强, 导致Cr(Ⅵ)的去除率降低.其次, 从pH值对材料本身的影响来看, nZVI在酸性条件下更容易释放出还原性电子, 促进Cr(Ⅵ)的去除和向低价态的转化;而当体系处于碱性环境时, 铁材料表面容易生成Fe(OH)3、Fe3O4等铁氧化物/氢氧化物沉淀, 从而产生钝化效应(吴敏蓉等, 2018).
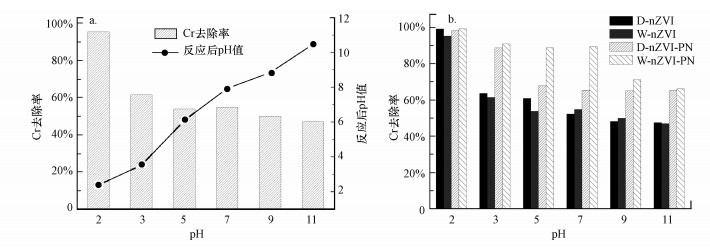 |
| 图 3 溶液pH(a)、材料干湿状态及表面活性剂修饰前后(b)对Cr(Ⅵ)去除效果的影响 Fig. 3 The effect of solution pH (a), material status and the surfactant modification (b) on the removal of Cr(Ⅵ) |
图 3a也展示了材料反应后溶液pH值的变化情况, 发现均有所升高.分析反应过程中溶液中的H+参与了反应, 使得体系pH值升高, 这与前人的研究结果相似(Zou et al., 2019).
3.2.2 不同材料的对比分析由图 3b可知, 表面活性剂的添加对去除效率起到促进作用, pH=2条件下每种材料都能保持95%以上的去除效率, 同种干湿状态下表面活性剂的修饰明显增强了nZVI对水中铬的去除率, 其中, 双表面活性剂修饰的零价铁湿样W-nZVI-PN在非碱性条件下即能保持约90%及以上的去除效率.pH=7条件下对湿样而言, nZVI的去除率仅为nZVI-PN的73.21%, 对于干样, 表面活性剂的修饰仍能使去除率提高约5%.结合电镜图片分析可知, nZVI-PN的优异去除性能或许与其分散度有关, 这也证明了PVP和NaOA对nZVI的修饰存在着协同促进作用.
对于同种材料而言, 不同的干湿状态又有着较大的差别, 整体表现为湿样比干样反应活性更强、去除率更高.干燥后的材料除在pH=2条件下还能保持大于99%的较高的去除效率外, 其余pH条件下去除效率均大大降低, 尤其在中性条件下去除效率下降了34.55%.对于双表面活性剂修饰的nZVI, 湿样在酸、中性条件下显示出不低于88.9%的去除效率.其粉末样品随着pH值的增高去除效率明显降低, pH=3条件即下降到60%.分析原因为在干燥的过程中加剧了材料的硬团聚, 并且干燥处理更容易引起材料的氧化.
3.2.3 初始浓度的影响及等温线拟合本文进行了2 h内nZVI-PN样品在不同初始浓度下去除Cr(Ⅵ)效率的对比, 结果如图 4a所示.在不超过40 mg·L-1的浓度下, 材料在2 h内对Cr(Ⅵ)的去除率达到90%以上, 随着初始浓度的升高去除效率逐步下降, 120 mg·L-1时的去除率仅为48.35%, 单位去除量在80 mg·L-1浓度下达到最大, 为153.80 mg·g-1.这一现象与张永祥等的(2018)研究结果一致.分析80 mg·L-1浓度以上单位去除量有所降低的原因, 可能是随着Cr(Ⅵ)浓度的增大, 反应钝化产物增多, 其在表面的沉积抑制了反应的进行.
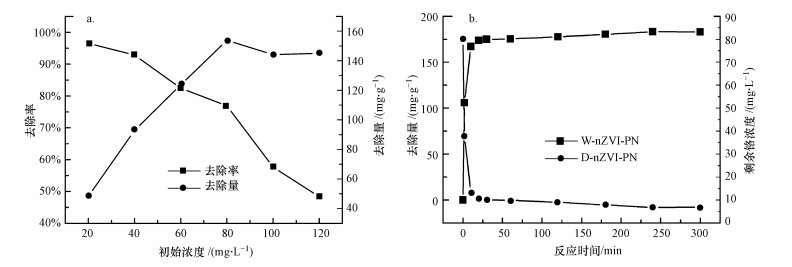 |
| 图 4 初始浓度对Cr(Ⅵ)去除效果的影响(a)及动力学曲线(b) Fig. 4 The effect of initial concentration on the removal of Cr(Ⅵ) (a) and reaction kinetic curves(b) |
对此条件下的结果进行等温线拟合(图 4b), 结果发现, Langmuir模型更能诠释nZVI-PN去除Cr(Ⅵ)的反应过程, R2为0.999(表 1).这说明nZVI-PN对水中Cr(Ⅵ)的吸附是单层吸附, 材料表面活性位点均匀分布(Liu et al., 2017).Freundlich模型中的1/n值可以体现反应的难易程度, 通常1/n越小表明反应越容易进行, 当1/n在0~0.5之间时, 说明反应极易进行(Boparai et al., 2011; Yu et al., 2013).本实验中nZVI-PN拟合的1/n为0.243, 为易于反应的体系.
| 表 1 等温线模型参数(25 ℃) Table 1 Parameters of isotherm models (25 ℃) |
采用动力学实验来考察吸附决速步骤.实验在25 ℃下进行, Cr(Ⅵ)初始浓度设定为80 mg·L-1, 材料使用量为20 mg, 在2~300 min内的不同时间点分别取样测定上清液剩余目标物浓度.数据拟合采用两种常用的动力学模型:准一级动力学模型(式(3))、准二级动力学模型(式(4))(Karthik et al., 2014).
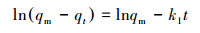
|
(3) |
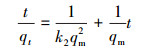
|
(4) |
式中, t为反应时间(min), k1(min-1)和k2(g·mg-1·min-1)分别是准一级、准二级动力学模型的速率常数, qm和qt分别是最大单位去除量(mg·g-1)和在t时间的去除量(mg·g-1), C为常数.
结果发现, 在实验条件下(pH=2), 干材料去除铬在3 h内可达到平衡, 且去除率大于90%(图 4b);而湿材料在2 min时的去除率即可达到99%以上.拟合动力学模型发现, 该过程符合准二级动力学方程, R2=0.999, 干、湿材料在实验条件下计算得到的最大单位去除量分别为185.19 mg·g-1和200 mg·g-1, 与实测值相吻合.有研究称准二级动力学模型表示反应的决速步骤是化学吸附过程(Li et al., 2014), 这与XRD及XPS的分析结果一致, 表明过程中发生了化学变化.
但值得注意的是, 在总铬浓度的分析中发现, 反应后静置的上清液中总铬的浓度仍然较高, 分别为71.2 mg·L-1(干样)和71.9 mg·L-1(湿样), 接近于Cr(Ⅵ)的初始浓度, 这也是一个六价铬转化为其他价态的有力证据.但遗憾的是, nZVI-PN材料几乎没能将转化的Cr(Ⅲ)固定于固相, 这一现象也有助于解释XRD中未发现明显含铬物质的特征峰.这可能与强酸性条件有关, 强酸性条件下不利于产物的固定.
3.2.5 共存离子的影响分析本研究同时考察了在pH=2、25 ℃及0.3 g·L-1 nZVI-PN条件下添加HCO3-、NO3-、SO42-、Cl-、Ca2+、Mg2+等6种离子对Cr(Ⅵ)去除的影响.以上离子的添加量控制为与溶液中的Cr(Ⅵ)等物质的量(1.538 mmol·L-1).图 5结果显示, 这6种离子在实验条件下均未表现出明显的对Cr(Ⅵ)去除的抑制或促进作用.这一现象与Lv等(2013)的结论不同, 他们考察了pH=8时NZVI-Fe3O4复合材料在Ca2+、Cu2+、Zn2+、Cd2+、Mg2+存在下对Cr(Ⅵ)的去除效果, 发现这些阳离子均对Cr(Ⅵ)去除有不同程度的促进作用.分析这一差别可能源于pH设定的不同, 在弱碱性条件下零价铁材料通常带负电荷, 而Cr(Ⅵ)的存在状态也是负离子CrO42-, 静电斥力使得反应难以进行.在此条件下其他阳离子的加入可以中和材料表面部分负电荷, 减小了静电斥力.当pH下降至等电点以下时, 尤其是在强酸性环境, 材料表面与Cr(Ⅵ)(通常为HCrO4-)本身就携带相反的电荷, 共存阳离子的促进机制也就不复存在.Lv等(2013)还考察了几种阴离子的影响, 发现高浓度SO42-和NO3-对Cr(Ⅵ)去除有促进作用, 而高浓度HCO3-和PO43+有抑制作用.理论上讲, 阴离子与Cr(Ⅵ)应该存在竞争吸附的关系, 但实验条件下并没有发现明显的影响, 这可能与共存离子浓度设定有关, 相等物质的量的阴离子并不足以影响nZVI-PN材料对Cr(Ⅵ)的去除.
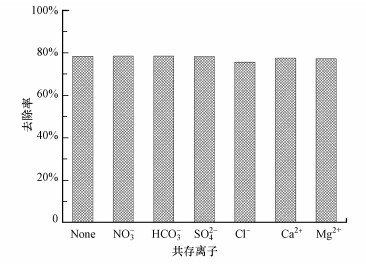 |
| 图 5 共存离子对去除效果的影响 Fig. 5 The effect of co-existing ions on the removal of Cr(Ⅵ) |
综合以上实验现象, 发现未经干燥的PVP和油酸钠共同修饰的零价铁nZVI-PN对Cr(Ⅵ)有着较高的去除效率及单位去除量, 干燥过程抑制了材料的反应活性.XRD及XPS分析结果表明, Cr(Ⅵ)已基本上完全转化为Cr(Ⅲ).酸性条件有利于反应的进行, 表明了氢离子的贡献作用.酸性条件可能具有以下三方面的贡献:①酸性条件使得材料带来表面带正电荷, 这种与Cr(Ⅵ)相反的电荷促使材料对HCrO4-产生静电吸引, 更易于接触到污染物本身;②可能有助于干燥后材料表面钝化层的瓦解, 释放活性位点(粉末状材料在强酸性条件下的去除率也可以达到99%);③直接作用于与Cr(Ⅵ)的反应过程, 提供反应所需的H+.
结合实验结果及前人的实验经验, 推断反应过程从前到后应包括对Cr(Ⅵ)的吸附、还原及产物固定作用.在还原过程中推测存在如下的反应:
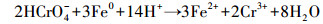
|
(5) |
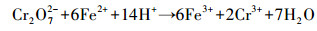
|
(6) |
表 2显示了nZVI-PN与其他类似基于零价铁的材料在去除水中Cr(Ⅵ)效果的对比, 发现本研究在较低投加量下材料具有较高的单位去除量.且相对来说, 材料制备过程简单、原料廉价易得.虽然在酸性条件下材料的表现更突出, 但在中性条件下仍有着较高的单位去除量(109.7 mg·g-1), 实际应用价值高.
| 表 2 不同材料去除铬效果比较 Table 2 The capacity comparison of different materials in Cr(Ⅵ) removal |
nZVI作为一类具有极强吸附还原活性的环境修复材料, 经常用于水中污染物质的去除, PVP-NaOA双表面活性剂对nZVI的修饰起到优化水中Cr(Ⅵ)去除的作用.实验表明, 酸性条件在反应中起到重要的促进作用, 样品干燥前反应活性更强.反应符合准二级动力学及Langmuir模型, 反应过程中Cr(Ⅵ)基本全部转化为Cr(Ⅲ), 推测该过程包括了Cr(Ⅵ)的吸附、还原及固定作用.这种简单的表面活性剂修饰的零价铁材料, 具有制备原料廉价易得、操作过程简单、污染物去除效果较强等特点, 因而具有广阔的应用前景.
5 展望(Prospect)nZVI-PN材料在表现出优异性能的同时也存在一些问题, 对此提出以下展望:①可以考虑材料与其他基质的结合, 增强反应后铬的固定效果, 减少溶出;②在解决产物溶出的基础上, 进一步优化中性条件下的去除效果, 并利用实际水样进行实验, 为材料的原位合成及污染场地修复应用提供理论依据.
Boparai H K, Joseph M, O'Carroll D M. 2011. Kinetics and thermodynamics of cadmium ion removal by adsorption onto nano zerovalent iron particles[J]. Journal of Hazardous Materials, 186(1): 458–465.
DOI:10.1016/j.jhazmat.2010.11.029
|
Chen H, Luo H, Lan Y, et al. 2011. Removal of tetracycline from aqueous solutions using polyvinylpyrrolidone (PVP-K30) modified nanoscale zero valent iron[J]. Journal of Hazardous Materials, 192(1): 44–53.
|
Fu R, Yang Y, Xu Z, et al. 2015. The removal of chromium(Ⅵ) and lead(Ⅱ) from groundwater using sepiolite-supported nanoscale zero-valent iron (S-NZVI)[J]. Chemosphere, 138: 726–734.
DOI:10.1016/j.chemosphere.2015.07.051
|
Han J, Zhang G, Zhou L, et al. 2018. Waste carton-derived nanocomposites for efficient removal of hexavalent chromium[J]. Langmuir, 34(21): 5955–5963.
DOI:10.1021/acs.langmuir.8b00225
|
Hu C, Lo S, Liou Y, et al. 2010. Hexavalent chromium removal from near natural water by copper-iron bimetallic particles[J]. Water Research, 44(10): 3101–3108.
DOI:10.1016/j.watres.2010.02.037
|
Jia Z, Shu Y, Huang R, et al. 2018. Enhanced reactivity of nZVI embedded into supermacroporous cryogels for highly efficient Cr(Ⅵ) and total Cr removal from aqueous solution[J]. Chemosphere, 199: 232–242.
DOI:10.1016/j.chemosphere.2018.02.021
|
Karthik R, Meenakshi S. 2014. Removal of hexavalent chromium ions using polyaniline/silica gel composite[J]. Journal of Water Process Engineering, 1: 37–45.
DOI:10.1016/j.jwpe.2014.03.001
|
Lamichhane S, Bal Krishna, K C, Sarukkalige R. 2017. Surfactant-enhanced remediation of polycyclic aromatic hydrocarbons:A review[J]. Journal of Environmental Management, 199: 46–61.
|
Li X, Cao J, Zhang W. 2008. Stoichiometry of Cr(Ⅵ) immobilization using nanoscale zerovalent iron (nZVI):A study with high-resolution X-ray photoelectron spectroscopy (HR-XPS)[J]. Industrial & Engineering Chemistry Research, 47(7): 2131–2139.
|
Li J, Wu Y, Li Z, et al. 2014. Zeolitic imidazolate framework-8 with high efficiency in trace arsenate adsorption and removal from water[J]. The Journal of Physical Chemistry C, 118(47): 27382–27387.
DOI:10.1021/jp508381m
|
Li X, Ai L, Jiang J. 2016. Nanoscale zerovalent iron decorated on graphene nanosheets for Cr(Ⅵ) removal from aqueous solution:Surface corrosion retard induced the enhanced performance[J]. Chemical Engineering Journal, 288: 789–797.
DOI:10.1016/j.cej.2015.12.022
|
Liu P, Yuan N, Xiong W, et al. 2017. Removal of nickel(Ⅱ) from aqueous solutions using synthesized β-zeolite and its ethylenediamine derivative[J]. Industrial & Engineering Chemistry Research, 56(11): 3067–3076.
|
李铁龙, 王丹, 金朝晖, 等. 2008. 油酸钠/Fe纳米粒子的制备及其脱氯性能研究[J]. 功能材料, 2008(8): 1385–1388.
DOI:10.3321/j.issn:1001-9731.2008.08.043 |
Lv X, Hu Y, Tang J, et al. 2013. Effects of co-existing ions and natural organic matter on removal of chromium (Ⅵ) from aqueous solution by nanoscale zero valent iron (nZVI)-Fe3O4 nanocomposites[J]. Chemical Engineering Journal, 218: 55–64.
DOI:10.1016/j.cej.2012.12.026
|
Mao X, Jiang R, Xiao W, et al. 2015. Use of surfactants for the remediation of contaminated soils:A review[J]. Journal of Hazardous Materials, 285: 419–435.
DOI:10.1016/j.jhazmat.2014.12.009
|
Mukherjee R, Kumar R, Sinha A, et al. 2016. A review on synthesis, characterization, and applications of nano zero valent iron (nZVI) for environmental remediation[J]. Critical Reviews in Environmental Science and Technology, 46(5): 443–466.
DOI:10.1080/10643389.2015.1103832
|
Olea-Mejía O, Cabral-Prieto A, Salcedo-Castillo U, et al. 2017. Orange peel+nanostructured zero-valent-iron composite for the removal of hexavalent chromium in water[J]. Applied Surface Science, 423: 170–175.
DOI:10.1016/j.apsusc.2017.06.173
|
Pang Y, Zeng G, Tang L, et al. 2011. Preparation and application of stability enhanced magnetic nanoparticles for rapid removal of Cr(Ⅵ)[J]. Chemical Engineering Journal, 175: 222–227.
DOI:10.1016/j.cej.2011.09.098
|
Qian L, Zhang W, Yan J, et al. 2017. Nanoscale zero-valent iron supported by biochars produced at different temperatures:Synthesis mechanism and effect on Cr(Ⅵ) removal[J]. Environmental Pollution, 223: 153–160.
DOI:10.1016/j.envpol.2016.12.077
|
Su H, Fang Z, Tsang P E, et al. 2016. Stabilisation of nanoscale zero-valent iron with biochar for enhanced transport and in-situ remediation of hexavalent chromium in soil[J]. Environmental Pollution, 214: 94–100.
DOI:10.1016/j.envpol.2016.03.072
|
Tian H, Liang Y, Zhu T, et al. 2018. Surfactant-enhanced PEG-4000-NZVI for remediating trichloroethylene-contaminated soil[J]. Chemosphere, 195: 585–593.
DOI:10.1016/j.chemosphere.2017.12.070
|
Veerakumar P, Thanasekaran P, Lin K C, et al. 2017. Biomass derived sheet-like carbon/palladium nanocomposite:An excellent opportunity for reduction of toxic hexavalent chromium[J]. Acs Sustainable Chemistry & Engineering, 5(6): 5302–5312.
|
吴敏蓉, 马邕文, 万金泉, 等. 2018. nZVI@mesoSiO2的可控合成及应用性能研究[J]. 环境科学学报, 2018, 38(12): 4652–4662.
|
辛梓弘, 凡小梅, 倪海晨, 等. 2017. 纳米零价铁的制备及其对废水中铬的去除作用研究[J]. 广州化工, 2017, 45(11): 74–76.
DOI:10.3969/j.issn.1001-9677.2017.11.030 |
Xin J, Tang F, Yan J, et al. 2018. Investigating the efficiency of microscale zero valent iron-based in situ reactive zone (mZVI-IRZ) for TCE removal in fresh and saline groundwater[J]. Science of the Total Environment, 626: 638–649.
DOI:10.1016/j.scitotenv.2018.01.115
|
Xu C, Yang W, Liu W, et al. 2018. Performance and mechanism of Cr(Ⅵ) removal by zero-valent iron loaded onto expanded graphite[J]. Journal of Environmental Sciences, 67: 14–22.
DOI:10.1016/j.jes.2017.11.003
|
Yu F, Wu Y, Ma J, et al. 2013. Adsorption of lead on multi-walled carbon nanotubes with different outer diameters and oxygen contents:Kinetics, isotherms and thermodynamics[J]. Journal of Environmental Sciences, 25(1): 195–203.
DOI:10.1016/S1001-0742(12)60023-0
|
Zhang R, Zhang N, Fang Z. 2018a. In situ remediation of hexavalent chromium contaminated soil by CMC-stabilized nanoscale zero-valent iron composited with biochar[J]. Water Science and Technology, 77(6): 1622–1631.
DOI:10.2166/wst.2018.039
|
Zhang S, Wu M, Tang T, et al. 2018b. Mechanism investigation of anoxic Cr(Ⅵ) removal by nano zero-valent iron based on XPS analysis in time scale[J]. Chemical Engineering Journal, 335: 945–953.
DOI:10.1016/j.cej.2017.10.182
|
Zhang W, Ruan X, Bai Y, et al. 2018c. The characteristics and performance of sustainable-releasing compound carbon source material applied on groundwater nitrate in-situ remediation[J]. Chemosphere, 205: 635–642.
DOI:10.1016/j.chemosphere.2018.04.133
|
张永祥, 马晓敏. 2018. 纳米零价铁去除水中六价铬的研究[J]. 应用化工, 2018, 47(8): 1569–1573.
DOI:10.3969/j.issn.1671-3206.2018.08.003 |
Zhou L, Li R, Zhang G, et al. 2018. Zero-valent iron nanoparticles supported by functionalized waste rock wool for efficient removal of hexavalent chromium[J]. Chemical Engineering Journal, 339: 85–96.
DOI:10.1016/j.cej.2018.01.132
|
Zou H, Hu E, Yang S, et al. 2019. Chromium(Ⅵ) removal by mechanochemically sulfidated zero valent iron and its effect on dechlorination of trichloroethene as a co-contaminant[J]. Science of the Total Environment, 650: 419–426.
DOI:10.1016/j.scitotenv.2018.09.003
|
 2019, Vol. 39
2019, Vol. 39


