铅(Pb)是一种剧毒挥发类痕量污染物, 长时间暴露在铅污染环境下会对人类的视力、心血管、智力发育等造成严重的危害(Zeman, 2012).目前环境中的铅类排放主要源自人类的工农业活动, 譬如:燃油汽车尾气排放、火力发电厂烟气排放、化工产业喷漆释放、农业杀虫剂扩散等(王英等, 2010).其中, 火力发电厂被认为是铅排放量最大的污染源(余岳溪等, 2017), 其总排放量已经达到燃油汽车尾气排放总量的35倍, 因此, 电厂脱铅已成为电力领域亟需解决的问题.
燃煤电厂中不存在专门的脱铅装置, 铅脱除主要依靠电厂脱汞时喷射的活性炭, 以及烟道中未燃尽的焦炭等炭基材料对铅进行吸附处理(Gao et al., 2016).邓双等(2013)采集了6台燃煤电站烟气中铅元素的分布数据, 结果表明, 烟气中80%的铅类污染物最终被吸附在炭基材料的表面, 可以进一步通过静电除尘器或者布袋除尘器有效脱除.烟气中的气体对炭基材料吸附重金属污染物有着显著影响, 高正阳等(Gao et al., 2016)研究了单质铅(Pb0)在活性炭表面的吸附, 并系统探索了NO气体对活性炭吸附单质铅的影响机理, 结果发现, 锅炉烟气中的NO分子可以提高炭基材料吸附Pb0的能力.但烟气中的组分非常复杂, 探究炭基材料对Pb0的吸附还必须充分考虑烟道中其他主要气体及烟气温度对吸附剂吸附Pb0的影响.
SO2是燃煤电厂排放的主要污染物之一, 相关研究表明, 烟道中SO2含量变化范围较大, 其中, 高硫煤燃烧释放出的SO2浓度可达17190 ppm(Park et al., 2019), 远大于锅炉烟气中的NO浓度(200 ppm)(Yang et al., 2018).此外, 由于大部分火电厂脱硫设备安装在除尘器之后, 因此, 在电厂使用活性炭吸附Hg0、Pb0等污染物时, 烟道中的烟气依然处于未脱硫状态, 而在喷射活性炭脱除Hg0和Pb0之前, 大部分NO气体已经被除尘器前的选择性催化还原(SCR)装置脱除.所以相比于NO气体, 研究SO2对活性炭吸附Pb0的影响在指导电厂脱铅方面更有价值.
量子化学方法能够很好地描述有害气体分子在炭基吸附剂表面的吸附特性.Liu等(2012)利用量子化学手段研究了烟气中少量SO2存在对活性炭吸附Hg0的影响, 计算结果显示, SO2的预吸附使炭基材料吸附Hg0的吸附能由-64.6 kJ·mol-1升高到-216.8 kJ·mol-1, 这就从原理上解释了实验中的脱汞效率随SO2含量的增加而升高的原因, 进而说明量子化学方法可视为研究炭基材料吸附重金属污染物的重要手段.基于此, 本研究同样利用量子化学手段结合密度泛函理论系统分析燃煤电站中SO2气体对炭基材料吸附Pb0的影响, 考虑不同的吸附构型, 计算相应构型对应的吸附能、原子间键长、键级等参数, 并对SO2和Pb0在298.15 ~1000 K温度范围内的竞争吸附进行分析.
2 计算理论(Method of calculation) 2.1 理论方法密度泛函理论(DFT)具有计算精度高和机时消耗少等方面的优势, 已经被广泛应用于量子化学计算中(Gao et al., 2017a).本文理论计算采用B3LYP/def2-SVP级别方法及基组的组合进行结构优化, 确定各个吸附结构的稳定构型;使用B3LYP/def2-TZVP进行单点能计算, 以提高能量计算的精度.根据笔者以往的研究(Gao et al., 2018a), B3LYP/def2-SVP方法基组能够很好地确定炭基材料吸附小分子气体的结构构型, B3LYP/def2-TZVP方法基组的组合在单点能计算中可以有效提高炭基吸附重金属污染物的能量计算精度.为了获取零点校正能(ZPE)和吸附体系在不同温度下的热力学参数, 本文在B3LYP/def2-SVP级别进行了频率计算;此外, 为了减少弱相互作用力对吸附结构和能量的影响, 本研究进行了D3色散校正(Grimme et al., 2010; Grimme et al., 2011).
气体分子在活性炭表面的吸附能(Eads)可由以下公式获得(Yang et al., 2019):

|
(1) |
式中, EA+B为吸附后体系的总能量(kJ·mol-1);EA表示炭基材料能量(kJ·mol-1);EB表示被吸附气体的能量(kJ·mol-1).吸附仅在吸附能为负值时发生, 且负值绝对值越大, 吸附效果越好.如果吸附能绝对值小于30 kJ·mol-1, 则吸附作用不稳定, 表示该吸附类型为物理吸附;如果吸附能绝对值大于50 kJ·mol-1, 则吸附作用较稳定, 表示该吸附类型为化学吸附.Mayor键级可以很好地描述原子间成键强度, 键级越接近1, 代表原子间成键强度越大, 键级越接近0, 代表原子间作用力越小(Gao et al., 2018a).
本文计算均基于Gaussian09软件包, 所有的稳定结构均考虑了不同自旋多重度下的基态结构, 波函数分析基于多功能波函数分析软件Multiwfn(Lu et al., 2012).
2.2 模型选择石墨烯型有限苯环簇模型被大量用于活性炭边缘的量子化学模拟.尽管现实中活性炭大小和表面结构多种多样, 但Montoya等(2001)通过固态核磁共振波谱表明炭基材料的吸附活性只与其边缘形状有关, 而与活性炭分子的大小无关.扶手椅型(armchair)模型和锯齿型(zigzag)模型是两种典型的活性炭边缘模型, 其结构能够很好地模拟真实活性炭的边缘结构(Chen et al., 2016), 故本研究同时应用扶手椅型(6苯环)和锯齿型(7苯环)两种活性炭模型, 系统研究锅炉烟气中SO2对活性炭吸附Pb0的影响.大量研究表明, 扶手椅和锯齿型两种活性炭模型在活性炭吸附有害气体的相关研究中具备较强的适用性, 其计算结果与实验现象能够很好地吻合.例如, Shen等(2018)开展了活性炭对H2S气体吸附的理论研究, 发现吸附能高达-664.9 kJ·mol-1;Gao等(2018a)进行了活性炭对As2O3气体吸附的理论研究, 结果表明, 吸附能达到-480.20 kJ·mol-1;Zhang等(2015)针对活性炭吸附NO气体展开了理论研究, 发现NO在活性炭表面的吸附能达到了-178.50 kJ·mol-1, 这与实验中活性炭对H2S(Nguyen-Thanh et al., 2005)、As2O3(López-Antón et al., 2007)、NO(Pedersen et al., 2010)具有良好的吸附效果相吻合.此外, Liu等(2012)利用扶手椅型模型结合量子化学手段研究了SO2对炭基材料吸附Hg0的影响, 成功解释了实验中少量SO2可以提升活性炭吸附Hg0, 但大量SO2会抑制Hg0吸附的原因;赵鹏飞等(2010)利用密度泛函理论研究发现, 氯改性明显提高了活性炭的吸附能力, 从而成功揭示了燃煤电厂利用卤素进行活性炭改性以期达到提高活性炭脱汞效率的机理.鉴于以上报道中理论与实验的吻合度, 本研究认为利用该计算模型得到的结果是可信的.
鉴于活性炭模型在吸附气体研究中展现出的良好适用性, Zhang等(2018)利用锯齿型活性炭模型研究了煤焦中氮的迁移, 并提供了煤焦生成NH3的反应路径;Gao等(2019)利用密度泛函理论研究了4种不同氧化汞团簇在两种活性炭模型上的吸附机理;陈萍等(2019)研究了含氮煤焦还原NO气体分子的反应路径.这些研究从分子层面揭示了化学吸附或者化学反应的微观机理, 有利于人们更深刻地理解化学过程.
经统计, 本文使用的两种模型的C—C平均键长均为1.41 Å, C—C—C平均键角分别为120.22°和120.06°, 这与实验中石墨烯的键长1.42 Å和C—C—C键角120°非常接近(赵鹏飞, 2010), 因此, 本计算选择的方法和基组是合理的.本文通过构建活性炭模型, 并结合量子化学计算方法, 系统研究烟气中SO2对活性炭吸附痕量有害气体Pb0的影响, 以期进一步指导燃煤电厂污染物的脱除.
3 结果分析(Results and discussion) 3.1 活性炭吸附Pb0为了探索SO2对炭基吸附Pb0的影响, 首先需要对炭基边缘吸附Pb0进行研究.本研究尝试对Pb0在活性炭不同位置(凹陷位置与凸起位置)的吸附构型进行结构优化, 其中, 扶手椅型和锯齿型活性炭吸附Pb0的结果见图 1.结果发现, Pb0在活性炭边缘凹陷位置时吸附能最大, 两种活性边缘的吸附能分别达到了-308.16 kJ·mol-1和-426.50 kJ·mol-1, 说明Pb0在活性炭边缘的吸附属于强烈的化学吸附, 从而很好地解释了实验中活性炭对Pb0具有良好吸附效果的原因.根据本课题组以往的研究工作, Mayor键级能够很好地反映活性炭吸附金属痕量元素时化学键的强弱(Gao et al., 2018a).由表 1可知, 铅原子与碳原子之间的Mayor键级在0.816以上, 说明Pb0和活性炭表面的碳原子形成了非常牢固的共价键, 进一步验证了炭基对Pb0吸附的良好效果.
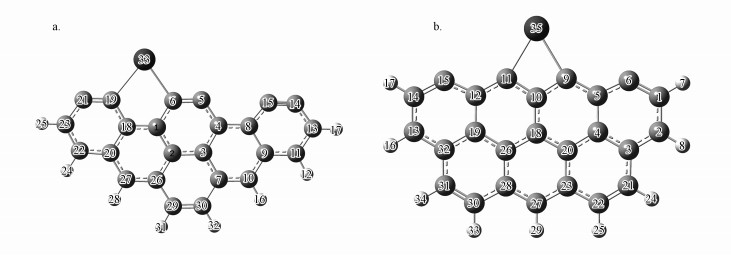 |
| 图 1 活性炭吸附Pb0的最佳构型 (a.扶手椅型, b.锯齿型) Fig. 1 The best adsorption configurations of Pb0 toward activated carbon (a.armchair, b.zigzag) |
| 表 1 气体分子(SO2及Pb0)的吸附参数 Table 1 Adsorption parameters of gases(SO2 and Pb0) |
烟气进入脱硫塔前含有大量的SO2, 且部分SO2会被活性炭吸附, 从而占据一定量的活性炭表面的活性位点, 进而影响汞、铅等痕量元素污染物的脱除.Serre等(2000)发现, 在燃煤电厂燃烧高硫煤时产生的大量SO2会与Hg0蒸汽在活性炭吸附剂表面展开竞争吸附, 因为Hg0惰性强、吸附能低, 难以竞争到吸附剂活性位点, 所以高浓度SO2的存在会对燃煤电厂脱汞工作造成严重阻碍.但有关SO2与Pb0在活性炭表面的吸附关系目前国内外均未见报道, SO2是否会影响Pb0的吸附脱除依然不甚明晰.基于此, 本文对Pb0和SO2在活性炭表面的吸附关系进行研究.
本文首先对SO2在活性炭表面的吸附进行研究.SO2在活性炭上的吸附构型见图 2, 吸附对应的吸附能、键长、键级等参数见表 1.由计算结果可知, 扶手椅型和锯齿型炭基模型各有两种不同的SO2吸附构型, 即OO型和OS型吸附构型.OO型吸附构型表示SO2分子通过两个氧原子分别与炭基材料中的两个碳原子连接在一起, OS型吸附构型则表示SO2通过一个氧原子和一个硫原子与炭基材料连接.扶手椅型活性炭边缘对SO2的吸附能在-190.07 kJ·mol-1以内, 锯齿型活性炭边缘对SO2的吸附能在-423.64 kJ·mol-1以内, 很显然, 两种活性炭边缘对SO2的吸附能均小于对Pb0的吸附能(分别为-308.16 kJ·mol-1和-426.50 kJ·mol-1).同时研究发现, 锯齿型炭基对SO2和Pb0分子的吸附能均强于扶手椅型炭基对SO2和Pb0的吸附能, 说明锯齿型炭基材料的活性强于扶手椅型炭基, 在污染物的吸附脱除中贡献更大.
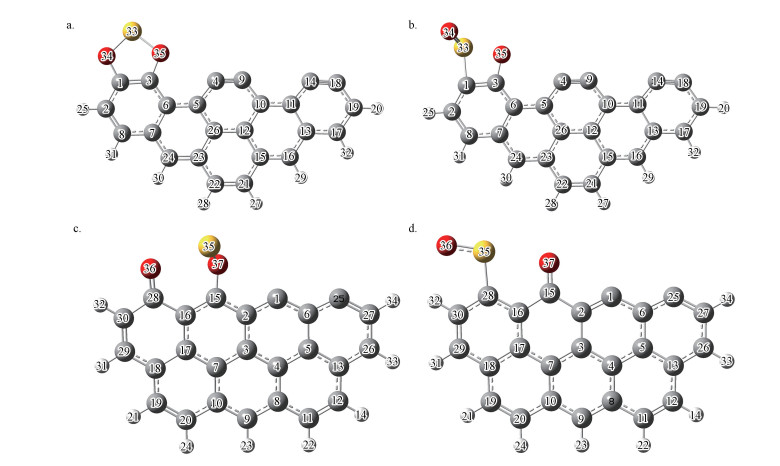 |
| 图 2 SO2在活性炭表面的吸附构型 (a.扶手椅型, OO吸附构型, b.扶手椅型, OS吸附构型, c.锯齿型, OO吸附构型, d.锯齿型, OS吸附构型) Fig. 2 The most stable adsorption configurations of SO2 toward activated carbon (a.armchair, OO, b.armchair, OS, c.zigzag, OO, d.zigzag, OS) |
虽然基于吸附前后物质电子能差值计算出来的吸附能表明Pb0在活性炭表面的吸附能大于SO2, 但考虑到锅炉烟道存在巨大的温度变化, 基于电子能的吸附能不足以说明Pb0在活性炭吸附剂表面的吸附优先于SO2.Yang等(2019)研究了燃煤电站烟气中痕量元素分子在石墨烯基单原子铁催化剂表面的竞争吸附行为, 结果发现, 不同气体在吸附剂表面的吸附顺序可能随着温度变化而发生改变.所以, 为了定量研究Pb0和SO2在活性炭表面的竞争吸附, 本研究引入了玻尔兹曼分布函数r.
Gao等(2018b)利用波尔兹曼分布函数定量描述了锅炉温度范围内NO和CO分子在炭基材料活性位点的竞争吸附关系, 得到了NO占据炭基活性位点的几率远远大于CO的结论.本文同样应用波尔兹曼分布描述Pb0和SO2在活性炭表面的吸附关系, 其数值可由下式获得:
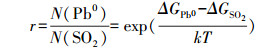
|
(2) |
式中, ΔG表示炭基对气体在吉布斯自由能下的吸附能(kJ·mol-1);k为波尔兹曼常数, 数值为8.32×10-3 kJ·mol-1·K-1;T为烟气的开尔文温度(K).
根据锅炉炉膛出口至烟囱的温度范围, 本研究在298.15 ~1000 K温度区间内, 利用玻尔兹曼分布函数得到Pb0与SO2在两种炭基模型表面竞争活性位点的概率比, 结果如图 3所示.显然, 随着温度的升高, 波尔兹曼分布函数的值逐渐下降, 说明高温对Pb0竞争炭基活性位点有抑制作用.在目标温度范围内, lnr的值恒大于零, 说明Pb0在温度范围内会优先于SO2被活性炭吸附剂吸附.因此, 在活性炭喷射过程中, Pb0比SO2分子更容易占据炭基的活性位点.说明Pb0吸附脱除的过程不会受到SO2竞争吸附的影响, 从而保证了燃煤电厂使用活性炭材料脱铅时, 炭基材料吸附剂保有足够的位点吸附并优先脱除Pb0, 使Pb0排放符合国家标准.
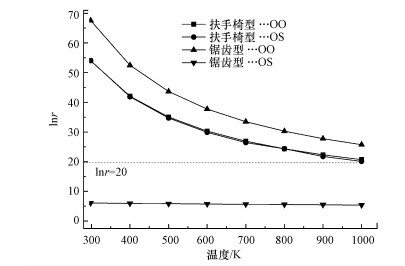 |
| 图 3 Pb0相对于SO2的玻尔兹曼分布函数 Fig. 3 Boltzmann distribution of Pb0 by SO2 |
虽然Pb0比SO2更有可能占据活性炭的吸附位点, 但Pb0作为一种痕量污染物在电厂烟气中的含量非常少, 而活性炭则由于表面多微孔结构导致其具有比表面积大、活性位点多的特点(Zhou et al., 2016), 所以炭基材料在吸附Pb0时依然保留有一定的空余位点吸附烟气中的SO2气体.吸附SO2分子之后, 活性炭表面的吸附性质会发生一定的改变, 从而对燃煤电厂利用活性炭吸附Pb0造成一定的影响.本研究进一步对4种预吸附SO2的活性炭吸附Pb0进行了探索, 即在4种SO2吸附构型的基础上在相邻位点继续吸附Pb0, 计算得到其最优吸附构型见图 4, 相应的吸附参数见表 2.显然, SO2的预先吸附使扶手椅型活性炭吸附Pb0的吸附能从-308.16 kJ·mol-1分别升高到-383.307、-400.135 kJ·mol-1, 使锯齿型活性炭吸附Pb0的吸附能从-426.50 kJ·mol-1分别升高到-499.769、-444.597 kJ·mol-1, 因此, SO2的预先吸附可以明显提高炭基材料的脱Pb0能力.
 |
| 图 4 SO2改性活性炭吸附Pb0 (a.扶手椅型, OO·Pb0吸附构型, b.扶手椅型, OS·Pb0吸附构型, c.锯齿型, OO·Pb0吸附构型, d.锯齿型, OO·Pb0吸附构型) Fig. 4 The adsorption configurations of Pb0 toward activated carbon modified by SO2 (a.armchair, OO·Pb0, b.armchair, OS·Pb0, c.zigzag, OO·Pb0, d.zigzag, OO·Pb0) |
| 表 2 SO2改性活性炭吸附Pb0的吸附参数 Table 2 Adsorption parameters of Pb0 on carbonaceous modified by SO2 |
为了揭示SO2预吸附提高活性炭吸附Pb0能力的深层机理, 本研究对活性炭表面进行了静电势(ESP)分布分析.吸附剂表面的静电势分布是决定吸附剂吸附能力的重要参数之一, 因为在活性炭吸附剂吸附Pb0的初期, 吸附剂与被吸附物质之间主要通过长程静电力吸引而相互靠近, 只有在吸附剂局部表现出足够强的电性, 并通过静电感应使中性的气体分子局部产生异于吸附剂位点的电性, 吸附剂与被吸附气体分子间才会逐渐接近(Gao et al., 2017b).通常认为, 静电势值为负且越小的吸附剂表面越容易发生亲核吸附行为, 而静电势值为正且越大的吸附剂表面越容易发生亲电吸附行为.本研究对活性炭吸附SO2前后活性炭表面的静电势分布变化情况进行了研究, 其具体分布见图 5.很明显, 在经历了SO2的预吸附改性之后, 扶手椅型活性炭的静电势分布从-18.6~21.6 kcal·mol-1拓展到-32~35 kcal·mol-1, 锯齿型活性炭的静电势分布由-14~25 kcal·mol-1拓展到-40~25 kcal·mol-1, 所以活性炭表面活性位点的静电势极大值增大(锯齿型极大值不变), 极小值减小, 活性炭表面亲电吸附与亲核吸附能力同时增强, 这就很好地解释了SO2改性后的活性炭对Pb0吸附能变强的原因.此外, 不论是扶手椅型活性炭还是锯齿型活性炭, SO2以OS型吸附的情况下, 静电势拓展部分的面积均大于SO2以OO型吸附的情况, 这说明SO2以OS构型吸附在活性炭表面对提高其吸附Pb0能力更有利.
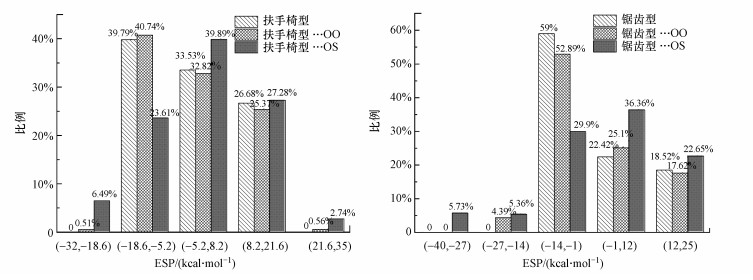 |
| 图 5 SO2吸附前后扶手椅型(a)和锯齿型(b)活性炭表面静电势分布 Fig. 5 ESP of armchair (a) and zigzag (b) models during SO2 adsorption |
吸附能分析虽然可以给出具体的吸附能数值来定量表征吸附强度, 但无法反映出吸附剂表面各个原子间的相互作用.原子间电子密度分析是吸附分析的一种重要手段, 其能够通过空间范围内电子的富集和流失直观描述原子间共价键的强弱, 进一步帮助人们了解Pb0吸附过程中Pb原子与活性炭表面的S原子、O原子、C原子之间的关系, 从而更好地理解SO2对Pb0吸附的影响.
图 6为Pb0在SO2改性后的活性炭表面吸附前后的电子密度差图, 黄色区域为电子的富集区, 青蓝色区域为电子流失区.从图 6a可以看出, SO2的两个O原子同时流失电子, 说明O原子是重要的给电子体.电子富集区主要出现在Pb原子和S原子之间, 说明这两个原子之间形成了较强的共价键, 故S原子不会在吸附过程中轻易脱离, 吸附体系比较稳定.从图 6b可以看出, O原子同样是给电子体, 而且由于一部分失去的电子富集在O34与Pb原子之间, 说明Pb0在吸附过程中与O原子形成了较强的共价键.综合图 6a和6b, 推断SO2改性的扶手椅型活性炭吸附Pb0时, SO2中的O原子通过提供电子直接参与吸附过程, SO2会与Pb0形成较强的共价键从而直接影响吸附结果.但观察图 6c和6d时发现, SO2改性的锯齿型活性炭吸附Pb0时, SO2与Pb0之间不存在共用电子对的情况, 二者未直接作用.但活性炭上与Pb0直接接触的C原子与Pb0分子在吸附过程中会有大量电子聚集在C—Pb键之间.因此, SO2只是通过影响邻位的炭原子间接影响Pb0的吸附结果.
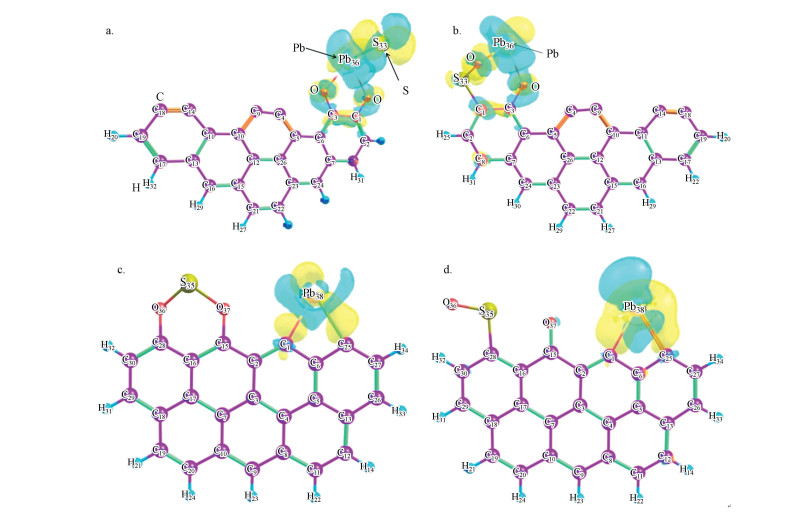 |
| 图 6 Pb0吸附前后活性炭表面电子密度差值图 (a.扶手椅型, OO吸附Pb0, b.扶手椅型, OS吸附Pb0, c.锯齿型, OO吸附Pb0, d.锯齿型, OS吸附Pb0) Fig. 6 The plot of electronic density difference of activated carbon surface during Pb0 adsorption (a.armchair, OO·Pb0, b.armchair, OS·Pb0, c.zigzag, OO·Pb0, d.zigzag, OO·Pb0) |
本研究表明, Pb0吸附在纯净活性炭上的吸附类型为强烈的化学吸附.电厂在烟道喷射的活性炭会优先吸附Pb0, 且Pb0不会受到SO2竞争吸附的影响.SO2改性后, 活性炭对Pb0的吸附效果增强.静电势分析表明, SO2改性后, 活性炭的吸附能力变强.电子密度差分析表明, SO2影响活性炭吸附Pb0能力的方式不同, 有直接和间接两种.
Chen Q, He K, Robertson A W, et al. 2016. Atomic structure and dynamics of epitaxial 2D crystalline gold on graphene at elevated temperatures[J]. ACS Nano, 10(11): 10418–10427.
DOI:10.1021/acsnano.6b06274
|
陈萍, 顾明言, 汪嘉伦, 等. 2019. 含氮煤焦还原NO反应路径研究[J]. 燃料化学学报, 2019, 47(3): 279–286.
|
邓双, 张凡, 刘宇, 等. 2013. 燃煤电厂铅的迁移转化研究[J]. 中国环境科学, 2013, 33(7): 1199–1206.
|
Gao Z, Ding Y, Yang W, et al. 2017a. DFT study of water adsorption on lignite molecule surface[J]. Journal of Molecular Modeling, 23(1): 27–46.
DOI:10.1007/s00894-016-3194-7
|
Gao Z, Ding Y. 2017b. DFT study of CO2 and H2O co-adsorption on carbon models of coal surface[J]. Journal of Molecular Modeling, 23(6): 187–204.
DOI:10.1007/s00894-017-3356-2
|
Gao Z, Li M, Sun Y, et al. 2018a. Effects of oxygen functional complexes on arsenic adsorption over carbonaceous surface[J]. Journal of Hazardous Materials, 360: 436–444.
DOI:10.1016/j.jhazmat.2018.08.029
|
Gao Z, Sun Y, Li M, et al. 2018b. Adsorption sensitivity of Fe decorated different graphene supports toward toxic gas molecules (CO and NO)[J]. Applied Surface Science, 456: 351–359.
DOI:10.1016/j.apsusc.2018.06.112
|
Gao Z, Liu X, Li A, et al. 2019. Adsorption behavior of mercuric oxide clusters on activated carbon and the effect of SO2 on this adsorption:a theoretical investigation[J]. Journal of Molecular Modeling, 25(5): 142–153.
DOI:10.1007/s00894-019-4026-3
|
Gao Z, Yang W. 2016. Effects of CO/CO2/NO on elemental lead adsorption on carbonaceous surfaces[J]. Journal of Molecular Modeling, 22(7): 166–177.
DOI:10.1007/s00894-016-3023-z
|
Grimme S, Antony J, Ehrlich S, et al. 2010. A consistent and accurate ab initio parametrization of density functional dispersion correction (DFT-D) for the 94 elements H-Pu[J]. The Journal of Chemical Physics, 132(15): 154104.
DOI:10.1063/1.3382344
|
Grimme S, Ehrlich S, Goerigk L. 2011. Effect of the damping function in dispersion corrected density functional theory[J]. Journal of Computational Chemistry, 32(7): 1456–1465.
DOI:10.1002/jcc.21759
|
Liu J, Qu W, Joo S W, et al. 2012. Effect of SO2 on mercury binding on carbonaceous surfaces[J]. Chemical Engineering Journal, 184: 163–167.
DOI:10.1016/j.cej.2012.01.023
|
López-Antón M A, Díaz-Somoano M, Fierro J, et al. 2007. Retention of arsenic and selenium compounds present in coal combustion and gasification flue gases using activated carbons[J]. Fuel processing technology, 88(8): 799–805.
DOI:10.1016/j.fuproc.2007.03.005
|
Lu T, Chen F. 2012. Multiwfn:A multifunctional wavefunction analyzer[J]. Journal of Computational Chemistry, 33(5): 580–592.
DOI:10.1002/jcc.22885
|
Montoya A, Truong T, Mondragon F, et al. 2001. CO desorption from oxygen species on carbonaceous surface:1.Effects of the local structure of the active site and the surface coverage[J]. The Journal of Physical Chemistry A, 105(27): 6757–6764.
DOI:10.1021/jp010572l
|
Nguyen-Thanh D, Bandosz T J.2005.Activated carbons with metal containing bentonite binders as adsorbents of Hydrogen Sulfide, 43(2): 359-367
|
Park J H, Ahn J W, Kim K H, et al. 2019. Historic and futuristic review of electron beam technology for the treatment of SO2 and NOx in flue gas[J]. Chemical Engineering Journal, 355: 351–366.
DOI:10.1016/j.cej.2018.08.103
|
Pedersen K H, Jensen A D, Dam-Johansen K J, et al. 2010. The effect of low-NOx combustion on residual carbon in fly ash and its adsorption capacity for air entrainment admixtures in concrete[J]. Combustion and Flame, 157(2): 208–216.
DOI:10.1016/j.combustflame.2009.10.018
|
Serre S D, Silcox G D. 2000. Adsorption of elemental mercury on the residual carbon in coal fly ash[J]. Industrial & Engineering Chemistry Research, 39(6): 1723–1730.
|
Shen F, Liu J, Zhang Z, et al. 2018. Density functional study of hydrogen sulfide adsorption mechanism on activated carbon[J]. China Environmental Science, 171: 258–264.
|
王英, 李令军. 2010. 北京大气铅污染的变化规律研究[J]. 中国环境科学, 2010, 30(6): 721–726.
|
余岳溪, 冯永新, 廖永进, 等. 2017. 烟气中NO分子对碳基吸附单质铅的影响机理[J]. 动力工程学报, 2017, 37(1): 39–44+65.
|
Yang W, Gao Z, Liu X, et al. 2018. Single atom iron catalyst with single vacancy graphene-based substrate as a novel catalyst for NO oxidation:A theoretical study[J]. Catalysis Science & Technology, 8(16): 4159–4168.
|
Yang W, Gao Z, Liu X, et al. 2019. The adsorption characteristics of As2O3, Pb0, PbO and PbCl2 on single atom iron adsorbent with graphene-based substrates[J]. Chemical Engineering Journal, 361: 304–313.
DOI:10.1016/j.cej.2018.12.087
|
Zeman F. 2012. Metropolitan Sustainability:Understanding and Improving the Urban Environment[M]. Amsterdam: Elsevier.
|
Zhang H, Liu J X, Liu J G, et al. 2018. DFT study on the alternative NH3 formation path and its functional group effect[J]. Fuel, 214: 108–114.
DOI:10.1016/j.fuel.2017.11.001
|
Zhang H, Liu J, Shen J, et al. 2015. Thermodynamic and kinetic evaluation of the reaction between NO (nitric oxide) and char (N)(char bound nitrogen) in coal combustion[J]. Energy, 82: 312–321.
DOI:10.1016/j.energy.2015.01.040
|
Zhou X J, Buekens A, Li X D, et al. 2016. Adsorption of polychlorinated dibenzo-p-dioxins/dibenzofurans on activated carbon from hexane[J]. Chemosphere, 144: 1264–1269.
DOI:10.1016/j.chemosphere.2015.10.003
|
赵鹏飞. 2010. 活性炭及氯改性活性炭吸附单质汞的机制研究[J]. 中国电机工程学报, 2010, 30(23): 40–44.
|
 2019, Vol. 39
2019, Vol. 39


