2. 铜仁职业技术学院, 铜仁 554300
2. Tongren Polytechnic College, Tongren 554300
苯甲酸(benzoic acid)被广泛应用于食品行业, 如饮料、水果制品和发酵烘焙食品的制作过程.产生的苯甲酸废水是一种剧毒的有机废水, 由于其可生化性差, 很难采用传统的微生物法对其进行处理(Xin et al., 2011).因此, 开发稳定有效去除水中苯甲酸的方法具有重要的实用价值.
催化臭氧氧化技术是去除水中有机物污染物常见的有效处理方法, 催化剂能促使臭氧分解产生氧化能力更强且无选择性的羟基自由基(Nawrocki et al., 2010;吴晓燕等, 2010).本课题组前期的研究表明CeOx/AC是一种催化活性高、稳定性好的臭氧氧化催化剂(Qin et al., 2014; 2015; 2016), 其催化活性与表面的Ce3+含量密切相关, Ce3+是主要的活性位点(Qin et al., 2014).为了提高CeOx/AC的催化活性, 课题组研究了Ce前驱体和煅烧气氛的影响, 结果表明Ce3+前驱体以及H2存在的还原气氛能提高CeOx/AC表面Ce3+含量, 从而提高其催化活性(Qin et al., 2014).
活性炭以及活性炭负载型催化剂的催化性能与活性炭其表面性质密切相关, 如活性炭表面官能团、表面酸碱性和比表面积等性质均会影响其催化活性.在活性炭催化臭氧氧化萘磺酸的研究中(Rivera-Utrilla et al., 2004), 改性之后的活性炭由于含氮官能团的引入使得其表面呈碱性, 活性炭催化活性随其pHpzc的增加而增强.此外, 本课题组前期的研究中(Qin et al., 2018a), 以氮-硫共改性活性炭为载体制备Fe/ACNS催化剂, 并用于湿式催化过氧化氢氧化苯甲酸, 结果表明氮-硫共改性活性炭由于含氮官能团和含硫官能团的引入不仅能提高催化剂表面Fe2+的含量, 还能抑制活性组分Fe的流失, 因而其催化活性得到了提高.
鉴于此, 为了寻求提高CeOx/AC催化活性的方法, 本文选择苯甲酸作为目标污染物, 考查载体AC的表面性质对CeOx/AC的催化活性的影响, 以苯甲酸的去除率和TOC的去除率表征CeOx/AC的催化活性, 并对其稳定性进行考查, 为制备高活性和稳定性的臭氧氧化催化剂提供理论基础, 为处理苯甲酸废水提供新途径.
2 材料与方法(Materials and methods) 2.1 催化剂的制备与表征柱状活性炭购买于宁夏新华活性炭有限公司, 将其粉碎并筛分出16~40目的颗粒, 用去离子水洗涤数次后于110 ℃干燥24 h, 冷却后的活性炭记为ACP, 并置于干燥器中备用.AC的改性参照本课题组前期的研究(Qin et al., 2018b), 将ACP加入装有300 mL 50%的硝酸溶液中, 在80 ℃下回流3 h, 过滤、洗涤后于110 ℃干燥12 h, 氧化后的活性炭记为ACO.然后采用尿素或硫脲分别对ACO进行改性, 改性方法为:在圆底烧瓶中将3.6 g尿素或4.55 g巯基乙酸或3 g硫脲溶于50 mL去离子水中, 然后加入5 g氧化后的ACO, 并超声30 min, 样品经过滤、干燥后在管式炉中于900 ℃下Ar气氛中热处理3 h, 冷却后置于干燥器中备用, 得到的样品分别记为ACN、ACS和ACNS.CeOx/AC催化剂的制备参照本课题组前期的研究(Qin et al., 2014), 采用不同的AC载体得到的催化剂分别记为CeOx/ACP、CeOx/ACO、CeOx/ACN、CeOx/ACS、CeOx/ACNS.
AC载体的C、H、N、S、O(差量)元素含量采用元素分析仪(EA300, 意大利)进行测定;AC载体和CeOx/AC催化剂的比表面积和孔体积采用Builder SSA-420型表面分析仪进行测定;采用Altamira AMI-300仪器获得AC载体的程序升温脱附(TPD)的CO和CO2图谱;AC载体的表面零电荷点(pHpzc)的测定采用pH漂移法进行测定(Yang et al., 2014);AC载体和CeOx/AC催化剂表面组成采用Kratos XSAM800型X-射线光电子能谱仪进行表征.
2.2 试验方法苯甲酸的吸附试验和臭氧氧化试验在500 mL的双层玻璃反应釜中进行, 每次实验采用的苯甲酸溶液的体积为300 mL, 初始浓度为50 mg·L-1, pH值采用盐酸调至2.1.当溶液温度达到30 ℃时, 通入臭氧, 并加入500 mg催化剂开始反应, 搅拌速度为200 r·min-1, 于不同时间取样, 样品经膜过滤后进行分析.吸附试验中, 采用氧气代替臭氧.
2.3 分析方法水中苯甲酸的浓度采用高效液相色谱(HPLC, LC-20A, 日本岛津公司)进行测定, 色谱柱为C18反相色谱柱(4.6 mm × 250 mm, 5 μm), 紫外检测器波长为230 nm, 流动相为V(甲醇)/V(醋酸铵溶液0.05 mol·L-1) = 5/95, 流速为1.0 mL·min-1, 柱温为室温.总有机碳(total organic carbon, TOC)表示水体中有机物总的碳含量, 采用TOC分析仪(TOC-2000, 美国热电公司)进行测定.从催化剂中流失到溶液中的Ce采用电感耦合等离子体发射光谱仪(ICPE-9000, 日本岛津公司)进行测定.
3 结果与讨论(Results and discussion) 3.1 催化剂的表征结果AC载体元素表征结果见前期的研究(Qin et al., 2018b), 采用HNO3对ACP处理后, ACO的O元素含量明显增大, 这表明在ACO表面形成了含氧官能团;而采用尿素、巯基乙酸或硫脲对ACO改性后, O元素的含量有所降低, 这是尿素、巯基乙酸或硫脲与其表面含氧官能团反应的结果所致, 同时将含氮官能团和含硫官能团引入到了AC表面(Di et al., 2016).
AC载体和CeOx/AC催化剂的孔结构性质如表 1所示, 原始的ACP具有较高的比表面积(SBET=1318 m2·g-1)和孔体积(Vt=1.12 cm3·g-1), 且其介孔较发达(介孔孔体积Vmeso占65.2%, 而微孔孔体积Vmicro占34.8%).经HNO3氧化后, SBET和Vt有较大幅度的减小.相比氧化后的ACO, 经尿素和硫脲改性后, 其SBET和Vt有所增大, 这可能是由于改性过程中尿素和硫脲与其表面含氧官能团反应生成了气体, 从而使得其孔隙结构更发达(Rivera-Utrilla et al., 2004).此外, 由于氧化铈的负载量不高, CeOx/AC催化剂的孔结构性质与AC载体相比, 未发生巨大的变化.
| 表 1 AC载体和CeOx/AC催化剂的孔结构性质 Table 1 Porous properties of AC and CeOx/AC catalysts |
在不同的温度下, 活性炭表面的含氧官能团会分解并释放出CO和CO2气体.羧酸类官能团在150~450 ℃时会分解产生CO2, 羧酸酐类官能团在400~650 ℃时会分解产生CO和CO2, 内酯在600~800 ℃也会分解产生CO2, 而醌类和酚类官能团在750~1000 ℃下会分解产生CO(Figueiredo et al., 2007).图 1是AC载体的TPD图谱, 由图谱可知, 经HNO3氧化后的ACO热分解释放的CO和CO2的量明显增多, 这表明HNO3氧化增加了其表面的含氧官能团.而经尿素、巯基乙酸或硫脲改性后, ACN、ACS和ACNS释放的CO和CO2均比ACO少, 这说明尿素、巯基乙酸和硫脲与其表面含氧官能团发生了反应, 这与元素分析的结果一致.
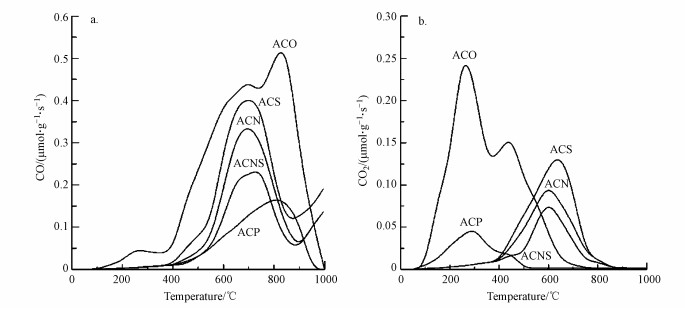 |
| 图 1 AC载体的TPD图谱 (a.CO, b.CO2) Fig. 1 TPD spectra of the AC (a.CO, b.CO2) |
AC载体在TPD过程中释放的总的CO和CO2的量及其pHpzc如表 2所示, 原始的ACP呈弱酸性, 其pHpzc为6.24.经HNO3氧化后的ACO释放的CO和CO2的量最多, 且其pHpzc最小, 这是由于引入的含氧官能团(主要是羧酸)呈酸性所致.ACN和ACNS呈弱碱性, 表明其表面引入了碱性的含氮官能团(Rivera-Utrilla et al., 2004).
| 表 2 AC载体释放的CO和CO2的量及其pHpzc Table 2 Total amounts of CO and CO2 released and pHpzc of AC supports |
通过XPS分析获得了CeOx/AC催化剂的表面组成, ACN和ACNS中N、S的化学形态在课题组前期的研究中已经报道(Qin et al., 2018a).CeOx/ACP、CeOx/ACO、CeOx/ACN、CeOx/ACS和CeOx/ACNS 5种催化剂表面Ce 3d的XPS图谱如图 2所示, Ce 3d区域可以拟合成8个峰, 其中v、u、v2、u2、v3、u3 6个峰表征Ce4+, v1、u1两个峰表征Ce3+(Qin et al., 2004; Faria et al., 2008).由图谱可以看出Ce3+/Ce4+氧化还原对存在于CeOx/AC催化剂表面, 为了确定Ce3+的相对含量, 采用v1和u1的峰面积之和除以全部峰的峰面积之和来计算.CeOx/ACO表面Ce3+的相对含量最低(19.85%), 而CeOx/ACNS表面Ce3+的相对含量最高(28.36%), CeOx/ACP、CeOx/ACN和CeOx/ACS表面Ce3+的相对含量分别为24.58%、26.26%和25.48%.
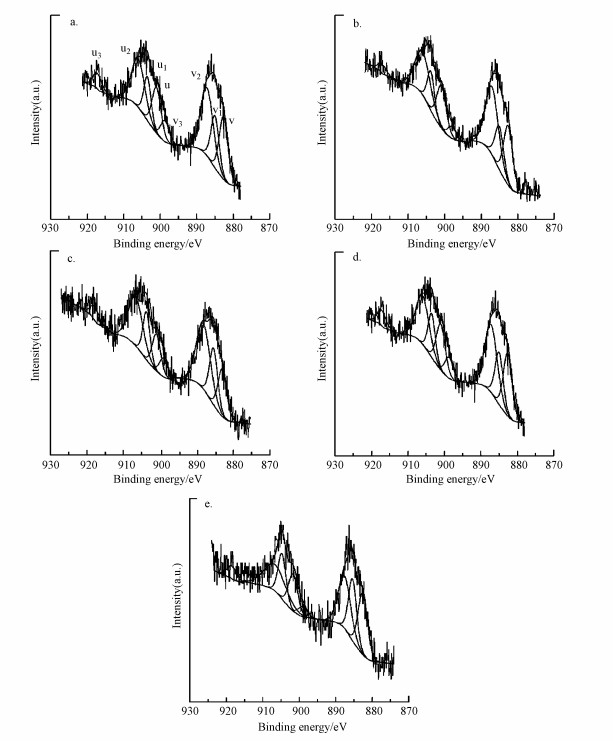 |
| 图 2 Ce 3d XPS图谱 (a.CeOx/ACP, b.CeOx/ACO, c.CeOx/ACN, d.CeOx/ACS, e.CeOx/ACNS) Fig. 2 Ce 3d XPS spectra of samples (a.CeOx/ACP, b.CeOx/ACO, c.CeOx/ACN, d.CeOx/ACS, e.CeOx/ACNS) |
上述结论表明AC载体的表面性质和Ce前驱体与煅烧气氛一样, 都会影响CeOx/AC催化剂表面Ce3+的含量.含氮官能团和含硫官能团的引入增加了AC表面的电子密度(Messele et al., 2014), 更多的电子能向氧化铈转移而形成更多的Ce3+(Faria et al., 2008).相反, 含氧官能团的引入降低了AC表面的电子密度, 向氧化铈转移的电子数量减少, 导致形成的Ce3+减少.
3.2 AC载体的吸附和催化性能为了研究AC载体的影响, 首先考查ACP、ACO、ACN、ACS和ACNS作为吸附剂和催化剂去除水中苯甲酸的性能.吸附、单独臭氧氧化和催化臭氧氧化过程中苯甲酸的去除率如图 3所示, 从图中可以看出ACNS的吸附性能最强, 而ACO对苯甲酸的吸附量比ACP小.虽然ACN和ACNS的比表面积比ACP略小(表 1), 但其吸附性能更强.在pH为2.1时, 苯甲酸(pKa = 4.2)主要以分子形式存在, 此时AC对苯甲酸的吸附主要靠AC基面的π电子和苯环的π电子之间的色散作用力, 而非静电作用力(Ayranci et al., 2005).含氮官能团和含硫官能团的存在增加了AC表面的电子密度, 有利于芳香族有机物的吸附(Figueiredo et al., 2007; Yang et al., 2014; Messele et al., 2014).
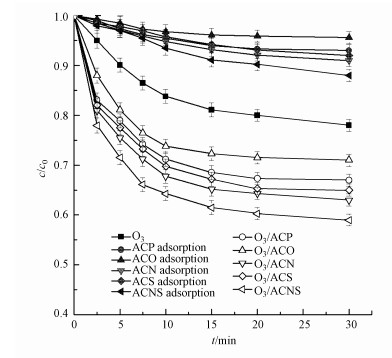 |
| 图 3 AC载体的吸附和催化臭氧氧化性能 Fig. 3 The performance of AC in adsorption and catalytic ozonation |
与单独臭氧氧化相比, AC的加入提高了苯甲酸的去除率, 这归因于AC能促使臭氧分解产生羟基自由基(Qin et al., 2014; 2015; 2016).苯甲酸的去除主要是催化臭氧氧化的结果而不是吸附造成的, 因为吸附性能最好的ACNS在30 min的反应时间内只能去除11%的苯甲酸.此外, 含氮官能团和含硫官能团的引入增强了AC的催化性能, 相似的结论出现在碱性活性炭催化臭氧氧化萘磺酸的报道中(Rivera-Utrilla et al., 2004).
3.3 CeOx/AC的催化性能采用不同AC载体制备的CeOx/ACP、CeOx/ACO、CeOx/ACN、CeOx/ACS和CeOx/ACNS作为催化剂催化臭氧氧化水中的苯甲酸, 苯甲酸的去除率如图 4a所示, 与单独臭氧氧化相比, CeOx/AC催化剂的加入加速了羟基自由基的形成, 因而增加了苯甲酸的去除率.其中CeOx/ACNS的催化活性最高, 反应30 min苯甲酸的去除率达到88%左右, 比单独臭氧氧化增加了66%.
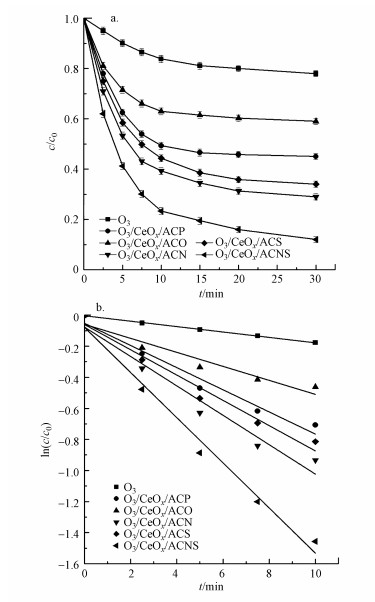 |
| 图 4 CeOx/AC的催化臭氧氧化性能(a)及苯甲酸的伪一级动力学降解(b) Fig. 4 The performance of CeOx/AC in catalytic ozonation(a) and the pseudo-first-order kinetics of benzoic acid degradation (b) |
如图 4b所示, 臭氧降解苯甲酸的过程符合伪一级动力学模型, 直线的斜率为反应的表观速率常数.不同体系的表观速率常数(kapp)和相关系数(R2)如表 3所示, 单独臭氧氧化的表观速率常数为0.017 min-1, 而CeOx/ACNS催化臭氧氧化的表观速率常数为0.145 min-1, 是单独臭氧氧化的8.5倍.
| 表 3 臭氧降解苯甲酸的表观速率常数(kapp)和相关系数(R2) Table 3 Apparent rate constants (kapp) and linear correlation coefficients (R2) of benzoic acid degradation in ozonation |
为了分析CeOx/AC催化剂表面Ce3+含量对其催化性能的影响, 通过构造参数kapp/SBET来排除比表面积对催化性能的影响, 其结果如图 5所示.由图可知, 苯甲酸的降解速率随CeOx/AC催化剂表面Ce3+含量的增大而升高, 这是因为Ce3+是CeOx/AC催化剂表面的主要活性位点, 它能促使臭氧分解产生氧化能力且与有机物反应速率更快的羟基自由基(Faria et al., 2008;Qin et al., 2014; Messele et al., 2014).由此可见, AC载体的表面性质能改变其吸附性能以及CeOx/AC催化剂表面的Ce3+含量, 从而影响其催化活性.
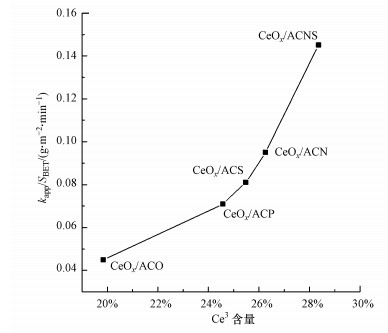 |
| 图 5 苯甲酸降解速率和CeOx/AC催化剂表面Ce3+含量之间的关系 Fig. 5 The relationship between benzoic acid degradation rate and Ce3+ content on CeOx/AC surface |
为了验证AC和CeOx/AC催化臭氧氧化苯甲酸是否属于羟基自由基过程, 在反应体系中加入常用的自由基抑制剂叔丁醇(t-BuOH), 其浓度为20 mg·L-1, 实验结果如图 6所示.从图中可知加入自由基抑制剂后, 很大程度的抑制了ACNS和CeOx/ACNS催化臭氧氧化降解苯甲酸的过程, 去除率分别从41%和88%降低到了15%和17%.上述实验结果表明AC和CeOx/AC催化臭氧氧化苯甲酸属于羟基自由基机理, 证实了苯甲酸的降解主要是由于臭氧分解产生的羟基自由基氧化所致(Rivera-Utrilla et al., 2004; Qin et al., 2004).
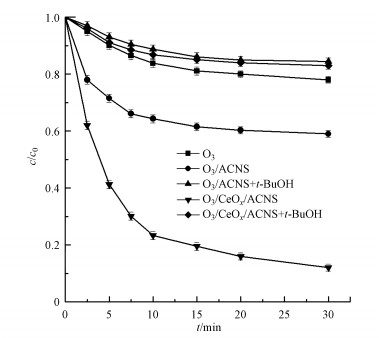 |
| 图 6 叔丁醇对催化臭氧氧化降解苯甲酸的影响 Fig. 6 Influence of t-BuOH on benzoic acid degradation in catalytic ozonation |
图 7是单独臭氧氧化和CeOx/AC催化臭氧氧化反应结束后体系TOC的去除率.从图中可以看出单独臭氧氧化很难将苯甲酸彻底矿化, 反应30 min后, TOC的去除率只有7%, 而单独臭氧氧化过程中苯甲酸的去除率能达到22%, 这表明臭氧氧化过程中生成了难以被臭氧直接降解的中间产物, 比如短链的羧酸等(Nawrocki et al., 2010).CeOx/AC催化剂的加入, 使得臭氧分解产生氧化能力更强且无选择性的羟基自由基, 能对生成的中间产物进一步的氧化(Orge et al., 2011;Beltran et al., 2014).尤其是CeOx/ACNS的加入, TOC的去除率达到了55%左右.
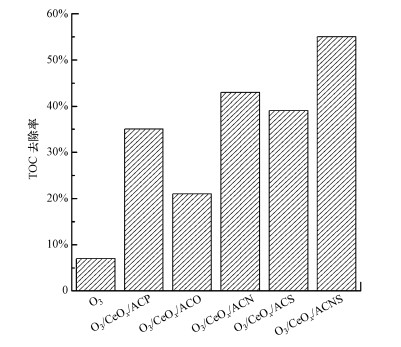 |
| 图 7 单独臭氧氧化和催化臭氧氧化降解苯甲酸过程中TOC的去除率 Fig. 7 TOC removal in the degradation of benzoic acid by single and catalytic ozonation |
稳定性是催化剂的一个重要指标, 为了考查CeOx/ACNS催化剂的稳定性, 将其重复使用6次, 每次反应结束后, 采用过滤回收溶液中的固体催化剂, 并测定溶液中Ce的含量.采用去离子水对回收的固体催化剂洗涤后, 置于110 ℃下干燥24 h, 冷却后投入下一个循环, 稳定性考查的结果如图 8所示.从图 8a可以看出6次循环使用后, 苯甲酸的去除率仅从88%降低到了82%, 仍远远高于单独臭氧氧化苯甲酸的去除率.苯甲酸去除率的降低一方面由于CeOx/ACNS催化剂表面吸附的有机物会影响其催化活性(Melero et al., 2007), 另一方面由于过滤回收过程难免会造成固体催化剂质量的减少.此外, 如图 8b所示前3次循环使用出现了Ce的流失, 而后3次溶液中Ce的浓度低于测量仪器的检出限, 循环6次后, 流失的Ce仅占0.32%.上述结论均表明CeOx/ACNS催化剂具有良好的稳定性和重复使用性.
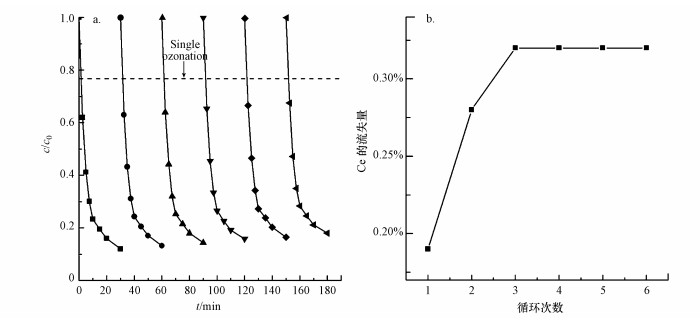 |
| 图 8 CeOx/ACNS催化剂的稳定性试验(a.苯甲酸的去除, b. Ce的流失) Fig. 8 Benzoic acid removal(a) and Ce leaching from the catalyst(b) in the stability tests of CeOx/ACNS catalyst |
1) AC的表面官能团和表面酸碱性能影响其吸附性能以及CeOx/AC催化剂表面的Ce3+含量, 从而影响CeOx/AC的催化臭氧氧化性能.
2) 氮-硫共改性活性炭(ACNS)表面的含氮官能团和含硫官能团增加了AC表面的电子密度, 使得其吸附性能和催化臭氧氧化性能得到了提高.
3) 采用氮-硫共改性活性炭为载体制备的CeOx/ACNS催化剂具有较高的催化活性, 苯甲酸的去除率能达到88%, TOC的去除率能达到55%, 去除率的提高归因于臭氧分解产生的羟基自由基.
4) CeOx/ACNS催化剂具有良好的稳定性, 循环使用6次仍具有较高的活性, 且流失的Ce只占总负载量的0.32%.
Ayranci E, Hoda N, Bayram E. 2005. Adsorption of benzoic acid onto high specific area activated carbon cloth[J]. Journal of Colloid and Interface Science, 284(1): 83–88.
DOI:10.1016/j.jcis.2004.10.033
|
Beltran F J, Rivas F J, Monte-de-Espinosa R. 2003. Mineralization improvement of phenol aqueous solutions through heterogeneous catalytic ozonation[J]. Journal of Chemical Technology & Biotechnology, 78(12): 1225–1233.
|
Di X X, Zhao J, Yu Y, et al. 2016. One-pot synthesis of nitrogen and sulfur co-doped activated carbon supported AuCl3 as efficient catalysts for acetylene hydrochlorination[J]. Chinese Chemical Letters, 27(9): 1567–1571.
DOI:10.1016/j.cclet.2016.03.004
|
Faria P C C, Orfao J J M, Pereira M F R. 2008. A novel ceria-activated carbon composite for the catalytic ozonation of carboxylic acids[J]. Catalysis Communication, 9(11/12): 2121–2126.
|
Figueiredo J L, Pereira M F, Freitas M M A, et al. 2007. Characterization of active sites on carbon catalysts[J]. Industrial & Engineering Chemistry Research, 46(12): 4110–4115.
|
Melero J A, Calleja G, Martínez F, et al. 2007. Nanocomposite Fe2O3/SBA-15: An efficient and stable catalyst for the catalytic wet peroxidation of phenolic aqueous solutions[J]. Chemical Engineering Journal, 131(1): 245–256.
|
Messele S A, Soares O S G P, Orfao J J M, et al. 2014. Zero-valent iron supported on nitrogen-containing activated carbon for catalytic wet peroxide oxidation of phenol[J]. Applied Catalysis B: Environmental, 154-155(11/12): 329–338.
|
Nawrocki J, Kasprzyk-Hordern B. 2010. The efficiency and mechanisms of catalytic ozonation[J]. Applied Catalysis B: Environmental, 99(1/2): 27–42.
|
Orge C A, Orfao J J M, Pereira M F R, et al. 2011. Ozonation of model organic compounds catalysed by nanostructured cerium oxides[J]. Applied Catalysis B: Environmental, 103(1): 190–199.
|
Qin H D, Chen H L, Yang G, et al. 2014. Efficient degradation of fulvic acids in water by catalytic ozonation with CeO2/AC[J]. Journal of Chemical Technology & Biotechnology, 89(9): 1402–1409.
|
Qin H D, Dong Q Z, Chen H L, et al. 2015. Kinetics and mechanism of humic acids degradation by ozone in the presence of CeO2/AC[J]. Ozone: Science & Engineering, 37(4): 1–8.
|
Qin H D, Chen H L. 2016. Pretreatment of concentrated leachate by the combination of coagulation and catalytic ozonation with Ce/AC catalyst[J]. Water Science & Technology, 73(3): 511–519.
|
Qin H D, Xiao R, Chen J. 2018a. Catalytic wet peroxide oxidation of benzoic acid over Fe/AC catalysts: Effect of nitrogen and sulfur co-doped activated carbon[J]. Science of the Total Environment, 626: 1414–1420.
DOI:10.1016/j.scitotenv.2018.01.206
|
Qin H D, Xiao R, Guo L, et al. 2018b. Mercury (Ⅱ) adsorption from aqueous solution using nitrogen and sulfur co-doped activated carbon[J]. Water Science & Technology, 2017(1): 310–318.
|
Rivera-Utrilla J, Sanchez-Polo M. 2004. Ozonation of naphthalenesulphonic acid in the aqueous phase in the presence of basic activated carbons[J]. Langmuir, 20(21): 9217–9222.
DOI:10.1021/la048723+
|
吴晓燕, 尹军, 蒋宝军. 2010. 几种催化剂对垃圾渗滤液臭氧氧化效能的影响[J]. 环境科学学报, 2010, 30(6): 1183–1187.
|
Xin X D, Si W, Yao Z X, et al. 2011. Adsorption of benzoic acid from aqueous solution by three kinds of modified bentonites[J]. Journal of Colloid & Interface Science, 359(2): 499–504.
|
Yang G, Chen H L, Qin H D, et al. 2014. Amination of activated carbon for enhancing phenol adsorption: effect of nitrogen-containing functional groups[J]. Applied Surface Science, 293(3): 299–305.
|
 2019, Vol. 39
2019, Vol. 39


