近年来, 随着我国工业的快速发展及人口数量的不断增加, 水体重金属污染问题越发严重, 其中镉(Cd(Ⅱ))对人体健康有着极大的危害(杨林等, 2016).镉是一种高毒性重金属, 生物半衰期达10~30 a, 能在人体肾脏中积聚, 过量时甚至导致人类死亡(Nawrot et al., 2006), 联合国环境规划署和国际劳动卫生重金属委员会已把镉列为第六位危害人体健康的有毒物质(周宏光, 2017).镉主要通过作为电子产品、镍镉电池、金属冶炼、合成颜料、金属涂层中的稳定剂和固体废物焚烧等方式进入环境中(Patar et al., 2016).目前国内外处理含镉废水的方法主要有吸附法、离子交换法、化学氧化还原法、膜分离法以及化学沉淀法等(Karami et al., 2013).其中吸附法因其高效经济、操作简便, 在实际工程中得到了广泛的应用(Zhou et al., 2018).
麦饭石是一种具有良好的矿物质溶出、杂质吸附功能的环境友好型复合矿物材料, 呈多孔性海绵状特殊结构, 对生物无毒无害, 比表面积大、吸附效果好(Gao et al., 2012), 且在我国资源丰富, 价格低廉, 因此常被用于给水处理领域(汪碧华等, 1988;李娟等, 2008).有研究表明麦饭石对Pb(Ⅱ)、Cd(Ⅱ)、Ni(Ⅱ)、Zn(Ⅱ)、Hg(Ⅱ)、Co(Ⅱ)金属离子具有一定的去除效果(汪碧华等, 1988), 但天然麦饭石表面呈叠状结构, 通透性差, 且空隙中填充了很多杂质, 其离子交换性能表现出一定的局限性, 对重金属离子去除效果有限.为提高天然麦饭石对Cd(Ⅱ)的吸附效果, 可将其进行适当改性处理, 例如去除孔道的部分杂质, 使孔道和孔隙结构得到改善(陈琳荔等, 2015).
层状双金属氢氧化物(Layered Double Hydroxides, LDHs)由带正电的混合金属氢氧化物组成, 是一种具有大孔容积和高比表面积的特殊层状结构复合无机材料(González et al., 2015).前期研究表明(张翔凌等, 2016;向洋等, 2018;Fang et al., 2018;Gao et al., 2018;张翔凌等, 2019), Zn-LDHs覆膜改性填料对污水中的氮、磷等水体富营养化污染物及Cr(Ⅵ)均有良好的去除效果.因此本次试验尝试采用ZnCl2溶液分别与AlCl3和FeCl3溶液合成ZnAl-LDHs及ZnFe-LDHs, 并覆膜于天然麦饭石表面;以制备的改性麦饭石为吸附剂, 天然麦饭石为对照组, 通过等温吸附试验、解吸附试验、吸附热力学试验、吸附动力学试验、不同pH值条件下的吸附试验和竞争性吸附试验, 对比天然麦饭石与覆膜改性麦饭石的吸附性能, 探究Zn-LDHs覆膜改性对麦饭石吸附Cd(Ⅱ)的影响因素及作用机理, 并筛选出较好吸附效果的Zn-LDHs覆膜类型, 为改性麦饭石有效应用于吸附Cd(Ⅱ)提供参考.
2 材料与方法(Materials and methods) 2.1 改性试验 2.1.1 试验材料试验所用天然麦饭石购自河南省巩义市, 其表面粗糙不平, 呈不透明的青褐色.天然麦饭石的主要物化特性为:粒径为2~4 mm, 表观密度为2.715 g·cm-3, 堆积密度为1.206 g·cm-3, 空隙率为55.6%, 所含主要化学成分为Si、O、Al等.
2.1.2 改性试剂改性试验所用试剂为:ZnCl2(AR)、AlCl3·6H2O(AR)、FeCl3·6H2O(AR)、NaOH(AR), 均购自国药集团化学试剂有限公司;Cd(Ⅱ)标准溶液采用CdSO4·3/8H2O(AR)加超纯水(UPT-11-10T超纯水机)配制.
2.1.3 改性方法碱性条件下采用水浴-共沉淀法制备Zn-LDHs(ZnAl-LDHs、ZnFe-LDHs)并覆膜改性麦饭石.以制备ZnAl-LDHs覆膜改性麦饭石为例:取800 g洗净的天然麦饭石放入2 L烧杯中, 置于80 ℃的恒温水浴锅中(SHZ-84, 江苏常州国华电器有限公司)加热, 加入25%NaOH溶液调节pH值, 使其维持在11左右;将配制的2 mol·L-1 ZnCl2溶液和1 mol·L-1AlCl3溶液同时加入装有天然麦饭石的烧杯中;持续搅拌2 h后取出固液混合物, 将其放入80 ℃烘箱陈化16 h;用去离子水清洗混合物至洗涤水为中性后, 置于60 ℃烘箱干燥, 即得ZnAl-LDHs覆膜改性麦饭石.
采用美国EDAX公司GENESIS系列能谱分析仪(EDS)配合场发射扫描电子显微镜(Field Emission Scanning Electron Microscope, FE-SEM)检测覆膜改性麦饭石和天然麦饭石的形貌和元素变化;采用德国AXS公司D8 Advance型号X射线衍射仪进行样品晶体材料和结构分析.
2.1.4 检测方法检测所用化学试剂为浓硫酸、碘化钾、抗坏血酸、聚乙烯醇-1750、罗丹明B, 以上试剂均为分析纯, 购自国药集团化学试剂有限公司.采用以上试剂配制1.0 mol·L-1硫酸溶液、1.0 mol·L-1碘化钾-抗坏血酸溶液、10 g·L-1聚乙烯醇-1750溶液、0.5 g·L-1罗丹明B溶液、10 mg·L-1的硫酸镉溶液.绘制标准曲线:取6个50 mL的容量瓶, 分别加入0、1.00、2.00、3.00、4.00、5.00 mL的10 mg·L-1的硫酸镉溶液;依次加入3 mL 1.0 mol·L-1硫酸溶液、4 mL 1.0 mol·L-1碘化钾-抗坏血酸溶液、2 mL 10 g·L-1聚乙烯醇-1750溶液、1.8 mL 0.5 g·L-1罗丹明B溶液;摇匀后静置10 min, 使用分光光度计(UV-1100, MAPADA)在最大吸收波长600 nm时测定吸光度值, 并根据测定结果绘制标准曲线;根据标准曲线与Cd(Ⅱ)溶液中测定的分光光度值计算待测溶液中Cd(Ⅱ)的质量浓度(沈昱等, 2016).
2.2 吸附试验 2.2.1 等温吸附试验对天然麦饭石及两种Zn-LDHs覆膜改性麦饭石进行等温吸附试验:分别称取0.5 g填料置于8个250 mL具塞锥形瓶中, 同时各自加入不同质量浓度(0、1、2、4、8、16、32、64 mg·L-1)的Cd(Ⅱ)标准溶液100 mL, 具塞放入恒温水浴振荡器中, 在温度为(25±1) ℃、转速为160 r·min-1、pH值为7的条件下振荡24 h, 静置、过滤后测定上清液中Cd(Ⅱ)的质量浓度.
2.2.2 解吸附试验将上述等温吸附试验后的各填料用去离子水洗涤, 重新放入250 mL具塞锥形瓶中, 同时加入3 mol·L-1的NaCl溶液100 mL, 置于恒温水浴振荡器中, 在温度(25±1) ℃、转速160 r·min-1的条件下振荡6 h, 静置、过滤后测定上清液中Cd(Ⅱ)的质量浓度.
2.2.3 吸附热力学试验分别在298.15、308.15、318.15 K等3个热力学温度下进行等温吸附试验, 试验步骤同2.2.1节等温吸附试验.
2.2.4 吸附动力学试验配制不同初始质量浓度(0、1、4、8、16 mg·L-1)的Cd(Ⅱ)标准溶液;分别称取0.5 g天然麦饭石及两种Zn-LDHs覆膜改性麦饭石于250 mL具塞锥形瓶, 准确量取100 mL Cd(Ⅱ)标准溶液加入锥形瓶中并置于恒温水浴振荡器, 在温度(25±1) ℃、转速160 r·min-1的条件下振荡, 于设置的一系列时间点后取出不同锥形瓶, 静置、过滤, 测定上清液中Cd(Ⅱ)的质量浓度.
2.2.5 不同pH值条件下的吸附试验分别称取0.5 g天然麦饭石和ZnFe-LDHs覆膜改性麦饭石于250 mL具塞锥形瓶中, 设置Cd(Ⅱ)初始浓度为8 mg·L-1, 在初始溶液pH值分别为6、7、8, 温度为(25±1) ℃, 转速160 r·min-1条件下, 置于恒温水浴振荡器振荡24 h, 静置、过滤取上清液测定Cd(Ⅱ)的质量浓度.
2.2.6 竞争离子吸附试验称取0.5 g ZnFe-LDHs覆膜改性麦饭石置于250 mL具塞锥形瓶中, 同时加入不同初始质量浓度(0、2、4、8、16、32 mg·L-1)的Cd(Ⅱ)标准溶液和16 mg·L-1的竞争离子(Mg2+、K+、PO43-、NH4+、NO3-)各50 mL.其它试验步骤同2.2.1节等温吸附试验.
3 结果及讨论(Results and discussions) 3.1 覆膜改性前后麦饭石的表观特性及化学成分变化图 1为利用场发射扫描电子显微镜(FE-SEM)对改性前后麦饭石表面形貌的检测结果.可以发现, 天然麦饭石(图 1c)表面不规整, 其凹层空隙有利于覆膜改性;而Zn-LDHs覆膜改性麦饭石(图 1a、1b)表面相对平整, 有明显晶体附着物;通过Zn-LDHs覆膜改性, 填料表面的形态结构有很大的变化, 天然麦饭石表面的空隙为覆膜物质所填充而变得较为光滑.结合天然麦饭石和ZnFe-LDHs覆膜改性麦饭石的能谱分析仪(EDS)检测结果(图 2)可以发现, 相较于天然麦饭石, ZnFe-LDHs覆膜改性麦饭石中Zn元素的质量分数从0增至3.18%, Fe元素的质量分数由0.6%增至3.92%;即ZnFe-LDHs的覆膜改性增加了麦饭石填料中元素的种类及某些特定元素的质量分数.
 |
| 图 1 天然麦饭石与覆膜改性麦饭石的FE-SEM图 (a. ZnAl-LDHs覆膜改性麦饭石;b. ZnFe-LDHs覆膜改性麦饭石;c.天然麦饭石) Fig. 1 FE-SEM images of natural and modified Maifanite (a. ZnAl-LDHs modified maifanite, b. ZnFe-LDHs modified maifanite, c. natural maifanite) |
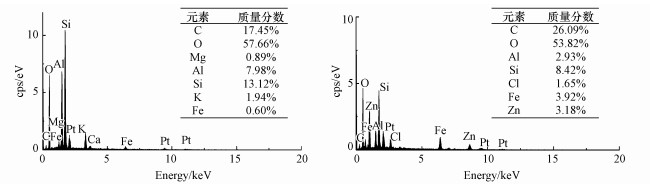 |
| 图 2 天然麦饭石(a)与ZnFe-LDHs覆膜改性麦饭石(b)的EDS分析结果 Fig. 2 EDS analysis results of natural (a) and ZnFe-LDHs modified Maifanite (b) |
图 3a、3b分别为吸附试验后ZnFe-LDHs覆膜麦饭石的FE-SEM和EDS检测结果.从图 3可知, 吸附Cd(Ⅱ)后的ZnFe-LDHs覆膜麦饭石表面仍有明显晶体附着物, 且通过EDS检测发现, 在ZnFe-LDHs覆膜麦饭石表面有镉的存在, 说明Cd(Ⅱ)确为ZnFe-LDHs覆膜改性麦饭石所吸附.
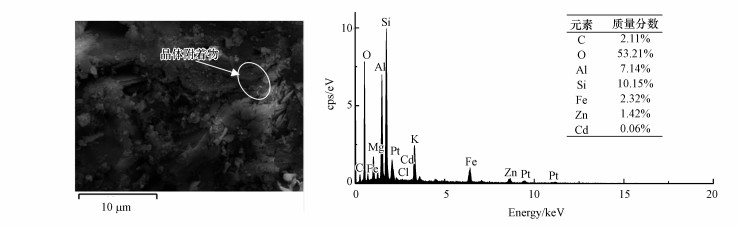 |
| 图 3 ZnFe-LDHs覆膜改性麦饭石吸附后的FE-SEM(a)和EDS分析(b)结果 Fig. 3 FE-SEM (a) and EDS (b)analysis results adsorbed ZnFe-LDHs modified Maifanite |
采用X射线衍射(XRD)分别对本试验中的纯ZnFe-LDHs、天然麦饭石和ZnFe-LDHs覆膜改性麦饭石进行分析, 结果如图 4所示.可以发现, 纯ZnFe-LDHs约在11°、23°、35°、39°、47°、60°和62°处有7个衍射峰, 分别对应LDHs典型特征峰(003)、(006)、(012)、(015)、(018)、(110)和(113), 与层状双氢氧化物的标准JCPDS 38-0715相匹配(Rajeshkhanna et al., 2018);且较明显看出, ZnFe-LDHs覆膜改性麦饭石的XRD图谱不仅有天然麦饭石的衍射峰, 而且还有强度减弱的LDHs的7个特征峰, 说明本试验确能制备ZnFe-LDHs并将其覆膜于天然麦饭石表面.
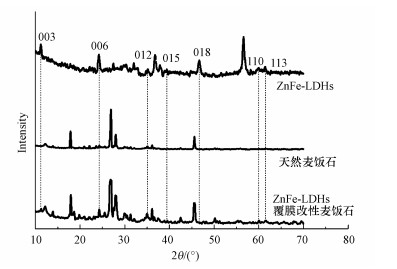 |
| 图 4 天然麦饭石和ZnFe-LDHs覆膜改性麦饭石的XRD图谱 Fig. 4 XRD patterns of natural maifanite and ZnFe-LDHs modified maifanite |
吸附等温线常用以描述一定温度下吸附剂最大饱和吸附容量及吸附机理(Acar et al., 2015);本研究采用Langmuir和Freundlich等温吸附模型, 对Zn-LDHs覆膜改性麦饭石和天然麦饭石在不同初始浓度下吸附平衡后的试验数据进行拟合.
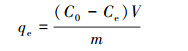
|
(1) |
式中, Ce为吸附平衡时Cd(Ⅱ)浓度(mg·L-1);C0为初始Cd(Ⅱ)浓度(mg·L-1);qe为平衡吸附量(mg·kg-1);V为溶液体积(L);m为填料质量(g).
Langmuir等温吸附模型:
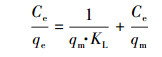
|
(2) |
式中, Ce和qe同上;qm为理论最大饱和吸附容量(mg·kg-1);KL为Langmuir平衡常数(L·mg-1).
Freundlich等温吸附模型:
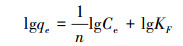
|
(3) |
式中, Ce和qe同上;1/n为非线性系数;KF为Freundlich常数(mg1-n·Ln·kg-1).其中1/n值表示吸附作用强度, 其值越小则吸附质与吸附剂的结合越稳定;lgKF能够表示填料吸附能力大小, 其值越大, 吸附能力越好(Carja et al., 2005).
对等温吸附试验数据进行Langmuir和Freundlich等温吸附模型拟合, 其结果如表 1所示.
| 表 1 Zn-LDHs覆膜改性麦饭石和天然麦饭石的等温吸附模型拟合参数 Table 1 Adsorption isothermal parameters of natural and Zn-LDHs Modified Maifanite |
在Langmuir等温吸附模型中, 相较于天然麦饭石(714.29 mg·kg-1)的理论最大饱和吸附容量, ZnFe-LDHs覆膜改性麦饭石(2500 mg·kg-1)提高了3倍以上, ZnAl-LDHs覆膜改性麦饭石(1000 mg·kg-1)也增大了50%;对理论最大饱和吸附容量进行排序:ZnFe-LDHs覆膜改性麦饭石> ZnAl-LDHs覆膜改性麦饭石>天然麦饭石.可见, Zn-LDHs覆膜改性能有效提高麦饭石对Cd(Ⅱ)的理论最大饱和吸附容量, 且改性方式不同, 饱和吸附容量的提升程度也不同.究其原因, 一方面由于覆膜改性麦饭石表面稳定附着Zn-LDHs, 溶液中的Cd(Ⅱ)可与麦饭石表面LDHs中的Zn发生同晶替代, 形成新的LDHs覆膜在填料表面(Zhou et al., 2018);另一方面, LDHs晶体表面存在大量与八面体金属原子键结合的羟基, 带有相反电荷的表面羟基与Cd(Ⅱ)形成外层表面络合物(Shan et al., 2015).除此之外, ZnFe-LDHs覆膜改性麦饭石最大饱和吸附容量是ZnAl-LDHs覆膜改性麦饭石的2.5倍, 有研究发现LDHs形成分为两步, 先结晶成不稳定的LDHs, 在随后陈化阶段中, 逐渐形成稳定的LDHs结晶体(Carja et al., 2005);对于不同类型的LDHs, Fe3+半径小于Al3+的离子半径, Fe3+极化能强于Al3+, 由FeCl3参与合成的ZnFe-LDHs增加了对LDHs层间Cl-的吸引力(Bruna et al., 2009), 因此ZnFe-LDHs的结晶效果优于ZnAl-LDHs, 相应地, ZnFe-LDHs覆膜改性麦饭石的吸附性能优于ZnAl-LDHs覆膜改性麦饭石.
R2是衡量模型拟合程度的重要参数;如表 1所示, Zn-LDHs覆膜改性麦饭石Langmuir等温吸附模型中的R2均高于Freundlich模型, 且R2均大于0.99, 说明Langmuir模型能更好地描述Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附过程, 即更趋向于单分子层吸附(孔旺盛等, 2007).对于天然麦饭石, Langmuir模型和Freundlich模型R2分别为0.9079和0.9478, 说明天然麦饭石更符合Freundlich模型, 即趋向于非均匀吸附剂表面多分子层吸附.由此推断, 填料表面的Zn-LDHs覆膜改性改变了麦饭石对Cd(Ⅱ)的吸附类型.
1/n值是与吸附强度和吸附剂表面不均匀性有关的常数, 1/n值越小, 吸附性能越好;一般情况下, 当0 < 1/n < 0.5时为容易吸附, 0.5 < 1/n < 1为优惠吸附, 1 < 1/n时为难于吸附(Arfaoui et al., 2008);由表 1可知, ZnAl-LDHs覆膜改性麦饭石和ZnFe-LDHs覆膜改性麦饭石的1/n值分别为0.3266和0.5124, 而天然麦饭石为0.6196.同时, lgKF能够间接反映填料吸附能力大小, 其值越大, 吸附能力越好;ZnAl-LDHs覆膜改性麦饭石、ZnFe-LDHs覆膜改性麦饭石和天然麦饭石的lgKF分别为2.3565、2.4883、2.1371, 其大小排序与Langmuir模型中理论最大饱和吸附容量一致, ZnFe-LDHs覆膜改性麦饭石> ZnAl-LDHs覆膜改性麦饭石>天然麦饭石.由此可见, 经Zn-LDHs覆膜改性, 填料的吸附能力由优惠吸附向容易吸附转化, 更有利于填料对Cd(Ⅱ)的吸附, 因而Zn-LDHs覆膜改性麦饭石表现出更佳的吸附性能.
3.3 解吸附试验为探究Zn-LDHs覆膜改性麦饭石的回收再利用性能, 对Zn-LDHs覆膜改性麦饭石在不同初始浓度等温吸附试验结束后进行解吸附试验;解吸率计算公式见式(4).
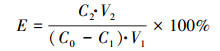
|
(4) |
式中, E为解吸率;C0为溶液中Cd(Ⅱ)的初始浓度(mg·L-1);C1为吸附平衡时溶液中Cd(Ⅱ)的浓度(mg·L-1);C2为解吸试验后平衡溶液中Cd(Ⅱ)的浓度(mg·L-1);V1、V2分别为吸附液和解吸液的体积(L).
经计算可得, ZnAl-LDHs覆膜改性麦饭石的解吸率为64.01%~95.99%、ZnFe-LDHs覆膜改性麦饭石解吸率为69.52%~98.50%, 天然麦饭石的解吸率略低, 为61.25%~92.93%, 说明两种覆膜改性麦饭石填料较天然麦饭石的可重复利用率提高, 有利于延长使用周期, 节约运行和再生成本.
3.4 吸附热力学试验采用Langmuir等温吸附方程对298.15、308.15、318.15 K等3个热力学温度下的吸附平衡数据进行拟合, 并绘制填料对Cd(Ⅱ)的理论最大吸附容量随温度变化的折线图, 如图 5所示.3个不同热力学温度下的理论最大饱和吸附容量排序均为:ZnFe-LDHs覆膜改性麦饭石> ZnAl-LDHs覆膜改性麦饭石>天然麦饭石, 这也与等温吸附试验排序一致.并且, 随着温度的升高, 天然麦饭石的理论最大饱和吸附容量略有增大, 在温度298.15 K时最小;而对于Zn-LDHs覆膜改性麦饭石, 随着温度升高, 理论最大饱和吸附容量不断减小, 降低温度有利于提升改性麦饭石对Cd(Ⅱ)的吸附性能.由此可知, Zn-LDHs覆膜改性麦饭石受温度的影响不同于天然麦饭石.
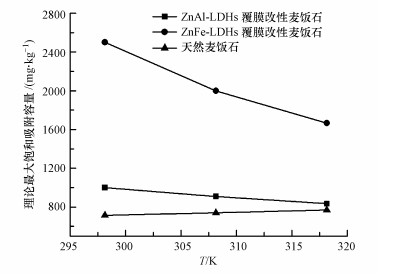 |
| 图 5 天然麦饭石和Zn-LDHs覆膜改性麦饭石理论最大饱和吸附容量随温度的变化 Fig. 5 Theoretical maximum saturation adsorption capacities of natural maifanite and Zn-LDHs modified maifanite vary with temperatures |
为进一步探究填料吸附Cd(Ⅱ)的热力学特性, 采用热力学参数吉布斯自由能(ΔGθ)、焓变(ΔHθ)和熵变(ΔSθ)来反应热力学效应.
对热力学参数进行计算, 公式如下:
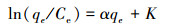
|
(5) |
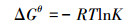
|
(6) |
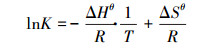
|
(7) |
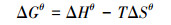
|
(8) |
式中, qe、Ce、T同上;ΔGθ、ΔHθ、ΔSθ分别为标准吉布斯自由能、焓、熵;R为气体常数8.314 J·mg-1·K-1;K为热力学平衡常数.
表 2为298.15、308.15、318.15 K等时各麦饭石对Cd(Ⅱ)吸附的热力学方程拟合参数.其中, 吉布斯自由能ΔGθ < 0, 说明3种麦饭石填料对Cd(Ⅱ)的吸附均可自发进行;熵变ΔSθ>0, 说明吸附过程固-液系统中混乱度增加;天然麦饭石ΔHθ>0, 说明反应为吸热过程, 随着温度的降低, 反应向负方向进行, 而Zn-LDHs覆膜改性麦饭石ΔHθ < 0, 说明反应为放热过程, 温度越低, 反应向正方向进行, 这也与Zn-LDHs覆膜改性麦饭石的饱和吸附量随温度降低而增大的结论相吻合.同时, 天然麦饭石焓变ΔHθ>0, 而Zn-LDHs覆膜改性麦饭石焓变ΔHθ < 0, 说明经LDHs覆膜改性, 麦饭石对Cd(Ⅱ)的吸附特性发生了变化.有研究表明LDHs能与水体中Cd(Ⅱ)发生同晶替代、离子交换、化学吸附等反应(Shan et al., 2015;Zhou et al., 2018), 相比于天然麦饭石, Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附增加了不同类型的反应机制, 因此其吸附更为复杂, 导致吸附类型从吸热逐渐转化成放热过程;且可以从表 2看出, ZnFe-LDHs覆膜改性麦饭石的放热量远高于ZnFe-LDHs覆膜改性麦饭石, 这可能是由于拥有更好结晶效果的ZnFe-LDHs在吸附过程中反应(同晶替代、离子交换、化学吸附)更加完全(Bruna et al., 2009), 从而增大了对Cd(Ⅱ)的吸附容量.
| 表 2 填料吸附Cd(Ⅱ)热力学拟合参数 Table 2 Thermodynamics parameters of Cd(Ⅱ) adsorption |
为探究Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附机理, 开展吸附动力学试验并对试验数据分别采用准一级动力学模型、准二级动力学模型、Elovich模型和颗粒内扩散模型进行拟合.拟合公式见(9)~(12).
准一级动力学和准二级动力学模型:

|
(9) |
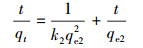
|
(10) |
式中, qe1为准一级动力学平衡吸附量(mg·kg-1);qe2为准二级动力学平衡吸附量(mg·kg-1);t为吸附时间(min);qt为t时刻的吸附量(mg·kg-1);k1为准一级动力学吸附速率常数(min-1);k2为准二级动力学吸附速率常数(g·mg-1·min-1).
Elovich模型:
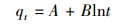
|
(11) |
式中, qt和t同上;A、B为Elovich方程吸附速率常数.
颗粒内扩散模型:

|
(12) |
式中, qt和t同上;ks为颗粒内扩散速率常数(mg·kg-1·min-0.5);C为常数, 表示吸附剂的边界层数.
表 3为天然麦饭石和Zn-LDHs覆膜改性麦饭石各吸附动力学拟合模型的相关系数R2值.从表 3可知, 天然麦饭石的准一级动力学模型拟合效果优于准二级动力学模型, 其吸附类型趋于物理吸附;对于LDHs覆膜改性麦饭石, 准一级动力学模型R2在不同初始浓度条件下呈不稳定的趋势且其值不高;而准二级动力学模型的R2均在0.99以上, 符合准二级动力学模型.
| 表 3 不同浓度下天然麦饭石和Zn-LDHs覆膜改性麦饭石吸附动力学模型的相关系数R2 Table 3 Correlation coefficient of adsorption kinetics at different concentrations |
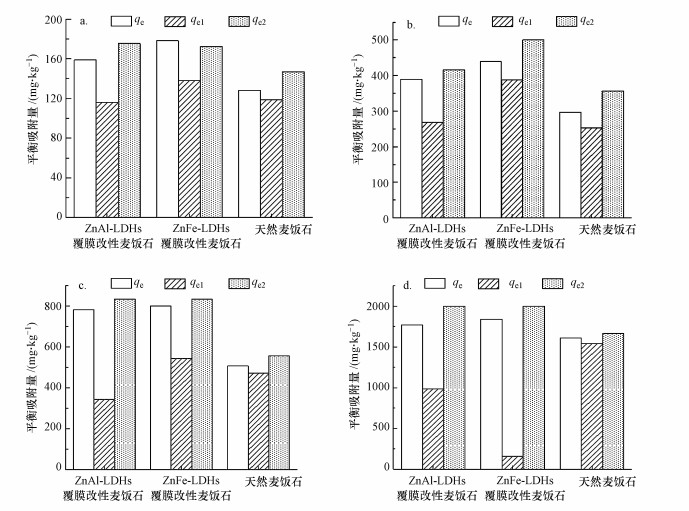
同时, 如图 6所示, 在不同初始Cd(Ⅱ)浓度下各麦饭石的平衡吸附量对比中, LDHs覆膜改性麦饭石准一级方程所拟合的平衡吸附量与试验数据结果相差较大, 准二级方程拟合的平衡吸附量与计算所得的吸附量较为吻合, 从另一个角度反映了LDHs覆膜改性麦饭石填料的吸附过程更符合准二级动力学模型, 即准二级动力学模型能更好地描述改性填料的吸附行为.这也说明LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附是以化学吸附为控制步骤的吸附过程(Lyu et al., 2019).
 |
|
图 6
不同初始Cd(Ⅱ)浓度下各麦饭石的平衡吸附量对比
(a. 1 mg·L-1, b. 4 mg·L-1, c. 8 mg·L-1, d. 16 mg·L-1) 注:图中qe为吸附试验所得平衡吸附量, qe1为拟合准一级动力学模型计算所得平衡吸附量, qe2为拟合准二级动力学模型计算所得平衡吸附量 Fig. 6 Adsorption capacity of three adsorbents at different concentrations of Cd(Ⅱ) in equilibrium time (a. 1 mg·L-1, b. 4 mg·L-1, c. 8 mg·L-1, d. 16 mg·L-1) |
颗粒内扩散模型是根据Weber和Morris所提出的理论形成的(Weber et al., 1962), 一般认为, 填料对Cd(Ⅱ)的吸附可分为4个步骤:① Cd(Ⅱ)从溶液中转移到填料表面附近;② Cd(Ⅱ)通过扩散作用穿过液膜到达填料颗粒的表面, 这一步通常被称为外扩散或传质;③填料表面的Cd(Ⅱ)通过扩散作用到达填料颗粒内部;④ Cd(Ⅱ)被填料内部吸附活性位点所吸附(周宏光, 2017).步骤①和④反应速率很快, 不是速率控制步骤, 吸附过程的速度取决于步骤②和③中最慢的一步;通过拟合内扩散模型可以确定吸附过程的控速步骤, 揭示吸附机理.表 4为填料的颗粒内扩散模型拟合参数.本实验中的颗粒内扩散模型拟合直线没有过原点, 说明颗粒扩散为吸附速率的限速因素, 但不是唯一限速因素, 可能还有其他过程共同控制吸附速率(Kumar et al., 2014);另外, 由表 4可知, ZnFe-LDHs覆膜改性麦饭石的内扩散模型的线性关系不如天然麦饭石, 说明LDHs覆膜改性之后的麦饭石对Cd(Ⅱ)吸附过程更为复杂, 为多种吸附机理共同作用.
| 表 4 填料的颗粒内扩散模型拟合参数 Table 4 Fitting parameters of intraparticle diffusion model of fillers |
同时, 本试验中的Elovich模型能更好地拟合Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附过程, R2均在0.98以上, 表明覆膜改性麦饭石在整个吸附过程中具有均匀分布的表面吸附性能(常春等, 2016).而天然麦饭石拟合的Elovich模型的R2为0.92~0.98, 拟合度不高, 说明天然麦饭石对Cd(Ⅱ)表面吸附性能不均匀, 这与天然麦饭石在等温吸附中拟合结果符合Freundlich模型一致, 天然麦饭石为非均质的多分子层吸附.这也验证了LDHs覆膜改性后能够改善麦饭石表面结构, 使其吸附位点更均匀, 有利于吸附的进行.
3.6 不同pH值条件下的吸附试验由于LDHs是在碱性条件下形成的, pH值过低易破坏LDHs结构, pH值过高则会产生Cd(OH)2沉淀, 不利于研究其吸附性能.因此本次实验选定初始Cd(Ⅱ)溶液的pH值为6、7、8的条件下进行等温吸附试验, 图 7为不同pH值条件下ZnFe-LDHs覆膜改性麦饭石的平衡吸附量.
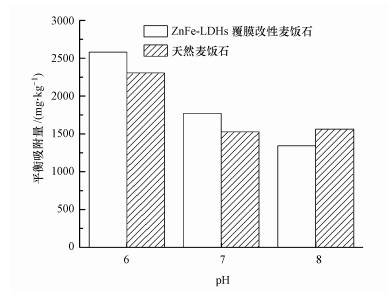 |
| 图 7 不同pH值条件下ZnFe-LDHs覆膜改性麦饭石的平衡吸附量 Fig. 7 Cd(Ⅱ)adsorption of ZnFe-LDHs modified maifanite under different of pH |
如图 7所示, 天然麦饭石在pH值为6时平衡吸附量最高, 在弱酸性条件下可能会促进天然麦饭石的吸附作用;在pH值为7~8时, 平衡吸附量无明显变化, 原因可能是天然麦饭石对溶液中pH的调节作用.高效江等发现麦饭石对重金属吸附前pH为7.82、8.81时, 而吸附后pH值都在7左右(高效江等, 1997), 因此, 溶液中麦饭石的pH值变化不大, 对其产生影响较小.同时, 试验结果表明, ZnFe-LDHs覆膜改性麦饭石的平衡吸附量随着pH升高呈逐渐降低的趋势;随着溶液中OH-含量逐渐增多, 由ZnCl2、FeCl3等参与合成的LDHs金属离子(如Zn2+, Fe3+)会与OH-产生化学沉淀, 堵塞LDHs改性麦饭石表面的孔道, 不利于其对Cd(Ⅱ)的吸附作用(Soltani et al, 2018), 而在pH值为6时能够抑制这种金属沉淀行为, 因此在pH值为6时, ZnFe-LDHs覆膜改性麦饭石对Cd(Ⅱ)吸附效果最佳, 吸附性能最好.
3.7 竞争离子吸附试验为探究水体中常见离子对ZnFe-LDHs覆膜改性麦饭石吸附的影响, 选择Mg2+、K+、PO43-、NH4+、NO3-等5种常见阴阳离子进行竞争性吸附试验;图 8为不同竞争离子条件下, ZnFe-LDHs覆膜改性麦饭石对Cd(Ⅱ)的平衡吸附量变化趋势图.
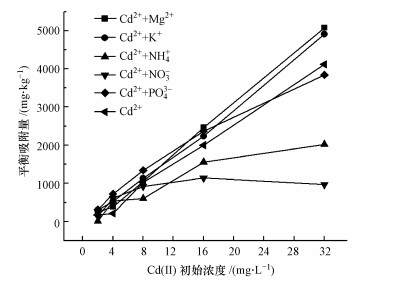 |
| 图 8 不同竞争离子条件下ZnFe-LDHs覆膜改性麦饭石平衡吸附量变化 Fig. 8 Cd(Ⅱ) adsorption of ZnFe-LDHs modified maifanite under different competitive ions |
由图 8可知, 各平衡吸附量均随Cd(Ⅱ)初始浓度升高而逐渐增大;当Cd(Ⅱ)初始浓度较低时, Mg2+、K+、PO43-、NH4+、NO3-等5种竞争离子对Cd(Ⅱ)的吸附效果无明显影响.究其原因, 在低浓度时ZnFe-LDHs覆膜改性麦饭石表面有足够的吸附位点, 此时竞争性离子对Cd(Ⅱ)吸附的影响也较小.当Cd(Ⅱ)初始浓度逐渐变大时, Mg2+、K+、PO43-这3种离子对Cd(Ⅱ)吸附无明显抑制作用, 含有Mg2+的平衡吸附量最大.而NO3-对Cd(Ⅱ)吸附具有一定的抑制, 可能与ZnFe-LDHs覆膜改性麦饭石表面的LDHs结构有关;对于一价阴离子的交换能力而言, NO3->Cl-, NO3-容易将LDHs中的Cl-交换出来, 因此部分NO3-可能会通过离子交换作用进入LDHs层间(王卫东等, 2017), 从而导致LDHs的结构发生不利于Cd(Ⅱ)吸附的变化.同时, NH4+在高Cd(Ⅱ)浓度下也会产生抑制作用, 这应可归结于麦饭石本身的特性, 麦饭石对极性分子较高的NH4+有很强的吸附作用(李娟等, 2008), 因此NH4+会优先吸附在填料表面, 占据填料的吸附位点, 从而导致麦饭石填料对Cd(Ⅱ)吸附效果变弱.
4 结论(Conclusions)1) Zn-LDHs覆膜改性有效提升麦饭石对Cd(Ⅱ)的吸附效果, 其中ZnFe-LDHs覆膜改性麦饭石的吸附效果最佳, 最大饱和吸附容量达到了2500 mg·kg-1;Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附过程为以化学吸附为主的单分子层吸附, 天然麦饭石为以物理吸附为主的多分子层吸附.
2) 麦饭石对Cd(Ⅱ)的吸附为表层扩散和内部扩散共同作用, Zn-LDHs覆膜改性麦饭石比天然麦饭石表面吸附性能更均匀, 扩散作用更为明显;且Zn-LDHs覆膜改性麦饭石对Cd(Ⅱ)的吸附为自发的放热过程;天然麦饭石为自发的吸热过程.
3) 综合来看, Zn-LDHs覆膜改性麦饭石去除水中Cd(Ⅱ)的机理主要为化学吸附、离子交换、同晶替代等;相较于天然麦饭石, ZnFe-LDHs覆膜改性麦饭石的最大饱和吸附量提升了3.5倍, 表明ZnFe-LDHs覆膜改性麦饭石是一种具有应用潜力的重金属Cd(Ⅱ)吸附剂.
Arfaoui S, Frini-Srasra N, Srasra E. 2008. Modelling of the adsorption of the chromium ion by modified clays[J]. Desalination, 222(1/3): 474-481. |
Acar E T, Ortaboy S, Atun G. 2015. Adsorptive removal of thiazine dyes from aqueous solutions by oil shale and its oil processing residues: Characterization, equilibrium, kinetics and modeling studies[J]. Chemical Engineering Journal, 276: 340-348. DOI:10.1016/j.cej.2015.04.089 |
Bruna F, Celis R, Pavlovic I, et al. 2009. Layered double hydroxides as adsorbents and carriers of the herbicide (4-chloro-2-methylphenoxy) acetic acid (MCPA): Systems Mg-Al, Mg-Fe and Mg-Al-Fe[J]. Journal of Hazardous Materials, 168(2/3): 1476-1481. |
Carja G, Niiyama H. 2005. From the organized nanoparticles of copper and vanadium containing LDHs to the small nanoparticles of mixtures of mixed oxides: A simple route[J]. Materials Letters, 59(24/25): 3078-3080. |
常春, 王胜利, 郭景阳, 等. 2016. 不同热解条件下合成生物炭对铜离子的吸附动力学研究[J]. 环境科学学报, 36(7): 2491-2502. |
陈琳荔, 邹华. 2015. 改性麦饭石对水中氮磷的去除[J]. 食品与生物技术学报, 34(3): 283-290. |
Fang C J, Zhang X L, Lei Y, et al. 2018. Nitrogen removal via core-shell bio-ceramic/Zn-layer double hydroxides synthesized with different composites for domestic wastewater treatment[J]. Journal of Cleaner Production, 181: 618-630. DOI:10.1016/j.jclepro.2018.01.249 |
Gao C G, Zhang X L, Yuan Y, et al. 2018. Removal of hexavalent chromium ions by core-shell sand/Mg-layer double hydroxides (LDHs) in constructed rapid infiltration system[J]. Ecotoxicology and Environmental Safety, 166: 285-293. DOI:10.1016/j.ecoenv.2018.09.083 |
Gao G H, Lei Y H, Dong L H, et al. 2012. Synthesis of nanocomposites of silver nanoparticles with medical stone and carbon nanotubes for their antibacterial applications[J]. Materials Express, 2(2): 85-93. DOI:10.1166/mex.2012.1056 |
高效江, 戎秋涛. 1997. 麦饭石对重金属离子的吸附作用研究[J]. 环境污染与防治, 19(4): 4-7. |
González M A, Pavlovic I, Barriga C. 2015. Cu(Ⅱ), Pb(Ⅱ) and Cd(Ⅱ) sorption on different layered double hydroxides. A kinetic and thermodynamic study and competing factors[J]. Chemical Engineering Journal, 269: 221-228. DOI:10.1016/j.cej.2015.01.094 |
Karami H. 2013. Heavy metal removal from water by magnetite nanorods[J]. Chemical Engineering Journal, 219(3): 209-216. |
孔旺盛, 刘燕. 2007. 生物污泥对染料的吸附及胞外聚合物的作用[J]. 环境科学, 28(12): 2716-2721. DOI:10.3321/j.issn:0250-3301.2007.12.009 |
Kumar P S. 2014. Adsorption of lead(Ⅱ) ions from simulated wastewater using natural waste: A kinetic, thermodynamic and equilibrium study[J]. Environmental Progress & Sustainable Energy, 33(1): 55-64. |
李娟, 张盼月, 高英, 等. 2008. 麦饭石的理化性能及其在水质优化中的应用[J]. 环境科学与技术, 31(10): 63-66. DOI:10.3969/j.issn.1003-6504.2008.10.016 |
Lyu F, Yu H, Hou T, et al. 2019. Efficient and fast removal of Pb2+ and Cd2+ from an aqueous solution using a chitosan/Mg-Al-layered double hydroxide nanocomposite[J]. Journal of Colloid and Interface Science, 539: 184-193. DOI:10.1016/j.jcis.2018.12.049 |
Nawrot T, Plusquin M, Hogervorst J, et al. 2006. Environmental exposure to cadmium and risk of cancer: A prospective population-based study[J]. Lancet Oncology, 7(2): 119-126. DOI:10.1016/S1470-2045(06)70545-9 |
Patar A, Giri S, Giri A, et al. 2016. Cadmium pollution and amphibians-Studies in tadpoles of Rana imnocharis[J]. Chemosphere, 144: 1043-1049. DOI:10.1016/j.chemosphere.2015.09.088 |
Rajeshkhanna G, Kandula S, Shrestha K R, et al. 2018. A new class of Zn1-xFex-Oxyselenide and Zn1-xFex-LDH nanostructured material with remarkable bifunctional oxygen and hydrogen evolution electrocatalytic activities for overall water splitting[J]. Small, 14: 1803638. DOI:10.1002/smll.201803638 |
沈昱, 吴艳波, 刘淑红, 等. 2016. 污水中镉含量的分光光度法测定[J]. 大连交通大学学报, 37(1): 78-81. |
Shan R R, Yan L G, Yang K, et al. 2015. Adsorption of Cd (Ⅱ) by Mg-Al-CO3-and magnetic Fe3O4/Mg-Al-CO3-layered double hydroxides: kinetic, isothermal, thermodynamic and mechanistic studies[J]. Journal of hazardous materials, 299: 42-49. DOI:10.1016/j.jhazmat.2015.06.003 |
Soltani R, Dinari M, Mohammadnezhad G. 2018. Ultrasonic-assisted synthesis of novel nanocomposite of poly(vinyl alcohol) and amino-modified MCM-41: A green adsorbent for Cd(Ⅱ) removal[J]. Ultrasonics Sonochemistry, 40: 533-542. DOI:10.1016/j.ultsonch.2017.07.045 |
汪碧华, 马凯林, 王璞君, 等. 1988. 麦饭石的净化机理[J]. 长春地质学院学报, 18(4): 423-430. |
王卫东. 2017.改性类水滑石制备及其氮磷吸附特性研究[D].北京: 北京工业大学 http://cdmd.cnki.com.cn/Article/CDMD-10005-1018704501.htm
|
Weber W J, Morris J C. 1962. Removal of biologically resistant pollutant from waste water by adsorption[J]. Advances in Water Pollution Research, 2: 231-266. |
向洋, 张翔凌, 雷雨, 等. 2018. 不同合成条件对ZnAl-LDHs覆膜改性生物陶粒除磷效果的影响[J]. 环境科学, 39(5): 2184-2194. |
杨林, 吴平霄, 刘帅, 等. 2016. 两性修饰蒙脱石对水中镉和四环素的吸附性能研究[J]. 环境科学学报, 36(6): 2033-2042. |
张翔凌, 邓礼楚, 方晨佳, 等. 2019. 不同类型LDHs负载改性麦饭石对Cr(Ⅵ)吸附性能[J]. 环境科学, 40(1): 300-309. |
张翔凌, 黄华玲, 郭露, 等. 2016. Zn系LDHs覆膜改性人工湿地沸石基质除磷机制[J]. 环境科学, 37(8): 3058-3066. |
Zhou H G, Jiang Z M, Wei S Q, et al. 2018. Adsorption of Cd(Ⅱ) from aqueous solutions by a novel layered double hydroxide FeMnMg-LDH[J]. Water Air & Soil Pollution, 229(3): 78-93. |
周宏光. 2017. FeMnMg-LDH的制备及其对环境铅镉污染的钝化效应研究[D].重庆: 西南大学 http://cdmd.cnki.com.cn/Article/CDMD-10635-1018807210.htm
|
 2019, Vol. 39
2019, Vol. 39


