炭凝胶(Carbon Gels)是近20年发展起来的一种新型多孔性纳米材料.自1987年美国Lawrence Livermore国家实验室的Pekala等用间苯二酚和甲醛作为反应前驱体, 在碳酸钠催化作用下采用溶胶-凝胶技术制备出有机气凝胶并进一步炭化得到RF炭气凝胶(Carbon Aerogel, CA)以来, 炭凝胶的制备及应用研究受到了广泛关注(文越华等, 2002).炭凝胶的制备过程包括老化、有机溶剂萃取、干燥和碳化4个阶段.根据干燥方式不同(CO2超临界干燥、亚临界干燥或常压干燥、冷冻干燥), 可将凝胶分为气凝胶(Carbon Aerogel, CA)、干凝胶(Carbon Xerogel, CX)和冷冻凝胶(Carbon Cryogel, CC).同时, 炭凝胶可制成块状、粉末状、微粒或薄膜状以适应不同的应用需要(Wu et al., 2007;Scherdel et al., 2009;Szczurek et al., 2011).炭凝胶具有丰富的孔隙率、大的比表面积和孔体积, 且它的形态及孔结构可通过调整原料的配比、间苯二酚(R)与催化剂(C)之比(R/C)、反应温度或凝胶化时间、碳化条件等条件加以调控(蒋伟阳等, 1996;Zanto et al., 2002;Job et al., 2004).作为吸附剂来说, 其最大优势在于结构的可调控性, 通过改变制备条件可改变炭凝胶材料孔结构, 以获得对吸附质的最强吸附性能, 实现对水环境中复杂污染物的去除.Celzard等(2012)制备的炭凝胶可以较好地吸附水中的有机物、卤化物及金属离子.黄燕等(2010)研究发现, 与常用炭质吸附剂相比, 炭凝胶CX800对邻二氯苯和腐殖酸的吸附量明显高于活性炭和碳纳米管;此外, 研究还发现, 较大的中孔体积和中孔分布可促进污染物的吸附, 反应30 min内即可达到吸附平衡, 说明炭凝胶对污染物的吸附速率较快.华东理工大学的张睿课题组制备了孔尺寸和凝胶微粒尺寸可调控的介孔炭凝胶, 并发现制得的炭凝胶硬度大, 比表面积大于600 m2·g-1, 孔体积大于1 cm3·g-1, 随着炭凝胶中孔尺寸的增大和凝胶颗粒尺寸的降低, 其对大分子维它命B12的吸附量增强(Long et al., 2009).Ribeiro等(2012)研究发现, 比表面积大且中孔丰富的炭凝胶对较大分子如染料酸性橙II和铬变素2R的吸附能力要明显强于孔体积较小的炭凝胶.因此, 在研究炭凝胶对较大分子污染物的吸附时, 可以通过调控合成过程中原料配比及反应条件, 制得以中孔为主的介孔炭凝胶, 以提高其吸附性能.
由于炭凝胶在水中呈现出良好的亲水性能, 其丰富的介孔结构可以同时实现不同性质及类型污染物的吸附, 并且易于吸附高水溶性、低脂溶性的大分子, 因此, 人们多将吸附目标物集中在水溶性污染物, 主要为染料(如酸性橙、甲基红)和金属离子等, 相关研究主要包括介孔炭凝胶制备工艺(原料/催化剂的筛选配比)、组分优化、吸附条件等对吸附容量的影响(Kabiri et al., 2011).然而, 通过文献分析不难发现, 目前对于介孔炭凝胶的吸附机理研究仍不够深入, 在以往描述炭凝胶吸附行为的研究中(Wu et al., 2004;Zhou et al., 2011;Magdalena et al., 2018), 只是单纯地从吸附等温线、热力学和动力学等方面去探讨其对污染物的吸附机理, 对于吸附剂进行表征的研究, 也只是做了简单的分析和介绍, 并未深入研究吸附结合键的情况.基于此, 本文主要采用溶胶-凝胶的方法, 以间苯二酚(R)和甲醛(F)为原料, 通过调节碳酸钠的添加量来改变其表面结构, 制备了一系列结构及孔径不同的介孔炭干凝胶(Mesoporous Carbon Xerogels, MCX), 并以染料孔雀石绿为污染物, 探究吸附剂的投加量、接触时间及吸附温度对吸附容量的影响.同时, 本文通过对炭凝胶进行动力学和热力学行为研究, 并对吸附剂表面官能团、孔结构和表面形貌进行分析, 深入研究其吸附构效关系, 以充分显示污染物从溶液中被吸附到吸附剂表面的过程, 进而揭示其吸附机制.
2 材料与方法(Materials and methods) 2.1 试剂和仪器实验所用吸附剂的制备原料包括间苯二酚、甲醛、碳酸钠.实验所用试剂包括浓盐酸、氢氧化钠、氯化钠, 均为分析纯, 实验用水为超纯水.实验所用污染物为阳离子型染料孔雀石绿(Malachite Green, CAS号569-64-2), 是一种具有金属光泽的翠绿色结晶体, 又称孔雀绿、碱基绿, 属于三苯甲烷类染料, 分子式为C23H25N2Cl, 极容易溶于水, 水溶液呈现蓝绿色, 能溶于甲醇、乙醇或者戊醇;在酸性条件下呈黄色, 稀释显暗黄色, 碱性条件下则会产生絮状沉淀物(陈若冰, 2007).由于连接3个苯基的碳上存在双键, 孔雀石绿容易在水生生物体内代谢形成无色的孔雀石绿(Leuco malachite Green, LGM), 分子式为C23H26N2, 这种物质连接苯基的碳都是以单键的形式存在, 所以比较稳定, 是合成孔雀石绿染料的前体物, 同时也是一种严重的工业废水污染物(张丽蓉, 2013).孔雀石绿及无色孔雀石绿具体的化学结构式如图 1所示.
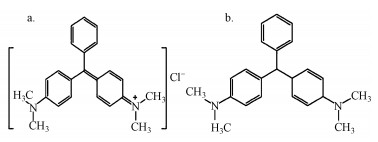 |
| 图 1 孔雀石绿(a)及无色孔雀石绿(b)的结构图 Fig. 1 Structure diagram of Malachite Green(a) and Leuco Malachite Green(b) |
实验仪器主要包括:DHG-9053A型电热鼓风干燥箱(上海一恒科学仪器有限公司)、ZD-85型气浴恒温振荡器(常州金坛高科仪器厂)、OTF-1200X管式炉(合肥科晶材料技术有限公司)、U-3900紫外可见分光光度计(日本高新技术公司)、Nicolet IS10型傅里叶变换红外光谱仪(德国BRUKER光谱仪器公司)、ASAP 2020表面积和孔隙度分析仪(美国康塔仪器公司)、TM-3000台式扫描电镜(日本日立公司).
2.2 介孔炭干凝胶的制备将10 g间苯二酚溶解在超纯水中, 并加入不同剂量的催化剂碳酸钠溶液.将溶液用磁力搅拌器中搅拌30 min后发现固体完全溶解且溶液呈现淡黄色, 接着将15 g甲醛加入到上述溶液中, 再搅拌60 min.然后将获得的水凝胶在烘箱中老化, 老化时间依次为25 ℃下1 d, 50 ℃下1 d, 80 ℃下5 d.待干燥老化后, 将凝胶置于丙酮中萃取, 最后在氮气流下在管式炉中炭化, 炭化过程为:以0.5 ℃·min-1的速度由室温升到110 ℃, 恒温5 h, 再以5 ℃·min-1的速度升到900 ℃, 恒温3 h.炭化后对样品进行研磨便得到一系列介孔炭干凝胶, 分别记为MCX100、MCX200、MCX250、MCX500、MCX1000、MCX1500、MCX2000, MCX3000 (其中, 数字表示间苯二酚与催化剂碳酸钠的物质的量比(R/C), 数字越大, 表示催化剂添加量越少).
2.3 吸附实验采用批量平衡法研究孔雀石绿在介孔炭干凝胶上的吸附性能.具体操作为:在100 mL的碘瓶中分别加入40 mL孔雀石绿水溶液, 以及一定量的介孔炭干凝胶, 盖紧后置于恒温振荡箱中;在25 ℃、180 r·min-1条件下振荡12 h, 以确保吸附达到平衡;充分吸附后, 将溶液通过滤膜进行过滤后, 用紫外分光光度计于617 nm下测得吸光度, 并计算其浓度.空白实验表明, 实验所用化合物的挥发和在瓶壁上的粘附损失可以忽略不计, 所有吸附实验和空白实验分别重复2次.
2.3.1 热力学实验在热力学吸附实验中, 设置介孔炭干凝胶的投加量为200 mg·L-1, 孔雀石绿溶液的初始浓度为10~60 mg·L-1, 分别在25、35、45 ℃的条件下进行吸附实验, 测定吸附后上清液的浓度, 根据吸附前后溶液的浓度来计算吸附容量.
2.3.2 动力学实验在动力学吸附实验中, 取一定量的介孔炭干凝胶(200 mg·L-1)加入到1000 mL 20 mg·L-1的孔雀石绿模拟废水中, 在25 ℃下进行磁力搅拌并间歇取样, 样品过滤后测定染料的浓度.
2.4 孔结构、表面形貌和官能团分析采用表面积和孔隙度分析仪对样品的比表面积和孔隙率进行测定, 实验前将样品在氮气保护下于77 ℃下进行吸附或解吸, 根据氮气的吸附等温线釆用BET法和BJH模型分别测定材料SBET(相对压力(P/P0)小于0.3)和Vtotal(P/P0为0.99), 用 t 图法计算样品的比表面积和孔体积(P/P0为0.2~0.5).采用扫描电镜(SEM)在放大100000倍的情况下观察吸附剂表面的形貌.采用傅里叶变换红外光谱法(FT-IR)检测样品的官能团和分子结构特征, 实验条件为:扫描范围400~4000 cm-1, 分辨率4.0 cm-1, 扫描32次.
3 结果与讨论(Results and discussion) 3.1 不同吸附剂及其投加量对孔雀石绿吸附效果的影响图 2展示了不同种类的吸附剂及其用量对孔雀石绿去除效果的影响.由图可知, 随着催化剂碳酸钠添加量的增加, 制备得到的吸附剂的吸附量先增大后减小, 其中以间苯二酚与碳酸钠的物质的量比(R/C)为1000:1(即MCX1000)时所制备的介孔炭干凝胶的吸附效果最佳.这主要是由于该比值会影响炭干凝胶的孔径、孔道结构和比表面积等特征.当添加量增大时, 介孔炭干凝胶的孔径变大, 密度下降, 且其比表面积降低(表 4), 从而形成聚合物状的介孔炭干凝胶, 反之, 则会形成胶体颗粒状的介孔炭干凝胶(文越华等, 2002).同时, 碳酸钠的添加量会影响溶液的pH值, 过高或者过低的pH值都会对缩聚反应产生影响(Honoria et al., 2009).因此, 选择适量的催化剂添加量有利于提高制备的介孔炭干凝胶的吸附性能.
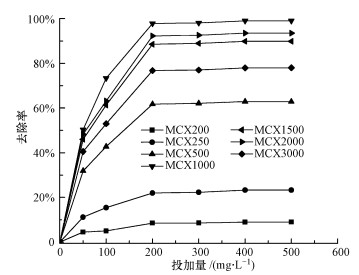 |
| 图 2 不同种类的吸附剂投加量对孔雀石绿的吸附效果的影响 Fig. 2 Effect of different dosages of adsorbent on the sorption of malachite green |
| 表 4 吸附前MCX1000、MCX500、MCX1500及吸附后MCX1000的比表面积和孔体积 Table 4 Specific surface area and pore volume of MCX1000, MCX500, MCX1500 before adsorption and MCX1000 after adsorption |
在吸附初始阶段, 随着吸附剂投加量的增加, 去除率迅速上升, 当投加量达到200 mg·L-1时, 再增加投加量, 去除率变化趋势已经不明显.这主要是因为一开始随着吸附剂投加量的增加, 其总体比表面积和有效的活性位点增加, 因而孔雀石绿的去除率迅速提高;之后随着投加量的继续增加, 吸附剂之间出现重叠和聚合, 导致可以利用的吸附剂的比表面积不再增加(钟倩倩等, 2018), 因而孔雀石绿的去除率提升不明显.当投加量增加到200 mg·L-1时, 吸附剂已经达到饱和, 因此, 确定介孔炭干凝胶MCX1000的最佳投加量为200 mg·L-1.
3.2 吸附动力学本试验同时研究了介孔炭干凝胶MCX1000对孔雀石绿的动力学去除过程, 结果如图 3所示.由图可知, 该吸附反应在0 ~10 min范围内的去除率迅速上升, 直到180 min后吸附达到平衡.主要是因为制备得到的介孔炭干凝胶具有丰富的介孔, 当它与染料接触时, 染料分子迅速被吸附, 并向其内部扩散, 但随着吸附时间的继续延长, 吸附剂表面的活性位点逐渐减少, 染料分子无法再向其内部扩散, 故逐渐达到吸附平衡(岳钦艳等, 2007;张建等, 2009;季雪琴等, 2016).
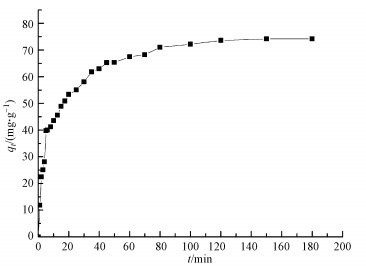 |
| 图 3 接触时间对MCX1000吸附容量的影响 Fig. 3 Effect of contact time on MCX1000 sorption capacity |
分别采用伪一阶和伪二阶模型对介孔炭干凝胶的吸附结果进行拟合, 拟合后的参数列在表 1中, 模型公式分别如式(1)和式(2)所示.
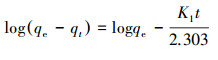
|
(1) |

|
(2) |
| 表 1 MCX1000的伪一阶和伪二阶模型拟合参数 Table 1 Pseudo-first and pseudo second-order model fitting parameters of MCX1000 |
式中, qe和qt分别为吸附平衡和t时刻时MCX1000对孔雀石绿的吸附容量(mg·g-1), K1为伪一阶速率常数(min-1), K2为伪二阶速率常数(g·mg-1·min-1).
由拟合系数(R2)可知, 伪二阶动力学模型能够更好地描述该吸附过程, 利用伪一阶模型计算的最大吸附容量为48.58 mg·g-1, 而利用伪二阶模型计算的最大吸附容量为76.92 mg·g-1, 且与实验值(73.58 mg·g-1)非常接近.
3.3 吸附热力学吸附热力学是分析温度对吸附影响的有效手段.介孔炭干凝胶MCX1000分别在不同温度下对孔雀石绿进行等温吸附的结果如图 4所示, 并通过下列方程对数据进行热力学拟合, 结果列于表 2中.
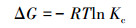
|
(3) |
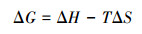
|
(4) |
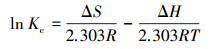
|
(5) |
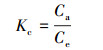
|
(6) |
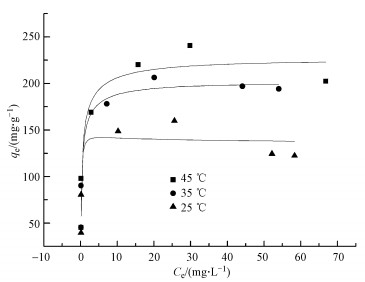 |
| 图 4 温度对MCX1000吸附容量的影响 Fig. 4 Effect of temperature on MCX1000 sorption capacity |
| 表 2 MCX1000热力学拟合参数 Table 2 Thermodynamic fitting parameters of MCX1000 |
式中, Ca和Ce分别是介孔炭干凝胶吸附的和吸附后残留的孔雀石绿浓度(mg·L-1);R是通用气体常数(8.314 J·mol-1·K-1);ΔG(kJ·mol-1)、ΔH0(kJ·mol-1)和ΔS0(kJ·mol-1·K-1)分别表示吸附反应过程中自由能变化、焓变和熵变.
ΔH0为正值, 表明此吸附是一个吸热过程, 升高温度有利于孔雀石绿分子克服空间位阻, 加速吸附的进行;ΔG为负值, 表明该吸附过程是自发进行的;ΔS0为正值, 表明体系随着反应的进行其混乱度增加.这是由于吸附过程中染料的阳离子替换了炭干凝胶表面的水分子, 而置换出来的水分子数量大于染料分子, 所以导致混乱度增加(梁琼等, 2016).
通过最适合的等温模型可以解释污染物的吸附机理.因此, 本文根据Langmuir和Freundlich等温方程对数据进行分析, 拟合结果见表 3, 其中, Langmuir和Freundlich等温线方程分别如式(7)、(8)所示.
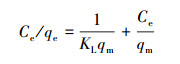
|
(7) |
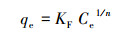
|
(8) |
| 表 3 MCX1000的等温拟合参数 Table 3 Isothermal fitting parameters of MCX1000 |
式中, Ce为孔雀石绿的平衡浓度(mg·L-1);qm为理论上最大单层吸附容量(mg·g-1);KL为Langmuir吸附平衡常数(L·mg-1), 与吸附剂对溶质的亲和力有关;KF((mg·g-1)(mg·L-1)-n)和n均为Freundlich吸附等温线常数, 分别是表示吸附能力和吸附强度的指标.
由可决系数可知, Langmuir等温线模型更加适合用来描述孔雀石绿在介孔炭干凝胶上的吸附, 说明该吸附反应的吸附方式为单分子层吸附(郎林等, 2014), 该结果与黄燕(2010)利用炭干凝胶对腐殖酸的吸附处理结果相似.同时发现MCX1000的qm值随着温度的升高而增加, 表明该吸附剂对孔雀石绿的吸附过程是吸热反应.随着温度的升高, 其吸附容量增加, 这是由其表面孔尺寸的增大和吸附剂表面的活化引起的.由Langmuir吸附等温线方程计算得到的MCX1000的最大吸附容量(qm, 318 K)最高可达208.33 mg·g-1, 与实验值比较接近.
3.4 吸附机理研究 3.4.1 孔结构分析图 5可知, MCX500的中孔的平均直径分布在2~12 nm范围内;MCX1000的微孔的平均直径分布在1.7~2.0 nm范围内, 而中孔的平均直径分布在2~32 nm范围内;MCX1500的微孔的平均直径分布在1.7~2.0 nm范围内, 而中孔的平均直径分布在2~45 nm范围内.表明这些材料由大量的中孔(2~50 nm)组成(Chen et al., 2017), 这与余呈祥(2013)对炭干凝胶孔结构分析的结果相似, 同时表明催化剂的添加量可以改变制备后的吸附剂的孔径大小.此外, 由表 4可知, 比表面积和介孔表面积是影响吸附效果的重要因素, 比表面积越大, 其吸附性能越强.
 |
| 图 5 不同吸附剂表面的孔径分布 Fig. 5 Pore size distribution of different adsorbent surfaces |
制备的3种吸附剂(MCX500、MCX1000、MCX1500)的SEM扫描电镜图如图 6所示.从图中可以发现, 炭干凝胶由许多纳米级颗粒组成, 且颗粒大小有着显著差异, MCX500的粒径大小在10 nm左右, MCX1000的粒径在50 nm左右, 而MCX1500的粒径在100 nm左右.因此可以认为, 炭干凝胶颗粒的尺寸随着催化剂添加量的减小而增大.这主要是因为制备时初始溶液的酸碱性对吸附剂的性质和表面形貌会产生一定的影响, 随着碳酸钠添加量的增加, 其pH值也随之上升, 从而影响吸附剂表面的性质(黄燕, 2010).从吸附前后MCX1000的电镜照片可知, 吸附剂在吸附孔雀石绿后, 其表面变得更加平整和饱满, 可见孔雀石绿被均匀地吸附在MCX1000的孔表面上(胡康博等, 2010).
 |
| 图 6 炭干凝胶的扫描电镜图(a.MCX500, b.MCX1500, c.MCX1000, d.吸附后的MCX1000) Fig. 6 SEM of mesoporous carbon xerogels |
由图 7可知, 吸附前的MCX1000在3323 cm-1处主要为羟基伸缩振动峰, 这主要是由炭干凝胶材料的特征所致, 也有可能是吸附剂表面存在水分引起的(Hao et al., 2016).在1090 cm-1处的吸收峰可以归属于—C—O的存在, 说明制备后的吸附剂中含有羧基, 其产生主要是由于原料中的甲醛与间苯二酚发生了缩聚反应, 这与文献中所述情况类似(Magdalena et al., 2018).通过比较MCX1000吸附孔雀石绿前后的谱图可以发现, 吸附后的MCX1000出现了2个新的峰, 即C—N峰和C—C峰, 而观察孔雀石绿的结构式可以发现孔雀石绿表面存在Ar—N(芳香族—氮键)和C—Ar(碳—芳香族键), 故在图 7中1358 cm-1和1622 cm-1处的吸收峰分别属于孔雀石绿的Ar—N键的伸缩振动吸收峰和Ar—C键的伸缩振动吸收峰.上述结果可以表明, MCX1000在吸附后, 孔雀石绿被吸附到炭干凝胶表面, 这与张丽蓉(2013)利用海泡石对孔雀石绿进行吸附处理的结果相似.同时发现在吸附孔雀石绿染料后, —OH和—C—O振动峰分别被蓝移至3415 cm-1和1150 cm-1处, 说明吸附反应后, 其羟基和羧基附近的基团发生了变化(孙运飞等, 2016), 这是由于阳离子染料孔雀石绿上含氮离子或官能团与介孔炭干凝胶表面的—O—H和—C—O之间存在静电作用、氢键作用及范德华力的作用(Faizah et al., 2018).
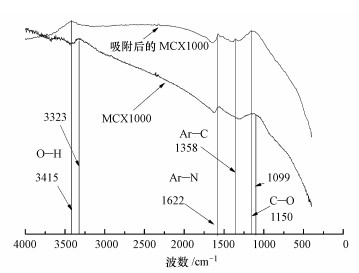 |
| 图 7 吸附前后MCX1000的红外分析光谱图 Fig. 7 FTIR spectra of MCX1000 before and after sorption |
1) 在催化剂不同添加量情况下制备的一系列炭干凝胶, 其对孔雀石绿的吸附容量随着催化剂添加量的减少先增大后减小, 并当间苯二酚与催化剂碳酸钠的物质的量比为1000:1(即MCX1000)时, 吸附效果最佳, 且其最适宜投加量为200 mg·L-1.
2) 随着催化剂添加量的增加, 炭干凝胶的粒径和孔径逐渐增大, 同时发现比表面积和介孔表面积是影响炭干凝胶吸附性能的重要因素, 比表面积和介孔表面积越大, 炭干凝胶的物理吸附性能越强, 这与吸附试验的数据相对应, 即MCX1000的比表面积和介孔面积最大, 相应的其对孔雀石绿的吸附量也最大.
3) 炭干凝胶对孔雀石绿的吸附行为可以用伪二阶动力学模型很好地描述, 其吸附等温线符合Langmuir方程, 在45 ℃时最大吸附量为208.33 mg·g-1, 该吸附过程是一个自发的吸热过程, 同时孔雀石绿上含氮离子或官能团与介孔炭干凝胶表面的羟基和羧基之间存在静电作用、氢键作用及范德华力的作用.
Álvarez S, Ribeiro R S, Gomes H T, et al. 2015. Synthesis of carbon xerogels and their application in adsorption studies of caffeine and diclofenac as emerging contaminants[J]. Chemical Engineering Research and Design, 95: 229–238.
DOI:10.1016/j.cherd.2014.11.001
|
Celzard A, Fierro V, Amaral-Labat G. 2012. Chapter 7-Adsorption by Carbon Gels[M]. Amsterdam: Elsevier.: 207–244.
|
陈若冰.2017.高浓度孔雀石绿染料废水的微波处理研究[D].成都: 四川师范大学
|
Chen L, Ji T, Mu L W, et al. 2017. Pore size dependent molecular adsorption of cationic dye in biomass derived hierarchically porous carbon[J]. Journal of Environmental Management, 196: 168–177.
DOI:10.1016/j.jenvman.2017.03.013
|
Faizah N, Hamid N S A, Suah F B M, et al. 2018. Adsorption of malachite green from aqueous solution by using novel chitosan ionic liquid beads[J]. International Journal of Biological Macromolecules, 107: 1270–1277.
DOI:10.1016/j.ijbiomac.2017.09.111
|
Hao P P, Ren J, Yang L L, et al. 2016. Direct and generalized synthesis of carbon-based yolk-shell nanocomposites from metal-oleate precursor[J]. Chemical Engineering Journal, 283: 1295–1304.
DOI:10.1016/j.cej.2015.08.069
|
Honoria F G, Goncalves F, Jose L, et al. 2009. Synthesis and characterization of nitrogen-doped carbon xerogels[J]. Science Direct, 47: 2032–2039.
|
胡康博, 王毅力, 李春荣, 等. 2010. 改性蒙脱土颗粒吸附直接染料的分形特征[J]. 环境科学学报, 2010, 30(11): 2174–2182.
|
黄燕.2010.炭干凝胶吸附和催化氧化处理微污染源水中特征污染物的研究[D].杭州: 浙江大学
http://cdmd.cnki.com.cn/Article/CDMD-10335-2010166334.htm |
季雪琴, 吕黎, 陈芬, 等. 2016. 秸秆生物炭对有机染料的吸附作用及机制[J]. 环境科学学报, 2016, 36(5): 1648–1654.
|
蒋伟阳, 张波, 周斌, 等. 1996. 间苯二酚-甲醛有机气凝胶的结构控制研究[J]. 材料科学与工艺, 1996, 4(2): 70–75.
|
Job N, Pirard R, Marien J, et al. 2004. Porous carbon xerogels with texture tailored by pH control during sol-gel process[J]. Carbon, 42(3): 619–628.
DOI:10.1016/j.carbon.2003.12.072
|
Kabiri K, Omidian H, Zohuriaan-Mehr M, et al. 2011. Superabsorbent hydrogel composites and nanocomposites:A review[J]. Polymer Composites, 32(2): 277–289.
DOI:10.1002/pc.v32.2
|
郎林, 江林. 2014. 碳纳米管对孔雀石绿的吸附特性[J]. 环境科学与技术, 2014, 37(12): 166–173.
|
梁琼, 汤斌斌, 杨胜祥, 等. 2016. 改性山核桃外果皮炭对碱性染料的吸附特性研究[J]. 工业水处理, 2016, 36(2): 51–54.
|
Long D H, Zhang R, Qiao W M, et al. 2009. Biomolecular adsorption behavior on spherical carbon aerogels with various mesopore sizes[J]. Journal of Colloid and Interface Science, 331(1): 40–46.
DOI:10.1016/j.jcis.2008.11.026
|
Magdalena P K, Joanna G, Robert P, et al. 2018. Removal of rhodamine B from water by modified carbon xerogels[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 543: 109–117.
|
Ribeiro R S, Fathy N A, Attia A A, et al. 2012. Activated carbon xerogels for the removal of the anionic azo dyes Orange Ⅱ and Chromotrope 2R by adsorption and catalytic wet peroxide oxidation[J]. Chemical Engineering Journal, 195: 112–121.
|
Scherdel J, Reichenauer G. 2009. Carbon xerogels synthesized via phenol-formaldehyde gels[J]. Microporous and Mesoporous Materials, 126: 133–142.
DOI:10.1016/j.micromeso.2009.05.033
|
孙运飞, 李文文, 汪燕南, 等. 2016. 磁性生物炭的制备及其吸附性能的研究[J]. 工业水处理, 2016, 36(3): 54–57.
|
Szczurek A, Amaral-Labat G, Fierro V, et al. 2011. The use of tannin to prepare carbon gels.Part Ⅰ:Carbon aerogels[J]. Carbon, 49(8): 2773–2784.
DOI:10.1016/j.carbon.2011.03.007
|
文越华, 曹高萍. 2002. 介孔炭干凝胶的研究进展[J]. 炭素, 2002, 110(2): 32–37.
DOI:10.3969/j.issn.1001-8948.2002.02.005 |
Wu X B, Wu D C, Fu R W. 2007. Studies on the adsorption of reactive brilliant red X-3B dye on organic and carbon aerogels[J]. Journal of Hazardous Materials, 147(3): 1028–1036.
DOI:10.1016/j.jhazmat.2007.01.139
|
Wu Z J, Ahn L S, Lee C H, et al. 2004. Enhancing the organic dye adsorption on porous xerogels[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 240: 157–164.
|
余呈祥.2013.含氮官能团改性炭干凝胶用于重金属离子的吸附研究[D].杭州: 浙江大学
http://cdmd.cnki.com.cn/Article/CDMD-10335-1014226082.htm |
岳钦艳, 解建坤, 高宝玉, 等. 2007. 污泥活性炭对染料的吸附动力学研究[J]. 环境科学学报, 2007, 27(9): 1431–1438.
DOI:10.3321/j.issn:0253-2468.2007.09.004 |
Zanto E J, Al-Muhtaseb S A, Ritter J A. 2002. Sol-gel-derived carbon aerogels and xerogels:Design of experiments approach to materials synthesis[J]. Industrial & Engineering Chemistry Research, 41(13): 3151–3162.
|
张建, 陈素红, 张成禄, 等. 2009. 水枝锦活性炭对孔雀石绿的吸附性能研究[J]. 环境污染与防治, 2009, 31(3): 1–5.
DOI:10.3969/j.issn.1001-3865.2009.03.002 |
张丽蓉.2013.有机改性海泡石对染料孔雀石绿的吸附试验研究[D].长沙: 湖南大学
http://cdmd.cnki.com.cn/Article/CDMD-10532-1014119827.htm |
钟倩倩, 沈丽, 王磊, 等. 2018. 浒苔基吸附剂对结晶紫的吸附性能研究[J]. 工业水处理, 2018, 38(1): 39–43.
|
Zhou G L, Tian H Y, Sun H Q, et al. 2011. Synthesis of carbon xerogels at varying sol-gel pHs, dye adsorption and chemical regeneration[J]. Chemical Engineering Journal, 171: 1399–1405.
DOI:10.1016/j.cej.2011.05.054
|
 2019, Vol. 39
2019, Vol. 39


