2. 成都理工大学环境学院, 成都 610059;
3. 南京大学环境学院, 南京 210023
2. Institute of Environment, Chengdu University of Technology, Chengdu 610059;
3. School of the Environment, Nanjing University, Nanjing 210023
随着工业经济的发展, 印染废水的污染日趋严重, 因此, 探索染料废水处理技术已成为近年来研究的热点(廉菲等, 2012;闫国伦, 2018;胡潇等, 2018).光催化法是一种比较热门的处理印染废水的方法(郭烨等, 2018;瓮青松等, 2016), 而BiOCl是具有很好光催化活性的铋系半导体材料(王晓雯等, 2014;黄文师等, 2018;毛晓明等2018), 其独特的层状结构使其在光催化过程中有足够空间来极化相应原子及原子轨道, 这一诱导偶极矩能够分离空穴与电子, 增加其光催化性能(杨冰叶等, 2017;Tanveer et al., 2018).Xie等(2014)合成了不同Sn掺杂量的Sn-doped BiOCl, 并对合成样品的光催化活性进行了评价, 结果显示, Sn掺杂能明显提高BiOCl对苯甲酸(BA)和罗丹明B(RhB)的脱色率, Sn掺杂量10%时光催化活性最好.韩珊珊等(2015)研究发现, 氙灯光照3.5 h后BiOCl对5 mg·L-1的罗丹明B的脱色率达到98.9%.Zhang等(2006)研究发现, 水解法合成的粉末状BiOCl在对甲基橙模拟废水的光催化降解反应中, 比TiO2的催化性能更好.实验表明, BiOCl对印染废水的去除具有很高的潜力(刘国等, 2017;练涛等, 2017;卢海晶, 2014).
针对工业废水处理来制备高效且便于回收的光催化复合材料, 这就要求所制备的光催化复合材料需具有化学稳定性高、水溶性好、生物相容性强等特点(李忠翠, 2016;Wang et al., 2013).鉴于磁偶极子引力和体积大小效应的原因, 磁性光催化材料的化学稳定性一般比较差, 容易相互团聚, 还容易被氧化(Chai et al., 2009;Wang et al., 2012), 这些也是磁性光催化材料难以被直接应用的原因(童玲, 2014).研究发现, SiO2具有较好的生物相容性及抗分解能力, 在磁性Fe3O4表面包裹一层SiO2后, 能有效地屏蔽磁偶极子的相互作用, 从而提高磁性光催化材料的水溶性、化学稳定性及生物相容性(Ding et al., 2012).
Yu等(2014)以氯化铁和醋酸钠为原料, 加聚乙醇2000作为分散剂, 用水热法制备出直径600 nm左右的磁性Fe3O4微球, 再以正硅酸乙酯为硅源, 制备出Fe3O4/nSiO2后加入溴化十六烷三甲基铵(CTAB), 制备成Fe3O4/nSiO2/CTAB/SiO2, 将CTAB溶解掉后得到半径约为500 nm的Fe3O4/nSiO2/mSiO2材料, 发现该材料具有分散均匀且层次分明的核-壳结构, 还具有优秀的磁响应性能.针对BiOCl回收困难的缺点, 本研究以微球型四氧化三铁(Fe3O4)为核, 在Fe3O4上包覆BiOCl, 使催化剂具有磁性, 并通过磁性分离有效回收催化剂.同时, 利用二氧化硅(SiO2)能够有效阻止粒子团聚且具有高稳定性的特点, 加入SiO2作为该复合催化剂的中间层, 通过在可见光条件下光催化降解亚甲基蓝以探究BiOCl/SiO2/Fe3O4的光催化性能.
2 实验部分(Experiments) 2.1 材料与仪器试剂:三氯化铁(FeCl3·6H2O)为优级纯, 亚甲基蓝为试剂纯, 氯化亚铁(FeCl2·4H2O)、正硅酸乙酯((C2H5)4SiO4)、无水乙醇(C2H5OH)、氨水(NH3·H2O)、硝酸铋(Bi(NO3)3·5H2O)、氮气(N2)、乙二醇(C2H6O2)、PEG-2000(HO(CH2CH2O)nH)、氯化钾(KCl)均为分析纯.
仪器:TB-214型电子天平(北京赛多利斯仪器系统有限公司)、JJ-1B型电动搅拌器(金坛市科析仪器有限公司)、UPW-50S型超纯水器(北京市历元电子仪器技贸公司)、TD-500型台式离心机(四川蜀科仪器有限公司)、DGX-9073B-1型电热鼓风干燥箱(北京赛多利斯仪器系统有限公司)、Nicolet 6700型傅里叶红外光谱仪(赛默飞世尔科技公司)、PHS-25型pH检测仪(上海雷磁仪器厂)、JSM-7001 F型扫描电子显微镜(日本电子株式会社)、D/max-2500型X射线衍射仪(日本理学公司)、UV-3600型紫外可见漫反射光谱仪(日本岛津公司)、聚四氟乙烯水热反应釜等.
2.2 催化剂的制备Fe3O4纳米粒子的制备:以氯化亚铁和三氯化铁为原料, 采用化学共沉淀法制备Fe3O4纳米粒子.具体实验步骤为:称取FeCl3·6H2O(28 mmol)和FeCl2·4H2O(16 mmol)于250 mL三口烧瓶中, 在氩气的保护下加入150 mL去离子水, 磁力搅拌使其迅速溶解, 混合均匀;温度升至80 ℃, 再通过恒压漏斗向烧瓶内快速滴加氨水至出现大量黑色沉淀, 调节pH到9~10, 继续快速搅拌1 h, 然后停止搅拌, 冷却至室温;再用强磁体进行固液分离, 之后用去离子水反复清洗至固液分离后上清液至中性, 再用无水乙醇清洗3次, 于60 ℃真空干燥12 h, 研磨, 收集备用.
SiO2/Fe3O4复合粒子的制备:采用Stober水解法制备SiO2包覆Fe3O4纳米粒子, 具体操作为:称取0.8 g Fe3O4粒子于250 mL三口烧瓶中, 加入80 mL无水乙醇、20 mL去离子水, 超声分散30 min, 再进行机械搅拌;然后加入4 mL TEOS(正硅酸乙酯)待搅拌均匀, 再迅速加入4 mL氨水之后持续搅拌12 h, 之后利用强磁体进行固液分离, 并用去离子水多次清洗, 直到上清液呈中性, 再用无水乙醇清洗3次, 在60 ℃条件下真空干燥12 h, 研磨, 收集备用.
BiOCl/SiO2/Fe3O4的制备:采用水热法制备BiOCl/SiO2/Fe3O4, 具体操作为:称取Bi(NO3)3·5H2O(1 mmol)和KCl(2.2 mmol)于30 mL去离子水中, 磁力搅拌30 min, 再称取Fe3O4/SiO2复合粒子0.1 g于上述溶液中, 超声分散30 min, 再将均匀混合的溶液加入到30 mL水热反应釜中密闭;然后将反应釜放入烘箱中, 在180 ℃的温度下反应12 h, 待反应结束后, 取出反应釜冷却至室温, 再取出反应产物, 利用强磁体进行固液分离, 先用去离子水清洗多次至中性, 再用无水乙醇清洗3次, 然后在60 ℃下真空干燥12 h, 研磨, 收集.
2.3 可见光催化性能评价通过亚甲基蓝在水溶液中的光降解来评价BiOCl/SiO2/Fe3O4催化剂的光催化活性.取100 mL 10 mg·L-1亚甲基蓝溶液于石英夹套烧杯, 加入0.05 g光催化剂, 在超声条件下暗反应30 min以达吸附-脱附平衡, 并用移液管取5 mL样品过滤待测;然后在300 W氙灯光源下进行光催化反应(使用滤光片滤掉λ < 420 nm的光, 以保证反应在可见光激发条件下进行), 光催化过程中石英夹套烧杯通入冷却水保证体系恒温, 每20 min用移液管取5 mL样品过滤, 取待测液在λ=664 nm下测其吸光度, 按式(1)计算亚甲基蓝脱色率η.
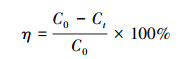
|
(1) |
式中, C0为亚甲基蓝的初始浓度(mg·L-1), Ct为吸附后亚甲基蓝的浓度(mg·L-1).
3 结果与讨论(Results and discussion) 3.1 表征与分析 3.1.1 SEM与TEM分析采用TEM对已制备好的Fe3O4及BiOCl/SiO2/Fe3O4催化剂样品的表面形貌进行表征, 结果如图 1所示.其中, 图 1a是采用化学共沉淀法制备的SiO2/Fe3O4的透射电镜图, 可以看出, 其形貌为球状, 且球状外表包裹着一层SiO2;图 1b和1c分别为采用水热法制备的BiOCl/SiO2/Fe3O4催化剂的透射电镜和扫描电镜图, 可以看出, 产物具有清晰的球状结构, 其大小为纳米级, 球状表面有片状BiOCl, 且完全、均匀地负载在SiO2/Fe3O4上.
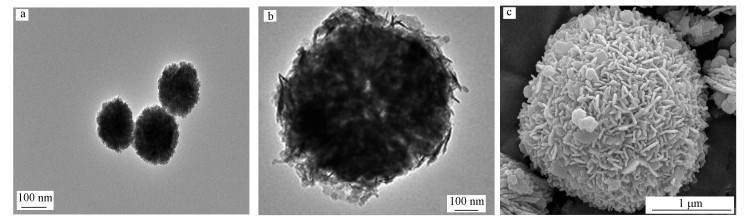 |
| 图 1 SiO2/Fe3O4 (a)、BiOCl/SiO2/Fe3O4 (b)的TEM图及BiOCl/SiO2/Fe3O4的SEM图(c) Fig. 1 TEM images of SiO2/Fe3O4(a), BiOCl/SiO2/Fe3O4(b) and SEM image of BiOCl/SiO2/Fe3O4(c) |
采用X射线衍射仪(XRD)对BiOCl/SiO2/Fe3O4进行表征, 结果如图 2a所示.SiO2的特征衍射峰分别与Fe3O4标准卡片(JCPDS No.74-0748)、四方晶系BiOCl的标准卡片(JCPDS No.82-0485)﹑SiO2的标准卡片(JCPDS N0.51-1381)相吻合, 未发现其他晶相和杂质峰, 说明合成的BiOCl/SiO2/Fe3O4复合物纯度较高.谱图表明, 该法制备的催化剂结晶度好, 结构完整且纯度高.谱图中BiOCl衍射峰在2θ为12.037°、25.933°、32.586°、33.555°时分别出现了BiOCl的(001)、(101)、(110)及(102)特征峰, 其峰型尖、高且窄, 说明BiOCl晶相的形成, 其结晶度较好.谱图中Fe3O4的衍射峰较弱, 这是由于Fe3O4的含量相对较低, 并且被SiO2及BiOCl包裹住.
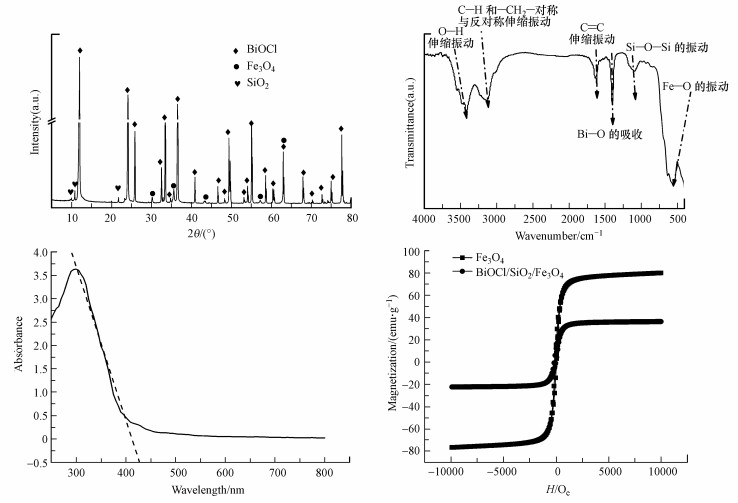 |
| 图 2 BiOCl/SiO2/Fe3O4的XRD(a)、FTIR(b)、UV-Vis(c)及磁滞回线图(d) Fig. 2 XRD(a)、FTIR(b)、UV-Vis(c) and magnetic hysteresis loops(d) of BiOCl/SiO2/Fe3O4 |
图 2b所示为BiOCl/SiO2/Fe3O4复合微粒的红外光谱表征结果.可以看出, 3500 cm-1处为O—H的伸缩振动且吸收带比较宽, 3120 cm-1处的—CH2—是乙醇的对称与反对称伸缩振动, 因为在制备过程中有乙二醇为溶剂的步骤, 表明有醇类的存在.在1630 cm-1处是C═C的伸缩振动, 为产物表面的结合水分子吸收峰.1390 cm-1处为Bi—O的吸收, 1090 cm-1处吸收峰为Si—O—Si反对称伸缩振动, 567 cm-1处特征吸收峰为Fe—O的振动吸收.
3.1.4 UV-Vis分析光催化剂的光吸收性能决定着其禁带宽度, 通过测定BiOCl的光吸收性能, 便可获得其禁带能, 从而对光催化行为进行预测.本文通过UV-Vis对制备的BiOCl/SiO2/Fe3O4磁性光催化剂进行了表征, 结果见图 2c.
以(ahv)1/2对光子能量(hv)做图, 将图中直线部分延长, 其与x轴交点的坐标值就是BiOCl/SiO2/Fe3O4的禁带能.从图中可以看出, BiOCl/SiO2/Fe3O4磁性光催化剂对光的吸收边带即吸收波长阈值λg为445 nm.根据式(2)计算样品的禁带宽度, 得到BiOCl/SiO2/Fe3O4的禁带宽度为2.78 eV, 预示着样品具有较好的可见光响应.
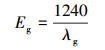
|
(2) |
式中, Eg为半导体材料禁带宽度(eV), λg为半导体材料吸收波长(nm).
3.1.5 振动样品磁强计(VSM)采用震动样品磁强计来测试BiOCl/SiO2/Fe3O4催化剂的磁滞回线, 结果见图 2d.结果表明, Fe3O4的饱和磁化强度为80 emu·g-1, BiOCl/SiO2/Fe3O4的饱和磁化强度为37 emu·g-1.这是因为没有磁性的SiO2包裹在Fe3O4的表面, BiOCl也负载在微球的表面, 从而影响了复合材料的磁化强度.BiOCl/SiO2/Fe3O4和Fe3O4都表现出很高的顺磁性, 剩余磁化强度接近零.虽然BiOCl/SiO2/Fe3O4的磁化强度弱于Fe3O4, 但其磁性完全可以满足磁性回收的要求.
3.2 BiOCl/SiO2/Fe3O4可见光催化性能与分析BiOCl和BiOCl/SiO2/Fe3O4光催化剂对亚甲基蓝的降解效果如图 3所示, 其中, 亚甲基蓝初始浓度为10 mg·L-1, BiOCl/SiO2/Fe3O4和BiOCl的剂量都为0.5 g·L-1.由图可知, 在没有催化剂的情况下, 亚甲基蓝溶液的浓度几乎没有改变, 说明亚甲基蓝自身的光分解可以忽略不计.在暗吸附的过程中, 亚甲基蓝的浓度几乎没有变化, 说明亚甲基蓝的降解过程是一个光驱动的反应过程, 同时也说明催化剂经过暗吸附平衡后, 对活性的影响可以忽略.一般情况下, 材料比表面积对染料的褪色作用表现在暗吸附中, 不管催化剂是BiOCl还是BiOCl/SiO2/Fe3O4, 亚甲基蓝的浓度都几乎没有变化.随着光催化反应的进行, 亚甲基蓝的脱色率逐渐增大, 当催化剂为BiOCl/SiO2/Fe3O4时, 光催化反应120 min后亚甲基蓝的脱色率达到93.2%;当催化剂为BiOCl时, 光催化反应120 min后亚甲基蓝的脱色率达到77.2%.BiOCl/SiO2/Fe3O4催化剂对亚甲基蓝的脱色率远大于单纯的BiOCl催化剂, 这是因为材料的比表面对光催化活性有很大影响, BiOCl/SiO2/Fe3O4的比表面积较大, 具有更多的活性位点, 因而其光催化活性也会更高.
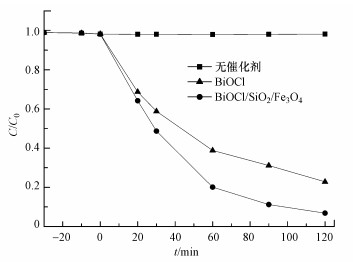 |
| 图 3 BiOCl和BiOCl/SiO2/Fe3O4催化剂对亚甲基蓝的降解曲线 Fig. 3 Degradation curve of methylene blue by BiOCl and BiOCl/SiO2/Fe3O4 catalysts |
不同投加量的BiOCl/SiO2/Fe3O4光催化剂对亚甲基蓝的降解效果如图 4a所示, 其中, 亚甲基蓝初始浓度为10 mg·L-1, BiOCl/SiO2/Fe3O4的剂量分别设为0、0.1、0.2、0.3、0.5和0.7 g·L-1.结果表明, 在催化剂对亚甲基蓝的暗吸附中, 亚甲基蓝的浓度几乎没有变化;当催化剂投加量从0.1 g·L-1增加到0.7 g·L-1时, 其对亚甲基蓝的降解具有积极的影响, 降解效率显著增加, 并在BiOCl/SiO2/Fe3O4投加量为0.5 g·L-1时达到最优, 120 min后亚甲基蓝降解效率达到93.2%.然而, 当BiOCl/SiO2/Fe3O4投加量进一步增加到0.7 g·L-1时, 亚甲基蓝的降解效率出现降低.图 4b所示为亚甲基蓝在BiOCl/SiO2/Fe3O4中降解的一级动力学拟合曲线.从图中可以看出, 不同投加量下BiOCl/SiO2/Fe3O4对亚甲基蓝的降解速率遵循一级动力学反应方程, 以ln(C0/C)为纵坐标, 时间为横坐标进行拟合, 拟合参数见表 1.由表 1可知, BiOCl/SiO2/Fe3O4投加量对亚甲基蓝降解速率有很明显的影响, 在投加量为0.5 g·L-1时, 速率常数最大为0.02251 min-1.说明在光催化降解亚甲基蓝过程中光催化剂存在一个最优投加量, 当投加量低于或高于这个值时都会对催化效率产生不利的影响.这是因为当催化剂的投加量未达到饱和时, 增加催化剂的剂量会增加亚甲基蓝的降解效率, 当催化剂投加量为0.5 g·L-1时, 投加剂量达到饱和, 则过量的催化剂分散在溶液中, 反而会造成光能利用效率的降低.由此可以得出, 当亚甲基蓝初始浓度为10 mg·L-1时, BiOCl/SiO2/Fe3O4的最佳投加剂量为0.5 g·L-1.
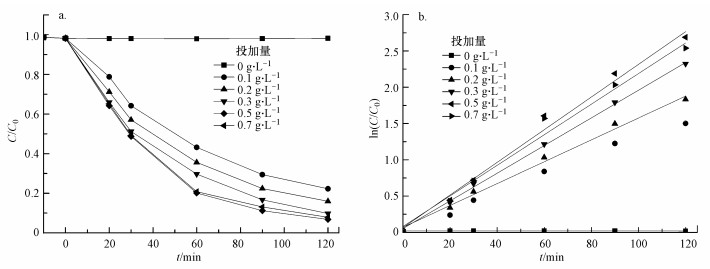 |
| 图 4 不同剂量的BiCl/SiO2/Fe3O4催化剂对亚甲基蓝的降解曲线(a)及一级动力学拟合曲线(b) Fig. 4 Degradation curves(a) and first-order kinetic fit curves(b) of methylene blue with different amounts of BiOCl/SiO2/Fe3O4 catalysts |
| 表 1 不同剂量催化剂对亚甲基蓝降解的一级动力学拟合参数 Table 1 First-order kinetic fitting parameters of degradation of methylene blue in BiOCl/SiO2/Fe3O4 |
光催化降解反应的催化效率与催化剂的表面性质、目标降解物的表面电荷、羟基自由基浓度等因素有关, 而这些因素又都与反应中的初始pH条件有关.因此, 本文考察了不同pH值条件下BiOCl/SiO2/Fe3O4对亚甲基蓝光催化降解的影响, 结果见图 5a.在初始pH分别为3、5、6、7和9时, 设置BiOCl/SiO2/Fe3O4的剂量为0.5 g·L-1, 亚甲基蓝初始浓度为10 mg·L-1, 随着pH值的增加, BiOCl/SiO2/Fe3O4对亚甲基蓝的脱色率呈先增高后降低的趋势, 在pH值为6时催化剂的催化效果最好, 120 min后亚甲基蓝的降解率达到96.9%.图 5b所示为不同pH条件下亚甲基蓝在BiOCl/SiO2/Fe3O4中降解的一级动力学拟合曲线, 以ln(C0/C)为纵坐标, 时间为横坐标进行拟合, 拟合参数见表 3.由表可知, 催化降解的最佳pH值为6, 此时BiOCl/SiO2/Fe3O4对亚甲基蓝的降解速率常数为0.02931 min-1, 表明催化剂在酸性条件下的催化效果优于碱性条件.这是因为在酸性条件下亚甲基蓝更容易降解, 但当反应条件过于偏酸性时, 反而会降低羟基自由基的量, 从而影响催化剂的催化效率.
 |
| 图 5 不同pH条件下BiOCl/SiO2/Fe3O4催化剂对亚甲基蓝的降解曲线(a)及一级动力学拟合曲线(b) Fig. 5 The degradation(a) and the first-order kinetic(b) curve of methylene blue on BiOCl/SiO2/Fe3O4 catalyst under different pH conditions |
| 表 2 不同pH条件下催化剂对亚甲基蓝降解的一级动力学拟合参数 Table 2 First-order kinetic fitting parameters of catalyst degradation of methylene blue under different pH conditions |
取0.5 g BiOCl/SiO2/Fe3O4复合材料和100 mL 10 mg·L-1的亚甲基蓝溶液, 进行时长为120 min的光催化降解实验, 在每组实验完成后将BiOCl/SiO2/Fe3O4复合材料回收、洗净, 干燥之后再重复进行光催化降解实验.BiOCl/SiO2/Fe3O4对亚甲基蓝的重复光催化降解曲线与回收率结果如图 6所示.由图可知, 第1~4次实验的脱色率分别为94.5%、92.21%、86.8%、78.65%, 回收率分别为95.65%、90.12%、86.31%和81.57%.随着重复利用次数的增加, 催化剂的性能仍然很稳定, 在经过4次的光催化降解实验之后, 催化剂对亚甲基蓝的脱色率依然能达到78.65%, 其中很大一部分原因是每次回收不完全, 导致催化剂部分流失, 由此也说明催化剂的稳定性好, 可重复利用.
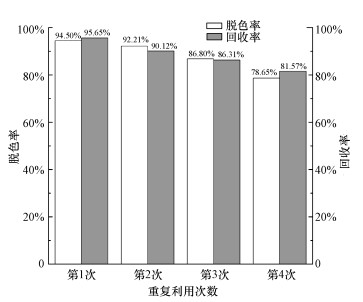 |
| 图 6 催化剂重复使用次数对脱色率及回收率的影响 Fig. 6 Effect of recycle times of catalyst on degradation rate and recovery rate |
1) 利用水热合成法制备了光催化剂BiOCl/SiO2/Fe3O4, XRD、EDS及SEM表征结果显示, BiOCl成功地负载在SiO2/Fe3O4磁性微球上, 且具有很好的可回收性.
2) EDS能谱图显示, 所制备的催化剂共检测出了Fe、O、Cl、Si和Bi 5种元素, 与BiOCl/SiO2/Fe3O4的元素组成一致, 没有其他杂质元素.XRD图谱各元素均与标准卡片(JCPDS NO.51-1381)相吻合, 未发现其他晶相和杂质峰, 说明合成的BiOCl/SiO2/Fe3O4复合物纯度较高.FT-IR显示其峰和元素组成及价态均与BiOCl/SiO2/Fe3O4一致.UV-Vis结果表明, BiOCl/SiO2/Fe3O4的禁带宽度为2.78 eV, 说明样品具有较好的可见光响应.表征结果表明, 本研究成功制备了结构完整、纯度高的BiOCl/SiO2/Fe3O4.
3) 光催化实验表明, 当催化剂投加量从0.1 g·L-1增加到0.7 g·L-1时, 其对亚甲基蓝的降解具有积极的影响, 降解效率显著增加, 并在BiOCl/SiO2/Fe3O4剂量为0.5 g·L-1时达到最优, 在120 min后催化效率达到93.2%.当BiOCl/SiO2/Fe3O4投加量进一步增加到0.7 g·L-1时, 亚甲基蓝的降解效率降低.在BiOCl/SiO2/Fe3O4光催化降解亚甲基蓝的脱色反应体系中, 亚甲基蓝主要与空穴反应, 将OH-和MB分别氧化成羟基自由基(·OH)和MB中间产物, ·OH具有强氧化能力, 从而加速了MB的脱色, 亚甲基蓝染料在BiOCl/SiO2/Fe3O4上的光催化作用使得电子由MB的中间态转移到激发态, 从而再转移到BiOCl/SiO2/Fe3O4的导带上, 最终氧化成CO2和H2O.重复实验表明, 该催化剂反复利用4次后, 降解效率依然能达到78.65%.
Chai S Y, Yong J K, Jung M H, et al. 2009. Heterojunctioned BiOCl/Bi2O3, a new visible light photocatalyst[J]. Journal of Catalysis, 262(1): 144–149.
|
Ding H L, Zhang Y X, Wang S, et al. 2012. Fe3O4@SiO2 Core/Shell nanoparticles:The silica coating regulations with a single core for different core sizes and shell thicknesses[J]. Chemistry of Materials, 24(23): 4572–4580.
DOI:10.1021/cm302828d
|
郭烨, 薛仕丽, 井然, 等. 2018. 两种MOFs材料降解染料废水的光催化活性[J]. 延安大学学报(自然科学版), 2018, 37(1): 59–62.
|
韩珊珊, 刘文韬, 毕晓峰, 等. 2015. 超声化学法合成高效BiOCl催化剂的研究[J]. 四川化工, 2015, 18(3): 18–20.
DOI:10.3969/j.issn.1672-4887.2015.03.006 |
胡潇, 梁虎南, 于大禹. 2018. 硅藻土处理染料废水的研究进展[J]. 硅酸盐通报, 2018, 37(1): 160–165.
|
黄文师, 孙莹, 王蕾, 等. 2018. BiOCl光催化改性的研究进展[J]. 合成材料老化与应用, 2018, 47(1): 112–118.
|
李忠翠.2016.Fe2O3/BiOCl系列复合材料的制备及其光催化性能研究[D].扬州: 扬州大学
http://cdmd.cnki.com.cn/Article/CDMD-11117-1016292994.htm |
廉菲, 刘畅, 李国光, 等. 2012. 高分子固体废物基活性炭对有机染料的吸附解吸行为研究[J]. 环境科学, 2012, 33(1): 147–155.
DOI:10.3969/j.issn.1673-1212.2012.01.036 |
练涛, 林远, 梁少强, 等. 2017. Fe3O4/G-BiOCl纳米复合光催化剂的制备及光催化性能研究[J]. 化工新型材料, 2017, 45(2): 162–164.
|
刘国, 刘家豪, 余雯雯, 等. 2017. BiOCl/ZnMgAl-HTLCs复合材料光催化去除水中的甲基橙[J]. 环境科学学报, 2017, 37(11): 4071–4077.
|
卢海晶.2014.BiOCl基复合光催化剂的制备与光催化性能研究[D].哈尔滨: 哈尔滨师范大学
|
毛晓明, 张娜娜, 李慧苗, 等. 2018. BiOCl的制备及其对苯酚的光催化氧化行为研究[J]. 人工晶体学报, 2018, 47(1): 150–154.
DOI:10.3969/j.issn.1000-985X.2018.01.024 |
Tanveer M, 吴宇, Abdul Q M, 等.2018.具有显著光催化响应的非典型BiOCl/Bi2S3异质结构(英文)[J].Science China.Materials, (1): 1-11
|
童玲.2014.新型磁性四氧化三铁@钨酸盐复合光催化剂的制备及其性能研究[D].扬州: 扬州大学
http://cdmd.cnki.com.cn/Article/CDMD-11117-1014359564.htm |
王晓雯, 张小超, 樊彩梅. 2014. BiOCl基光催化材料的研究进展[J]. 化工进展, 2014, 33(1): 124–132.
|
Wang D H, Gao G Q, Zhang Y W, et al. 2012. Nanosheet-constructed porous BiOCl with dominant {001} facets for superior photosensitized degradation[J]. Nanoscale, 4(24): 7780–7785.
DOI:10.1039/c2nr32533k
|
Wang X J, Wang Q, Li F T, et al. 2013. Novel BiOCl-C3N4, heterojunction photocatalysts:In situ preparation via an ionic-liquid-assisted solvent-thermal route and their visible-light photocatalytic activities[J]. Chemical Engineering Journal, 234(12): 361–371.
|
瓮青松, 杨富国, 阮善. 2016. 电化学方法处理分散红染料废水的研究[J]. 广东化工, 2016, 43(10): 173–174.
DOI:10.3969/j.issn.1007-1865.2016.10.087 |
Xie F, Mao X, Fan C, et al. 2014. Facile preparation of Sn-doped BiOCI photocatalyst with enhanced photocatalytic activity for benzoic acid and rhodamine B degradation[J]. Materials Science in Semiconductor Processing, 27(3): 380–389.
|
闫国伦. 2018. 纳米CdS的制备及其在印染废水处理上的探索[J]. 四川化工, 2018, 21(1): 1–12.
DOI:10.3969/j.issn.1672-4887.2018.01.001 |
杨冰叶, 李航, 商宁昭, 等. 2017. 中空花状可见光响应催化剂g-C3N4@BiOCl的制备及其光催化活性[J]. 无机化学学报, 2017, 33(3): 396–404.
|
Yu Q, Sang J J, Fu A P, et al. 2014. Synthesis and characterization of magnetic nanocomposite Fe3O4@nSiO2@mSiO2 with dual shells containing non-porous silica and mesoporous silica structure[J]. Advanced Materials Research, 926/930: 308–311.
DOI:10.4028/www.scientific.net/AMR.926-930
|
Zhang K L, Liu C M, Huang F Q, et al. 2006. Study of the electronic structure and photocatalytic activity of the BiOCl photocatalyst[J]. Applied Catalysis B Environmental, 68(3): 125–129.
|
 2019, Vol. 39
2019, Vol. 39


