目前, 合成染料已被广泛用于印染、纺织、食品、药品和化妆品等行业(Singh et al., 2015).研究发现, 废水中的染料会显著降低水体透明度, 进而影响光合作用、溶解氧水平、水体的COD水平等, 从而造成严重的环境问题(Fatima et al., 2017).同时, 由于染料废水具有成分复杂、有机物含量高、色度大、毒性强等特点, 使其成为较难处理的工业废水.
近年来, 零价铁(ZVI)技术由于具有成本低和环境友好的优点, 成为有机废水处理领域的研究热点.可以通过ZVI处理的污染物的主要类型有:含氯有机物(El-Temsah et al., 2016)、含硝基的芳香化合物(Guet al., 2015)、砷化物(Klaset al., 2013)、重金属离子(Zhanget al., 2011).纳米级零价铁(nZVI)具有相对较大的表面积及更强的还原活性, 从而使其能够更迅速、更高效地清除废水中难降解的合成染料(Lvet al., 2014).然而nZVI具备活性高、稳定性差、极易团聚的特性, 使其对污染物的降解速率大幅下降;并且纳米材料特殊的化学氧化性质和物理性质会对微生物的致死率和细胞内活性氧自由基的含量变化都产生一定的影响.如Lee等(2008)从nZVI与大肠杆菌细胞接触后的TEM中发现, 当大肠杆菌暴露在nZVI中时, 细胞膜会发生破碎, 致使微生物失活.Keenan等(2008)根据ZVI染毒微生物后细胞内的活性氧物质(ROS)含量变化推测细胞内的氧化压力增加, 从而导致细胞毒性.
因此, 需要对nZVI进行改性, 以解决nZVI活性高、稳定性差、易团聚及易氧化钝化的缺点, 使其能够在有氧条件下稳定存在并能够应用于染料废水的连续处理中.目前, 纳米铁的改性主要有以下途径:纳米双金属、固体载体和表面改性.纳米双金属可以有效提高环境污染物的去除能力;固体载体的应用提高了纳米零价铁在环境中的迁移能力;加入表面改性剂可以抑制纳米铁颗粒的团聚, 促进水相中目标污染物向纳米零价铁表面的迁移, 加速污染物的降解(庞龙等, 2011).本研究拟在纳米零价铁外包覆SiO2之后对其进行氨基化的修饰, 包覆的SiO2带有伯氨基(—NH2)的化学性质, 可能会对工业废水中染料的降解和生物毒性产生新的影响(Robinsonet al., 2001).因此, 在对染料降解的同时还应评估所合成的纳米材料是否对微生物具有毒性, 在对染料降解的过程及结果中是否会对环境中微生物的生长及繁殖产生影响.
基于此, 本文采用液相还原法合成纳米零价铁和氨基修饰二氧化硅的包覆型纳米零价铁(nZVI@SiO2-NH2), 对合成的包覆型材料的稳定性及降解染料的有效性进行研究, 并初步探讨所合成纳米材料对微生物的生物毒性.以期为包覆型纳米零价铁的应用与合成染料的无害化脱色提供理论基础及技术支持.
2 材料与方法(Materials and methods) 2.1 试剂与仪器试剂:FeCl3·6H2O、KBH4、TEOS、无水乙醇、APTMS均为分析纯(AR), 购自麦克林生化试剂有限公司;PEG-20000(≥96.0%)购自纳川生物技术工作室;考马斯亮蓝(三苯甲烷, λmax=557 nm)、刚果红(偶氮, λmax=527 nm)、苯胺蓝(偶氮, λmax=595 nm)、依莱铬红B(蒽醌, λmax=465 nm)、洋红(偶氮, λmax=520 nm)均为分析纯(AR), 购自光复精细化工有限公司;超氧化歧化酶试剂盒(EC1.15.1.1)和乳酸脱氢酶试剂盒(EC1.1.1.27)购自苏州科铭生物技术有限公司
仪器:超声振荡清洗仪(KQ-500DE, 超声仪器有限公司);XRD分析仪(X′Pert3Powder, Panalytical);FTIR分析仪(Nicolet is50, Thermo fisher);透射电子显微镜(JEM-1400, Hitachi);真空烘干箱(DZF-6020, 博迅生物股份有限公司);超声细胞破碎仪(JY92-IIN, 东芝生物股份有限公司).
2.2 研究方法 2.2.1 纳米零价铁的制备本研究采用液相还原法制备纳米零价铁, 具体过程如下:将0.541 g FeCl3·6H2O溶于醇水体积比为7:3的溶液中, 加入1 g PEG-20000作为分散剂, 以1 mL·min-1的速度滴加5 mL 1.5 mol·L-1的KBH4并持续机械搅拌;滴加过程中持续通入氮气, 待无气泡产生后, 静置沉淀去上清;使用无水乙醇和去离子水各清洗3次, 在75 ℃下真空烘干4 h, 待冷却降温后取出保存.
2.2.2 氨基修饰二氧化硅壳型纳米零价铁的制备利用液相还原法制备纳米零价铁后, 滴加5 mL的正硅酸乙酯(TEOS)反应15 min;缓慢加入3-氨丙基三甲氧基硅烷(APTMS)(关泽宇, 2015), 在50 ℃下机械搅拌(4 h), 得到nZVI@SiO2-NH2纳米粒子;无水乙醇和去离子水各清洗3次, 75 ℃真空烘干5 h, 待冷却降温后取出保存.
2.2.3 纳米零价铁的表征检测利用TEM、FTIR和XRD对nZVI和nZVI@SiO2-NH2的形态、晶体组成和功能团结构的变化情况进行分析.
TEM表征:取微量制备好的nZVI和nZVI@SiO2-NH2样品置于离心管中, 加入无水乙醇, 超声波清洗仪分散30 min, 乙醇稀释, 滴至300目双面铜网上待测.
FTIR表征:将制备好的nZVI和nZVI@SiO2-NH2样品充分研磨后保存备测.
XRD表征:将充分干燥、新制备的两种样品在玻璃测定模具中进行压片, 压片平齐, 将样品置于X射线衍射分析仪中, 2θ范围为10°~90°, 约4~5 min后检测结束, 将样品取出回收.
2.2.4 纳米零价铁对合成染料脱色效果测定分别配制不同种类的染料洋红、苯胺蓝、依莱铬红B、刚果红和考马斯亮蓝溶液, 浓度均为100 mg·L-1, 将nZVI以0.6 g·L-1的剂量加入到装有50 mL染料的反应管中, nZVI@SiO2-NH2以6 g·L-1的剂量加入到装有50 mL染料的反应管中(相等原料制作出的nZVI和nZVI@SiO2-NH2质量比约为1:10), 120 r·min-1下持续振荡反应, 间隔时间取样(0、1、2、3、4、5、10、15、20、25、30 min), 测定不同时间脱色后的吸光度.
合成染料的脱色分析:每种合成染料做3个平行, 脱色结束后, 以时间和脱色率为横、纵坐标绘制样品对不同染料的脱色图并进行分析.
染料的连续脱色:测定nZVI和nZVI@SiO2-NH2对洋红的连续脱色情况.配制100 mg·L-1的洋红染料, 脱色处理10 min后, 测定溶液在520 nm处的吸光度, 离心弃上清, 重复上述步骤, 直至染料不能再脱色.
脱色后样品的TEM检测:将上述脱色后的nZVI和nZVI@SiO2-NH2超声后直接对表面形态进行TEM检测.
2.2.5 纳米零价铁对大肠杆菌的毒性影响以实验室的大肠杆菌作为生物研究对象, 对1 g·L-1和6 g·L-1 nZVI和nZVI@SiO2-NH2培养后的大肠杆菌进行平板计数.SOD的产生及对生物体的毒害作用是迄今为止最为普遍接受的纳米材料致毒机制(Kahru et al., 2008), LDH则可以测出细胞的破损程度.因此, 本文使用LDH和SOD测试盒对大肠杆菌的生物毒性进行检测.
大肠杆菌的复苏与培养:对实验室保存的E.coil CD-2进行复苏.
大肠杆菌的平板计数:分别将少量细菌接种到一定体积、含有不同浓度nZVI(0、1、6 g·L-1)和nZVI@SiO2-NH2(0、1、6 g·L-1)的PBS中, 恒温振荡器中(37 ℃)进行培养, 分别于0~6 h测定600 nm处的吸光值(OD600);并取第6 h的培养液进行稀释(稀释倍数为104~107), 取100 μL涂布(每组3个平行), 37 ℃过夜培养, 数单菌落, 进行毒性对比并拍照记录统计结果.
大肠杆菌内细胞酶活性的测定:离心收集第7 h培养液上清, 依照LDH和ROS试剂盒使用说明进行酶活和抑制率的检测.
3 结果与分析(Results and analysis) 3.1 纳米零价铁表征nZVI和nZVI@SiO2-NH2的透射电镜(TEM)结果见图 1.TEM图清晰地显示了nZVI的形态, 其中, 黑色颗粒均为nZVI, 颗粒大小约为10~50 nm, 且二者在一定程度上均有聚集情况.其中, 图 1 a为未包覆的纳米零价铁, 由透射电镜及其能谱结果可知, 在纳米颗粒周围有一层颜色较浅的零价铁氧化薄膜;图 1b所示为包覆氨基修饰的二氧化硅膜的链状连接结构, 能够很好地隔绝空气中的氧气, 使nZVI得到保护, 不被空气氧化.未进行修饰的纳米零价铁仍紧密相连, 易被氧化.
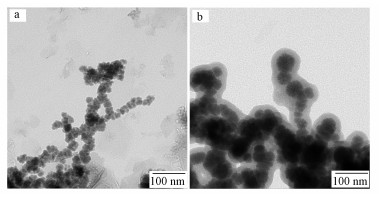 |
| 图 1 nZVI(a)和nZVI@SiO2-NH2(b)的TEM图 Fig. 1 Electron microscopic analysis of nZVI(a) and nZVI@SiO2-NH2(b) |
nZVI和nZVI@SiO2-NH2的傅里叶红外光谱(FTIR)结果见图 2.氧化后的氧化铁Fe—O峰在540 cm-1左右处, nZVI在540 cm-1处有一个比较强的峰, 说明纳米零价铁在一定程度上已经被氧化, 而对照修饰后的样品, Si—O—Si在1000~1100 cm-1处有伸缩振动峰, 在2992 cm-1处出现了—NH的弯曲振动峰和APTMS的—CH3的峰(关泽宇, 2015), 表明该材料在包裹二氧化硅的同时, 进行了氨基化修饰.图 2中其它共有的峰基本为O—H, 可能是由于未充分干燥或在测量过程接触杂质所致.
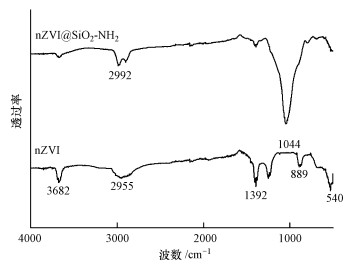 |
| 图 2 nZVI和nZVI@SiO2-NH2的FTIR分析结果 Fig. 2 FTIR analysis of nZVI and nZVI@SiO2-NH2 |
nZVI和nZVI@SiO2-NH2的X射线衍射(XRD)结果见图 3.由于XRD结果体现了样品的晶体结构, 所以根据图 3可以分析得出, nZVI在2θ=42°、65°、83°处分别存在3个衍射峰, 对比nZVI标准XRD图谱可知, 3个特征峰分别属于Fe的(110)、(200)和(211)晶面的衍射峰, 且在2θ=28°处出现了Fe3O4的衍射峰, 说明该样品已经被氧化;而nZVI@SiO2-NH2仅在2θ=44°处有一个Fe的衍射峰, 且强度减弱, 在2θ=23°处出现了代表SiO2的特征吸收峰, 结合减弱的Fe的衍射峰, 说明nZVI@SiO2-NH2样品实现了SiO2对nZVI的包覆.
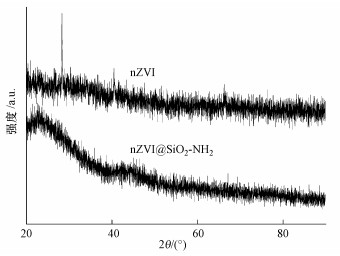 |
| 图 3 nZVI和nZVI@SiO2-NH2的XRD分析结果 Fig. 3 XRD analysis of nZVI and nZVI@SiO2-NH2 |
采用nZVI和nZVI@SiO2-NH2分别对多种染料进行脱色, 结果如图 4所示.nZVI@SiO2-NH2较未修饰的nZVI可对更多的合成染料进行脱色, 在5 min左右, 洋红、刚果红和考马斯亮蓝的脱色率均达到90%以上, 其中, 洋红和刚果红的脱色率接近99%;在10 min左右, 苯胺蓝的脱色率能达到80%以上, 依莱铬红B的脱色率则在60%以上.对比图 4b可知, 未处理的nZVI对依莱铬红B和刚果红20 min后的脱色率不足10%, 几乎未脱色, 而其他染料也仅在20 min后脱色率稳定在50%~60%, 不能继续脱色.
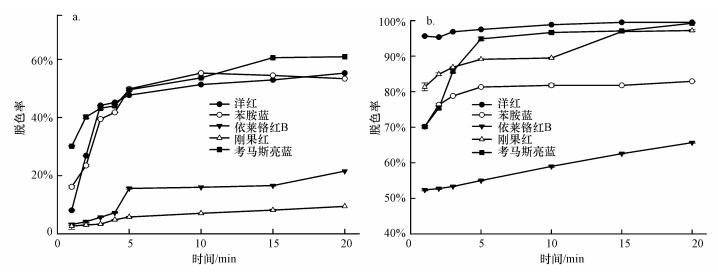 |
| 图 4 nZVI(a)和nZVI@SiO2-NH2(b)对不同染料的脱色效果 Fig. 4 Decolorization of different dyes by nZVI(a) and nZVI@SiO2-NH2(b) |
本研究对洋红进行连续脱色10 min, 结果见表 1.由表 1可知, 相同条件下, nZVI@SiO2-NH2在连续使用3次后脱色率依然可以达到80%以上, 在第4次时脱色率也可达到50%以上;而未修饰的nZVI, 仅在第1次的脱色率可以达到50%以上, 第4次之后已经对染料没有脱色作用.已有报道表明, 未修饰的nZVI对甲基橙(Robinsonet al., 2001)、酸性蓝(Wanget al., 2014)、橙黄(Shu et al., 2010)、活性红(Satapanajaru et al., 2011)和活性黑5(Fu et al., 2014)等具有较高的降解率.本研究发现, 未修饰的nZVI由于其活性高、稳定性差、在空气环境中易氧化, 严重降低了合成染料与nZVI的接触表面积, 使其在连续脱色方面处于劣势.而改性后的nZVI无论从脱色效果还是连续使用上, 都优于未修饰的nZVI, 尤其在连续脱色方面具有优势, 可以重复使用3次以上.
| 表 1 nZVI和nZVI@SiO2-NH2对洋红的连续脱色效果 Table 1 Repeated decolorization of magenta by nZVI and nZVI@SiO2-NH2 |
经过脱色处理的nZVI和nZVI@SiO2-NH2的透射电镜结果如图 5所示.图 5a样品中呈长针状的为彻底氧化后的纳米铁, 可以看出几乎所有的nZVI在经过首次染料脱色后都被氧化;而对比发现, 图 5b中的样品与图 1b中的样品几乎无差别, 中间有大量黑色颗粒, 即未氧化的纳米零价铁.并且结合图 4b可知, nZVI@SiO2-NH2具有很好的染料脱色能力, 且由于其大部分纳米零价铁并未被氧化, 因此, 该样品在染料脱色中可以连续多次使用.
 |
| 图 5 nZVI(a)和nZVI@SiO2-NH2(b)脱色后的TEM图 Fig. 5 TEM analysis of decolorized samples of nZVI(a) and nZVI@SiO2-NH2(b) |
通过对1、6 g·L-1的nZVI和nZVI@SiO2-NH2培养后的大肠杆菌进行平板计数, 统计得到如表 2所示结果, 对比可知, 1 g·L-1的nZVI在稀释倍数为105和6 g·L-1的nZVI在稀释倍数为104时的单菌落数, 与稀释倍数为106的空白对照及修饰后的纳米零价铁在同一数量级上.图 6为上述处理条件下菌落数在同一数量级的平板菌落生长情况(每组3个平行, 本文挑选每组拍照结果较好的一个), 可以看出, 稀释105的1 g·L-1的nZVI和稀释104的6 g·L-1的nZVI与稀释106的空白对照和nZVI@SiO2-NH2对菌落生存的影响程度在同一数量级上.整体来看, 修饰后的nZVI的毒性要明显小于未修饰的nZVI, 而且未修饰的nZVI浓度越高对大肠杆菌的毒性越大, 修饰后的nZVI对大肠杆菌的毒性基本保持在一定水平, 1 g·L-1和6 g·L-1时无太大区别.尤其在适合于染料脱色的浓度下, 氨基修饰的包覆型纳米零价铁的毒性要明显小于同浓度下未修饰的纳米零价铁.
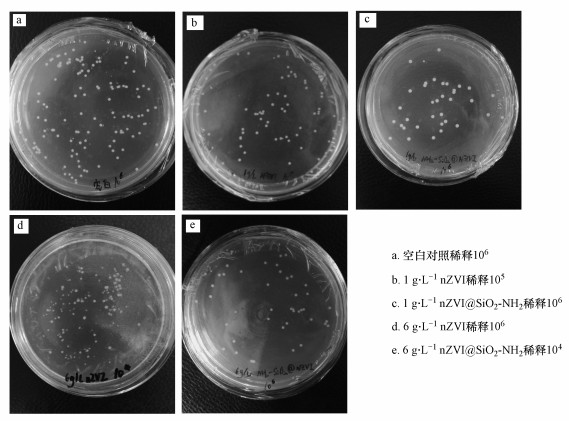 |
| 图 6 不同处理下的大肠杆菌平板计数 Fig. 6 Dilution of different multiple E. coli plate counts under different conditions |
| 表 2 不同条件下稀释不同倍数大肠杆菌平板计数情况 Table 2 Dilution of different multiple E. coli plate counts under different conditions |
乳酸脱氢酶(LDH)酶活性的测定:测定的胞外乳酸脱氢酶(LDH)酶活性越强, 细胞破损量越大, 该样品的毒性就越强.本文中LDH的酶活性见图 7.由图 7可知, 两种样品在1 g·L-1和6 g·L-1时均有毒性, 但氨基修饰后的样品和1 g·L-1的nZVI的毒性要明显较小, 而6 g·L-1的nZVI毒性远远大于其他样品, 与平板计数后的活细胞数量最少相对应.并且修饰后的nZVI在1 g·L-1和6 g·L-1时的酶活性差别很小, 说明这种修饰方法能有效地降低纳米零价铁对生物的毒性.
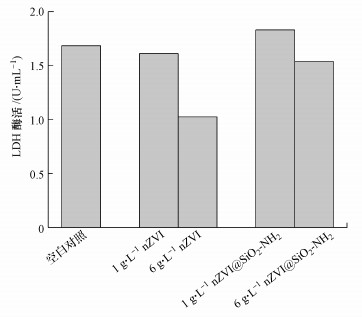 |
| 图 7 不同浓度样品处理细胞后的LDH酶活 Fig. 7 LDH enzyme activity after treatment of cells with different content samples |
超氧化物歧化酶(SOD)酶活性的测定:SOD酶活性主要是为消除细胞中的超氧阴离子, 而因为纳米零价铁的氧化还原能力很强, 能和超氧阴离子反应, 因此, 如果纳米零价铁越多, 毒性越强, 测得的SOD酶活性越低.不同条件下SOD酶的抑制率如图 8所示.由图可知, 所有样品的SOD抑制率均低于空白对照, 而1 g·L-1样品的整体抑制率要低于6 g·L-1样品, 说明样品浓度越高则毒性越大, 对大肠杆菌的影响越大;而两种样品对比而言, nZVI@SiO2-NH2的抑制率要低于nZVI, 说明其包覆壳型结构对纳米零价铁的保护性较强, 可以防止与大肠杆菌中的超氧阴离子反应, 维持生物的正常生存环境.
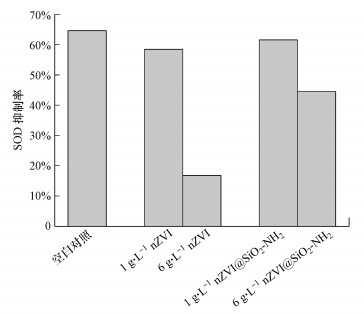 |
| 图 8 不同浓度样品处理细胞后的SOD抑制率 Fig. 8 SOD inhibition rate after treatment of cells with different contents |
1) 本研究利用液相还原法合成了nZVI和nZVI@SiO2-NH2, 表面形态(TEM)、表面晶体组成(FTIR)和表面功能团结构(XRD)3个方面的表征结果表明, 修饰后的纳米零价铁防氧化能力较好, 更能保证零价铁的使用率.
2) 本研究发现, nZVI@SiO2-NH2对试验中合成染料的脱色率更高, 尤其在连续脱色方面具有优势.未修饰的nZVI由于活性高、稳定性差、在空气环境中易氧化, 严重降低了合成染料与nZVI的接触表面积, 使其在连续脱色方面处于劣势.
3) 由于纳米材料特殊的物理化学性质会对生物产生一定的毒性, 本研究还基于对合成染料脱色有效的样品浓度下对微生物的毒性进行了相关研究, 发现无论从平板计数后大肠杆菌的存活程度, 还是细胞LDH和SOD的酶活两个方面来分析, 均表明nZVI@SiO2-NH2的生物毒性相对较小, 说明此种氨基修饰的包覆型方法可以降低纳米零价铁对生物的毒性.
综上所述, 从脱色效果和连续利用次数及对环境中微生物的毒性进行比较, nZVI@SiO2-NH2均更能降低生产成本, 更适合于生产生活.
El-Temsah Y S, Sevcu A, Bobcikova K, et al. 2016. DDT degradation efficiency and ecotoxicological effects of two types of nano-sized zero-valent iron(nZVI)in water and soil[J]. Chemosphere, 144: 2221–2228.
DOI:10.1016/j.chemosphere.2015.10.122
|
Fatima M, Farooq R, Lindströmb R W, et al. 2017. A review on biocatalytic decomposition of azo dyes and electrons recovery[J]. Journal of Molecular Liquids, 246: 275–281.
DOI:10.1016/j.molliq.2017.09.063
|
Fu F, Dionysiou D D, Hong L. 2014. The use of zero-valent iron for groundwater remediation and wastewater treatment:A review[J]. Journal of Hazardous Materials, 267(3): 194–205.
|
Gu C, Jia H, Li H, et al. 2015. Synthesis of highly reactive subnano-sized zero-valent iron using smectite clay templates[J]. Environmental Science & Technology, 44(11): 4258–4263.
|
关泽宇.2015.氨基修饰的壳核型纳米铁强化厌氧微生物脱氯特性及机理研究[D].广州: 华南理工大学
http://cdmd.cnki.com.cn/Article/CDMD-10561-1016738251.htm |
Jiang Z, Lv L, Zhang W, et al. 2011. Nitrate reduction using nanosized zero-valent iron supported by polystyrene resins:Role of surface functional groups[J]. Water Research, 45(6): 2191–2198.
DOI:10.1016/j.watres.2011.01.005
|
Kahru A, Dubourguier H C, Blinova I, et al. 2008. Biotests and biosensors for ecotoxicology of metal oxide nanoparticles:A minireview[J]. Sensors, 8(8): 5153–5170.
DOI:10.3390/s8085153
|
Keenan C R, Sedlak D L. 2008. Factors affecting the yield of oxidants from the reaction of nanoparticulate zero-valent iron and oxygen[J]. Environmental Science & Technology, 42(14): 5377–5378.
|
Klas S, Kirk D W. 2013. Advantages of low pH and limited oxygenation in arsenite removal from water by zero-valent iron[J]. Journal of Hazardous Materials, 252-253: 77–82.
DOI:10.1016/j.jhazmat.2013.02.044
|
Lee C, Kim J Y, Lee W I, et al. 2008. Bactericidal effect of zero-valent iron nanoparticles on Escherichia coli[J]. Environmental Science & Technology, 42(13): 4927–33.
|
Lv X, Xue X, Jiang G, et al. 2014. Nanoscale zero-valent iron(nZVI) assembled on magnetic Fe3O4/graphene for chromium(VI) removal from aqueous solution[J]. Journal Colloid Interface Sciences, 417(417): 51–59.
|
庞龙, 周庆祥, 苏现伐. 2011. 纳米零价铁修饰技术研究进展[J]. 化工进展, 2011, 30(6): 1361–1368.
|
Robinson T, Mcmullan G, Marchant R, et al. 2001. Remediation of dyes in textile effluent:a critical review on current treatment technologies with a proposed alternative[J]. Bioresource Technology, 77(3): 247–255.
DOI:10.1016/S0960-8524(00)00080-8
|
Satapanajaru T, Chompuchan C, Suntornchot P, et al. 2011. Enhancing decolorization of Reactive Black 5 and Reactive Red 198 during nano zerovalent iron treatment[J]. Desalination, 266(1): 218–230.
|
Shirin S, Balakrishnan V K. 2011. Using chemical reactivity to provide insights into environmental transformations of priority organic substances:The Fe0-mediated reduction of Acid Blue 129[J]. Environmental Science & Technology, 45(24): 10369–10377.
|
Shu H Y, Chang M C, Chen C C, et al. 2010. Using resin supported nano zero-valent iron particles for decoloration of Acid Blue 113 azo dye solution[J]. Journal of Hazardous Materials, 184(1): 499–505.
|
Singh R L, Singh P K, Singh R P. 2015. Enzymatic decolorization and degradation of azo dyes-A review[J]. International Biodeterioration & Biodegradation, 104: 21–31.
|
Wang X, Yang J, Zhu M. 2014. Effects of PMMA/anisole hybrid coatings on discoloration performance of nano zerovalent iron toward organic dyes[J]. Journal of the Taiwan Institute of Chemical Engineers, 45(3): 937–946.
DOI:10.1016/j.jtice.2013.08.019
|
Zhang X, Lin S, Chen Z, et al. 2011. Kaolinite-supported nanoscale zero-valent iron for removal of Pb2+ from aqueous solution:reactivity, characterization and mechanism[J]. Water Research, 45(11): 3481–3488.
DOI:10.1016/j.watres.2011.04.010
|
 2019, Vol. 39
2019, Vol. 39


