2. 安徽建筑大学环境与能源工程学院, 合肥 230601;
3. 水污染控制与废水资源化安徽省重点实验室, 合肥 230601
2. School of Environment and Energy Engineering, Anhui Jianzhu University, Hefei 230601;
3. Provincial Key Laboratory of Water Pollution Control and Waste Water Utilization, Hefei 230601
水生生态系统中, 沉积物既可以吸附污染物作为它们的汇, 亦可以释放污染物作为上层水体的二次污染源(Wang et al., 2011a;Liu et al., 2013a).分子扩散是沉积物释放污染物的一个重要途径, 决定着污染物的环境归趋和水环境质量, 甚至进一步影响污染物的生物富集和人体暴露(Dai et al., 2013).污染物在水体和沉积物孔隙水中自由溶解态浓度是决定分子扩散方向和通量大小的关键因素, 同时也是客观评价污染物生态风险的重要指标(Forsberg et al., 2014).然而, 传统方法仍然难以准确测定水体和沉积物孔隙水中污染物的自由溶解态浓度.近年来, 被动采样技术的发展为准确测定污染物自由溶解态浓度提供了便利.这些被动采样技术包括固相微萃取(Doong et al., 2000; Ouyang et al., 2006)和半透膜被动式采样(Chang et al., 2014)等, 但通常需要对吸附相进行保护以防止破损和外在干扰.同时,这些采样装置只能测定水体和表层沉积物孔隙水中污染物浓度(Liu et al., 2013a).为此, 科研人员以低密度聚乙烯(LDPE)作为吸附相, 扩展了被动采样技术的应用(范娟等, 2015), 也为研究污染物在沉积物-水体界面交换提供了方便(Liu et al., 2013b).
研究表明, 巢湖流域在20世纪70—90年代受到当地工业废水排放的影响, 造成了多环芳烃(PAHs)在沉积物中的明显富集, 并可能对生态环境造成威胁(Wang et al., 2011b; Ren et al., 2015).近年来, 随着各级政府对巢湖环境污染排放的大力整治, 大量污水处理设施的运行和多级生态湿地的建设在一定程度上有效地减少了PAHs外源输入, 然而内源问题却日趋突出.(刘大超等2018)利用逸度方法模拟PAHs在巢湖水体和沉积物间的交换过程时发现, 巢湖底部沉积物是上层水体中PAHs的重要污染源.但对这一问题的认识仅局限于模型的预测, 同时并未明确定量释放速率, 因此, 有必要进一步深入探究其释放过程和速率.
本研究基于课题组研发的原位被动采样装置(王继忠, 2017), 利用LDPE膜作为吸附相, 使用性能参考化合物(PRCs)的校准方法(Fernandez et al., 2014), 选择巢湖西半湖典型河流入湖(PAHs高污染区域)区域作为研究区域, 同步测定不同深度上层水体和沉积物孔隙水中PAHs的自由溶解态浓度.依此探讨研究区域水体和沉积物孔隙水中PAHs的垂直分布特征和界面处扩散通量, 进一步论证巢湖底部沉积物是否是上层水体中PAHs的二次污染源.
2 理论分析(Theoretical analysis) 2.1 基于PRCs法确定自由溶解态浓度一般认为有机污染物在LDPE膜上的富集是简单的物理过程, 可以分为两个阶段, 即:动力学扩散过程和平衡分配过程.其中, 平衡分配过程时化合物在水体和LDPE膜上达到分配平衡, 即可通过测定LDPE膜中浓度和膜-水体分配系数(Kpew)来推导水体中该污染物的浓度(Booij et al., 2003).尽管该方法简单方便, 但污染物在水体和LDPE膜间的平衡非常缓慢, 且随着污染物的物理化学性质不同而变化(Cornelissen et al., 2008).同时, Kpew随着环境介质的改变而变化(Difilippo et al., 2010).而动力学扩散过程的最初阶段接近于吸附量与吸附时间和外界环境浓度呈现线性相关, 符合菲克第一扩散定律, 因此, 只要知道吸附速率(Rs)和吸附时间即可确定吸附量和环境浓度, 但大量研究表明, Rs值随着环境因素的改变而发生变化, 难以用于被动采样技术的定量.
为了更加准确有效地利用被动采样技术测定水体中有机污染物, 一些学者采用了PRCs进行校正(Huckins et al., 2002).该方法是利用与目标化合物物理化学性质极为接近的PRCs, 并假设PRCs的解析和目标物的吸附是同步异向, 如果采样前将PRCs富集在LDPE膜上,放到环境介质中后, 可以通过分析PRCs的解析过程来推导目标物的吸附过程(Huckins et al., 1993).如果PRCs是目标污染物的同位素标记物, 可以假设目标污染物的Rs与PRCs的解析速率(R′S-PRC)相同.
假设采样前和采样后LDPE膜上PRCs的量分别为N0和Nt, 则PRCs的R′S-PRC为:

|
(1) |
式中, R′S-PRC为解析速率(L · d-1), Kpew为化合物在LDPE膜上的吸附常数(g · kg-1)(g · L-1)-1, t为采样时间(d), Mpe为LDPE膜的质量(kg).
考虑到实际情况(如同位素标记物缺少或者母体与同位素标记物难以分离等), 并非所有目标污染物的Rs都可以通过同位素标记物来进行确定, 但可以通过相似PRCs的R′S-PRC、Kpew或摩尔体积来校正确定(Tomaszewski et al., 2008).先前的研究表明, 在适当的lgKpew范围内, 一般可将lgR′S-PRC与其对应的lgKpew进行线性拟合, 获得直线方程(2).

|
(2) |
式中, a和b是拟合参数, 再根据目标污染物的lgKpew值确定对应的R′S-PRC和Rs.
通过PRCs校正确定各目标污染物的Rs后, 水体中自由溶解态浓度(Cw)可以根据其动力学扩散方程进行计算, 具体如式(3)所示。
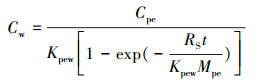
|
(3) |
式中, Cpe为污染物在LDPE膜上的浓度(ng · kg-1).
2.2 沉积物-水体界面扩散通量如果上层水体深度ZW(沉积物-水体界面为原点)处的目标物浓度为Cw, 则该深度浓度可以表示为泰勒级数(Liu et al., 2013b):

|
(4) |
式中, C0是沉积物-水界面(Zw = 0)处的化学浓度, 上层水和沉积物孔隙水浓度收敛, ai(i = 1, 2, ..., n)是拟合参数.因此, 沉积物-水界面处的扩散通量(Fs)由下式计算:
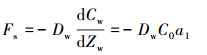
|
(5) |
式中, Fs是瞬时通量, Dw为理论扩散系数(Liu et al., 2013b).实际上, 使用被动采样装置是确定给定时间段的化学浓度.为了与上述用于定量化学浓度的方法一致, 采用时间加权平均(TWA)浓度, 则式(5)可以写成:
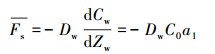
|
(6) |
由于实际水体和沉积物是一个巨大的库, 短时间内被动采样对C0的影响极小, 因此, 可以假设公式(6)中C0与时间无关.另一方面, 用被动采样装置获得的TWA化学浓度(Cw)的深度分布也可以表示为泰勒级数:

|
(7) |
式中, C0 =C0, 并且a′i(i=1, 2, 3, ..., n)是拟合参数, 因此, 一段时间内(采样期间)沉积物-水扩散通量(Fs)可以推导为:

|
(8) |
实验中采用的LDPE膜(厚度为25 μm)购于TRMManufacturing公司(Corona, CA, USA).3种PRC标样(anthracenc-d10、benz[a]anthracene-d12和benzo[a]pyrene-d12)、回收率指示物(naphthalene-d8、acenaphene-d10、phenanthrene-d10、chrysene-d10和perylene-d12)、内标(2-fluoro-1, 1-biphenyl、p-terbenyl-d14和dibenzo[a, h]anthrancene-d14)和16种USEPA优控的PAHs标样均购于百灵威科技有限公司(上海).实验所用正己烷、二氯甲烷均为HPLC级别, 纯度≥99.9%.丙酮和甲醇分别为HPLC/Spectro级别.滤纸为国标快速滤纸, 使用前经过二氯甲烷溶液超声清洗30 min, 重复两次后在烘箱中60 ℃烘干, 置于干燥器中保存.所有玻璃器皿, 如鸡心瓶、平底烧瓶、胶头滴管、细胞瓶等使用前都经过纯水和玻璃器皿清洗剂清洗干净, 经甲醇润洗后, 在纯水中浸泡24 h, 用锡纸包裹放入110 ℃烘箱中干燥, 之后放进干燥的箱子中待用.
3.2 采样器的设计和准备原位被动采样器为不锈钢六边形, 可以同时测定水体和沉积物孔隙水中污染物的垂直分布(王继忠, 2017).图 1a所示为整体装置, 图 1b为水平六边型架子, 上面的正方形钢片用于放置块状LDPE膜, 两端用螺母固定于架子上, 可以测定不同水体深度污染物的浓度.图 1c为竖直放置时的示意图, 中间的横槽用于放置条形LDPE膜, 每边一面, 总计六面, 四周用螺母固定在架子上, 防止脱落, 用于富集不同深度沉积物孔隙水中污染物.装置还包括竖直连接在六棱柱体上端面的中心支撑柱, 以及分别竖直连接在六棱柱体上端面各个棱角处的侧支撑柱, 由中心支撑柱及侧支撑柱构成支撑架, 支撑架内水平设有多组水体采样单元, 多组水体采样单元从下至上依次排列, 且水体采样单元之间间隔距离从下至上依次增大.采样器通过上端的连杆和手柄在外力的作用下将采样器压至预期的深度, 并在四边连接4个重物使采样器稳定, 减少外力对采样器的扰动.其中, 沉积物孔隙水的深度为30 cm, 上层水体为1 m深.
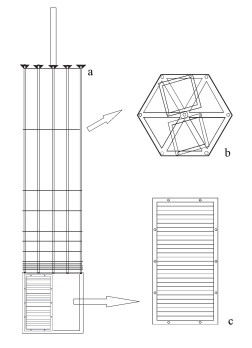 |
| 图 1 原位被动采样器结构图 Fig. 1 Configuration of the in-situ passive sampler |
实验前将LDPE膜分别裁剪成9 cm×9 cm和20 cm×1 cm(长×宽)两种大小规格, 并将剪好的LDPE膜浸泡在正已烷中清洗24 h, 重复3次后, 放入以甲醇和去离子水为溶剂的PCRs混合溶液(500 ng · L-1)中浸泡, 并装入棕色瓶中, 密封后放置在振荡器上以120 r · min-1持续振荡15 d.之后将棕色瓶中的LDPE膜取出用干净滤纸擦净, 铝箔包裹后用密封袋密封, 储存于-20 ℃冰柜中直至现场使用.并从中随机选取若干条LDPE膜, 运回实验室, 用以确定PRCs的初始浓度C0.
回收的LDPE膜运至实验室后用清水洗净表面的附着物, 滤纸擦干, 剪成碎片装入处理好的滤纸包中, 放在30 mL的棕色小瓶内, 加入定量的回收率指示物, 并在瓶中加入正己烷溶剂连续浸泡萃取3次, 每次24 h, 合并3次萃取液于鸡心瓶中.通过旋转蒸发将萃取液浓缩至1 mL, 最终将萃取液转移到细胞瓶中氮吹至0.5 mL, 加入定量的内标后密封等待仪器分析.用于测定C0的LDPE膜运回实验室后立即采取相同的处理过程以确定膜中富集PRCs的初始浓度.
3.4 野外采样于2016年11月18日将原位被动采样器放置于巢湖西半湖南淝河入湖口处(117°24′52.66″E, 31°41′31.60″N, 图 2), 放置前将已吸附PRCs的LDPE薄膜装入采样器中, 并于2016年12月3日回收原位被动采样器.现场对LDPE膜进行清洗, 并将其装入Teflon瓶(100 mL)中, 置于冰盒中保存至实验室内进行萃取分析, 具体操作详见3.3节LDPE处理中所述.
 |
| 图 2 巢湖西半湖入口原位被动采样器野外放置点(五角星为采样点) Fig. 2 Site map of estuary in western part of Chaohu Lake for in-situ passive sampler |
利用安捷伦气相色谱-质谱联用仪(7890A-5975C)进行分析定量, 采用电子轰击源(EI)全扫(Full-Scan)模式.使用HP-5型色谱柱, 以高纯氦气作为载气, 柱流量为1.0 mL · min-1.色谱柱升温程序为:初始温度40 ℃, 以20 ℃ · min-1升温到220 ℃, 再以10 ℃ · min-1升温到260 ℃并保留10 min, 最后以5 ℃ · min-1升至300 ℃, 保留20 min.离子源和气相色谱质谱端接口的温度分别为250 ℃和280 ℃。设置7个浓度梯度(10、20、50、100、500、1000和2000 ng · mL-1)的PAHs标准溶液, 利用内标法建立标准曲线对各化合物进行定量分析, 标准曲线的回归系数R2均大于0.98. 5种回收率指示物的回收效率分别为:naphthalene-d8 65%±10%、acenaphene-d10 90%±10%、phenanthrene-d10 95%±10%、chrysene-d10 100%±10%和perylene-d12 105%±5%.
3.6 数据分析所有数据分析均在Excel2007中进行, 由于样品中高环PAHs(包括茚苯[1, 2, 3-cd]芘(IcdP)、苯并[a, h]蒽(DahA)、苯并[g, h, i]苝(Bghip))的浓度低于仪器检出限, 因此, 文中不予讨论.仅讨论其中的13种PAHs, 分别为萘(Nap)、苊烯(Ace)、苊(Ac)、芴(Fl)、菲(Phe)、蒽(Ant)、荧蒽(Flu)、芘(Pyr)、苯并[a]蒽(BaA)、(Chr)、苯并[a]芴(BbF)、苯并[k]荧蒽(BkF)和苯并[a]芘(BaP).
4 结果与讨论(Results and discussion) 4.1 R′S-PRC和Rs的确定经计算, 3种PRCs(Ant-d10、BaA-d12、BaP-d12)在上层水体中的R′S-PRC值分别为0.82、8.45和40.44 L · d-1, 而在沉积物孔隙水中的R′S-PRC值分别为0.405、4.25和18.77 L · d-1.上层水体和沉积物孔隙水中PRCS的R′S-PRC存在明显的差别, 上层水体的解析速率几乎是沉积物孔隙水的2倍, 这主要是由于污染物的吸附和解析速率与温度、水流流速等因素有着密切的关系(Ouyang et al., 2009), 上层水体流动快, 污染物易于交换, 但沉积物孔隙水不易交换流动, 因而导致PRCs在上层水体中的解析速率大于其在沉积物孔隙水中的解析速率.
假设目标污染物与其对应的同位素标记物的吸附和解析过程同步异向, 则LDPE膜在上层水体中和沉积物孔隙水中的吸附速率与其对应的解析速率相同.经过线性拟合发现, Ant、BaA、BAP的lgRs与lgKpew之间存在显著的线性关系, 其中, 上层水体中lgRs=-3.15+0.91lgKpew(R2=0.95, p < 0.0001), 而沉积物孔隙水中lgRs=-2.04+0.54lgKpew(R2=0.99, p < 0.0001).根据线性方程, 可以确定LDPE膜在上层水体和沉积物孔隙水中对其它目标污染物的Rs值(表 1).
| 表 1 PAHs的lgKpew及其吸附速率(Rs) Table 1 The values of lgKpew and the absorption rates(Rs) of PAHs |
上层水体中LDPE膜对目标污染物PAHs的Rs范围为0.817~40.440 L · d -1, 但在沉积物孔隙水中, LDPE膜对PAHs的吸附速率则为0.405~18.770 L · d -1, 并且都随着lgKpew的增大而增大.这主要是因为环数大的PAHs疏水性增强, 易于被LDPE膜吸附.
4.2 定量PAHs的溶解态浓度通过方程(3)可以计算出不同深度上层水体和沉积物孔隙水中PAHs的浓度, 上层水体中13种PAHs浓度总和(ΣPAHs)为130~250 ng · L-1, 沉积物孔隙水中ΣPAHs浓度为180~253 ng · L-1, 沉积物孔隙水中PAHs浓度略高于上层水体(图 3), 但无显著性差异.先前的研究表明, 巢湖上层水体中17种PAHs(16种USEPA优控污染物加苝)的浓度为5.75~276 ng · L-1, 算术均值为98.6 ng L-1(刘大超等, 2018).同时, (Qin等2013)分析得出巢湖水体中16种USEPA优控PAHs的浓度为95.2~370.1 ng · L-1, 平均值为(181.5±70.8) ng · L-1.本研究通过被动采样测定的13种PAHs浓度与这些结果接近, 说明通过这种原位被动采样技术分析获得的数据较为可靠.
 |
| 图 3 上层水体和沉积物孔隙水中各PAHs的浓度 Fig. 3 The concentration of individual PAHs in overlying water and sediment porewater |
沉积物作为污染物的汇, 富集了大量PAHs, 因此, 这些污染物易于在沉积物颗粒和孔隙水中进行交换, 导致沉积物孔隙水中污染物浓度较高.不同环数PAHs浓度在上层水体和沉积物孔隙水中的垂直变化规律不同(图 4).对于上层水体而言, 2和3环PAHs浓度基本上无明显的垂直变化归趋, 呈现出不同水体深度PAHs浓度相当的现象.可能归因于低环PAHs分子易于在水体中扩散, 同时研究区域水体较浅, 因此, 在垂直梯度上, 低分子量PAHs呈现一致的浓度水平.但4、5和6环PAHs在上层水体中主要呈现随着深度增加浓度逐渐降低的趋势(图 4), 表层水体中这些污染物浓度最高, 而在沉积物-水体界面处浓度最低, 可能反映了大气沉降对研究区域水体中PAHs的贡献.采样期间是冬季, 大气污染较为严重, 大量吸附PAHs的大气颗粒物沉降至巢湖水体中, 通过与水体的交换溶解到水体中.先前的研究也表明, 如果没有新鲜输入源, 沉积物作为二次污染源释放污染物再次进入水体, 则这些污染物在水体中呈现随着水深增加而增加的趋势(Liu et al., 2013b).
 |
| 图 4 巢湖西半湖PAHs在水体和沉积物孔隙水中垂直分布 Fig. 4 Vertical profiles of PAHs in water column and sediment porewater in western part of Chaohu Lake |
沉积物孔隙水中2环PAHs在最底层(距沉积物-水体界面25 cm)呈最大浓度, 而其他深度其浓度变化不明显, 可能原因在于Nap分子小, 易于扩散和下渗, 从而导致最底层沉积物孔隙水中浓度最高.其他PAHs(3~6环)在距沉积物-水体界面下15 cm处呈现一个峰值, 反映了这一深度孔隙水中赋存高浓度PAHs, 这可能源于历史残留的PAHs通过沉积物-水体交换进入孔隙水.先前的研究表明, 巢湖流域明显受到周围工业企业废水排放的影响, 尤其是南淝河口处在20世纪70—90年代受到当地钢铁冶炼行业的污染, 造成西半湖底部沉积物中PAHs明显富集(Ren et al., 2015).同时, 随着沉积物深度减小, PAHs浓度主要呈现减小的趋势, 这主要归功于20世纪90年代国家和地方政府对环境保护的重视, 建设运行了多家污水处理厂, 随着后期对巢湖流域环境保护重视程度的增加, 开展实施了多项措施, 减小了对湖区的污染, 因此, 表层区域沉积物孔隙水中PAHs浓度呈现降低趋势.
4.3 垂直组成的变化在垂直组成上, 以2环Nap为主, 其在上层水体中的浓度占总浓度的42.9%±6.7%, 在沉积物孔隙水中的浓度占总浓度的28.6%±10.1%, 尽管Nap在上层水体中所占比例大于其在沉积物孔隙水中, 但无显著差异性(p>0.05).同时, Ace、Ant、Flu、BaA、Chr、BbF和BkF在上层水体和沉积物孔隙水中所占的比例相当, 其在上层水体中的浓度占总浓度的比例分别为2.74%±0.50%、1.53%±0.42%、14.7%±3.85%、1.24%±0.27%、1.51%±0.33%、0.21%±0.04%和0.20%±0.08%, 在沉积物孔隙水中的浓度占总浓度的比例分别为2.29%±0.20%、2.21%±0.37%、10.40%±2.27%、0.90%±0.20%、1.76%±0.41%、0.39%±0.12%和0.40%±0.12%(图 5), 且通过均值检验发现, 它们在上层水体和沉积物孔隙水中所占比例无明显差异性(所有p值均大于0.05).但Ac、Fl、Phe、Pyr和BaP在上层水体和沉积物孔隙水中的浓度占各自总浓度的比例呈明显差异(p值均小于0.05).其中, Ac、Fl、Phe和BaP在上层水体中的比例明显小于在沉积物孔隙水中的比例, 其在上层水体中的比例分别为3.92%±0.94%、7.10%±1.90%、7.26%±0.83%和0.05%±0.01%, 在沉积物孔隙水中的比例分别为14.2%±1.58%、13.3%±0.89%、16.9%±3.42%和0.08%±0.03%.Pyr在上层水体(16.7%±3.8%)中的比例则明显高于其在沉积物孔隙水中(8.56%±1.90%)(p < 0.05).
垂直方向上, 几乎所有PAHs从表层水体向下均有逐渐增加的趋势, 其中, Nap和Ace在距水体-沉积物界面上10~15 cm处比例最高, Ac、Fl和Phe在沉积物-水体界面上方10 cm处出现最大比例, 其它污染物在水体中的比例均出现双峰, Ant、Flu、Pyr和BaA分别在沉积物-水体界面上方5 cm处和次表层(距界面70 cm)处出现峰值, 而Chr、BbF、BkF和BaP分别在沉积物-水体界面上方5 cm处和表层(距界面100 cm)处出现峰值, 这些实验结果说明大气沉降和水体-沉积物界面扩散的双重作用.对于低环PAHs, 其易于扩散, 大气沉降和水体-沉积物界面扩散的PAHs在水体中叠加, 形成了一个单峰, 但高环PAHs扩散缓慢, 因而在水体中出现双峰现象, 并且随着环数增加, 大气沉降的PAHs更趋向于赋存在表层水体, 而界面扩散的PAHs更倾向于赋存在水体-沉积物界面处.
 |
| 图 5 不同深度水体和沉积物孔隙水中多环芳烃的比例分布 Fig. 5 Vertical variation on the relative abundance of PAHs in water column and sediment porewater |
通过式(8)计算得出, 南淝河入湖口处PAHs在沉积物-水体界面的交换通量变化范围为-384~1445 ng · m-2 · d-1(图 6).除了Flu和Pyr的通量为负值外, 其余均为正值, 说明Flu和Pyr是从水体向沉积物中迁移富集, 沉积物为它们的汇.但其他PAHs则呈现出从沉积物向水体释放的过程, 反映了现阶段研究区域沉积物是上层水体中PAHs的重要二次污染源.比较不同PAHs, 低环(2~3环)PAHs因具有较大的水体溶解度, 沉积物中PAHs易于通过交换进入孔隙水, 再进一步扩散到上层水体中, 表现出从沉积物向水体扩散; 高环(5~6环)PAHs在水体中溶解度低, 易于以颗粒物形式赋存, 再通过沉降作用沉积在底部沉积物中, 因此, 一般沉积物中赋存大量高环PAHs(Wang et al., 2011b; Ren et al., 2015), 这些PAHs亦可以进入沉积物孔隙水, 再扩散至上层水体.但对于中环(4环)PAHs, 因其在水体中浓度较高, 但沉积物中浓度则相对较低, 因此, 在界面处则呈现向沉积物孔隙水中扩散.先前(刘大超等2018)利用逸度扩散模型模拟了PAHs在巢湖流域水体-沉积物的交换过程, 结果显示, 南淝河口外PAHs均呈现从沉积物向水体扩散的趋势, 反映了这一区域沉积物向水体释放PAHs, 造成水体污染.因此, 本文实验结果更进一步证实了早期工业排放的PAHs残留在底部沉积物中, 会通过界面扩散再次进入水体, 成为水体中PAHs的二次污染源.
 |
| 图 6 不同PAHs在沉积物-水体界面分子扩散通量 Fig. 6 Molecular diffusion flux of individual PAHs across sediment-water interface |
本研究采用新型原位被动采样器测定了巢湖西半湖南淝河入湖口处不同深度水体和沉积物孔隙水中PAHs的自由溶解态浓度, 观察了其垂直变化规律及其沉积物-水体界面分子扩散通量.结果表明, 通过PRCs预测的LDPE吸附膜对上层水体中PAHs的吸附速率较沉积物孔隙水大, 但研究区域沉积物孔隙水中PAHs浓度较上层水体高.高环PAHs在上层水体中呈现随深度增加而降低的趋势, 但在沉积物孔隙水中则在中间层出现峰值, 反映了历史沉积记录.通过扩散方程, PAHs在水体-沉积物间分子扩散通量为-384~1445 ng · m-2 · d-1, 除Flu和Pyr, 其它PAHs均从沉积物向水体释放, 证明了底部沉积物中PAHs是造成巢湖水体二次污染的重要因素.同时也反映了近年来对巢湖的治理大大限制了外源污染物的输入后, 内源污染问题需要给予进一步关注.
Booij K, Hoedemaker J R, Bakker J F. 2003. Dissolved PCBs, PAHs, and HCB in pore waters and overlying waters of contaminated harbor sediments[J]. Environmental Science & Technology, 37(18): 4213–4220.
|
Chang W T, Fang M D, Lee C L, et al. 2014. Measuring bioavailable PAHs in estuarine water using semipermeable membrane devices with performance reference compounds[J]. Marine Pollution Bulletin, 89(1/2): 376–383.
|
Cornelissen G, Pettersen A, Broman D, et al. 2008. Field testing of equilibrium passive samplers to determine freely dissolved native polycyclic aromatic hydrocarbon concentrations[J]. Environmental Toxicology and Chemistry, 27(3): 499–508.
DOI:10.1897/07-253.1
|
Dai G H, Liu X H, Liang G, et al. 2013. Evaluating the sediment-water exchange of hexachlorocyclohexanes(HCHs) in a major lake in North China[J]. Environmental Science-Processes & Impacts, 15(2): 423–432.
|
Difilippo E L, Eganhouse R P. 2010. Assessment of PDMS-water partition coefficients:implications for passive environmental sampling of hydrophobic organic compounds[J]. Environmental Science & Technology, 44(18): 6917–6925.
|
Doong R A, Chang S M, Sun Y C. 2000. Solid-phase microextraction for determining the distribution of sixteen US Environmental Protection Agency polycyclic aromatic hydrocarbons in water samples[J]. Journal of Chromatography A, 879(2): 177–188.
DOI:10.1016/S0021-9673(00)00347-2
|
范娟, 周岩梅. 2015. LDPE膜被动采样技术预测模型的建立及其应用[J]. 中国环境科学, 2015, 35(11): 3340–3345.
DOI:10.3969/j.issn.1000-6923.2015.11.019 |
Fernandez L A, Lao W, Maruya K A, et al. 2014. Calculating the diffusive flux of persistent organic pollutants between sediments and the water column on the Palos Verdes Shelf Superfund site using polymeric passive samplers[J]. Environmental Science & Technology, 48(7): 3925–3934.
|
Forsberg N D, Smith B W, Sower G J, et al. 2014. Predicting polycyclic aromatic hydrocarbon concentrations in resident aquatic organisms using passive samplers and partial least-squares calibration[J]. Environmental Science & Technology, 48(11): 6291–6299.
|
Ouyang G F, Cui S F, Qin Z P, et al. 2009. One-calibrant kinetic calibration for on-site water sampling with solid-phase microextraction[J]. Analytical Chemistry, 81: 5629–5636.
DOI:10.1021/ac900315w
|
Huckins J N, Manuweera G K, Petty J D, et al. 1993. Lipid-containing semipermeable membrane devices for monitoring organic contaminants in water[J]. Environmental Science & Technology, 27(12): 2489–2496.
|
Huckins J N, Petty J D, Lebo J A, et al. 2002. Development of the permeability/performance reference compound approach for in situ calibration of semipermeable membrane devices[J]. Environmental Science & Technology, 36(1): 85–91.
|
Liu H H, Bao L J, Feng W H, et al. 2013a. A multisection passive sampler for measuring sediment porewater profile of dichlorodiphenyltrichloroethane and its metabolites[J]. Analytical Chemistry, 85(15): 7117–7124.
DOI:10.1021/ac400589a
|
Liu H H, Bao L J, Zhang K, et al. 2013b. Novel passive sampling device for measuring sediment-water diffusion fluxes of hydrophobic organic chemicals[J]. Environmental Science & Technology, 47(17): 9866–9873.
|
刘大超, 徐秋萍, 张浏, 等. 2018. 基于逸度方法评价巢湖流域PAHs在水体-沉积物间扩散过程[J]. 环境科学学报, 2018, 38(3): 930–939.
|
Ouyang G, Pawliszyn J. 2006. SPME in environmental analysis[J]. Analytical and Bioanalytical Chemistry, 386(4): 1059–1073.
DOI:10.1007/s00216-006-0460-z
|
Qin N, He W, Kong X Z, et al. 2013. Ecological risk assessment of polycyclic aromatic hydrocarbons(PAHs) in the water from a large Chinese lake based on multiple indicators[J]. Ecological Indicators, 24: 599–608.
DOI:10.1016/j.ecolind.2012.08.019
|
Ren C, Wu Y, Zhang S, et al. 2015. PAHs in sediment cores at main river estuaries of Chaohu Lake:implication for the change of local anthropogenic activities[J]. Environmental Science and Pollution Research, 22(3): 1687–1696.
DOI:10.1007/s11356-014-3141-z
|
Tomaszewski J E, Luthy R G. 2008. Field deployment of polyethylene devices to measure PCB concentrations in pore water of contaminated sediment[J]. Environmental Science & Technology, 42(16): 6086–6091.
|
Wang D G, Alaee M, Byer J, et al. 2011a. Fugacity approach to evaluate the sediment-water diffusion of polycyclic aromatic hydrocarbons[J]. Journal of Environmental Monitoring, 13(6): 1589–1596.
DOI:10.1039/c0em00731e
|
Wang J Z, Zhang K, Liang B, et al. 2011b. Occurrence, source apportionment and toxicity assessment of polycyclic aromatic hydrocarbons in surface sediments of Chaohu, one of the most polluted lakes in China[J]. Journal of Environmental Monitoring, 13(12): 3336–3342.
DOI:10.1039/c1em10599j
|
王继忠.2017.水体沉积物界面有机污染物渐升式被动采样器[P].中国.CN206523320U.2017-09-26
http://cprs.patentstar.com.cn/Search/Detail?ANE=5BCA9BIA9HHG9CIDAIIA9EHC9BIF9ICF9GCE9BEF5DCA8ADA |
 2019, Vol. 39
2019, Vol. 39


