2. 青岛环能沧海生态科技有限责任公司, 青岛 266041
2. SCIMEE Technology & Science Co., Ltd., Qingdao 266041
近年来, 伴随着采矿、制革、电镀、电池和金属表面涂层处理等行业的快速发展(Cheng et al., 2012; 师杰等, 2016), 产生了大量含Cu2+、Pb2+、Zn2+、Cd2+等重金属离子的废水(Zwonitzer et al., 2003; 王哲等, 2016).重金属具有剧毒、难降解等特点, 进入环境后会对生态环境和人类健康造成不利的影响(刘旸等, 2014; 王棋等, 2017; Wang et al., 2018), 目前已成为全球性的环境问题.
重金属废水处理的方法有很多, 包括化学沉淀法、离子交换吸附法、电解法和膜分离法等, 然而上述这些常规方法存在管理复杂、运行费用高、可能产生二次污染等问题(Gao et al., 2016; 任博等, 2016; Wang et al., 2018).人工湿地作为一种高效、环保的污水处理技术, 被广泛用于重金属污水的处理中(Ciarkowska et al., 2014; Lv et al., 2017).填料作为人工湿地的重要组成部分, 在去除重金属过程中起主导作用(Yagub et al., 2014; Vymazal et al., 2016).然而, 当前研究主要集中在人工湿地植物去除重金属方面(Březinová et al., 2015;Bragato et al., 2009), 对传统填料的研究较少且不深入.而土壤、沸石、石灰石(Allende et al., 2011)等传统填料及工业废料(Hua et al., 2015)等普遍存在吸附量少、吸附后易解吸等问题(易文涛, 2015), 这限制了人工湿地在重金属废水处理中的应用.
纳米材料具有表面能高、吸附容量大等优点, 在重金属废水处理中展现出巨大的应用前景(肖乐勤等, 2011; Ma et al., 2017).其中, 钛酸钠纳米纤维材料具有TiO6八面体结合形成的负电荷层状结构, 层间有可交换的钠离子, 可以选择性地通过离子交换吸收二价重金属离子(Yang et al., 2008a; Di et al., 2017), 而且吸附会引起负电荷层状结构的显著变形, 从而使重金属永久封存到纤维里(Yang et al., 2008b).然而, 实际应用中粉末状的纳米材料存在粒径小、难分离回收及容易导致二次污染等问题(Liu et al., 2008).因此, 将填料和纳米材料的优势结合起来, 将纳米材料制成填料并应用于人工湿地, 会在很大程度上解决传统填料吸附容量低、易解吸造成二次污染等问题.
在前期的研究中, 本课题组研究了钛酸钠纳米纤维制备成新型填料对单一重金属的吸附性能, 结果表明, 钛酸钠填料对单一重金属具有良好的吸附能力.但实际水环境是多种重金属离子的混合体系, 各种离子之间会发生协同或拮抗的作用, 其吸附过程远比单一重金属吸附复杂(曹煊等, 2009; Chen et al., 2011), 而目前关于多种重金属共存情况下的竞争性吸附研究较少.针对上述问题, 本实验探究Cu2+、Pb2+、Zn2+和Cd2+共存条件下新型钛酸钠填料的竞争吸附规律, 以获得竞争吸附分配系数, 评估该新型填料对多种重金属共存的吸附行为, 确定填料在自然环境下对重金属的吸附容量, 为钛酸钠填料在人工湿地去除重金属中的应用提供理论依据和技术支持.
2 材料与方法(Materials and methods) 2.1 试验材料以钛酸钠(Na2Ti3O7)纳米纤维为原料, 制备新型钛酸钠填料(图 1).首先将钛酸钠纳米材料、固化剂和NH4HCO3按1:1:0.5的质量比均匀混合, 加入适量的水, 用玻璃棒搅拌后倒入模具, 在110 ℃下干燥4 h, 冷却至室温后形成一定直径(约17 mm)的半球状填料; 然后将其粉碎并过60目筛, 装入聚乙烯塑料自封袋中备用.实验所用的Cu(NO3)2·3H2O、Pb(NO3)2、Zn(NO3)2·6H2O、Cd(NO3)2·4H2O、HNO3、NaOH等均为分析纯, 实验用水为蒸馏水, 分别配制重金属离子浓度均为10 mmol·L-1的4种标准溶液备用.采用电感耦合等离子体发射光谱仪(ICP-OES, optima 8000, 铂金埃尔默企业管理有限公司)测定溶液中重金属离子浓度.
 |
| 图 1 新型钛酸钠填料的制备及吸附重金属示意图 Fig. 1 Preparation of new-sodium titanate filler and schematic diagram of heavy metal adsorption |
填料的比表面积与孔径采用比表面积及孔隙度分析仪(Tristar-3000, 上海Micromeritics公司)测定, 测试气体为氮气, 饱和蒸气压为1.0316 bar(1 bar=105 Pa).表面形貌采用JSM-7100F发射扫描电子显微镜进行分析.样品与溴化钾的质量比约为1:10, 压成薄片, 用NEXU-670傅立叶红外光谱仪(FT-IR, 美国Thermo Scientific公司)进行红外光谱分析.
2.3 吸附实验单一重金属吸附实验:分别配制初始浓度为0.3~1.5 mmol·L-1的Cu2+、Pb2+、Zn2+和Cd2+溶液, 结果显示, 新型钛酸钠填料对Cu2+、Pb2+、Zn2+和Cd2+的最大吸附容量分别为1.610、1.986、1.565和1.616 mmol·g-1.
多元竞争吸附实验:吸附质为Cu2+、Pb2+、Zn2+和Cd2+ 4种离子的混合溶液体系, 研究4种重金属离子共存条件下, 填料对其竞争吸附的能力.每种重金属离子浓度相同, 分别设置为0.3、0.5、0.8、1.0和1.5 mmol·L-1.分配系数Kd表示经过一段反应时间, 吸附达到平衡时重金属离子在固相中的浓度与其在液相中浓度的比值(Park et al., 2016), 是评估吸附剂对重金属离子吸附容量的一个非常重要的指标.Kd值越高, 说明固相通过吸附反应对重金属离子的截留率越高, 重金属离子的生物可利用度越低; 反之, 说明溶液中剩余重金属离子浓度越高.Kd可以通过式(1)计算得到(Alloway, 1995).

|
(1) |
式中, Kd为吸附分配系数(L·kg-1); Co、Ce分别为重金属溶液初始浓度及平衡浓度(mmol·L-1); V是重金属废水的体积(mL); m为吸附剂质量(g).
对于二元竞争实验, 分别设置Cu2+-Pb2+、Cu2+-Zn2+、Cu2+-Cd2+、Pb2+-Zn2+、Pb2+-Cd2+和Zn2+-Cd2+ 6组二元竞争实验, 每组离子的浓度之和为2 mmol·L-1.以Cu2+-Pb2+为例说明重金属离子的初始浓度设置情况(表 1), 其它5组与此相同.
| 表 1 二元竞争溶液初始浓度值 Table 1 Initial concentration of binary systems |
对于三元竞争实验, 分别设置Cu2+-Pb2+-Zn2+、Cu2+-Pb2+-Cd2+、Pb2+-Zn2+-Cd2+、Cu2+-Zn2+-Cd2+ 4组实验, 每组中3种重金属离子浓度相同, 分别为0、0.5、0.8、1.0、1.5和1.8 mmol·L-1.
上述所有实验, 样品溶液体积均为100 mL, pH为(5.2±0.2), 加入30 mg新型钛酸钠填料吸附剂, 在恒温25 ℃下振荡36 h, 上清液均用0.45 μm滤膜过滤, 滤液用于测试.每个实验做3个平行样, 平衡吸附量(Qe)由式(2)进行计算.
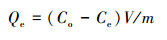
|
(2) |
新型钛酸钠填料的SEM和EDS结果如图 2所示.可以看出, 该填料的纤维状结构在混合和干燥过程中没有遭到破坏, 其表现出的层状结构及层间含有可交换的钠离子(Yang et al., 2008b; Liu et al., 2013), 使新型钛酸钠填料具有较大的重金属吸附容量.钛酸钠填料由Na2Ti3O7、固化剂和造孔剂(NH4HCO3)制作而成, 由于NH4HCO3在110 ℃干燥过程中挥发, 所以填料的主要元素组成为Ti、Na、C、O、Si(表 2).Na元素约占填料中所有元素的10%, 说明其在制作过程中没有流失, 因而可以保证有较多的Na+与重金属进行离子交换, 达到去除重金属的目的.
| 表 2 新型钛酸钠填料主要元素组成 Table 2 Element compositions of new-sodium titanate filler |
 |
| 图 2 新型钛酸钠填料的SEM(a)及EDS(b)图 Fig. 2 SEM(a) and EDS(b) images of new-sodium titanate filler |
由表 3可知, 该填料比表面积较小, 可能是由于固化剂粘结过程中多个纤维粘结在一起造成的.而填料具有较大的孔径, 则是由具有规则的纤维状的空隙结构导致的(王棋等, 2017).
| 表 3 新型钛酸钠填料的BET参数 Table 3 New-sodium titanate filler parameters of BET |
从填料的红外谱图可以看出, Na2Ti3O7和钛酸钠填料的主要吸收峰位具有相似性, 但也存在一定的差异(图 3).3133 cm-1处较宽的吸收峰对应于不饱和烃C—H的伸缩振动, 1632 cm-1处的吸收峰对应于烯烃C=C的伸缩振动, 烯烃C—H面外弯曲振动对应681 cm-1峰; 907 cm-1附近的吸收峰由Ti—O伸缩振动所致(Xiong et al., 2011); 472 cm-1附近的吸收峰是TiO6(八面体)键的对称伸缩振动引起的(Chen et al., 2010; Zhu et al., 2018).当固化剂修饰到Na2Ti3O7上后, 钛酸钠填料的红外光谱(图 3)与Na2Ti3O7相比, 之前的Na2Ti3O7所有的峰都还保留着, 说明固化剂的修饰没有对Na2Ti3O7造成影响.此外, 钛酸钠填料还增加了新的吸收峰:在2959 cm-1附近有一个较弱的吸收峰, 代表了饱和C—H伸缩振动峰; 2188 cm-1处对应于C≡N三键吸收峰; 1508 cm-1吸收峰主要由于苯环骨架的伸缩振动引起; 1241 cm-1对应C—O伸缩振动; 1040 cm-1处的吸收峰对应伯醇振动吸收.2188 cm-1和1508 cm-1处的吸收峰分别对应固化剂的主要成分双氰胺和双酚A型环氧树脂.
 |
| 图 3 Na2Ti3O7和新型钛酸钠填料的红外光谱图 Fig. 3 FT-IR spectra of Na2Ti3O7 and new-sodium titanate filler |
实际重金属废水中通常含有多种金属离子, 多种金属离子共存的条件下可能会影响某一重金属离子在吸附剂表面的结合效率.不同重金属离子的物理化学性质不同, 因此, 与吸附剂表面官能团的结合强度存在差异, 从而导致多种金属离子共存时的吸附效率与单一重金属离子吸附不尽相同.如图 4所示, 四元重金属离子之间的竞争影响了所有重金属的吸附.当4种金属离子处于较低初始浓度时, 它们之间不存在竞争关系, 这是由于填料具有较大的吸附容量; 随着初始浓度的逐渐升高, 4种金属离子的吸附差异越来越明显, 表现为:Cu2+、Zn2+和Cd2+的吸附量在高平衡浓度下呈下降趋势, Pb2+的吸附量依然随着平衡浓度的升高而升高, 这说明重金属离子的初始浓度越高, 不同金属离子对吸附位点的竞争越激烈.当有其它离子参与吸附时, Cu2+、Zn2+和Cd2+这3种重金属离子相比于单一离子吸附, 吸附容量都大幅度降低, 而Pb2+的吸附量没有降低反而比单一吸附量还要高一些, 说明当溶液中存在其它重金属离子时, 不会影响填料对Pb2+的吸附量, 填料仍然优先吸附Pb2+.在高浓度下, 4种金属离子的总吸附量为1.956 mmol·g-1, 而新型钛酸钠填料对Cu2+、Pb2+、Zn2+和Cd2+的最大吸附容量分别为1.610、1.986、1.565和1.616 mmol·g-1.由于4种金属离子竞争吸附, 吸附容量受每种离子水解常数、电负性及水合半径等影响(Park et al., 2016), 使总吸附量有所变化.
 |
| 图 4 4种重金属离子单一和竞争吸附的吸附实验结果对比 Fig. 4 The adsorption results of four heavy metal ions were compared between single and competitive adsorption |
四元竞争吸附分配系数如表 4所示, 当初始浓度一定时, Pb2+的Kd值最高, Cu2+的Kd值次之, Zn2+和Cd2+的Kd值最低.上述结果表明, 在竞争吸附过程中, 重金属在钛酸钠填料上的选择性顺序为:Pb2+>Cu2+>Zn2+>Cd2+.
| 表 4 4种重金属离子四元竞争分配系数Kd Table 4 Kd of four heavy metal ions |
竞争离子的选择性吸附除了与分配系数有关外, 也与重金属离子本身的水解常数、电负性及水合半径等有关(林青等, 2008; 庞婷雯等, 2018).金属吸附亲和力随水解常数负对数(pK)的增大而减小, 即随着重金属离子水解常数的升高, 吸附剂对离子的专性吸附降低.由表 5可知, Pb2+的pKH(7.71)低于Zn2+和Cd2+, 而电负性比其它离子高; 此外, 对于相同价态的阳离子, 吸附能力的大小很大程度上取决于水合离子半径, 其中,水合离子半径越小, 越容易与吸附剂发生离子交换(王哲等, 2016).由于Pb2+的水合半径小于Cd2+和Zn2+, 因此, Pb在有机质大多数官能团中具有较大的亲和力.上述因素都保证了Pb2+比Cd2+和Zn2+更利于通过表面络合或吸附反应被吸附.分析该填料优先吸附Pb2+的原因有:①水解常数较大; ②原子质量较高; ③离子半径大(即水合半径小); ④Misono柔软度值较大, Misono柔软度参数通常是由金属离子半径和电离电势决定的指数(Sposito, 1989).该吸附剂选择性吸附重金属离子的结果也与其他学者的实验结果一致(Inyang et al., 2012; Xue et al., 2012; Park et al., 2016).
| 表 5 基于重金属性质的吸附亲和作用大小 Table 5 Sequence of adsorption affinity based on the properties of heavy metals |
Kd值随着重金属离子初始浓度的增大而降低, 说明参与吸附过程的活性位点的性质变化.实验中离子浓度越低, 对应的Kd值越高, 这是与吸附位点强的键合能力而具有的高选择性相关的.重金属离子浓度越高, 活性吸附位点则相对不足, 吸附逐渐趋于饱和, 从而导致Kd值下降.
3.2.3 三元竞争吸附三元竞争吸附结果如图 5所示.当有Pb2+参与竞争吸附时, 其余两种重金属离子的吸附被显著地抑制, 表现为Pb2+的吸附量远远高于其它两种重金属离子的吸附量, 并且随着平衡浓度的升高, Pb2+的吸附量大致呈现一种上升的趋势, 而其余两种重金属离子的吸附量逐渐降低或短暂的升高, 随后降低.当没有Pb2+参与竞争时, Cu2+的吸附量高于其它两种重金属离子的吸附量(图 5c), 但与Pb2+相比, Cu2+对Zn2+和Cd2+的竞争影响作用稍小一些.随着浓度的升高, Cu2+、Zn2+和Cd2+的吸附量都呈下降的趋势, 说明在低浓度下, 该填料优先吸附Cu2+, 但也不抑制吸附Zn2+和Cd2+; 而在高浓度下, 3种重金属离子之间相互抑制.从4种离子整体吸附量来看, Zn2+和Cd2+的竞争吸附最弱, Pb2+和Cu2+更容易被吸附去除, 这与之前四元竞争的研究结果一致.
 |
| 图 5 三元重金属离子的竞争吸附吸附量随平衡浓度的变化曲线 Fig. 5 The variation of adsorption quantity with the equilibrium concentrations in ternary systems |
另外, 从图中可以看出, Cu-Pb-Zn三元体系中, 高浓度时Pb2+和Zn2+的吸附量都增加, 而其他三元体系中高浓度时金属的吸附量降低, 这主要是因为对于竞争吸附, 吸附效果不仅与水解常数有关, 还与金属离子的电负性、水合半径和相对原子质量有关.其他三元体系(Cu-Pb-Cd和Pb-Zn-Cd)中, 高浓度时Pb2+的吸附量降低, 则归因于Cd的电负性、水合半径及相对原子质量较高(表 5), 导致Pb2+的吸附量降低; 另外, 在三元体系(Cu-Zn-Cd和Pb-Zn-Cd)中, Zn2+浓度较高时, 其吸附量降低也是这个原因.
3.2.4 双组分竞争吸附图 6A是竞争吸附时钛酸钠填料对Cu2+和Pb2+的吸附情况, 可以看出, Cu2+和Pb2+二者相互作用比较明显.竞争吸附时, Pb2+对Cu2+的影响比Cu2+对Pb2+的影响更大, 即使在Pb2+初始浓度较低的情况下, 填料也是优先吸附Pb2+.二者的总吸附量最大为1.83 mmol·g-1, 最低为1.29 mmol·g-1.在填料对Cu2+和Zn2+的竞争吸附情况中(图 6B), 在Cu2+初始浓度较低、Zn2+初始浓度较高时, 填料优先吸附Cu2+; 在二者初始浓度相同时, 填料仍然优先吸附Cu2+, 可见Cu2+对Zn2+的抑制作用比Zn2+对Cu2+的更大, 二者的总吸附量最大为1.29 mmol·g-1, 最低为1.17 mmol·g-1.由于单一吸附时Cd2+的吸附量和Cu2+相差不大, 竞争吸附时, 二者吸附量都大幅度降低, 说明二者存在竞争关系, 在吸附过程中相互抑制, 二者的总吸附量最大为1.28 mmol·g-1, 最低为1.1 mmol·g-1(图 6C).图 6D是Zn2+和Cd2+的竞争吸附情况, 由图可以看出, Zn2+浓度低、Cd2+浓度高时, 二者之间的抑制作用不大.随着Zn2+初始浓度的升高, Cd2+的吸附逐渐被抑制, 说明Zn2+在二者竞争吸附中占优势, 二者的总吸附量最大为1.52 mmol·g-1, 最低为1.41 mmol·g-1.图 6E中Pb2+与Zn2+的竞争关系和图 6F中Pb2+与Cd2+的竞争关系与图 6A基本相同, 都表现为有Pb2+参与竞争时, 其余离子都被抑制.而图 6E中Pb2+与Zn2+的竞争吸附中, 二者的总吸附量最大为1.98 mmol·g-1, 最低为1.79 mmol·g-1.图 6F中Pb2+与Cd2+的竞争吸附中, 二者的总吸附量最大为1.99 mmol·g-1, 最低为1.82 mmol·g-1.
 |
| 图 6 双组分竞争吸附吸附量随初始浓度变化关系 Fig. 6 The variation of adsorption quantity with the equilibrium concentrations in binary systems |
从总吸附量来看, 当有Pb2+参与竞争时, 总吸附量相对较高, 只是因为其他离子的存在促进了Pb2+的吸附, 导致总体吸附量偏高; 而没有Pb2+参与竞争时, 总吸附量较低, 这是因为这两种离子吸附过程中相互抑制, 导致总体吸附量偏低.Zn2+和Cd2+竞争吸附过程中, 先是互不影响, 而后其中一种离子被抑制, 导致其总体吸附量相比之下处于中等(易文涛, 2015).图 6a~6f对应图 6A~6F竞争吸附量的变化, 根据线性拟合的可决系数可知, 拟合度非常高, 由此可知, 每两种离子之间都存在明显的离子替换作用.
4 结论(Conclusions)重金属离子在新型钛酸钠填料上的吸附主要是离子交换作用.单一吸附时, 钛酸钠填料表现出较高的吸附容量.四元金属竞争吸附结果表明, 该新型填料竞争总吸附量仍显著高于传统填料吸附量.填料对4种金属离子(Cu2+、Pb2+、Zn2+和Cd2+)具有不同的优先选择性, 其分配系数Kd的大小为Pb2+>Cu2+>Zn2+>Cd2+, 这与重金属离子的第一水解常数大小顺序一致.因此, Cu2+和Pb2+, 尤其是Pb2+, 是填料吸附效果最好的重金属离子, 而Zn2+和Cd2+在吸附过程中容易受到其它二价金属离子的影响.三元竞争和双组分竞争实验进一步证实4种金属离子之间的竞争关系, 当有其它金属离子参与竞争时, 会促进Pb2+的吸附, 而Cu2+、Zn2+和Cd2+相互之间竞争时表现出相互抑制的拮抗作用.
Allende K L, Fletcher T D, Sun G. 2011. The effect of substrate media on the removal of arsenic, boron and iron from an acidic wastewater in planted column reactors[J]. Chemical Engineering Journal, 179(4): 119–130.
|
Alloway B J. 1995. Soil processes and the behaviour of metals[J]. Heavy Metals in Soils, 13: 3488.
|
Bragato C, Schiavon M, Polese R, et al. 2009. Seasonal variation of Cu, Zn, Ni and Cr concentration in Phragmites australis (Cav.) Trin.ex Steudel in a constructed wetland of North Italy[J]. Desalination, 246(1): 35–44.
|
Březinová T, Vymazal J. 2015. Evaluation of heavy metals seasonal accumulation in Phalaris arundinacea in a constructed treatment wetland[J]. Ecological Engineering, 79(3): 94–99.
|
曹煊, 孙继昌, 金春姬, 等. 2009. 碱渣对重金属的竞争吸附实验研究[J]. 山东科学, 2009, 22(6): 17–20.
|
Chen X, Chen G, Chen L, et al. 2011. Adsorption of copper and zinc by biochars produced from pyrolysis of hardwood and corn straw in aqueous solution[J]. Bioresource Technology, 102(19): 8877–8884.
DOI:10.1016/j.biortech.2011.06.078
|
Chen Y C, Lo S L, Kuo J, et al. 2010. Pb(Ⅱ) adsorption capacity and behavior of titanate nanotubes made by microwave hydrothermal method[J]. Colloids and Surfaces A, 361(1): 126–131.
|
Cheng T W, Lee M L, Ko M S, et al. 2012. The heavy metal adsorption characteristics on metakaolin-based geopolymer[J]. Applied Clay Science, 56(1): 90–96.
|
Ciarkowska K, Sołekpodwika K, Wieczorek J. 2014. Enzyme activity as an indicator of soil-rehabilitation processes at a zinc and lead ore mining and processing area[J]. Journal Environmental Management, 132(132C): 250–256.
|
Di B L, Volpe A, Pagano M, et al. 2017. Amorphous boron-doped sodium titanates hydrates:Efficient and reusable adsorbents for the removal of Pb2+ from water[J]. Journal of Hazardous Materials, 324(Part B): 168–177.
|
Gao X M, Zhang Y, Dai Y, et al. 2016. High-performance magnetic carbon materials in dye removal from aqueous solutions[J]. Journal of Solid State Chemistry, 239: 265–273.
DOI:10.1016/j.jssc.2016.05.001
|
Hua T, Haynes R J, Zhou Y F, et al. 2015. Potential for use of industrial waste materials as filter media for removal of Al, Mo, As, V and Ga from alkaline drainage in constructed wetlands——adsorption studies[J]. Water Research, 71: 32–41.
DOI:10.1016/j.watres.2014.12.036
|
Inyang M, Gao B, Yao Y, et al. 2012. Removal of heavy metals from aqueous solution by biochars derived from anaerobically digested biomass[J]. Bioresource Technology, 110(2): 50–56.
|
林青, 徐绍辉. 2008. 土壤中重金属离子竞争吸附的研究进展[J]. 土壤, 2008, 40(5): 706–711.
DOI:10.3321/j.issn:0253-9829.2008.05.005 |
Liu W, Wang T, Borthwick A G, et al. 2013. Adsorption of Pb2+, Cd2+, Cu2+ and Cr3+ onto titanate nanotubes:competition and effect of inorganic ions[J]. Science of the Total Environment, 456-457(7): 171–180.
|
Liu X, Hu Q, Fang Z, et al. 2008. Magnetic chitosan nanocomposites:a useful recyclable tool for heavy metal ion removal[J]. Langmuir, 25(1): 3–8.
|
刘旸, 赵雪松, 潘学军, 等. 2014. Fe3O4基多功能磁性纳米颗粒吸附重金属研究进展[J]. 水处理技术, 2014, 40(12): 5–10.
|
Lv T, Carvalho P N, Zhang L, et al. 2017. Functionality of microbial communities in constructed wetlands used for pesticide remediation:influence of system design and sampling strategy[J]. Water Research, 110: 241–251.
DOI:10.1016/j.watres.2016.12.021
|
Ma J, Li F, Qian T W, et al. 2017. Natural organic matter resistant powder activated charcoal supported titanate nanotubes for adsorption of Pb(Ⅱ)[J]. Chemical Engineering Journal, 315: 191–200.
DOI:10.1016/j.cej.2017.01.029
|
庞婷雯, 杨志军, 黄逸聪, 等. 2018. 巯基化、钠化和酸化膨润土对Cu2+, Pb2+和Zn2+的吸附性能研究[J]. 光谱学与光谱学分析, 2018, 38(4): 1203–1208.
|
Park J H, Ok Y S, Kim S H, et al. 2016. Competitive adsorption of heavy metals onto sesame straw biochar in aqueous solutions[J]. Chemosphere, 142: 77–83.
DOI:10.1016/j.chemosphere.2015.05.093
|
任博, 马丽丽, 游少鸿. 2016. 人工湿地技术处理矿山重金属废水现状与发展[J]. 资源信息与工程, 2016, 31(6): 201–202.
|
师杰, 赵志伟, 崔福义, 等. 2016. 化学改性强化活性炭纤维吸附重金属离子[J]. 哈尔滨工业大学学报, 2016, 48(8): 102–107.
|
Sposito G. 1989. The Chemistry of Soils[M]. New York: Oxford University Press.
|
Vymazal J, Březinová T. 2016. Accumulation of heavy metals in aboveground biomass of Phragmites australis in horizontal flow constructed wetlands for wastewater treatment:A review[J]. Chemical Engineering Journal, 290: 232–242.
DOI:10.1016/j.cej.2015.12.108
|
王棋, 王斌伟, 谈广才, 等. 2017. 生物炭对Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)和Cd(Ⅱ)的单一及竞争吸附研究[J]. 北京大学学报, 2017, 53(6): 1122–1132.
|
Wang Y Y, Liu Y X, Lu H H, et al. 2018. Competitive adsorption of Pb(Ⅱ), Cu(Ⅱ), and Zn(Ⅱ) ions onto hydroxyapatite-biochar nanocomposite in aqueous solutions[J]. Journal of Solid State Chemistry, 261: 53–61.
DOI:10.1016/j.jssc.2018.02.010
|
王哲, 徐毅, 黄国和, 等. 2016. 对硝基苯酚和重金属在高炉水淬渣上的竞争吸附研究[J]. 中国环境科学, 2016, 36(12): 3686–3695.
DOI:10.3969/j.issn.1000-6923.2016.12.021 |
肖乐勤, 陈霜艳, 周伟良. 2011. 改性活性炭纤维对重金属离子的动态吸附研究[J]. 环境工程, 2011, 29(S1): 289–293.
|
Xiong L, Chen C, Chen Q, et al. 2011. Adsorption of Pb (Ⅱ) and Cd (Ⅱ) from aqueous solutions using titanate nanotubes prepared via hydrothermal method[J]. Journal of Hazardous Materials, 189(3): 741–748.
DOI:10.1016/j.jhazmat.2011.03.006
|
Xue Y, Gao B, Yao Y, et al. 2012. Hydrogen peroxide modification enhances the ability of biochar (hydrochar) produced from hydrothermal carbonization of peanut hull to remove aqueous heavy metals:batch and column tests[J]. Chemical Engineering Journal, 200-202(34): 673–680.
|
Yagub M T, Sen T K, Afroze S, et al. 2014. Dye and its removal from aqueous solution by adsorption:A review[J]. Advances in Colloid & Interface Science, 209(7): 172–184.
|
Yang D J, Zheng Z F, Liu H W, et al. 2008a. Layered titanate nanofibers as efficient adsorbents for removal of toxic radioactive and heavy metal ions from water[J]. Journal of Physical Chemistry C, 112(42): 16275–16280.
DOI:10.1021/jp803826g
|
Yang D J, Zheng Z F, Zhu H Y, et al. 2008b. Titanate nanofibers as intelligent absorbents for the removal of radioactive ions from water[J]. Advanced Materials, 20: 2777–2781.
DOI:10.1002/adma.v20:14
|
易文涛.2015.沸石填料人工湿地去除雨水径流重金属污染的研究[D].杭州: 浙江大学
http://cdmd.cnki.com.cn/Article/CDMD-10335-1015591960.htm |
Zhu J H, Liu Q, Li Z S, et al. 2018. Efficient extraction of uranium from aqueous solution using an aminofunctionalized magnetic titanate nanotubes[J]. Journal of Hazardous Materials, 353: 9–17.
DOI:10.1016/j.jhazmat.2018.03.042
|
Zwonitzer J C, Pierzynski G M, Hettiarachchi G M. 2003. Effects of phosphorus additions on lead, cadmium, and zinc bioavailabilities in a metal-contaminated soil[J]. Water Air and Soil Pollution, 143(1/4): 193–209.
DOI:10.1023/A:1022810310181
|
 2019, Vol. 39
2019, Vol. 39


