2. 国家环境保护水土污染协同控制与联合修复重点实验室, 成都 610059;
3. 成都理工大学环境学院, 成都 610059;
4. 成都理工大学环境与土木工程学院, 成都 610059
2. State Environmental Protection Key Laboratory of Synergetic Control and Joint Remediation for Soil & Water Pollution(SEKL-SW), Chengdu 610059;
3. College of Environment, Chengdu University of Technology, Chengdu 610059;
4. College of Environment and Civil Engineering, Chengdu University of Technology, Chengdu 610059
邻苯二甲酸酯(Phthalate Esters, PAEs)俗称酞酸酯, 在工业中常作为增塑剂, 是一种典型的内分泌干扰素, 会影响人体的生殖健康(张蕴晖等, 2007).随着对PAEs研究的不断深入, 大量实验表明, PAEs还具有“三致”性(张海光等, 2013), 但近年来PAEs的使用日趋广泛(刘庆等, 2012).目前, 许多国家已经将邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二辛酯(DOP)、邻苯二甲酸丁苄酯(BBP)、邻苯二甲酸二正丁酯(DBP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二甲酯(DMP)列为优先控制的有毒污染物(Chang et al., 2007).PAEs的辛醇-水分配系数较大, 具有容易吸附于沉积物和土壤颗粒物上的环境性质(梁婧等, 2014), 因此, 土壤是环境中PAEs的重要归趋(宋广宇等, 2010).土壤PAEs污染将会对人体健康构成严重威胁(Li et al., 2017), 所以修复PAEs污染土壤具有重要的现实意义.
根据PAEs的性质, 修复PAEs污染土壤通常可采用化学氧化、土壤淋洗等方法(Wang et al., 2016).其中, 土壤淋洗法是土壤修复中一种常用的技术, 一般常见的淋洗剂有表面活性剂类(程洪珍等, 2014)、有机溶剂、环糊精及其衍生物等(王光辉等, 2016).表面活性剂类通常会减小水土界面张力, 造成污染物扩散(Cheng et al., 2016); 有机溶剂(如甲醇等)通常具有一定的毒性.研究表明, 环糊精类的立体空腔结构不会造成水土界面张力的变化, 同时, 环糊精主要由淀粉水解得到, 因此, 环糊精用于土壤淋洗更加安全可靠(Flaherty et al., 2013).环糊精按照葡萄糖单元数量分为α-、β-、γ- 3种, 其内腔径分别为0.47~0.53、0.60~0.65、0.75~0.83 nm.环糊精类衍生物有“内腔疏水、外缘亲水”的特性(Trellu et al., 2016), 能够与多种难溶有机物形成易溶于水的主客体包合物(Rafin et al., 2009), 这种包合物的稳定性与环糊精的腔径有直接关系.PAEs分子由1个苯环及2个酯键基团组成, 苯环大小约为0.58 nm, 其尺寸大小与β-环糊精相近, 这说明在理论上用环糊精对PAEs污染土壤进行修复具有一定的可行性.而目前有关利用环糊精淋洗修复DBP污染土壤的研究还未见报道, 其淋洗修复的基本参数不明确.因此, 本文着重研究羟丙基-β-环糊精(HPCD)在土壤介质中吸附解吸PAEs(以DBP为例)的规律, 通过平衡吸附法研究加入HPCD的实验组与对照组中DBP的等温吸附模型及吸附动力学, 并考察HPCD浓度、pH、离子强度对DBP吸附解吸的影响.
2 材料与方法(Materials and methods) 2.1 实验土壤及污染土壤制备选择校园土壤为试验土壤, 所选的校园土壤为典型的成都粘土, 经风干、研碎, 过100目筛待用, 其基本物化性质见表 1.
| 表 1 试验土壤的理化性质 Table 1 Physical and chemical properties of soil |
污染土壤制备:称取500 g供试土壤, 将其与配制好的250 mL 500 mg·L-1的DBP甲醇溶液混合, 持续搅拌, 待充分混匀后自然风干老化4周, 测定得到配制土壤的DBP含量为(244±4) mg·kg-1.
2.2 试剂与仪器试剂:邻苯二甲酸二丁酯标准品, 纯度为99%;甲醇(色谱纯)、氯化钙(分析纯)、正己烷(分析纯, 经二次蒸馏)均购自成都市科龙化工试剂厂.
仪器:日立L-7200型高效液相色谱仪(日本HITCHI公司), 配DAD检测器; SHZ-82型水浴恒温振荡器、TDL-4A型离心机、紫外可见光分光光度计.
2.3 实验设计 2.3.1 吸附实验等温吸附:取2.0 g供试土壤及0.125 g HPCD于200 mL具塞三角瓶中, 加入50 mL浓度为0~20 mg·L-1的DBP污染液溶液(先用甲醇配制50 mg·L-1的DBP, 再按实验浓度进行稀释); 加塞后置于恒温振荡器中, 25 ℃条件下振荡7 h, 实验共设3个平行.
吸附动力学:取2.0 g供试土壤及0.125 g HPCD于200 mL具塞三角瓶中, 加入一系列50 mL 10 mg·L-1 DBP溶液, 分别在0.5、1、2、3、4、5、7 h时取样测定, 实验共设3个平行.
影响因素:取2.0 g供试土壤, pH范围设定为3~9, 环糊精浓度设定为0~5 g·L-1, 实验通过CaCl2溶液控制体系离子强度, 其浓度设定为0~5 g·L-1, 实验体积为50 mL, 25 ℃条件下振荡7 h, 实验共设3个平行.
2.3.2 解吸实验影响因素:取2.0 g制备老化的污染土壤, pH范围设定为3~9, 环糊精浓度设定为0~5 g·L-1, 实验通过CaCl2溶液控制体系离子强度, 其浓度设定为0~5 g·L-1, 实验体积为50 mL, 25 ℃条件下振荡7 h, 实验共设3个平行.
2.4 分析方法 2.4.1 前处理土壤:取实验后的土壤, 在超声环境下(每次10 min)用50 mL丙酮/正己烷(1:1, 体积比)分3次萃取, 合并萃取液; 取10 mL萃取液, 过硅胶/氧化铝(2:1)层析柱(净化柱为1 cm内径的层析柱), 采用正己烷湿法装柱, 从下至上依次为硅胶12 cm、氧化铝6 cm、无水硫酸钠2 cm, 用40 mL丙酮/正己烷(2:8, 体积比)淋洗出邻苯二甲酸酯; 收集全部洗脱液, 取10 mL洗脱液, 用氮吹仪浓缩至0.2 mL, 再加入正己烷进行溶剂置换, 定容至10 mL.
水样:将土壤悬浮液转移至玻璃离心管中, 以4000 r·min-1离心20 min, 取上清液25 mL至125 mL的分液漏斗中, 加入25 mL正己烷萃取, 剧烈振荡后, 静置分层, 取上清液过0.45 μm孔径有机相滤膜, 待HPLC测定.
2.4.2 DBP的测定高效液相色谱(HPLC)测定:色谱柱为Waters Acquity UPLC@BEHC18柱(sommx2.1 mm.1.7lain); 流动相为甲醇/水(75/25, 体积比), 流速为1.0 mL·min-1, 进样量为20 μL, 柱温为40 ℃, 保留时间为7.09 min, 检测波长为228 nm.DBP在0.5~10 mg·L-1浓度范围之间线性良好, 可决系数R2=0.9987.
环糊精测定:环糊精含量测定采用酚酞分光光度法(李文德等, 1995).
3 结果与讨论(Results and discussion) 3.1 等温吸附曲线土壤中有机物的吸附模型主要包括线性模型、Langmuir模型、Freundlich模型、Temkin模型等.本研究采用Langmuir模型(式(1))、Freundlich模型(式(2))、Temkin模型(式(3))3种模型对DBP在土壤中的吸附等温线进行定量描述(姜鲁等, 2016).
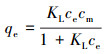
|
(1) |
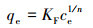
|
(2) |

|
(3) |
式中, qe为平衡吸附量(mg·kg-1); ce为平衡浓度(mg·L-1); cT、KL、n、KF、cm均为模型参数.
DBP在土壤中的吸附与土壤组分相关, 土壤矿物质、无定形有机质、紧密结合有机质的类别和含量均能对DBP在土壤中的吸附产生影响(Chen et al., 2017).由表 2可知, Freundlich方程能够较好地拟合实验组与对照组的吸附特性.模型参数1/n能反映吸附的非线性程度及吸附机理的差异, 1/n=1, 表示为线性分配等温线, 1/n < l, 为非线性等温线, 1/n值越小表示等温线的非线性越大(Li et al., 2019).根据Freundlich模型拟合结果, 两组实验中DBP的吸附接近线性吸附, 说明线性分配作用在吸附过程起到主导作用(Wang et al., 2015).此外, 一般认为常数KF表示吸附的程度与强弱, 其值越大, 表示DBP在土壤上吸附能力越强, 流动性越差(Kaur et al., 2018).拟合数据表明, 在添加HPCD后, 实验组KF值明显变小.由此可见, HPCD能削弱土壤吸附DBP的能力.这主要有以下几方面原因:在吸附时, 液相中的DBP被HPCD包裹, 游离的DBP浓度下降, 导致吸附减弱; HPCD具有疏水性及亲水性, 能将吸附在土壤表面的DBP包裹洗脱, 增强其在固液界面的流动性(Báez et al., 2017).
| 表 2 等温吸附拟合参数 Table 2 Fitting parameters of isothermal adsorption |
DBP与HPCD的包裹作用可以用紫外分析进行表征(图 1c), 实验中控制DBP及HPCD的浓度相同.HPCD在190~200 nm的远紫外吸收峰是由于环糊精中氧的n电子发生n→σ*的跃迁(苏克曼等, 2002); DBP在202 nm及210 nm的紫外吸收是苯环的特征吸收峰(主要是苯环结构的π→π*跃迁产生); 228 nm处的紫外吸收是生色基团(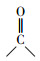
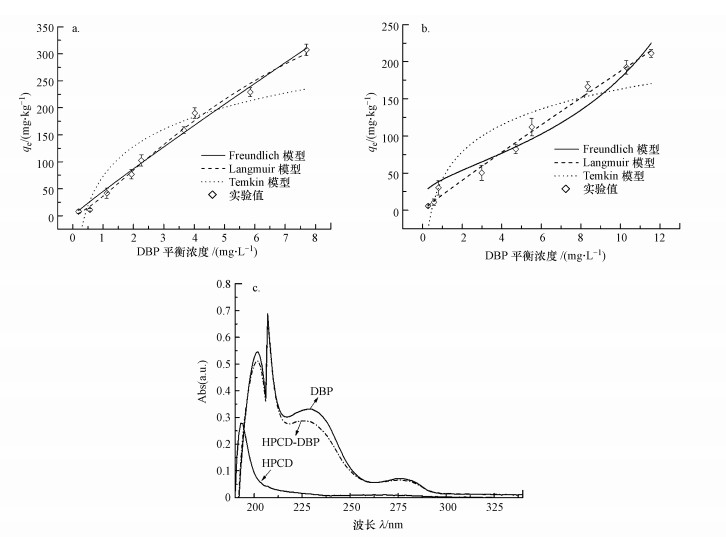 |
| 图 1 等温吸附拟合曲线(a.对照组, b.实验组, c.紫外吸收光谱) Fig. 1 Sorption isotherm(a.control group, b.experimental group, c.Ultraviolet absorption spectrum) |
吸附动力学主要探究土壤对污染物吸附与时间的关系, 这种关系与相对应状态下的吸附速率相关.吸附过程的控制包括质量转移、扩散控制、化学反应、微粒扩散, 而且因污染物与土壤性质的不同, 吸附动力学方程也有众多不同(Li et al., 2019).目前, 吸附概念认为土壤是一种多域吸附剂, 土壤中的吸附域决定了诸如线性吸附、吸附容量及吸附速率等吸附特征, 因此, 常采用多域吸附模型描述动力学(Griffiths, 2004).其中, 双室一级动力学模型考虑了吸附解吸过程, 同时依据土壤多域吸附机制, 认为土壤吸附分为特性不同的快吸附室和慢吸附室, 2个过程假定吸附反应符合一级动力学; 其与多域吸附理论及其他简单吸附理论具有较好的一致性, 是一种常见的描述土壤对有机物吸附动力学的模型(姜鲁等, 2012).相对应的单室模型是简单假设土壤的性质均一对吸附进行讨论.吸附动力学单室模型和双室模型描述的土壤吸附浓度与时间的关系如下所示(Griffiths, 2004):
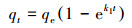
|
(4) |

|
(5) |
式中, qt为反应时间t时DBP的土壤吸附量(mg·kg-1), qe代表DBP的土壤平衡吸附量(mg·kg-1), t和k分别为吸附时间(min)和吸附速率常数(min-1), k1和k2分别代表快、慢吸附室的速率常数, f1和f2分别代表快、慢吸附室的贡献率.
在HPCD存在时及对照组条件下, 土壤样品对DBP的吸附动力学数据及其单室、双室一级动力学模型拟合结果如图 2所示, 模型拟合参数列于表 3.
 |
| 图 2 吸附动力学拟合曲线(a.对照组, b.实验组) Fig. 2 Adsorption kinetics fitting curve(a.control group, b.experimental group) |
| 表 3 动力学拟合参数 Table 3 Kinetic fitting parameters |
由图 2和表 3的结果可知, 双室模型对于DBP动态吸附数据的拟合效果明显优于单室模型(双室模型拟合得到的R2大于单室模型), 说明土壤有机质多域吸附机制适于描述DBP在受试土壤中的吸附过程, 双室一级动力学模型比单室一级动力学模型能够更准确地描述DBP在受试土壤中的吸附过程.
从图 2可以看出, 两组实验在7 h内逐渐达到吸附平衡.对照组在168 mg·kg-1左右达到平衡, 实验组在136 mg·kg-1左右达到平衡.单室模型拟合表明, 在加入HPCD后, 土壤对DBP的吸附速率减慢, 其吸附速率常数由2.2138 h-1衰减至1.9249 h-1.双室拟合数据显示, 快、慢吸附室的速率相差巨大, 在未加入HPCD时, 相差约7个数量级, 加入HPCD之后仍然相差3个数量级.同时, 实验组的快室吸附速率常数较对照组减少4个数量级, 慢室吸附速率常数小幅增加, 这种变化强度与姜鲁等(2012)的研究一致.分析快慢室吸附的贡献率发现, 在吸附反应初始阶段, 快吸附室的贡献占据主导地位, 此后, 慢吸附室的贡献逐渐增大, 快吸附室相对贡献逐渐减小, 直至达到吸附平衡后, 两者比例保持稳定.总体而言, 快室吸附贡献占主要地位, 慢室吸附速率的小幅增加不足以对整个吸附过程造成决定性影响.
3.3 环糊精作用下土壤对DBP吸附解吸影响因素HPCD作用下影响有机物在土壤中吸附的因素主要有两方面:HPCD、土壤与有机物三者的理化特性及外部环境.本文主要通过控制变量法消除部分理化性质的影响, 探究HPCD浓度、pH、离子强度对HPCD作用下DBP在固液相吸附解吸的影响.
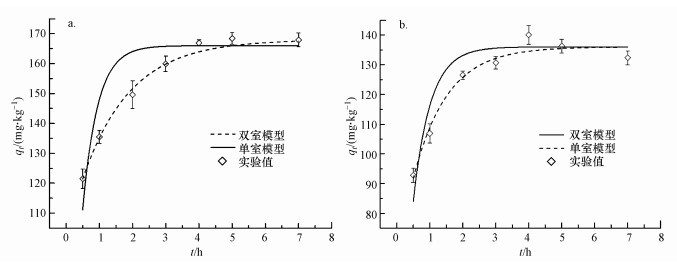
3.3.1 环糊精浓度的影响保持土壤与水的固液比为1/25(g·mL-1, 下同), 不同HPCD浓度下土壤对DBP的吸附性能及污染土壤DBP的释放量如图 3所示.
 |
| 图 3 不同HPCD浓度对吸附(a)、解吸(b)的影响 Fig. 3 Effect of HPCD concentration on adsorption(a) and desorption(b) |
由图 3a可知, HPCD初始浓度对DBP吸附的影响是显著的.在HPCD浓度为0~2.5 g·L-1时, 随着HPCD浓度的增大, 土壤对DBP的吸附明显减弱, 吸附量从162 mg·kg-1减少至72 mg·kg-1.当HPCD浓度大于2.5 g·L-1时, DBP的吸附趋于稳定, 维持在60~70 mg·kg-1.对制备的污染土壤的研究表明, HPCD浓度与DBP的释放明显相关, 在HPCD浓度为0~2 g·L-1时, 土壤的DBP释放量急剧增加; 当HPCD浓度大于2 g·L-1, 土壤的DBP释放量逐渐缓和直至稳定, 这种趋于平缓的趋势与王光辉等(2016)研究的天冬氨酸-β-环糊精对芴在土壤中分配情况的结果相似.分析体系的反应过程, 可以通过数学模型解释这种趋势.方程(13)表明, DBP初始浓度一定时, 土壤对DBP的吸附量与HPCD浓度成反比.显然, 表达式存在数学极限, 这就解释了DBP吸附量后期随HPCD浓度上升趋于平缓的原因.总体而言, DBP吸附量随HPCD浓度的变化规律与HPCD和DBP的包合作用(式(6))及水土体系的分配作用(式(7))有关.

|
(6) |

|
(7) |
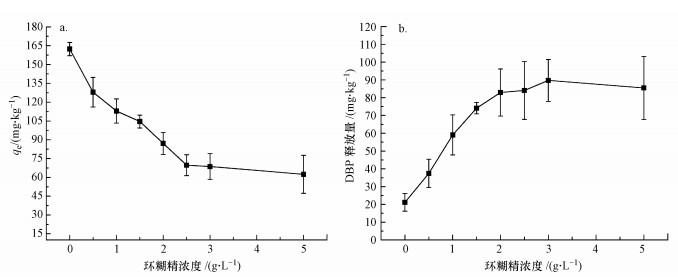
根据经典化学原理可得平衡常数K(式(8)), DBP在水土中的分配系数Kd如式(9)所示.
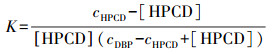
|
(8) |
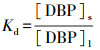
|
(9) |
式中, cHPCD表示HPCD的初始浓度; [HPCD]表示HPCD的平衡浓度; cDBP表示DBP的初始浓度; [DBP]s表示土壤中DBP的平衡浓度; [DBP]l表示水相中DBP的平衡浓度.
图 4所示为土壤吸附HPCD时HPCD浓度与时间的变化关系.数据表明, 土壤对HPCD的吸附可以忽略.因此, 可建立如式(10)、(11)所示的质量守恒方程(其中, [DBP-HPCD]表示DBP与HPCD包合物浓度).显然, 对于土壤吸附量qe可简化为式(12).
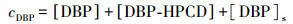
|
(10) |
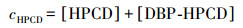
|
(11) |
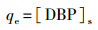
|
(12) |
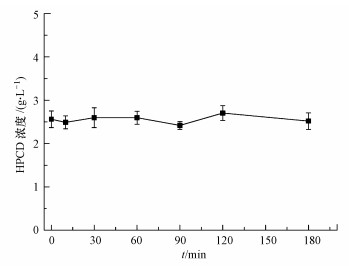 |
| 图 4 HPCD在土壤上的吸附 Fig. 4 Adsorption of HPCD on soil |
联立方程(8)~(12)得到的吸附量如下所示:
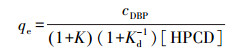
|
(13) |
保持固液比为1:25, 环糊精浓度为2.5 g·L-1, 不同pH下土壤对DBP的吸附性能及污染土壤DBP的释放量如图 5所示.本研究发现, DBP在酸性介质中更易被吸附, pH值降低有效地增强了土壤对DBP的吸附能力, 而随着pH值的升高吸附作用逐渐减弱, 这与前人的研究结果一致(王继芳等, 2016).在加入HPCD后, 这种随pH变化的趋势没有改变; 仅在土壤对DBP的吸附量上, 吸附量从148.23~179.98 mg·kg-1降低至118.74~155.26 mg·kg-1.同时, 对制备的污染土壤的解吸实验表明, 碱性条件有利于DBP的释放, 在加入HPCD后, DBP释放规律保持不变, DBP释放量从11.45~20.36 mg·kg-1增加至12.37~90.89 mg·kg-1.此外, 在pH=6.5~9时, 解吸释放量逐渐趋缓.吸附实验及解吸实验的变化趋势说明HPCD不会改变pH对土壤吸附DBP的作用的影响, 吸附量及释放量的变化主要归功于HPCD对DBP的包合作用.
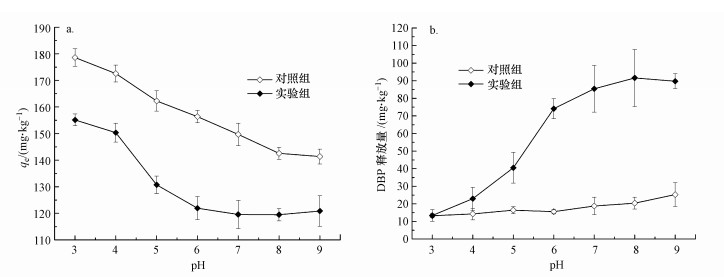 |
| 图 5 pH对吸附(a)、解吸(b)的影响 Fig. 5 Effect of pH on adsorption(a) and desorption(b) |
土壤的酸碱性改变了污染物和土壤的带电特征, 并改变了有机物与土壤间的作用过程, 引起了土壤中有机物含量及迁移性能的变化.而HPCD是一种中性物质, 其加入并不会引起土壤表面电荷的剧烈变化.因此, 在利用HPCD洗脱土壤中的DBP时应尽量控制在pH=6.5~8.0, 这与自然条件下的土壤pH值接近.
3.3.3 离子强度的影响保持固液比为1:25, 环糊精浓度为2.5 g·L-1, 不同离子强度下土壤对DBP的吸附性能及污染土壤DBP的释放量如图 6所示.吸附研究表明, 随着离子强度的增加, 土壤对DBP的吸附作用增强, 其吸附量从201.27 mg·kg-1增至221.78 mg·kg-1.对制备的污染土壤的解吸实验表明, 离子强度的增加不利于污染土壤中DBP的释放, 其释放量从18.16 mg·kg-1减少至10.92 mg·kg-1.产生这种现象的原因可能包括以下几个方面:①支持电解质压缩了土壤胶体双电层, 从而使土壤胶体的厚度发生变化; ②电解质与DBP分子竞争土壤中的吸附位点, 削弱了土壤对淋溶液中DBP分子的吸附作用; ③电解质与土壤胶体之间通过离子缔合作用形成离子对, 降低了土壤胶体的有效浓度, 造成吸附DBP作用的减弱, 吸附量减少; ④电解质破坏了表面的静电平衡, 削弱了土壤颗粒与DBP分子之间的静电作用力(吴志坚等, 2010).此外, 离子强度的影响趋势还有助于分析吸附过程是专性吸附还是非专性吸附.一般认为, 依靠土壤表层的基团与吸附质结合形成络合基团的吸附过程是专性吸附; 如果吸附量受离子强度影响较小或与离子强度正相关, 则吸附可认为是专性吸附; 非专性吸附是靠吸附剂表面的物理作用力, 一般随离子强度的增大吸附量减小(王强等, 2016).因而根据离子强度对土壤吸附DBP的情况分析, 实验土壤对DBP的吸附主要是专性吸附作用.
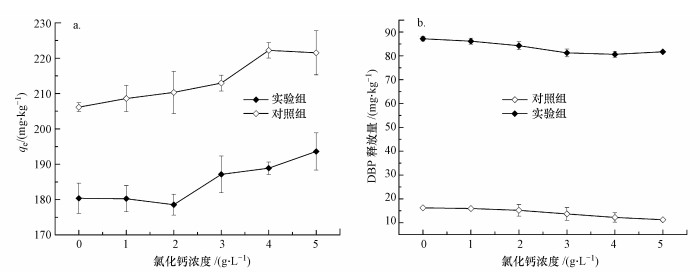 |
| 图 6 离子强度对吸附(a)、解吸(b)的影响 Fig. 6 Effect of ionic strength on adsorption(a) and desorption(b) |
在环糊精存在时, DBP的吸附量及释放量均保持相同规律.吸附量从181.14 mg·kg-1增加至189.95 mg·kg-1, 与对照组相比, 吸附量呈下降的趋势.释放量从91.25 mg·kg-1下降至80.23 mg·kg-1, 与对照组相比, 释放量呈上升的趋势.这说明环糊精不会对土壤与电解质之间的相互作用造成影响.电解质对环糊精与土壤介质中DBP的这种包合作用影响不大.在加入环糊精后, 这种吸附特性没有发生变化.两组吸附实验及解吸实验的变化趋势说明环糊精不会改变离子强度对土壤吸附DBP的作用的影响, 吸附量及释放量的变化主要归功于环糊精对DBP的包合作用.
4 结论(Conclusions)1) DBP在供试土壤中的吸附可以用Freundlich模型描述, 动力学研究表明其吸附过程更符合双室一级动力学模型; HPCD能削弱土壤吸附DBP的能力, 使等温吸附常数KF减小, 吸附动力学常数K1成数量级变化.
2) 土壤对DBP的吸附量随HPCD浓度的增大先减小后趋于平缓; 导出公式表明这与HPCD、DBP的包合作用及DBP在水土体系的分配作用有关.综合经济成本考虑淋洗土壤中的DBP时, HPCD的浓度选择为2.5 g·L-1.
3) 随着pH的增大, 吸附、解吸均趋于平缓, 表明在自然土壤pH范围内HPCD的解吸能力不受pH影响.离子强度增大可促进DBP的吸附而削弱DBP的解吸, 说明土壤对DBP吸附属于专性吸附.
Báez M E, Espinoza J, Silva R, et al. 2017. Influence of selected cyclodextrins in sorption-desorption of chlorpyrifos, chlorothalonil, diazinon, and their main degradation products on different soils[J]. Environmental Science and Pollution Research, 24(26): 20908–20921.
DOI:10.1007/s11356-017-9652-7
|
Chang B V, Wang T H, Yuan S Y. 2007. Biodegradation of four phthalate esters in sludge[J]. Chemosphere, 69(7): 1116–1123.
DOI:10.1016/j.chemosphere.2007.04.011
|
Chen K, Liu L, Chen W. 2017. Adsorption of sulfamethoxazole and sulfapyridine antibiotics in high organic content soils[J]. Environmental Pollution, 231: 1163–1171.
DOI:10.1016/j.envpol.2017.08.011
|
Cheng Z, Gao B, Xu H, et al. 2016. Effects of surface active agents on DNAPL migration and distribution in saturated porous media[J]. Science of the Total Environment, 571: 1147–1154.
DOI:10.1016/j.scitotenv.2016.07.109
|
程洪珍, 葛蔚, 史衍玺, 等. 2014. 表面活性剂淋滤对土壤中邻苯二甲酸酯纵向迁移的影响[J]. 环境工程学报, 2014, 8(8): 3495–3504.
|
Flaherty R J, Nshime B, Delamarre M, et al. 2013. Cyclodextrins as complexation and extraction agents for pesticides from contaminated soil[J]. Chemosphere, 91(7): 912–920.
DOI:10.1016/j.chemosphere.2013.02.005
|
Griffiths R A. 2004. Sorption and desorption by ideal two-compartment systems:unusual behavior and data interpretation problems[J]. Chemosphere, 55(3): 443–454.
DOI:10.1016/j.chemosphere.2003.07.009
|
姜鲁, 王继华, 李建忠, 等. 2012. 炔雌醇和壬基酚在土壤中的吸附-解吸特征[J]. 环境科学, 2012, 33(11): 3885–3892.
|
Kaur P, Makkar A, Kaur P, et al. 2018. Temperature dependent adsorption-desorption behaviour of pendimethalin in punjab soils[J]. Bulletin of Environmental Contamination and Toxicology, 100(1): 167–175.
|
Li F, Fang X, Zhou Z, et al. 2019. Adsorption of perfluorinated acids onto soils:Kinetics, isotherms, and influences of soil properties[J]. Science of the Total Environment, 649: 504–514.
DOI:10.1016/j.scitotenv.2018.08.209
|
Li R, Liang J, Gong Z, et al. 2017. Occurrence, spatial distribution, historical trend and ecological risk of phthalate esters in the Jiulong River, Southeast China[J]. The Science of the Total Environment, 580: 388–397.
DOI:10.1016/j.scitotenv.2016.11.190
|
梁婧, 欧延, 弓振斌. 2014. 环境中的邻苯二甲酸酯[J]. 科技导报, 2014, 2(32): 73–79.
|
刘庆, 杨红军, 史衍玺, 等. 2012. 环境中邻苯二甲酸酯类(PAEs)污染物研究进展[J]. 中国生态农业学报, 2012, 20(8): 968–975.
|
Rafin C, Veignie E, Fayeulle A, et al. 2009. Benzo[a]pyrene degradation using simultaneously combined chemical oxidation, biotreatment with Fusarium solani and cyclodextrins[J]. Bioresource Technology, 100(12): 3157–3160.
DOI:10.1016/j.biortech.2009.01.012
|
宋广宇, 代静玉, 胡峰. 2010. 邻苯二甲酸酯在不同类型土壤一植物系统中的累积特征研究[J]. 农业环境科学学报, 2010, 29(8): 1502–1508.
|
苏克曼, 潘铁英, 张玉英. 2002. 波谱解析法[M]. 上海: 华东理工大学出版社.
|
Trellu C, Mousset E, Pechaud Y, et al. 2016. Removal of hydrophobic organic pollutants from soil washing/flushing solutions:A critical review[J]. Journal of Hazardous Materials, 306: 149–174.
DOI:10.1016/j.jhazmat.2015.12.008
|
Wang G, Wang Y, Hu S, et al. 2015. Cysteine-β-cyclodextrin enhanced phytoremediation of soil co-contaminated with phenanthrene and lead[J]. Environmental Science and Pollution Research, 22(13): 10107–10115.
DOI:10.1007/s11356-015-4210-7
|
Wang L, Li Y, Al Y D E. 2016. In-situ leaching-immobilization of lead in soil-vegetable system based on coupling of remediation & production[J]. Agricultural Science & Technology, 17(9): 2074–2077.
|
王光辉, 徐兰, 胡苏杭, 等. 2016. 天冬氨酸-p-环糊精对土壤中芴和镉的分配行为研究[J]. 环境污染与防治, 2016, 38(7): 56–60.
|
王继芳, 葛蔚, 程洪珍, 等. 2016. 土壤酸碱性和有机质含量对邻苯二甲酸酯纵向迁移的影响[J]. 青岛农业大学学报(自然科学版), 2016, 33(4): 275–281.
DOI:10.3969/J.ISSN.1674-148X.2016.04.008 |
王强, 宋娇艳, 曾微, 等. 2016. 紫色土对邻苯二甲酸二甲酯的淋溶吸持特征及影响因素[J]. 环境科学, 2016, 37(2): 726–733.
|
吴志坚, 刘海宁, 张慧芳. 2010. 离子强度对吸附影响机理的研究进展[J]. 环境化学, 2010, 29(6): 997–1003.
|
张海光, 孙国帅, 孙磊, 等. 2013. 典型覆膜作物土壤中邻苯二甲酸酯污染的初步研究[J]. 中国环境监测, 2013, 29(4): 60–63.
DOI:10.3969/j.issn.1002-6002.2013.04.013 |
张蕴晖, 林玲, 阚海东, 等. 2007. 邻苯二甲酸二丁酯的人群综合暴露评估[J]. 中国环境科学, 2007, 27(5): 651–656.
DOI:10.3321/j.issn:1000-6923.2007.05.017 |
朱明华, 胡坪. 2007. 仪器分析(第四版)[M]. 北京: 高等教育出版社.
|
 2019, Vol. 39
2019, Vol. 39


