药物是环境中一类新型污染物, 据报道, 50%以上的药物具有手性对映体特性(Agranat et al., 2012; Ribeiro et al., 2014).手性药物单体虽然具有相同的物理化学属性, 但在环境中却表现出不同的生物代谢作用、生物毒性和对映体选择性降解途径(Liu et al., 2011; Kasprzykhordern et al., 2010; Kasprzyk-Hordern, 2011).因此, 环境介质中药物手性特征及行为已引起了越来越高的关注(Bagnall et al., 2012; Evans et al., 2015; Ma et al., 2016a; 2016b), 然而手性药物的分离分析成为其环境行为及效应研究的制约因素.扑尔敏是H型受体阻断剂, 抗变态反应作用强, 是优良的抗组胺类药物, 已被广泛应用于过敏及上呼吸道感染等疾病的治疗中.研究表明, 扑尔敏右旋体的药理活性是消旋体的2倍(王世玉, 1998).因此, 建立扑尔敏对映体手性拆分方法, 对环境中该药物的环境行为、生物毒性及风险评价研究具有重要意义.
1994年Armstrong等首次以万古霉素为手性选择剂成功拆分了多种手性药物和氨基酸(Armstrong et al., 1994).万古霉素是具有“篮状”结构、18个立体选择中心的糖肽大环抗生素类手性选择剂, 其结构中的氨基、酚基和羧基可作为氢键和静电作用的活性点位, 在手性识别中起到重要作用(Gasper et al., 1996; Mojtahedi et al., 2007).万古霉素作为流动相添加剂和固定相填料已被证明能有效分离多种酸性和碱性药物对映体, 并且在正相、反相和极性有机相模式下都有应用(Svensson et al., 2000; Bosáková et al., 2005).据报道, 扑尔敏对映体的拆分方法主要有:环糊精类手性固定相的高效液相色谱(HPLC)法(Shen et al., 2011)、以环糊精为手性添加剂的毛细管电泳法(CE)(Sun et al., 2015)和以环糊精类为流动相添加剂的HPLC法(程燕等, 2012).目前, 尚未见到以万古霉素手性固定相拆分马来酸扑尔敏对映体的文献报道.因此, 本文利用万古霉素手性柱和四氢呋喃(THF)-冰醋酸+三乙胺缓冲水溶液(TEAA)流动相体系拆分马来酸扑尔敏对映体, 考察流动相比例、pH值、流速和温度等条件对分离效果的影响, 并利用分子对接技术初步探究其手性识别机理.以期为手性药物马来酸扑尔敏对映体在环境介质中的迁移转化规律研究提供基础数据和必要手段.2材料与方法(Materials and methods)
2.1 仪器与试剂对映体分离在高效液相色谱仪(HPLC, Agilent 1260)-紫外检测器系统上进行, 流动相经0.22 μm尼龙滤膜(CNW, GER)过滤.R型和S型马来酸扑尔敏分别购自TLC Pharmaceutical Standards Ltd(Canada)和Toronto Research Chemicals Inc.(Canada), 纯度为99.0%, 其结构式见图 1a.四氢呋喃(THF)为色谱纯(MREDA, USA), 三乙胺和冰醋酸为分析纯(国药集团药业股份有限公司), TEAA缓冲溶液为含有0.1%冰醋酸和0.1%三乙胺的水溶液.
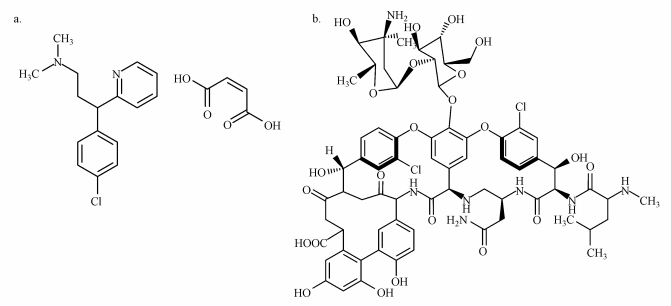 |
| 图 1 马来酸扑尔敏(a)与万古霉素(b)结构式 Fig. 1 Structure of chlorphenamine maleate (a) and vancomycin (b) |
分别取S-马来酸扑尔敏与R-马来酸扑尔敏适量, 溶于甲醇中, 配制10 mg·L-1对映体单体标准储备溶液, 在4 ℃下储存, 使用前配制成1 mg·L-1的单体和外消旋体供试溶液.
2.3 色谱条件色谱柱为Astec Chirobiotic® V(15 cm×2.1 mm, 5 μm, Sigma-Aldrich), 填料为万古霉素, 其结构式见图 1b.流动相比例范围(TEAA:THF, 体积比)为95:5~80:20, 控制pH为3~5, 流动相流速为0.1~0.4 mL·min-1, 柱温度控制在5~25 ℃, 进样体积为5 μL, 检测波长为214 nm.
选择性因子(α)和对映体分离度(Rs)是衡量分离效果的关键参数, 其中, 对映体分离度利用公式(1)计算.
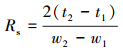
|
(1) |
式中, t1、t2分别表示第1个和第2个流出对映体的出峰时间, w1、w2分别表示第1个和第2个流出对映体的峰宽.
2.4 分子对接方法本文应用Autodock 4.0程序模拟配体和受体的相互作用.在模拟计算过程中, 采用拉马克-遗传算法搜索配体与受体结合构象, 基于半经验自由能的方法评价配体与受体之间的能量匹配.半经验结合自由能公式(Morris et al., 2015)如下:
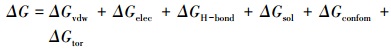
|
(2) |
自由能计算包括了短距离范德华力(ΔGvdw)、静电作用(ΔGelec)、氢键作用(ΔGH-bond)、去溶剂化作用(ΔGsol)、背离实际键长和键角偏差(ΔGconfom)、内部转动、全局转动和平动的限制(ΔGtor).最稳定结合能(ΔG)越小, 则物质间相互作用能越高, 结合越稳定.
扑尔敏对映体分子结构来自Pubchem数据库(https://pubchem.ncbi.nlm.nih.gov/), 万古霉素分子结构来自RCSB Protein Data Bank数据库(www.rcsb.org).利用Autodock 4.0软件对万古霉素大分子及扑尔敏对映体进行预处理, 除去万古霉素结构水分子及配体分子, 添加氢原子, 并利用Gasteiger-Marsili方法计算表面电荷(Osterberg et al., 2002).
万古霉素大分子存在两个空间区域的作用位点(胡昌勤等, 2009), 分别以万古霉素两个区域的活性位点为格点中心, 格点盒子设置为40×40×40点(格点间距为0.375 nm), 其他参数为程序默认值, 个体数量为150, 利用拉马克遗传算法进行10次独立对接得到10个构象, 最终根据结合自由能寻找到配体与受体能量最低的结合状态.
3 结果与讨论(Results and discussion) 3.1 流速对分离效果的影响在流动相比例TEAA:THF=90:10、pH=3.5和柱温15 ℃的条件下, 改变流动相流速, 考察其对分离度与选择性因子的影响.如图 2所示, 随着流速增大, 选择性因子基本不变, 分离度明显下降.van Deemter方程描述了塔板高度与流动相流速的关系(Knox et al., 1983; AlHarthy, 2009):
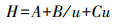
|
(3) |
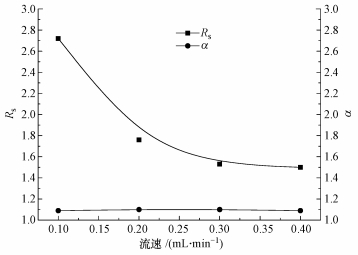 |
| 图 2 流动相流速对马来酸扑尔敏对映体分离度(Rs)与选择性因子(α)的影响 Fig. 2 Effect of flow rate on resolution(Rs) and selectivity factor (α) of chlorphenamine maleate |
式中, H为理论塔板高度, u为流动相线速度, A为涡流扩散项, B/u为分子扩散项, Cu为传质阻力项.由于在高效液相色谱中, 液体扩散系数远小于气体, 因此, 公式(3)中纵向分子扩散项(B/u)对峰展宽的影响很小, 可忽略不计.从而可以得出, 对于同一色谱柱来说, 理论塔板高度随流动相流速的降低而降低, 低流速下具有更高的理论塔板数; 另外, 在低流速下待分析物与固定相作用时间更长, 从而手性对映体具有更高的分离度(胡曼玲, 2003).本研究中, 在流速为0.3 mL·min-1时, 扑尔敏对映体可达到基线分离(Rs=1.53), 因此, 为缩短色谱分离时间, 确定最优流速为0.3 mL·min-1.
3.2 柱温对分离效果的影响有研究表明, 万古霉素在低于37 ℃下稳定(Raverdy et al., 2013), 因此, 设定柱温范围为5~25 ℃.在流动相比例TEAA:THF=90:10、pH=3.5和流速为0.3 mL·min-1的条件下, 扑尔敏对映体的分离度及选择性因子随柱温的变化如图 3所示.结果表明, 分离度和选择性因子都随柱温的升高先增大后减小, 由此可推测扑尔敏与万古霉素固定相形成的络合物在15 ℃下较为稳定, 最佳柱温为15 ℃.
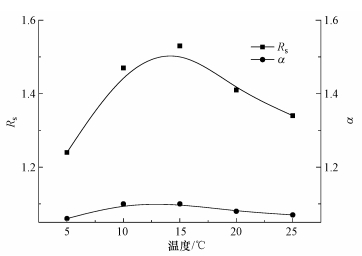 |
| 图 3 柱温对马来酸扑尔敏对映体分离度(Rs)与选择性因子(α)的影响 Fig. 3 Effect of column temperature on resolution (Rs) and selectivity factor (α) of chlorphenamine maleate |
由于万古霉素手性柱适用pH值范围为3~7, 因此, 在流动相比例TEAA:THF=90:10、流速0.3 mL·min-1和柱温为15 ℃条件下, 利用冰醋酸调节TEAA溶液pH值范围为3~5, 考察pH值对分离的影响.如图 4所示, 当pH值为3时, 扑尔敏对映体具有最大的分离度(1.67), 随着pH值的增大, 分离度逐渐减小.另外, 选择性因子随着pH值的增大略有降低, 如从pH=3时的1.10降低到pH=5时的1.02.造成此结果的主要原因在于:一方面, 马来酸扑尔敏在含水溶液的流动相中电离为马来酸根和扑尔敏, 根据马来酸的电离常数(pKa1=1.92, pKa2=6.23), 当流动相pH值在3~5之间时, 马来酸扑尔敏以马来酸根和质子化的扑尔敏形态存在, 二者可达到色谱分离; 另一方面, pH减小可促使万古霉素质子化, 从而有利于使药物对映体与万古霉素固定相形成氢键作用, 从而提高对扑尔敏对映体的分离性能.
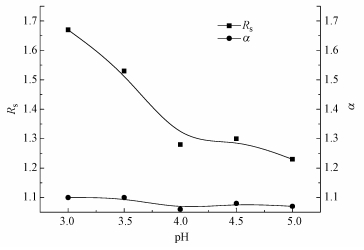 |
| 图 4 流动相pH值对马来酸扑尔敏对映体分离度(Rs)与选择性因子(α)的影响 Fig. 4 Effect of pH value on resolution (Rs) and selectivity factor (α) of chlorphenamine maleate |
万古霉素固定相在反相模式下进行手性分离时, 通常以有机相与水相的复合体系为流动相, 并采用冰乙酸和三乙胺作为流动相添加剂以改善峰形、提高分离度(丁国生等, 2004; Zhang et al., 2015).本研究在流动相流速为0.3 mL·min-1、柱温为15 ℃、流动相pH值为3.5时, 以不同比例的TEAA:THF为流动相, 探究扑尔敏对映体的分离效果.分离度和选择性因子随流动相比例的变化如图 5所示, 随着THF含量的增加, 由于扑尔敏对映体的保留时间缩短, 分离度明显降低, 选择性因子也有所减小.THF作为质子受体可与万古霉素中的氨基形成氢键, 因此, THF的存在减弱了扑尔敏与万古霉素固定相的氢键作用力.由图 5可知, 当流动相比例为TEAA:THF=95:5时, 其分离度和选择性因子分别为2.46和1.15, 并且对映体出峰时间小于20 min, 分析时间较短.因此, 选择流动相比例TEAA:THF=95:5为最优色谱条件.
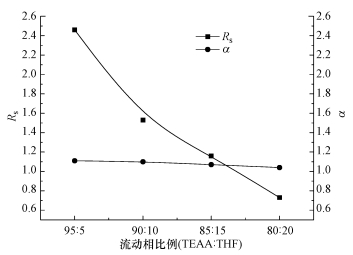 |
| 图 5 流动相比例(TEAA:THF)对马来酸扑尔敏对映体分离度(Rs)与选择性因子(α)的影响 Fig. 5 Effect of moblie phase proportion (TEAA:THF) on resolution (Rs) and selectivity factor (α) of chlorphenamine maleate |
通过上述色谱条件的优化, 本研究选择的条件为:流动相比例95:5, 流速0.3 mL·min-1, pH=3, 柱温15 ℃.在优化色谱条件下, 连续进样6次, S-和R-马来酸扑尔敏对映体出峰时间的相对标准偏差(RSD)分别为0.45%和0.47%, 峰面积的RSD分别为0.52%和0.55%, 其分离度为2.2, 选择性因子为1.13.由色谱图(图 6)可知, 在20 min内, 马来酸扑尔敏对映体达到完全分离, 并且S-扑尔敏先于R-扑尔敏流出.结果表明, 该方法重现性和分离效果较好, 可用于扑尔敏对映体的手性分离.
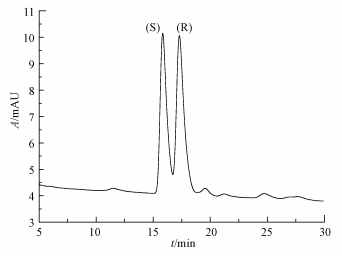 |
| 图 6 马来酸扑尔敏分离谱图(色谱条件:流动相TEAA:THF=95:5, pH=3, 柱温15 ℃, 流速0.3 mL·min-1) Fig. 6 Chromatogram of chlorphenamine maleate on the vancomycin CSP |
利用Autodock 4.0半柔性配体与大分子受体对接技术, 获得小分子配体的多种构象, 采用拉马克遗传算法和半经验自由能计算方法寻找受体与配体最稳定结合构象.由计算得到的扑尔敏对映体在万古霉素两个空间区域结合的最稳定结合能(ΔG)和最稳定结合能差(ΔΔG)如表 1所示.由表 1可见, S-扑尔敏与R-扑尔敏的最稳定结合能均为负值, 表明扑尔敏与万古霉素形成的络合物在热力学上是稳定的; 扑尔敏对映体在DomainⅠ的结合能均小于在DomainⅡ的结合能, 意味着在DomainⅠ的结合更稳定.另外, 由表 1中最稳定结合能差可知, R-扑尔敏与S-扑尔敏在DomainⅠ的最稳定结合能差为-0.25 kcal·mol-1, 说明R-型对映体与万古霉素结合较S-型更稳定, 由此推测S-型对映体先于R-型对映体流出, 该预测结果与实验出峰顺序是一致的, 由此可知, 万古霉素DomainⅠ是拆分扑尔敏对映体的手性识别位点.扑尔敏对映体在万古霉素DomainⅠ的分子对接构象见图 7, 由于R-扑尔敏与万古霉素之间有氢键作用(绿色虚线), 而S-构型没有氢键作用, 因此可推测出氢键是万古霉素对扑尔敏手性识别的关键作用.
| 表 1 万古霉素与扑尔敏对映体的最稳定结合能(ΔG)与结合能差(ΔΔG) Table 1 Most steady combination energy (ΔG) and combination energy difference (ΔΔG) of vancomycin interaction with chlorphenamine enantiomers |
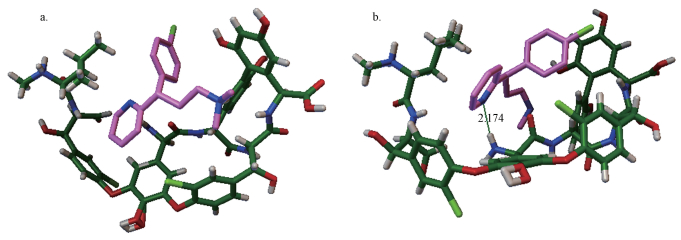 |
| 图 7 扑尔敏对映体与万古霉素分子对接构象图 (a.S-(+)-扑尔敏对接构象, b.R-(-)-扑尔敏对接构象, 绿色虚线表示氢键) Fig. 7 Molecular docking configurations between chlorphenamine and vancomycin |
本研究首次应用万古霉素色谱柱在反相条件下成功分离了马来酸扑尔敏对映体.流动相组成比例TEAA:THF=95:5、pH=3、柱温15 ℃为最优分离色谱条件; 流动相流速越低, 分离效果越好.分子对接结果表明, R-型扑尔敏与万古霉素结合较S型更稳定, 该结果与实验得到的对映体出峰顺序是一致的.根据分子对接构型图推测, 氢键是扑尔敏手性识别中关键的作用因素.本研究采用的方法重现性好, 操作简便快速, 扩展了此类固定相的应用范围, 可为进一步研究此种药物的环境行为及环境效应提供方法和数据支撑.
Agranat I, Wainschtein S R, Zusman E Z. 2012. The predicated demise of racemic new molecular entities is an exaggeration[J]. Nature Reviews Drug Discovery, 11(12): 972–973.
DOI:10.1038/nrd3657-c1
|
AlHarthy F.2009.Separation of aryl nitro-compounds by HPLC on monolithic columns[D].Loughborough: Loughborough University.32-34
|
Armstrong D W, Tang Y, Chen S, et al. 1994. Macrocyclic antibiotics as a new class of chiral selectors for liquid chromatography[J]. Analytical Chemistry, 66(9): 1473–1484.
DOI:10.1021/ac00081a019
|
Bagnall J P, Evans S E, Wort M T, et al. 2012. Using chiral liquid chromatography quadrupole time-of-flight mass spectrometry for the analysis of pharmaceuticals and illicit drugs in surface and wastewater at the enantiomeric level[J]. Journal of Chromatography A, 1249(15): 115–129.
|
Bosáková Z, Curínová E, Tesarová E. 2005. Comparison of vancomycin-based stationary phases with different chiral selector coverage for enantioselective separation of selected drugs in high-performance liquid chromatography[J]. Journal of Chromatography A, 1088(1): 94–103.
|
程燕, 贾欣欣, 刘健艺, 等. 2012. 以CM-β-CD为HPLC手性流动相添加剂分离扑尔敏等6种手性药物对映体[J]. 沈阳药科大学学报, 2012, 29(2): 121–125.
|
丁国生, 刘莺, 丛润滋, 等. 2004. 去甲万古霉素键合手性固定相拆分β-受体阻滞剂类药物及其结构类似物的研究[J]. 色谱, 2004, 22(4): 386–389.
DOI:10.3321/j.issn:1000-8713.2004.04.024 |
Evans S E, Davies P, Lubben A, et al. 2015. Determination of chiral pharmaceuticals and illicit drugs in wastewater and sludge using microwave assisted extraction, solid-phase extraction and chiral liquid chromatography coupled with tandem mass spectrometry[J]. Analytica Chimica Acta, 882(30): 112–126.
|
Gasper M P, Berthod A, Nair U B, et al. 1996. Comparison and modeling study of vancomycin, ristocetin A, and teicoplanin for CE enantioseparations[J]. Analytical Chemistry, 68(15): 2501–2514.
DOI:10.1021/ac960154q
|
胡昌勤, 洪建文. 2009. 毛细管电泳中万古霉素拆分氧氟沙星对映体手性识别位点的探讨[J]. 药学学报, 2009, 44(8): 905–910.
DOI:10.3321/j.issn:0513-4870.2009.08.014 |
胡曼玲. 2003. 卫生化学(第5版)[M]. 北京: 人民卫生出版社: 56–59.
|
Kasprzyk-Hordern B. 2011. ChemInform abstract:Pharmacologically active compounds in the environment and their chirality[J]. Cheminform, 42(8): 4466–4503.
|
Kasprzykhordern B, Kondakal V V, Baker D R. 2010. Enantiomeric analysis of drugs of abuse in wastewater by chiral liquid chromatography coupled with tandem mass spectrometry[J]. Journal of Chromatography A, 1217(27): 4575–4586.
DOI:10.1016/j.chroma.2010.04.073
|
Knox J H, Scott H P. 1983. B and C terms in the Van Deemter equation for liquid chromatography[J]. Journal of Chromatography A, 282(DEC): 297–313.
|
Liu Y, Gu X H.2011.Pharmacology of Chiral Drugs//Lin G Q, You Q D, Cheng J F.Chiral Drugs: Chemistry and Biological Action[M].Hoboken: John Wiley & Sons, Inc.323-345
|
Ma R, Wang B, Lu S, et al. 2016a. Characterization of pharmaceutically active compounds in Dongting Lake, China:Occurrence, chiral profiling and environmental risk[J]. Science of the Total Environment, 557-558: 268–275.
DOI:10.1016/j.scitotenv.2016.03.053
|
Ma R, Wang B, Yin L, et al. 2016b. Characterization of pharmaceutically active compounds in Beijing, China:Occurrence pattern, spatiotemporal distribution and its environmental implication[J]. Journal of Hazardous Materials, 323(Pt A): 147–155.
|
Mojtahedi M M, Chalavi S, Ghassempour A, et al. 2007. Chiral separation of three agrochemical toxins enantiomers by high-performance liquid chromatography on a vancomycin crystalline degradation products-chiral stationary phase[J]. Biomedical Chromatography, 21(3): 234–240.
DOI:10.1002/(ISSN)1099-0801
|
Morris G M, Goodsell D S, Halliday R S, et al. 2015. Automated docking using a Lamarckian genetic algorithm and an empirical binding free energy function[J]. Journal of Computational Chemistry, 19(14): 1639–1662.
|
Osterberg F, Morris G M, Sanner M F, et al. 2002. Automated docking to multiple target structures:incorporation of protein mobility and structural water heterogeneity in AutoDock[J]. Proteins Structure Function & Bioinformatics, 46(1): 34–40.
|
Raverdy V, Ampe E, Hecq J D, et al. 2013. Stability and compatibility of vancomycin for administration by continuous infusion[J]. Journal of Antimicrobial Chemotherapy, 68(5): 1179–1182.
DOI:10.1093/jac/dks510
|
Ribeiro A R, Maia A S, Cass Q B, et al. 2014. Enantioseparation of chiral pharmaceuticals in biomedical and environmental analyses by liquid chromatography:an overview[J]. Journal of Chromatography B, 968: 8–21.
DOI:10.1016/j.jchromb.2014.02.049
|
Shen J, Wei H, Yu X, et al. 2011. Chiral separation of chlorpheniramine by HPLC with β-Cyclodextrin nitro group derivative as stationary phase[J]. Journal of South-Central University for Nationalities (Natural Science Edition), 30(4): 32–35.
|
Sun J Y, Xing Y P, Song J X, et al. 2015. Chiral separation of 4 drugs by capillary electrophoresis[J]. Journal of Shenyang Pharmaceutical University, 32: 199–203.
|
Svensson L A, Dönnecke J, Karlsson K E, et al. 2000. Polar organic phase liquid chromatography with packed capillary columns using a vancomycin chiral stationary phase[J]. Chirality, 12(8): 606–613.
DOI:10.1002/1520-636X(2000)12:8<>1.0.CO;2-Z
|
王世玉. 1998. 世界手性药物选集[M]. 北京: 国家医药管理局信息中心: 234–246.
|
Zhang D, Xu X, Ma S. 2015. The study of enantioseparation of zolmitriptan on vancomycin-bonded chiral stationary phase[J]. Journal of Separation Science, 28(18): 2501–2504.
|
 2019, Vol. 39
2019, Vol. 39


