2. 青岛海洋科学与技术试点国家实验室海洋生态与环境科学功能实验室, 青岛 266237;
3. 中国海洋大学海洋化学研究所, 青岛 266100
2. Laboratory for Marine Ecology and Environmental Science, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266237;
3. Institute of Marine Chemistry, Ocean University of China, Qingdao 266100
海洋是硫的第二大储库, 是挥发性有机硫化物(VSCs)的主要自然源.VSCs是硫循环的主要参与者, VSCs及其氧化产物是大气硫酸盐气溶胶和云凝结核(CCN)的重要来源, 对全球辐射平衡和臭氧浓度有重要影响.羰基硫(COS)、二甲基硫(DMS)和二硫化碳(CS2)作为3种主要的VSCs, 在全球硫循环中发挥重要作用, 并能够影响全球气候变化.
COS是大气中分布最广、含量最丰富的还原性硫痕量气体, 在对流层中的平均寿命长达2~7年(Brühl et al., 2011).由于其化学惰性, 它能在对流层中充分混合并传输至平流层, 最终转化为硫酸盐气溶胶(Crutzen, 1976).COS所形成的硫酸盐气溶胶不仅影响全球辐射平衡, 还为非均相化学反应提供反应表面, 从而加速平流层中臭氧层的损耗.因此, COS成为硫循环中的研究热点.DMS是自然硫源释放的主要含硫气体, 大气中的DMS主要来自海洋.据估算, 通过海-气交换进入大气中的DMS约占自然硫释放的50%(Cline et al., 1983).DMS在大气中与·OH、·NO3等自由基发生光化学反应, 生成SO2和甲磺酸(CH3SO3H, MSA)并进一步生成非海盐硫酸盐(nss-SO42-), 都对酸沉降有重要贡献.另外, 硫酸盐气溶胶能够增加CCN数目, 进而影响云的形成和太阳辐射, 导致气候变化(Charlson et al., 1987).虽然CS2在环境中的浓度较前两者低, 但CS2大气中有2~7 d的寿命, 能经直接氧化过程产生COS和SO2(Kim et al., 1987), 是大气中COS的主要前体物, 也是海洋大气中SO2的重要来源, 对全球气候变化有重要影响.
近些年来, VSCs的研究越来越受到关注.Chin等(1993)估算了全球COS和CS2向大气的释放量, 分别为1.23和0.57 Tg·a-1.王艳君等(2011;2012)建立了大气和环境水中VSCs的检测方法.田旭东等(2005)测定了青岛近岸海水与大气中COS、DMS和CS2的浓度.朱蓉等(2017)优化了海水和大气中VSCs的分析方法.中国近岸海域海洋源VSCs的研究主要集中于DMS, 包括海水中DMS的产生、浓度分布、海-气通量等(Yang et al., 2000), 对海水和大气中COS和CS2的研究很少.孙茗歆等(2018)观测了春季东海海水及大气中VSCs的浓度分布.东海是世界上最典型的陆架海之一, 受陆源输入的影响, 是VSCs的主要排放源.本文研究了秋季东海海水及大气中VSCs的浓度分布、相互关系及海-气通量, 对于探讨VSCs的源与汇、生物地球化学循环过程以及估算中国近海对全球硫循环的贡献具有重要意义.
2 材料与方法(Materials and methods) 2.1 仪器装置Agilent 7890A气相色谱仪(GC-7890A), 配置火焰光度检测器(FPD, 美国Agilent Technologies公司); Agilent7890A/5975C气相色谱-质谱仪(GC-MSD, 美国Agilent Technologies公司); G2070化学工作站(美国Agilent Technologies公司); 2101DS采样罐清洗系统(美国Nutech公司); 2202A动态稀释仪(美国Nutech公司); 8900D低温预浓缩系统(美国Nutech公司); 2.5 L苏码不锈钢采样罐(美国Nutech公司); 色谱柱:CP7529(CP-Sil 5 CB for Sulfur 30 m × 0.32 mm × 4.0 μm)(美国Agilent公司); 吹扫-捕集前处理装置.
2.2 实验试剂3种VSCs混合标准气体(99.9%, 色谱纯, 北京明尼克分析仪器设备中心):COS、DMS、CS2浓度均为1×10-6(以混合体积分数计); 分析纯无水CaCl2(天津市北辰方正试剂厂); 载气:高纯N2(GC-7890A)、高纯He(GC-MSD), 纯度> 99.999%(青岛豪森气体有限公司); 液氮(青岛豪森气体有限公司).
2.3 实验方法2017年9月14—24日搭载“向阳红18号”科学考察船对东海海域VSCs进行了现场调查, 调查海域及站位如图 1所示.本航次调查选取7个断面的39个站位进行表层海水样品的采集, 其中12个站位采集大气样品.
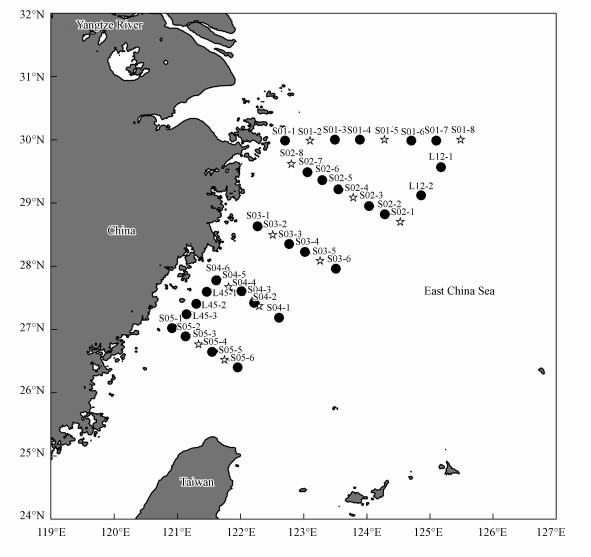 |
| 图 1 2017年9月中国东海调查站位图 (☆表示同时采集海水和大气样品的站位) Fig. 1 Sampling stations in the East China Sea in September 2017 (☆ indicates stations where both seawater and atmospheric samples were simultaneously collected) |
海水样品利用12 L Niskin Rosette采水器进行采集, 通过一根半透明硅胶管将海水注入100 mL玻璃钳口瓶, 控制海水流速, 装满至海水溢出瓶体积2倍时, 轻缓提出硅胶管移出, 立即压盖密封.样品采集完毕后, 进行现场测定.采样站位的海水温度、盐度等环境和水文参数, 由船载CTD设备在采集海水样品时同步测定.
海水中VSCs的浓度通过气提冷阱捕集-气相色谱法进行测定.用注射器抽取30 mL海水样品注入大体积吹扫室中, 通入60 mL·min-1的高纯N2吹扫15 min.吹扫出的VSCs先后经过无水CaCl2填装的干燥管和100%脱脂棉填充的1/4 Teflon管除去水和氧化物, 最后通过六通阀富集于浸在液氮中的捕集管内.吹扫完成后, 将捕集管从液氮中取出, 放入热水(> 90 ℃)中热解析.解析出的VSCs在高纯N2携带下进入GC进行分离, 然后通过FPD进行检测, 用外标法进行定量分析.该方法对VSCs的检出限为2.5~3.5 ng, 精密度范围是3.5%~5.3%(朱蓉等, 2017).
2.3.2 大气样品的采集与测定大气样品使用冲洗干净并抽成真空的不锈钢苏玛罐, 将采样罐置于距海平面约10 m的前甲板, 面向迎风方向采集.大气样品采集完毕带回实验室用GC-MSD进行分析.将不锈钢苏玛罐与预浓缩仪连接, 经三级冷阱预浓缩仪富集, 再由高纯He携带进入GC-MSD进行测定.用外标法对大气样品进行定量分析.该方法对VSCs的检出限为0.1×10-12~0.5×10-12, 精密度小于2%(孙茗歆等, 2018).
2.3.3 VSCs海-气通量的计算方法通过计算VSCs的海-气通量可以估算VSCs对全球气候变化及硫循环的影响.本研究采用Liss和Slater建立的双层滞膜模型(Liss et al., 1974)对VSCs的海-气通量进行估算, 计算公式为:
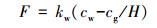
|
(1) |
式中:F为海-气通量(μmol·m-2·d-1); kw为气体交换常数(m·d-1); cw和cg分别为VSCs在表层海水和大气中的平衡浓度(nmol·L-1); H为亨利常数(田旭东, 2004), 计算公式见表 1.利用Sander(2015)的转化公式将其转化为无量纲的常数.kw采用国际上通用的N2000来计算(Nightingale et al., 2000).田旭东(2004)、孙茗歆等(2018)介绍了具体计算方法.
| 表 1 亨利常数计算公式 Table 1 The calculation formulas of Henry constant |
为了更好地了解3种VSCs在海洋与大气间的传输, 根据海水与大气中VSCs的浓度计算其过饱和系数α:
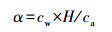
|
(5) |
式中, cw和ca分别为海水与大气中VSCs的浓度(nmol·L-1); H为亨利常数.当α>1时, 海水中VSCs为过饱和状态(田旭东, 2004).
3 结果与讨论(Results and discussion) 3.1 海水中COS、DMS和CS2的水平分布2017年秋季东海表层海水温度、盐度、叶绿素(Chl-a)以及COS、DMS和CS2的水平分布如图 2所示.调查海域受长江冲淡水、东海沿岸流以及台湾暖流的综合影响, 表层海水温度和盐度总体呈现南高北低, 近岸低、远海高的趋势(张颖杰等, 2018).东海秋季航次的调查结果表明, 表层海水中Chl-a的浓度范围为0.03~5.56 μg·L-1.从Chl-a的浓度水平分布可以看出, Chl-a总体分布趋势为近岸高, 远海低.Chl-a浓度最高值出现在工业发达、人口密集的闽浙沿海区(L45-2站位), 可能是工业废水和生活污水的排放, 以及东海沿岸流与陆地径流向该区域输送了大量的营养盐(颜廷壮, 1991), 为浮游植物的生长提供了有利条件.此外, 该区域西侧是台湾暖流的主干, 台湾暖流带来高温高盐的海水, 丰富的营养盐与温暖的海水为浮游植物提供了适宜的生长条件, 使Chl-a浓度出现高值.
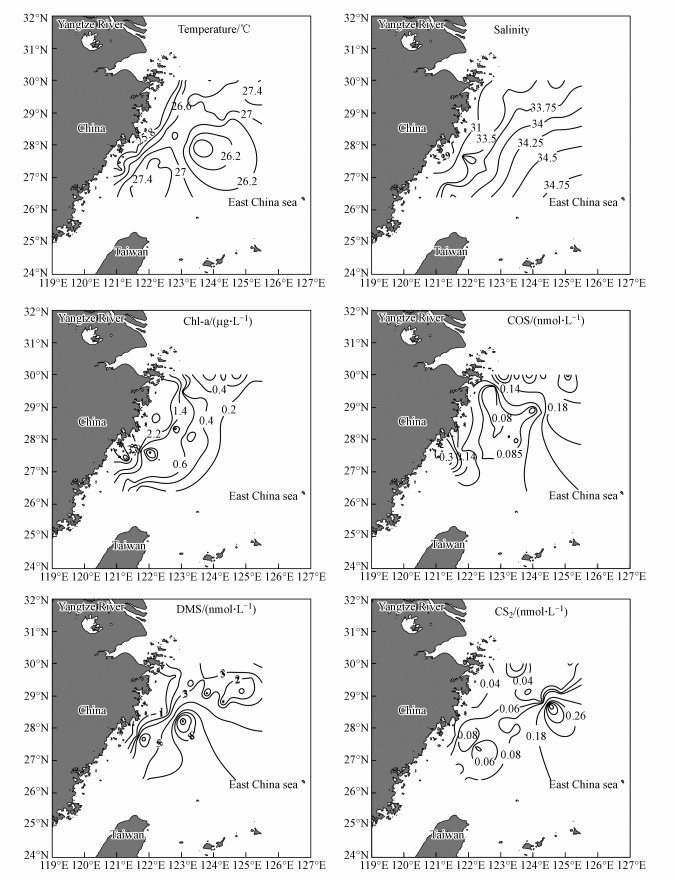 |
| 图 2 秋季东海表层海水中温度、盐度、Chl-a、COS、DMS和CS2的水平分布 Fig. 2 Horizontal distributions of temperature, salinity, Chl-a, COS, DMS, and CS2 in the surface seawater of the East China Sea in autumn |
秋季东海表层海水中COS、DMS和CS2的浓度范围分别是0.07~0.45、0.44~12.56和0.02~0.42 nmol·L-1, 平均值为(0.14±0.08)、(3.58±2.81)和(0.06±0.06) nmol·L-1.表层海水中3种VSCs的浓度由高到低分别为:DMS > COS > CS2, 这与田旭东等(2005)在青岛近岸海域的调查结果一致.此外, 表 2列出了中国近岸海域与大西洋等远海地区海水中3种VSCs平均浓度的对比, 结果表明, 由于东海等近岸海域受河流输入和人为排放的影响, 近岸海域海水中COS、DMS和CS2的浓度明显高于北大西洋等远洋地区(Kim et al., 1987; Ulshofer et al., 1995; Simó et al., 1997).
| 表 2 不同海域海水中VSCs浓度的比较 Table 2 Comparison of VSCs concentration in seawater in different oceans |
在海水中, COS、DMS和CS2的产生机制都与生物的硫酸盐同化还原有关, 但具体的生产机制不同, 导致它们的水平分布也有差异.秋季东海表层海水中DMS浓度在S03-4站位出现浓度高值, 研究表明, DMS主要是由海洋浮游植物产生(Lovelock et al., 1972), 因此浮游植物的生物量是影响海水中DMS浓度的一个重要因素.但该站位附近Chl-a浓度并不高, 这表明海水中DMS的生产过程较为复杂, 会受到多种因素的影响, 如浮游植物的种群结构、细菌丰度等.海水中COS的浓度高值出现在近岸站位L45-2附近, Zepp等(1994)认为, COS在海洋中的光化学生产速率为近岸大于远海.此外, 该站位与Chl-a高值区重合, 由于浮游植物显著生长, 水体中有机物含量较高, 腐殖酸、芳烃聚合物等有色溶解有机物(CDOM)的浓度也相对较高(王翔等, 2010), 有利于含有巯基的有机物在光敏剂——CDOM的催化下光化学生成COS(Flöck et al., 1997).另外, L45-2站位靠近闽浙沿海区, 该地区受人类活动影响, 可能造成COS出现高值.在杭州湾东部海域, 尤其是舟山群岛近岸的S01-2站位附近, 海水中COS浓度也较高, 这可能是由于钱塘江等陆地径流以及人类活动向该海域输送了大量高活性的CDOM及陆源有机质, 促进了COS的光化学生成.王翔等(2010)在秋季长江口及其邻近海域的调查发现, 杭州湾东部海域CDOM的含量较高.CS2的高值区出现在东海外侧海域(S02-1站位), 该站位附近COS也表现为明显的高值.有研究表明, CS2与COS有相似的光化学生产机制(Xie et al., 1998).东海外侧海水透明度较高(薛宇欢等, 2015), 有利于COS和CS2的光化学生成.
3.2 大气中COS、DMS和CS2的浓度分布秋季东海大气中COS、DMS和CS2的浓度分别为(336.5~719.9)×10-12、(2.4~89.2)×10-12和(27.9~199.0)×10-12, 平均浓度为(414.9±107.4)×10-12、(39.7±29.9)×10-12和(92.9±55.6)×10-12.其中, COS在大气中含量最高, 其次是CS2, 而DMS的含量最低.如表 3所示, 对比春季东海大气中3种VSCs的浓度(孙茗歆等, 2018), 发现秋季大气中COS和DMS的浓度高于春季, 而CS2的浓度则是春季略高于秋季.邱天雪等(2015)对厦门近海海域大气中VSCs的季节变化进行研究, 发现VSCs浓度季节变化明显, 其中DMS的季节变化与本研究一致.对比Cooper等(1993)在北大西洋的研究结果发现, 秋季东海大气中DMS浓度低于北大西洋, 而CS2浓度明显高于北大西洋.这可能是由于海洋是大气中DMS的主要源, 不同季节和海域DMS的生产能力存在差别.而CS2主要来源于人为排放, 近海海域受人类活动和工业污染影响显著使大气中CS2浓度高于远洋.
| 表 3 不同海域大气中VSCs浓度的比较 Table 3 Comparison of VSCs concentration in overlying atmosphere of different oceans |
大气中COS、DMS和CS2的浓度分布如图 3所示.由图 3可知, COS在大气中的分布相对于海水较为均匀.这主要与其化学惰性有关(Crutzen, 1976).大气中COS和CS2的浓度高值均出现在S02-1站位附近, 而大气中DMS的浓度高值出现在S03-5站位, 对应站位海水中VSCs浓度较高.这表明, 海-气扩散对大气中COS、DMS和CS2的浓度有重要影响.另外, 大气中的COS在近岸站位S03-2附近也有较高的浓度, 近岸海域大气中COS浓度总体高于远海, 可能与人为排放的污染气体有关.大气中CS2呈现近岸高、远海低的趋势, 表明人为排放是影响CS2在大气中含量的重要因素.有研究指出, 人为输入占全球大气中CS2总来源的50%左右(Chin et al., 1993), 工业化学品生产、制药工业等会向大气排放CS2.
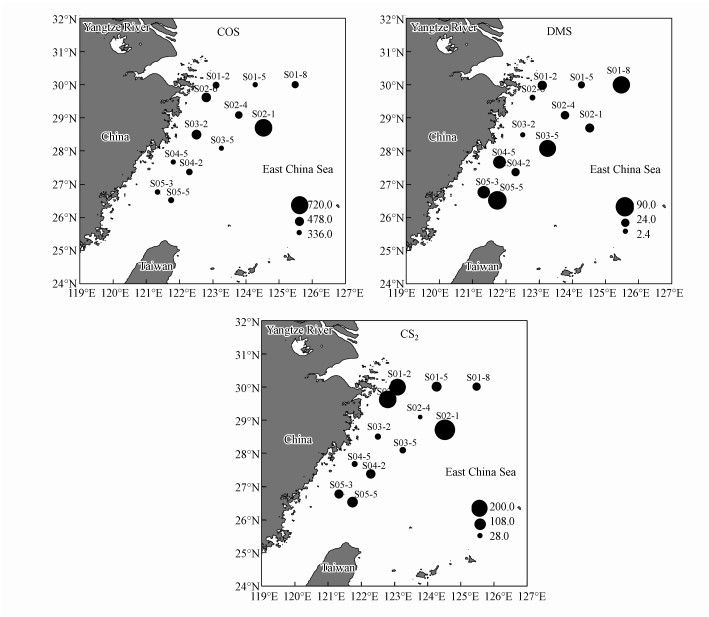 |
| 图 3 秋季东海大气中COS、CS2和DMS的浓度(×10-12)分布 Fig. 3 Distributions of COS, CS2 and DMS concentrations (×10-12) in the atmosphere over the East China Sea in autumn |
为了更好地认识3种VSCs的源汇关系及影响其浓度分布的因素, 运用SPSS软件对秋季东海海水和大气中3种VSCs与Chl-a的浓度进行相关性分析(表 4).Yang等(2000)在东海的研究表明, DMS与Chl-a浓度有明显的相关性.但在本研究中, 两者并无显著相关关系.Vila-Costa等(2008)认为尽管DMS的前体物质——二甲巯基丙酸内盐(DMSP)来源于浮游植物, 但表面海水中DMS的浓度与浮游植物生物量没有直接关系.这主要是由于DMSP的生产取决于浮游植物的种类和生长阶段, 而且DMSP并非直接转化为DMS.DMS的浓度是由DMS和DMSP在微生物食物链中复杂的生产与消费机制决定的, 受到海洋中多种物理和化学要素的影响.因此, DMS与Chl-a之间存在不确定性.
| 表 4 秋季东海3种VSCs与Chl-a的相关性分析 Table 4 Correlation analysis of three VSCs and Chl-a in the East China Sea in autumn |
同时, 本研究对海水与大气中3种VSCs的浓度进行了相关性分析.结果显示, 海水中的DMS和CS2都与其在大气中的浓度呈现明显的相关关系.这表明, 海洋对大气中DMS和CS2的浓度有重要贡献.而海水中COS与大气中的COS浓度没有显著相关关系, 可能是由于大气中COS来源复杂, 如不完全生物质燃烧以及工业释放等.秋季东海表层海水中DMS与CS2存在相关关系, 孙茗歆等(2018)春季在东海的研究也发现了两者之间显著相关.据推测, 海水中DMS主要来源于藻类细胞破裂释放DMSP的降解, 而死亡的藻类有机体会提供大量的含硫有机物(如光肽氨酸等)降解能产生CS2(药怡良, 2016), 两者来源上的共性, 导致了海水中DMS与CS2较好的相关关系.此外, 大气中COS和CS2的相关性最为显著(0.901, p < 0.01), 通常认为, CS2是大气中COS的主要源, 大气中的CS2被·OH等自由基氧化为COS, 转化效率达到0.81(Chin, 1992).
3.4 VSCs的海-气通量秋季东海表层海水中COS、DMS和CS2的海-气通量范围分别为0.03~3.48、0.64~59.44和0.01~0.99 μmol·m-2·d-1, 平均值为(0.45±0.58)、(13.15±12.66)和(0.20±0.22) μmol·m-2·d-1.其中, 3种VSCs的海-气通量大小顺序为:DMS > COS > CS2, 与3种VSCs在海水中浓度顺序一致.
秋季东海海水中VSCs的海-气通量呈现明显的空间差异, COS、DMS、CS2在海水中的浓度、海-气通量与风速之间的关系如图 4所示.3种VSCs的海-气通量空间变化趋势与风速基本一致, 这可能是由于海-气通量是由海水中物质的浓度和传输速率决定的, 而传输速率又与海洋表面风速、海水粘度等有关(马奇菊等, 2004).COS和DMS海-气通量的最高值均出现在S01-4站位, 该站位风速达到最大值(15.0 m·s-1), 而其最低值则出现在风速较小和海水中COS、DMS浓度较低的站位.CS2海-气通量最高值出现在站位, 该站位CS2的浓度和风速都较高; 最低值出现在S05-1站位, 是由于该站位附近海水中CS2的浓度为调查站位中的最低值, 而且该处较低的风速(4.2 m·s-1)也影响了CS2在海-气界面的传输速率.综上所述, 秋季东海VSCs的海-气通量随风速和VSCs在海水中浓度的变化而变化, 但风速是主要的影响因素.
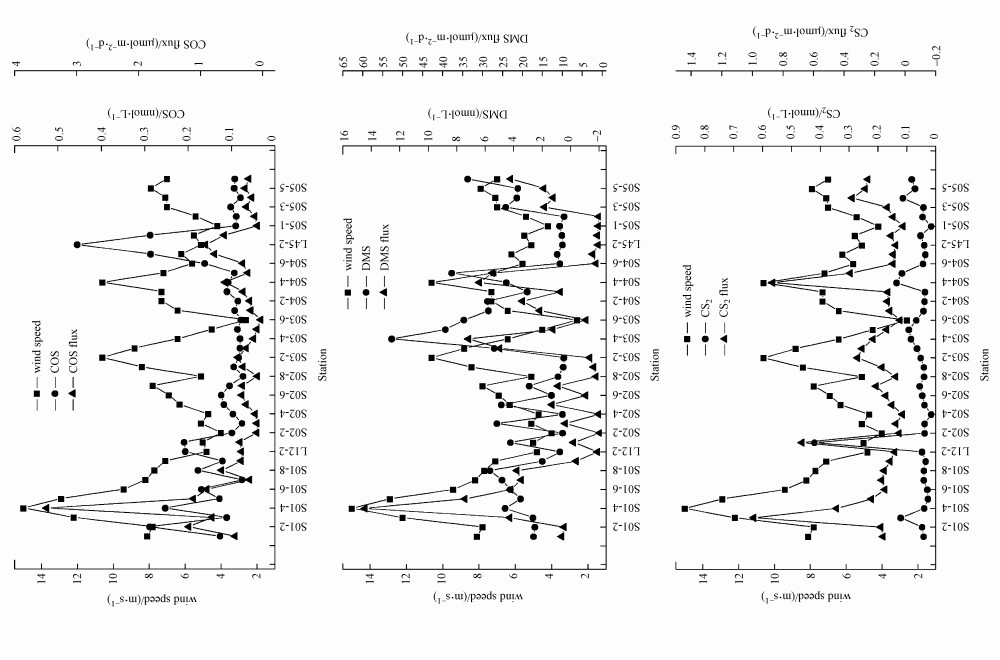 |
| 图 4 秋季东海各站位海水中海-气通量随VSCs浓度与风速的变化 Fig. 4 Variations of sea-to-air fluxes with VSCs concentrations and wind speeds in the East China Sea during autumn |
Ferek等(1983)发现海水中COS是过饱和的.研究表明, 海水中的DMS也是过饱和的(Lana et al., 2011).本研究计算了部分站位VSCs的过饱和系数, COS、DMS和CS2的过饱和系数分别为1.82~8.64、569.12~6191.86和5.57~72.73, 平均值为(3.57±1.82)、(3392.04±1749.70)和(21.19±20.61).结果表明, 3种VSCs的过饱和系数大于1, 说明秋季东海海水中COS、DMS和CS2相对于大气都是过饱和的.此外, 3种VSCs的海-气通量均为正值, 说明海水中COS、DMS和CS2的浓度都高于大气, 都能从海洋扩散进入大气, 是大气中COS、DMS及CS2的源.虽然Chin等(1993)认为海洋是大气中COS的一个主要的源, 但Weiss等(1995)发现一些海域存在明显的不饱和现象, 这说明海洋在一定程度上可能会成为大气中COS的汇.将本研究结果与中国近海以及大洋的研究结果结合, 发现大部分近海和陆架海域(孙茗歆等, 2018)、河口区域(田旭东等, 2004)都是大气中COS的源, 而远海海域可能成为大气中COS的汇(Khalil et al., 1984).对于大气中的DMS和CS2, 由于其较低的含量使得海洋成为其主要源.
4 结论(Conclusions)1) 秋季东海表层海水中3种VSCs的浓度由高到低分别为:DMS > COS>CS2; 大气中3种VSCs的浓度由高到低分别为:COS > CS2 > DMS.在海水中, 近岸海域VSCs浓度明显高于远洋地区, COS和CS2可能有相似的光化学生产机制; 在大气中, COS分布均匀, DMS主要来源于海-气扩散, CS2主要受人为排放影响.
2) 海水中DMS与CS2存在相关性, 可能是由于海水中DMS与CS2的来源途径有一定的相似性.大气中COS和CS2的相关性最为显著, 大气中的CS2是COS的主要来源.
3) 秋季东海表层海水中3种VSCs都呈过饱和状态, 其海-气通量大小顺序为:DMS > COS > CS2, 与海水中浓度大小顺序一致, 风速是影响VSCs海-气通量的主要因素.由于较大的过饱和度和海-气通量, 秋季东海是大气COS、DMS、CS2的主要源.
Brühl C, Lelieveld J, Crutzen P J, et al. 2011. The role of carbonyl sulphide as a source of stratospheric sulphate aerosol and its impact on climate[J]. Atmospheric Chemistry & Physics, 11(7): 20823–20854.
|
Charlson R J, Lovelock J E, Andreae M O, et al. 1987. Oceanic phytoplankton, atmospheric sulphur, cloud albedo and climate[J]. Nature, 326(6114): 655–661.
DOI:10.1038/326655a0
|
Chin M, Davis D D. 1993. Global sources and sinks of OCS and CS2 and their distributions[J]. Global Biogeochemical Cycles, 7(2): 321–337.
DOI:10.1029/93GB00568
|
Chin M. 1992. Atmospheric studies of carbonyl sulfide and carbon disulfide and their relationship to stratospheric background sulfur aerosol[D]. Georgia Institute of Technology, Atlanta
|
Cline J D, Bates T S. 1983. Dimethyl sulfide in the Equatorial Pacific Ocean:A natural source of sulfur to the atmosphere[J]. Geophysical Research Letters, 10(10): 949–952.
DOI:10.1029/GL010i010p00949
|
Cooper D J, Saltzman E S. 1993. Measurements of atmospheric dimethylsulfide, hydrogen sulfide, and carbon disulfide during GTE/CITE 3[J]. Journal of Geophysical Research-Atmospheres, 98(D12): 23397–23409.
DOI:10.1029/92JD00218
|
Crutzen P J. 1976. The possible importance of CSO for the sulfate layer of the stratosphere[J]. Geophysical Research Letters, 3(2): 73–76.
DOI:10.1029/GL003i002p00073
|
Ferek R J, Andreae M O. 1983. The supersaturation of carbonyl sulfide in surface waters of the Pacific Ocean off Peru[J]. Geophysical Research Letters, 10(5): 393–396.
DOI:10.1029/GL010i005p00393
|
Flöck O R, Andreae M O, Dräger M. 1997. Environmentally relevant precursors of carbonyl sulfide in aquatic systems[J]. Marine Chemistry, 59(1/2): 71–85.
|
Johnson J E, Harrison H. 1986. Carbonyl sulfide concentrations in the surface waters and above the Pacific Ocean[J]. Journal of Geophysical Research, 91(D7): 7883–7888.
DOI:10.1029/JD091iD07p07883
|
Khalil M A K, Rasmussena R A. 1984. Global sources, lifetimes and mass balances of carbonyl sulfide (OCS) and carbon disulfide (CS2) in the earth's atmosphere[J]. Atmospheric Environment, 18(9): 1805–1813.
DOI:10.1016/0004-6981(84)90356-1
|
Kim K H, Andreae M O. 1987. Carbon disulfide in seawater and the marine atmosphere over the North Atlantic[J]. Journal of Geophysical Research-Atmospheres, 92(D12): 14733–14738.
DOI:10.1029/JD092iD12p14733
|
Lana A, Bell T G, Simó R, et al. 2011. An updated climatology of surface dimethlysulfide concentrations and emission fluxes in the global ocean[J]. Global Biogeochemical Cycles, 25(1): 3–25.
|
Liss P S, Slater P G. 1974. Flux of gases across the air-sea interface[J]. Nature, 247(5438): 181–184.
DOI:10.1038/247181a0
|
Lovelock J E, Maggs R J, Rasmussen R A. 1972. Atmospheric dimethylsulfide and the natural sulfur cycle[J]. Nature, 237: 452–453.
DOI:10.1038/237452a0
|
马奇菊, 胡敏, 田旭东, 等. 2004. 青岛近岸海域二甲基硫排放和大气中二甲基硫浓度变化[J]. 环境科学, 2004, 25(1): 20–24.
|
Nightingale P D, Malin G, Law C S, et al. 2000. In situ evaluation of air-sea gas exchange parameterizations using novel conservative and volatile tracers[J]. Global Biogeochemical Cycles, 14(1): 373–387.
DOI:10.1029/1999GB900091
|
邱天雪, 陈进生, 陈衍婷, 等. 2015. 厦门近海域大气中挥发性有机硫化物特征研究[J]. 环境科学与技术, 2015, 38(1): 111–116.
|
Sander R. 2015. Compilation of Henry's law constants (version 4.0) for water as solvent[J]. Atmospheric Chemistry & Physics, 14(21): 29615–30521.
|
Sciare J, Mihalopoulos N, Nguyen B C. 2002. Spatial and temporal variability of dissolved sulfur compounds in European estuaries[J]. Biogeochemistry, 59(1/2): 121–141.
DOI:10.1023/A:1015539725017
|
Simó R, Grimalt J O, Joan Albaigés. 1997. Dissolved dimethylsulphide, dimethylsulphoniopropionate and dimethylsulphoxide in western Mediterranean waters[J]. Deep-sea research Part Ⅱ. Topical studies in oceanography, 44(3/4): 929–950.
|
孙茗歆, 张洪海, 马乾耀, 等. 2018. 春季东海挥发性有机硫化物(VSCs)分布的研究[J]. 中国环境科学, 2018, 38(4): 1490–1498.
|
田旭东, 胡敏, 马奇菊. 2005. 青岛环境大气和海洋表层水中挥发性硫化物的测定[J]. 环境科学学报, 2005, 25(1): 30–33.
DOI:10.3321/j.issn:0253-2468.2005.01.005 |
田旭东. 2004.中国近海大气和海水中挥发性硫化物的测定[D].北京: 北京大学
http://d.wanfangdata.com.cn/Thesis/Y634287 |
Ulshofer V S, Uher G, Andreae M O. 1995. Evidence for a winter sink of atmospheric carbonyl sulfide in the northeast Atlantic Ocean[J]. Geophysical Research Letters, 22(19): 2601–2604.
DOI:10.1029/95GL02656
|
Vila-Costa M, Kiene R P, Simí R. 2008. Seasonal variability of the dynamics of dimethylated sulfur compounds in a coastal northwest Mediterranean site[J]. Limnology & Oceanography, 53(1): 198–211.
|
王翔, 杨红, 孔德星, 等. 2010. 长江口外海水中有色溶解有机物(CDOM)的光吸收特性[J]. 应用海洋学学报, 2010, 29(4): 518–524.
|
王艳君, 郑晓玲, 何鹰, 等. 2011. 大气中总挥发性有机硫化物检测方法的研究[J]. 环境科学, 2011, 32(12): 3617–3622.
|
王艳君, 郑晓玲, 何鹰, 等. 2012. 环境水中总挥发性有机硫化物的检测方法[J]. 中国环境科学, 2012, 32(6): 1040–1045.
DOI:10.3969/j.issn.1000-6923.2012.06.013 |
Weiss P S, Johnson J E, Gammon R H, et al. 1995. Reevaluation of the open ocean source of carbonyl sulfide to the atmosphere[J]. Journal of Geophysical Research-Atmospheres, 100(D11): 23083–23092.
DOI:10.1029/95JD01926
|
Xie H X, Moore R M, Miller W L. 1998. Photochemical production of carbon disulphide in seawater[J]. Journal of Geophysical Research Oceans, 103(C3): 5635–5644.
DOI:10.1029/97JC02885
|
薛宇欢, 熊学军, 刘衍庆. 2015. 中国近海海水透明度分布特征与季节变化[J]. 海洋科学进展, 2015, 33(1): 38–44.
DOI:10.3969/j.issn.1671-6647.2015.01.005 |
颜廷壮. 1991. 中国沿岸上升流成因类型的初步划分[J]. 海洋通报, 1991, 10(6): 1–6.
|
Yang G P, Li L, Qi J L, et al. 2000. Dimethylsulfide in the surface water of the East China Sea[J]. Continental Shelf Research, 20(1): 69–82.
DOI:10.1016/S0278-4343(99)00039-4
|
药怡良. 2016.黄东海水体及沉积物中有色溶解有机物的研究[D].北京: 中国科学院研究生院(海洋研究所)
http://cdmd.cnki.com.cn/Article/CDMD-80068-1016206075.htm |
Zepp R G, Andreae M O. 1994. Factors affecting the photochemical production of carbonyl sulfide in seawater[J]. Geophysical Research Letters, 21(25): 2813–2816.
DOI:10.1029/94GL03083
|
张颖杰, 何真, 杨桂朋. 2018. 东海海水和大气中挥发性卤代烃的分布[J]. 中国环境科学, 2018, 38(1): 14–25.
DOI:10.3969/j.issn.1000-6923.2018.01.002 |
朱蓉, 张洪海, 杨桂朋. 2017. 海水和大气中挥发性硫化物分析方法的研究[J]. 分析化学, 2017, 45(10): 1504–1510.
DOI:10.11895/j.issn.0253-3820.170291 |
 2019, Vol. 39
2019, Vol. 39


