在工业生产和日常生活中均会产生大量的有机废水, 这些废水中的有机污染物必须进行降解处理达标后才能排放, 否则将严重污染环境水体.由于废水中的有机物成分复杂, 除了含有可以常规生化降解的有机物外, 还有大量诸如偶氮类染料、芳烃、苯酚、抗生素等有难生化降解的有机物(Lapworth et al., 2012; Petrie et al., 2015).对于这类难生化降解的有机物, 若采用传统有机废水处理技术进行处理, 存在降解效率低、处理费用高、会附带产生二次污染等缺点.为了解决这类难生化降解的有机废水处理问题, 众多研究人员提出了各种用于有机物废水处理的高级氧化技术(Advanced oxidation processes, AOPs)(Lee et al., 2003; Pera-titus et al., 2004; Anotai et al., 2012; Uribe et al., 2015; Ammar et al., 2015; Cheng et al., 2016).这些AOPs技术的共同特点是:需要消耗大量的高品位能量(电或高温热源), 其有机废水处理成本相对高昂, 经济性较差, 因而在工业规模化应用方面受到了一定的限制(孙怡等, 2017).
为了降低难生化降解有机废水的处理成本, 徐士鸣等(2017b;2018b)提出了一种基于逆电渗析(Reverse Electro-Dialysis, RED), 由低品位热能驱动的有机废水氧化降解技术.该技术的基本思路和工作循环是:采用热分离方法先将低品位热能转换成工作溶液浓差(化学势)能, 然后利用RED反应器将溶液浓差能转换成废水中有机物的降解能和部分电能.
包括企业生产过程排放的余/废热、太阳能、地热能等在内的低品位热能来源广泛, 使用成本极低, 而RED反应器的特殊结构使得流经RED反应器的有机废水具有较高的降解速率.因此, 该技术特别适用于既排放大量难生化降解有机废水, 又排放大量低品位热能的企业.
RED技术是基于利用自然界浓差能发电所提出的一项“蓝色”能源技术(Jia et al., 2014).以往对该技术研究的重点是设法将溶液浓差能尽可能多的转换成电能, 尽可能抑制其电极氧化还原反应生成物的产生(Scialdone et al., 2012; Burheim et al., 2012).但对于用于有机废水降解的RED反应器却相反, 要求在反应器两电极处产生尽可能多的氧化剂, 以快速氧化降解流经反应器电极流道的有机废水.尽管RED反应器还需要通过外电路输出一定的电能, 但此时外电路的主要作用是作为电子迁移通道.
目前对于包括低温多效蒸馏、低温多级闪蒸、膜蒸馏等在内的热分离技术的研究已非常成熟, 并在实践中得到广泛应用(Khawaji et al., 2008; Youssef et al., 2014).但对RED技术的研究相对较少, 尤其是在国内, 而且所进行的研究工作主要还是针对溶液浓差能发电(徐士鸣等, 2017a; 2018a).作为一项新的AOPs技术, 国内外仅有少量的有关溶液浓差能驱动RED反应器氧化降解有机或无机废水的文献发表.在Scialdone教授的指导下, D′Angelo在其博士论文研究期间从事过利用自然界盐差能驱动RED反应器氧化降解有机废水方面的研究(D′Angelo, 2016), 并发表了两篇相关的学术论文(Scialdone et al., 2014; 2015), 但后续再未检索到有新的研究论文发表.Zhou等(2018)对利用RED反应器降解废水中的氨氮进行了研究, 但仅利用RED反应器中阳极氧化反应所生产的HClO来降解废水中的氨氮.徐士鸣等(2018b)为了验证RED反应器阴、阳极氧化降解有机废水的工作机理, 对RED反应器阴、阳极独立降解有机废水进行了机理性实验研究, 结果表明, RED反应器阴/阳极处的还原/氧化反应均能生成对有机物具有强降解作用的H2O2和HClO, 并对流经电极的有机废水具有较高的降解率.但因RED反应器阳极产生的Cl2与水反应及HClO与废水中的有机物反应均会产生HCl, 使得被处理的有机废水pH降低, 需要消耗碱对其进行中和后才能排放, 从而会使废水处理成本增加.同时, RED反应器阴极的电芬顿反应需要消耗H+并需要维持溶液的pH, 因此, 必须向流经RED反应器阴极的有机废水中添加HCl, 用以维持被处理废水的H+浓度和pH值, 从而也会增加废水处理成本.
RED反应器阴、阳极独立降解有机废水的优点是, 流经两电极的有机废水各自独立, 氧化降解过程互不受影响, 但缺点也较为明显.如果采用RED反应器阴、阳极联合降解有机废水, 则阴极电芬顿反应可以利用阳极产生的HCl, 使其阴、阳极H+消耗/生成到达平衡, 不需要额外添加酸、碱, 有利于降低有机废水的处理成本.但缺点是RED反应器阴、阳极反应相互干扰, 可能导致有机废水降解率降低.
在前期RED反应器阴、阳极独立降解偶氮染料—酸性橙Ⅱ研究的基础上(徐士鸣等, 2018b), 本文对由溶液浓差能驱动的RED反应器阴、阳极联合降解酸性橙Ⅱ进行实验研究, 对影响废水中有机物降解的因素进行分析并提出改进措施, 以期为后续的由低品位热能驱动的RED反应器氧化降解有机废水循环特性研究奠定基础.
2 RED反应器及作用机理(RED reactor and its working mechanism)徐士鸣等(2018b)在对RED反应器阴、阳极独立降解有机废水的机理性实验研究的文章中, 已对RED反应器结构及其对流经阴、阳电极时强氧化剂的生成及对废水中有机物的降解机理进行了较为充分的描述, 本文仅作简单介绍.
RED反应器结构如图 1所示, 它由端板、阴\阳电极、交错排布的阴\阳离子交换膜(IEMs)及丝网隔垫所组成.当稀、浓溶液流经由阴离子交换膜(AEM)、阳离子交换膜(CEM)和隔垫所构成的稀、浓溶液流道时, 在溶液浓度(化学势)差作用下, 浓溶液中的阴、阳离子分别穿过其对应的IEMs进入稀溶液流道, 并在膜两侧形成膜电势.在膜电势的作用下, 反应器阴、阳两极发生氧化还原反应并生成相应的产物(强氧化剂).
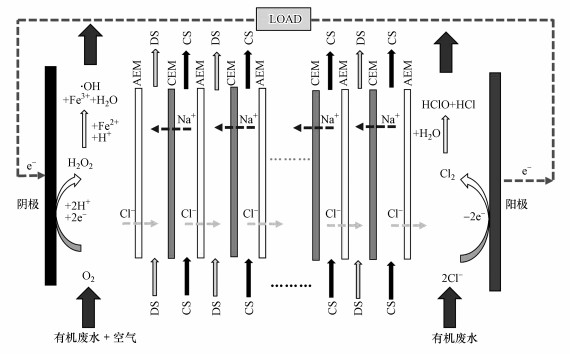 |
| 图 1 RED反应器基本构造及氧化还原反应 Fig. 1 The structure of RED reactor and its redox reaction |
由工作溶液经AEM迁移到阳极流道的两个氯离子(Cl-), 在阳极处被氧化并放出两个电子生成氯气(Cl2), Cl2与废水作用产生次氯酸(HClO)和盐酸(HCl).因HClO是弱电解质, 在水中会部分电离成氢离子(H+)和次氯酸根离子(ClO-).作为强氧化剂, HClO和ClO-均对废水中的有机物起到氧化降解作用(Martinez-Huitle et al., 2009; Garcia-Segura et al., 2018).具体反应式如下所示:

|
(1) |
在RED反应器阴、阳极联合降解有机废水流程中, 流经反应器两电极的电极液(有机废水)是联通的.由阳极反应生成的H+会随电极液的流动进入阴极流道.在膜电势作用下, 阳极获得的两个电子经外电路迁移到阴极, 并使流经阴极电极液中的两个H+被还原并与溶解于电极液中的氧气(O2)发生反应, 生成过氧化氢(H2O2).在催化剂二价铁离子(Fe2+)的作用下, H2O2会被分解成羟基自由基(·OH)和氢氧根(OH-), 同时Fe2+被氧化成三价铁离子(Fe3+).Fe3+又会从阴极获得一个电子再次被还原成Fe2+.由此可知, RED反应器阴极反应是电芬顿反应(Brillas et al., 2009), 电极液中有机物可被·OH氧化并降解.具体反应式如下所示:
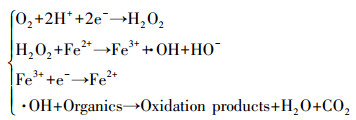
|
(2) |
与常规电解和电芬顿反应器不同的是, 为了降低RED反应器电极室电阻, 其电极液流道非常狭窄, 电极液几乎是紧贴电极表面流动.因此, 在电极表面还可能产生直接的有机物氧化降解反应(Bechtold et al., 2001).
3 联合降解实验流程设计(Flow design for joint degradation)由RED反应器有机废水氧化降解反应式(1)和(2)可知, 在膜电势的作用下RED反应器阴、阳两极均能生成强氧化剂, 对流经的废水中有机物进行氧化降解.对于RED反应器而言, 既可以采用阴、阳两极独立降解有机废水的方式, 也可以采用阴、阳两极联合降解的方式.就当前对以溶液浓差能驱动的RED反应器氧化降解有机废水的研究深度而言, 两种方式各有利弊.考虑到采用RED反应器阴、阳两极联合降解方式时可使阳极产生的H+与阴极消耗的H+达到平衡, 从而在对有机废水处理过程中不需要额外消耗酸、碱, 有利于降低有机废水的处理费用, 这应该是今后利用低品位热能驱动的RED反应器氧化降解有机废水技术的重点研究方向.
图 2给出了串联和并联两种RED反应器阴、阳极联合降解有机废水的流程.串联流程仅采用一台电极液泵, 流程相对简单, 但RED反应器阴、阳极生成物之间的相互影响较大, 并联流程正好与其相反.本研究除了探索影响RED反应器阴、阳极联合降解有机废水降解速率的因素外, 还对两种降解流程的有机废水降解效果进行比较和分析.
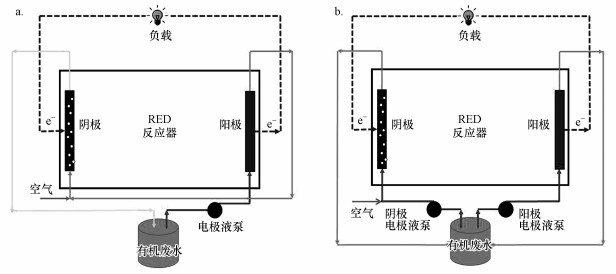 |
| 图 2 RED反应器阴、阳极联合降解有机废水流程(a.串联流程, b.并联流程) Fig. 2 The joint degradation flow of organic wastewater by two electrodes in a RED |
本研究采用自制的RED反应器, 由40个膜电池单元组成, 各部件参数如表 1所示.RED反应器外形和内部丝网隔垫的照片与文献(徐士鸣等, 2018a)给出的相同, 仅增加了膜电池单元数和阴、阳IEMs的排列方式.反应器中, 阳极采用厚度为1.5 mm的钛板镀铱釕(Ti/RuO2-IrO2)电极, 阴极采用孔隙率约为65%、厚度为5 mm的气体扩散电极(碳毡).IEMs采用日本旭硝子公司生产的Selemion型仪器, 有效膜面积为7 cm×11.5 cm.RED两端封膜采用日本富士公司生产的AEM, 原因在于该公司生产的AEM对模拟废水中的酸性橙Ⅱ具有极好的隔离性及极好的耐强氧化剂腐蚀性, 可以避免电极液中的酸性橙Ⅱ进入到工作溶液.有机废水氧化降解实验系统照片如图 3所示.实验所用的测试及运转设备型号、参数及精度如表 2所示.
| 表 1 RED反应器各部件基本参数 Table 1 Basic parameters of each part in RED reactor |
 |
| 图 3 有机废水氧化降解实验系统 Fig. 3 Experimental system for oxidation degradation of organic sewage |
| 表 2 实验设备型号、参数及精度 Table 2 The model, parameter and precision of experiment equipment |
RED反应器电势变化会影响反应物生成速率, 从而影响对流经其阴、阳电极有机废水的降解速率.但影响RED反应器电势大小的因素主要有:包括膜型号、膜生产厂家、膜对数等在内的反应器结构参数, 以及包括浓度比、流率比、过膜流速等在内的工作溶液参数.为了避免反应器电势变化对有机废水降解实验结果的影响, 本次实验采用固定结构参数的RED反应器和固定的工作溶液运行参数.
采用人工配置的固定浓度比为100(3 mol·L-1/0.03 mol·L-1)的浓/稀NaCl水溶液作为工作溶液, 采用蠕动泵使浓/稀溶液以1:1的流率比并以84 mL·min-1的流率通过RED反应器的阴、阳电极流道.以印染行业中常用的偶氮染料—酸性橙Ⅱ作为阴、阳极联合氧化降解的研究对象.人工配置浓度为150 mg·L-1的酸性橙Ⅱ水溶液1 L作为氧化降解的模拟废水, 并添加一定量的NaCl和FeCl2作为支撑电解质和电芬顿反应催化剂, 添加HCl调节溶液初始pH值.将配制好的模拟废水作为RED反应器的电极液使用.在阴极流道进口处, 利用空气泵向电极液注入一定量的空气来满足阴极电芬顿反应对O2的需求.配制的工作溶液和电极液所用到的电解质均为分析纯, 所含杂质可以忽略.溶剂均为去离子水.实验过程中, 使用紫外可见分光光度计对模拟废水中的酸性橙Ⅱ浓度进行检测并计算其降解率.采用可调电阻作为RED反应器外部负载, 并用电数字万用表检测氧化降解过程中RED反应器的输出电功率.
根据前期研究结果(徐士鸣等, 2018b), 在RED反应器结构和工作溶液运行参数确定的情况下, 对有机废水氧化降解影响较大的电极液参数包括:支撑电解质NaCl浓度、催化剂FeCl2浓度、pH值、空气流率和电极液流率.RED反应器输出电流可以表征电荷的迁移速度及物质传输速度, 故输出电流的大小也对降解反应具有影响.
由于影响流经RED反应器有机废水氧化降解速率的因素较多, 需要了解每一因素对有机废水氧化降解速率的影响程度, 因此, 本文先对RED反应器阴、阳极联合降解并联流程按表 3所列的7因素5水平进行正交试验.实验中, 通过人为改变电极液因素/水平组合方式来配置模拟废水(电极液), 而反应器输出电流则通过调节外加负载电阻(可调电阻)来维持电流稳定.在正交实验条件下, 通过测试一次性流经阴、阳两极的电极液中酸性橙Ⅱ的浓度变化值, 选出最优的电极液参数和电流大小, 然后在此条件下进行串、并联流程的RED反应器阴、阳极联合降解有机废水实验, 降解时间均为20 min.对比2种流程对酸性橙Ⅱ的降解效果, 并与前期研究(徐士鸣等, 2018b)的RED反应器阴、阳极独立降解有机废水的研究结果进行比较和分析.
| 表 3 RED反应器阴、阳极联合降解并联流程正交实验因素和水平 Table 3 Factors and levels for orthogonal experiment of the joint degradation by two electrodes in RED reactor with parallel flow |
实验分析方法与前期研究(徐士鸣等, 2018b)的RED反应器阴、阳极独立降解有机废水时相同, 以有机物降解率(Rdg)和偶氮染料脱色率(Rdc)作为降解指标.其中, 采用紫外可见分光光度计测定处理有机废水吸光度, 根据测得的酸性橙Ⅱ标准曲线反推其浓度并根据式(3)计算降解率; 采用紫外可见分光光度计测定被处理有机废水吸光度, 并根据式(4)计算其脱色率.
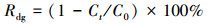
|
(3) |
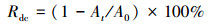
|
(4) |
式中, C0为酸性橙Ⅱ水溶液初始浓度(mg·L-1); Ct为降解反应t时间后酸性橙Ⅱ水溶液浓度(mg·L-1); A0为酸性橙Ⅱ在最大吸收峰值(484 nm)处的初始吸光度; At为降解反应t时间后在最大吸收峰值处的酸性橙Ⅱ吸光度.
5 结果与分析(Results and analysis) 5.1 正交试验对正交实验所得结果进行分析, 得到如表 4所示的正交实验数据, 并得出各因素/水平组合对模拟废水中酸性橙Ⅱ去除率的影响程度和极差.对极差进行排序得到如表 5所示的排序结果.由表 4可知, 电流对RED反应器阴、阳极联合降解效果的影响程度远大于其它因素.其主要原因在于:电流的大小决定了单位时间内传输的电子数量, 电子的迁移速率会直接影响RED反应器阴、阳极氧化剂产速率, 从而影响有机物的降解速率.由于RED反应器内部存在电阻, 其输出电压与电流呈线性下降关系, 输出功率与电流呈上凸抛物线关系(徐士鸣等, 2017a).本实验中当输出电流为0.2 A时, 反应器输出功率达到最大值, 再继续增大电流时, 不仅反应器输出功率会降低, 而且反应器电极电压会继续降低, 甚至低于反应物生成电势, 导致氧化剂产率降低, 有机物降解速率降低.
| 表 4 正交实验阴、阳极的酸性橙Ⅱ降解率均值及极差 Table 4 The degradation ratemean value and range of acid Orange 7 of orthogonal experiment |
根据表 5的极差排序结果可知, 电极液及电流参数对阴、阳两极联合降解效果的影响程度从大到小排列依次为:电流>pH值>阳极电极液流率>NaCl浓度>阴极电极液流率>空气流率>FeCl2浓度.
| 表 5 降解率因素/水平组合影响程度排序 Table 5 Rank of influence of factor/level combination on organic degradation rate |
将表 5所列由正交实验获得的最优因素/水平组合, 作为溶液浓差能驱动的RED反应器阴、阳极联合降解酸性橙Ⅱ模拟废水(电极液)配制及运行参数, 并分别对串、并联流程的浓度为150 mg·L-1、容积为1 L的酸性橙Ⅱ模拟废水进行20 min的氧化降解实验, 每隔2 min取样一次并注入比色管, 其色泽直观变化如图 4所示.同时, 测定比色管内模拟废水中酸性橙Ⅱ的质量浓度和pH值变化, 计算酸性橙Ⅱ的降解率和脱色率, 实验重复3次.
 |
| 图 4 酸性橙Ⅱ模拟废液色泽随降解时间的变化(a.并联流程; b.串联流程) Fig. 4 Color variation of AO7 simulated sewage with time during oxidation degradation process |
从图 4可以直观地看到, 无论采用何种流程, 经过RED反应器阴、阳极联合降解后的酸性橙Ⅱ模拟废水的色泽随降解时间会发生明显变化, 色泽逐渐变淡, 说明模拟废水中的酸性橙Ⅱ被氧化降解.通过比较采用并联或串联流程氧化降解的酸性橙Ⅱ模拟废水色泽随降解时间的变化可以直观地发现, 在相同的降解时间内采用并联流程时酸性橙Ⅱ模拟废水的脱色情况要优于采用串联流程.这与通过紫外可见分光光度计测定的酸性橙Ⅱ模拟废水脱色率和降解率随实验运行时间的变化关系一致(图 5).
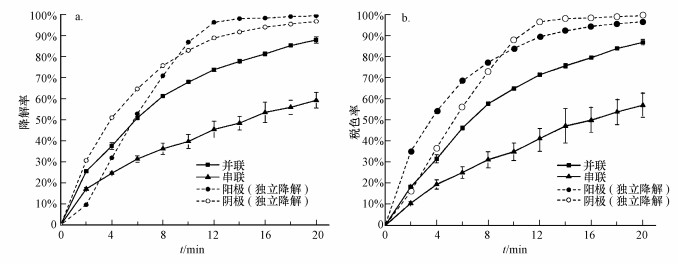 |
| 图 5 酸性橙Ⅱ模拟废水降解率(a)和脱色率(b)随时间的变化 Fig. 5 Variation of AO7 simulated sewage degradation rate(a) and decoloration rate(b) with degradation time |
在图 5中复合了在相同RED反应器结构参数和工作溶液浓度比条件下, 反应器阴、阳极独立降解酸性橙Ⅱ时测得的降解率和脱色率(徐士鸣等, 2018b).从图中可知, 采用并联流程时, 酸性橙Ⅱ模拟废水的氧化降解率和脱色率均优于采用串联流程.降解20 min后, 采用并联流程时酸性橙Ⅱ模拟废水的降解率和脱色率可分别达到87.93%和86.87%, 而采用串联流程时, 两者仅分别达到59.26%和57.08%.但与阴、阳极独立降解酸性橙Ⅱ模拟废水情况相比, 无论何种流程, 阴、阳极联合降解效果均低于独立降解时的效果.
通过实验数据分析可知, RED反应器阴、阳极独立降解与阴、阳极联合降解之间产生差异的原因有以下两方面.
1) 独立降解时, 阴、阳极氧化还原反应所生成的产物不会互相干扰; 而采用阴、阳极联合降解时所产生的产物却会互相干扰.有文献报道(Held et al., 1978), HClO与H2O2之间会发生氧化还原反应, 生成水、氧气和盐酸(式(5)).
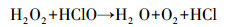
|
(5) |
这在RED反应器阴、阳极联合降解串、并联流程的降解效果中得到显现.采用串联流程时, 流出阳极流道的电极液中的HClO尚未与有机物完全反应就立即流入阴极流道, 会与阴极产生的H2O2发生反应而消耗H2O2, 使阴极处的电芬顿反应减弱, 从而对有机废水的降解效果变差.采用并联流程时, 流经阳极的电极液流入敞口玻璃烧杯, 一方面可使阳极生成的HClO在烧杯内还可以继续与有机物发生氧化降解反应; 另一方面, 因HClO的不稳定性, 在外界的干扰下很容易分解成氯气和水, 氯气通过敞口玻璃烧杯液面逸出.这两方面因素均会使烧杯内电极液中的HClO浓度降低, 当其流经阴极时与阴极生成的H2O2反应会减弱, 使得对有机废水的解效果提高.从图 5中还可以看到, 并联流程下3次实验所得测试数据基本不变, 说明具有较好的机废水降解率稳定性.
2) 联合降解时, 作为催化剂的Fe2+会随电极液流入阳极, 在膜电势的作用下会失去电子, 被氧化成Fe3+而失去活性, 使阴极电芬顿反应效果减弱.从图 4的废水色泽随降解时间的变化看, 降解20 min后, 通过紫外可见分光光度计测定的酸性橙Ⅱ模拟废水脱色率可达86.87%, 但废水的直观色泽仍然偏黄, 表明氧化降解后废水中含有一定量的Fe3+导致废水色泽偏黄.
RED反应器阴、阳极联合降解过程中酸性橙Ⅱ模拟废水pH值及反应器输出功率随降解时间的变化关系如图 6所示.由图 6a可知, 无论采用何种降解流程, 降解过程中模拟废水pH值基本稳定在初始值1.5附近, 但采用并联流程时废水的pH值稍大于串联流程.这也说明采用并联流程时反应器阴极消耗的H+数要大于采用串联流程时反应器阴极消耗的H+数, 即采用并联流程时反应器阴极的H2O2产率要大于采用串联流程时反应器阴极的H2O2产率.这也从另一个角度验证了上述两条影响RED阴、阳极联合降解有机废水效果的因素分析结果.但与RED反应器阴、阳极独立降解时的情况相比, 联合降解时阳极氧化反应产生的H+可以与阴极电芬顿反应所需消耗的H+基本保持平衡, 并能维持电芬顿反应所要求的pH值.
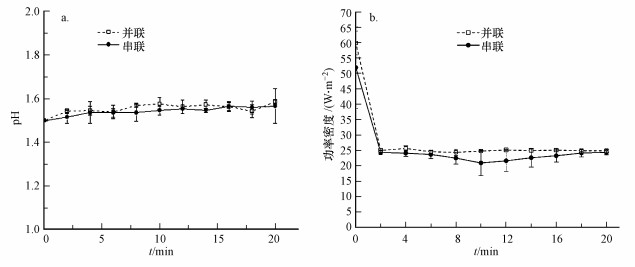 |
| 图 6 模拟废水pH值(a)和RED反应器输出功率密度(b)随降解时间的变化 Fig. 6 Variation of the simulated wastewater pH value(a) and output power density of RED reactor(b) with degradation time |
由图 6b可知, RED反应器在氧化降解有机废水的同时, 还对外输出一定的电能(图中的功率密度是指单位电极面积输出的电功率).因在降解过程中通过调节负载电阻阻值来控制RED反应器输出电流, 并恒定维持在0.2 A, 故RED反应器输出功率随降解时间的变化也反映其输出电压(U=P/I)随降解时间的变化.而反应器输出电压不仅与电流有关, 而且还与反应器内阻和反应生成物消耗电势有关.尽管影响反应器输出电压的因素较多, 但从图 6b中还是可以看到, 当降解开始时, 输出功率有突降.说明反应器电极有生成物产生, 需要消耗一部分反应功率使反应器输出电压降低.随着降解反应的进行, 反应器输出功率基本上维持在25 W·m-2附近, 不再有大的变化.另外, 串联流程时的反应器输出功率略低于并联流程时的反应器输出功率, 这也说明串联流程时的反应器内部能量损失要大于并联流程时的反应器内部能量损失.
通过本次实验研究发现, 尽管在相同的RED反应器结构和工作溶液参数下, 阴、阳极联合降解有机废水效果不如阴、阳极独立降解有机废水效果, 但已经远好于其它AOPs技术对酸性橙Ⅱ模拟废水的降解效果(李国亭等, 2006; Yang et al., 2011; Lin et al., 2014).下一阶段将研究如何进一步提高RED反应器阴、阳极联合降解有机废水的效果, 使其接近或达到甚至超过阴、阳极独立降解时的效果并降低运行费用.
6 结论(Conclusions)1) 正交实验结果表明, 电流对RED反应器有机物氧化降解效果的影响最大, 其次是电极液pH值, 影响最小的是FeCl2浓度.
2) 除了需要调节废水的初始pH值和电导率外, RED反应器阴、阳极联合降解有机废水时, 其H+能够达到产/耗平衡, 不需要额外添加其它化学物质, 有利于降低有机废水处理费用并避免二次污染.
3) RED反应器阴、阳极联合降解有机废水过程中, 阴、阳极处的生成物(H2O2和HClO)具有强氧化性, 对有机物氧化降解起到关键作用, 但二者之间的相互反应会降低有机废水降解效率, 应设法避免.
4) 在阴极被还原的Fe2+会随电极液流经阳极, 被氧化成Fe3+而失去活性, 削弱阴极电芬顿反应, 这一点应设法避免.
5) 阴、阳极联合降解有机废水的并联流程降解效果优于串联流程, 1 L浓度为150 mg·L-1的酸性橙Ⅱ模拟废水经20 min降解, 并联流程的脱色率和降解率分别为86.87%和87.93%, 串联流程的脱色率和降解率分别为57.08%和59.26%.
7 展望(Prospects)尽管RED反应器阴、阳极联合降解酸性橙Ⅱ有机废水时的降解率低于阴、阳独立降解时的降解率, 但采用阴、阳极联合降解后, 阳极产生的H+与阴极消耗的H+可以平衡, 使得有机废水处理过程不需要额外添加酸、碱, 有利于降低有机废水的处理成本.
利用低品位热能驱动的RED反应器氧化降解有机废水技术, 特别适合于既有高浓度/高盐度有机废水需要处理, 又有大量低品位能热需要排放的场合, 用以降低有机废水处理能耗和费用.作为一项新的AOPs技术, 对于RED反应器氧化降解有机废水技术实用化, 无论是理论还是技术方面仍有许多问题有待解决.
Ammar S, Oturan M A, Labiadh L, et al. 2015. Degradation of tyrosol by a novel electro-Fenton process using pyrite as heterogeneous source of iron catalyst[J]. Water Research, 74: 77–87.
DOI:10.1016/j.watres.2015.02.006
|
Anotai J, Thuptimdang P, Su C C, et al. 2012. Degradation of o-toluidine by fluidized-bed Fenton process: statistical and kinetic study[J]. Environmental Science And Pollution Research, 19(1): 169–176.
DOI:10.1007/s11356-011-0553-x
|
Bechtold T, Burtscher E, Turcanu A. 2001. Cathodic decolourisation of textile waste water containing reactive dyes using a multi-cathode electrolyser[J]. Journal of Chemical Technology And Biotechnology, 76(3): 303–311.
DOI:10.1002/(ISSN)1097-4660
|
Burheim O S, Seland F, Pharoah J G, et al. 2012. Improved electrode systems for reverse electro-dialysis and electro-dialysis[J]. Desalination, 285: 147–152.
DOI:10.1016/j.desal.2011.09.048
|
Brillas E, Sires I, Oturan M A. 2009. Electro-fenton process and related electrochemical technologies based on Fenton′s reaction chemistry[J]. Chemical Reviews, 109(12): 6570–6631.
DOI:10.1021/cr900136g
|
Cheng M, Zeng G M, Huang D L, et al. 2016. Hydroxyl radicals based advanced oxidation processes (AOPs) for remediation of soils contaminated with organic compounds:A review[J]. Chemical Engineering Journal, 284: 582–598.
DOI:10.1016/j.cej.2015.09.001
|
Garcia-Segura S, Ocon J D, Chong M N. 2018. Electrochemical oxidation remediation of real wastewater effluents - A review[J]. Process Saf Environ Protect, 113: 48–67.
DOI:10.1016/j.psep.2017.09.014
|
D′Angelo A.2016.Reverse electrodialysis process for the production of chemicals and the treament of contaminated wastewater[D].Palermo: Università degli Studi di Palermo
|
Held A M, Halko D J, Hurst J K. 1978. Mechanisms of chlorine oxidation of hydrogen peroxide[J]. Journal of the American Chemical Society, 100(18): 5732–5740.
DOI:10.1021/ja00486a025
|
Jia Z, Wang B, Song S, et al. 2014. Blue energy:Current technologies for sustainable power generation from water salinity gradient[J]. Renewable & Sustainable Energy Reviews, 31: 91–100.
|
Khawaji A D, Kutubkhanah I K, Wie J M. 2008. Advances in seawater desalination technologies[J]. Desalination, 221(1/3): 47–69.
|
Lapworth D J, Baran N, Stuart M E, et al. 2012. Emerging organic contaminants in groundwater:A review of sources, fate and occurrence[J]. Environmental Pollution, 163: 287–303.
DOI:10.1016/j.envpol.2011.12.034
|
Lee H J, Kang D W, Chi J W, et al. 2003. Degradation kinetics of recalcitrant organic compounds in a decontamination process with UV/H2O2 and UV/H2O2/TiO2 processes[J]. Korean Journal of Chemical Engineering, 20(3): 503–508.
DOI:10.1007/BF02705556
|
Lin H, Zhang H, Hou L. 2014. Degradation of C.I.Acid Orange 7 in aqueous solution by a novel electro/Fe3O4/PDS process[J]. Journal Of Hazardous Materials, 276: 182–191.
DOI:10.1016/j.jhazmat.2014.05.021
|
李国亭, 曲久辉, 张西旺, 等. 2006. 光助电催化降解偶氮染料酸性橙Ⅱ的降解过程研究[J]. 环境科学学报, 2006, 26(10): 1618–1623.
DOI:10.3321/j.issn:0253-2468.2006.10.007 |
Martinez-Huitle C A, Brillas E. 2009. Decontamination of wastewaters containing synthetic organic dyes by electrochemical methods:A general review[J]. Applied Catalysis B-Environmental, 87(3/4): 105–145.
|
Ozcan A, Oturan M A, Oturan N, et al. 2009. Removal of Acid Orange 7 from water by electrochemically generated Fenton′s reagent[J]. Journal of Hazardous Materials, 163: 1213–1220.
DOI:10.1016/j.jhazmat.2008.07.088
|
Pera-Titus M, Garcia-Molina V, Banos M A, et al. 2004. Degradation of chlorophenols by means of advanced oxidation processes:a general review[J]. Applied Catalysis B-Environmental, 47(4): 219–56.
DOI:10.1016/j.apcatb.2003.09.010
|
Petrie B, Barden R, Kasprasprzyk-Hordern B. 2015. A review on emerging contaminants in wastewaters and the environment:Current knowledge, understudied areas and recommendations for future monitoring[J]. Water Research, 72: 3–27.
DOI:10.1016/j.watres.2014.08.053
|
Scialdone O, Guarisco C, Grispo S, et al. 2012. Investigation of electrode material - Redox couple systems for reverse electrodialysis processes.Part Ⅰ:Iron redox couples[J]. Journal of Electroanalytical Chemistry, 681: 66–75.
DOI:10.1016/j.jelechem.2012.05.017
|
Scialdone O, D′angelo A, Galia A. 2015. Energy generation and abatement of Acid Orange 7 in reverse electrodialysis cells using salinity gradients[J]. Journal of Electroanalytical Chemistry, 738: 61–68.
DOI:10.1016/j.jelechem.2014.11.024
|
Scialdone O, D′angelo A, De Lume E, et al. 2014. Cathodic reduction of hexavalent chromium coupled with electricity generation achieved by reverse-electrodialysis processes using salinity gradients[J]. Electrochimica Acta, 137: 258–265.
DOI:10.1016/j.electacta.2014.06.007
|
孙怡, 于利亮, 黄浩斌, 等. 2017. 高级氧化技术处理难降解有机废水的研发趋势及实用化进展[J]. 化工学报, 2017, 68(5): 1743–1756.
|
Uribe I O, Mosquera-Corral A, Rodicio J L, et al. 2015. Advanced technologies for water treatment and reuse[J]. Aiche Journal, 61(10): 3146–3158.
DOI:10.1002/aic.15013
|
徐士鸣, 吴德兵, 吴曦, 等. 2017a. 氯化锂溶液为工质的溶液浓差发电实验研究[J]. 大连理工大学学报, 2017a, 57(4): 337–344.
|
徐士鸣, 吴曦, 冷强.2017b.一种利用低品位热降解高浓有机废水方法[P].中国, 发明, CN201711384061.2.2017-12-20
|
徐士鸣, 张凯, 吴曦, 等. 2018a. 电流与浓差对逆电渗析电堆内质量传递的影响[J]. 化工学报, 2018a, 69(10): 4206–4215.
|
徐士鸣, 徐志杰, 吴曦, 等. 2018b. 溶液浓差能驱动的逆电渗析有机废水氧化降解机理研究[J]. 环境科学学报, 2018b, 38(12): 4642–4651.
|
Youssef P G, Al-Dadah R K, Mahmoud S M.2014.Comparative analysis of Desalination Technologies[C].The 6th International Conference on Applied Energy- ICAE2014.Amsterdam, America: 2604-2607
https://www.sciencedirect.com/science/article/pii/S1876610214032871 |
Yang S Y, Yang X, Shao X, et al. 2011. Activated carbon catalyzed persulfate oxidation of Azo dye Acid Orange 7 at ambient temperature[J]. Journal of Hazardous Materials, 186: 659–666.
DOI:10.1016/j.jhazmat.2010.11.057
|
Zhou Y, Zhao K, Hu C, et al. 2018. Electrochemical oxidation of ammonia accompanied with electricity generation based on reverse electrodialysis[J]. Electrochimica Acta, 269: 128–135.
DOI:10.1016/j.electacta.2018.02.136
|
 2019, Vol. 39
2019, Vol. 39


