2. 中国科学技术大学研究生院, 合肥 230026;
3. 中国科学技术大学环境科学与光电技术学院, 合肥 230026;
4. 中国科学院安徽光学精密机械研究所大气光学重点实验室, 合肥 230031
2. Graduate School, University of Science and Technology of China, Hefei 230026;
3. School of Environmental Science and Optoelectronic Technology, University of Science and Technology of China, Hefei 230026;
4. Key Laboratory of Atmospheric Optics, Anhui Institute of Optics and Fine Mechanics, Chinese Academy of Sciences, Hefei 230031
大气气溶胶是指悬浮在大气中的空气动力学直径为0.001~100 μm的液体、固体微粒体系(Seinfeld et al., 2006;唐孝炎等, 2006).吸湿性是气溶胶的主要性质之一, 是指气溶胶在周围环境相对湿度(RH)增加时的吸水能力, 与粒径、化学成分等有关(Gasparini et al., 2004).为了评估气溶胶粒子对环境、气候和健康的影响, 必须知道它们在不同大气RH条件下的吸湿特性(Cappa et al., 2012; Hakala et al., 2016).然而迄今为止, 虽然对于粒径大于100 nm的纯无机盐或一定程度盐混合物的吸湿性已经开展了较为广泛的研究(Swietlicki et al., 2008;刘新罡等, 2010;王轩等, 2010), 然而针对核模态细粒子(特别是粒径小于30 nm)的研究仍相对匮乏.近年来的研究表明, 这些核模态细粒子, 无论是在大陆边界层、污染城市区域、工业烟羽, 还是在对流云或潮间带, 都被广泛观测到(Kulmala et al., 2004).这些广泛存在的高浓度的核模态细粒子, 一方面可能会影响云凝结核(CCN)的浓度, 进而影响云的光学特性, 最终影响地球辐射平衡;另一方面也可能影响气溶胶的粒径分布, 从而影响气溶胶的直接辐射效应.因此, 要想深入认识核模态细粒子在环境大气中的重要角色, 对它们的吸湿性开展相关研究是必要的前提与基础.
根据探测的物理性质不同, 研究气溶胶的吸湿性也具有多种不同的方法.而这其中, 吸湿性串联差分迁移率分析仪(HTDMA)由于能实时获得纳米颗粒物的吸湿性数据, 并且具有较高的测量精度, 因此, 成为最广泛采用的方法之一.国内外不同的研究团队都陆续建立了自己的HTDMA系统并开展了相关研究(Liu et al., 1978;Swietlicki et al., 2008;Ye et al., 2009;王轩等, 2011;Shi et al., 2012;郑晓宏等, 2012;Tan et al., 2013;Wu et al., 2013).但所建立的系统及开展的研究主要针对的是积聚模态(粒径为0.05~2 μm) (Whitby, 1978; 唐孝炎等, 2006)的气溶胶粒子, 对于核模态的细粒子却较少涉猎.随着研究的不断深入, 人们发现小粒径气溶胶粒子的吸湿性表现出与大粒径气溶胶粒子不同的演化特征.例如, Hämeri等(2000;2001)利用自行设计的Nano-HTDMA对粒径小于50 nm的硫酸铵((NH4)2SO4)和氯化钠(NaCl)(大气中常见的无机纳米颗粒物)的吸湿性展开了系统性的研究, 发现与大粒径的气溶胶相比, 小粒径的气溶胶粒子的g因子会随着粒径的减小而减小, 并且粒径对其潮解点(DRH)也有影响.此外, 他们还发现氯化钠g因子的测量值与理论值偏差较大.而Biskos等(2006a; 2006b; 2006c)的系列研究表明, 对于非球体纳米颗粒物, 计算它们的g因子时必须要考虑开尔文效应并引入尺寸相关形状因子.最近Giamarelou等(2018)利用Nano-HTDMA系统测量了8~60 nm卤化钾粒子的g因子, 再次拓展了人们对无机纳米颗粒吸湿性质的认识.更为重要的是, 通过测量纳米颗粒物的g因子, 还可以间接得到粒子的化学组成, 进而深入认识大气气溶胶初始成核机制(Sakurai et al., 2005; Kim et al., 2016).最近的模型研究表明, 即使在污染的大气边界层中也存在着成核事件(Chen et al., 2012).而近年来在中国的外场研究也发现了大量的成核事件, 并且进一步的研究表明与灰霾的形成有重要的关系(Guo et al., 2014; Yao et al., 2018).
鉴于核模态气溶胶粒子在大气环境与气候中的重要角色, 大力开展对核模态细粒子的吸湿性研究对理解灰霾的形成机制及对国家相关污染减控政策的制定具有重要的科学意义与潜在的应用价值.但与之对应的是, 目前国内对粒径小于30 nm的颗粒物的吸湿性研究还相当匮乏.由于RH是影响气溶胶粒径准确测量的最大误差来源之一, 已有的商品化的集成静电分级器受限于其固有的一体化设计, 造成其难以适应外场中对超细粒径(dp < 30 nm)的粒子进行长时间高湿度加湿的要求, 因此, 国际上只有少数几个研究团队搭建了自己的Nano-HTDMA(Sakurai et al., 2005; Smith et al., 2010; Zhang et al., 2012), 还没有商品化的产品, 而国内还未见有Nano-HTDMA研制的相关报道.因此, 本研究在商业化的Nano-DMA系统的基础上, 设计搭建了一套纳米吸湿性串联差分迁移率分析仪, 并完成相关控制程序及采集分析程序的编写.在此基础上, 针对30 nm以下的气溶胶细粒子开展系列测试与验证研究, 并利用理论模型对实验结果进行评估.
2 实验装置与理论模型(Experimental set up and modeling) 2.1 纳米吸湿性串联差分迁移率分析仪本工作搭建的纳米吸湿性串联差分迁移率分析仪基本框架如图 1所示.主要包括3个功能模块:①单分散系气溶胶粒子的选取系统;②加湿系统;③加湿后粒径分布测量系统.
 |
| 图 1 纳米吸湿性串联差分迁移率分析仪装置框架示意图(nDMA:纳米差分电迁移率分析仪;T/RH:温湿度传感器) Fig. 1 Schematic diagram of the nano- hygroscopic tandem differential mobility analyzer(nDMA: nano differential mobility analyzer; T/RH: Sensor of temperature and relative humidity) |
多分散系的待测气溶胶粒子首先经过硅胶干燥管进行干燥, RH下降到10%以下;然后经过静电分级器(TSI 3080)、第一级差分迁移率分析仪(DMA1, Differential Mobility Analyzer, TSI 3085)选出单分散系的气溶胶.由于通过DMA1的样气是经过干燥的, 所以DMA1中的鞘气与其置换一段时间后, RH可以下降到15%左右.随后经过温湿度传感器(Rotronic HC2-C05, 图 1中T/RH1)测量单分散系气溶胶的温度(T)和RH, 精度分别为±0.1 ℃和±1.5%.
2.1.2 加湿系统加湿系统主要包括3个部分:①湿气发生装置;②样气加湿部分;③加湿后粒径测量系统中DMA2鞘气的加湿部分.
湿气发生装置的基本结构如图 2所示.首先, 将零空气发生器产生的零空气(RH<5%)分成两路, 分别用于制备加湿样气和加湿DMA2鞘气的Nafion管的吹扫气, 这样可以实现对两路吹扫气的独立控制.然后每一路再各分成两路, 其中一路保持干燥(称为干气), 另一路经过加湿管(PERMA PURE FC-125 7″)将相对湿度加湿到约100%(称为湿气).每路气体流速由质量流量计控制, 利用比例-积分-微分控制器(PID)快速调节干气和湿气流速的大小, 最后两路混合即可获得目标RH的混合气, 作为样气或DMA2鞘气加湿部分的Nafion管的吹扫气.其中, 加湿管的使用方法为:管壁内层进气, 外层反向进去离子水, 并用3 L·min-1抽速的水泵使水流保持循环.为了能获得稳定的100%RH的湿气, 本装置采用水浴锅对去离子水进行加热, 水温始终保持比室温高1 ℃左右.
 |
| 图 2 湿气发生装置(MFC:质量流量控制器) Fig. 2 The block diagram of the moisture generator(MFC:Mass Flow Controller) |
如上所述, 用于加湿样气和加湿DMA2鞘气的Nafion管的吹扫气是独立控制的.经过第一步粒径筛分的单分散系的气溶胶样气首先进入样气加湿部分的Nafion管(PERMA PURE MD-700 24″)进行加湿. MD系列Nafion管的优点是颗粒物流失率低, 其加湿原理是Nafion膜壁只允许水分子自由通过, 利用样气(从膜壁内层通过)和反向吹扫气(从膜壁外层通过)的水汽压差, 快速地加湿或干燥样气.本装置就是通过控制吹扫气的RH来间接控制样气的RH.在吹扫气流速(4.5 L·min-1)为样气流速(1.5 L·min-1)3倍的条件下, 当吹扫气的RH稳定后, 通常约7 min后样气的RH也趋于稳定, 其波动范围小于0.5%.为了更好地达到水汽平衡(Villani et al., 2008), 加湿后的样气进入一个300 mL的缓冲玻璃容器, 在此容器中样气约有12 s的驻留时间.随后利用温湿度传感器T/RH4测量获得水汽平衡后的样气的温度和RH.
2.1.3 加湿后粒径分布测量系统最后, 用扩展的扫描电迁移率粒径谱仪(SMPS)测量加湿后的单分散系气溶胶粒径的变化.为了防止加湿后的待测样品在SMPS系统中被第二级差分电迁移率分析仪(DMA2)中的鞘气干燥风化或二次加湿, 在DMA2的循环气中加入Nafion管(PERMA PURE PD-200 24")用来加湿, 其温湿度由T/RH5监测, 以控制DMA2中鞘气的RH和加湿后待测样气的RH相一致(图 1右上).考虑到DMA2的鞘流若太大会导致加湿困难, 而太小又会导致SMPS扫描的粒谱分布太宽, 测量不够精确, 因此, 在本研究中DMA2鞘流采用12 L·min-1, PD-200 24″ Nafion管的吹扫气流速为20 L·min-1.为了确保测量结果的准确性, 第二级静电分级器的鞘流和样流都利用皂膜流量计进行了校准.图 3显示了本装置实验过程中样气和DMA2鞘气的典型动态加湿过程, 结果表明通过精确设计和调控, 本装置运行中加湿后样气和DMA2鞘气的RH差值完全控制在±2%以内, 基本避免了二次加湿或风化现象的发生(Villani et al., 2008).同时, 为了有效降低温度波动对加湿后样气与DMA2鞘气RH的影响, 本实验期间实验室内的温度维持在(25±1) ℃.
 |
| 图 3 样气和DMA2鞘气的典型动态加湿 Fig. 3 Humidification of the sample and the sheath flow of DMA2 according to the time |
由Nano-HTDMA测量的迁移率粒径增长因子g定义为:
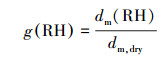
|
(1) |
式中, dm, dry和dm(RH)分别对应于干燥状态下(RH<5%)和加湿到某一RH状态下相应粒子的迁移率粒径.
假设粒子潮解之后形成的含水颗粒是球体的, 则dm(RH)=dve(RH), 其中, dve是体积等效粒径.如果粒子在干燥状态下是球体的, 则dm, dry=dve, dry, 从而可以得到:

|
(2) |
式中, ρs为干粒子的密度(kg·m-3), ρ(wt)为水溶液液滴的密度(kg·m-3), 可表示为ρ(wt)=A0+∑Aiwti, 其中,wt为水溶液中溶质的质量百分数, Ai为各物质的参数.将式(2)变形即可得到吸湿增长因子g与wt的关系.
同时, RH可以通过水活度aw与wt相关联, aw=Ci+∑Ciwti, 其中, Ci是参数.对于粒径大于100 nm的粒子(Giamarelou et al., 2018), RH=100aw, 但对于纳米级颗粒物则要考虑开尔文效应:

|
(3) |
式中, Mw为水的摩尔质量(g·mol-1), R为理想气体常数, T为温度(K), σaq为液滴的表面张力(N·m-1), σaq=(a+b×m)×10-3, 其中, m为质量摩尔浓度(mol·g-1), a、b为参数.联立式(1)~(3)可以获得g(RH), 即模型1.表 1给出了计算硫酸铵、氯化钠吸湿增长因子所需的具体参数值.
| 表 1 计算硫酸铵、氯化钠g因子所需的物理参数 Table 1 Physical parameters for calculating g factor of ammonium sulfate and sodium chloride |
模型1是建立在干粒子都是标准球体的基础上, 但实际上很多干粒子都是不规则的, 因此, 需要引入从非球体(干粒子)到球体(潮解点之后的含水颗粒)变化的修正.迁移粒径和体积等效粒径的关系可表示为(Biskos et al., 2006c):
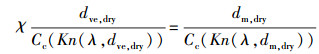
|
(4) |
带入式(2), 再由式(1)得:

|
(5) |
式中, Cc为坎宁安滑移校正因子, Kn为克努森数, χ为形状因子, 用来表征气溶胶粒子的形状和微结构, 定义为粒子所受的阻力与等质量球体所受的阻力之比(Krämer et al., 2000).在电子显微镜下, 干的硫酸铵粒子近似为球形, 其χ值为1.02(Biskos et al., 2006b);而干的氯化钠粒子是立方体(Hämeri et al., 2001; Gysel et al., 2002; Biskos et al., 2006c), χ值为1.08;对于聚集物或不规则形状的粒子, χ值可以高达2及以上(Krämer et al., 2000).再联立式(3)可得到吸湿增长因子g随相对湿度RH的变化曲线, 即模型2.
模型3是在模型2的基础上考虑尺寸相关形状因子(Biskos et al., 2006c).在0.1 < Kn < 10的过渡区, 尺寸相关形状因子可表述为:

|
(6) |
式中, χc是Kn < 0.1的连续区的形状因子, χυ是在Kn>10的自由分子区的形状因子.用χt替换式(4)中的χ, 然后带入式(1)和(2)可得式(7).再联立式(3)可得到g随RH的变化曲线.对于一些形状简单的粒子(如球形、立方体、圆柱体等), χc与χυ存在一定的关系分布(Decarlo et al., 2004), 当χ值较小时(< 2), χc近似等于χυ, 模型3退化成模型2.

|
(7) |
由于DMA1与DMA2存在系统性偏差, 所以需要对新搭建的nano-HTDMA系统进行校准.实验选取(20±2) nm的PSL小球与超纯水按照体积比1:1000混合, 然后通过气溶胶发生器(TSI 3076)产生恒定粒径的PSL气溶胶(徐学哲等, 2016)进入nano-HTDMA.实验测得在85%RH条件下, PSL的吸湿增长因子g为0.993.由于PSL小球是没有吸湿性的, g的理论值为1, 从而得到校准因子为0.007.
为了验证nano-HTDMA系统的可靠性, 针对大气中普遍存在的无机气溶胶, 选取了硫酸铵和氯化钠两种测试体系.实验分别利用浓度为0.02 g·L-1的纯硫酸铵和氯化钠溶液, 由气溶胶发生器产生相应的纳米气溶胶, 选取了粒径为20 nm的气溶胶粒子测量了它们的吸湿性增长, 相应的实验数据参见图 4中数据点.由于干的硫酸铵粒子近似为球体, χ值只有1.02, 所以模型1和模型2计算的结果基本一致.且χc近似等于χυ, 所以不需要再考虑模型3.但对于立方体的氯化钠粒子, χc为1.08, 而χυ达到1.24, 在利用模型1和模型2进行理论模拟的基础上, 还引入尺寸相关形状因子, 即利用模型3进行了相应的理论模拟.所有的模型模拟的结果参见图 4中相应的模拟曲线.
 |
| 图 4 20 nm的硫酸铵(a)与氯化钠(b)的吸湿增长曲线 Fig. 4 Hygroscopic growth curves of (NH4)2SO4 (a) and NaCl (b) nanoparticles with diameter of 20 nm |
本系统测量的硫酸铵、氯化钠g因子的总体不确定度为±2.1%, 其中, 温湿度传感器的探测误差会导致±2%的不确定度;另外, 不同DMA粒径测量存在系统性偏差, 会导致±0.7%的不确定度.由图 4可见, 本研究利用新搭建的nano-HTDMA系统得出的实验测量值和理论值基本一致, 偏差在±0.03范围内.对于20 nm的硫酸铵气溶胶粒子, 本实验获得的潮解点DRH为78.8%, 与Biskos等(2006b;2006c)报道的79.0%±2.5%非常一致.同时, 由于硫酸铵粒子近似为球形, 模型1及模型2计算的结果与实验值三者也基本一致(图 4a).对于氯化钠粒子, 由于其粒子为立方体结构, 偏离于标准球形, 因此, 基本的模型1和模型2很难模拟实验结果.而考虑了尺寸相关形状因子的模型3的模拟结果与实验测量值表现出完美的一致性(图 4b).对于20 nm的氯化钠粒子, 本实验的测得的DRH为77.5%, 与Biskos等(2006b;2006c)的测量结果也具有较好的一致性.无论是理论模拟结果的对比, 还是与前人的实验结果的对比都证实了本系统的可靠性.
3.2 粒径对g、DRH的影响前人的理论研究表明, 较小的气溶胶颗粒(如粒径小于50 nm)与同样体系的大颗粒的气溶胶粒子可能具有不同的吸湿增长因子g和潮解点DRH (Hämeri et al., 2000; Hämeri et al., 2001; Russell et al., 2002).基于自行搭建的nano-HTDMA系统, 在系统校准与验证后, 针对硫酸铵和氯化钠体系, 本研究还在不同粒径下探究了其吸湿增长因子g和潮解点DRH, 相关实验结果与理论模拟结果见图 5.结果表明, 在相同RH下, 纳米级硫酸铵、氯化钠粒子的吸湿增长因子g会随着粒径的减小而减小.如在84% RH条件下, 迁移粒径为30 nm的氯化钠粒子的g因子为1.84, 而15 nm的氯化钠粒子的g因子只有1.71. Park等(2009)在研究硫酸铵、氯化钠粒子时也发现了类似的现象;而Giamarelou等(2018)在研究卤化钾粒子的吸湿性时也发现了相似的性质.对于50 nm以下的粒子, 随着粒径的减小吸湿增长变弱的这种现象可以用开尔文效应来解释(Hämeri et al., 2001; Biskos et al., 2006c; Hu et al., 2010).
 |
| 图 5 不同粒径的硫酸铵、氯化钠的吸湿增长曲线(是人为加上以帮助判断潮解点) Fig. 5 Hygroscopic growth curves of (NH4)2SO4 and NaCl nanoparticles with different diameter |
研究还发现, 粒径对某些纳米颗粒物的DRH也有影响.对于氯化钠粒子, DRH会随着粒径的减小而增大.例如, 30 nm的氯化钠粒子的DRH只有76.3%, 而15 nm的氯化钠粒子的DRH可达到80.2%.但硫酸铵粒子的DRH并没有表现出对粒径的依赖性, 30 nm和15 nm的硫酸铵粒子的DRH很相近. Park等(2009)在研究硫酸铵、氯化钠体系时也发现了与本工作相类似的结果;Giamarelou等(2018)发现卤化钾粒子也有相似的潮解行为.为了解释这种现象, Cheng等(2015)提出并证明, 在气溶胶纳米颗粒物的平衡相图中, 应该将粒径作为附加维度.
4 结论(Conclusions)1) 本文在商用DMA的基础上自主设计并搭建了一套nano-HTDMA, 实现了对加湿的精确控制并对系统进行了校准, 可以用于测量粒径30 nm以下气溶胶颗粒的吸湿性.受粒子传输过程中损耗(特别是小粒径颗粒物)的影响, 检测的最小粒径与颗粒物浓度相关, 如对于粒径12 nm的气溶胶粒子, 本装置吸湿性测量的浓度阈值为2.3×103个·cm-3.在室温条件下, 该装置加湿范围在20%~90% RH之间可控, 波动范围为±0.5%;装置运行中, 加湿后样气和DMA2鞘气的RH差值可以完全控制在±2%以内.动态加湿过程中, 测量颗粒物在一个RH下的g因子大约需要10 min.该装置测量g因子的总体不确定度为±2.1%, 主要来源于温湿度传感器的探测误差.
2) 在此基础上, 针对硫酸铵和氯化钠纳米颗粒的吸湿增长开展了系列实验和理论研究, 结果表明:①形状不规则粒子的吸湿增长g因子的理论计算中需要考虑形状因子χ的影响;②g因子随粒径的减小而减小;③对于不同的无机盐气溶胶粒子, 粒径的变化对DRH呈现出不同影响效应.
3) 系列验证与测试结果表明, 对于30 nm以下的纳米气溶胶粒子, 基于自主搭建的nano-HTDMA的实验结果与前人的研究结果, 以及与模型理论模拟结果都表现出较好的一致性, 表明该装置有望应用于未来核模态细粒子的实验室与场地吸湿性研究.
Biskos G, Malinowski A, Russell L M, et al. 2006a. Nanosize effect on the deliquescence and the efflorescence of sodium chloride particles[J]. Aerosol Science & Technology, 40(2): 97–106.
|
Biskos G, Paulsen D, Russell L M, et al. 2006b. Prompt deliquescence and efflorescence of aerosol nanoparticles[J]. Atmospheric Chemistry and Physics, 6: 4633–4642.
DOI:10.5194/acp-6-4633-2006
|
Biskos G, Russell L M, Buseck P R. 2006c. Nanosize effect on the hygroscopic growth factor of aerosol particles[J]. Geophysical Research Letters, 33(7): 266–280.
|
Cappa C D, Onasch T B, Massoli P, et al. 2012. Radiative absorption enhancements due to the mixing state of atmospheric black carbon[J]. Science, 337(6098): 1078–1081.
DOI:10.1126/science.1223447
|
Chen M, Titcombe M, Jiang J, et al. 2012. Acid-base chemical reaction model for nucleation rates in the polluted atmospheric boundary layer[J]. Proceedings of the National Academy of Sciences of the United States of America, 109(46): 18713–18718.
DOI:10.1073/pnas.1210285109
|
Cheng Y, Su H, Koop T, et al. 2015. Size dependence of phase transitions in aerosol nanoparticles[J]. Nature Communications, 6: 5923.
DOI:10.1038/ncomms6923
|
Decarlo P, Slowik J, Worsnop D, et al. 2004. Particle morphology and density characterization by combined mobility and aerodynamic diameter measurements. Part 1:Theory[J]. Aerosol Science & Technology, 38(12): 1185–1205.
|
Gasparini R, Li R J, Collins D R, et al. 2004. Integration of size distributions and size-resolved hygroscopicity measured during the Houston Supersite for compositional categorization of the aerosol[J]. Atmospheric Environment, 38: 3285–3303.
DOI:10.1016/j.atmosenv.2004.03.019
|
Giamarelou M, Smith M, Papapanagiotou E, et al. 2018. Hygroscopic properties of potassium-halide nanoparticles[J]. Aerosol Science & Technology, 52(5): 536–545.
|
Guo S, Hu M, Zamora M L, et al. 2014. Elucidating severe urban haze formation in China[J]. Proceedings of the National Academy of Sciences of the United States of America, 111(49): 17373–17378.
DOI:10.1073/pnas.1419604111
|
Gysel M E, Weingartner A, Baltensperger U. 2002. Hygroscopicity of aerosol particles at low temperatures.2.Theoretical and experimental hygroscopic properties of laboratory generated aerosols[J]. Environmental Science & Technology, 36(1): 63–68.
|
Hakala J, Mikkilä J, Hong J, et al. 2016. VH-TDMA:A description and verification of an instrument to measure aerosol particle hygroscopicity and volatility[J]. Aerosol Science & Technology, 51(1): 97–107.
|
Hämeri K, Väkevä M, Hansson H C, et al. 2000. Hygroscopic growth of ultrafine ammonium sulphate aerosol measured using an ultrafine tandem differential mobility analyzer[J]. Journal of Geophysical Research Atmospheres, 105(D17): 22231–22242.
DOI:10.1029/2000JD900220
|
Hämeri K, Laaksonen A, Väkevä M, et al. 2001. Hygroscopic growth of ultrafine sodium chloride particles[J]. Journal of Geophysical Research Atmospheres, 106(D18): 20749–20757.
DOI:10.1029/2000JD000200
|
Hu D, Qiao L, Chen J, et al. 2010. Hygroscopicity of inorganic aerosols:size and relative humidity effects on the growth factor[J]. Aerosol & Air Quality Research, 10(3): 255–264.
|
Kim J, Ahlm L, Ylijuuti T, et al. 2016. Hygroscopicity of nanoparticles produced from homogeneous nucleation in the CLOUD experiments[J]. Atmospheric Chemistry & Physics, 15(14): 19803–19833.
|
Krämer L, Pöschl U, Niessner R. 2000. Microstructural rearrangement of sodium chloride condensation aerosol particles on interaction with water vapor[J]. Journal of Aerosol Science, 31(6): 673–685.
DOI:10.1016/S0021-8502(99)00551-0
|
Kulmala M H, Vehkamaki T, Petaja, et al. 2004. Formation and growth rates of ultrafine atmospheric particles:A review of observations[J]. Journal of Aerosol Science, 35: 143–176.
DOI:10.1016/j.jaerosci.2003.10.003
|
Liu B Y H, Pui D Y H, Whitby K T, et al. 1978. The aerosol mobility chromatograph:a new detector for sulfuric acid aerosols[J]. Atmospheric Environment, 12: 99–104.
DOI:10.1016/0004-6981(78)90192-0
|
刘新罡, 张远航. 2010. 大气气溶胶吸湿性质国内外研究进展[J]. 气候与环境研究, 2010, 15(6): 808–816.
DOI:10.3878/j.issn.1006-9585.2010.06.10 |
Mcmurry P H, Stolzenburg M R. 1989. On the sensitivity of particle size to relative humidity for Los Angeles aerosols[J]. Atmospheric Environment, 23(2): 497–507.
DOI:10.1016/0004-6981(89)90593-3
|
Park K, Kim J S, Miller A L. 2009. A study on effects of size and structure on hygroscopicity of nanoparticles using a tandem differential mobility analyzer and TEM[J]. Journal of Nanoparticle Research, 11: 175–183.
DOI:10.1007/s11051-008-9462-4
|
Russell LM, Ming Y. 2002. Deliquescence of small particles[J]. The Journal of Chemical Physics, 116: 311–321.
DOI:10.1063/1.1420727
|
Sakurai H, Fink M A, Mcmurry P H, et al. 2005. Hygroscopicity and volatility of 4~10 nm particles during summertime atmospheric nucleation events in urban Atlanta[J]. Journal of Geophysical Research Atmospheres, 110: D22S04.
|
Seinfeld J H, Pandis S N. 2006. Atmospheric Chemistry and Physics:From Air Pollution to Climate Change (2nd Edition)[M]. New York: Wiley: 204–283.
|
Shi Y, Ge M, Wang W, et al. 2012. Hygroscopicity of internally mixed aerosol particles containing benzoic acid and inorganic salts[J]. Atmospheric Environment, 60: 9–17.
DOI:10.1016/j.atmosenv.2012.06.034
|
Smith J N, Barsanti K C, Friedli H R, et al. 2010. Observations of aminium salts in atmospheric nanoparticles and possible climatic implications[J]. Proceedings of the National Academy of Sciences of the United States of America, 107(15): 6634–6639.
DOI:10.1073/pnas.0912127107
|
Swietlicki E, Hanssson H C, Hämeri K, et al. 2008. Hygroscopic properties of submicrometer atmospheric aerosol particles measured with H-TDMA instruments in various environments-a review[J]. Tellus, 60B: 432–469.
|
Tan H, Xu H, Wan Q, et al. 2013. Design and application of an unattended multifunctional H-TDMA system[J]. Journal of Atmospheric and Oceanic Technology, 30: 1136–1148.
DOI:10.1175/JTECH-D-12-00129.1
|
Tang I N, Tridico A C, Fung K H. 1997. Thermodynamic and optical properties of sea salt aerosols[J]. Journal of Geophysical Research Atmospheres, 102(D19): 23269–23275.
DOI:10.1029/97JD01806
|
唐孝炎, 张远航, 邵敏. 2006. 大气物理化学(第二版)[M]. 北京: 高等教育出版社: 268–290.
|
Villani P, Picard D, Michaud V, et al. 2008. Design and validation of a volatility hygroscopic tandem differential mobility analyzer(VH-TDMA) to characterize the relationships between the thermal and hygroscopic properties of atmospheric aerosol particles[J]. Aerosol Science & Technology, 42(9): 729–741.
|
王轩, 陈建华, 王玮. 2010. 气溶胶吸湿特性研究现状[J]. 中国粉体技术, 2010, 16(1): 101–107.
DOI:10.3969/j.issn.1008-5548.2010.01.022 |
王轩, 陈建华, 陈建民, 等. 2011. 实验室发生纳米气溶胶吸湿性表征[J]. 环境科学研究, 2011, 24(6): 621–631.
|
Whitby K T. 1978. Physical characteristics of sulfur aerosols[J]. Atmospheric Environment, 12: 135–159.
DOI:10.1016/0004-6981(78)90196-8
|
Wu Z J, Poulain L, Henning S, et al. 2013. Relating particle hygroscopicity and CCN activity to chemical composition during the HCCT-2010 field campaign[J]. Atmospheric Chemistry & Physics, 13: 7983–7996.
|
徐学哲, 赵卫雄, 方波, 等. 2016. 标准气溶胶发生系统的建立与性能评估[J]. 环境科学学报, 2016, 36(7): 2355–2361.
|
Yao L, Garmash O, Bianchi F, et al. 2018. Atmospheric new particle formation from sulfuric acid and amines in a Chinese megacity[J]. Science, 361: 278–281.
DOI:10.1126/science.aao4839
|
Ye X, Chen T, Hu D, et al. 2009. A multifunctional HTDMA system with a robust temperature control[J]. Advances in Atmospheric Sciences, 26(6): 1235–1240.
DOI:10.1007/s00376-009-8134-3
|
Zhang R, Khalizov A, Wang L, et al. 2012. Nucleation and growth of nanoparticles in the atmosphere[J]. Chemical Reviews, 112(3): 1957–2011.
DOI:10.1021/cr2001756
|
郑晓宏, 胡长进, 潘刚, 等. 2012. 苯乙烯-臭氧暗反应生成二次有机气溶胶的吸湿性[J]. 大气与环境光学学报, 2012, 7(4): 254–262.
DOI:10.3969/j.issn.1673-6141.2012.04.003 |
 2019, Vol. 39
2019, Vol. 39


