植物源挥发性有机物(Biogenic volatile organic compounds, BVOCs)是植物通过次生代谢途径合成的低沸点、易挥发小分子化合物.BVOCs种类繁多, 以异戊二烯(Isoprene, C5H8)和单萜烯(Monoterpene, C10H16)为主, 分别占总BVOCs的50%和15%(Guenther et al., 2012).全球每年BVOCs释放量约为1150 Tg(以C计)(Guenther et al., 1995; Guenther et al., 2012), 占VOCs总释放量的90%(Calfapietra et al., 2013).BVOCs释放量大且反应活性高, 可以改变大气的气体组成, 从而影响城市大气环境.一方面, 城市区域氮氧化物(Nitrogen oxides, NOx)含量较高, 在光照条件下BVOCs与NOx通过一系列反应, 在对流层产生大量的臭氧(Sanford et al., 1990; Calfapietra et al., 2013); 李用宇等(2013)和安俊琳等(2013)分别研究南京北郊VOCs的光化学特征和体积分数发现, 烯类物质对臭氧生成的贡献最大.另一方面, BVOCs经大气氧化和气/粒分配等过程而生成二次有机气溶胶(Secondary organic aerosol, SOA)悬浮于大气中(Hallquist et al., 2009), SOA是大气中细颗粒物的重要组成部分, 对灰霾的形成影响重大(郑玫等, 2014).
绿色植物是城市生态系统的重要组成部分, 具有维持城市碳氧平衡、蒸腾吸热、净化空气和降低城市噪音等的生态效应而备受人们的重视(苏泳娴等, 2011).然而不同植物释放的BVOCs存在着一定差异, 将释放量较高的树种栽植在城区同样会影响大气环境.Willis等(2017)研究表明, 在城市中种植黑紫树、杨树、橡树、洋槐、梧桐、枫木等会导致城区BVOCs浓度升高, 不仅无法带来预期的生态效益反而使得治理人为源挥发性有机物的成果被抵消.目前关于城市绿色植物释放BVOCs的研究主要集中在其成分及相对含量、树种差异等方面.武利玉等(2014)研究表明, 夹竹桃、万年青、变叶木3种典型绿色植物主要释放烷烃、烯烃、醛类和芳香烃.Matsunaga等(2017)调查东京市区常见的29种行道树, 发现有18种树木大量释放BVOCs(异戊二烯、α-蒎烯和柠檬烯为主).
随着城市化进程的加快, 人们对生存环境的生态质量要求不断提高, 城市绿地的面积逐年增加.Ren等(2017)指出, 由于城区面积的扩大, 预计2050年BVOCs释放量将会达到现在的3倍.在城市中, 绿色植物受到诸多因素的影响, 释放的BVOCs较多, 对城市环境造成的影响可能更为深远.一方面, 城市环境以水泥结构为主, 土壤养分贫瘠、旱涝不均、根系生长空间小等严苛的生存条件都会对绿色植物产生一定的损害, 应激产生更多的BVOCs(Ghirardo et al., 2016).另一方面, 城市环境因子(温度、光照)的改变, 同样也会影响绿色植物释放BVOCs(胡春芳等, 2018).由于“热岛效应”, 城区温度通常比周围郊区高10 ℃左右(Peng et al., 2012), 这将会导致植物释放的BVOCs在一定范围内大幅增加(Guenther et al., 1993); 此外, 随着政府对大气颗粒物的治理逐见成效, 太阳辐射增强、光照强度增大, 光照成为影响城市环境的另一个重要因子.而光照改变势必影响植物光合参数(Perry et al., 1986), 从而影响着植物BVOCs的释放(Guenther et al., 1991; 邹宇等, 2015; Van Meeningen et al., 2017).城市环境的胁迫将会使得绿色植物释放更多BVOCs, 进而加剧臭氧和SOA的生成, 影响城市大气环境.
现阶段关于温度、光照对植物BVOCs释放的影响研究主要集中在森林植物, 而关于绿色植物的研究较少.因此, 在全球气候变化和新时代建设美丽中国的战略部署, 以及“推进生态文明先行示范区建设, 努力建设美丽福建”的大背景下, 以福建省常见绿化树种为研究对象进行室内模拟, 探究当前城市重要环境因子(温度、光照)的变化对绿化树种释放主要BVOCs(异戊二烯、单萜烯)的影响, 可为城市绿化选择树种提供一定参考依据, 并对城市生态环境改善具有重要的现实意义.
2 材料与方法(Materials and methods) 2.1 实验设计以2年龄福建省常见城市绿色植物红花檵木(Loropetalum chinense)、南天竹(Nandina domestica)为研究对象, 二者均为常绿小灌木.植物盆栽3个月后, 选取4棵长势良好且基本一致的植株, 利用人工气候箱进行控温、控光处理.分别设置3个温度(25、30、35 ℃), 光合有效辐射(Photosynthetically active radiation, PAR)控制为500 μmol · m-2 · s-1(距离LED灯板15 cm处, 下同), 3个光照梯度(PAR分别为0、500、1000 μmol · m-2 · s-1, 温度控制为30 ℃).在气候箱预培养1 d后进行样品采集.
2.2 样品采集与分析使用动态箱法采集植物释放气体样品(张倩等, 2018).具体如下:将植物用特氟龙袋(Teflon, 体积70 L)罩住地上部分, 尽量避免损伤植物, 通入去除VOCs等杂质的洁净空气(流速9 L · min-1), 并打开Teflon材质小风扇混匀空气; 稳定30 min后, 用PCXR8通用型采样泵(美国SKC公司)以500 mL · min-1的流速收集气体于容积为2 L的Tedlar袋中, 采样时间2 min, 随后避光保存并尽快上机进行分析.同时采集无植物空白对照气体样品.使用Gsome HQ-WS211温湿度记录仪(杭州尽享科技有限公司)动态箱中温湿度; 使用F3-CO2红外分析仪(德国SmartGas公司)进行CO2的实时监测; 使用MQ-500光量子记录仪(美国Apogee公司)测量光合有效辐射; 用CI-203叶面积仪(美国CID公司)测量供试植物的叶面积.
气体样品使用Entech-7200预浓缩和Agilent 7890B/5977A GC-MS联用仪进行分析.气体样品经三级液氮冷阱除去H2O和CO2后, 经-150 ℃冷聚焦进入GC-MS分离检测.选用HP-1色谱柱(60 m × 250 μm×0.32 μm), 设置初始温度10 ℃, 保持3 min, 后以5 ℃ · min-1升到120 ℃, 再以10 ℃ · min-1升温至250 ℃, 保持7 min.质谱选择EI电离源, 电离电压为70 eV, 离子源温度270 ℃, 数据采集采用单扫模式(SIM).以广州地球化学研究所Std 16为标样, 采用标准质谱图库(NIST14)标准气体保留时间双重条件定性化合物, 具体参照文献(张丽丽等, 2017).
2.3 数据分析采用峰面积-释放通量标准曲线内标法定量, 计算各化合物浓度(异戊二烯、α-蒎烯、β-蒎烯、α-松油烯、γ-松油烯、柠檬烯和3-蒈烯, 本研究中此7种化合物总和为BVOCs), 并根据以下公式计算各化合物的释放通量:
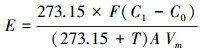
|
(1) |
式中, E表示植物不同BVOCs种类的释放速率(pmol · m-2 · s-1); C1、C0分别表示样品和空白动态箱中BVOCs的体积分数(10-9); F表示动态箱流量(mL · min-1); A表示叶面积(m2); Vm表示标准状况下1 mol气体体积为22.4 L.
光合参数(净光合速率、气孔导度、胞间CO2和蒸腾速率)通过样品和空白动态箱中的H2O和CO2体积分数差进行换算(Huang et al., 2018).使用Excel整合基础数据, 差异显著性用SPSS18.0进行单因素方差(one-way ANOVA)、LSD多重检验法检验和独立样本t检验, 显著性水平为p < 0.05, 植物BVOCs释放与光合参数进行spearman相关性分析.使用SigmaPlot 12.5作图.
3 结果(Results) 3.1 温度对绿色植物主要BVOCs及光合参数的影响在光照强度为500 μmol · m-2 · s-1时, 不同温度处理下两种绿色植物都以释放异戊二烯为主, 单萜烯的释放较小(图 1), 整体而言南天竹释放的BVOCs大于红花檵木(表 1).随着温度增加, 红花檵木和南天竹异戊二烯的释放迅速增加, 且在35 ℃达到最大, 分别为(8436.48±2322.94)和(15138.81±3038.18) pmol · m-2 · s-1.而温度对单萜烯的影响因植物而异(图 1), 红花檵木在30 ℃时释放通量显著高于25 ℃和35 ℃的通量(p < 0.05), 达到(4.69±2.23) pmol · m-2 · s-1; 南天竹单萜烯释放随温度变化差异不显著(p>0.05).
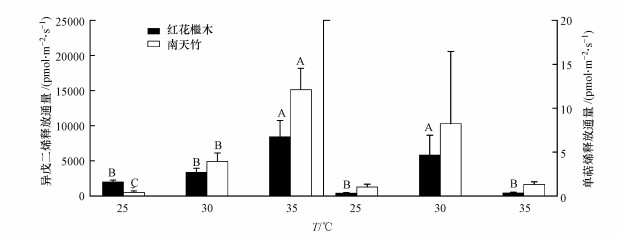 |
| 图 1 温度变化对植物异戊二烯和单萜烯释放的影响 (平均值±标准差; n=4;不同字母表示同种植物不同温度间差异显著(p < 0.05)) Fig. 1 Effect of temperature change on isoprene and monoterpene emission in green plants |
| 表 1 不同处理下植物总BVOCs释放速率 Table 1 Total BVOC emission rates of the two plants in different treatments |
不同温度条件下, 两种植物释放的单萜烯都以α-蒎烯、3-蒈烯和β-蒎烯为主(图 2).各处理下, 两种植物释放α-蒎烯的相对含量均高于3-蒈烯和β-蒎烯.随着温度增加, 红花檵木的α-蒎烯相对含量降低, 从54.0%下降到39.0%;而3-蒈烯的相对含量先升高后降低.南天竹α-蒎烯的相对含量先降低后升高, 而3-蒈烯和β-蒎烯的变化与之呈现相反规律, 柠檬烯无明显变化.
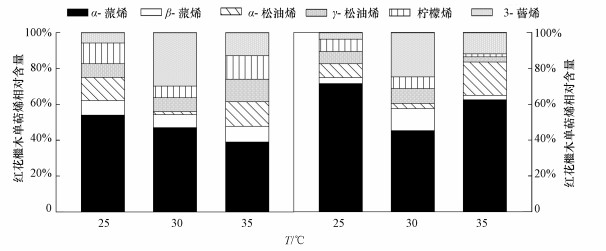 |
| 图 2 温度变化对单萜烯组成的影响 Fig. 2 Effect of temperature change on the composition of monoterpenes |
温度影响植物光合参数, 且不同植物对温度的响应不一致(图 3).在500 μmol · m-2 · s-1时, 南天竹和红花檵木的气孔导度和蒸腾速率随温度增加而增大, 且在35 ℃时高于25 ℃(p < 0.05).南天竹净光合速率先降低后升高, 在30 ℃时显著低于35 ℃时(p < 0.05).两种绿色植物胞间二氧化碳随温度变化无显著差异(p>0.05).不同温度条件下, 南天竹的蒸腾速率均显著(p < 0.05)高于红花檵木.
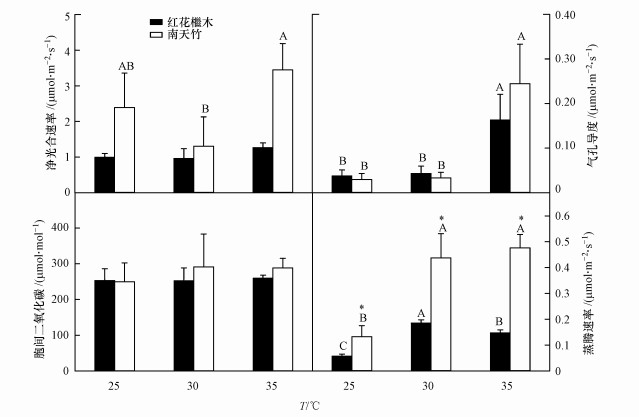 |
| 图 3 温度变化对绿色植物光合参数的影响 (平均值±标准差; n=4;不同字母表示同种植物不同温度间差异显著(p < 0.05);*表示在同一处理下不同植物差异显著(p < 0.05)) Fig. 3 Effect of temperature change on photosynthetic parameters of green plant |
红花檵木和南天竹在黑暗条件下只释放少量异戊二烯, 其通量随光照增强显著增加(图 4), 在1000 μmol · m-2 · s-1时达到最大, 分别为(3279.21±1178.23) pmol · m-2 · s-1和(7355.17±1662.35) pmol · m-2 · s-1.整体而言不同光照下南天竹释放BVOCs通量大于红花檵木(表 1), 其中, 南天竹在1000 μmol · m-2 · s-1条件下释放通量显著高于500 μmol · m-2 · s-1时.两种植物单萜烯释放显著低于异戊二烯的释放, 通量约为0.33~8.24 pmol · m-2 · s-1.红花檵木在500 μmol · m-2 · s-1时通量显著高于其他光照处理时, 而南天竹在不同光照处理间无显著差异(p>0.05).
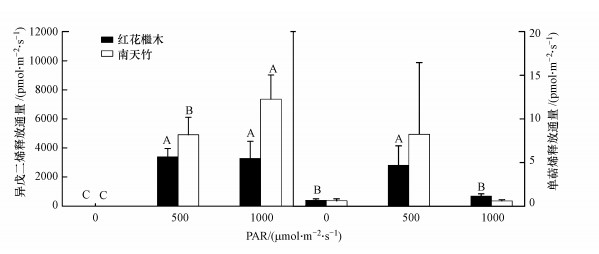 |
| 图 4 光照变化对植物异戊二烯和单萜烯释放的影响 (平均值±标准差; n=4;不同字母表示同种植物不同光照间差异显著(p < 0.05)) Fig. 4 Effect of light change on isoprene and monoterpene emission in green plants |
在30 ℃时, 不同光照条件下红花檵木和南天竹释放的单萜烯以α-蒎烯和3-蒈烯为主(图 5).红花檵木释放的α-蒎烯和柠檬烯相对含量随光照增强逐渐下降, 前者从59.3%下降到15.8%, 后者从16.6%下降到2.9%;3-蒈烯则逐渐升高, 从2.7%升高到71.3%;其他化合物含量无明显变化.南天竹α-蒎烯的相对含量随光照增强先上升后下降, α-松油烯反之; 3-蒈烯逐渐升高, γ-松油烯逐渐降低; β-蒎烯和柠檬烯无明显变化.
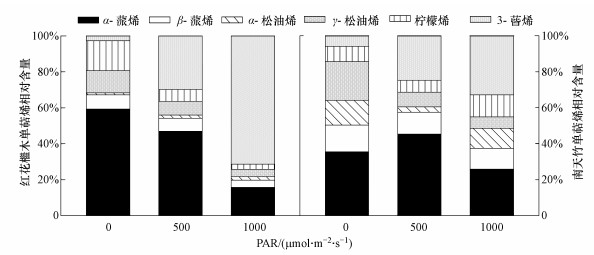 |
| 图 5 光照变化对单萜烯组成的影响 Fig. 5 Effect of light change on the composition of monoterpenes |
光照影响植物光合参数(图 6).在30 ℃时, 随光照条件升高, 红花檵木和南天竹的净光合速率和蒸腾速率逐渐升高, 胞间二氧化碳浓度逐渐降低, 且在0 μmol · m-2 · s-1和1000 μmol · m-2 · s-1处理下都具有显著的差异, 气孔导度随光照变化无明显差异(p>0.05).在0 μmol · m-2 · s-1和1000 μmol · m-2 · s-1处理下, 南天竹的净光合速率和蒸腾速率显著高于红花檵木(p < 0.05).
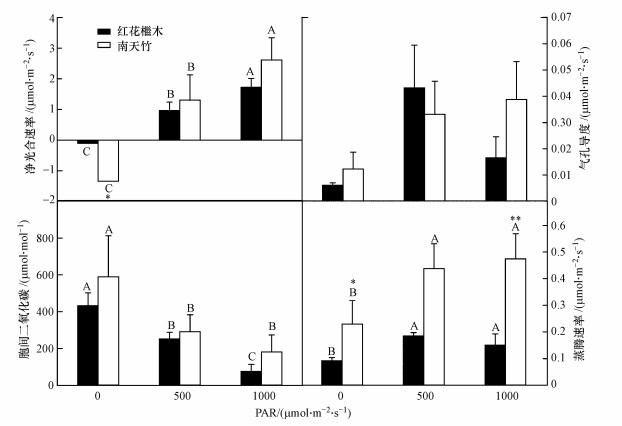 |
| 图 6 光照变化对绿色植物光合参数的影响 (平均值±标准差; n=4;不同字母表示在同种植物不同光照之间差异显著(p < 0.05);*表示在不同植物间差异显著(p < 0.05);**表示在不同植物间差异极显著(p < 0.01)) Fig. 6 Effect of light change on photosynthetic parameters of green plants |
本实验中两种绿色植物(红花檵木和南天竹)异戊二烯和单萜烯的释放通量在一定范围内随温度升高呈增大趋势(图 1), 这与Guenther等(1993)报道的植物对温度的响应相吻合.宁平等(2013)指出植物BVOCs的释放依赖于温度.Lindwall等(2016)研究也表明气候变暖使极地沼泽BVOCs释放量增加, 当温度升高1.3~1.6 ℃时, 植物异戊二烯释放增幅达240%~380%.这可能是由于植物通过释放异戊二烯用于提高其对高温的耐受性, 从而保护植物自身(Sharkey et al., 1995).植物异戊二烯是由二甲基烯丙基二磷酸(DMAPP)在叶绿体中通过异戊二烯合成酶催化形成的(Silver et al., 1991), 而温度升高能够提升其合成酶的活性, 进而导致两种绿化树种异戊二烯的释放随温度升高而升高(图 1).温度变化同样影响着单萜烯的合成酶活性(Fischbach et al., 2000), 使得两种绿色植物的释放通量均在30 ℃显著升高(图 1).也有研究认为温度可以通过影响单萜烯的挥发性从而影响其释放量(Calfapietra et al., 2013).
通过分析两种绿色植物释放BVOCs的通量与其光合参数关系(表 2), 发现二者之间存在多组显著相关关系(p < 0.05), 可见植物BVOCs的释放与其光合作用息息相关.有研究表明, 合成异戊二烯所需碳源主要来自于近期光合作用固定的碳(Monson et al., 1989).Guidolotti等(2011)研究10种基因型的杨树发现用于合成异戊二烯的碳占光合作用固定碳的0.55%~1.30%.本实验中红花檵木随着温度升高异戊二烯通量占净光合速率百分比从1.01%上升到1.88%, 南天竹从0.13%上升到2.24%(表 3).光合作用会影响叶绿体内DMAPP浓度, 而异戊二烯合成酶的活性受DMAPP浓度控制(Silver et al., 1991).因此, 改变温度强度能间接控制异戊二烯合成酶的活性, 从而改变异戊二烯释放速率.温度升高, 两种植物异戊二烯通量随着气孔导度和蒸腾速率增加而升高, 红花檵木的单萜烯释放变化规律与其蒸腾速率一致(图 1、图 3).气孔是植物与大气进行气体交换的通道(Hetherington et al., 2003), 气孔导度升高有利于异戊二烯和单萜烯的逸出.综上, 温度的变化可以通过影响植物光合作用的效率来改变BVOCs释放.
| 表 2 红花檵木和南天竹主要BVOCs释放速率与其光合参数相关性分析 Table 2 Correlation analysis of the main BVOC emission rates and photosynthetic parameters of L. chinense and N. domestica |
| 表 3 异戊二烯占光合作用固定碳百分比 Table 3 Isoprene as a percentage of fixed carbon in photosynthesis |
红花檵木和南天竹释放的异戊二烯受到光照的影响较为明显, 与Guenther等(1991)的研究结果相一致.分析异戊二烯和光合参数的变化, 发现二者存在相似规律:当异戊二烯在光照条件为0 μmol · m-2 · s-1时几乎没有释放, 相应的净光合速率为负值, 远低于其它光照条件时(p < 0.05, 图 4和6).光照增强可以促进光合作用, 净光合速率升高使得异戊二烯的合成获得充足碳源, 气孔导度和蒸腾速率的提升进一步促进了异戊二烯的释放(Meeningen et al., 2016; Yuan et al., 2016).邹宇等(2015)研究广州异戊二烯日变化发现在光照最强的中午时段, 异戊二烯释放通量最大; Rosenstiel等(2002)研究植物释放异戊二烯日变化也发现, 中午植物叶绿体中DMAPP含量上升到65%~70%;Silver等(1991)认为光照可以改变叶绿体基质中的Mg2+和pH值, 激活DMAPP合成酶, 导致DMAPP浓度升高.本实验中红花檵木和南天竹异戊二烯对光照的响应可能是由于异戊二烯合成底物与相应酶活性受到光照积极影响的结果.本实验中, 红花檵木随光照增强异戊二烯通量占净光合速率百分比从0增长到2.20%, 南天竹增长到1.91%(表 3), 可见光照可以通过释放异戊二烯影响植物的碳分配过程.
一般认为光照强度对单萜类化合物合成、释放的影响不大(Leung et al., 2010).而在本实验中, 两种植物释放的单萜烯在光照条件改变下均呈现先升高后下降的态势(图 4), 进一步分析其单萜烯的组分变化发现其3-蒈烯有着一定的光依赖性(图 5), 这与Van Meeningen等(2017)研究英国橡属和欧洲山毛榉得出随着光照增强, 3-蒈烯的相对含量逐步上升相一致.
5 结论(Conclusions)1) 两种城市绿化树种(红花檵木和南天竹)都是以释放异戊二烯为主, 而单萜烯的释放量相对较少.红花檵木的BVOCs释放速率低于南天竹.作为城市环境的重要因子, 温度和光照能够通过影响植物光合参数(净光合速率、气孔导度和蒸腾速率)促进异戊二烯的释放, 而单萜烯的通量先增加后减少.红花檵木和南天竹释放的单萜烯以α-蒎烯和3-蒈烯为主.两种植物3-蒈烯相对含量随温度升高先升高后降低, 随光照升高而升高.植物释放异戊二烯碳量占光合作用固定碳随着温度和光照的增加而增加.
2) 不同植物BVOCs释放速率差异较大, 且不同植物BVOCs释放对温度和光照变化的响应也有较大的差异.考虑到BVOCs对城市大气臭氧生成的贡献, 以及城市温度和光照的增加, 有必要加强对城市绿化树种BVOCs释放对环境因子的响应, 以便为城市绿化树种选择及城市生态环境改善提供参考依据.责任作者简介:易志刚, 教授、博士生导师, 主要研究方向为痕量气体界面交换、有机污染物生物地球化学循环.在国内外核心期刊上发表论文40余篇, 其中SCI期刊收录11篇.
Calfapietra C, Fares S, Manes F, et al. 2013. Role of Biogenic Volatile Organic Compounds (BVOC) emitted by urban trees on ozone concentration in cities:A review[J]. Environmental Pollution, 183: 71–80.
DOI:10.1016/j.envpol.2013.03.012
|
Fischbach R J, Zimmer I, Steinbrecher R, et al. 2000. Monoterpene synthase activities in leaves of Picea abies (L.) Karst. and Quercus ilex L[J]. Phytochemistry, 54(3): 257–265.
DOI:10.1016/S0031-9422(00)00119-9
|
Ghirardo A, Xie J, Zheng X, et al. 2016. Urban stress-induced biogenic VOC emissions and SOA-forming potentials in Beijing[J]. Atmospheric Chemistry & Physics, 16(5): 2901–2920.
|
Guenther A, Hewitt C N, Erickson D, et al. 1995. A global model of natural volatile organic compound emissions[J]. Journal of Geophysical Research:Atmospheres, 100(D5): 8873–8892.
DOI:10.1029/94JD02950
|
Guenther A B, Jiang X, Heald C L, et al. 2012. The Model of Emissions of Gases and Aerosols from Nature version 2.1 (MEGAN2.1):an extended and updated framework for modeling biogenic emissions[J]. Geosci. Model Dev., 5(6): 1471–1492.
DOI:10.5194/gmd-5-1471-2012
|
Guenther A B, Monson R K, Fall R. 1991. Isoprene and monoterpene emission rate variability:Observations with eucalyptus and emission rate algorithm development[J]. Journal of Geophysical Research, 96(D6): 10799–10808.
DOI:10.1029/91JD00960
|
Guenther A B, Zimmerman P R, Harley P C, et al. 1993. Isoprene and monoterpene emission rate variability:Model evaluations and sensitivity analyses[J]. Journal of Geophysical Research Atmospheres, 98(D7): 12609–12617.
DOI:10.1029/93JD00527
|
Guidolotti G, Calfapietra C, Loreto F. 2011. The relationship between isoprene emission, CO2 assimilation and water use efficiency across a range of poplar genotypes[J]. Physiologia Plantarum, 142(3): 297–304.
DOI:10.1111/j.1399-3054.2011.01463.x
|
Hallquist M, Wenger J C, Baltensperger U, et al. 2009. The formation, properties and impact of secondary organic aerosol:current and emerging issues[J]. Atmospheric Chemistry and Physics, 9(14): 5155–5236.
DOI:10.5194/acp-9-5155-2009
|
Hetherington A M, Woodward F I. 2003. The role of stomata in sensing and driving environmental change[J]. Nature, 424: 901–908.
DOI:10.1038/nature01843
|
Huang J, Hartmann H, Hellén H, et al. 2018. New perspectives on CO2, temperature, and light effects on BVOC emissions using online measurements by PTR-MS and Cavity Ring-Down spectroscopy[J]. Environmental Science and Technology, 52(23): 13811–13823.
DOI:10.1021/acs.est.8b01435
|
Leung D Y C, Wong P, Cheung B K H, et al. 2010. Improved land cover and emission factors for modeling biogenic volatile organic compounds emissions from Hong Kong[J]. Atmospheric Environment, 44(11): 1456–1468.
DOI:10.1016/j.atmosenv.2010.01.012
|
Lindwall F, Svendsen S S, Nielsen C S, et al. 2016. Warming increases isoprene emissions from an arctic fen[J]. Science of the Total Environment, 553: 297–304.
DOI:10.1016/j.scitotenv.2016.02.111
|
Matsunaga S N, Shimada K, Masuda T, et al. 2017. Emission of Biogenic Volatile Organic Compounds from trees along streets and in urban parks in Tokyo, Japan[J]. Asian Journal of Atmospheric Environment, 11(1): 29–32.
DOI:10.5572/ajae.2017.11.1.029
|
Meeningen Y V, Schurgers G, Rinnan R, et al. 2016. BVOC emissions from English oak (Quercus robur) and European beech (Fagus sylvatica) along a latitudinal gradient[J]. Biogeosciences Discussions, 13(21): 1–30.
|
Monson R K, Fall R. 1989. Isoprene emission from aspen leaves:Influence of environment and relation to photosynthesis and photorespiration[J]. Plant Physiology, 90(1): 267–274.
DOI:10.1104/pp.90.1.267
|
Peng S, Piao S, Ciais P, et al. 2012. Surface Urban Heat Island Across 419 Global Big Cities[J]. Environmental Science & Technology, 46(2): 696–703.
|
Perry M H, Friend D J C, Yamamoto H Y. 1986. Photosynthetic and leaf morphological characteristics in Leucaena leucocephala as affected by growth under different neutral shade levels[J]. Photosynthesis Research, 9(3): 305–316.
|
Ren Y, Qu Z, Du Y, et al. 2017. Air quality and health effects of biogenic volatile organic compounds emissions from urban green spaces and the mitigation strategies[J]. Environmental Pollution, 230: 849–861.
DOI:10.1016/j.envpol.2017.06.049
|
Rosenstiel T N, Fisher A J, Ray F, et al. 2002. Differential accumulation of dimethylallyl diphosphate in leaves and needles of isoprene- and methylbutenol-emitting and nonemitting species[J]. Plant Physiology, 129(3): 1276–1284.
DOI:10.1104/pp.002717
|
Sanford S, Logan J A, Wofsy S C. 1990. The sensitivity of ozone to nitrogen oxides and hydrocarbons in regional ozone episodes[J]. Journal of Geophysical Research Atmospheres, 95(D2): 1837–1851.
DOI:10.1029/JD095iD02p01837
|
Sharkey T D, Singsaas E L. 1995. Why plants emit isoprene[J]. Nature, 374: 769.
|
Silver G M, Fall R. 1991. Enzymatic synthesis of isoprene from dimethylallyl diphosphate in Aspen leaf extracts[J]. Plant Physiology, 97(4): 1588–1591.
DOI:10.1104/pp.97.4.1588
|
Van Meeningen Y, Schurgers G, Rinnan R, et al. 2017. Isoprenoid emission response to changing light conditions of English oak, European beech and Norway spruce[J]. Biogeosciences, 14(18): 4045–4060.
DOI:10.5194/bg-14-4045-2017
|
Willis K J, Petrokofsky G. 2017. The natural capital of city trees[J]. Science, 356(6336): 374–376.
DOI:10.1126/science.aam9724
|
Yuan X, Calatayud V, Gao F, et al. 2016. Interaction of drought and ozone exposure on isoprene emission from extensively cultivated poplar[J]. Plant, Cell & Environment, 39(10): 2276–2287.
|
安俊琳, 朱彬, 李用宇. 2013. 南京北郊大气VOCs体积分数变化特征[J]. 环境科学, 2013, 34(12): 4504–4512.
|
胡春芳, 袁相洋, 田媛, 等. 2018. 常见花卉植物释放挥发性有机化合物的研究进展[J]. 生态学杂志, 2018, 37(2): 588–595.
|
花圣卓, 陈俊刚, 余新晓, 等. 2016. 温带典型森林树种的萜烯类化合物排放及其与环境要素的相关性[J]. 林业科学, 2016, 52(11): 19–28.
DOI:10.11707/j.1001-7488.20161103 |
李用宇, 朱彬, 安俊琳, 等. 2013. 南京北郊秋季VOCs及其光化学特征观测研究[J]. 环境科学, 2013, 34(8): 2933–2942.
|
宁平, 郭霞, 田森林, 等. 2013. 昆明地区典型乔木主要挥发性有机物释放规律[J]. 中南大学学报(自然科学版), 2013, 44(3): 1290–1296.
|
苏泳娴, 黄光庆, 陈修治, 等. 2011. 城市绿地的生态环境效应研究进展[J]. 生态学报, 2011, 31(23): 302–315.
|
武利玉, 孙迎雪, 田媛, 等. 2014. 北京市典型绿地花卉植物BVOCs释放成分谱研究[J]. 环境科学与技术, 2014, 37(10): 154–158.
|
张丽丽, 印亮, 郑丽丽, 等. 2017. 模拟氮沉降对鼎湖山典型森林地表烷烃、烯烃通量的影响[J]. 生态学杂志, 2017, 36(12): 3462–3469.
|
张倩, 李洪远, 贺梦璇, 等. 2018. 天津市常用绿化树种挥发性有机物排放潜力估算[J]. 环境科学研究, 2018, 31(2): 245–253.
|
郑玫, 闫才青, 李小滢, 等. 2014. 二次有机气溶胶估算方法研究进展[J]. 中国环境科学, 2014, 34(3): 555–564.
|
邹宇, 邓雪娇, 李菲, 等. 2015. 广州大气中异戊二烯浓度变化特征、化学活性和来源分析[J]. 环境科学学报, 2015, 35(3): 647–655.
|
 2019, Vol. 39
2019, Vol. 39


