染料废水处理是国内外环境工程领域学者关注和研究的重要方向.除生物法外, 用于染料废水处理的方法目前主要涵盖以膜过滤(如纳滤、反渗透、电渗析)和吸附为主的物理分离技术及以混凝、零价铁和高级氧化法(如光催化、臭氧、Fenton氧化)为主的化学方法(陈银生等, 2001).然而, 这些方法普遍存在效率低、造价高、二次污染等问题, 限制了其在印染工业废水处理中的工程应用和推广.
近年来, 电化学氧化法在处理难降解有机废水领域以其高效、操作灵活、集成化程度高等优点受到广泛关注(Martinez-Huitle et al., 2015).除了直接电子转移氧化反应外, 还能通过电解产生的羟基自由基(·OH)、活性氯等高活性物质氧化降解机污染物, 这主要取决于电极的性质;此外, 大量研究证实, 有机污染物在电化学体系中的氧化效率主要受控于传质过程(Chaplin, 2014; Martinez-Huitle et al., 2015).因此, 寻求高效稳定的电极材料并强化界面传质是实现电化学氧化废水处理工程化应用的重要方向.
最近, 以TiO2半导体为原材料制备的亚氧化钛TinO2n-1(4≤n≤10, TiSO)电极在电化学氧化、化学电源、阴极保护等领域展现出巨大的发展潜力(Graves et al., 1991; Stoyanova et al., 2010; Walsh et al., 2010; Zaky et al., 2013; Guo et al., 2016; You et al., 2016; Teng et al., 2020).亚氧化钛结构中每隔n层有一个氧原子的缺失, 使TiO2在八面体晶格中形成共用的剪切面来弥补氧原子的缺失(Smith et al., 1998).其中, Ti4O7 (n=4, 即EbonexⓇ)具有良好的导电性(1500 S·cm-1)(Walsh et al., 2010)、高析氧电位(2.6 V vs SHE)(Chen et al., 1999)和优异的耐腐蚀性能.这些独特的性质意味着Ti4O7阳极有可能作为一种新的惰性电极材料实现有机物的氧化降解.
对于电极来说, 高析氧电位是保证产生·OH而避免氧析出的必要条件.由于·OH氧化性强、寿命短, 仅存在于电极表面微米甚至是纳米级的边界层内(Kapałka et al., 2009; Pei et al., 2019), 因此, 反应物向这一薄层的传质是电化学氧化过程的速控步骤.传统的电化学氧化体系大多采用与电极平行的旁流式操作, 传质效率低、反应速率慢、处理能耗和成本高.最近的研究发现, 穿流式膜电极(ME)可以将扩散层厚度从100 μm显著降低至1 μm(Chaplin, 2014), 有效打破了旁流式操作传质限制的桎梏, 实现了在极短的水力停留时间内污染物的降解甚至矿化(停留时间 < 5 s;Zaky et al., 2013; Guo et al., 2016; Gayen et al., 2018), 极大地提升了电化学氧化效能.然而, 迄今为止报道的膜电极均以模拟污染物为去除目标, 而对于实际产生的工业废水处理给予的关注很少.事实上, 实际工业废水中的有机物成分复杂, 无机离子浓度高, 在阳极放电与水分子发生竞争, 有可能对污染物的氧化降解机制和效能产生未知的影响.
本课题组在之前的工作中对亚氧化钛电极进行了大量的基础和应用研究(You et al., 2016; Gao et al., 2018; Teng et al., 2018; Liu et al., 2019; Pei et al., 2019; 2020; Teng et al., 2020; Ma et al., 2020).在此基础上, 本文进一步报道亚氧化钛膜电极(TiSO-ME)的电化学特性及其处理实际印染工业废水的效能.首先, 对TiSO-ME的组成和孔结构进行表征;其次, 考察TiSO-ME的电化学活性面积、析氧电位和极限寿命;最后, 评价不同电流密度和膜通量条件下TiSO-ME处理印染废水过程中的效率和能耗.
2 材料与方法(Materials and methods) 2.1 TiSO-ME电极制备与表征本研究所使用的TiSO-ME电极由Ti-Dynamics公司提供.简言之, 电极由金红石型TiO2粉末在1050 ℃的高温H2氛围下还原4 h制得.电极的微观形貌、晶体结构、孔径分布分别采用扫描电子显微镜(SEM, Helios Nanolab600i, FEI, 美国)、X射线衍射仪(XRD, Bruke D8 Adv., 德国)和压汞仪(Micromeritics Autopore IV 9520, 美国)进行分析.利用电化学工作站(CHI 750D, 上海辰华有限公司)在三电极体系中对TiSO-ME电极于0.5 mol·L-1 NaClO4电解液中进行循环伏安曲线(CV)、线性扫描伏安测试(LSV)、交流阻抗曲线(EIS)及强酸环境下的加速测试(3 mol·L-1 H2SO4, 1 A·cm-2, 30 ℃), 以便分析电极的电化学活性面积、析氧电位、电阻分布及使用寿命.在三电极体系中, TiSO-ME为工作电极, 不锈钢片为对电极, Ag/AgCl为参比电极(0.195 V vs SHE).
2.2 印染工业废水来源及水质实际印染工业废水取自杭州市萧山区某化工园区(主要为印染废水)的二沉池出水, 主要的水质参数见表 1.可见, 废水经过生物处理后TOC和COD指标仍无法达到间接排放标准, BOD5/COD值仅为0.029, 说明可生化性极差.
| 表 1 实际印染工业废水主要水质参数 Table 1 Parameters of dominant water quality for collected dyeing wastewater |
电化学氧化反应装置主要由TiSO-ME阳极(高为7.7 cm, 直径为2.8 cm, 有效表面积为67.5 cm2)、不锈钢阴极(8 cm×15 cm)、直流电源(0~30 V, 0~3 A)和蠕动泵等部分组成, 如图 1所示.在蠕动泵的抽吸作用下, 印染工业废水由外部进入并穿过TiSO-ME后再循环至反应器中.
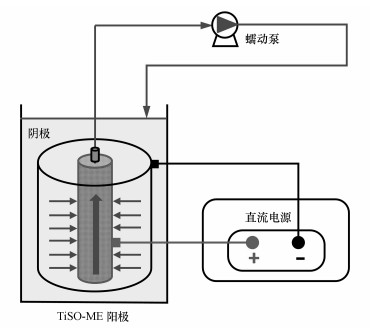 |
| 图 1 穿流式膜电极反应装置图 Fig. 1 Schematic illustration of setup for flow-through operation of membrane electrode |
传质速率常数采用Fe(CN)63-/4-为氧化还原电对进行测试并根据极限电流进行计算(式(1)).电极的粗糙度和在特定电流密度下的工作年限可分别由公式(2)(You et al., 2016)和(3)(Hine et al., 1979)进行估算.
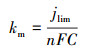
|
(1) |
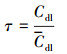
|
(2) |
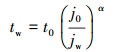
|
(3) |
式中, jlim为极限电流密度(mA·cm-2), n为电子转移数, C为Fe(CN)64-的初始浓度(mol·L-1), τ为电极粗糙度, Cdl和dl分别为分析得到的比电极双电层电容(F·cm-2)和平均比双电层电容(60 μF·cm-2)(Regonini et al., 2011), t0和tw分别为电极在电流密度为j0(mA·cm-2)测试时的稳定时间(h)和电极在电流密度为jw(mA·cm-2)工作时的稳定时间(h), α为1.4~2.0的无量纲常数.
溶解性有机碳(DOC)和溶解性化学需氧量(sCOD)分别在使用0.45 μm醋酸纤维膜过滤后采用总有机碳分析仪(Shimadzu VSCN8, 日本)和重铬酸钾法进行定量分析.sCOD的去除率(RsCOD)及基于sCOD去除的库伦效率(CEsCOD)和能耗W(kWh·g-1)根据下式进行计算:
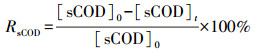
|
(4) |
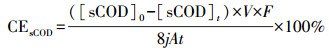
|
(5) |
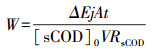
|
(6) |
式中, [sCOD]0、[sCOD]t分别为sCOD在初始时刻和电解t(min)后的浓度(mg·L-1), V为废水的体积(m3), F为法拉第常数, 取值为96485 C·mol-1, j为电流密度(mA·cm-2), A为阳极面积(cm2), △E为反应时间内的平均电压值(V).
3 TiSO-ME的结构特征与电化学性质(Structural and Electrochemical Properties of TiSO-ME) 3.1 TiSO-ME结构表征从XRD图(图 2a)可以看出, TiSO电极的主要物相组成为Ti4O7, 衍射角2θ分别为20.71°、25.43°、28.56°、31.71°的衍射峰与标准图谱中Ti4O7 (10-2)、(-1-11)、(02-2)、(10-4)晶面的特征衍射峰(Graves et al., 1991)所报道的衍射角一致, 此外, 还观察到有少量Ti5O9(021)、(11-4)、(1-32)晶面的衍射峰存在.从SEM图(图 2b)观察到, TiSO电极表面凹凸不平, 颗粒呈现不规则的形状分布, 有明显的烧结团聚现象, 使得电极的颗粒粒径增大, 表面孔径尺寸基本分布在0.5~2 μm范围内.烧结熔融现象在一定程度上使颗粒间相互粘结, 形成丰富的孔结构, 这种结构有利于污染物在孔内部的传质过程(王愚, 2016).压汞测试结果表明, TiSO电极孔比表面积为0.316 m2·g-1, 平均孔径为0.508 μm, 其中小于1 μm的孔比表面积约占92.7%且均在大孔范围, 其余7.3%的孔径分布在1~3.5 μm范围内(图 2c和图 2d).这样的大孔孔结构意味着电解质溶液可以在较低的外界压力作用下穿过膜电极, 有利于实现膜过滤功能, 达到改善电化学氧化传质效率的目的.
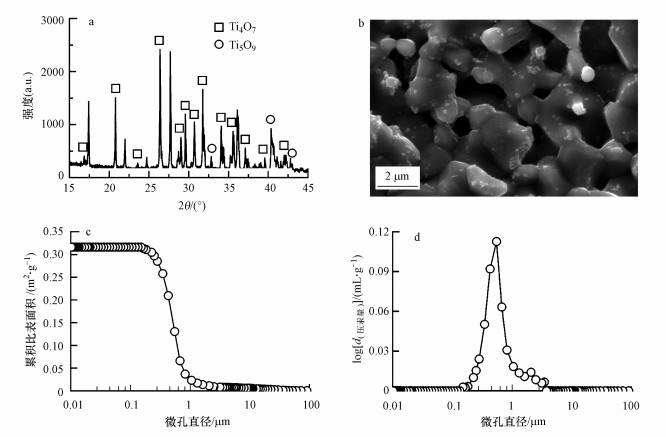 |
| 图 2 TiSO-ME的XRD (a)、SEM (b)、压汞累积孔面积分布(c)和对数微分侵入孔体积分布(d) Fig. 2 XRD pattern(a), SEM image(b), mercury-intrusion cumulative pore area distribution(c), and log differential intrusion pore volume distribution of TiSO-ME(d) |
电极的电化学性质对其废水处理的性能起着决定性的作用.如图 3a所示, TiSO-ME表现出良好的电容特性.当扫描速度从1 mV·s-1增加到15 mV·s-1时, 采用采用循环伏安法计算得到的电极界面双电层电容为0.04 F·cm-2, 与金属氧化物电极的平均双电层电容相比高出近667倍, 依据此方法估算得到TiSO-ME的粗糙度约为667, 这与此前You等(2016)报道的结果一致.这意味着在相同的体积或质量下, 多孔电极的活性表面积是平面电极的667倍, 可为电化学反应提供更大的表面积和数量更多的活性位点.
高析氧电位是电极产生·OH的必要条件, 本研究以石墨电极作为对照来测试TiSO-ME的析氧电位.如图 3b所示, TiSO-ME的析氧电位高达2.5 V (vs SHE), 远高于石墨电极的1.5 V (vs SHE), 且与已报道的掺硼金刚石电极(BDD)的析氧电位(~2.8 V (vs SHE))相当(Santanaet et al., 2005), 说明TiSO-ME具有更高的析氧电位, 有助于在电解水过程中产生活性·OH.
从EIS图可以看出, 石墨和TiSO-ME的欧姆内阻十分接近, 分别为3.74 Ω和3.81 Ω(图 3c), 表明TiSO-ME的导电性与石墨接近, 均为良好的导体.相比之下, TiSO-ME的电荷转移内阻(20.31 Ω)比石墨电极低了近两个数量级(1151.22 Ω), 说明TiSO-ME具有更低的活化阻力, 便于水分子在其表面发生电解产生·OH.
从图 3d的加速寿命测试结果可以看到, TiSO-ME从起始电位的3.5 V (vs SHE)缓慢增加至5.0 V (vs SHE)左右的临界点, 对应的极限寿命为350 h (由式(3)推算在j=10 mA·cm-2下工作约65年), 推测与电极长时间在强极化条件下晶体结构的崩塌和氧化有关.相同条件下的石墨电极使用寿命仅为80 h (由式(3)推算在j=10 mA·cm-2下工作约23年), 这是由于石墨电极的层状结构在强酸高电位下很容易发生剥离和断裂, 导致石墨发生电化学氧化腐蚀.利用这一原理, Wang等(2017)实现了利用电化学氧化的方法制备氧化石墨烯, 这与本研究观察到的现象是一致的.
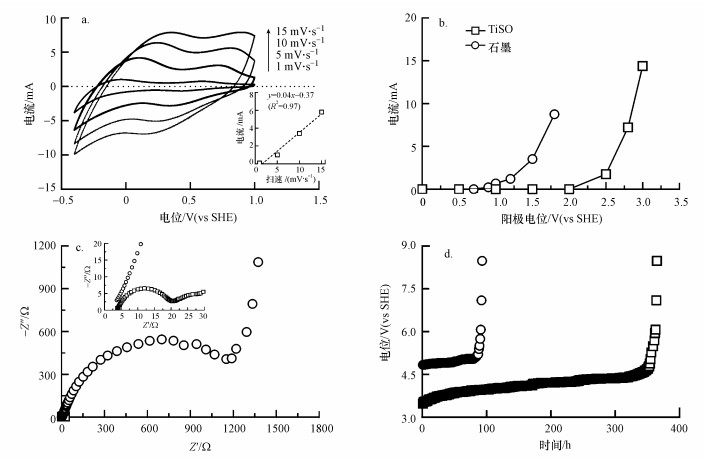 |
| 图 3 TiSO-ME与石墨电极的CV扫描(a)、LSV扫描(b)、EIS (c)和加速寿命(d)测试 Fig. 3 CV scan(a), LSV scan(b), EIS profile(c) and accelerated life test(d) of TiSO-ME and graphite electrode |
从表 1可以看出, 印染工业废水二沉池出水的可生化性较差, 其中主要以难降解有机污染物为主, 因此, 利用TiSO-ME对印染工业废水二沉池出水进行电化学氧化以期实现深度处理.如图 4a所示, 当电流密度在2~20 mA·cm-2范围内变化时, 废水的sCOD随着电流密度的增大均有不同程度的降低.反应2 h后, 浓度分别达到106.6、92.9、62.6及55.7 mg·L-1, 可见电流密度大于8 mA·cm-2即可使出水sCOD达到GB 4287-2012的间接排放标准.其中, 在电流密度为8 mA·cm-2的条件下, 观察到印染废水的颜色随电解时间的延长逐渐变浅, 在50 min时几乎达到无色, 说明TiSO-REM对色度具有良好的去除效果.当电流密度增至30 mA·cm-2时, 反应2 h后的sCOD为60.4 mg·L-1, 相比于20 mA·cm-2时反而有所增加, 这可能与高电流密度下的析氧和析氯副反应加剧有关, 从而占据了TiSO-REM上更多的反应活性位点, 使得以·OH诱导的间接氧化速率不再随电流密度的增加而增加(Martinez-Huitle et al., 2015).
废水中DOC的去除与sCOD相似(图 4b), 电解2 h后, 各个电流密度下对原水DOC的去除效率分别为20.51%、39.13%、46.37%、55.67%和54.44%.在电流密度8 mA·cm-2条件下, 电解2 h可使BOD5/COD提高近一个数量级, 大大提升了废水的可生化性, 因此, 可以考虑将电化学氧化处理后的废水回流到生物反应池.可以看出, 有机物去除率随电流密度的增大而增加的主要原因是污染物降解所需要的电量增加, 活性中间产物产率也相应增加, 有助于提升污染物降解效率(You et al., 2016).当电流密度增加到临界值时, 进一步增加电流密度会使界面上的副反应加剧, 从而导致有机物的降解不再受反应控制而趋于稳定.
从电能消耗的角度分析, 增大电流密度会大幅降低电流效率(图 4d)和增加能耗(图 4c), 尤其电流密度由8 mA·cm-2增大到20和30 mA·cm-2时, 能耗分别达到1.48和2.71 kWh·g-1, 分别为8 mA·cm-2下的3.76和6.90倍, 相比之下, sCOD去除率增加并不显著, 因此, 最佳电流密度为8 mA·cm-2.
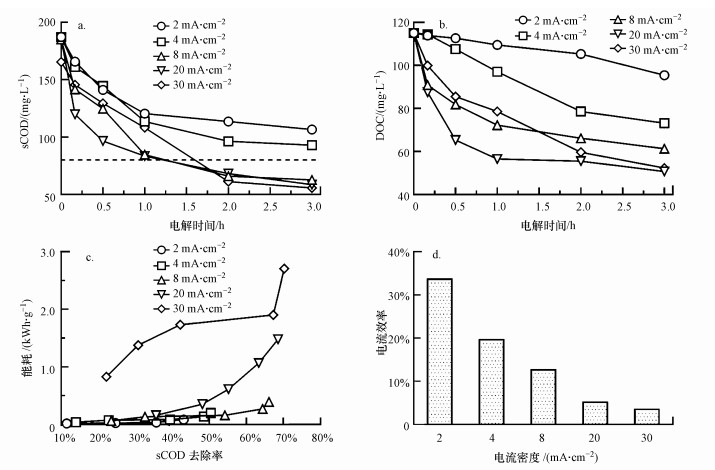 |
| 图 4 TiSO-ME处理印染工业废水的sCOD变化(a)、DOC变化(b)、能耗与sCOD去除率的关系(c)及电流效率(d) Fig. 4 Performance of TiSO-ME for treatment of dyeing wastewater(a.sCOD, b.DOC, c.energy consumption vs sCOD removal, d.current density) |
TiSO-ME的膜通量变化会影响废水在膜内部的流体形态, 进而影响传质过程(Yang et al., 2009).如图 5a所示, 膜通量从0 mL·cm-2·s-1增加到4.53×10-4 mL·cm-2·s-1(即4.53×10-6 m·s-1)时, 根据极限电流密度计算的传质系数从2.24×10-6 m·s-1增加至5.96×10-6 m·s-1, 这与利用舍伍德数常数计算的传质系数5.25×10-6 m·s-1近似, 说明膜通量在此范围内电极表面的传质过程受水平对流和扩散共同控制.伴随膜通量进一步增大至0.82×10-3~3.14×10-3 mL·cm-2·s-1(即0.82×10-5~3.14×10-5 m·s-1), 传质系数从0.81×10-5 m·s-1增加至3.22×10-5 m·s-1, 说明提高膜通量强化了溶质向阳极表面的对流扩散(谭阳, 2018; Geng et al., 2016; Zaky et al., 2013).拟合得到的线性方程斜率(1.08)接近于1.0, 表明此时膜孔内的对流传质在TiSO-ME电极表面占主导地位, 从而消除了传统旁流式操作由于速率梯度而产生的扩散边界层.在旁流操作中如果实现相同的传质速率则需满足雷诺数>20000(即湍流状态), 而本研究中雷诺数仅为476, 仍属于层流范畴.可见, TiSO-ME的穿流式操作便于大幅提升污染物向电极表面的传质系数.
电流密度为8 mA·cm-2, 膜通量为0 mL·cm-2·s-1 (即旁流式操作时), 电解1.5 h后的sCOD去除率为64.37%;当膜通量增加至1.7×10-3~3.7×10-3 mL·cm-2·s-1时, sCOD去除率均可达到80%以上且均符合一级反应动力学方程.从图 5b可以看出, sCOD的去除率随膜通量增加呈现出先增加后略有减小的趋势.膜通量从0 mL·cm-2·s-1增加到2.31×10-3 mL·cm-2·s-1, 电流效率也相应地从的16.23%增加到24.22%, 随后略有下降, 能耗则显著降低了32.99%.与旁流式操作相比, TiSO-ME可作为三维电极增加与污染物的接触面积, 不仅大幅提高污染物在电极表面的直接氧化速率, 而且有助于改善传质从而提升电极界面上·OH的利用率.电流密度为8 mA·cm-2, 膜通量为2.31×10-3 mL·cm-2·s-1时, TiSO-ME电解1.5 h能够使印染废水出水中的sCOD降为7.07 mg·L-1, 库伦效率为24.22%, 能耗仅为0.14 kWh·g-1, BOD5/sCOD提高了30.32倍.因此, TiSO-ME作为一种全新的电极, 有望在废水电化学处理中发挥重要作用.
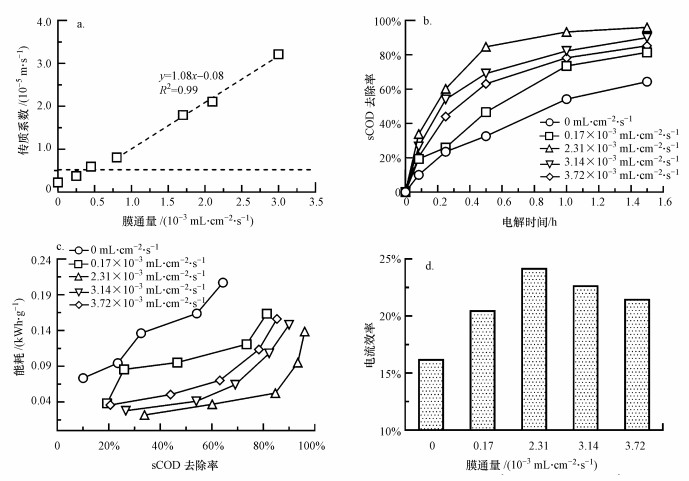 |
| 图 5 传质系数与膜通量的关系(a)、不同膜通量下印染废水sCOD去除效果(b)、能耗与sCOD去除率的关系(c)及电流效率与膜通量的关系(d) Fig. 5 Mass transfer coefficient as function of permeation flux(a), sCOD removal vs permeation flux(b), energy consumption vs sCOD removal(c), and current density vs permeation flux(d) |
1) TiSO-ME电极主要由Ti4O7和少量Ti5O9组成, 二者均为亚氧化钛的导电相.电极的比表面积为0.32 m2·g-1, 内部具有明显的孔结构特征, 其中92.7%的孔径 < 1 μm.
2) TiSO-ME电极的电化学活性面积是平面电极的667倍, 析氧电位高达2.5 V (vs SHE), 导电性与石墨相当, 加速寿命测试表明TiSO-ME的寿命可达30年.
3) 随着电流密度从2 mA·cm-2增加到30 mA·cm-2, 印染废水的sCOD去除率从43.05%增加到70.21%;考虑到废水处理效率和能耗之间的平衡, 最优电流密度为8 mA·cm-2.
4) TiSO-ME的穿流式操作能够大幅提升污染物在膜电极孔内部的传质, 在电流密度为8 mA·cm-2, 膜通量为2.31×10-3 mL·cm-2·s-1时, 电解1.5 h能够使印染废水处理效率达到96.07%, 能耗为0.14 kWh·g-1, BOD5/sCOD提高了30.32倍.
Chaplin B P. 2014. Critical review of electrochemical advanced oxidation processes for water treatment applications[J]. Environmental Science:Processes & Impacts, 16: 1182-1203. |
Chen G, Betterton E A, Arnold R G. 1999. Electrolytic oxidation of trichloroethylene using a ceramic anode[J]. Journal of Applied Electrochemistry, 29(8): 961-970. DOI:10.1023/A:1003541706456 |
陈银生, 张新胜, 袁渭康. 2001. 印染废水处理技术[J]. 化工进展, (5): 41-44. |
Gao Y, Zhang J, Bai X, et al. 2018. Monolithic ceramic electrode for electrochemical deactivation of Microcystis aeruginosa[J]. Electrochimica Acta, 259: 410-418. DOI:10.1016/j.electacta.2017.10.127 |
Gayen P, Spataro J, Avasarala S, et al. 2018. Electrocatalytic reduction of nitrate using Magneli phase TiO2 reactive electrochemical membranes doped with Pd-based catalysts[J]. Environmental Science & Technology, 52: 9370-9379. |
Geng P, Chen G. 2016. Magnéli Ti4O7 modified ceramic membrane for electrically-assisted filtration with antifouling property[J]. Journal of Membrane Science, 498: 302-314. DOI:10.1016/j.memsci.2015.07.055 |
Guo L, Jing Y, Chaplin B P. 2016. Development and characterization of ultrafiltration TiO2 Magneli phase reactive electrochemical membranes[J]. Environmental Science & Technology, 50(3): 1428-1436. |
Graves J E, Pletcher D, Clarke R L, et al. 1991. The electrochemistry of Magnéli phase titanium oxide ceramic electrodes Part I. The deposition and properties of metal coatings[J]. Journal of Applied Electrochemistry, 21(10): 848-857. DOI:10.1007/BF01042450 |
Hine F, Yasuda M, Noda T, et al. 1979. Electrochemical behavior of the oxide-coated metal anodes[J]. Journal of the Electrochemical Society, 126: 1439-445. DOI:10.1149/1.2129303 |
Liu G, Zhou H, Teng J, et al. 2019. Electrochemical degradation of perfluorooctanoic acid by macro-porous titanium suboxide anode in the presence of sulfate[J]. Chemical Engineering Journal, 371: 7-14. DOI:10.1016/j.cej.2019.03.249 |
Ma C, Pei S, You S. 2020. Closed bipolar electrode for decoupled electrochemical water decontamination and hydrogen recovery[J]. Electrochemistry Communications, 109: 106611. |
Martinez-Huitle C A, Rodrigo M A, Sirés I, et al. 2015. Single and coupled electrochemical processes and reactors for the abatement of organic water pollutants:a critical review[J]. Chemical Reviews, 115(24): 13362-13407. DOI:10.1021/acs.chemrev.5b00361 |
Panizza M, Cerisola G. 2009. Direct and mediated anodic oxidation of organic pollutants[J]. Chemical Reviews, 109(12): 6541-6569. DOI:10.1021/cr9001319 |
Pei S, Shen C, Zhang C, et al. 2019. Characterization of interfacial Joule heating effect in electrochemical advanced oxidation process[J]. Environmental Science & Technology, 53(8): 4406-4415. |
Pei S, Teng J, Ren N, et al. 2020. Low-temperature removal of refractory organic pollutants by electrochemical oxidation:role of interfacial Joule heating effect[J]. Environmental Science & Technology, 54(7): 4573-4582. |
Regonini D, Dent A C E, Bowen C R, et al.2011.Impedance spectroscopy analysis of TinO2n-1 Magnéli phases[J].Materials Letters 65: 3590-3592
|
Santana M H P, Faria L A D, Boodts J F C. 2005. Electrochemical characterisation and oxygen evolution at a heavily boron doped diamond electrode[J]. Electrochimica Acta, 50(10): 2017-2027. DOI:10.1016/j.electacta.2004.08.050 |
Smith J R, Walsh F C, Clarke R L. 1998. Electrodes based on Magneli phase titanium oxides:the properties and applications of Ebonex® materials[J]. Journal of Applied Electrochemistry, 28(10): 1021-1033. DOI:10.1023/A:1003469427858 |
谭阳.2018.亚氧化钛电极膜反应器降解4-氯酚废水的研究[D].哈尔滨: 哈尔滨工业大学.37-38 http://cdmd.cnki.com.cn/Article/CDMD-10213-1018894521.htm
|
Teng J, Liu G, Liang J, et al. 2020. Electrochemical oxidation of sulfadiazine with titanium suboxide mesh anode[J]. Electrochimica Acta, 331: 135441. DOI:10.1016/j.electacta.2019.135441 |
Teng J, Zhang J, Wang X, et al. 2018. Chlorophenolic compounds degradation based on electrolyte-free electrochemical cells[J]. ACS Sustainable Chemistry & Engineering, 6: 4516-4520. |
Walsh F C, Wills R G A. 2010. The continuing development of Magneli phase titanium sub-oxides and Ebonex® electrodes[J]. Electrochimica Acta, 55(22): 6342-6351. DOI:10.1016/j.electacta.2010.05.011 |
Wang H, Wei C, Zhu K, et al. 2017. Preparation of graphene sheets by electrochemical exfoliation of graphite in confined space and their application in transparent conductive films[J]. ACS Applied Materials & Interfaces, 9(39): 34456-34466. |
王愚.2016.亚氧化钛电化学阳极氧化降解印染废水研究[D].哈尔滨: 哈尔滨工业大学.23-24 http://cdmd.cnki.com.cn/Article/CDMD-10213-1016913685.htm
|
Yang J, Wang J, Jia J. 2009. Improvement of electrochemical wastewater treatment through mass transfer in a seepage carbon nanotube electrode reactor[J]. Environmental Science & Technology, 43(10): 3796-3802. |
You S, Liu B, Gao Y, et al. 2016. Monolithic porous Magnéli-phase Ti4O7 for electro-oxidation treatment of industrial wastewater[J]. Electrochimica Acta, 214: 326-33. |
Zaky A M, Chaplin B P. 2013. Porous Substoichiometric TiO2 anodes as reactive electrochemical membranes for water treatment[J]. Environmental Science & Technology, 47(12): 6554-6563. |
 2020, Vol. 40
2020, Vol. 40


