氯霉素(Chloramphenicol, CAP)是一种被广泛用于治疗人畜感染性疾病的广谱抑菌性抗生素(Samsonova et al., 2012).然而临床已经证实CAP具有严重的毒副作用, 例如可能会引起白血病、再生障碍性贫血等(Zhao et al., 2015), 并且其毒副作用的发生与用药量和使用频率无关(Hanekamp et al., 2015).因此, 自20世纪90年代开始CAP被欧美、中国等地区和国家禁止使用.但由于CAP高效低廉、可利用性高等特点, 至今仍然被广泛用在家禽和渔业养殖中, 用于提高产量和控制疾病传染(Sapkota et al., 2008).此外, 由于CAP无法被生物体完全吸收, 其摄入量的30%~90%仍可通过粪便、尿液排出(Heberer, 2002; Bound et al., 2004), 并且难以被常规水处理工艺完全去除(Chang et al., 2010), 因此, 常在环境中被检测出来, 呈现出一种“伪”持久性(Chen et al., 2014).
吸附作用是影响环境中CAP迁移和转化的重要过程之一, 并可进一步影响CAP在环境中的分布和生物可利用性.研究表明, 吸附过程受吸附剂性质的影响较大, 例如, 多壁碳纳米管对CAP的吸附力随比表面积的增大而增大(Zhao et al., 2016);经NaOH改性后的竹炭对CAP吸附量的增加归因于吸附剂与吸附质之间π-π相互作用的增强(Fan et al., 2010);自然水环境沉积物对CAP吸附比例的增加亦受有机质含量增加的影响(余绵梓等, 2019).但以往研究中大多是以沉积物、生物材料、纳米材料等为研究对象, 而对自然环境中细颗粒物(如胶体)在CAP吸附行为中的影响作用关注较少.
胶体(Colloids)广泛存在于环境中, 一般是指一维粒径范围在1 nm~1 μm之间的多相混合物质, 其具有化学异质性、较大的比表面积和丰富的表面活性基团等特点, 因此, 在环境中易与各种污染物相结合(Lead et al., 2006).研究表明, 水环境中胶体对药物的吸附率可高达45%, 深刻影响着水环境中药物的赋存分配行为, 这与胶体的理化性质有关(Yang et al., 2011).胶体颗粒物中49%~71%为有机质(Wilding et al., 2005), 其中, 有机碳含量和芳香碳含量对内分泌干扰物的吸附具有一定的控制作用(Zhou et al., 2007).并且类腐殖质胶体能够促进沉积物对土霉素的吸附, 而类蛋白质胶体则抑制这一过程(Zhang et al., 2019a).此外, 胶体粒径往往能够决定其物化特性(刘娜娜等, 2014), 多环芳烃、烷基酚等污染物更容易被小粒径的胶体颗粒吸附(Kalmykova et al., 2013).然而, 目前对天然胶体及其对污染物环境行为影响的研究还不够全面, 以土壤和沉积物中胶体为吸附剂并探究其对CAP环境行为影响的研究更加匮乏.因此, 有必要了解不同来源土壤和沉积物中胶体的理化性质及其对CAP吸附行为的影响及作用机理.
基于此, 本研究以2种河湖沉积物和3种不同来源土壤中胶体为研究对象, 结合切向超滤技术及多种纳米分析法(包括动态光散射、紫外-可见分光光度法、三维荧光光谱法等), 对不同来源土样胶体的粒径和物质组成等理化性质进行表征, 同时利用超滤法对CAP在胶体及溶解相中的吸附分配行为进行初探.通过冗余分析法分析胶体理化性质对CAP, 以期为天然胶体对CAP环境行为的影响机制研究提供理论和数据支持.
2 材料与方法(Materials and methods) 2.1 样品采集与制备本研究选取2种沉积物(A1(抚河与鄱阳湖交汇处)和A2(南昌市区象湖))、2种天然土壤(B1(花圃)和B2(油菜花田))及1种市售的营养土(B3)作为土样中胶体来源, 所有样品经冷冻干燥后研磨, 过200目筛.5种土样及CAP的基本理化参数详见表 1和表 2.本研究未对溶液进行pH值调节, 吸附实验中的溶液pH值基本与土壤pH值一致(5.02~8.03).结合CAP的pKa值可知, 本研究中CAP的形态为分子态.称取适量过筛后的5种土样(A1、A2、B1、B2、B3)至离心管, 并加入Milli-Q超纯水(土壤和超纯水的比例为1:10), 密封好后放置于振荡器中振荡48 h, 接着使用离心机于3500 r·min-1转速条件下离心30 min, 取出上清液后采用0.45 μm滤膜(PVDF, Millipore, USA)过滤, 过滤液置于锥形瓶中, 加入CAP储备液及Milli-Q超纯水定容至250 mL, 定容后过滤液中CAP的浓度为5 mg·L-1.
| 表 1 不同土样的基本理化参数 Table 1 Physicochemical properties of different soils |
| 表 2 CAP基本理化参数a Table 2 Physicochemical properties of CAP |
为了检验切向超滤系统对CAP的回收情况, 将CAP溶于超纯水中, 接着采用分子截留孔径为1 kDa(1 kDa=1000 Da)的超滤膜进行回收率实验(Yang et al., 2011).切向超滤方法参照Yan等(2018)的研究.将 < 0.45 μm的过滤液通过蠕动泵带入超滤系统中, 系统压力方向与水流方向呈正交, 能透过1 kDa超滤膜的部分被分离出来并单独收集, 即 < 1 kDa的超滤液;而被截留下来的部分回流至进样瓶, 直至浓缩过程结束, 所得浓缩液即为1 kDa~0.45 μm的胶体浓缩液.实验结果表明, CAP在1 kDa超滤膜上的回收率情况较好, 达到91.32%.接着, 对上述含有CAP的5种土样胶体溶液进行胶体分离处理.所有胶体浓缩液的浓缩倍数均为10倍, 所得样品保存在4 ℃的冰箱中待测.
CAP浓度采用高效液相色谱仪(1260 Infinity Ⅱ, Agilent, USA)进行测定.分析条件如下:色谱柱为Athena-C18-WP(150 mm×2.1 mm, 5 μm), 流动相为超纯水30%(A)和甲醇70%(B), 流速为0.2 mL·min-1, 柱温为40 ℃, 进样量为5 μL, 紫外检测波长为273 nm.
2.3 胶体理化性质测定 2.3.1 三维荧光光谱(3D-EEMs)经切向超滤技术分离得到的过滤液、胶体浓缩液和超滤液样品采用三维荧光分光光度计(HITACHI, F7100)进行3D-EEMs测定.响应时间为自动;样品扫描范围为:激发波长λEx=200~450 nm, 增量为5 nm, 发射波长λEm=250~600 nm, 增量为2 nm;扫描速度为12000 nm·min-1;狭缝宽度为5 nm;测定前以Milli-Q超纯水做空白.
2.3.2 紫外-可见吸收光谱不同来源土样的过滤液、胶体浓缩液和超滤液样品采用紫外-可见分光光度计(UV3300, 美普达, 上海)测定紫外-可见吸收光谱, 以1 nm为扫描间隔;扫描波长为200~800 nm;以1 cm光路径比色皿测定, 测定前以Milli-Q超纯水做空白(聂明华等, 2018).
2.3.3 胶体粒径胶体浓缩液中的胶体粒径采用Zeta-sizer分析仪(Malvern, Nano-zs90)进行分析检测.测样前利用超声法对胶体进行分散处理, 依据液体水温设定温度(一般为15 ℃), 连续测样3次, 取平均值.
2.3.4 溶解性有机碳过滤液、胶体浓缩液和超滤液中有机碳含量采用liquiTOC Ⅱ(Elementar, Germany)测定.
2.4 数据处理 2.4.1 三维荧光光谱的校正及光谱指数计算不同来源土样的胶体浓缩液和超滤液的3D-EEMs测定结果使用Milli-Q超纯水在λEx=350 nm、λEm=370~428 nm的拉曼峰面积进行拉曼单位矫正(Lawaetz et al., 2009);在Matlab 2010a中对3D-EEMs进行拉曼瑞利散射矫正(Zepp et al., 2004), 以相应的超滤液和胶体浓缩液的3D-EEMs数据为基础, 计算对应胶体的3D-EEMs, 计算方法如式(1)所示.
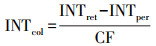
|
(1) |
式中, INTcol、INTret、INTper分别为胶体、胶体浓缩液、超滤液的荧光强度;CF为浓缩倍数.
为进一步分析不同来源土样中胶体荧光组分的差异, 采用腐殖化指数HIX表征胶体的腐殖化程度(Ohno, 2002), 计算方法如式(2)所示.当HIX为10~16时, 表明荧光组分具有较高的腐殖化程度, 主要为陆源;当HIX<4时, 主要为自生源有机质(Zsolnay et al., 1999).
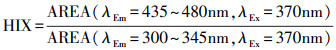
|
(2) |
式中, AREA(λEm=x, λEx=y)为λEx=370 nm波长下指定发射波长范围内的光谱区域积分面积.
2.4.2 荧光区域积分荧光区域积分法(Fluorescence Regional Integration, FRI)是一种定量分析技术, 通过对3D-EEMs中不同激发-发射波长区域计算积分体积, 分析3D-EEMs中所有波长下的荧光强度并判断出主要荧光物质(Chen et al., 2003).根据前人研究将胶体的EEMs划分为5个荧光区域(Chen et al., 2003; Song et al., 2019), 相关描述见表 3.
| 表 3 FRI识别的5个积分区的激发和发射波长范围及物质类型 Table 3 The excitation and emission wavelength ranges of the five integrated regions identified and material type by fluorescence regional integration |
首先将荧光区域i(i=Ⅰ.n、Ⅱ、Ⅲ、Ⅳ、Ⅴ)的积分体积归一化为积分标准体积Φi.n(au·nm2), 从而得到总荧光区域的积分标准体积ΦT.n(au·nm2), 以及Φi.n与ΦT.n的比值Pi.n, 相关计算公式如式(3)~(5)所示.
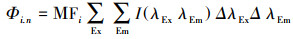
|
(3) |
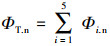
|
(4) |
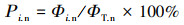
|
(5) |
式中, ΔλEx、ΔλEm为波长增量(nm), I(λExλEm)为激发、发射波长的荧光强度(r.u.);MFi为倍增系数(荧光区域i的积分面积占总荧光区域积分面积比例的倒数).
2.4.3 紫外-可见光谱参数UV254值即波长254 nm处的吸光度, 同一有机碳浓度的胶体在该波长下的吸光度值与芳香碳含量及腐殖化程度呈正相关(Nishijima et al., 2004).
α355为波长355 nm处的吸收系数(m-1), 可根据式(6)得出, 该值可表征胶体中有色溶解性有机质(CDOM)的相对丰度(Guéguen et al., 2011).
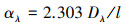
|
(6) |
式中, Dλ为参考波长处的吸光度, l为光程路径(m).
UV253/UV220为波长253 nm和220 nm处吸光度的比值, 可反映芳环上的取代基种类和取代程度.该值越小, 说明芳环上的取代基中脂肪链的比重较大;该值越大, 说明芳环上取代基中羧基、羰基、酯类等比重较大(Peuravuori et al., 1997).
S275~295和S350~400是指275~295 nm和350~400 nm波段的吸收光谱斜率, 可通过SigmaPlot 14.0软件中的单指数衰减法拟合出, 详见式(7).
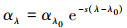
|
(7) |
式中, αλ0为参考波长下的吸收系数;λ0为参照波长(nm).
SR为光谱斜率S275~295和S350~400的比值(Helms et al., 2008), 常用来表征胶体的来源组成及结构变化, 与分子量呈反比(Xiao et al., 2013).
2.4.4 CAP吸附指标胶体中CAP的浓度和胶体对CAP的吸附率可通过式(8)、(9)计算得到, 胶体吸附率能够反映CAP在不同来源和性质胶体的分配情况(Yan et al., 2015a).
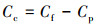
|
(8) |
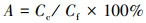
|
(9) |
式中, Cc、Cf和Cp分别是胶体、过滤液和超滤液中CAP浓度(mg·L-1);A为胶体吸附率.
为进一步了解CAP与胶体的结合情况, 根据式(10)计算CAP在胶体浓缩液(胶体相)和超滤液(真溶解相)中浓度(mg·L-1)的比值Cr/Cp(Xia et al., 2013), 以及CAP与胶体的有机碳归一化结合系数KDOC值(L·kg-1)(Bai et al., 2019).
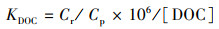
|
(10) |
式中, Cr为胶体浓缩液中CAP的浓度(mg·L-1);[DOC]为胶体浓缩液中溶解性有机碳含量(mg·L-1).
2.4.5 数理统计分析利用SPSS 26.0的单因素方差法(One-way ANOVA)对胶体理化性质和CAP吸附指标进行显著性差异分析.胶体理化性质和CAP吸附指标之间的潜在关系通过CANOCO 4.5软件进行分析, 去趋势对应分析结果显示最大梯度长度为0.228(<3), 因此, 采用线性模型对相关数据进行冗余分析(Redundancy Analysis, RDA).
3 结果与讨论(Results and discussions) 3.1 不同来源土样胶体理化性质分析 3.1.1 胶体粒径分析不同来源土样胶体的粒径分布见图 1.由图可知, 各土样虽已经过0.45 μm的滤膜, 但仍存在粒径大于0.45 μm的胶体, 这可能是因为胶体在浓缩过程中发生絮凝, 也可能是因为部分胶体的一维或二维尺寸大于0.45 μm(晏彩霞, 2015).对比各胶体粒径范围和集中程度发现, A1、A2、B1、B2、B3的胶体粒径主要分布在40~610、190~530、220~610、60~610、250~615 nm之间.各胶体粒径均呈单峰分布, 其中, B3胶体粒径分布最为集中, 34%的胶体其粒径在峰值400 nm处;而A1和B2的胶体粒径分布较为分散, 分别只有14%和12.5%的胶体其粒径在峰值220、190 nm附近;A2和B1胶体粒径分布规律相似, 均有25%的胶体其粒径在峰值340 nm附近, 但整体上B1胶体平均粒径略大于A2.总体来说, 各胶体平均粒径大小关系为B3>B1>A2>A1>B2.
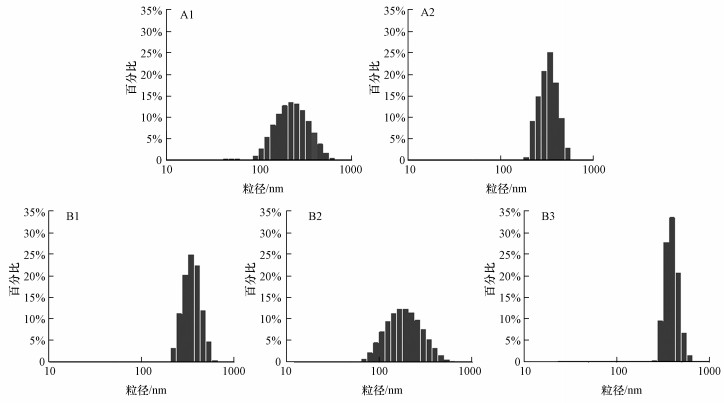 |
| 图 1 不同来源土样胶体的粒径分布特征 Fig. 1 Particle size distribution of different soil colloids |
不同荧光区域的积分标准体积与相应区域荧光强度成正比, Pi.n值则指示荧光物质成分对总荧光强度的相对贡献率(Song et al., 2019).不同来源土样胶体的3D-EEMs、Φi.n和Pi.n分布情况分别见图 2和图 3.由图 3a可知, A1胶体的ΦT.n值最高, B3胶体次之, B1胶体最低, A2和B2胶体则相差不大, 说明A1胶体的荧光物质最多, 荧光强度高于其它土样胶体.A1、A2、B1、B2胶体的荧光峰出现在区域Ⅲ, PⅢ.n值在39.86%~46.96%之间, 并且这些胶体的PⅡ.n值也较大, 在29.71%~40.65%之间, 说明胶体的主要荧光物质为类富里酸并存在一定量的色氨酸类蛋白物质;B3胶体的荧光峰则出现在区域Ⅴ(PⅤ.n值为47.08%), 并且区域Ⅲ的荧光强度也较大(PⅢ.n值为33.23%), 说明其荧光物质主要为类富里酸和类腐殖酸物质(图 2和图 3b).除此之外, 胶体的PⅠ.n值和PⅣ.n值分别在4.28%~17.21%和0.49%~4.26%之间, 说明不同来源土样胶体中络氨酸类蛋白物质和溶解性微生物代谢物质含量较少.
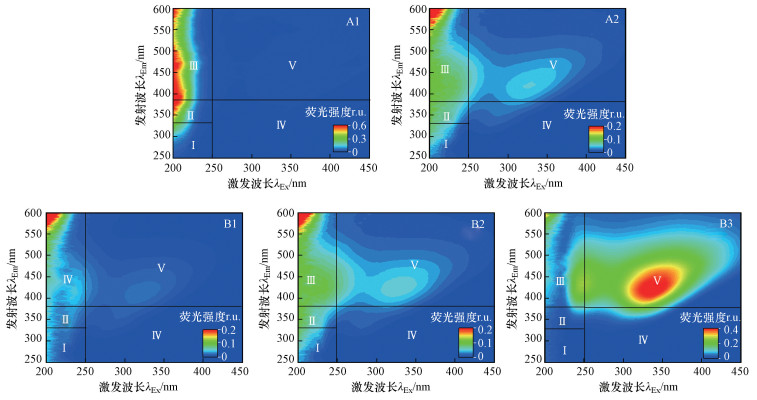 |
| 图 2 不同来源土样胶体的EEMs和FRI分布 Fig. 2 The EEMs and FRI distribution of different soil colloids |
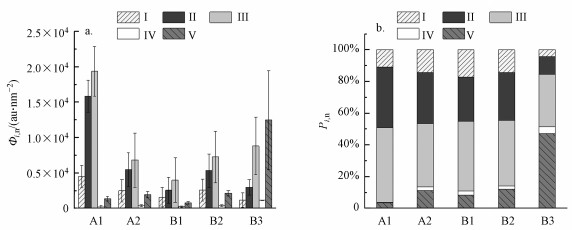 |
| 图 3 不同来源土样胶体的Φi.n和Pi.n分布情况 Fig. 3 Distribution of Φi.n and Pi.n of different soil colloids |
不同来源土样胶体的光谱指数(HIX、UV254、α355、UV253/UV220、SR)分布特征见图 4.HIX用于表征有机质组分的腐殖化程度(Ohno, 2002).由图 4a可知, 各胶体的HIX均值在4.95~32.38之间, 其中, B2、B3胶体的HIX值大于10, 说明具有强腐殖化特征;A1、A2和B1胶体的HIX值在4~6之间, 腐殖化相对较弱, 并具有一定的自生源特征.
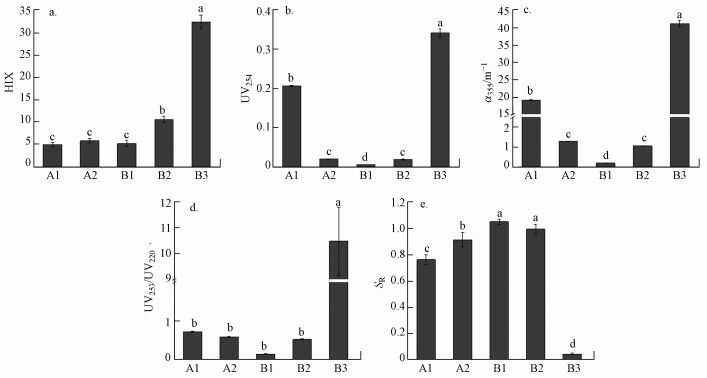 |
| 图 4 不同来源土样胶体的光谱指数(同一坐标轴内柱状图上方不同字母表示差异性显著, p < 0.05) Fig. 4 Spectral indices of different soil colloids |
UV254值可表征胶体的芳香度, 且该值越大其组分中不饱和键越多(Nishijima et al., 2004).各胶体的UV254均值在0.01~0.34之间, 其中, B3胶体的UV254均值远高于其它胶体(图 4b), 说明B3胶体的芳香度高且不饱和键较多.
吸收系数α355值可表征胶体中CDOM的相对丰度(Guéguen et al., 2011).各胶体的α355均值在0.18 ~41.18 m-1之间, 其中, B3胶体的α355值最大, B1胶体的α355值最小(图 4c), 可见B3胶体的CDOM丰度远高于其它土样胶体, 而B1胶体的CDOM丰度最低.
UV253/UV220值可表征芳环上的取代基种类和取代程度(Peuravuori et al., 1997).各胶体的UV253/UV220均值在0.15~10.48之间, 其中, B3胶体的UV253/UV220均值显著高于其它胶体, 而A1、A2、B1、B2胶体之间无显著差异性(图 4d), 说明B3胶体的芳环上含有更加丰富的羧基、羰基、羟基等官能团.
SR值常用来表征胶体的来源组成及结构变化, 与分子量呈反比(Xiao et al., 2013).各胶体的SR值在0.04~1.05之间, 其中, B3胶体的SR值最小, 并且与其它胶体差异显著(图 4e), 表明B3胶体的分子量大, 这与前文B3的胶体粒径主要集中在400 nm附近且平均粒径大于其它胶体的结果一致.
从以上分析中可以发现, 营养土胶体B3的光谱参数值与天然土壤胶体B1、B2相比, 分子量较大、腐殖化程度较高;而河湖沉积物胶体A1、A2的UV254值、α355值、UV253/UV220值大于天然土壤胶体B1、B2, 且HIX值、SR值低于天然土壤胶体B1、B2.这表明与天然土壤胶体相比, 河湖沉积物胶体具有较大的分子量、较高的CDOM丰度和芳化度及较多的含氧官能团, 这与李璐璐等(2014)发现三峡库区沉积物胶体的分子量和腐殖化程度高于土壤胶体的结论一致.
3.2 CAP吸附指标分析不同来源土样的过滤液、胶体浓缩液、超滤液和胶体所携带的CAP浓度及胶体吸附率如图 5所示.由图 5a可以发现, 胶体浓缩液中CAP浓度均高于过滤液和超滤液中CAP浓度, 表明胶体能够吸附CAP, 该结果与城市废水中新型有机污染物在胶体浓缩液中含量高于超滤水中含量的结论相一致(Yan et al., 2015a).由图 5b可知, 不同来源土样胶体中CAP的浓度(Cc)为0.77~2.52 mg·L-1, 均值为1.31 mg·L-1.胶体吸附率能够综合反映CAP在不同来源和性质胶体中的分配情况.图 5c显示不同来源土样胶体的吸附率为14.00%~36.35%, 均值为21.62%.各胶体的吸附率与Cc值的大小关系排序一致, 即B3>A1>B2>A2>B1, 其中, B3胶体的CAP浓度和吸附率显著高于其它胶体.另外, 河湖沉积物胶体A1、A2的平均吸附率为19.29%, 该值接近长江水体中胶体对CAP的平均吸附率(19%~20%)(Yan et al., 2015b).营养土B3的胶体吸附率与天然土壤B1、B2的胶体吸附率相差较大, 天然土壤胶体B1、B2的平均吸附率为16.58%, 该值低于河湖沉积物胶体的平均吸附率.
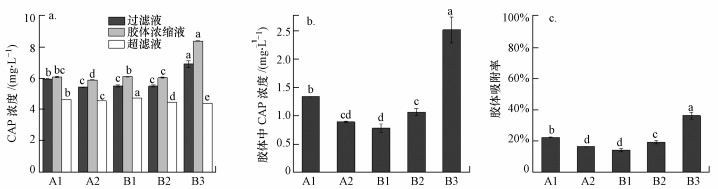 |
| 图 5 CAP在不同来源土样胶体中的吸附参数(a.各相中CAP浓度; b.胶体中CAP浓度; c.胶体吸附率) Fig. 5 Sorption parameters of CAP with different soil colloids (a. CAP concentration in each phase; b. CAP concentration in colloids; c. colloidal sorption rate) |
胶体浓缩液中DOC浓度、Cr/Cp值和结合系数logKDOC值见表 4.各胶体浓缩液中DOC平均浓度在6.53~222.4 mg·L-1之间, 均值为57.33 mg·L-1, 大小关系为B1 < B2 < A2 < A1 < B3.其中, 营养土B3的DOC浓度远大于其它土样, 沉积物A1、A2的DOC浓度高于天然土壤B1、B2.Cr/Cp值可衡量CAP在胶体浓缩液和超滤液的浓度分配(田家英等, 2017).各个土样的Cr/Cp值大小依次为B3>B2>A1>A2≈B1, 范围为1.29~1.91, 均值为1.43, 该值低于长江口地区水体胶体浓缩液和超滤液中检测到的CAP浓度的比值(2.3~4.8)(晏彩霞, 2015).沉积物A1、A2的Cr/Cp平均值约为1.30, 天然土壤B1、B2的Cr/Cp平均值约为1.33, 可见天然土壤中CAP浓度在两相的分配比例略高于河湖沉积物.
| 表 4 不同来源土样胶体的Cr/Cp、DOC浓度和logKDOC Table 4 Cr/Cp, DOC concentration and logKDOC of different soil colloids |
CAP与不同来源土样胶体的logKDOC值在3.93~5.30之间, 平均值为4.77, 该值大于土壤或沉积物胶体与内分泌干扰物的logKDOC均值(双酚A为3.42, 17β-雌二醇为3.91, 17α-乙炔雌二醇为3.98)(Sun et al., 2007).5种胶体的logKDOC值大小依次为B1>B2>A2>A1>B3, 其中, CAP与B1胶体的结合能力最强, 而与B3胶体的结合能力最弱.另外, 沉积物胶体A1、A2的logKDOC值相差较小, 天然土壤胶体B1、B2的logKDOC值亦有相似规律, 表明同一来源的胶体可能对CAP具有相似的结合亲和力.而营养土胶体、天然土壤胶体和沉积物胶体三者之间logKDOC值相差较大, 天然土壤胶体对CAP的结合能力要强于沉积物胶体, 而营养土胶体B3对CAP的结合能力则要弱于天然土壤胶体和沉积物胶体.
3.3 胶体理化性质与CAP吸附指标的RDA分析胶体理化性质与CAP吸附指标的RDA结果见表 5.胶体理化性质所处的象限表示与排序轴之间的相关性, 由表可知, 大部分胶体理化性质与第一排序轴呈显著正相关, 而ΦⅠ.n值、ΦⅡ.n值、ΦⅢ.n值和粒径则与第二排序轴相关性较大.前两轴胶体理化性质和CAP吸附指标的相关累计解释量达到99.4%, 其中, 第一排序轴的解释量为98.4%, 第二排序轴仅为1%, 说明第一排序轴可以很好地解释CAP吸附指标和胶体理化性质的相关关系.
| 表 5 胶体理化性质与排序轴的相关性及与CAP吸附指标的RDA结果 Table 5 Correlation between colloidal physicochemical properties and sorting axis and redundancy analysis results of CAP sorption index |
胶体理化性质和CAP吸附指标的RDA排序见图 6.胶体理化性质的箭头连线越长表示该因子对CAP吸附指标作用越大;胶体理化性质与CAP吸附指标的夹角表示二者之间的相关性, 锐角为正相关, 钝角为负相关, 直角为不相关;胶体理化性质箭头连线在CAP吸附指标箭头连线上的投影越长(余弦值越大), 则对CAP吸附指标影响越大(Lepš et al., 2003).
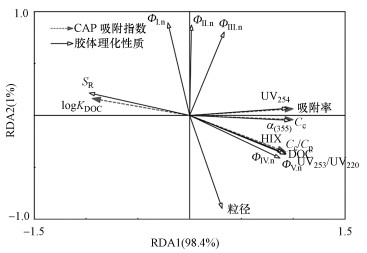 |
| 图 6 胶体理化性质和CAP吸附指标的RDA排序 Fig. 6 Ordination of redundancy analysis of colloidal physicochemical properties and sorption index of CAP |
由图 6可知, α355值与Cc值呈显著正相关, 即胶体中CAP的浓度会随着CDOM丰度的增大而升高.研究表明, 增加吸附剂中有机质含量能加强对污染物的吸附能力(茶丽娟等, 2011).这是因为有机质在吸附过程中通常是电子供体, 而CAP中的酮基、硝基和苯环等官能团均为π电子受体, 二者之间容易形成π-π键, 并且电子供体数越多则吸附越紧密(Sun et al., 2010; Liao et al., 2013).另外, 有文献报道城市河流胶体中大部分抗生素的浓度随类富里酸和类腐殖酸荧光物质含量的增加而增加(Yan et al., 2015b; Zhang et al., 2019b).然而本研究中ΦⅤ.n值与Cc值之间虽存在正相关关系, 但未发现ΦⅢ.n值与Cc值之间具有相关性, 这可能与不同药物的性质差异大及类富里酸物质的结构和来源不同有关.此外, UV254值与胶体吸附率呈显著正相关, 即胶体中芳香性和组分中不饱和键越多, 对CAP的吸附贡献就越大, 这与文献报道的有机质组分芳香性是影响土霉素吸附量的主要因素的结论一致(Zhang et al., 2019a).
同时, 从图 6可以发现, DOC浓度、HIX值、UV253/UV220值、ΦⅣ.n值和ΦⅤ.n值的箭头连线分布密集, 表明这些理化性质之间存在显著正相关, 并且均与Cr/Cp值存在显著正相关.说明胶体的腐殖化程度、以羰基和羧基等为主的官能团比重、DOC浓度、类腐殖酸和溶解性微生物代谢物质含量均对CAP在胶体浓缩液和超滤液中的分配比例具有一定程度的影响.这是因为腐殖质含有大量羰基、酚羧基等官能团, 这些官能团易与CAP中的N—H、—OH形成氢键, 利于CAP与胶体之间吸附作用的发生(朱秀珍, 2018; Zhang et al., 2019a).同时, 研究还发现ΦⅤ.n值与Cr/Cp值的箭头连线夹角的余弦值大于ΦⅣ.n值与Cr/Cp值夹角的余弦值.根据ΦⅣ.n值和ΦⅤ.n值的荧光区域范围和前人研究可知(Li et al., 2018; Zhang et al., 2019b), 类腐殖质对CAP的分配影响大于类蛋白物质.与HIX值、UV253/UV220值、ΦⅣ.n值和ΦⅤ.n值相比, DOC与Cr/Cp值箭头连线夹角的余弦值最大, 说明DOC浓度为影响Cr/Cp值的关键因子, 这与长江口水体中CAP的分布研究发现DOC浓度与Cr/Cp值之间存在线性相关性的结论一致(Yan et al., 2015b).另外, 发现SR值与α355值、HIX值、ΦⅤ.n值、UV253/UV220值、DOC浓度存在较强的负相关关系, 说明本研究中大分子量胶体具有更丰富的CDOM、DOC、类腐殖酸和含氧官能团, 这与文献报道的类腐殖酸是相对稳定的高分子量芳香族类腐殖物质(Baker et al., 2004), 以及典型污水厂及养殖区水体中DOC主要集中在大分子量胶体(300 kDa~1 μm)上的结论一致(晏彩霞, 2015).此外, CAP结合系数logKDOC值与SR值呈显著正相关, 表明在排除有机碳含量的影响后, 胶体对CAP的结合能力会随着胶体分子量的减小而增强.这与文献报道的胶体粒径越小、比表面积越大, 对农药、多环芳烃及重金属元素等污染物的吸附能力越强的规律一致(Meland et al., 2010; Ngueleu et al., 2013).但在本研究中却未发现胶体粒径与logKDOC值或者其它CAP吸附指标之间存在显著相关性, 这可能与胶体出现絮凝现象导致粒径检测时出现偏差有关.而ΦⅠ.n值、ΦⅡ.n值及ΦⅢ.n与各CAP吸附指标之间均未发现显著的相关性, 由此可见, 胶体中络氨酸类蛋白质、色氨酸类蛋白质及类富里酸荧光物质在胶体与CAP的吸附作用中贡献较小.
4 结论(Conclusions)1) CAP吸附实验表明, 胶体吸附在CAP的分配中起着重要作用, 胶体理化性质与CAP的吸附行为和存在形式密切相关.
2) 不同来源土样胶体理化性质分析结果显示, 胶体分子量、CDOM丰度、DOC浓度、芳香性及芳环上含氧官能团比重均以营养土最大, 河湖沉积物胶体次之, 天然土壤胶体最小.FRI分析结果表明, 胶体的荧光组分以类富里酸、类腐殖酸和色氨酸类蛋白质为主, 络氨酸类蛋白质和溶解性微生物代谢物质组分较少.
3) 胶体对CAP吸附行为的影响研究发现, 不同来源土样胶体的吸附率在14.00%~36.25%之间, 以营养土最大;胶体对CAP的吸附使胶体浓缩液中CAP浓度明显大于超滤液中CAP浓度;另外, 与河湖沉积物胶体相比, CAP更倾向与天然土壤胶体结合, 而营养土胶体对CAP的结合能力最弱.
4) RDA结果显示, 芳香度、CDOM丰度、DOC浓度、分子量分别与胶体中CAP浓度、胶体吸附率、CAP在胶体浓缩液与超滤液中的分配比例、logKDOC值正相关性最大;胶体的腐殖化程度和芳环上含氧官能团的比重对CAP的吸附也起着重要作用;另外, 荧光组分中只有类腐殖酸物质和溶解性微生物代谢产物对CAP吸附行为产生显著影响, 且前者的影响力大于后者.
Bai L, Zhang Q, Wang C, et al. 2019. Effects of natural dissolved organic matter on the complexation and biodegradation of 17α-ethinylestradiol in freshwater lakes[J]. Environmental Pollution, 246: 782-789. DOI:10.1016/j.envpol.2018.12.098 |
Baker A, Curry M. 2014. Fluorescence of leachates from three contrasting landfills[J]. Water Research, 38: 2605-2613. |
Bound J P, Voulvoulis N. 2004. Pharmaceuticals in the aquatic environment-a comparison of risk assessment strategies[J]. Chemosphere, 56: 1143-1155. DOI:10.1016/j.chemosphere.2004.05.010 |
茶丽娟, 张迪, 彭红波, 等. 2011. 卡马西平在云南典型土壤上的吸附研究[J]. 昆明理工大学学报:自然科学版, 36(6): 61-66. |
Chang X, Meyer M T, Liu X, et al. 2010. Determination of antibiotics in sewage from hospitals, nursery and slaughter house, wastewater treatment plant and source water in Chongqing region of Three Gorge Reservoir in China[J]. Environmental Pollution, 158(5): 1444-1450. DOI:10.1016/j.envpol.2009.12.034 |
Chen K, Zhou J L. 2014. Occurrence and behavior of antibiotics in water and sediments from the Huangpu River, Shanghai, China[J]. Chemosphere, 95: 604-612. DOI:10.1016/j.chemosphere.2013.09.119 |
Chen W, Westerhoff P, Leenheer J A, et al. 2003. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 37(24): 5701-5710. |
Fan Y, Wang B, Yuan S, et al. 2010. Adsorptive removal of chloramphenicol from wastewater by NaOH modified bamboo charcoal[J]. Bioresource Technology, 101: 7661-7664. DOI:10.1016/j.biortech.2010.04.046 |
Guéguen C, Granskog M A, McCullough G, et al. 2011. Characterisation of colored dissolved organic matter in Hudson Bay and Hudson Strait using parallel factor analysis[J]. Journal of Marine Systems, 88(3): 423-433. DOI:10.1016/j.jmarsys.2010.12.001 |
Hanekamp J C, Bast A. 2015. Antibiotics exposure and health risks:Chloramphenicol[J]. Environmental Toxicology and Pharmacology, 39(1): 213-220. DOI:10.1016/j.etap.2014.11.016 |
Heberer T. 2002. Occurrence, fate, and removal of pharmaceutical residues in the aquatic environment:a review of recent research data[J]. Toxicology Letters, 131(1/2): 5-17. |
Helms J R, Stubbins A, Ritchie J D, et al. 2008. Absorption spectral slopes and slope ratios as indicators of molecular weight, source, and photobleaching of chromophoric dissolved organic matter[J]. Limnology and Oceanography, 53(3): 955-969. DOI:10.4319/lo.2008.53.3.0955 |
Kalmykova Y, Bj rklund K, Str mvall A M, et al. 2013. Partitioning of polycyclic aromatic hydrocarbons, alkylphenols, bisphenol A and phthalates in landfill leachates and stormwater[J]. Water Research, 47(3): 1317-1328. DOI:10.1016/j.watres.2012.11.054 |
Lawaetz A J, Stedmon C A. 2009. Fluorescence intensity calibration using the raman scatter peak of water[J]. Applied Spectroscopy, 63: 936-940. DOI:10.1366/000370209788964548 |
Lead J R, Wilkinson K J. 2006. Aquatic colloids and nanoparticles:current knowledge and future trends[J]. Environmental Chemistry, 3: 159-171. DOI:10.1071/EN06025 |
Lepš J, Šmilauer P.2003.Multivariate analysis of ecological data using CANOCO[M].Cambridge: Cambridge University Press
|
李璐璐, 江韬, 闫金龙, 等. 2014. 三峡库区典型消落带土壤及沉积物中溶解性有机质(DOM)的紫外-可见光谱特征[J]. 环境科学, 35(3): 933-941. |
Li S J, Ju H Y, Ji M C, et al. 2018. Terrestrial humic-like fluorescence peak of chromophoric dissolved organic matter as a new potential indicator tracing the antibiotics in typical polluted watershed[J]. Journal of Environmental Management, 228: 65-76. |
Liao P, Zhan Z, Dai J, et al. 2013. Adsorption of tetracycline and chloramphenicol in aqueous solutions by bamboo charcoal:a batch and fixed-bed column study[J]. Chemical Engineering Journal, 228: 496-505. DOI:10.1016/j.cej.2013.04.118 |
刘娜娜, 李斌, 刘瑞霞, 等. 2014. 浑太水系水体中不同粒径有机胶体荧光光谱特性[J]. 环境科学, 35(11): 4103-4110. |
Meland S, Borgstrφm R, Heier L S, et al. 2010. Chemical and ecological effects of contaminated tunnel wash water runoff to a small Norwegian stream[J]. Science of the Total Environment, 408: 4107-4117. DOI:10.1016/j.scitotenv.2010.05.034 |
Ngueleu S K, Grathwohl P, Cirpka O A. 2013. Effect of natural particles on the transport of lindane in saturated porous media:laboratory experiments and model-based analysis[J]. Journal of Contaminant Hydrology, 149: 13-26. DOI:10.1016/j.jconhyd.2013.02.009 |
聂明华, 刘慧慧, 熊小英, 等. 2018. 南昌市湖泊水体中不同粒径胶体的三维荧光光谱特征研究[J]. 环境科学学报, 38(5): 244-253. |
Nishijima W, Speitel G E. 2004. Fate of biodegradable dissolved organic carbon produced by ozonation on biological activated carbon[J]. Chemosphere, 56: 113-119. DOI:10.1016/j.chemosphere.2004.03.009 |
Ohno T. 2002. Fluorescence inner-filtering correction for determining the humification index of dissolved organic matter[J]. Environmental Science & Technology, 36(4): 742-746. |
Peuravuori J, Pihlaja K. 1997. Isolation and characterization of natural organic matter from lake water:comparison of isolation with solid adsorption and tangential membrane filtration[J]. Environment International, 23: 441-451. DOI:10.1016/S0160-4120(97)00049-4 |
Samsonova J V, Cannavan A, Elliott C T. 2012. A critical review of screening methods for the detection of chloramphenicol, thiamphenicol, and florfenicol residues in foodstuffs[J]. Critical Reviews in Analytical Chemistry, 42(1): 50-78. |
Sapkota A, Sapkota A R, Kucharski M, et al. 2008. Aquaculture practices and potential human health risks:current knowledge and future priorities[J]. Environment International, 34(8): 1215-1226. DOI:10.1016/j.envint.2008.04.009 |
Song K, Shang Y, Wen Z, et al. 2019. Characterization of CDOM in saline and freshwater lakes across China using spectroscopic analysis[J]. Water Research, 150: 403-417. DOI:10.1016/j.watres.2018.12.004 |
Sun K, Gao B, Zhang Z, et al. 2010. Sorption of endocrine disrupting chemicals by condensed organic matter in soils and sediments[J]. Chemosphere, 80: 709-715. DOI:10.1016/j.chemosphere.2010.05.028 |
Sun K, Shi Y, Wang X, et al. 2017. Organokaolin for the uptake of pharmaceuticals diclofenac and chloramphenicol from water[J]. Chemical Engineering Journal, 330: 1128-1136. DOI:10.1016/j.cej.2017.08.057 |
Sun W L, Ni J R, Xu N, et al. 2007. Fluorescence of sediment humic substance and its effect on the sorption of selected endocrine disruptors[J]. Chemosphere, 66(4): 700-707. DOI:10.1016/j.chemosphere.2006.07.078 |
田家英, 谭睿婕, 柳玉英, 等. 2017. 基于现场检测和批试验条件下双酚A和雌二醇在沉积物上的分配系数[J]. 环境工程技术学报, 7(2): 140-145. |
Wilding A, Liu R, Zhou J L. 2005. Dynamic behaviour of river colloidal and dissolved organic matter through cross-flow ultrafiltration system[J]. Journal of Colloid and Interface Science, 287(1): 152-158. DOI:10.1016/j.jcis.2005.01.114 |
Xia X, Rabearisoa A H, Jiang X, et al. 2013. Bioaccumulation of perfluoroalkyl substances by daphnia magna in water with different types and concentrations of protein[J]. Environmental Science & Technology, 47(19): 10955-10963. |
Xiao Y H, Sara-Aho T, Hartikainen H, et al. 2013. Contribution of ferric iron to light absorption by chromophoric dissolved organic matter[J]. Limnology and Oceanography, 58: 653-662. DOI:10.4319/lo.2013.58.2.0653 |
晏彩霞.2015.长江口滨岸水中胶体对新型有机污染物环境行为的影响研究[D].上海: 华东师范大学
|
Yan C, Liu H, Sheng Y, et al. 2018. Fluorescence characterization of fractionated dissolved organic matter in the five tributaries of Poyang Lake, China[J]. Science of the Total Environment, 637: 1311-1320. |
Yan C, Nie M, Yang Y, et al. 2015a. Effect of colloids on the occurrence, distribution and photolysis of emerging organic contaminants in wastewaters[J]. Journal of Hazardous Materials, 299: 241-248. DOI:10.1016/j.jhazmat.2015.06.022 |
Yan C, Yang Y, Zhou J L, et al. 2015b. Selected emerging organic contaminants in the Yangtze Estuary, China:a comprehensive treatment of their association with aquatic colloids[J]. Journal of Hazardous Materials, 283: 14-23. DOI:10.1016/j.jhazmat.2014.09.011 |
Yang Y, Fu J, Peng H, et al. 2011. Occurrence and phase distribution of selected pharmaceuticals in the Yangtze Estuary and its coastal zone[J]. Journal of Hazardous Materials, 190(1/3): 588-596. |
余绵梓, 袁啸, 李适宇, 等. 2019. 典型PPCPs在河流沉积物中的吸附特性[J]. 中国环境科学, 39(4): 382-391. |
Zepp R G, Sheldon W M, Moran M A. 2004. Dissolved organic fluorophores in southeastern US coastal waters:correction method for eliminating Rayleigh and Raman scattering peaks in excitation-emission matrices[J]. Marine Chemistry, 89: 15-36. DOI:10.1016/j.marchem.2004.02.006 |
Zhang D, Yang S, Wang Y, et al. 2019a. Adsorption characteristics of oxytetracycline by different fractions of organic matter in sedimentary soil[J]. Environmental Science and Pollution Research, 26: 5668-5679. DOI:10.1007/s11356-018-4028-1 |
Zhang Y, Zhang B, He Y, et al. 2019b. DOM as an indicator of occurrence and risks of antibiotics in a city-river-reservoir system with multiple pollution sources[J]. Science of the Total Environment, 686: 276-289. DOI:10.1016/j.scitotenv.2019.05.439 |
Zhao H, Liu X, Cao Z, et al. 2016. Adsorption behavior and mechanism of chloramphenicols, sulfonamides, and non-antibiotic pharmaceuticals on multi-walled carbon nanotubes[J]. Journal of the Hazardous Materials, 310: 235-245. DOI:10.1016/j.jhazmat.2016.02.045 |
Zhao H, Zhou J L, Zhang J. 2015. Tidal impact on the dynamic behavior of dissolved pharmaceuticals in the Yangtze Estuary, China[J]. Science of the Total Environment, 536: 946-954. DOI:10.1016/j.scitotenv.2015.06.055 |
Zhou J L, Liu R, Wilding A, et al. 2007. Sorption of selected endocrine disrupting chemicals to different aquatic colloids[J]. Environmental Science & Technology, 41(1): 206-213. |
朱秀珍.2018.有机钾盐活化法制备活性炭及其对氯霉素吸附性能的研究[D].济南: 山东大学
|
Zsolnay A, Baigar E, Jimenez M, et al. 1999. Differentiating with fluorescence spectroscopy the sources of dissolved organic matter in soils subjected to drying[J]. Chemosphere, 38(1): 45-50. DOI:10.1016/S0045-6535(98)00166-0 |
 2020, Vol. 40
2020, Vol. 40