2. 华南理工大学环境与能源学院, 工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006;
3. 广东工业大学土木与交通工程学院, 广州 510006;
4. 韩山师范学院化学与环境工程学院, 潮州 521041
2. The Key Laboratory of Pollution Control and Ecosystem Restoration in Industrial Clusters, Ministry of Education, School of Environment and Energy, South China University of Technology, Guangzhou 510006;
3. School of Civil and Transportation Engineering, Guangdong University of Technology, Guangzhou 510006;
4. School of Chemistry and Environmental Engineering, Hanshan Normal University, Chaozhou 521041
电子垃圾拆解场地土壤中常伴随有大量Cd、Pb、Cu等重金属(叶昊等, 2015), 其形态分布特征差异大, 且具有不可降解、毒性长期持续等特点(Guo et al., 2018), 对生态环境和人体健康常造成不可逆的影响(Luo et al., 2012).化学淋洗修复因具有效率高、周期短的特点而被广泛应用于重金属污染土壤修复方面(Yao et al., 2012; Khalid et al., 2017), 应用此法的关键在于淋洗剂的选择.目前, 常用的4类典型化学淋洗剂包括人工螯合剂(Xiang et al., 2016; Zhu et al., 2019)、天然有机酸(Freitas et al., 2013; Tang et al., 2014; Tang et al., 2018)、无机盐(Liu et al., 2014)和生物表面活性剂(Maity et al., 2013; Shatrohan et al., 2018).其中, 以柠檬酸(CA)为代表的天然小分子有机酸因其去除重金属效果稳定、易在环境中降解等特点, 正逐渐取代无机酸和人工螯合剂成为土壤淋洗研究的热点(孙涛等, 2015; 马良等, 2017).目前的相关研究主要集中在新型重金属淋洗剂的开发及对土壤中重金属的淋洗效率方面(肖雪峰等, 2018; 黄启华等, 2018; 张翔等, 2019), 而对淋洗后产生的络合态重金属废水的回收处理研究较少.
土壤淋洗废液中的络合态重金属能在较宽的pH范围内稳定存在, 难以有效去除.普通的离子交换法、吸附法、铁还原法和氧化法等方法普遍存在处理费用高、产泥量大、材料再生与更新困难、易引起二次污染等问题而难以应用到实际处理中(Ashraf et al., 2019).关智杰等(2018)采用臭氧-重金属捕集剂(SN-9)体系处理络合态Ni, 发现臭氧氧化可将高稳态镍络合物氧化成易失稳的小分子Ni络合物及部分离子态Ni, 随后SN-9利用—SH可从低分子易失稳的Ni络合物上竞争夺取Ni离子形成稳定的四边形配位螯合沉淀物, 从而达到去除Ni的目的.薛璐璐等(2019)采用芬顿、高锰酸钾及过硫酸钠3种氧化法对柠檬酸络合铜、镍离子废水进行破络, 并结合加碱沉淀工艺去除铜、镍.
化学沉淀法因具有处理效果好、出水稳定可靠、工艺简单、投资少等优点而得到广泛应用(李雪莹, 2016; Deng et al., 2019).传统化学沉淀法主要为硫化物沉淀法和酸碱中和法, 其中, 硫化物沉淀比氢氧化物沉淀具有更小的溶度积, 且硫化物具备更好的重金属选择性和破络效果(曹雪峰, 2015).新型化学沉淀法是指利用具有强大络合或螯合能力的重捕剂与污水中重金属形成稳定络合物从而去除液相中重金属离子的方法(冯修等, 2016; Ma et al., 2019).目前, 国内外学者已经开展了大量关于某类重捕剂或复合型重捕剂对单一络合态重金属废水的脱络特征及优化条件的研究(肖晓等, 2016; Wang et al., 2018;Cao et al., 2019), 而有关分离CA-Cd、CA-Pb、CA-Cu复合络合态重金属污染废水的研究还相对匮乏.
实际的土壤淋洗废液组成复杂, 为能更好地探究沉淀剂对淋洗废液的作用机理, 本研究根据邢宇(2014)的方法对柠檬酸淋洗实际土壤后的淋洗废液的主要组成进行分析, 并配置成模拟土壤淋洗废液.并以硫化钠(Na2S)、乙基黄原酸钾(PEX)、二甲基二硫代氨基甲酸钠(DTC)作为重金属沉淀剂, 采用振荡混匀法考察各沉淀剂在不同投加量时对柠檬酸络合态Cd、Pb、Cu模拟废水的分离效率, 从中筛选出较为理想的重金属沉淀剂.在此基础上, 采用单因素实验探究反应温度、沉淀剂投加量、初始pH值对理想沉淀剂分离CA-Cd、CA-Pb、CA-Cu的影响.同时, 采用Visual MINTEQ ver 3.1软件模拟S2-投加前后液相重金属的形态分布, 并采用SEM-EDS、XRD对反应产物表征分析, 以推测Na2S分离CA-Cd、CA-Pb、CA-Cu的机理, 旨在为同步去除土壤淋洗废液中络合态重金属和实现淋洗液的回收提供理论依据.
2 材料与方法(Materials and methods) 2.1 实验试剂与材料硫化钠、柠檬酸、氯化镉、硝酸铅购自国药集团化学试剂有限公司, PEX购于麦克林, 氢氧化钠、盐酸、硝酸铜购自天津市大茂化学试剂厂, DTC购自阿拉丁公司, 无水乙醇购自广州化学试剂厂, 以上试剂均为分析纯;实验用水均为去离子水.
实验模拟废水根据实际土壤淋洗状况采用过量的柠檬酸和一定量的氯化镉、硝酸铜和硝酸铅配置而成, 其中, Cu2+、Pb2+、Cd2+浓度分别为200、50、2.00 mg·L-1, 柠檬酸浓度为0.10 mol·L-1, 并用0.1 mol·L-1 NaOH溶液调节废水pH至5.0±0.2(刑宇, 2014).
2.2 实验方法 2.2.1 沉淀剂对络合态重金属分离效果的比较在(27.0±0.5) ℃下, 取50 mL模拟废水于100 mL厌氧瓶中, 通氮气15 min后, 分别向其中投入一定量的沉淀剂,使溶液中Na2S、PEX和DTC的浓度分别为1.8、2.8、3.8、4.8、5.8、6.8、7.8、8.8、9.8、10.8、11.8、12.8 mmol·L-1;再通氮气10 s后, 加塞, 置于恒温摇床中以150 r·min-1转速振荡60 min, 静置10 min;取上清液经0.45 μm膜过滤后, 用火焰原子吸收分光光度计法(HITACHI, Z-2300型)分别测定反应前后溶液中Cd2+、Pb2+、Cu2+的浓度, 并用高效液相色谱法(Agilent, 1200型)测定反应前后溶液中柠檬酸根离子的浓度, 每组实验重复3次.
2.2.2 反应温度对络合态重金属分离效果的影响取50 mL模拟废水于100 mL厌氧瓶中, 通氮气15 min后, 将其分别加热至20、25、30、35、40、45、50 ℃;向厌氧瓶中投入一定量的Na2S,使溶液中Na2S浓度为4.8 mmol·L-1, 再通氮气10 s后, 加塞, 置于恒温摇床中以150 r·min-1转速振荡60 min, 静置10 min;取上清液经0.45 μm膜过滤后, 测定反应前后溶液中Cd2+、Pb2+、Cu2+及柠檬酸根离子的浓度, 每组实验重复3次.
2.2.3 Na2S投加量对重金属去除的影响在(27.0±0.5) ℃下, 取50 mL模拟废水于100 mL厌氧瓶中, 通氮气15 min后, 分别向其中投入一定量的Na2S,使溶液中Na2S的浓度分别为1.8、2.8、3.8、4.8、5.8、6.8、7.8、8.8、9.8、10.8、11.8、12.8 mmol·L-1;再通氮气10 s后, 加塞, 置于恒温摇床中以150 r·min-1转速振荡60 min, 静置10 min;取上清液经0.45 μm膜过滤后, 测定反应前后溶液中Cd2+、Pb2+、Cu2+的浓度, 每组实验重复3次.
2.2.4 溶液初始pH值对Na2S分离络合态重金属及重金属形态变化的影响在(27.0±0.5) ℃下, 用0.1 mol·L-1的盐酸或氢氧化钠溶液调节模拟废水的pH值为3、5、7、9, 并取50 mL相应的模拟废水于100 mL厌氧瓶中, 向厌氧瓶中投入一定量的Na2S,使溶液中Na2S浓度为4.8 mmol·L-1;再通氮气10 s后, 加塞, 置于恒温摇床中以150 r·min-1转速振荡60 min, 静置10 min;取上清液经0.45 μm膜过滤后, 测定反应前后溶液中Cd2+、Pb2+、Cu2+及柠檬酸根离子的浓度, 每组实验重复3次.并采用Visual MINTEQ ver 3.1软件预测模拟土壤淋洗废液中投加S2-前后Cd、Pb、Cu的形态分布.
2.2.5 反应产物的表征将Na2S与模拟土壤淋洗废液反应后的混合液经布氏漏斗固液分离后, 用蒸馏水和乙醇分别冲洗2次, 并于-20 ℃冷冻干燥后得到固体.通过场发射扫描电镜和能谱扫描(SEM-EDS)分析沉淀固体的形态和表面成分;使用X射线衍射仪(XRD)于10°~80°进行常规扫描以探究沉淀固体组成.
3 结果与讨论(Results and discussion) 3.1 沉淀剂对络合态重金属分离效果的比较不同重金属沉淀剂对模拟废水中Cd2+、Pb2+、Cu2+去除率和CA回收率的影响如图 1所示.由图可知:随沉淀剂浓度不断增大, Na2S、PEX、DTC对CA-Cd、CA-Pb、CA-Cu的去除率显著增大.当Na2S浓度为4.8 mmol·L-1时, 模拟废水中Cd2+、Pb2+、Cu2+的去除趋于稳定, 去除率分别达到99.79%、99.03%和99.19%;当PEX浓度为10.8 mmol·L-1时, Cd2+、Pb2+、Cu2+的去除趋于稳定, 去除率分别达到93.20%、99.57%和98.10%;当DTC浓度为12.8 mmol·L-1时, Cd2+、Pb2+、Cu2+的去除趋于稳定, 去除率分别达到98.63%、99.37%和99.21%.由此可见, Na2S、PEX、DTC对CA-Cd、CA-Pb、CA-Cu的去除均呈现出较好的效果.
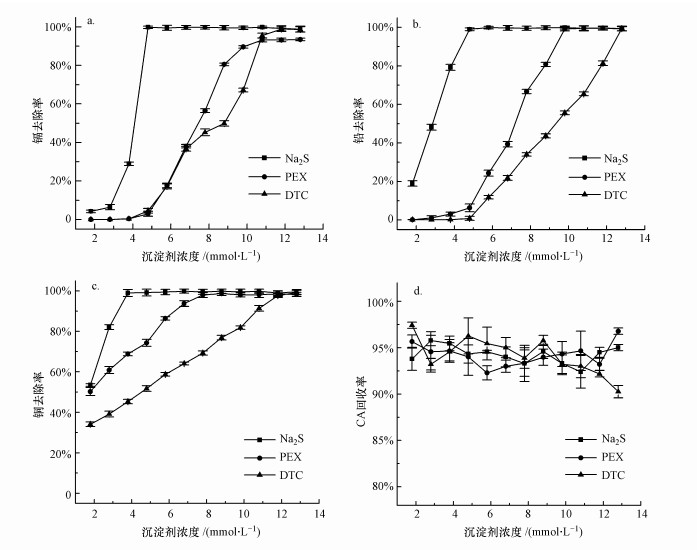 |
| 图 1 不同沉淀剂对重金属(a.镉, b.铅, c.铜)去除率和CA回收率(d)的影响 Fig. 1 Removal rates of heavy metals(a.Cd, b.Pb, c.Cu) by different precipitants and recovery rate of CA(d) |
PEX分子含有二硫代羧酸根(—CS2), 其能以配位键或共价键形式与重金属离子M2+反应生成稳定的具有交联空间网状结构的不溶性重金属螯合沉淀(Chang et al., 2007), 从而有效去除液相中的重金属离子.在实验中观察到大量黄色沉淀生成, 说明—CS2与Cd2+、Pb2+、Cu2+反应生成螯合物, 且随着PEX投加量的增大, 溶液中沉淀物显著增多, 重金属去除率显著增大.这与王刚(2013)用自制PEX处理有机络合态镉的研究发现一致, 且该研究还发现柠檬酸的存在可促进二硫代羧基的电离, 从而促进对溶液中重金属离子的去除.
DTC分子在结构上与PEX分子相似, 两者均属于巯基重金属捕集剂, 且其与重金属离子反应的原理与PEX基本一致, 均依靠—CS2捕捉溶液中的重金属离子, 且两种重金属沉淀剂去除络合态重金属的先后顺序均为Cu2+> Pb2+> Cd2+, 这与前人的研究结果一致(Xiang et al., 2016; 陈辉等, 2018).
由图 1d可知, Na2S、PEX、DTC处理组CA的回收率均保持在90%以上, 这表明柠檬酸在各沉淀剂沉淀重金属的过程中损耗较少, 因此, 可通过脱络方式实现柠檬酸再生回收.然而, 在获得相同重金属去除率的情况下, 各重金属沉淀剂的用量依次为DTC(12.8 mmol·L-1)>PEX (10.8 mmol·L-1)>Na2S(4.8 mmol·L-1).因此, 本文选择Na2S做进一步探究.
3.2 反应温度对络合态重金属分离效果的影响反应温度对重金属去除率和CA回收率的影响如图 2所示, 由图可知, 当温度为20~50 ℃时, 重金属去除率无显著变化, 均保持在91.12%~99.11%.主要原因是Na2S易受热分解成H2S气体逸于气相中, 但由于反应体系密闭且反应时间较长, 逸于气相中的S2-在与液面不断碰撞中回溶至液相参与重金属沉淀反应, 导致重金属去除率变化不明显.由图 2b可知, 随着温度的提高, CA回收率由96.10%下降至92.50%.
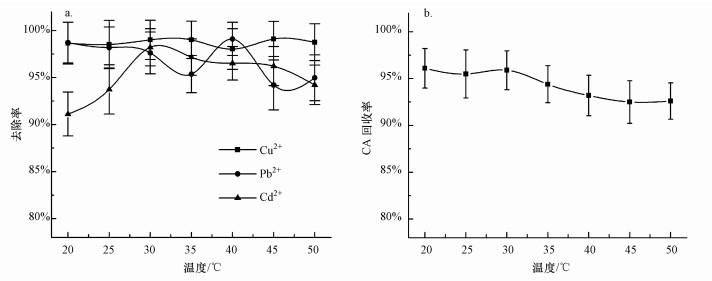 |
| 图 2 反应温度对重金属去除率(a)和CA回收率(b)的影响 Fig. 2 Effect of reaction temperature on removal rate of heavy metals(a) and recovery rate of CA(b) |
Na2S投加量对废液中重金属去除率的影响如图 3所示, 由图可知, Na2S浓度为0~5 mmol·L-1时, Cd2+、Pb2+和Cu2+的去除率均随Na2S浓度的增大而显著上升, 其中, 当Na2S的投加量为3.8 mmol·L-1时, 混合液中Cu2+的去除率为98.99%, 而Pb2+、Cd2+的去除率仅分别为79.22%、28.91%.但随着Na2S的投加量增大到4.8 mmol·L-1时, Cd2+、Pb2+、Cu2+的去除率均能达到99%以上.从重金属离子的去除顺序来看, Cu、Pb、Cd依次从溶液中去除, 这一现象可能与反应产物CuS、PbS和CdS的溶解度依次递增有关, 25 ℃时, Ksp(CuS)= 6.3×10-36 < Ksp(PbS)= 8.0×10-28 < Ksp(CdS)= 8.0×10-27, Ksp越小的物质越先从溶液中分离出来(郭燕妮等, 2011).由图还可知, 使重金属完全沉淀时的Na2S实际投加量(4.8 mmol·L-1)大于理论投加量(3.4 mmol·L-1).这说明仍有部分S2-以H2S的形式存在于气相或液相中不参与反应(Flávia et al., 2013).
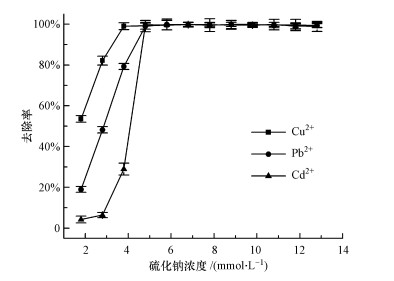 |
| 图 3 Na2S投加量对废液中重金属去除率的影响 Fig. 3 Effect of Na2S dosage on removal rate of heavy metals in wastewater |
Na2S投加量是处理废液中重金属的关键因素.Na2S投加量过小, 则重金属沉淀不完全, Na2S投加量过大, 则不仅会浪费药剂、增加成本, 还会导致处理后出水含有较多的S2-、HS-甚至出现多硫化重金属结合物MS22-、MS32-等.因此, 本文选择Na2S投加量为4.8 mmol·L-1做进一步探究.
3.4 溶液初始pH值对Na2S分离络合重金属及重金属形态变化的影响Na2S在酸性条件下易产生H2S气体, 从而影响对重金属的去除.因此, 本文讨论了各初始pH值对Na2S去除Cd2+、Pb2+、Cu2+及回收CA效果的影响, 并对S2-投加前后重金属的形态变化进行探究, 以揭示其在不同pH值下对重金属的捕捉机理.
3.4.1 溶液初始pH值对Na2S分离柠檬酸络合态重金属的影响初始pH值对废水中重金属去除率及CA回收率的影响如图 4所示.由图可知, 在初始pH为3~9时, Na2S对Cd2+、Pb2+的去除率逐渐增加而后趋于稳定, Cd2+去除率从91.74%增至97.78%, Pb2+去除率从89.22%增至99.23%, 而对Cu2+去除率无显著影响, 去除率均保持在98.5%以上, 这表明初始pH值对Na2S沉淀Cd2+、Pb2+、Cu2+无显著影响. CA回收率受初始pH影响不显著, 回收率均保持在93%以上.
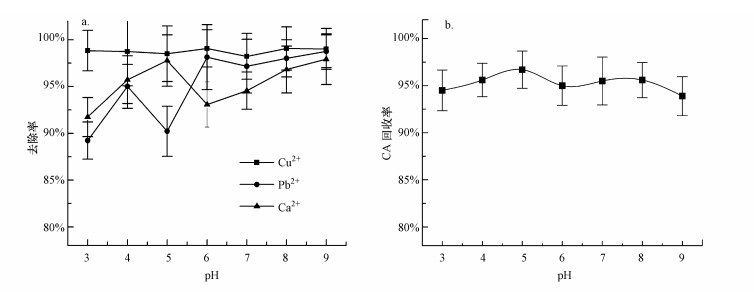 |
| 图 4 初始pH值对废水中重金属去除率(a)及CA回收率(b)的影响 Fig. 4 Effect of initial pH on removal of heavy metals from wastewater by Na2S(a) and recovery of CA(b) |
溶液中重金属离子浓度、螯合物稳定性及金属配合物的物相分布会随pH值的变化而变化.由Visual MINTEQ模拟数据(图 5)可知, S2-投加前液相中的Cd/Pb/Cu-CA配合物主要以完全去质子化形式(CdCA-、PbCA-、CuCA-)分别存在于pH为4.5~12.5、4.5~12、4.5~11.5之间的溶液中.但当pH为0~5时, 溶液中主要的配合物种类分别是CdH2CA+、CdHCA(aq)、Cd2OH3+、CdCA-、PbH2CA+、PbHCA(aq)、PbCA-、Cu3(OH)42+、CuCA-、CuH2CA+等, 而Cd(OH)2(aq)、Cd(OH)3-、Cd(CA)42-、Pb(OH)3-、Pb(OH)2(aq)、Cu(OH)42-、Cu(OH)3-等主要存在于pH大于10的溶液中.
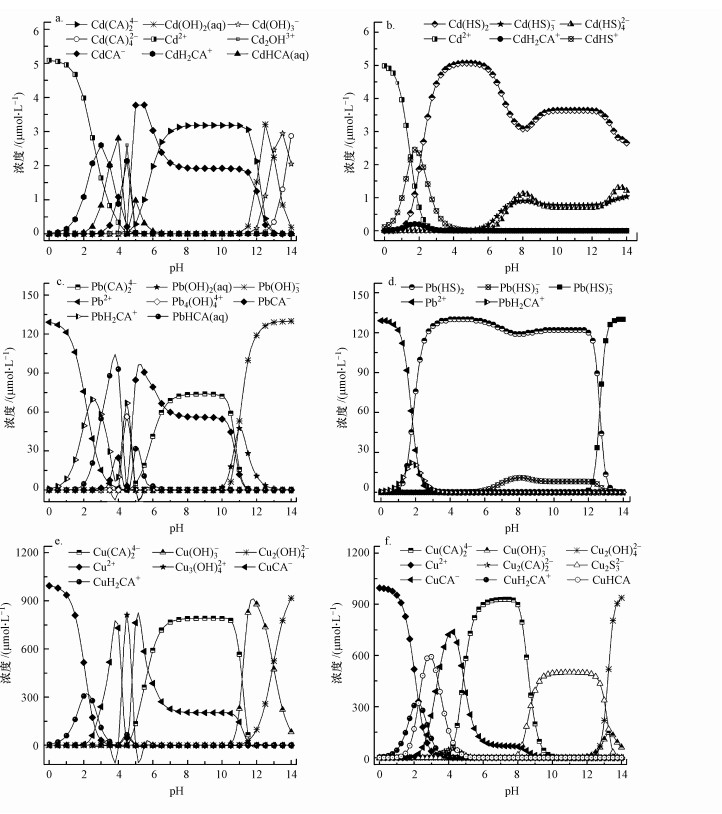 |
| 图 5 不同pH值条件下S2-投加前后模拟废水中重金属的主要物相分布 (a, b.Cd2+形态分布, c, d.Pb2+形态分布, e, f.Cu2+形态分布;a、c、e为投加量前, b、d、f为投加后) Fig. 5 The main phase distribution of heavy mtals in simulated wastewater before and after S2- dosing at different pH values |
由图 5可知, S2-投加后液相中Cd(HS)2、Cd(HS)3-、Cd(HS)42-、CdHS+、Pb(HS)2、Pb(HS)3-、Cu2S32-明显增多, 说明当投入Na2S后, 溶液中存在大量HS-和S2-, 即发生式(1)、(2)所示的反应.
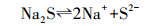
|
(1) |
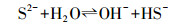
|
(2) |
当pH在2~5时, S2-投加前溶液中重金属配合物主要以CuHCA、PbHCA、CdHCA等易失稳状态存在, 可为S2-或HS-与HCA-结合态重金属发生反应创造更有利的条件.重金属配合物常含有配位水分子, 其可与其它配体(如NH3和OH-)交换(Thomas et al., 2015), 但由于S2-或HS-配体对重金属离子位点的亲和力比OH-更强(Nag et al., 2011), 使得S2-或HS-对CA、HCA-等形式结合的重金属具有较强的去除能力.且从整体上看, 随着初始pH值的增大, S2-投加后溶液中S2-和HS-结合态重金属的浓度呈显著增大趋势.
3.5 Na2S与模拟废水反应后产物的表征 3.5.1 SEM-EDS为探究pH对产物形貌的影响, 对pH=5、7条件下Na2S与Cd/Pb/Cu-CA完全反应后产生的样品形态进行SEM表征, 结果如图 6所示.图中硫化物产物主要以团聚、成簇和圆片状分布存在, 这种形态可能是由表面聚集和沉降的CuS、CdS、PbS、CuPbS2等物质造成.对比不同pH处理下的SEM图像可知, 当pH=7时, 颗粒与颗粒之间能够形成凝聚层并呈片状结构存在, 粒径较大, 且含夹着小片状物质;但当pH为5时, 片状大小较为均一, 颗粒粒径较小, 更有益于固液分离.同时, 通过pH=5时反应产物EDS谱图(图 7)发现, 沉淀物中Cd:Pb:Cu:S元素比例约为1:20:80:100, 与预配溶液浓度基本相符, 证明产物中S与Cd、Pb、Cu以1:1比例生成沉淀.
 |
| 图 6 沉淀产物SEM图(a.pH=5;b.pH=7) Fig. 6 SEM image of precipitated product |
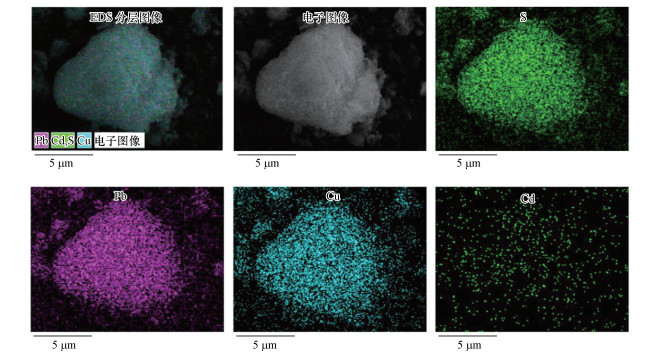 |
| 图 7 pH=5时反应产物的EDS图像 Fig. 7 EDS image of reaction product at pH=5 |
在pH=5、温度(27.0±0.5) ℃、Na2S浓度4.8 mmol·L-1条件下反应沉淀物的XRD衍射图如图 8所示.结果显示, 沉淀物的主要成分为CuS, 并掺杂有少量CdS、PbS和CuPbS2.图谱中CuS峰宽较大, 根据Debye-Scherrer公式可推断CuS颗粒尺寸较小.CdS所对应的衍射峰峰型尖锐, 半峰宽小, 表明沉淀产物中CdS具有较为完整的结晶度, 但在XRD图谱上还存在明显的散杂峰型, 这表明生成的3种重金属硫化混合物形态结构不稳定, 且含有一定的杂质.
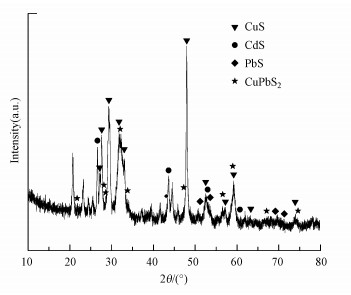 |
| 图 8 反应产物的XRD图谱 Fig. 8 XRD pattern of reaction product |
Na2S、PEX、DTC对分离柠檬酸络合态镉、铅、铜均有良好的效果, 其去除重金属效果的优异顺序依次为Na2S> PEX >DTC, 三者对柠檬酸的回收率均保持在90%以上.反应温度、初始pH值均对Na2S处理络合态重金属无显著影响, S2+与Cd2+、Pb2+、Cu2+以1:1比例生成沉淀, 沉淀物大多为圆饼片状结构, 其中包含CuS、CdS、CuPbS2和PbS等物质.
Ashraf S, Ali Q, Zahir Z A, et al. 2019. Phytoremediation:Environmentally sustainable way for reclamation of heavy metal polluted soils[J]. Ecotoxicology and Environmental Safety, 174: 714-727. |
曹海峰. 2015. 络合态重金属废水处理技术研究进展[J]. 工业水处理, 35(11): 14-17+91. |
Cao Y, Qian X C, Zhang Y X, et al. 2019. Decomplexation of EDTA-chelated copper and removal of copper ions by non-thermal plasma oxidation/alkaline precipitation[J]. Chemical Engineering Journal, 362: 487-496. |
Chang Q, Wang G. 2007. Study on the macromolecular coagulant PEX which traps heavy metals[J]. Chemical Engineering Science, 62(17): 4636-4643. |
陈辉, 陆勇刚, 程东旭, 等. 2018. 新型DTC类络合重金属捕集剂的合成及其在废水处理中的应用[J]. 环境工程学报, 12(3): 731-740. |
Deng Z, Oraby E A, Eksteen J J. 2019. The sulfide precipitation behaviour of Cu and Au from their aqueous alkaline glycinate and cyanide complexes[J]. Separation and Purification Technology, 218: 181-190. |
冯修, 马楠楠, 职红涛, 等. 2018. 重金属捕集剂UDTC对低浓度镉废水的处理研究[J]. 广西师范大学学报(自然科学版), 36(3): 63-67. |
Flávia D R, Adarlene M S, Emanoelle C C, et al. 2013. Application of sodium- and biogenic sulfide to the precipitation of nickel in a continuous reactor[J]. Separation and Purification Technology, 120: 346-353. |
Freitas E V, Nascimento C W, Souza A, et al. 2013. Citric acid-assisted phytoextraction of lead:A field experiment[J]. Chemosphere, 92(2): 213-217. |
关智杰, 郭艳平, 区雪连, 等. 2019. 臭氧预破络-重金属捕集耦合体系高效去除废水中络合态镍的机理研究[J]. 环境科学学报, 39(6): 1754-1762. |
Guo X F, Zhao G H, Zhang G X, et al. 2018. Effect of mixed chelators of EDTA, GLDA, and citric acid on bioavailability of residual heavy metals in soils and soil properties[J]. Chemosphere, 209: 776-782. |
黄启华.2018.重金属捕集剂HDTC的制备及其应用性能研究[D].昆明: 昆明理工大学 http://cdmd.cnki.com.cn/Article/CDMD-10674-1018715481.htm
|
郭燕妮, 方增坤, 胡杰华, 等. 2011. 化学沉淀法处理含重金属废水的研究进展[J]. 工业水处理, 31(12): 9-13. |
Khalid S, Shahid M, Niazi N K, et al. 2017. A comparison of technologies for remediation of heavy metal contaminated soils[J]. Journal of Geochemical Exploration, 182: 247-268. |
Liu J Y, Zeng J J, Sun S Y, et al. 2016. Combined effects of FeCl3 and CaO conditioning on SO2, HCl and heavy metals emissions during the DDSS incineration[J]. Chemical Engineering Journal, 299: 449-458. |
李雪莹.2016.巯基化合物修饰碳纳米材料及其对重金属废水的处理研究[D].长沙: 湖南大学 http://cdmd.cnki.com.cn/Article/CDMD-10532-1016253756.htm
|
Luo X S, Ding J, Xu B, et al. 2012. Incorporating bioaccessibility into human health risk assessments of heavy metals in urban park soils[J]. Science of the Total Environment, 424: 88-96. |
Maity J P, Huang Y M, Hsu C M, et al. 2013. Removal of Cu, Pb and Zn by foam fractionation and a soil washing process from contaminated industrial soils using soapberry-derived saponin:A comparative effectiveness assessment[J]. Chemosphere, 92(10): 1286-1293. |
Ma W C, Chen D M, Pan M H, et al. 2019. Performance of chemical chelating agent stabilization and cement solidification on heavy metals in MSWI fly ash:A comparative study[J]. Journal of Environmental Management, 247: 169-177. |
马良, 秦余丽, 蔡璐瑶, 等. 2017. 小分子有机酸诱导野苋菜修复Pb污染土壤[J]. 环境工程学报, 11(6): 3861-3865. |
Nag A, Kovalenko M V, Lee J S, et al. 2011. Metal-free inorganic ligands for colloidal nanocrystals:S2-, HS-, Se2-, HSe-, Te2-.HTe32-, OH-, and NH2- as surface ligands[J]. Journal of the American Chemical Society, 133(27): 10612-10620. |
Shatrohan L, Sheel R, Olfa B S, et al. 2018. Biosurfactant and exopolysaccharide-assisted rhizobacterial technique for the remediation of heavy metal contaminated soil:An advancement in metal phytoremediation technology[J]. Environmental Technology & Innovation, 10: 243-263. |
孙涛, 毛霞丽, 陆扣萍, 等. 2015. 柠檬酸对重金属复合污染土壤的浸提效果研究[J]. 环境科学学报, 35(8): 2573-2581. |
Tang Q, Gu F, Gao Y F, et al. 2018. Desorption characteristics of Cr(Ⅲ), Mn(Ⅱ), and Ni(Ⅱ) in contaminated soil using citric acid and citric acid-containing wastewater[J]. Soils and Foundations, 58(1): 50-64. |
Tang W W, Zeng G M, J L, et al. 2014. Impact of humic/fulvic acid on the removal of heavy metals from aqueous solutions using nanomaterials:A review[J]. Science of the Total Environment, 468-469: 1014-1027. |
Thomas S A, Gaillard J F. 2015. The molecular structure of aqueous Hg(Ⅱ)-EDTA as determined by X-ray Absorption Spectroscopy[J]. Journal of Physical Chemistry A, 119(12): 2878-2884. |
王刚.2013.重金属絮凝剂聚乙烯亚胺基黄原酸钠的制备及性能研究[D].兰州: 兰州交通大学 http://d.wanfangdata.com.cn/Thesis_D540043.aspx
|
Wang Q W, Chen J J, Zheng A H, et al. 2019. Dechelation of Cd-EDTA complex and recovery of EDTA from simulated soil-washing solution with sodium sulfide[J]. Chemosphere, 220: 1200-1207. |
Xiang B, Fan W, Yi X W, et al. 2016. Dithiocarbamate-modified starch derivatives with high heavy metal adsorption performance[J]. Carbohydrate Polymers, 136: 30-37. |
肖晓, 孙水裕, 严苹方, 等. 2016. 高效重金属捕集剂EDTC的结构表征及对酸性络合铜的去除特性研究[J]. 环境科学学报, 36(2): 537-543. |
肖雪峰, 孙永军, 沈浩, 等. 2018. CSC-P(AM-AA)重金属捕集絮凝剂的光谱表征及其对重金属去除研究[J]. 光谱学与光谱分析, 38(6): 1809-1813. |
邢宇.2014.电子垃圾污染场地土壤中重金属的淋洗去除研究[D].广州: 华南理工大学 http://cdmd.cnki.com.cn/Article/CDMD-10561-1014064432.htm
|
薛璐璐, 袁翔, 朱梦羚, 等. 2019. 高级氧化法破络处理柠檬酸铜镍电镀废水[J]. 净水技术, 38(3): 9-14+50. |
Yao Z T, Li J H, Xie H H, et al. 2012. Review on remediation technologies of soil contaminated by heavy metals[J]. Procedia Environmental Sciences, 16: 722-729. |
叶昊, 李良忠, 向明灯, 等. 2015. 电子垃圾拆解场地土壤重金属和溴代阻燃剂的污染现状及其对生态环境和人体健康影响[J]. 环境卫生学杂志, 5(3): 293-297. |
张翔, 冯修, 职红涛, 等. 2019. 重金属捕集剂TDDP的合成及性能研究[J]. 郑州大学学报(工学版), 40(3): 48-51. |
Zhu Y, Fan W H, Zhou T T, et al. 2019. Removal of chelated heavy metals from aqueous solution:A review of current methods and mechanisms[J]. Science of the Total Environment, 678: 253-266. |
 2020, Vol. 40
2020, Vol. 40


