2. 中国科学院生态环境研究中心环境化学与生态毒理学国家重点实验室, 北京 100085;
3. 北京联合大学生物化学工程学院, 北京 100023
2. State Key Laboratory of Environmental Chemistry and Ecotoxicology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085;
3. College of Biochemical Engineering, Beijing Union University, Beijing 100023
自双酚A(BPA)被禁用以来, 双酚S(BPS)就作为BPA的替代产品被广泛地用于聚碳酸酯、环氧树脂、聚酯、酚醛树脂等高分子材料的生产, 或作为中间体制备农药、染料、固色剂、皮革鞣剂和阻燃剂等化工产品(Changkhamchom et al., 2010;罗世鹏等, 2014).据统计, 仅欧共体国家每年生产和进口的BPS量就高达1~10万吨(ECHA, 2019;Hu et al., 2019).这些BPS最终不可避免地会随着工业废水的排放、污水污泥的施用和工业制品的渗出进入到自然水体和土壤环境中, 成为环境污染的潜在隐患(Wu et al., 2018).目前人们已经在自然水体(0~6840 ng·L-1)、沉积物(0.002~1970 ng·g-1干重)、市政污泥(0.17~110 ng·g-1干重)、食品甚至人体尿液等许多环境介质中检测到BPS的存在, 并且发现其含量呈逐年上升的趋势(Choi et al., 2017).近年来的研究表明, BPS并不是一个安全的替代产品, BPS同BPA一样也具有内分泌干扰效应.很低浓度的BPS就可以引起动物生殖和甲状腺系统的紊乱(Qiu et al., 2016; Gingrich et al., 2018; Speidel et al., 2018)、蛋白酶失活(Rosenmai et al., 2014)、视网膜损伤(刘文敏等, 2018)、阻碍大脑发育(Kinch et al., 2015)甚至诱导心血管病的发生(Pal et al., 2017)等.因此, 了解环境中BPS的吸附解吸行为和迁移规律, 对正确评价和降低BPS的生态健康风险具有重要的意义.从当前的研究现状看, 有关BPS的研究大多集中在环境调查和毒性方面(袁琳嫣, 2017;李晓蒙等, 2018;沈杰等, 2018).虽然近年来已有多项关于BPS在土壤中吸附行为的工作, 并且发现土壤有机质和pH是影响BPS吸附的关键因素(Choi et al., 2017; Zhang et al., 2019; Shi et al., 2019).但关于BPS在中国不同地带性土壤中吸附特征的研究还很少, 尤其是缺乏BPS解吸的相关数据.
黑土和红壤是我国重要的两种土壤, 占我国耕地面积的比重很大.因此, 本文选择这两种性质差别比较大的东北黑土和江西红壤作为研究对象, 探究BPS在这两种土壤中的吸附动力学、吸附热力学及其解吸行为.通过它们之间性质的对比和溶液条件的改变, 揭示BPS在两种土壤中吸附解吸的特征.以期为研究BPS在土壤中的迁移规律和生态治理提供有力的数据支持.
2 材料与方法(Materials and methods) 2.1 实验材料实验所用土壤分别采自黑龙江省克山县和江西省鹰潭市的表层耕作土(0~20 cm), 置于阴凉通风处, 经自然风干, 混匀研碎及1.0 mm筛筛分, 储存于广口瓶中备用.黑土的部分物理化学性质为:有机质69.0 g·kg-1、阳离子交换容量32.7 cmol·kg-1、pH=7.3和比表面积19.4 m2·g-1.红壤的部分物理化学性质为:有机质7.0 g·kg-1、阳离子交换容量14.7 cmol·kg-1、pH=5.3和比表面积31.7 m2·g-1.详细信息可参考先前的工作(Pei et al., 2006).BPS、BPA和二苯砜(DS)购自百灵威科技有限公司, 纯度均为99.0%.3种化合物的部分物理化学性质如表 1所示.氯化钠和叠氮化钠均为分析纯, 购自国药集团化学试剂(北京)有限公司.甲醇为色谱纯, 实验所用其它试剂均为分析纯以上, 实验用水为默克公司(Merck Milliproe德国)提供的超纯水.
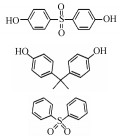
| 表 1 BPS、BPA和DS的化学结构及部分物理化学性质 Table 1 Chemical structure and selected properties of BPS, BPA, and DS |
BPS溶于0.01 mol·L-1 NaCl的支持电解质溶液中, 并加入0.1 g·L-1的NaN3用于抑制微生物的生长.准确称取2.0 g土壤于40.0 mL的玻璃离心管中, 加入20.0 mL 0.01 mol·L-1的NaCl支持电解质溶液, 其中BPS的浓度为5.0 mg·L-1.用聚四氟乙烯内衬的螺旋盖封闭.为了避光, 用铝箔包覆管壁.在298 K条件下以100 r·min-1的速度持续振荡.样品在不同的平衡时间内被分别取出, 以3000 r·min-1的速率离心20 min后, 取上清液并过0.22 μm聚四氟乙烯滤膜, 利用高效液相色谱(HPLC)测定滤液中BPS的浓度.
2.2.2 吸附等温线实验称2.0 g土壤于40.0 mL的玻璃离心管中, 并加入20.0 mL含有不同浓度BPS(1.0、5.0、10.0、15.0、20.0、30.0和50.0 mg·L-1)的支持电解质溶液.把离心试管放入恒温振荡培养箱振荡24.0 h, 反应温度分别设置为298、308和318 K.振荡完毕, 在3000 r·min-1下离心20.0 min后取上清液过0.22 μm聚四氟乙烯滤膜, 利用HPLC测定滤液中BPS的浓度.
2.2.3 溶液pH对BPS吸附的影响准确称取2.0 g土壤于40.0 mL的玻璃离心管中, 加入20.0 mL 5.0 mg·L-1的BPS溶液, 然后用0.1 mol·L-1的HCl或NaOH调节溶液pH至2.0~10.0.把离心试管放入摇床振荡24 h, 反应温度为298 K.在这个过程中, 调节pH两次.振荡完毕, 在3000 r·min-1下离心20.0 min后取上清液过0.22 μm聚四氟乙烯滤膜, 利用HPLC测定滤液中BPS的浓度.
2.2.4 BPS在土壤中的解吸行为研究吸附实验完毕后, 离心分出固液体, 并取10.0 mL上清液用HPLC测定BPS的浓度.然后在试管中再加入10.0 mL支持电解质溶液, 继续振荡24 h.这个过程被重复3次, 每次上清液中BPS的浓度都通过HPLC测定.解吸实验中BPS的解吸量通过解吸前后吸附质浓度的变化来计算.
2.2.5 BPS、BPA和DS在两种土壤中的吸附行为比较在40.0 mL玻璃离心管中加入2.0 g土壤后, 分别加入20.0 mL不同浓度的BPS(5.0、10.0、20.0和50.0 mg·L-1)、BPA(1.0、5.0、10.0、15.0、20.0、30.0和50.0 mg·L-1)和DS(0.1、0.6、1.0、2.0、4.0、6.0、10.0和15.0 mg·L-1)溶液, 反应温度为298 K, 其它步骤同2.2.2节.
2.2.6 测定方法水相中BPS的浓度通过HPLC(Agilent 1200)测定.仪器配有紫外检测器, 色谱柱为安捷伦SB-C18柱(100 mm× 2.0 mm, dp 5 μm), 流动相为V(甲醇):V(水)=40:60, 检测波长为258 nm, 流速为1.0 mL·min-1, 进样量为15.0 μL.吸附到两种土壤上BPS的量, 可以通过吸附平衡后上清液中BPS的量与外加BPS量的差值换算得到.另外相同条件下, 在空白离心管中只加BPS溶液而不加入土壤, BPS的回收率大于98%, 表明实验过程中的BPS的损失可以忽略不计.
3 结果与讨论(Results and discussion) 3.1 BPS在两种土壤中的吸附动力学研究图 1是BPS在两种土壤中的吸附动力学曲线.从图中可以看出, BPS在两种土壤中的吸附趋势不尽相同.在红壤中, BPS的吸附速率非常快, 在最初的2.0 h左右就达到了吸附平衡.继续增加吸附时间, BPS在红壤上的吸附容量增加并不明显.而在黑土中, BPS的吸附过程包括3个阶段:开始的快速吸附阶段、随后的慢吸附阶段和最后的平衡阶段.BPS的吸附在第一阶段增加比较明显, 0.5 h的吸附容量就占到BPS总吸附容量的63.0%左右, 这与在红壤中的情况类似.在第二个阶段, BPS的吸附增加变的较为缓慢, 可以认为这是其慢速扩散进入土壤有机质或黑炭刚性微孔中的缘故(Huang et al., 2003).Pignatello和Xing (1996)曾把土壤有机质分为溶解相和孔隙填充相两个部分, 认为有机污染物在溶解相上的吸附是一个分配过程, 具有较大的扩散系数, 吸附速率都很快, 而在孔隙填充相中的吸附则要慢的多, 是造成慢吸附的主要原因.另外相较而言, BPS在黑土中的吸附容量要高于红壤.这主要是由于黑土具有高的有机质含量, 提供了更多的吸附位点, 使BPS可以通过疏水性作用和π-π等作用吸附在土壤中.近来的研究也表明, 土壤有机质和黑炭是影响BPS吸附的主要控制因素(Choi et al., 2017;Zhang et al., 2019).
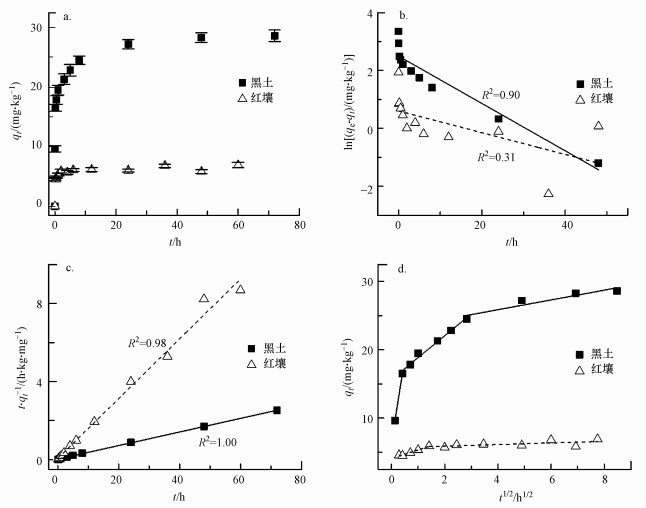 |
| 图 1 BPS在两种土壤上吸附动力学曲线(a)、拟一级动力学(b)、拟二级动力学(c)和颗粒内扩散(d)模型拟合结果 Fig. 1 Sorption kinetics of BPS in two soils(a), pseudo first-order rate equation (b), pseudo second-order rate equation (c) and intra-particle diffusion equation (d) |
对于污染物的吸附行为而言一般存在有3个过程:①液膜扩散, 也叫外扩散, 是指吸附质从溶液中扩散到吸附剂外表面的过程;②内扩散, 是指吸附质从吸附剂的外表面扩散到内表面的过程, 而这一过程又先后分为大孔扩散和微孔扩散过程;③吸附质在吸附点位上的吸附.污染物的吸附行为主要受哪一过程控制可以通过不同的动力学模型拟合得到.根据先前的文献, 拟一级动力学模型假设液膜扩散是吸附过程的速率控制步骤;拟二级吸附动力学模型假设化学吸附是吸附的速率控制步骤;颗粒内扩散模型假设内扩散是吸附的速率控制步骤.为了进一步了解BPS在土壤中的吸附过程, 本研究分别利用拟一级动力学模型、拟二级动力学模型和颗粒扩散模型对动力学数据进行拟合(Liu et al., 2013).3个模型的数学表达式如下所示:
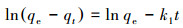
|
(1) |
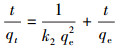
|
(2) |
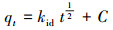
|
(3) |
式中, qt为在反应时间t时的吸附量(mg·kg-1);qe为吸附平衡时的吸附量(mg·kg-1);k1为拟一级动力学模型的速率常数(h-1);k2为拟二级动力学模型的速率常数(kg·mg-1·h-1);kid为颗粒扩散速率常数(mg·kg-1·h-1/2);C为与边界层厚度有关的常数.
3种动力学模型的拟合结果如表 2所示.通过比较它们的拟合可决系数可知, 实验数据更符合拟二级动力学模型和颗粒内扩散模型, 表明BPS在两种土壤上的吸附受化学吸附和微孔扩散共同控制.
| 表 2 BPS在两种土壤上的吸附动力学拟合参数 Table 2 Parameters of kinetic models regression of BPS in two soils |
图 2为不同反应温度下BPS在两种土壤中的吸附等温线.实验数据分别利用Langmuir(式(4))和Freundlich(式(5))方程进行拟合.
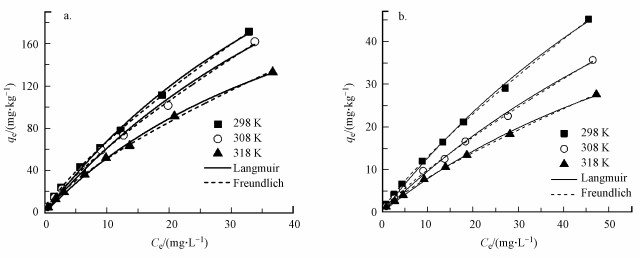 |
| 图 2 不同反应温度下BPS在黑土(a)和红壤(b)上的吸附等温线 Fig. 2 Sorption isotherms of BPS in black soil (a) and red soil (b) at different reaction temperatures |
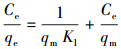
|
(4) |
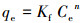
|
(5) |
式中, qe为吸附平衡时BPS在土壤中的吸附量(mg·g-1);Ce为吸附平衡时BPS在溶液中的浓度(mg·L-1);qm为BPS在土壤中的最大吸附量(mg·g-1);Kl为与吸附能有关的常数(L·mg-1).Kf为Freundlich吸附系数, 与溶质的吸附能力相关;n为Freundlich吸附指数, 反映了吸附等温线偏离线性的程度及吸附机理的不同.
结果显示, Freundlich和Langmuir方程均能较好地拟合BPS在两种土壤中的吸附等温线.由表 3可以看到, 所有的拟合可决系数R2均在0.98~1.00之间.在Langmuir方程的拟合中, 298 K反应温度下BPS在黑土和红壤上的最大吸附量qm分别为497.8和156.6 mg·kg-1, 说明有机质丰富的黑土更有利于BPS的吸附, 这和前面动力学的结果相一致.在Freundlich方程的拟合中, 298 K反应温度下BPS在黑土和红壤上吸附的Kf分别为11.1和1.97, n值分别为0.78和0.82.由于BPS在两种土壤中的n值均小于1, 吸附等温线呈非线性, 说明在吸附过程中BPS与土壤之间还存在着专性吸附作用.例如, 在土壤微孔中的扩散、与有机质之间的氢键作用和π-π作用等(Li et al., 2016).
| 表 3 BPS在两种土壤上的吸附等温线拟合参数 Table 3 Parameters for Langmuir and Freundlich models of BPS in two soils |
另外, 本研究还发现, 反应温度对BPS的吸附行为有明显的影响(图 2), 随着反应温度的逐渐升高, BPS在两种土壤上的吸附量明显减小, 这说明BPS在土壤上的吸附是一个放热的过程, 增加反应温度不利于BPS的吸附.这与BPS在石墨烯上的吸附行为一致(Li et al., 2016).
3.3 溶液pH值对BPS吸附的影响溶液pH值一方面可以引起土壤表面官能团的解离, 从而影响其表面电荷的密度;另一方面, pH也和BPS的质子化程度密切相关.因此, 本文研究了溶液pH值对BPS吸附的影响.如图 3所示, 当溶液pH值在2.0~6.0范围时, BPS在土壤中的吸附量呈缓慢下降的趋势.而当溶液pH大于6.0时, 继续增加溶液pH导致BPS的吸附容量迅速下降, 其中, 在黑土中的吸附量下降尤为明显.在pH为10.0时, BPS在黑土中的吸附量下降至12.0 mg·kg-1左右, 在红壤中的吸附量下降至8.0 mg·kg-1左右, 这与Choi和Lee(2017)的结果相一致.BPS的pKa1和pKa2分别为7.42和8.03, 明显地, 低pH条件下BPS是以中性分子的形式存在的.随着pH的持续增大, BPS逐渐解离, 主要以阴离子的形式存在, 而这时土壤表面裸露的硅羟基、羧基等基团也解离出质子.这样阴离子形式的BPS与负电荷的土壤表面形成了静电斥力, 因此不利于BPS的吸附(王黎等, 2018).另外, 中性分子形态的BPS比阴离子形态的BPS具有更高的正辛醇-水分配系数(Kow), 因此, 更容易分配于土壤有机质中, 这应该也是BPS在低pH范围具有高吸附容量的原因之一(Choi et al., 2017).
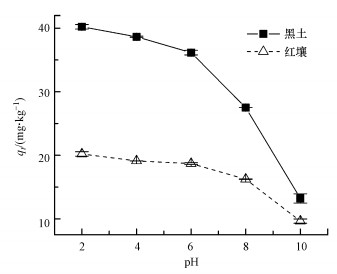 |
| 图 3 pH值对BPS在两种土壤中吸附的影响 Fig. 3 Effect of solution pH on the sorption of BPS in two soils |
污染物的解吸行为对于正确认识污染物的二次污染能力, 评价其生态风险是至关重要的.但遗憾的是迄今为止还没有关于BPS在土壤中解吸的数据.在本研究中检查了BPS在两种土壤上的解吸行为(图 4), 表 4为Freundlich方程所拟合的解吸参数.其中, 解吸系数(HI)等于1.0时, 表示没有解吸滞后的情况发生;当HI小于1.0时, 表示有解吸滞后情况发生, 并且HI越小表示解吸滞后情况越严重.由表 4中的HI可以看出, BPS在黑土中存在解吸滞后情况, 并且随着初始添加浓度的减小, 解吸滞后的程度越来越大.这可能是由于在黑土中存在着有限的高能吸附位点, 低浓度时BPS主要吸附在这些高能位点或进入土壤微孔中.随着浓度的增大, 这些高能位点逐渐被饱和, 更多的BPS与低能量位点结合或吸附于土壤表面.所以在高浓度时BPS更容易被解吸.与黑土相比, BPS在红壤中同样存在解吸滞后现象, 但滞后程度要小于黑土.这可能是由于红壤具有低的有机质含量, 因此, 只能提供非常有限的专性吸附位点的缘故(Pei et al., 2014).另外, 在红壤中解吸系数HI值与BPS初始浓度之间的相关关系也不如在黑土中明显.由于土壤中污染物的生物可利用性与其在水相中的浓度密切相关, 因此, BPS在黑土中高的滞后程度意味着其在土壤中的迁移性和生物可利用性较低.而BPS在红壤中更易解吸, 则预示着其在红壤中的迁移性和生物可利用性较高.
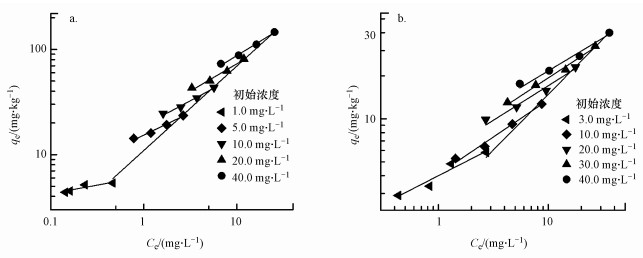 |
| 图 4 BPS在黑土(a)和红壤(b)上的解吸等温线 Fig. 4 Desorption isotherms of BPS from black soil(a) and red soil(b) |
| 表 4 BPS在两种土壤上的解吸参数 Table 4 Freundlich parameters and desorption hysteresis coefficients of BPS from two soils |
为了进一步探讨BPS的分子结构与其吸附行为之间的关系, 本研究选择了与BPS结构相似但又有所不同的BPA和DS作为研究对象, 比较了它们在土壤中吸附行为的不同.其中, BPA的两个苯环之间是丙烷基, BPS的两个苯环之间是磺酰基, 而DS与BPS的区别是没有酚羟基.由图 5可以看出, 3种化合物在黑土上的吸附容量均大于红壤, 说明土壤有机质是影响它们吸附的主要因素(郭惠莹, 2013;赵嫚, 2015).另外在黑土中, 3种化合物的吸附能力是不同的:BPA>DS>BPS.其中, BPS具有极性的磺酰基, 而BPA却拥有更加疏水的丙烷基, 这导致了BPA比BPS具有更大的Kow和更小的溶解度(表 1), 因此有利于BPA在土壤有机质中吸附.同时这也说明BPS比BPA在土壤中具有更高的迁移性, 可能会引起更高的环境健康风险.非常有趣的是DS, 它的Kow在3个化合物中最大、溶解度最小, 但它在黑土中的吸附容量却小于BPA, 这说明除了疏水性分配作用外, 化合物的分子结构基团也会影响它们的吸附行为.在黑土中, BPS和DS分子中的磺酰基明显不利于其在黑土中的吸附.
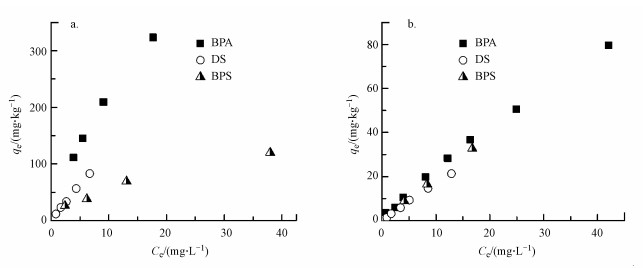 |
| 图 5 BPS, BPA和DS在黑土(a)和红壤(b)上的吸附等温线 Fig. 5 Sorption isotherms of BPS, BPA and DS on black soil (a) and red soil (b) |
在红壤中, BPA的吸附能力要略强于BPS和DS, 但3种化合物的吸附差别并不如黑土中明显.这可能是由于红壤的有机质含量特别低, 因此, 由3种污染物Kow的不同所造成的吸附差异在整个吸附中体现并不明显.另外, BPS和DS在红壤中的吸附无差别, 说明由于水分子的竞争, BPS分子上的酚羟基对整个吸附反应的贡献不大.
4 结论(Conclusions)BPS能够很快地吸附于红壤中并达到吸附平衡, 而在黑土中的吸附则包括最初的快速吸附和随后的慢速扩散过程.土壤有机质和溶液pH是控制BPS吸附的主要因素.这导致了BPS在高有机质含量黑土上的吸附量要大于红壤, 并且中性形态的BPS比阴离子形态的BPS更容易吸附于土壤中.BPS在两种土壤中均存在解吸滞后现象, 且在黑土中的滞后程度更高.与BPA相比, BPS在土壤中的迁移能力更强, 因此具有更高的环境健康风险.
Changkhamchom S, Sirivat A. 2010. Synthesis and properties of sulfonated poly (ether ketone ether sulfone) (S-PEKES) via bisphenol S:effect of sulfonation[J]. Polymer Bulletin, 65(3): 265-281. |
Choi Y J, Lee L S. 2017. Partitioning behavior of bisphenol alternatives BPS and BPAF compared to BPA[J]. Environmental Science & Technology, 51(23): 3725-3732. |
ECHA.2019.Bisphenol S Registration Data[OL].2019-10-21.https://echa.europa.eu/substanceinformation/-/substanceinfo/100.001.137
|
Gingrich J, Pu Y, Ehrhardt R, et al. 2018. Toxicokinetics of bisphenol A, bisphenol S, and bisphenol F in a pregnancy sheep model[J]. Chemosphere, 220: 185-194. |
郭惠莹.2016.双酚S在工程碳基材料和天然土壤上的吸附机理研究[D].昆明: 昆明理工大学.43 http://cdmd.cnki.com.cn/Article/CDMD-10674-1016229811.htm
|
Hu Y, Zhu Q, Yan X, et al. 2019. Occurrence, fate and risk assessment of BPA and its substituents in wastewater treatment plant:A review[J]. Environmental Research, 178: 108732. DOI:10.1016/j.envres.2019.108732 |
Huang W, Peng P A, Yu Z, et al. 2003. Effects of organic matter heterogeneity on sorption and desorption of organic contaminants by soils and sediments[J]. Applied Geochemistry, 18(7): 955-972. DOI:10.1016/S0883-2927(02)00205-6 |
Kinch C D, Ibhazehiebo K, Jeong J H, et al. 2015. Low-dose exposure to bisphenol A and replacement bisphenol S induces precocious hypothalamic neurogenesis in embryonic zebrafish[J]. Proceedings of the National Academy of Sciences of the United States of America, 112(5): 1475-1480. DOI:10.1073/pnas.1417731112 |
Li L Y, Xu D H, Pei Z G. 2016. Kinetics and thermodynamics studies for bisphenol S adsorption on reduced graphene oxide[J]. RSC Advances, 6(65): 60145-60151. DOI:10.1039/C6RA10607B |
李晓蒙, 张立实, 隋海霞, 等. 2018. 双酚S和双酚F的危害识别[J]. 卫生研究, 47(6): 1018-1021. |
刘文敏, 张晓娜, 魏朋浩, 等. 2018. 双酚S长期暴露对雌性斑马鱼视觉系统的影响[J]. 中国海洋大学学报(自然科学版), 48(11): 71-78. |
Liu Y, Chen M, Yongmei H. 2013. Study on the adsorption of Cu(Ⅱ) by EDTA functionalized Fe3O4 magnetic nano-particles[J]. Chemical Engineering Journal, 218: 46-54. DOI:10.1016/j.cej.2012.12.027 |
罗世鹏, 吴泽颖, 商贵芹, 等. 2014. 超高效液相色谱-串联质谱法测定食品包装材料中双酚S含量[J]. 食品安全质量检测学报, 5(11): 3576-3579. |
Pal S, Sarkar K, Nath P P, et al. 2017. Bisphenol S impairs blood functions and induces cardiovascular risks in rats[J]. Toxicology Reports, 4: 560-565. DOI:10.1016/j.toxrep.2017.10.006 |
Pei Z G, Shan X Q, Liu T, et al. 2006. Sorption of p-nitrophenol on two Chinese soils as affected by copper[J]. Environmental Toxicology and Chemistry, 25(10): 2584-2592. DOI:10.1897/05-505R.1 |
Pei Z G, Yang S, Li L Y, et al. 2014. Effects of copper and aluminum on the adsorption of sulfathiazole and tylosin on peat and soil[J]. Environmental Pollution, 184: 579-585. DOI:10.1016/j.envpol.2013.09.038 |
Pignatello J J, Xing B. 1996. Mechanisms of slow sorption of organic chemical to natural particles[J]. Environmental Science & Technology, 30(1): 1-11. |
Qiu W, Zhao Y, Yang M, et al. 2016. Actions of bisphenol A and bisphenol S on the reproductive neuroendocrine system during early development in Zebrafish[J]. Endocrinology, 157: 636-647. DOI:10.1210/en.2015-1785 |
Rosenmai A K, Dybdahl M, Pedersen M, et al. 2014. Are structural analogues to bisphenol a safe alternatives?[J]. Toxicological Sciences, 139(1): 35-47. DOI:10.1093/toxsci/kfu030 |
沈杰, 刘建超, 陆光华, 等. 2018. 双酚S和双酚F在水环境中的分布、毒理效应及其生态风险研究进展[J]. 生态毒理学报, 13(5): 37-48. |
Shi Y, Sun Y, Gao B, et al. 2019. Importance of organic matter to the retention and transport of bisphenol A and bisphenol S in saturated soils[J]. Water, Air & Soil Pollution, 230(2): 43. |
Speidel J T, Xu M, Abdel-Rahman S Z. 2018. Bisphenol A (BPA) and bisphenol S (BPS) alter the promoter activity of the ABCB1 gene encoding P-glycoprotein in the human placenta in a haplotype-dependent manner[J]. Toxicology and Applied Pharmacology, 359: 47-54. DOI:10.1016/j.taap.2018.09.022 |
王黎, 刘娟, 沈晓芳, 等.2018.柚子皮生物质活性炭去除水体中双酚A和双酚S[C].《环境工程》2018年全国学术年会.北京: 4
|
Wu L H, Zhang X M, Wang F, et al. 2018. Occurrence of bisphenol S in the environment and implications for human exposure:A short review[J]. Science of the Total Environment, 615: 87-98. DOI:10.1016/j.scitotenv.2017.09.194 |
袁琳嫣. 2017. 食品接触包装材料中双酚S的研究进展[J]. 上海包装, (4): 58-60. |
Zhang S, Yang X, Liu L, et al. 2019. Bisphenol S adsorption behavior on ferralsol and biochar modified soil with dissolved organic matter[J]. International Journal of Environmental Research and Public Health, 16(5): 764. DOI:10.3390/ijerph16050764 |
赵嫚.2015.多种土壤对双酚A的吸附行为及吸附预测模型的构建[D].武汉: 华中农业大学.58 http://cdmd.cnki.com.cn/Article/CDMD-10504-1015380721.htm
|
 2020, Vol. 40
2020, Vol. 40