2. 东华理工大学核资源与环境国家重点实验室, 南昌 330013;
3. 山东建筑大学市政与环境工程学院, 济南 250101
2. State Key Laboratory Breeding Base of Nuclear Resources and Environment, East China University of Technology, Nanchang 330013;
3. School of Municipal and Environmental Engineering, Shandong Jianzhu University, Jinan 250101
抗生素在人类生产和生活中被广泛应用于人类和动物疾病的治疗, 并添加到动物饲料或投放到养殖环境中以提高其生长速率和饲养效率(Pei et al., 2014).仅在我国, 2013年抗生素的使用量即高达16.2万吨(张国栋等, 2018).由于抗生素不能被动物完全吸收, 因此, 约有40%以上以母体或其代谢产物形式通过排泄物而排出(Kemper, 2008), 并通过动物粪肥的施用进入环境.此外, 由于抗生素对传统污染物处理方法体现出的高抗性, 使其还可通过污水灌溉和污泥处置等多种途径进入环境(Miao et al., 2004; Zorita et al., 2009; Berkner et al., 2014; Yang et al., 2016).目前, 抗生素已经在全球范围内的地表水、土壤及地下水等多种环境基质中频繁检出(Tong et al., 2014;Ma et al., 2015;孙秋根等, 2018).大量研究表明, 抗生素及其环境残留物可对陆生和水生微生物造成诸多不利影响, 比如, 其能够抑制细菌菌落的增长并增加抗生素抗性基因的形成(Miguel et al., 2013; Amy, 2014; Rodriguez-Mozaz et al., 2015).可见环境一旦被抗生素污染, 将给地球上各类生命体健康带来巨大威胁.因此, 系统研究抗生素在环境中的迁移及归趋对环境污染防治至关重要, 尤其是地下水系统, 因为地下水不仅是人类重要的水源, 还通常是环境中污染物的最终归宿地(童蕾等, 2016).
之前的研究表明, 抗生素在多孔介质中的迁移行为受到抗生素类型、水化学组成、介质性质、共存物质、饱和度及水动力条件等诸多因素的影响, 其迁移规律因上述因素的变化而有所不同(Park et al., 2016; Dong et al., 2016; Sun et al., 2018; Sun et al., 2019).抗生素按其结构一般可分为九大类, 从属于每大类的抗生素具有一定的相似理化性质, 但同时也存在着差异(祁彦洁等, 2014).目前在模拟多孔介质中变因素条件下抗生素的迁移研究中, 多集中于某一大类中不同种抗生素或某两种及以上各自属于不同大类抗生素的对照研究(Chen et al., 2011; Chen et al., 2013; Dong et al., 2016), 这可能不足以充分对比反映出影响因素对各大类抗生素的影响是更趋于相似还是无明显相关.例如, 据作者所知, 关于Ca2+对LEV在多孔介质中迁移的影响目前还未有研究, 无法得知其行为与CIP是否相似(Chen et al., 2013).因此, 在对比影响因素对各大类抗生素的迁移影响时, 有必要在每大类抗生素中选择两种及以上进行系统的对比研究.
石英砂作为一类典型多孔介质广泛存在于自然界中且组分单一, 常被用来研究污染物在多孔介质中的迁移和滞留行为.因此, 本研究选取石英砂作为多孔介质, 以环境中普遍检出的典型SAs和FQs, 即磺胺二甲氧嘧啶(Sulfadimethoxine, SDM)、磺胺醋酰(Sulfacetamide, SCA)、左氧氟沙星(Levofloxacin, LEV)和环丙沙星(Ciprofloxacin, CIP)为研究对象(Thiele-Bruhn, 2003; Batt et al., 2006; Hu et al., 2010; López-Serna et al., 2013; Tong et al., 2014; Doorslaer et al., 2014; Postigo et al., 2015), 通过室内砂柱迁移实验, 重点探讨pH值、离子强度和类型及介质粒径对抗生素迁移的影响, 具体研究内容如下:①pH值对SAs和FQs在饱和石英砂多孔介质中迁移的影响;②NaCl及CaCl2对SAs和FQs在饱和石英砂多孔介质中迁移的影响;③介质粒径对SAs和FQs在饱和石英砂多孔介质中迁移的影响.旨在系统对比研究SAs和FQs在多孔介质中的迁移特征和影响因素, 为了解土壤及地下水系统中不同类型抗生素的分配与迁移提供科学依据.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 抗生素本实验使用的SDM(CAS 1037-50-9, >98%;pKa1/pKa2:3.40/5.80)和SCA(CAS 144-80-9, >98%;pKa1/pKa2:1.90/5.90)均购自阿拉丁生物化学技术有限公司(中国), LEV(CAS 177325-13-2, >98.5%;pKa1/pKa2:6.02/8.15)和CIP(CAS 86393-32, >99%;pKa1/pKa2:6.05/8.37)均购自美伦生物科技公司(中国).制备抗生素溶液, 4 ℃避光贮存备用.
将盛有0.5 mg·L-1 SDM、SCA、LEV和CIP溶液的无色烧杯置于无光照控制的实验室中, 分别在12、24、48、72和96 h时取样分析抗生素的浓度.结果表明, 4种抗生素在整个实验过程几乎没有质量损失.因此, 4种抗生素在本实验研究条件下稳定性较好, 光降解和生物降解可以忽略不计.
2.1.2 多孔介质材料实验所用的多孔介质材料石英砂购自美国尤尼明公司(Unimin-LeSueur, MN, USA).分别筛选出粗(Coarse, 0.70~0.85 mm)、中(Media, 0.35~0.45 mm)、细(Fine, 0.11~0.15 mm)3种不同粒径的石英砂, 依次使用自来水、10%硝酸(体积比)和去离子水清洗, 用以去除金属氧化物及其他杂质, 最后将清洗好的石英砂在40 ℃条件下烘干备用(Tian et al., 2010; Dong et al., 2016).
2.2 实验方法 2.2.1 背景溶液和工作溶液制备为研究溶液pH值、NaCl离子强度、CaCl2离子强度和介质粒径对4种抗生素在饱和石英砂多孔介质中迁移的影响, 在开展实验工作前需要根据实验要求制备相应的背景溶液和工作溶液(表 1).在设置溶液pH值对迁移影响的实验中, 考虑到通常地下水pH值大多在弱酸性到微碱性范围内(张玉玺等, 2011;沈志红, 2011), 因此, 本实验设置pH在5.6~9.5之间.分别配制低、中、高3组pH值(5.6、7.0和9.5), 且离子强度均为1.50 mmol·L-1 NaCl的分别含有4种抗生素的工作溶液和不含抗生素的背景溶液.在NaCl离子强度对迁移影响实验中, 分别配制离子强度为0、1.50、100 mmol·L-1 NaCl, 且pH值均为7.0的分别含有4种抗生素的工作溶液和不含抗生素的背景溶液.在CaCl2离子强度对迁移影响实验中, 分别配制离子强度为0、1.50、50 mmol·L-1 CaCl2, pH值均为7.0的分别含有4种抗生素的工作溶液和不含抗生素的背景溶液.在介质粒径对迁移影响实验中, 配制离子强度为1.50 mmol·L-1 NaCl, pH值均为7.0的分别含有4种抗生素的工作溶液和不含抗生素的背景溶液.所有溶液以去离子水配置, 使用0.1 mol·L-1 HCl和2.5 mol·L-1 NaOH调节溶液pH值.由于调节pH值所加入的HCl和NaOH溶液量极少, 离子强度和溶液体积变化可忽略不计.
| 表 1 迁移实验条件汇总 Table 1 Summary of experimental condition for packed column experiments |
实验中饱和石英砂柱的制备:将石英砂作为饱和多孔介质采用湿法填装于丙烯酸柱内(内径2.5 cm, 长度16.8 cm), 柱两端均封有30 μm不锈钢滤网, 用于支撑柱内多孔介质并同时起到均匀分布水流的作用(Tian et al., 2010; Chen et al., 2011).所有石英砂柱填装的孔隙度为0.36~0.38.使用蠕动泵控制水流为恒定流速, 流速为1.0 mL·min-1(达西流速=2.94 m·d-1).在每次实验开始前, 先用去离子水冲洗石英砂柱约10个孔隙体积(Pore Volumes, PVs)以更好地去除石英砂介质中的杂质, 然后用背景溶液冲洗石英砂柱约10 PVs用以平衡孔隙间离子强度和pH值(Dong et al., 2016).实验开始, 将初始浓度为500 μg·L-1的抗生素工作溶液持续注入柱中130 min(> 4 PVs), 随后用背景溶液持续冲洗柱4 PVs.出水样品使用部分收集器采集用以分析抗生素浓度.所有柱实验设置两组平行样.
2.3 分析方法 2.3.1 介质的表征和分析采用扫描电镜-能量色散X射线(SEM-EDX, 日本电子株式会社JSM-6400)、BET比表面积测定仪(德国麦克默瑞提ASAP 2020 PLUS HD88)、元素分析仪(意大利NC科技ECS 4024 CHNSO)、ZetaPlus电位仪(英国马尔文Nano ZSE)对石英砂进行表面形态及性质分析.
2.3.2 抗生素的分析本实验中抗生素浓度分析使用Agilent 1200高效液相色谱(High performance liquid chromatography, HPLC), 配备的色谱柱为C18色谱柱(150 mm×4.6 mm, Thermofisher, Hypersil GOLD), 检测器为二极管阵列检测器(Diode array detector, DAD).SAs的HPLC检测条件:流动相为0.1%(V:V)甲酸和乙腈(80:20, V:V), 进样流速为1 mL·min-1, 柱温箱温度为30 ℃, SDM和SCA检测波长分别为267 nm和255 nm. FQs的HPLC检测条件:流动相为0.025 mol·L-1磷酸二氢钠(使用磷酸调节pH至2.5~3.0)和乙腈(80:20, V:V), 进样流速为1 mL·min-1, 柱温箱温度为30 ℃, LEV和CIP检测波长分别为294 nm和276 nm.
3 结果与讨论(Results and discussion) 3.1 介质性质分析SEM图像(图 1)结果显示, 石英砂颗粒在放大91倍条件下展现出较圆滑的边缘及较光滑的表面, 当放大倍数扩大至3700倍时, 颗粒表面仍显示较为平整, 无明显凹凸及孔洞.不同粒径(0.11~0.15、0.35~0.45、0.70~0.85 mm)石英砂颗粒的比表面积分别为0.058、0.046、0.032 m2·g-1.EDX分析结果(图 2)显示, 石英砂表面仅有氧元素和硅元素被检出(其中碳元素和铂元素为测试方法中添加元素).总有机碳含量分析表明石英砂中未有有机碳检出.
 |
| 图 1 不同放大倍数下石英砂颗粒的SEM图像 (a.91倍, b.3700倍) Fig. 1 SEM image of the quartz sand under different magnification |
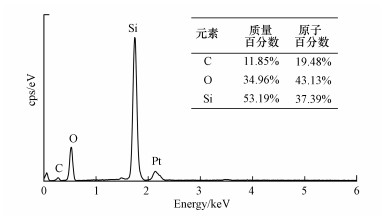 |
| 图 2 石英砂样品的EDX分析结果 Fig. 2 EDX analyses results from the quartz sand |
图 3a、3b为溶液pH对SCA和SDM在饱和石英砂多孔介质中迁移影响的穿透曲线.如图所示, 两种磺胺类抗生素在3种不同pH值条件下迁移能力均很高, 且均展现出相似的典型穿透行为, 即初始穿透时间略提前于1 PV, 然后出水浓度/初始浓度(C/C0, 归一化浓度)快速升至平台期, 峰值在1附近, 注入背景溶液后C/C0迅速降至基线.并且, 如放大图所示(图a1、a2、b1、b2), 溶液pH的变化对SCA及SDM的上升及下降过程中的速度同样影响很小.表 1显示流出液SCA和SDM出水回收率均>98%, 说明在该实验条件下几乎所有的SDM和SCA在该实验条件下均穿出饱和石英砂柱, 溶液pH值对SDM和SCA在饱和石英砂柱中的迁移几乎没有影响.Chen等(2011)和Dong等(2016)也得出类似结论, 不同溶液pH值条件下SAs在饱和石英砂柱中几乎完全穿透, 且SAs在饱和石英砂柱中的迁移与pH值不相关.
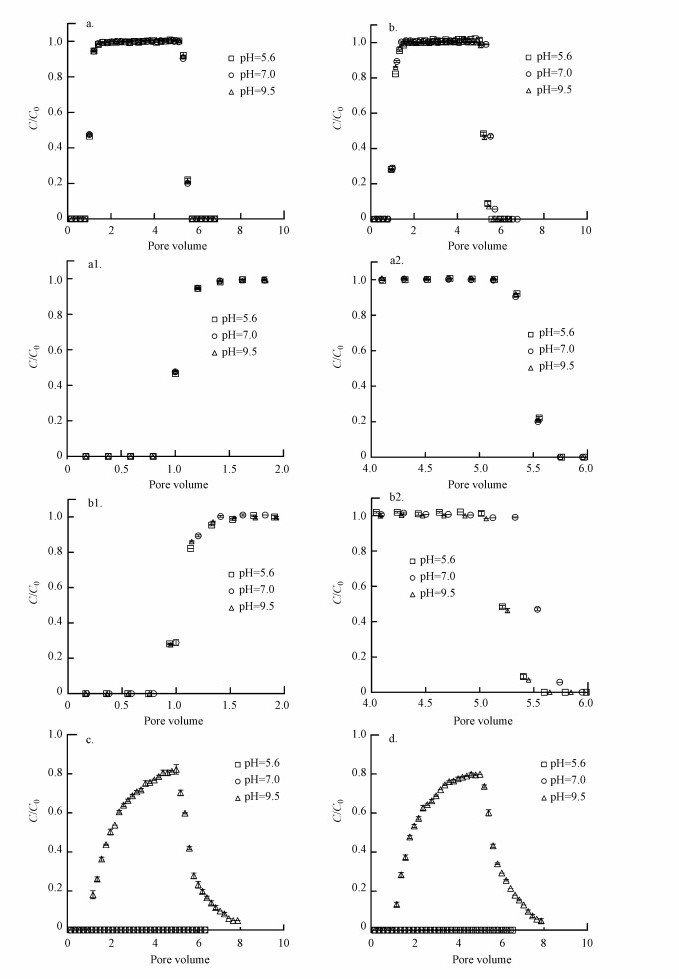 |
| 图 3 溶液pH对SCA(a)、SDM(b)、LEV(c)和CIP(d)在饱和石英砂多孔介质中迁移的影响及SCA(a1, a2)和SDM(b1, b2)穿透曲线上升及下降部分放大图 Fig. 3 Effect of pH on the transport of SCA (a), SDM (b), LEV (c) and CIP (d) in saturated quartz sand porous media and detailed ascending and descending part of breakthrough curves of SCA(a1, a2) and SDM(b1, b2) |
pH值对抗生素迁移的影响与pKa值和等电点相关, 其中, 等电点可通过pKa值粗略计算得出, 计算方法为1/2(pKa1+ pKa2)(Qiang et al., 2004; Kurwadkar et al., 2011).已知SDM和SCA的pKa1/pKa2分别为1.8/5.9和3.4/5.8, 因此, 得出SDM和SCA的等电点约为3.9和4.6(Park et al., 2016).在等电点以下, SAs在水溶液中以阳离子形态和中性/两性形态占主导, 反之, 则是阴离子形态和中性形态占主导, 并且随pH升高阴离子形态占比逐渐增加.因此如图 4所示, 在本实验溶液各pH条件下(5.6、7.0、9.5), SDM和SCA主要以阴离子形态和中性/两性形态存在, 易与表面同为带负电荷的石英砂颗粒(石英砂的零点电荷点在pH~2.9)之间产生静电排斥作用, 从而抑制其吸附(Dong et al., 2016; Park et al., 2016).
 |
| 图 4 溶液pH对SAs和FQs在多孔介质中迁移影响机制 Fig. 4 Effect of pH on the transport of SAs in saturated quartz sand porous media |
图 3c、3d分别为不同溶液pH对LEV和CIP在饱和石英砂多孔介质中迁移影响的穿透曲线.与SAs相比, 同样条件下FQs在石英砂柱中的迁移能力较差.两种FQs的穿透仅发生于pH=9.5条件下, 而在pH=5.6和7.0条件下流出液中没有FQs被检出, 这表明溶液pH值是FQs在饱和石英砂多孔介质中迁移的一个重要控制因素.在pH=9.5条件下, LEV和CIP的穿透曲线形状非常相似, 均具有明显不对称性, 初始穿透时间在~1 PV, 然后C/C0缓慢上升, 在~5.2 PVs升至最大值, 随后开始缓慢下降, 并且在解吸阶段均具有明显拖尾.LEV和CIP的穿透曲线高度和回收率明显低于SAs, 二者的C/C0最大值均在0.8附近, 最大流出液回收率分别为72.1%和75.2%(表 1).
LEV和CIP具有非常相似的pKa1/pKa2(分别为6.02/8.15和6.05/8.37), 计算得知二者的等电点分别约为7.1和7.2(Qiang et al., 2004; Kurwadkar et al., 2011).同时结合图 5判断得出在实验溶液pH=5.6和7.0条件下LEV和CIP主要以阴离子形态和中性/两性形态存在, 易与表面带负电荷的石英砂颗粒之间产生静电吸引作用, 从而促进其吸附.然而在溶液pH=9.5条件下, 由于绝大部分LEV和CIP均为带负电形态, 因此, 在一定程度上抑制了FQs在石英砂颗粒上的沉积(图 4)(Chen et al., 2011; Dong et al., 2016).FQs的穿透曲线展现出的明显拖尾效应, 反映了FQs在石英砂表面的可逆吸附.此外, 先前研究表明, LEV和CIP在相同溶液pH条件下具有相似比例的阴离子数(图 5), 这将导致二者与石英砂颗粒表面产生相似的静电引力(Sandra et al., 2010; Qin et al., 2014).因此, LEV和CIP在相同溶液pH条件下展现出极为相似的穿透行为和出水回收率.溶液pH值对SAs和FQs在饱和多孔介质中不同的影响表明抗生素的随pH值变化而形态发生改变的特性是控制其迁移行为的重要因素之一.
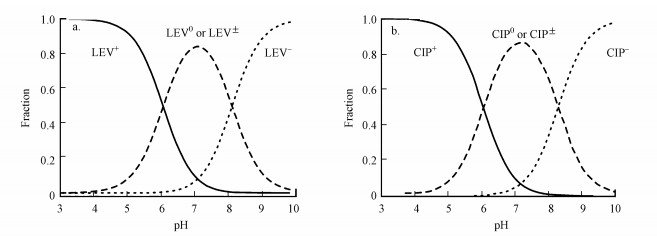 |
| 图 5 pH 3~10范围内LEV(a)和CIP(b)的形态变化 (Qin et al., 2014; Tan et al., 2015) Fig. 5 pH-dependent speciation of LEV(a) and CIP(b) |
图 6a、6b分别为不同NaCl离子强度对SCA和SDM在饱和石英砂多孔介质中迁移的影响.如图所示, 两种SAs在溶液离子强度由0 mmol·L-1增至100 mmol·L-1时始终保持高迁移能力, 均展现出相似的典型穿透行为.表 1显示NaCl组中SDM和SCA流出液回收率均≥98.5%, 说明几乎所有的SDM和SCA在该实验条件下均穿出饱和石英砂柱, 同时表明NaCl离子强度对SDM和SCA在饱和石英砂柱中的迁移几乎没有影响.
 |
| 图 6 NaCl对饱和石英砂多孔介质中SCA(a)、SDM(b)、LEV(c)和CIP(d)迁移的影响 Fig. 6 Effect of NaCl on the transport of SCA (a), SDM (b), LEV (c) and CIP (d) in saturated quartz sand porous media |
NaCl离子强度由0 mmol·L-1增至100 mmol·L-1时, 石英砂介质的Zeta电位由-34.0 mV升至-17.7 mV.然而介质Zeta电位的升高并没有在一定程度上减弱SAs的迁移, 表明在-17.7 mV条件下SAs在多孔介质中受到的静电斥力已足以使SAs不沉积.因此, 在本实验Zeta电位变化范围内SAs与石英砂颗粒之间的静电相互作用的变化(离子交换或库仑力)可以不被考虑, 同时表明NaCl溶液中不存在来自阳离子或阴离子的竞争作用(Chen et al., 2011).此外, Chen等(2011)也发现, 在pH=5.6和9.5条件下, 溶液离子强度的变化对石英砂柱中SMZ迁移的影响也很小, 同时两种pH条件下不同离子强度的SMZ的4条穿透曲线也极其相似.Gao和Pedersen(2005)在批吸附实验中同样发现, 在上述这些pH范围内离子强度对磺胺类抗生素在粘土颗粒上的吸附几乎没有影响.
图 6c、6d分别为不同离子强度NaCl对LEV和CIP在饱和石英砂多孔介质中迁移的穿透曲线.如图所示, 与SAs相反的是, 同样条件下FQs表现出极弱的迁移能力.与SAs相似的是, 溶液离子强度增加66.7倍对FQs迁移没有显著的影响, 流出液中始终未有LEV和CIP检出(表 1).同样地, Chen等(2011)研究发现, 在CIP迁移能力较高的溶液pH=9.5条件下, 离子强度的变化也几乎不影响CIP的迁移;在CIP迁移能力极弱的溶液pH=5.6条件下, 离子强度对CIP的影响也非常有限, 整个实验过程出水中无CIP检出;并且在高离子强度下, 柱剖面显示仅有5%的CIP从第一个1 cm层移至第二个1 cm层.
3.4 CaCl2对迁移的影响图 7a、7b分别为不同CaCl2离子强度对SCA和SDM在饱和石英砂多孔介质中迁移的穿透曲线.如图所示, 与NaCl组相似, 两种SAs在CaCl2溶液离子强度由0 mmol·L-1增至100 mmol·L-1时始终保持高迁移能力, 且均展现出相似的典型穿透行为.表 1显示CaCl2离子强度组中流出液中SDM和SCA回收率均≥98.7%, 说明几乎所有SDM和SCA在该实验条件下均穿出饱和石英砂柱, 同时表明CaCl2离子强度对SDM和SCA在饱和石英砂柱中的迁移几乎没有影响.
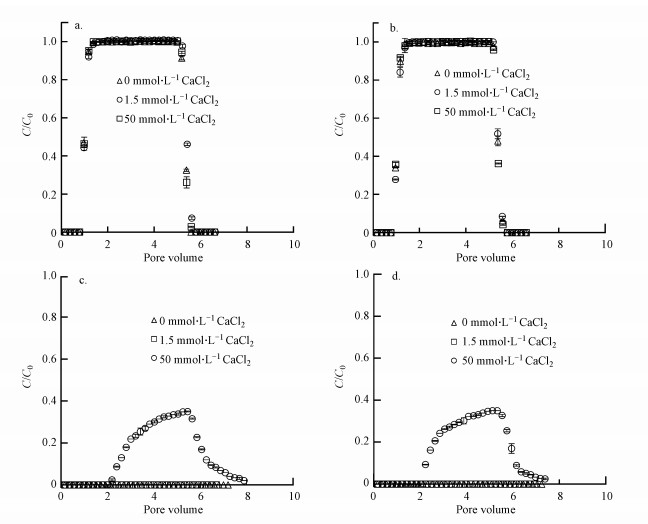 |
| 图 7 CaCl2对饱和石英砂多孔介质中SCA(a)、SDM(b)、LEV(c)和CIP(d)迁移的影响 Fig. 7 Effect of CaCl2 on the transport of SCA (a), SDM (b), LEV (c) and CIP (d) in saturated quartz sand porous media |
CaCl2离子强度由0 mmol·L-1增至50 mmol·L-1时, 石英砂介质Zeta电位由-34.0 mV升至-7.46 mV.然而, 介质Zeta电位的明显升高没有对SAs的迁移产生负影响, 这与NaCl组的结论相似, 进一步证实SAs能够在绝对值较小的负Zeta电位条件下获得保持高迁移能力的静电斥力, 因此, 与石英砂颗粒之间的静电相互作用(离子交换或库仑力)可以不被考虑, 同样CaCl2溶液中不存在来自阳离子或阴离子的竞争作用.
图 7c、7d分别为CaCl2对LEV和CIP在饱和石英砂多孔介质中迁移的穿透曲线.与SAs相比, 同样条件下FQs在柱中的迁移能力仍较差.值得注意的是, CaCl2离子强度对FQs迁移存在显著影响.当溶液中未添离子强度时, LEV和CIP均未穿透;当添加离子强度为1.50 mmol·L-1时, 出水中仍未有LEV或CIP检出, 穿透率为0(表 1);然而当离子强度升至50.0 mmol·L-1时, LEV和CIP发生显著穿透, 并且其穿透曲线具有明显不对称性:LEV和CIP的初始穿透较SAs延迟, 均在~2 PV时开始穿出, 然后C/C0缓慢上升并均在~5.8 PV升至峰值(C/C0最大值约为0.4), 随后开始缓慢下降并存在明显拖尾显现.表 1显示离子强度增至50.0 mmol·L-1时, LEV和CIP流出液回收率分别增至25.4%和25.3%.综上表明, 随CaCl2离子强度升高FQs在饱和石英砂介质中的迁移显著升高.
在溶液中FQs的官能团携带的电荷非常重要, 因为这会影响其在Ca2+存在条件下与石英砂介质间的相互作用(Chen et al., 2013), 因此, 了解LEV和CIP的官能团在溶液中的存在形态十分重要.Chen等(2013)研究表明, CIP在溶液pH=5.6的条件下, 100%的哌嗪基以NH2+形式存在和20%的羧基以COO-形式存在.本实验溶液pH值为7.0, CIP的哌嗪基将部分以NH形式存在, 部分以NH2+形式存, 而羧基则因pH值高于5.6而有多于20%的COO-存在.由于LEV和CIP的解离常数非常相似, 因此, 同样条件下羧基存在状态也与CIP相似.所以当FQs与Ca2+共存时, Ca2+可通过LEV或CIP带负电的羧基与其络合(Chen et al., 2013).由于本实验中添加的Ca2+浓度远远大于FQs浓度, 因此仅考虑1:1 Ca-FQs形态, 即当溶液中Ca2+与CIP/LEV相遇后, 将形成Ca-CIP+/Ca-LEV+.这时溶液中将同时存在大量游离的Ca2+及Ca-CIP+/Ca-LEV+.如图 8所示, 当无Ca2+加入时, 石英砂表面活性位点能够满足注入LEV/CIP的占据;当溶液中加入较少量Ca2+时, 位点数仍能够满足迁移溶质的占据;而当溶液中Ca2+达到较高浓度时, 大量Ca2+在迁移过程中能够与Ca-CIP+/Ca-LEV+在石英砂表面活性位点形成吸附竞争, 即Ca2+占据了部分吸附位点导致CIP/LEV的吸附减少, 从而促进其迁移(Chen et al., 2013).尽管溶液中较高浓度的Ca2+与LEV/CIP共存能够有效提高二者在饱和石英砂介质中的迁移能力, 但相比SAs的穿透曲线, LEV/CIP的穿透却存在一定的延迟(图 6、图 7).这可能是由于Ca-CIP+/Ca-LEV+在石英砂表面能够有效吸附, 并且只有当注入的Ca2+达到足够大的数量时才能够与Ca-CIP+/Ca-LEV+在石英砂表面活性位点形成有效竞争.FQs在低CaCl2离子强度(1.50 mmol·L-1)条件下穿透率为0(表 1)这一现象可进一步支持上述观点.
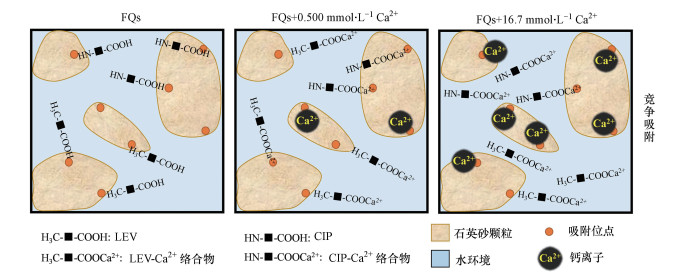 |
| 图 8 CaCl2对FQs在石英砂多孔介质中迁移的影响机制 Fig. 8 Effect of CaCl2 on the transport of FQs in saturated quartz sand porous media |
图 9a、9b显示了不同介质粒径对SCA和SDM在饱和石英砂多孔介质中迁移的影响.如图所示, 在溶液pH=7.0条件下, SCA和SDM在3种不同介质粒径的饱和石英砂柱中均保持很高的迁移能力, 且均展现出相似的典型穿透行为, 表 1显示粒径组中SCA和SDM出水回收率均>97%.然而, SCA和SDM在细砂(SCA:97.7%, SDM:98.7%)填充的柱中迁移能力略微低于中砂(SCA:98.5%, SDM:99.6%)和粗砂(SCA:98.9%, SDM:100.2%), 表明石英砂粒径对SAs在饱和石英砂柱中的迁移存在微弱的影响, 这与Dong等(2016)的研究结果一致.这可能是由于细砂(0.058 m2·g-1)具有比中砂(0.046 m2·g-1)和粗砂(0.032 m2·g-1)更大的比表面积, 这为其中迁移的抗生素提供了更多的接触面积, 从而将作用于SAs滞留的那部分微弱的吸附位点数量在一定程度上增加.
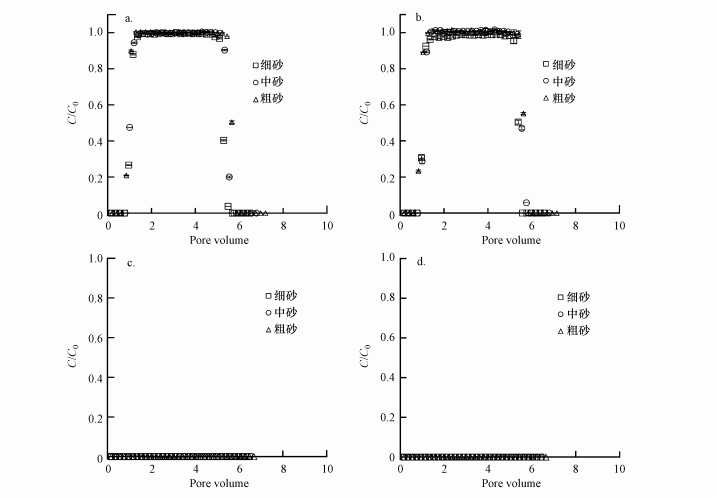 |
| 图 9 粒径对饱和石英砂多孔介质中SCA(a)、SDM(b)、LEV(c)和CIP(d)迁移的影响 Fig. 9 Effect of grain size on the transport of SCA(a), SDM(b), LEV(c) and CIP(d) in saturated quartz sand porous media |
图 9c、9d显示了不同介质粒径对LEV和CIP在饱和石英砂多孔介质中迁移的影响.如图所示, 与SAs相比, 同样条件下FQs在柱中仍表现出极弱的迁移能力, 出水中无LEV和CIP检出, 穿透率为0(表 1).即使粗砂具有更少的接触面积和吸附位点, FQs在实验条件下(pH=7.0, NaCl离子强度1.5 mmol·L-1)仍无法穿透, 表明FQs在石英砂上的吸附能力极强.因此, 在自然界常见地下水环境pH条件下, 介质粒径的改变很难显著影响FQs的迁移情况.
4 结论(Conclusions)1) 以SDM和SCA代表的SAs在饱和石英砂多孔介质中的迁移能力强, 流出液中二者回收率均>97%, 且溶液pH、离子强度(NaCl和CaCl2)和介质粒径变化对SDM和SCA迁移的影响不大.这是因为在多数地下水pH条件下, 低解离常数使得磺胺多以带负电形态出现, 因静电斥力作用导致磺胺在石英砂介质中迁移能力强.
2) 相同条件下, FQs多呈阳离子形态及两性形态, 与石英砂介质间的静电引力导致LEV和CIP迁移能力相对较弱, 且其移动性随pH升高而增大.当溶液pH由5.6升至9.5, 流出液中LEV和CIP回收率显著增加, 由0分别增加至72.1%和75.2%.
3) NaCl浓度对LEV和CIP在石英砂介质中的迁移能力几乎无影响;而CaCl2浓度对LEV和CIP迁移影响较大, CaCl2浓度由1.5 mmol·L-1增至50 mmol·L-1时, LEV和CIP的迁移能力均明显增加, 二者迁移率由0分别增加至25.4%和25.3%, 其原因可能是Ca2+的竞争吸附作用.
Amy P. 2014. Balancing water sustainability and public health goals in the face of growing concerns about antibiotic resistance[J]. Environmental Science & Technology, 48(1): 5-14. |
Batt A L, Snow D D, Aga D S. 2006. Occurrence of sulfonamide antimicrobials in private water wells in Washington County, Idaho, USA[J]. Chemosphere, 64(11): 1963-71. |
Berkner S, Konradi S, Schonfeld J. 2014. Antibiotic resistance and the environment-there and back again:Science & society series on science and drugs[J]. EMBO Reports, 15(7): 740-744. |
Chen H, Gao B, Li H, et al. 2011. Effects of pH and ionic strength on sulfamethoxazole and ciprofloxacin transport in saturated porous media[J]. Journal of Contaminant Hydrology, 126(1/2): 29-36. |
Chen H, Ma L Q, Gao B, et al. 2013. Influence of Cu and Ca cations on ciprofloxacin transport in saturated porous media[J]. Journal of Hazardous Materials, 262(22): 805-811. |
Dong S, Gao B, Sun Y, et al. 2016. Transport of sulfacetamide and levofloxacin in granular porous media under various conditions:Experimental observations and model simulations[J]. Science of the Total Environment, 573: 1630-1637. DOI:10.1016/j.scitotenv.2016.09.164 |
Doorslaer X V, Dewulf J, Langenhove H V, et al. 2014. Fluoroquinolone antibiotics:An emerging class of environmental micropollutants[J]. Science of the Total Environment, 500-501(1/3): 250-69. |
Gao J, Pedersen J A. 2005. Adsorption of sulfonamide antimicrobial agents to clay minerals[J]. Environmental Science & Technology, 39(24): 9509-9516. |
Hu X, Zhou Q, Luo Y. 2010. Occurrence and source analysis of typical veterinary antibiotics in manure, soil, vegetables and groundwater from organic vegetable bases, northern China[J]. Environmental Pollution, 158(9): 2992-2998. |
Kemper N. 2008. Veterinary antibiotics in the aquatic and terrestrial environment[J]. Ecological Indicators, 8(1): 1-13. DOI:10.1016/j.ecolind.2007.06.002 |
Kurwadkar S T, Adams C D, Meyer M T, et al. 2011. Comparative mobility of sulfonamides and bromide tracer in three soils[J]. Journal of Environmental Management, 92(7): 1874-1881. |
López-Serna R, Jurado A, Vázquez-Suñé E, et al. 2013. Occurrence of 95 pharmaceuticals and transformation products in urban groundwaters underlying the metropolis of Barcelona, Spain[J]. Environmental Pollution, 174: 305-315. |
Ma Y, Li M, Wu M, et al. 2015. Occurrences and regional distributions of 20 antibiotics in water bodies during groundwater recharge[J]. Science of the Total Environment, 518/519: 498-506. DOI:10.1016/j.scitotenv.2015.02.100 |
Miao X S, Bishay F, Chen M, et al. 2004. Occurrence of antimicrobials in the final effluents of wastewater treatment plants in Canada[J]. Environmental Science & Technology, 38(13): 3533-3541. |
Miguel G P, Soledad G, Ismael R P, et al. 2013. Toxicity of five antibiotics and their mixtures towards photosynthetic aquatic organisms:implications for environmental risk assessment[J]. Water Research, 47(6): 2050-2064. |
Park J Y, Huwe B. 2016. Effect of pH and soil structure on transport of sulfonamide antibiotics in agricultural soils[J]. Environmental Pollution, 213: 561-570. |
Pei Z, Yang S, Li L, et al. 2014. Effects of copper and aluminum on the adsorption of sulfathiazole and tylosin on peat and soil[J]. Environmental Pollution, 184: 579-585. |
Postigo C, García-Galán M J, KöCK-Schulmeyer M, et al.2015.Occurrence of Polar Organic Pollutants in Groundwater Bodies of Catalonia//Munné A, Ginebreda A, Prat N.Experiences from Ground, Coastal and Transitional Water Quality Monitoring[M].Springer: 63-89
|
祁彦洁, 刘菲. 2014. 地下水中农抗生素污染检测分析研究进展[J]. 岩矿测试, 33(1): 1-11. DOI:10.3969/j.issn.0254-5357.2014.01.002 |
Qiang Z M, Craig A. 2004. Potentiometric determination of acid dissociation constants (pKa) for human and veterinary antibiotics[J]. Water Research, 38(12): 2874-90. |
Qin X, Liu F, Wang G, et al. 2014. Adsorption of levofloxacin onto goethite:Effects of pH, calcium and phosphate[J]. Colloids & Surfaces B Biointerfaces, 116(14): 591-596. |
Rodriguez-Mozaz S, Chamorro S, Marti E, et al. 2015. Occurrence of antibiotics and antibiotic resistance genes in hospital and urban wastewaters and their impact on the receiving river[J]. Water Research, 69: 234-242. |
Sandra B, Dragana M P, Danijela A, et al. 2010. Determination of multi-class pharmaceuticals in wastewater by liquid chromatography-tandem mass spectrometry (LC-MS-MS)[J]. Analytical & Bioanalytical Chemistry, 398(3): 1185-1194. |
Sun K, Dong S, Sun Y, et al. 2018. Graphene oxide-facilitated transport of levofloxacin and ciprofloxacin in saturated and unsaturated porous media[J]. Journal of Hazardous Material, 348: 92-99. DOI:10.1016/j.jhazmat.2018.01.032 |
Sun K, Sun Y, Gao B, et al. 2019. Effect of cation type in mixed Ca-Na systems on transport of sulfonamide antibiotics in saturated limestone porous media[J]. Environmental Science and Pollution Research International, 26(11): 11170-11178. |
沈志红.2019.去除地下水中硝酸盐的混合碳源研究[D].杨凌: 西北农林科技大学 http://cdmd.cnki.com.cn/article/cdmd-10712-1012260507.htm
|
孙秋根, 王智源, 董建玮, 等. 2018. 太湖流域河网4种典型抗生素的时空分布和风险评价[J]. 环境科学学报, 38(11): 4400-4410. |
Tan Y, Guo Y, Gu X, et al. 2015. Effects of metal cations and fulvic acid on the adsorption of ciprofloxacin onto goethite[J]. Environmental Science and Pollution Research, 22(1): 609-617. |
Thiele-Bruhn S. 2003. Pharmaceutical antibiotic compounds in soils-a review[J]. Journal of Plant Nutrition and Soil Science, 166(2): 145-157. DOI:10.1002/jpln.200390023 |
Tian Y, Gao B, Silvera-Batista C, et al. 2010. Transport of engineered nanoparticles in saturated porous media[J]. Journal of Nanoparticle Research, 12(7): 2371-2380. |
Tong L, Huang S, Wang Y, et al. 2014. Occurrence of antibiotics in the aquatic environment of Jianghan Plain, central China[J]. Science of the Total Environment, 497/498: 180-187. |
童蕾, 姚林林, 刘慧, 等. 2016. 抗生素在地下水系统中的环境行为及生态效应研究进展[J]. 生态毒理学报, 11(2): 27-36. |
Yang L, Wu L, Liu W, et al. 2016. Dissipation of antibiotics in three different agricultural soils after repeated application of biosolids[J]. Environmental Science and Pollution Research, 25(1): 104-114. |
Zorita S, Martensson L, Mathiasson L. 2009. Occurrence and removal of pharmaceuticals in a municipal sewage treatment system in the south of Sweden[J]. Science of the Total Environment, 407(8): 2760-2770. DOI:10.1016/j.scitotenv.2008.12.030 |
张玉玺, 孙继朝, 陈玺, 等. 2011. 珠江三角洲浅层地下水pH值的分布及成因浅析[J]. 水文地质工程地质, 38(1): 16-21. DOI:10.3969/j.issn.1000-3665.2011.01.004 |
张国栋, 董文平, 刘晓辉, 等. 2018. 我国水环境中抗生素赋存、归趋及风险评估研究进展[J]. 环境化学, 37(7): 1491-1500. |
 2020, Vol. 40
2020, Vol. 40


