2. 西北水资源与环境生态教育部重点实验室, 西安 710055;
3. 中国环境科学研究院大气污染控制技术研究中心, 北京 100012
2. Key Laboratory of Northwest of Water Resources and Environmental Ecology, Ministry of Education, Xi'an 710055;
3. Research Center of Air Pollution Control Technology, Chinese Research Academy of Environmental Sciences, Beijing 100012
挥发性有机污染物(VOCs)种类繁多, 成分复杂, 对环境及人体均有较大危害(Charbotel et al., 2014;Sott et al., 2014;Macleod et al., 2017), 其排放源主要以机动车尾气、溶剂使用和工业过程的废气为主(栾志强等, 2011;Mok et al., 2011).低温等离子体作为近些年兴起的去除VOCs的一种新技术, 其耦合吸附/催化技术用于VOCs的氧化获得了学者广泛的关注与研究.吸附/催化剂的存在不仅延长了污染物在介质阻挡反应器(DBD)中的停留时间, 提高了活性物种与污染物的碰撞几率, 还为VOCs的氧化提供了活性位点, 从而提高了VOCs的脱除效率(Durme et al., 2008).
目前的研究表明, 针对不同种类的VOCs, 等离子体耦合催化系统中所适用的催化剂也不同.针对丙酮和乙醇的降解, Lyulyukin等(2016)的研究发现负电晕放电联合MnO2/TiO2催化剂不仅促进了污染物的降解, 还抑制了副产物的生成, 提高了CO2选择性.针对三氯乙烯的降解, Vandenbroucke等(2016)研究结果表明, 负直流电晕放电联合Pd/LaMnO3大大提高了其矿化率, 且有效抑制了O3的排放.针对甲苯的降解, 廖晓斌等(2010)对比了Fe、Mn、Cu、Co 4种金属氧化物的氧化效果, 结果表明, FeOx具有最高的甲苯去除率和能量效率, 而MnOx有效地减少了副产物O3并提高了CO2的选择性.乙酸乙酯是印刷、家具制造涂装行业中各个大多数生产环节中VOCs的常见成分(王海林等, 2012;刘楠等, 2017;佟瑞鹏等, 2018), 而目前等离子体耦合催化系统中针对乙酸乙酯降解所使用的催化剂研究尚不充分, 从而限制了等离子体耦合催化技术在上述行业中的应用.
针对上述问题, 本研究以13X为载体, 采用等体积浸渍法分别制备Mn、Mo和Fe的金属氧化物催化剂, 并将其作为介质阻挡放电(DBD)的填料用于吸附态乙酸乙酯的氧化降解.以矿化率、CO2选择性以及副产物的生成量为评价指标, 探究了不同活性组分及13X和γ-Al2O3的混合比例对乙酸乙酯的氧化性能的影响.最后, 结合FTIR测定的反应器出口气体中和GC-MS测定的催化剂表面的中间有机副产物, 分析了吸附态乙酸乙酯在DBD中的降解机理.
2 实验(Experiment) 2.1 催化剂的制备与表征采用等体积浸渍法制备Mn/13X、Fe/13X和Mo/13X.具体制备方法如下:将一定量的Mn(NO3)2、(NH4)6Mo7O24或Fe(NO3)3 · 9H2O前驱体溶液缓慢滴加于13X小球上(直径为3 mm, 上海有新催化剂厂), 静置24 h, 之后在105 ℃的烘箱内烘6 h, 最后置于500 ℃马弗炉中煅烧6 h, 制得所需催化剂.
催化剂的还原性能采用美国麦克ChemiSorb 2720化学吸附仪通过氢气程序升温还原(H2-TPR)测定.测定方法如下:先将100 mg的催化剂在250 ℃于N2中预处理1 h, 冷却至室温, 然后在40 mL · min-1的H2中, 以10 ℃ · min-1的升温速率从50 ℃升至950 ℃.催化剂表面的副产物采用二氯甲烷进行萃取后用GC-MS(GCMS-QP2010 Ultra, Japan)测定.色谱柱为Rtx-5MS, 程序升温条件为:初始温度40 ℃, 保持2 min, 然后以6 ℃ · min-1的速率升温至220 ℃并维持5 min.质谱检测器采用全扫描方式.
2.2 实验系统实验系统如图 1所示, 主要包括模拟废气发生部分、高压供电部分、等离子体反应装置和气体分析部分.模拟废气发生部分包含:模拟空气(79% N2、21% O2)、质量流量计、注射泵、恒温水浴锅和缓冲混合瓶, 用于产生1 L · min-1、1571 mg · m-3的乙酸乙酯.高压供电部分包括:50 Hz交流高压电源(GJTK-0.01/30K, 上海南罡电除尘器有限公司)、高压探针和示波器.等离子体反应装置为自制的线管式反应器, 材质为石英玻璃(内径=21.5 mm), 内电极为不锈钢丝(直径=0.8 mm), 外电极为100 mm长的铜皮缠绕在反应器外壁接地.本实验分为吸附和放电两个阶段:①1 L · min-1、1571 mg · m-3的废气吸附20 min, 吸附存储31.42 mg的乙酸乙酯在填充的催化剂表面, 此过程不放电;②在放电阶段, 以1 L · min-1的空气为放电背景气, 利用放电产生的活性粒子将吸附态乙酸乙酯氧化降解.吸附阶段与放电阶段反应器出口均无乙酸乙酯逃逸.实验中CO2、CO、N2O和C4H8O2(乙酸乙酯)浓度均由采用傅里叶变换红外光谱仪(Nicolet Antaris IGS, Thermo Scientific Company)测定, O3浓度由臭氧检测仪(2B Technologies Model 106-M)在线检测.
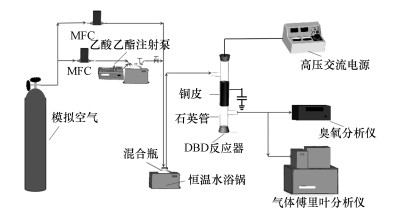 |
| 图 1 实验系统流程图 Fig. 1 Schematic view of the experimental set-up |
实验中乙酸乙酯氧化的评价指标为矿化率(MR)和CO2选择性(SCO2), 方法分别见式(1)和式(2).
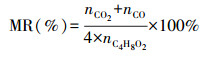
|
(1) |
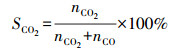
|
(2) |
式中, nC4H8O2为乙酸乙酯的初始吸附量(mmol);nCO2、nCO分别为等离子体氧化降解阶段反应器出口的CO2及CO的量(mmol).
3 结果与讨论(Results and discussion) 3.1 催化剂活性组分对乙酸乙酯降解的影响 3.1.1 矿化率图 2a为不同活性组分的催化剂与低温等离子体联合氧化降解吸附态乙酸乙酯时, COx浓度随放电时间的变化曲线图.随着放电时间的延长, 所有催化剂的COx浓度均呈先上升后降低的趋势.这是因为放电开始阶段, 活性粒子与催化剂表面大量的乙酸乙酯反应生成了较多的COx, 而随着放电时间的推移, 活性粒子数量没变, 但催化剂表面的乙酸乙酯量减少, 所以氧化生成的COx逐渐降低.与13X相比, 负载活性组分后COx的峰值浓度明显提高, 说明活性组分的负载对乙酸乙酯的等离子体矿化有明显的促进作用.王爱华等(2015)研究中指出, 与γ-Al2O3相比, 负载Mn-Ag后, 甲苯降解率显著增加, 说明活性组分的负载有助于提高催化剂活性.Zhu等(2015)的研究显示, 活性组分的负载不仅有效提高丙酮的降解率, 也大大降低了副产物的排放.本实验中, Mn/13X的矿化效果最佳, 不仅峰值浓度最高, 放电120 min后, 矿化率也最高可达61.5%.图 2b是等离子体联合不同催化剂降解乙酸乙酯时放电120 min过程中CO2的选择性.从图中可以看出, Mn/13X的SCO2最高, 这是由于Mn对O3有较强的分解能力, 分解产生的活性氧可将CO进一步氧化为CO2, 从而有效提高了SCO2(廖晓斌等, 2010).
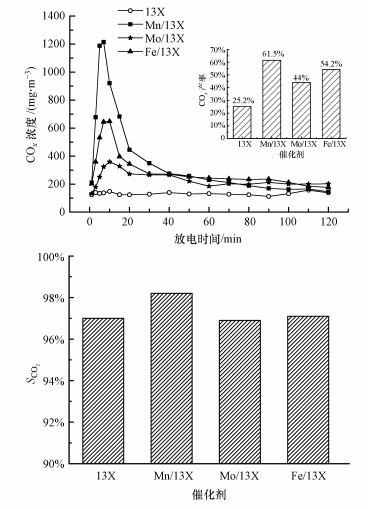 |
| 图 2 不同活性组分的COx浓度(a)和CO2选择性(b) Fig. 2 COx concentration(a) and CO2 selectivity(b)of catalyst |
催化剂的比表面积见表 1.活性组分的负载会占据一定的分子筛孔道(康忠利等, 2017), 使得13X的比表面积显著降低, 相比于Fe/13X和Mo/13X, Mn/13X的比表面积最高, 有效增加了乙酸乙酯及等离子体活性物质在催化剂表面的碰撞几率(陈春雨等, 2012), 同时也有利于乙酸乙酯及产物在催化剂上快速吸附和脱附(张玮等, 2013), 从而促进了乙酸乙酯的氧化.但催化剂的比表面积并不与其氧化活性成正比, 说明, 比表面积对催化活性存在一定影响, 但并不是唯一影响因素.为进一步探究Fe、Mo与Mn的等离子体催化活性之间存在差异的原因, 对其进行了H2-TPR表征, 结果如图 3所示.Fe/13X在662 ℃处有一个还原峰, Mo/13X在793 ℃处有一个还原峰, Mn/13X在430 ℃和650 ℃处各存在1个还原峰, 分别代表Mn4+被还原为Mn3+, Mn3+被还原为Mn2+(Song et al., 2018;Wang et al., 2019).还原峰温度从高到低次序为Mo/13X>Fe/13X>Mn/13X, 与其COx产率顺序刚好相反, 说明催化剂的还原峰的温度越低即催化剂的还原性越好(贾永芹等, 2018)越有利于等离子体的催化氧化.
| 表 1 催化剂的比表面积 Table 1 Specific surface area of the catalysts |
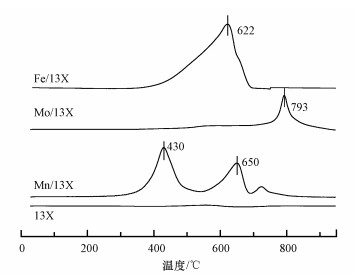 |
| 图 3 催化剂的H2-TPR Fig. 3 H2-TPR of catalysts |
图 4a为不同活性组分的催化剂与低温等离子体联合氧化降解吸附态乙酸乙酯时反应器出口的O3浓度, 该浓度由O3的产生量与分解量共同决定.O3的产生及分解过程如式(3)~(6)所示(Einaga et al., 2009;Guo et al., 2015).
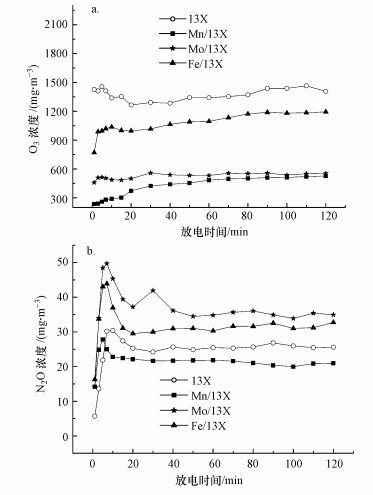 |
| 图 4 O3(a)和N2O(b)浓度随放电时间的变化 Fig. 4 Change of O3 (a) and N2O (b)concentration with discharge time |
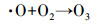
|
(3) |
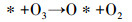
|
(4) |
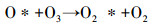
|
(5) |

|
(6) |
从图 4a中可以看出, 与13X相比, 负载活性组分后, 反应器出口O3排放浓度显著降低, 这是由于活性组分的负载促进了臭氧的分解(式(4)).填充Mn/13X的反应器出口的O3浓度最低, 这可能是由于与Fe和Mo的氧化物相比, Mn的氧化物对O3的分解能力最强.赵业红(2016)的研究里也证明了Mn的氧化物对O3有很强的分解能力.
N2O是等离子体降解乙酸乙酯过程中的另一种副产物, 其形成过程如式(7)和(8)所示(Zheng et al., 2014).图 4b是介质阻挡放电联合不同催化剂氧化降解乙酸乙酯时, N2O的排放浓度.与13X相比, 仅负载MnOx时, N2O排放量有所降低, Dang等的研究也得到了相似的结论(Dang et al., 2013), 这可能是因为Mn等金属氧化物存在时, 产生的活性氧原子将部分N2O直接分解为N2和O2(式(9)~(10))(薛莉, 2007).但负载Fe和Mo后, N2O的排放浓度反而比13X高, 这可能是由于Fe和Mo的负载促进了空气中N2的活化, 产生了更多的N2(A)所致, 具体如式(7)和式(8)所示.
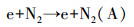
|
(7) |
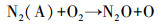
|
(8) |

|
(9) |
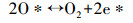
|
(10) |
课题组前期的研究表明, 13X中添加适量的γ-Al2O3可以提高NTP氧化挥发性有机物的性能(秦彩虹等, 2017).为了进一步提高乙酸乙酯的氧化性能, 故在Mn/13X中添加了不同质量的γ-Al2O3, 结果如图 5所示.随着γ-Al2O3添加比例的增加, 乙酸乙酯的矿化率呈现先增加后减少的趋势, 当Mn/13X与γ-Al2O3的质量比为1 : 1时, 乙酸乙酯的矿化率最高, 可达64.4%.Mn/13X与γ-Al2O3的混合存在最佳的质量比是由于乙酸乙酯的矿化取决于两方面:①低温等离子体产生的活性粒子数;②催化剂的活性位点.γ-Al2O3的介电常数较高(Kim et al., 2015), 其含量越高产生的活性粒子也较多, 而Mn/13X虽然介电常数相对较低, 但其含量越高可为乙酸乙酯的氧化提供的催化活性位点越多.
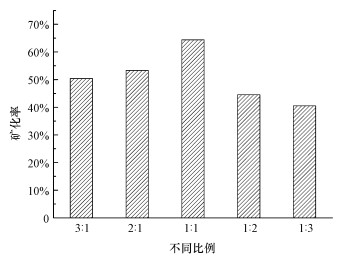 |
| 图 5 混合催化剂的矿化率 Fig. 5 Mineralization rate of mixed catalyst |
图 6a显示, 由不同质量比混合的Mn/13X和γ-Al2O3的催化剂联合NTP氧化乙酸乙酯时, 反应器出口O3浓度从大到小顺序为:1 : 3>1 : 2>1 : 1≈2 : 1≈3 : 1.显然, O3浓度随Mn/13X占比的增加而降低, 再次证明Mn的氧化物对O3有很好的分解作用.图 6b表明NTP联合不同混合比催化剂产生N2O浓度从大到小顺序依次为:1 : 3>1 : 2>1 : 1>2 : 1>3 : 1.γ-Al2O3比例越高, N2O产生量越高, 这可能是因为γ-Al2O3具有较高的介电常数, 产生了较多的高能电子, 从而提高了N2(A)的产率, 如式(5)所示, 导致N2O的排放较高.
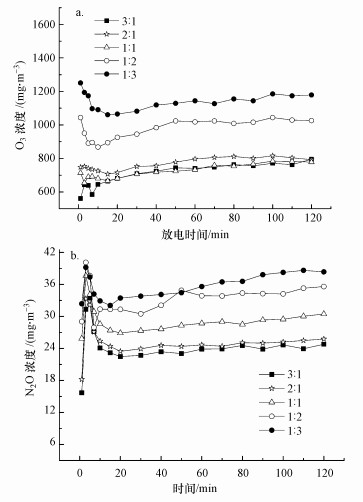 |
| 图 6 O3(a)和N2O(b)浓度随放电时间的变化 Fig. 6 Change of O3 (a) and N2O(b) concentration with discharge time |
图 7a为催化剂在放电阶段反应器出口气体的FT-IR图谱.从图中可以看出, 吸附态乙酸乙酯降解过程中产生的副产物除了O3和N2O外, 还存在少量的中间有机产物如甲醛、甲酸和有机酸等.催化剂表面副产物的GC-MS分析表明除了残留的乙酸乙酯外, 还存在少量甲醇和丙酸乙烯基酯(图 7b).结合以上结果可以推测, 吸附态乙酸乙酯在NTP中的氧化途径如图 8所示, 可分为3部分:①放电过程中产生的高能电子直接将乙酸乙酯轰击为碎片, 之后各种碎片进一步与其他活性基团发生反应;②高能电子与空气(N2和O2)发生碰撞形成的多种活性粒子(· OH、O ·和N2(A)等)直接参与乙酸乙酯的氧化(Cai et al., 2019);③O3在催化剂表面分解产生的活性氧将吸附态乙酸乙酯逐步氧化, 最终生成CO2、CO和H2O.
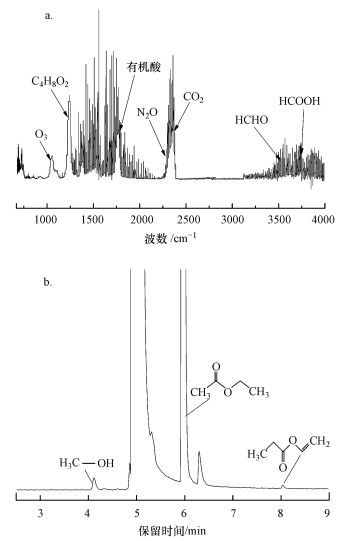 |
| 图 7 催化剂的FT-IR谱图(a)和GC-MS(b) Fig. 7 FT-IR(a) and GC-MS (b)of catalyst |
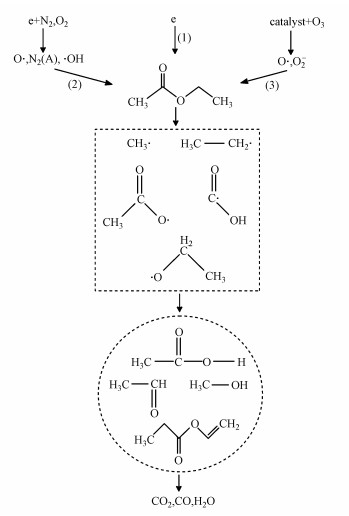 |
| 图 8 乙酸乙酯的氧化降解路径 Fig. 8 Degradation pathway of ethyl acetate |
1) 13X负载Mn、Fe、Mo后的NTP氧化吸附态乙酸乙酯的矿化率明显提高, 其中Mn/13X的矿化效果最佳, 放电120 min后, 其矿化率可达61.5%.另外, 填充Mn/13X的反应器出口的副产物O3和N2O浓度也最低.
2) γ-Al2O3的添加, 可以提高Mn/13X的NTP氧化性能, 但其添加量存在最佳值, 实验结果表明当Mn/13X和γ-Al2O3的质量比为1 : 1时, 矿化率最高.
3) 吸附态乙酸乙酯的降解途径有3种:①放电过程中产生的高能电子直接将乙酸乙酯轰击为碎片;②高能电子与空气(N2和O2)碰撞形成的活性粒子直接参与乙酸乙酯的氧化;③O3在催化剂表面分解产生的活性氧参与吸附态乙酸乙酯的氧化.
陈春雨, 刘彤, 王卉, 等. 2012. 低温等离子体与MnOx/γ-Al2O3协同催化降解正己醛[J]. 催化学报, 33(6): 941-951. |
Cai Y X, Zhu X B, Hu W X, et al. 2019. Plasma-catalytic decomposition of ethyl acetate over LaMO3 (M=Mn, Fe, and Co) perovskite catalysts[J]. Journal of Industrial and Engineering Chemistry, 70: 447-452. DOI:10.1016/j.jiec.2018.11.007 |
Charbotel B, Fervers B, Droz J P. 2014. Occupational exposures in rare cancers:A critical review of the literature[J]. Critical Reviews in Oncology/Hematology, 90: 99-134. DOI:10.1016/j.critrevonc.2013.12.004 |
Dang X Q, Huang J Y, Cao L, et al. 2013. Plasma-catalytic oxidation of adsorbed toluene with gas circulation[J]. Catalysis Communications, 40: 116-119. DOI:10.1016/j.catcom.2013.06.025 |
Durme J V, Dewulf J, Leys C, et al. 2008. Combining non-thermal plasma with heterogeneous catalysis in waste gas treatment:A review[J]. Applied Catalysis B Environmental, 78: 324-333. DOI:10.1016/j.apcatb.2007.09.035 |
Einaga H, Ogata A. 2009. Benzene oxidation with ozone over supported manganese oxide catalysts:Effect of catalyst support and reaction conditions[J]. Journal of Hazardous Materials, 164: 1236-1241. DOI:10.1016/j.jhazmat.2008.09.032 |
Guo Y F, Liao X B, Fu M L, et al. 2015. Toluene decomposition performance and NOx by-product formation during a DBD-catalyst process[J]. Journal of Environmental Sciences, 28: 187-194. DOI:10.1016/j.jes.2014.06.048 |
贾永芹, 张晓晶. 2018. MnOx催化剂用于甲苯催化氧化反应的研究[J]. 环境污染与防治, 40(5): 518-520. |
康忠利, 党小庆, 秦彩虹, 等. 2017. 锰银复合催化剂对NTP降解吸附态甲苯的影响[J]. 环境工程, 35(2): 72-77. |
Kim H H, Teramoto Y, Negishi N, et al. 2015. A multidisciplinary approach to understand the interactions of nonthermal plasma and catalyst:A review[J]. Catalysis Today, 256: 13-22. DOI:10.1016/j.cattod.2015.04.009 |
刘楠, 滕富华, 陆建海, 等. 2017. 光催化-吸收法处理家具涂装废气中试试验[J]. 浙江大学学报, 51(2): 393-398. |
廖晓斌, 郭玉芳, 叶代启. 2010. 不同金属氧化物对等离子体降解甲苯的作用研究[J]. 环境科学学报, 30(9): 1824-1832. |
栾志强, 郝郑平, 王喜芹. 2011. 工业固定源VOCs治理技术分析评估[J]. 环境科学, 32(12): 3476-3486. |
Lyulnyukin M N, Besov A S, Vorontsov A V. 2016. Acetone and ethanol vapor oxidation via negative atmospheric corona discharge over titania-based catalysts[J]. Applied Catalysis B:Environmental, 183: 18-27. DOI:10.1016/j.apcatb.2015.10.025 |
Macleod J S, Harris M A, Tjepkema M, et al. 2017. Cancer risks among welders and occasional welders in a national population-based cohort study:Canadian census health and environmental cohort[J]. Safety and Health at Work, 8: 258-266. DOI:10.1016/j.shaw.2016.12.001 |
Mok Y S, Kim D H. 2011. Treatment of toluene by using adsorption and nonthermal plasma oxidation process[J]. Current Applied Physics, 11: S58-S62. DOI:10.1016/j.cap.2011.05.023 |
秦彩虹, 党小庆, 黄家玉, 等. 2017. 混合吸附剂对吸附-间歇低温等离子体氧化甲苯的影响[J]. 环境科学学报, 37(2): 520-527. |
Scott C E, Rap A, Spracklen D V, et al. 2014. The direct and indirect radiative effects of biogenic secondary organic aerosol[J]. Atmospheric Chemistry and Physics, 14: 447-470. DOI:10.5194/acp-14-447-2014 |
Song H, Hu F Y, Peng Y, et al. 2018. Non-thermal plasma catalysis for chlorobenzene removal over CoMn/TiO2 and CeMn/TiO2:Synergistic effect of chemical catalysis and dielectric constant[J]. Chemical Engineering Journal, 347: 447-454. DOI:10.1016/j.cej.2018.04.018 |
佟瑞鹏, 张磊, 杨校毅, 等. 2018. 家具制造过程中VOCs的来源分析及环境健康风险评价[J]. 环境科学, 39(2): 672-683. |
Vandenbroucke A M, Dinh M T N, Nuns N, et al. 2016. Combination of non-thermal plasma and Pd/LaMnO3 for dilute trichloroethylene abatement[J]. Chemical Engineering Journal, 283: 668-675. DOI:10.1016/j.cej.2015.07.089 |
Wang H Q, Chen S, Wang C, et al. 2019. A novel hybrid Bi2MoO6-MnO2 catalysts with the superior plasma induced pseudo photocatalytic-catalytic performance for ethyl acetate degradation[J]. Applied Catalysis B:Environmental, 254: 339-350. DOI:10.1016/j.apcatb.2019.05.018 |
薛莉, 贺泓. 2007. Co-M(M=La, Ce, Fe, Mn, Cu, Cr)复合金属氧化物催化分解N2O[J]. 物理化学学报, 23(5): 664-670. DOI:10.3866/PKU.WHXB20070509 |
王爱华, 樊星, 梁文俊, 等. 2015. 低温等离子体协同锰银催化剂降解甲苯[J]. 工业催化, 23(1): 63-68. DOI:10.3969/j.issn.1008-1143.2015.01.013 |
王海林, 聂磊, 李靖, 等. 2012. 重点行业挥发性有机物排放特征与评估分析[J]. 科学通报, 57(19): 1739-1746. |
张玮, 杨懿, 王沛涛, 等. 2013. 氧化物催化剂对非热等离子体催化降解甲苯的影响[J]. 环境工程学报, 7(7): 2655-2661. |
赵业红. 2016.直流电晕低温等离子体协同催化降解低浓度挥发性有机废气的研究[D].杭州: 浙江大学 http://cdmd.cnki.com.cn/Article/CDMD-10335-1016054604.htm
|
Zheng C H, Zhu X B, Gao X, et al. 2014. Experimental study of acetone removal by packed-bed dielectric barrier discharge reactor[J]. Journal of Industrial & Engineering Chemistry, 20: 2761-2768. |
Zhu X B, Gao X, Yu X N, et al. 2015. Catalyst screening for acetone removal in a single-stage plasma-catalysis system[J]. Catalysis Today, 256: 108-114. DOI:10.1016/j.cattod.2015.01.028 |
 2020, Vol. 40
2020, Vol. 40


