2. 中国科学院安徽光学精密机械研究所大气物理化学实验室, 合肥 230031
2. Laboratory of Atmospheric Physico-Chemistry, Anhui Institute of Optics and Fine Mechanics, Chinese Academy of Sciences, Hefei 230031
来源于机动车尾气等人为源排放的甲苯等苯系物是大气中主要的污染性挥发性有机化合物和二次有机气溶胶(secondary organic aerosol, SOA)的前体物(Drozd et al., 2019).除了本身具有较大的毒性, 排放到大气中的甲苯会同OH自由基发生甲基氢提取和OH添加到苯环的加成反应, 产生苯甲基自由基(C6H5CH2·)和OH-甲苯自由基(CH3C6H5OH·).这两个自由基随后与氧气和氮氧化物反应, 产生苯甲醛、5-甲基-6-氧代-2, 4-己二烯、乙二醛、甲基乙二醛和其他醛类产物.这些产物通过自身凝结或与发生气体相/微粒相均分过程形成SOA粒子(Hinks et al., 2018).SOA粒径小于2.5 μm, 是大气细粒子(PM2.5)的重要组成部分, 它们能够吸收太阳辐射, 引起大气能见度下降, 危害人类健康(Baltensperger, 2010).因此, SOA形成机理和化学组分研究引起了人们的极大关注.
大气中存在各种各样无机气溶胶细粒子, 它们具有比较大的比表面积, 可以作为种子气溶胶, 可成为光氧化产物凝结、成核和反应的场所, 从而影响SOA的形成和化学组分(Ge et al., 2017).由氨与硫酸反应形成的硫酸铵((NH4)2SO4)是城市大气中常见的无机细粒子(Robinson et al., 2013).前期烟雾腔实验主要开展硫酸铵种子气溶胶对苯系物SOA产率的研究(Edney et al., 2000;Cocker Ⅲ et al., 2001;Jang et al., 2002;Hao et al., 2007;Kroll et al., 2007;Lu et al., 2009;Huang et al., 2013).Edney等(2000)研究发现, 低浓度(0.2~40 μg · m-3)硫酸铵种子气溶胶对甲苯SOA的产率几乎没有影响.Cocker等(2001)的烟雾腔实验也证实低浓度硫酸铵种子气溶胶与甲苯SOA不存在正相关或负相关的关系.Jang等(2002)的实验则发现当低浓度硫酸铵种子气溶胶中存在硫酸等无机酸时, 酸性硫酸铵能够催化气相羰基化合物发生水合、聚合等非均相反应产生低挥发性、高分子量产物进入粒子相, 从而提高SOA的产率.而当烟雾腔内存在较高浓度(40~100 μg · m-3)硫酸铵种子气溶胶时, Hao等(2007)、Kroll等(2007)、Lu等(2009)和Huang等(2013)观察到苯系物SOA的产率明显提高.他们认为, 高浓度(NH4)2SO4种子气溶胶具有较大的比表面积, 既有利于苯系物光氧化气相产物在其表面凝结, 又可以为气相产物提供更多的非均相反应的位点, 从而有利于SOA的形成.
上述烟雾腔实验开展了高浓度硫酸铵种子气溶胶对苯系物SOA产率的影响, 但这些实验仅限于单一硫酸铵种子气溶胶对产率的考察, 仅将硫酸铵种子气溶胶作为气相产物凝结和非均相反应中心来解释SOA产率的增加.而实际大气中多为酸性硫酸铵细粒子(Riccobono et al., 2012), 这些粒子具有较强的吸湿性, 其表面吸湿后形成水相气溶胶.水相中的NH4+具有一定的还原性, 可跟羰基化合物反应形成含氮有机物.Kampf等(2012)和Maxut等(2015)研究发现NH4+能与乙二醛发生水相反应形成咪唑类含氮产物.因此酸性硫酸铵种子气溶除作为气相产物凝结和非均相反应中心外, NH4+能够参与反应促进含氮有机物和SOA的形成.然而, 这些实验未见含氮有机物组分信息和形成机理的报道.
随着我国经济的快速发展, 机动车保有量日益增多, 化石燃料的大量使用, 城市大气含有浓度较大的无机细粒子和SO2(Li et al., 2018).SO2被氧化成H2SO4, 因为其低挥发性, 形成的H2SO4主要存在于颗粒相中, 导致城市大气中含有高浓度的酸性细粒子(Riccobono et al., 2012).如北京和上海等城市发生灰霾污染时, 气溶胶颗粒中H+、NH4+、SO42-和其他无机离子的浓度可达100~300 μg · m-3 (Shao et al., 2018).因此, 我国城市大气中含有较高浓度的酸性硫酸铵细粒子.这些细粒子具有较大的比表面积, 可作为种子气溶胶, 成为气相羰基化合物凝结和非均相反应的中心.此外, 酸性硫酸铵细粒子表面吸湿后形成水相气溶胶, 有利于NH4+与羰基化合物反应形成咪唑类含氮有机物.咪唑类含氮有机物具有较强的吸光能力, 是大气棕色碳的主要组分(Laskin et al., 2015).因此, 开展高浓度的酸性硫酸铵种子气溶胶对苯系物SOA的形成和化学组分的影响有助于了解咪唑类含氮产物组分信息和形成机理.课题组前期利用烟雾腔研究了硫酸铵、硝酸钠、氯化钙等种子气溶胶对甲苯、1, 3, 5三甲苯SOA化学组分的影响(Huang et al., 2013;Huang et al., 2016).在此基础上, 本文利用PM2.5粒子检测仪、紫外-可见分光光度计(UV-Vis)和液相色谱-质谱(LC-MS)测量不同浓度的酸性硫酸铵种子气溶胶存时甲苯SOA的浓度和化学组分, 考察酸性硫酸铵种子气溶胶对甲苯SOA形成和化学组分的影响情况, 为研究酸性无机细粒子背景下咪唑类棕色碳的形成机制提供实验依据.
2 材料与方法(Materials and methods) 2.1 实验药品甲苯(AR, ≥99.5%)购于汕头市达濠精细化学品有限公司;甲醇(GR, ≥99.0%), 购于Sigma Aldrich(上海)贸易有限公司;硫酸(AR, 98%)购于国药集团化学试剂有限公司;硫酸铵(AR, ≥99.0%), 购于西陇化工股份有限公司;酸性硫酸种子气溶胶由美国TSI 9302雾化气溶胶发生器将硫酸铵和硫酸混合溶液雾化、并通过硅胶扩散干燥管后产生.以上药品未作提纯处理, 直接用于实验.
2.2 实验方法酸性硫酸铵种子气溶胶实验是在自制的烟雾腔系统中进行的.该装置主要由零空气产生系统、进样系统、光照反应系统和产物收集检测系统4部分组成(徐俊等, 2018;徐俊等, 2019).空气压缩机产生的压缩空气依次通过活性炭、变色硅胶和Balston DFU Grade BX过滤器去除碳氢化合物、水分和悬浮颗粒物, 得到洁净空气.用泵吸式VOCs检测仪(XLA-BX-VOC, 深圳市普利通电子科技有限公司)和PM2.5粒子检测仪(CEM-DT96, 深圳华盛昌机械实业有限公司)测得洁净空气中VOCs和颗粒物的浓度均为零, 满足实验要求.洁净空气通过250 mL的反应物液体气化瓶, 进入厚度为0.1 mm Teflon制作的400 L烟雾腔中.实验在常温常压下进行, 烟雾腔内的相对湿度为37%±3%.每次实验开始前先用约200 L洁净空气清洗气袋3次, 再向气袋中充入约为1/3~1/2体积的洁净空气.用TSI 9302雾化气溶胶发生器以12 psi的压强将硫酸铵和硫酸混合溶液雾化产生粒径小于2 μm的酸性硫酸铵种子气溶胶, 通过硅胶扩散干燥管后由进气口注入烟雾腔中.随后用微升注射器抽取一定量甲苯注入到已用控温电热套加热至80 ℃的液体气化瓶中, 使其受热挥发, 并随洁净空气通过进气口进入烟雾腔中.O3由O3发生器(XM-TS, 青岛新美净化设备有限公司)产生, 通过进气口充入烟雾腔中.最后用洁净空气充至满体积.打开4只特征波长为254 nm的紫外灯光照启动光化学反应和O3在波长为254 nm的紫外光照射下会产生OH自由基, 启动甲苯光氧化反应形成二次有机气溶胶.依次采用GC-FID(Agilent 7890B, 安捷伦科技有限公司)和O3分析仪(SPT-GT-1000-O3, 北京思普特科技有限公司)测量烟雾腔内甲苯和O3的浓度.利用PM2.5粒子检测仪测量腔内SOA粒子的浓度, 该仪器的分辨率为1 μg · m-3, 测量误差在±3%范围内.
所有实验腔内甲苯和O3的浓度保持不变, 分别为1×10-6和10×10-6.在种子气溶胶酸度实验中, 保持0.001 mol · L-1 (NH4)2SO4的浓度不变, 通过控制(NH4)2SO4与H2SO4物质的量浓度来控制种子气溶胶的酸度.依次配制了(NH4)2SO4与H2SO4物质的量浓度比分别为1:1、1:2、1:3、1:4、1:5、1:6和1:7的混合溶液250 mL, 使用TSI 9302产生种子气溶胶通入烟雾腔一段时间, 使腔内酸性种子气溶胶的浓度为100 μg · m-3.而在种子气溶胶浓度实验中, 用0.001 mol · L-1 (NH4)2SO4和0.005 mol · L-1 H2SO4混合溶液雾化产生酸性种子气溶胶.利用TSI 9302产生的细粒子的通入时间来改变腔内种子气溶胶的浓度, 依次设置为20、40、60、80、100、150、200 μg · m-3.每个实验平行进行3次, 每次实验光照反应结束后, 用装有3%甲醇溶液10 mL的洗气瓶以4 L · min-1的流速收集SOA粒子, 通过洗瓶的气体经硅胶扩散干燥管后用PM2.5粒子检测仪测得颗粒物的浓度为零, 表明SOA粒子被收集到3%甲醇溶液中.将烟雾腔内所有的SOA收集完毕后, 随即以3%甲醇溶液为参比, 利用双光束紫外-可见分光光度计(UV-6100s, 上海Mapada公司)测量紫外可见吸收光谱, 光谱扫描范围为200 ~ 600 nm, 扫速为中速, 扫描间隔为1 nm.同时, 甲苯SOA收集液经滤膜(0.45 μm Nylon 66, 津腾实验设备有限公司)过滤后, 采用高效液相色谱质谱仪(ABI 3200QTRAP, 美国Applied Biosystems公司)测量甲苯SOA样品的质谱.自动进样器将5 μL甲苯SOA收集液样品注入到未装有色谱柱的液相色谱系统, 采用甲醇和正己烷的混合溶液作为流动相, 其体积比为2:3, 流速为0.20 mL · min-1, 将样品引入电离区.该质谱仪采用电喷雾(ESI)电离, 质量测量范围为5 ~ 1700 amu, 分辨率> 6900, 扫描速度为4000 amu · s-1.根据测得的质谱图上的离子峰获得甲苯SOA化学组分信息.值得注意的是, 实验使用烟雾腔的体积较小, 存在气相和颗粒相的壁损失.但是本文的主要侧重点是利用PM2.5粒子检测仪、高效液相色谱串联质谱仪和紫外-可见分光光度计定性研究不同浓度酸性硫酸铵种子气溶胶对甲苯SOA形成和化学组分的影响.因此, 本文未校正气相和颗粒相的壁损失.壁损失的存在虽导致所有实验测量和收集的SOA的量减小, 仍能定性揭示酸性硫酸铵种子气溶胶对甲苯SOA形成和化学组分的影响规律.
3 结果与讨论(Results and discussion) 3.1 酸性硫酸铵种子气溶胶对甲苯SOA形成的影响没有种子气溶胶存在时, 对于甲苯1×10-6和10×10-6 O3的反应体系, 不同辐照时间时烟雾腔内甲苯SOA的浓度如图 1所示.OH自由基与甲苯反应产生半挥发性和难挥发性气相产物, 这些产物需要达到饱和的蒸气压才能凝结形成SOA粒子, 因此, 在反应的前15 min内, 腔内SOA的浓度仅为12 μg · m-3.在随后的15~180 min内, 随着反应的进行, 产生更多的半挥发性有机物, 这些产物参加气相/粒子相均分, 形成的SOA的浓度逐渐增大.在光照180 min时, 利用GC-FID未能检测到甲苯, 表明腔内的甲苯已经完全反应, 对应的SOA的浓度达到最大值87 μg · m-3.此后, 由于甲苯反应完全, 光化学反应趋于停止, SOA粒子由于湍流, 布朗扩散和重力沉降等原因沉积在烟雾腔壁上, 造成SOA粒子浓度逐渐减少(刘宪云等, 2009).
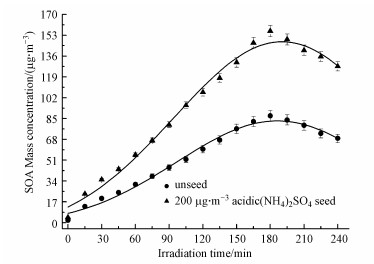 |
| 图 1 没有种子气溶胶和200 μg · m-3酸性硫酸铵种子气溶胶存在时, 不同光照时间下甲苯SOA的浓度 Fig. 1 Concentration of toluene SOA at different light times in the absence of seed aerosol and with 200 μg · m-3 acidic ammonium sulfate seed aerosol |
对于种子气溶胶实验, 从PM2.5粒子检测仪测得的气溶胶质量浓度减去酸性(NH4)2SO4种子气溶胶的初始浓度, 得到了甲苯SOA的质量浓度.在不同(NH4)2SO4与H2SO4物质的量浓度比溶液产生的100 μg · m-3酸性(NH4)2SO4种子气溶胶存在时, 形成的甲苯SOA的最大质量浓度见图 2.由图 2可知, 甲苯SOA的最大质量浓度随着(NH4)2SO4与H2SO4物质的量浓度比的增大而逐渐增加, 酸性(NH4)2SO4种子气溶胶对甲苯SOA形成有促进作用.根据Jang等(2002)提出的酸催化非均相反应机理, 吸湿的种子气溶胶表面含有的氢离子越多, 酸催化效应越强, 会有更多气相的羰基化合物进入粒子相, 从而导致形成SOA的量越大.由于本论文中甲苯和臭氧的浓度保持不变, 因而产生的气相羰基产物也是一定的.当硫酸铵与硫酸物质的量浓度比为1:5产生的种子气溶胶中的氢离子已能够催化所有产生的气相二醛化合物发生水合反应, 再增大氢离子浓度, 催化效应不再增强, SOA的浓度几乎保持不变.因此用0.001 mol · L-1 (NH4)2SO4和0.005 mol · L-1 H2SO4混合溶液雾化产生酸性种子气溶胶, 开展不同浓度酸性硫酸铵种子气溶胶对甲苯SOA的形成和组分影响实验.
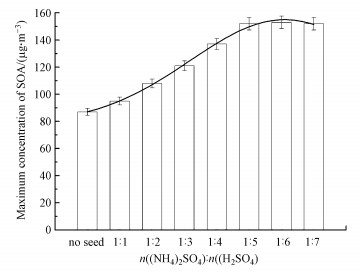 |
| 图 2 不同硫酸铵和硫酸摩尔比混合溶液产生的酸性硫酸铵种子气溶胶存在时形成的最大甲苯SOA质量浓度 Fig. 2 The maximum concentration of toluene SOA in the presence of acidic ammonium sulfate seed aerosol produced by mixed solutions with different molar ratios of ammonium sulfate and sulfuric acid |
200μg · m-3酸性(NH4)2SO4种子气溶胶存在时, 如图 1所示, 甲苯SOA粒子浓度随光照时间的变化曲线与没有种子气溶胶的情形相类似.然而, 光照180 min时, 腔内甲苯SOA的最大浓度达到156 μg · m-3, 比没有种子气溶胶的情形增加了79%.此外, 图 3所示的不同浓度酸性(NH4)2SO4种子气溶胶存在时, 甲苯1 ×10-6和10×10-6 O3的反应体系产生的SOA的最大质量浓度在102~158 μg · m-3范围内, 大于没有种子气溶胶时产生的SOA最大质量浓度(87 μg · m-3).这表明, 酸性(NH4)2SO4种子气溶胶对甲苯SOA形成有显著促进作用.值得注意的是, 当(NH4)2SO4种子气溶胶的浓度大于100 μg · m-3时, 甲苯SOA的最大浓度不再继续增加.
 |
| 图 3 不同浓度酸性硫酸铵种子气溶胶存在时产生的最大甲苯SOA质量浓度 Fig. 3 The maximum concentration of toluene SOA in the presence of different concentrations of acidic ammonium sulfate seed aerosol |
图 4a显示了在没有种子气溶胶存在时, 甲苯SOA粒子在200~600 nm范围内的紫外可见吸收光谱.该谱图在205 nm附近有一个较强的吸收带.根据Carlton等(2007)的实验结果, 该吸收带是羧酸化合物的羧基(—COOH)发生n→π*电子跃迁产生的特征吸收.这表明羧酸化合物是没有种子气溶胶存在时甲苯SOA粒子的主要化学组分.前期烟雾腔实验已经测得苯甲醛、5-甲基-6-氧代-2, 4-己二醛、乙二醛、甲基乙二醛等醛类化合物是OH自由基和甲苯光氧化反应的主要气相产物(Jang et al., 2001;Huang et al., 2011;Huang et al., 2013;Hinks et al., 2018).当反应体系存在较高浓度OH自由基时, 醛类化合物能被OH自由基、氧气等氧化生成羧酸产物(Jang et al., 2001).Jang等(2001)和Huang等(2011)利用气相色谱-质谱和气溶胶激光飞行时间质谱仪检测没有种子气溶胶存在时甲苯SOA粒子的化学组分, 也测得苯甲醛、乙二醛酸等羧酸产物.
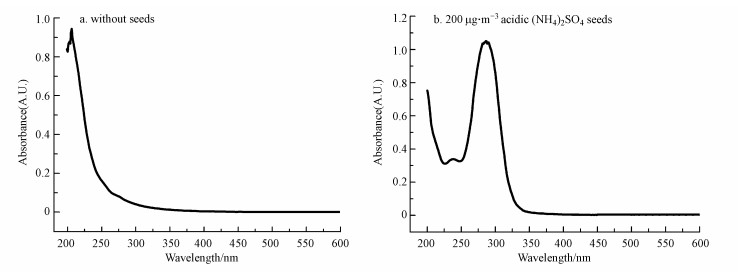 |
| 图 4 没有种子气溶胶(a)和200 μg · m-3酸性种子气溶胶(b)存在时, 甲苯SOA粒子的紫外可见吸收光谱 Fig. 4 UV-Vis spectra of the toluene SOA without(a) and with 200 μg · m-3 acidic (NH4)2SO4 seeds(b) |
甲苯SOA样品溶液不经色谱柱分离, 进入质谱仪经电喷雾电离后测量质谱.电喷雾电离是软电离技术, 采用低电压的方法不会使分子离子峰发生断裂.负电离模式使有机化合物去质子化, 负离子质谱中的质谱峰主要来源于去质子化分子离子[M—H]-, 它提供了有机化合物分子量的信息(Carlton et al. 2007).图 5所示的没有种子气溶胶存在时甲苯SOA粒子的负离子质谱图中明显含有前期烟雾腔实验(Jang et al., 2001;Huang et al., 2011;Hinks et al., 2018;Huang et al., 2013)测得的乙醛酸(m/z 73)、甲基乙醛酸(m/z 87)、草酸(m/z 89)、4-氧代-2-戊烯酸(m/z 113)和苯甲酸(m/z 121)去质子化分子离子.类似的, 新探测到的m/z 129、139、145、155将对应于羧酸化合物的去质子化分子离子.这些质谱结果证实羧酸是没有种子气溶胶存在时甲苯SOA粒子的主要组分, 它们是图 4a中所示的205 nm处的吸收带的主要贡献者.
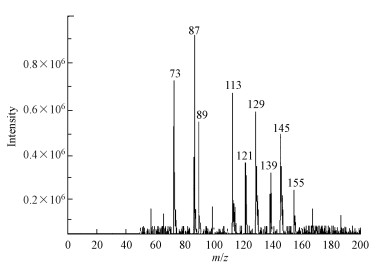 |
| 图 5 没有种子气溶胶存在时甲苯SOA粒子的负离子质谱图 Fig. 5 Negative ion mass spectrum of toluene SOA particles in the absence of seed aerosol |
苯甲醛、乙二醛、甲基乙二醛、4-氧代-2-戊烯醛、2-甲基-2, 3-环氧-丁二醛和5-甲基-6-氧代-2, 4-己二烯等醛类化合物是甲苯光氧化反应的主要气相产物(Jang et al., 2001;Huang et al., 2011;Huang et al., 2013;Hinks et al., 2018).这些形成的气相羰基产物在酸性(NH4)2SO4种子不存在和存在时的后续反应机理是不同的.在没有种子气溶胶存在时, 甲苯SOA粒子主要是由反应产物通过自身凝结形成的.产生的醛类化合物在凝结成SOA粒子之前, 会被OH自由基、氧气氧化成羧酸化合物(Jang et al., 2001).如图 6所示, OH自由基提取苯甲醛羰基上的氢原子, 氧气随即加合形成过氧自由基, 并继续与HO2自由基反应生成O3和苯甲酸(m/z 121).类似的, 乙二醛、甲基乙二醛、4-氧代-2-戊烯醛、2-甲基-2, 3-环氧-丁二醛和5-甲基-6-氧代-2, 4-己二烯能够被氧化成乙二醛酸(m/z 73)、乙二酸(m/z 89)、甲基乙二醛酸(m/z 87)、4-氧代-2-戊烯酸(m/z 113)、2-甲基-4-氧代-2, 3-环氧-丁酸(m/z 129)、2-甲基-2, 3-环氧-丁二酸(m/z 145)、5-甲基-6-氧代-2, 4-己二烯酸(m/z 139)和5-甲基-2, 4-己二烯二酸(m/z 155).生成的羧酸比醛类化合物具有更小的挥发性, 更容易凝结形成SOA粒子.
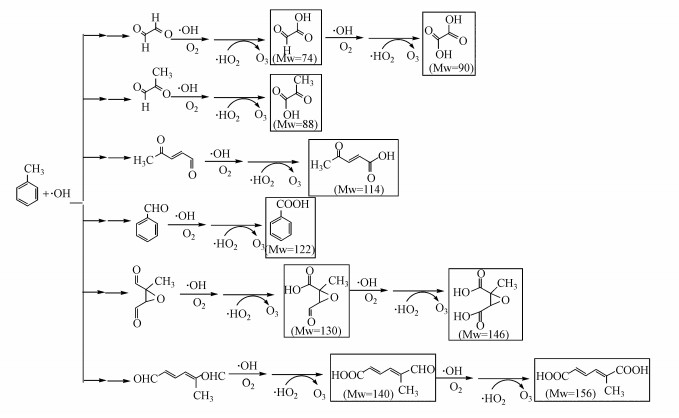 |
| 图 6 形成羧酸产物的可能反应机理 Fig. 6 The possible reaction mechanism for the formation of carboxylic acid products |
图 4b所示的200 μg · m-3酸性(NH4)2SO4种子气溶胶存在时, 甲苯SOA粒子的紫外可见吸收光谱明显不同于没有种子气溶胶存在时的谱图.该谱图的吸收峰红移至280 nm, 表明有新组分产生.Kampf等(2012)和Maxut等(2015)测量的乙二醛和硫酸铵液相反应产物的紫外可见吸收光谱时也呈现有280 nm的吸收带.他们认为发色团可能是由NH4+和乙二醛反应形成的咪唑类产物, 这类产物C N双键中的n→π*跃迁是280 nm吸收带的主要贡献者.由于乙二醛、甲基乙二醛是甲苯SOA主要的α-二羰基组分(Jang et al., 2001;Huang et al., 2011;Huang et al., 2013;Hinks et al., 2018), 因此在酸性(NH4)2SO4种子形成酸性表层后, 发生类似反应以形成咪唑类化合物.
图 7所示的200 μg · m-3酸性(NH4)2SO4种子气溶胶存在时甲苯SOA粒子的负离子质谱图明显不同于图 4, 表明有新的组分产生.图中m/z 67、81、95、123去质子化分子离子[M-H]-对应于咪唑类化合物中的咪唑(C3H3N2-)、甲基咪唑(C4H5N2-)、咪唑醛(C6H4N2O-)和4-甲基-咪唑-2-乙醛(C4H3N2O-). Liu等(2015)在研究间-二甲苯SOA非均相吸收氨的实验也探测到这些咪唑类产物.这些结果表明, 酸性(NH4)2SO4种子气溶胶能够促进咪唑类化合物的形成.由于H2SO4的强吸水性, 酸性(NH4)2SO4种子气溶胶通过吸水在其表面形成含有H+和NH4+的酸性层.OH自由基与甲苯反应产生的乙二醛、甲基乙二醛等醛类化合物在酸性(NH4)2SO4种子气溶胶表面分配时, 发生非均相酸催化反应形成咪唑类产物.如图 8所示, 乙二醛和甲基乙二醛可以通过H+质子化并水解成四醇产物(1).同时, 凝结的二醛化合物可与NH4+反应生成二亚胺产物(2).二亚胺产物(2)上N上的氢会同(1)的OH发生脱水反应形成(3), (3)是不稳定的, N上的孤对电子会亲核进攻四醇上的碳原子, 发生脱水反应, 形成(4), (4)发生电子重排和断裂形成咪唑(m/z 67)或甲基咪唑(m/z 81).此外, (4)也会发生电子重排形成(5), (5)可脱水形成咪唑醛(m/z 95)或4-甲基-咪唑-2-乙醛(m/z 123).形成的咪唑(或甲基咪唑)继续同(1)发生脱水反应形成水合N-乙二醛取代咪唑(m/z 143)(或水合N-甲基乙二醛取代4-甲基咪唑(m/z 171))和水合乙二醛二聚体取代咪唑(m/z 201)(或水合甲基乙二醛二聚体取代4-甲基咪唑(m/z 243))(Kampf et al., 2012;Maxut et al., 2015;Liu et al., 2015).
 |
| 图 7 200 μg · m-3酸性(NH4)2SO4种子气溶胶存在时甲苯SOA粒子的负离子质谱图 Fig. 7 Negative ion mass spectrum of toluene SOA particles in the presence of 200 μg · m-3 acidic (NH4)2SO4 seed aerosol |
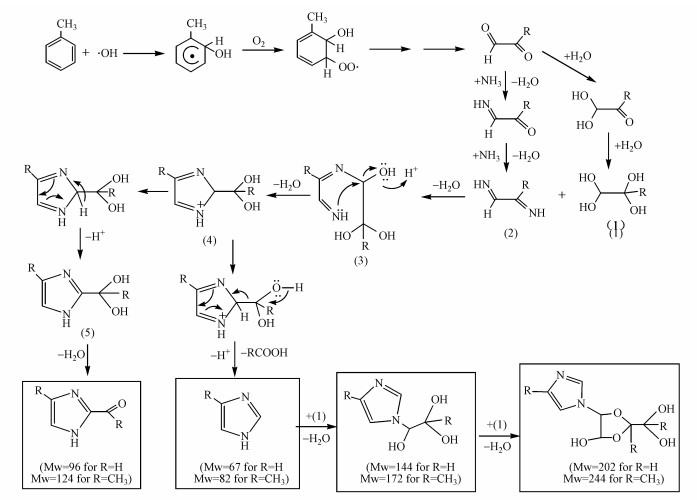 |
| 图 8 形成咪唑类产物的可能反应机理 Fig. 8 The possible reaction mechanism for the formation of imidazole products |
为了考察酸性(NH4)2SO4种子气溶胶对咪唑类产物形成的影响, 分别测定了不同浓度酸性(NH4)2SO4种子气溶胶存在时甲苯SOA粒子的紫外-可见吸收光谱.如图 9所示, 随着酸性(NH4)2SO4种子气溶胶的浓度从20 μg · m-3增加到200 μg · m-3, 280 nm处吸光度(对应于甲苯SOA中咪唑类产物的含量)逐渐增大.由图 7可知, 二醛化合物催化形成四醇和二亚胺产物是产生咪唑类化合物的先决条件.随着酸性(NH4)2SO4种子气溶胶浓度的增加, 更多的二醛化合物在其表面凝结, 并与H+和NH4+反应形成更多的咪唑产物.但是当酸性(NH4)2SO4种子气溶胶的浓度超过100 μg · m-3时, 280 nm处吸光度几乎保持不变.这可能是因为对于甲苯1×10-6和10×10-6 O3的反应体系, 甲苯的光氧化产生的二醛化合物是一定的, 当体系中存在100 μg · m-3酸性(NH4)2SO4种子气溶胶时, 已将所有的二醛化合物反应完全.再增加酸性(NH4)2SO4种子气溶胶的浓度, 已没有二醛化合物参与反应, 甲苯SOA中咪唑类组分的含量保持不变.
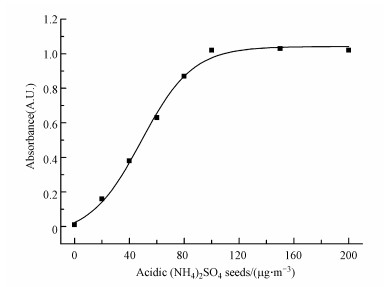 |
| 图 9 不同浓度酸性(NH4)2SO4种子气溶胶存在时甲苯SOA过滤提取液在280 nm处吸光度 Fig. 9 The absorbance of 280 nm of filter extract solution of toluene SOA with different concentration of acidic (NH4)2SO4 seeds |
综合上述紫外-可见光谱和电喷雾电离质谱的分析可知, 随着酸性(NH4)2SO4种子气溶胶浓度的增大, 形成咪唑类含氮产物的量增多, 甲苯SOA粒子在280 nm处的吸光度随之增大.在200 μg · m-3酸性(NH4)2SO4种子气溶胶存在时甲苯SOA粒子的负离子质谱主要是咪唑类化合物的去质子化分子离子[M-H]-峰.这是因为随着酸性硫酸铵种子气溶胶浓度的增大, H+和NH4+随之增大, 而单位比表面积凝结的乙二醛等羰基化合物则随之减少, 因而二醛化合物酸催化水合, 并与NH4+反应就越完全.二醛化合物在高浓度酸性硫酸铵细粒子表面凝结和反应是形成含氮有机物的主要通道.气相二醛化合物在高浓度酸性(NH4)2SO4细粒子表面非均相酸催化反应快速产生咪唑类产物.相比于Lu等(2009)和Jang等(2002)的实验, 本论文将酸性(NH4)2SO4种子气溶胶浓度增加至200 μg · m-3, 利用紫外-可见光谱仪和液相色谱-质谱测量甲苯SOA粒子的化学组分, 进一步证实了酸性(NH4)2SO4种子气溶胶能够提供酸性表面层, 促进二醛化合物在其表面凝结形成咪唑类产物.高浓度的种子气溶胶还为非均相酸催化反应提供了更多的反应性位点, 将更多的气相二醛化合物转化为颗粒相的咪唑类产物, 从而显著促进SOA的形成.
按照Bones等(2010)的实验结果, 乙二醛与硫酸铵液相反应需要几天的时间才能形成咪唑类产物.而在实际大气中, 雾滴, 水滴等水相气溶胶因水气挥发, 湿沉降等原因在大气停留时间较短(Herckes et al., 2013), 乙二酸与铵离子不易通过水相反应形成咪唑类化合物.而Teich等(2016)利用毛细管-质谱联用装置分离出中国和欧洲地区的大气气溶胶的咪唑、咪唑甲醛等咪唑类含氮有机物, 测得其浓度在0.2~14 ng · m-3之间.这证实大气气溶胶粒子中存在咪唑含氮有机物, 表明存在快速产生咪唑类产物的反应路径.而本文的实验结果表明, 气相乙二醛等二醛化合物能够在高浓度酸性硫酸铵种子气溶胶表面凝结, 并快速发生酸催化水合, 并与NH4+反应形成咪唑类产物.这为高浓度酸性硫酸铵细粒子背景下, 大气咪唑类棕色碳的形成机理研究提供了实验依据.
4 结论(Conclusions)亚微米酸性无机种子气溶胶具有较大的比表面积, 能够影响SOA的形成和化学组分.本文采用PM2.5粒子检测仪、紫外-可见吸收光谱仪和高效液相色谱质谱仪测量不同酸性(NH4)2SO4种子气溶胶存在时甲苯SOA的浓度和化学组分.测得的光谱和质谱信息显示羧酸化合物是没有种子气溶胶存在时甲苯SOA的主要组分.由于H2SO4的强吸水性, 酸性(NH4)2SO4种子气溶胶形成酸性表面层, 气相二醛化合物快速在其表面凝结和反应转化为颗粒相咪唑类产物, 从而显著促进甲苯SOA的产生.咪唑类含氮有机物具有较强的吸光性能, 后续的实验可开展酸性无机细粒子存在时SOA的光学特性研究.
Baltensperger U. 2010. Aerosols in clearer focus[J]. Science, 329(5998): 1468-1470. |
Bones D L, Henricksen D K, Mang S A, et al. 2010. Appearance of strong absorbers and fluorophores in limonene-O3 secondary organic aerosol due to NH4+-mediated chemical aging over long time scales[J]. Journal of Geophysical Research -Atmospheres, 115(D05203): 1-14. |
Carlton A G, Turpin B J, Altieri K E, et al. 2007. Atmospheric oxalic acid and SOA production from glyoxal:Results of aqueous photooxidation experiments[J]. Atmospheric Environment, 41(35): 7588-7602. DOI:10.1016/j.atmosenv.2007.05.035 |
Cocker Ⅲ D R, Clegg S L, Flagan R C, et al. 2001. The effect of water on gas-particle partitioning of secondary organic aerosol. Part II. m-xylene and 1, 3, 5-trimethylbenzene photooxidation systems[J]. Atmospheric Environment, 35(35): 6073-6085. DOI:10.1016/S1352-2310(01)00405-8 |
Drozd G T, Zhao Y L, Saliba G, et al. 2019. Detailed speciation of intermediate volatility and semivolatile organic compound emissions from gasoline vehicles:Effects of cold-starts and implications for secondary organic aerosol formation[J]. Environmental Science & Technology, 53(3): 1706-1714. |
Edney E O, Driscoll D J, Speer R E, et al. 2000. Impact of aerosol liquid water on secondary organic yields of irradiated toluene/propylene/NOx/(NH4)2SO4/Air Mixtures[J]. Atmospheric Environment, 34(23): 3907-3919. |
Ge S, Xu Y, Jia L. 2017. Effects of inorganic seeds on secondary organic aerosol formation from photochemical oxidation of acetone in a chamber[J]. Atmospheric Environment, 170: 205-215. DOI:10.1016/j.atmosenv.2017.09.036 |
Hao L Q, Wang Z Y, Huang M Q, et al. 2007. Effects of seed aerosols on the growth of secondary organic aerosols from the photooxidation of toluene[J]. Journal of Environmental Sciences, 19(6): 704-708. DOI:10.1016/S1001-0742(07)60117-X |
Herckes P, Valsaraj T, Collett Jr J L. 2013. A review of observations of organic matter in fogs and clouds:origin, processing and fate[J]. Atmospheric Research, 132-133: 434-449. DOI:10.1016/j.atmosres.2013.06.005 |
Huang M Q, Hao L Q, Cai S Y, et al. 2017. Effects of inorganic seed aerosols on the particulate products of aged 1, 3, 5-trimethylbenzene secondary organic aerosol[J]. Atmospheric Environment, 152: 490-502. DOI:10.1016/j.atmosenv.2017.01.010 |
Huang M Q, Hao L Q, Gu X J, et al. 2013. Effects of inorganic seed aerosols on the growth and chemical composition of secondary organic aerosol formed from OH-initiated oxidation of toluene[J]. Journal of Atmospheric Chemistry, 70(2): 151-164. DOI:10.1007/s10874-013-9262-9 |
Huang M Q, Zhang W J, Wang Z Y, et al. 2011. Mass spectrometry study of OH-initiated photooxidation of toluene[J]. Chinese Journal of Chemical Physics, 24(6): 672-678. DOI:10.1088/1674-0068/24/06/672-678 |
Hinks M L, Montoya-Aguilera J, Ellison L, et al. 2017. Effect of relative humidity on the composition of secondary organic aerosol from the oxidation of toluene[J]. Atmospheric Chemistry and Physics Discussions, 18(2018): 1643-1652. |
Jang M, Czoschke N M, Lee S, et al. 2002. Heterogeneous atmospheric aerosol production by acid-catalyzed particle-phase reactions[J]. Science, 298(5594): 814-817. DOI:10.1126/science.1075798 |
Jang M S, Kamens R M. 2001. Characterization of secondary aerosol from the photooxidation of toluene in the presence of NOx and 1-propene[J]. Environmental Science & Technology, 35(18): 3626-3639. |
Kampf C J, Jakob R, Hoffmann T. 2012. Identification and characterization of aging products in the glyoxal/ammonium sulfate system-implications for light-absorbing material in atmospheric aerosols[J]. Atmospheric Chemistry and Physics, 12(14): 6323-6333. DOI:10.5194/acp-12-6323-2012 |
Kroll J H, Chan A W H, Ng N L, et al. 2007. Reactions of semivolatile organics and their effects on secondary organic aerosol formation[J]. Environmental Science & Technology, 41(10): 3545-3550. |
Laskin A, Laskin J, Nizkorodov S A. 2015. Chemistry of atmospheric brown carbon[J]. Chemical Review, 115(10): 4335-4382. DOI:10.1021/cr5006167 |
Li M, Klimont Z, Zhang Q, et al. 2018. Comparison and evaluation of anthropogenic emissions of SO2 and NOx over China[J]. Atmospheric Chemistry and Physics, 18(5): 3433-3456. DOI:10.5194/acp-18-3433-2018 |
刘宪云, 黄明强, 王振亚, 等. 2009. 用于模拟SOA形成的烟雾腔的构造和表征[J]. 环境科学与技术, 32(9): 105-109. DOI:10.3969/j.issn.1003-6504.2009.09.024 |
Liu Y, Liggio J, Staebler R, et al. 2015. Reactive uptake of ammonia to secondary organic aerosols:kinetics of organonitrogen formation[J]. Atmospheric Chemistry and Physics, 15(23): 13569-13584. DOI:10.5194/acp-15-13569-2015 |
Lu Z F, Hao J M, Takekawa H, et al. 2009. Effect of high concentrations of inorganic seed aerosols on secondary organic aerosol formation in the m-xylene/NOx photooxidation system[J]. Atmospheric Environment, 43(4): 897-904. DOI:10.1016/j.atmosenv.2008.10.047 |
Maxut A, Nozière B, Fenet B, et al. 2015. Formation mechanism and yield of small imidazoles from reactions of glyoxal with NH4+ in water at neutral pH[J]. Physical Chemistry Chemical Physics, 17(31): 20416-20424. DOI:10.1039/C5CP03113C |
Riccobono F, Rondo L, Sipilä M, et al. 2012. Contribution of sulfuric acid and oxidized organic compounds to particle formation and growth[J]. Atmospheric Chemistry and Physics, 12(20): 9427-9439. DOI:10.5194/acp-12-9427-2012 |
Robinson C B, Schill G P, Zarzana K J, et al. 2013. Impact of organic coating on optical growth of ammonium sulfate particles[J]. Environmental Science & Technology, 47(23): 13339-13346. |
Shao P Y, Tian H Z, Sun Y J, et al. 2018. Characterizing remarkable changes of severe haze events and chemical compositions in multi-size airborne particles (PM1, PM2.5 and PM10) from January 2013 to 2016-2017 winter in Beijing, China[J]. Atmospheric Environment, 189: 133-144. DOI:10.1016/j.atmosenv.2018.06.038 |
Teich M, van Pinxteren D, Kecorius S, et al. 2016. First quantification of imidazoles in ambient aerosol particles:potential photosensitizers, brown carbon constituents, and hazardous components[J]. Environmental Science & Technology, 50(3): 1166-1173. |
徐俊, 黄明强, 冯状状, 等. 2018. 氨对甲苯二次有机气溶胶形成和化学组分的影响研究[J]. 环境科学学报, 38(8): 3243-3251. |
徐俊, 黄明强, 冯状状, 等. 2019. 氨与甲苯SOA形成含氮有机物的影响因素研究[J]. 中国环境科学, 39(2): 533-541. DOI:10.3969/j.issn.1000-6923.2019.02.011 |
 2020, Vol. 40
2020, Vol. 40


