2. 中国地质大学(武汉), 武汉 430074
2. China University of Geosciences, Wuhan 430074
多氯联苯(PCBs)作为典型的持久性有机污染物目前已受到人们的广泛关注, 因其具有较强的亲脂性, 易在生物体内富集, 并具有较大的毒性, 且可经过食物链不断叠加富集, 从而会对生态环境和人类健康造成极大危害(Ricardo et al., 2015).PCBs的209种同系物中, 其中19种PCBs的两个对映体在空间构型上均呈现出轴对称的特性并且可在室温下稳定存在(Izabela et al., 2016), PCBs在围绕手性轴进行旋转的过程中, 邻位取代基个数多、受空间位阻效应影响越大进而能保持手性构型相对稳定的PCBs被称为阻转类手性PCBs, 简称手性PCBs.因此, PCBs的同系物有228种, 而不是209种(Zheng et al., 2015).手性PCBs可长期存留于自然环境条件下, 属于难降解类PCBs(Kaiser, 1974).
外消旋PCBs的两种手性对映体在环境中可能展现出不同行为和归趋, 手性PCBs被动植物吸收、在动植物体内迁移、代谢、转化及累积等一切涉及生命活动的过程均可能存在对映体选择性, 动植物体内对映体分数(EFs)的变化可被用于评价潜在的生植物转化途径和对映体水平的生物活性(Zhai et al., 2011; Qiao et al., 2019).近年来, 有关生物体内手性PCBs的研究越来越多(He et al., 2018; Li et al., 2019; Wu et al., 2019), 例如, 农业部农产品质量安全环境因素控制重点实验室的科研人员对蚯蚓体内PCB95和PCB149的立体选择性进行了研究(He et al., 2018).还有研究通过肝特异性缺失细胞色素P450还原酶的小鼠(KO)和同基因野生型(WT)小鼠暴露于外消旋PCB 136, 证实了小鼠体内细胞色素P450酶与手性PCB136及其羟基代谢产物的代谢机理和手性选择性(Li et al., 2019).Wong等(2004)在淡水水生生物食物网中发现PCBs在传递过程中表现出一定的选择性代谢特征, 其中, 虹鳟鱼对于(+)-PCB136消除要显著优于(-)-PCB136.仅考虑外消旋PCBs的毒理学效应可能会低估或高估手性PCBs的环境安全和健康风险.开展对映体水平上的毒理学研究对于正确评估这类持久性有机污染物的环境、健康风险显得尤为重要.
我国是电子垃圾拆解的主要地区之一, 电子拆解活动如电子设备的拆解, 导致电容器和涂料层中的多氯联苯释放到环境中(穆熙等, 2019), 进入环境中的PCBs可通过呼吸、接触和膳食等多种暴露途径富集于人体(Kiviranta et al., 2004; Evanthia et al., 2009), 进而通过生物放大作用引发免疫、生殖系统及内分泌系统的干扰效应等负面健康效应(Williams et al., 2016).目前, 电子垃圾拆解活动已导致环境介质中残留的PCBs浓度居高不下.研究表明, 电子垃圾拆卸集中区域周边鱼类体内PCBs的检出浓度是对照组的百倍乃至千倍(Wu et al., 2008), 即高浓度暴露条件下的鱼类负荷水平十分显著.残留在鱼类体内的PCBs可通过膳食暴露途径传递到人体内从而产生负面健康风险.目前, 人们对电子垃圾拆解区水生生物样品中PCBs的研究主要集中于外消旋体(Fu et al., 2011; Tang et al., 2015; Shi et al., 2016; Igbo et al., 2018), 有关手性PCBs在鱼肉组织中的分布特征和选择性富集则较鲜有报道.因此, 本研究利用课题组前期所建立的方法对电子垃圾拆解区城镇居民经常食用的鱼类样品中7种典型的手性PCBs进行拆分测定, 并对手性单体的手性特征进行探讨, 以期深入理解鱼类体内手性PCBs的代谢和富集特征, 为准确评价手性PCBs对人类的暴露水平及风险特征提供参考.
2 材料与方法(Materials and methods) 2.1 仪器Agilent 7890B-5975N型气相色谱-质谱联用仪(美国Agilent公司)、加速溶剂萃取仪(Dionex ASE 350, USA)、氮吹浓缩仪(Organomation Associates, USA)、旋转蒸发仪(Heidolph, Germany)、Cyclosil-B(30 m×0.25 mm×0.25 μm)气相色谱手性柱(美国Agilent公司).
2.2 标准品与有机溶剂7种多氯联苯标准品PCB45、PCB91、PCB95、PCB132、PCB136、PCB149和PCB174购自美国AccuStandard公司, 纯度>97%;提取和净化过程中所用试剂均为农残级和国产分析纯级, 其中, 甲醇、二氯甲烷、丙酮、正己烷及甲苯(美国J.T.Baker公司)或Dikma(Scarborough, USA)为农残级, 浓硫酸、甲醇、二氯甲烷、丙酮和无水硫酸钠(北京精细化工厂)为分析纯级;硫酸(优级纯)购自北京精细化工厂, 硅藻土由戴安公司提供, 柱层析硅胶(100~200目)购自山东青岛海洋化工厂分厂, 优级纯无水Na2SO4购自国药集团化学试剂有限公司.
2.3 样品的采集、预处理、脂肪含量和手性PCBs的测定鲮鱼(Cirrhinus moliorella)、鲫鱼(Carassius auratus)和乌鳢(Ophicephalus argu)是当地居民经常食用的淡水鱼类, 污染可能会引起当地居民经食鱼而发生PCBs暴露风险.鲮鱼、鲫鱼和乌鳢采集于龙塘镇某电子垃圾拆解车间附近水塘, 该水塘为周边居民提供可食用的大部分鱼肉样品, 选择生长周期为一年内、大小形态相似的3种鱼类各采集7条.鲮鱼从鱼头到鱼尾的长度为18.3~22.6 cm, 质量为210.7~250.2 g;鲫鱼从鱼头到鱼尾的长度为15.7~17.4 cm, 质量为210.3~240.8 g;乌鳢从鱼头到鱼尾的长度为24.1~26.8 cm, 质量为180.6~220.0 g.鱼类样品采完后用保温箱冰浴运输至实验室放入-20 ℃冰箱中保存, 实验前取出化冻, 每条鱼取鱼肉(不包含鱼皮和内脏)剪碎匀浆后, 冷冻干燥.采集鱼肉样品的同时采集池塘内沉积物, 鱼肉和沉积物样品解冻后, 用万能粉碎机粉碎搅匀, 称取约8.0 g粉碎后的样品冷冻干燥后与硅藻土充分混合并转移至提取筒中, 用加速溶剂萃取仪提取.提取液转入到已经准确称重m1(天平精密度为0.001 mg)的鸡心瓶内旋转蒸发至溶液呈稠状, 静置24 h称量至恒重后记录质量m2, 利用重量法计算脂肪含量.将提取后的样品浓缩液经过凝胶渗透色谱除脂及大分子物质后, 依次通过酸性硅胶柱和复合硅胶柱净化, 利用碱性氧化铝柱分离得到PCBs组分, 将所得样品浓缩后, 转入进样瓶, 封装待测.详细的鱼肉中手性对映异构体的前处理及含量测定方法见文献(朱帅等, 2017).
2.4 生物/沉积物富集因子(BSAF)及生物放大因子(BMF)的计算BSAF和BMF分别按式(1)和式(2)计算.
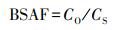
|
(1) |
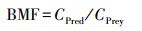
|
(2) |
式中, CO为生物体中PCBs含量(ng·g-1, 以脂重计);CS为表层沉积物中该污染物的含量(ng·g-1, 以有机碳计);CPred为捕食者(乌鳢)PCBs含量(ng·g-1, 以脂重计);CPrey为被捕食者(鲮鱼和鲫鱼)PCBs含量(ng·g-1, 以脂重计).乌鳢、鲮鱼和鲫鱼的脂肪含量分别为1.2%、2.1%和2.6%.
2.5 样品的质量控制与质量保证样品提取、净化、分析过程中严格按照前期所建立的鱼肉中手性对映异构体的前处理及含量测定方法(朱帅等, 2017)对样品进行质量控制.在样品分析时, 每7个样品设置一个流程空白作为实验室背景干扰.实验过程中, 流程空白样品中仅部分检测到PCB136(检出率为25%, 含量为6.2~7.7 ng·g-1), 7种PCBs的方法检出限(S/N=3)为0.4~5.0 ng·g-1, 回收率为89.2%~114.0%, 相对标准偏差(RSD)为0.3%~2.1%, 通过标准品测定证实实验过程不会影响PCBs手性的结果.
3 结果和讨论(Results and discussion) 3.1 鱼肉样品典型手性同系物的分布和累积对采集的3种鱼肉样品中的7条鱼分别进行测定, 获得了鱼肉样品中7种手性PCBs的平均含量, 结果如表 1所示.由表 1可知, ΣPCBs在3种鱼肉样品中的含量为386.7~602.8 ng·g-1, 该结果与中国科学院广州地球化学研究所有机地球化学国家重点实验室团队在电子垃圾拆解区测得的PCBs含量相当(唐斌等, 2014), 远远高于渤海湾海域鱼类样品中指示性PCBs的含量(王莎莎等, 2014)和上海地区鱼肉中31种PCBs的含量(韩姝媛等, 2010).由此可以推测由于电子垃圾拆解区不规范的拆解活动造成当地鱼类PCBs的污染, 其中, 乌鳢污染最为严重, 鲮鱼污染最轻.利用测定数据绘制不同鱼肉样品中典型手性PCBs同类物的分布特征, 结果如图 1所示.由图可知, 3种鱼肉组织中PCBs具有相似的同类物特征, 均以PCB91、PCB95、PCB132、PCB136和PCB149为主, 稍有不同的是鲮鱼中手性PCBs以PCB132和PCB149为主, 而鲫鱼和乌鳢中手性PCBs以PCB95和PCB149为主.
| 表 1 鱼肉样品中7种手性PCBs的含量 Table 1 Contents of 7 chiral PCBs in the fish smaples |
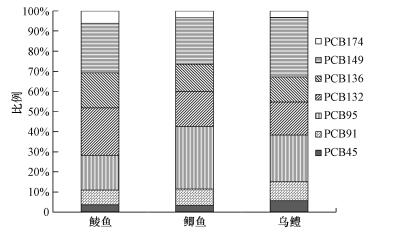 |
| 图 1 不同鱼肉样品中典型手性PCBs的同类物分布特征 Fig. 1 PCBs profiles in difference fish samples |
根据鱼肉组织中7种手性PCBs的含量计算得到对映体分数(EF值), 为了更好地说明鱼体内PCBs的EF值变化特征, 本研究对采自同一池塘的沉积物中手性PCBs的含量也进行了测定, 计算得到沉积物中PCBs的EF值.将沉积物及鱼类样品中各手性PCBs单体的EF值绘制成箱式图, 结果如图 2所示.由图可知, 沉积物中各手性PCBs单体的EF值为0.436~0.523, 与标准值有一定的差异, 表明沉积物中微生物对这些手性单体的对映体选择性代谢能力较强.3种鱼肉样品各手性PCBs单体的EF值与沉积物具有显著差异, 说明这些手性PCBs通过生物转化具有对映体选择性富集和代谢作用.乌鳢体内的手性PCBs的EF值除PCB174外均低于鲮鱼和鲫鱼, 可能是由于乌鳢是肉食性鱼类, 以小鱼、小虾类为食物, 这些手性PCBs单体通过食物链的生物放大效应导致其较低的EF值.乌鳢样品中PCB174的EF值高于鲮鱼、鲫鱼, 却与沉积物中PCB174的EF值相当, 这可能是因为乌鳢体内富集的PCB174一部分来自于鲮鱼、鲫鱼等鱼类中, 一部分来自于沉积物, 同时乌鳢对于高于6个氯原子的PCBs的选择性富集代谢过程与低于6个氯原子的PCBs不同, 导致(+)-PCB176比(-)-PCB176更容易被选择性富集.从图 2中可知, 在所有的鱼肉样品中(-)-PCB95比(+)-PCB95更容易被选择性富集, 此结果与文献报道的北极红点鲑中(-)-PCB95被选择性优先富集的结果相同(Lu et al., 2014).
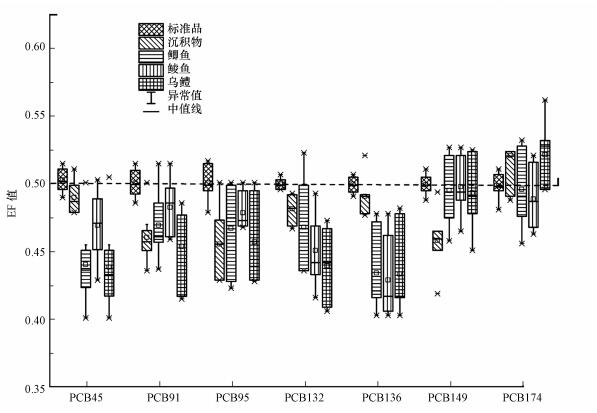 |
| 图 2 标准品、沉积物及鱼肉样品中手性PCBs的EF值 Fig. 2 Enantiomer fractions of chiral PCBs in standard solution, sediment and fish |
生物/沉积物富集因子(BSAF)是评估水生生物(特别是底栖性水生生物)对污染物富集行为及其生态风险的一个重要参数.根据BSAF计算公式(1)将鱼肉和沉积物中PCBs含量(湿重)换算成PCBs含量(脂重), 结果见表 2.由表 2可知, 鱼肉和沉积物中ΣPCBs的含量为17609~28931 ng·g-1(脂重), 与比利时斯海尔德河中鱼肉样品中PCBs的残留量在同一水平(Roosens et al., 2008), 是瑞典南部的19个湖泊中鱼肉中PCBs含量的20倍(Berglund et al., 2000), 是非洲坦干依喀湖鱼类PCBs含量的百倍(Manirakiza et al., 2002).同时, 计算获得了鲮鱼、鲫鱼和乌鳢对PCBs的BSAF(表 3), 分别为0.31~1.71、0.30~1.86和0.50~2.64, 其中, 大部分同系物的BSAF在0.5~2.0之间.如果不考虑生物对PCBs的代谢作用(生物降解)和生物放大作用, 根据平衡分配理论, PCBs在沉积物有机碳和生物脂肪中的分配应该相似, 即BSAF应该在1~2之间(Burkhard et al., 2004; 2005).本研究中底栖性鱼类对某些同系物的BSAF值超出平衡分配理论预测范围, 证明这些鱼类可能对某些PCB同系物具有选择性生物降解作用或生物放大作用.
| 表 2 鱼肉和底泥样品中7种手性PCBs的含量 Table 2 Contents of 7 chiral PCBs in the fish and sediments smaples |
| 表 3 3种底栖性鱼类的BSAF值 Table 3 BSAF values of PCBs in the three bottom fish species |
由于不同生物种类的生活习性及其所处的营养级不同, 它们对PCBs的富集能力也不同.鲮鱼和乌鳢具有相似的营养级, 对PCBs的BSAF高于鲫鱼(图 3), 可能与其独特的生活习性有关.鲮鱼喜舐刮沉积物上的附着物, 同时也摄取腐殖质和其他有机碎屑, 沉积物和有机碎屑中很高的PCBs含量可能导致其较高的BSAF.对于高于6个氯原子的PCBs, 乌鳢的BSAF显著高于鲮鱼和鲫鱼, 可能是由于乌鳢通过捕食其他鱼类, 这些化合物的生物放大效应导致了其较高的BSAF.乌鳢栖息于底泥中, 底泥中较高的PCBs含量也可能是导致其较高的BSAF的原因之一.
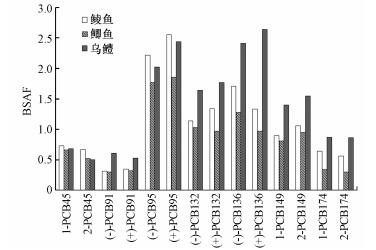 |
| 图 3 3种底栖性鱼类对PCBs的富集能力 Fig. 3 Bioaccumulation potentials of PCBs in the threebottom fish species |
乌鳢是一种肉食性鱼类, 主要以鲮鱼、鲫鱼等其他较小鱼类为食, 根据乌鳢/鲮鱼和乌鳢/鲫鱼食物关系计算的生物放大因子(BMF)分别为1.35~4.51和2.17~5.10.如图 4所示, 4氯代PCBs即PCB45的BMF较高(BMF在4~5), 而7氯代PCBs具有最小的BMF值(BMF在1~3之间).可能是因为水生生物对高氯代PCBs同系物具有代谢和排泄作用, 而富集于体内的低氯代PCBs同系物较为稳定, 导致了其较高的生物放大能力(BMF).除PCB95之外, 乌鳢/鲮鱼和乌鳢/鲫鱼作用过程中均表现出方向一致的对映体选择性, (-)-PCB95在乌鳢/鲫鱼中被选择性富集, 而乌鳢/鲮鱼作用过程则表现为(+)-PCB95富集, 造成这种结果的原因可能是不含有间对位邻位原子的PCBs具有更强的持久性不易被生物所利用代谢.PCB95分别含有一对邻对和间对位, 具有间对位邻位, 属于易代谢类型, 导致PCB95在鳢/鲮鱼和乌鳢/鲫鱼两个过程中的对映选择性不同;此外, 还受到PCBs的溶解性、稳定性、生物种类、在生物体内的对映体选择性迁移和代谢作用、生物体内环境及外界环境条件等多种因素影响.
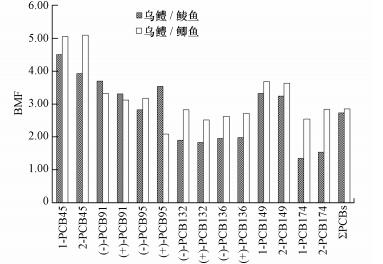 |
| 图 4 手性PCBs对映体在乌鳢对鲮鱼和鲫鱼的生物富集作用 Fig. 4 Bioaccumulation potentials of PCBs in the fish species |
本研究从同系物和对映体水平探讨了鱼肉样品中手性PCBs的污染水平、分布规律、生物转化作用的对映体选择性, 并对对映体选择性富集作用进行了初步分析, 证实了生物富集作用具有一定的对映体选择性.具体如下:ΣPCBs在3种鱼肉样品中的含量为386.7~602.8 ng·g-1, 可以推断由于电子垃圾拆解区的拆解活动造成当地鱼类PCBs的污染.3种鱼肉样品的各手性PCBs单体(PCB45、PCB91、PCB95、PCB132、PCB136、PCB149和PCB174)的EF值与沉积物具有显著差异, 表明这些手性PCBs在鱼类体内可能具有对映体选择性富集和代谢作用.不同种类鱼肉样品的EF值不同, 说明它们对PCBs的富集能力不同, 这可能与它们的生活习性及其所处营养级不同有关.底栖性鱼类对某些同系物的BSAF值超出平衡分配理论预测范围, 证明这些鱼类可能对某些PCBs同系物具有选择性生物降解作用或生物放大作用.由于不同生物种类的生活习性及其所处的生态位(营养级)不同, 它们对PCBs的富集能力也不同.根据乌鳢/鲮鱼和乌鳢/鲫鱼食物关系计算的生物放大因子(BMF)分别为1.35~4.51和2.17~5.10, 表明乌鳢对手性PCBs具有生物放大作用.除PCB95之外, 乌鳢/鲮鱼和乌鳢/鲫鱼作用过程中均表现出方向一致的对映体选择性, 这可能是手性PCB95本身的结构特点导致(-)-PCB95在乌鳢/鲫鱼中被选择性富集, (+)-PCB95在乌鳢/鲮鱼中被选择性富集.
Berglund O, Larsson P, Ewald G, et al. 2000. Bioaccumulation and differential partitioning of polychlorinated biphenyls in freshwater, planktonic food webs[J]. Canadian Journal of Fisheries and Aquatic Sciences, 57(6): 1160-1168. DOI:10.1139/f00-045 |
Burkhard L P, Cook P M, Lukasewycz M T. 2004. Biota-sediment accumulation factors for polychlorinated biphenyls, dibenzo-p-dioxins, and dibenzofurans in Southern Lake Michigan Lake Trout (Salvelinus namaycush)[J]. Environmental Science & Technology, 38(20): 5297-5305. |
Burkhard L P, Cook P M, Lukasewycz M T. 2005. Comparison of biota-sediment accumulation factors across ecosystems[J]. Environmental Science & Technology, 39(15): 5716-5721. |
Evanthia D K, Jeanpierre B G, Linda C G, et al. 2009. Endocrine-disrupting chemicals:An endocrine society scientific statement[J]. Endocrine Reviews, 30(4): 293-342. DOI:10.1210/er.2009-0002 |
Fu J J, Wang Y W, Zhang A Q, et al. 2011. Spatial distribution of polychlorinated biphenyls (PCBs) and polybrominated biphenyl ethers (PBDEs) in an e-waste dismantling region in Southeast China:Use of apple snail (Ampullariidae) as a bioindicator[J]. Chemosphere, 82(5): 648-655. DOI:10.1016/j.chemosphere.2010.11.014 |
He Z Y, Xu Y P, Wang W W, et al. 2018. Stereoselective bioaccumulation and elimination of chiral PCBs 95 and 149 in earthworm Eisenia fetida[J]. Chemosphere, 212: 497-503. DOI:10.1016/j.chemosphere.2018.08.075 |
韩姝媛, 余应新, 李俊岭. 2010. 上海地区肉类和鱼类食品中多氢耳关苯含量特征及其对人体的生物有效性[J]. 环境科学学报, 30(6): l322-l330. |
Igbo J K, Chukwu L O, Oyewo E O. 2018. Assessment of Polychlorinated Biphenyls (PCBs) in water, sediments and biota from e-waste dumpsites in Lagos and Osun States, South-West, Nigeria[J]. Journal of Applied Sciences and Environmental Management, 22(4): 459-464. DOI:10.4314/jasem.v22i4.3 |
Izabela K K, Hans J L. 2016. Chiral polychlorinated biphenyls:Absorption, metabolism and excretion-a review[J]. Environmental Science and Pollution Research, 23(3): 2042-2057. DOI:10.1007/s11356-015-4150-2 |
Kaiser K L. 1974. On the optical activity of polychlorinated biphenyls[J]. Environmental Pollution (1970), 7(2): 93-101. DOI:10.1016/0013-9327(74)90076-7 |
Kiviranta H, Ovaskainen M L, Vartiainen T. 2004. Market basket study on dietary intake of PCDD/Fs, PCBs, and PBDEs in Finland[J]. Environment International, 30(7): 923-932. DOI:10.1016/j.envint.2004.03.002 |
Li X S, Wu X N, Kelly K M, et al. 2019. Toxicokinetics of chiral PCB 136 and its hydroxylated metabolites in mice with a liver-specific deletion of cytochrome P450 reductase[J]. Chemical Research in Toxicology, 32(4): 727-736. DOI:10.1021/acs.chemrestox.8b00389 |
Lu Z, Fisk A T, Kovacs K M, et al. 2014. Temporal and spatial variation in polychlorinated biphenyl chiral signatures of the greenland shark (Somniosus microcephalus) and its arctic marine food web[J]. Environmental Pollution, 186: 216-225. DOI:10.1016/j.envpol.2013.12.005 |
Manirakiza P, Covaci A, Nizigiymana L, et al. 2002. Persistent chlorinated pesticides and polychlorinated biphenyls in selected fish species from Lake Tanganyika, Burundi, Africa[J]. Environmental Pollution, 117(3): 447-455. DOI:10.1016/S0269-7491(01)00188-9 |
穆熙, 李尧捷, 曹红梅, 等. 2019. 中国西部某规模化电子垃圾拆解厂多氯联苯排放污染特征及职业呼吸暴露风险[J]. 环境科学学报, 39(8): 2800-2810. |
Qiao L, Zheng X B, Zheng J, et al. 2019. Legacy and currently used organic contaminants in human hair and hand wipes of female E-waste dismantling workers and workplace dust in South China[J]. Environmental Science & Technology, 53(5): 2820-2829. |
Ricardo F G, Iria Y P, Elena M C, et al. 2015. A critical review about human exposure to Polychlorinated Dibenzo-p-Dioxins (PCDDs), Polychlorinated Dibenzofurans (PCDFs) and Polychlorinated Biphenyls (PCBs) through foods[J]. Critical Reviews in Food Science and Nutrition, 55(11): 1590-1617. DOI:10.1080/10408398.2012.710279 |
Roosens L, Dirtu A C, Goemans G, et al. 2008. Brominated flame retardants and polychlorinated biphenyls in fish from the river Scheldt, Belgium[J]. Environment International, 34(7): 976-983. DOI:10.1016/j.envint.2008.02.009 |
Shi J S, Zheng J S, Wong M H, et al. 2016. Health risks of polycyclic aromatic hydrocarbons via fish consumption in Haimen bay (China), downstream of an e-waste recycling site (Guiyu)[J]. Environmental research, 147: 233-240. DOI:10.1016/j.envres.2016.01.036 |
Tang W, Cheng J P, Zhao W C, et al. 2015. Mercury levels and estimated total daily intakes for children and adults from an electronic waste recycling area in Taizhou, China:Key role of rice and fish consumption[J]. Journal of Environmental Sciences, 34: 107-115. DOI:10.1016/j.jes.2015.01.029 |
唐斌, 罗孝俊, 曾艳红, 等. 2014. 电子垃圾拆解区污染池塘中鱼类多氯联苯及其代谢产物的组织分配及暴露风险[J]. 环境科学, 35(12): 4655-4662. |
Williams K E, Lemieux G A, Hassis M E, et al. 2016. Quantitative proteomic analyses of mammary organoids reveals distinct signatures after exposure to environmental chemicals[J]. Proceedings of the National Academy of Sciences, 113(10): E1343-E1351. DOI:10.1073/pnas.1600645113 |
Wong C S, Mabury S A, Whittle D M, et al. 2004. Organochlorine compounds in Lake Superior:Chiral polychlorinated biphenyls and biotransformation in the aquatic food web[J]. Environmental science & technology, 38(1): 84-92. |
Wu J P, Luo X J, Zhang Y, et al. 2008. Bioaccumulation of polybrominated diphenyl ethers (PBDEs) and polychlorinated biphenyls (PCBs) in wild aquatic species from an electronic waste (e-waste) recycling site in South China[J]. Environment international, 34(8): 1109-1113. DOI:10.1016/j.envint.2008.04.001 |
Wu X N, Zhai G S, Schnoor J L, et al. 2019. Atropselective disposition of 2, 2', 3, 4', 6-Pentachlorobiphenyl (PCB 91) and identification of its metabolites in mice with liver-specific deletion of cytochrome P450 reductase[J]. Chemical Research in Toxicology, 33(3): 1328-1338. DOI:10.1021/acs.chemrestox.9b00255 |
王莎莎, 高丽荣, 田益玲, 等. 2014. 渤海湾海域10种鱼类中二噁英类及指示性多氯联苯的污染特征研究及风险评价[J]. 环境科学, 35(6): 2281-2286. |
Zhai G S, Hu D F, Lehmler H J, et al. 2011. Enantioselective biotransformation of chiral PCBs in whole poplar plants[J]. Environmental Science & Technology, 45(6): 2308-2316. |
Zheng X B, Luo X J, Zeng Y H, et al. 2015. Chiral Polychlorinated Biphenyls (PCBs) in bioaccumulation, maternal transfer, and embryo development of chicken[J]. Environmental Science & Technology, 49(2): 785-791. |
朱帅, 饶竹. 2017. 鱼肉样品中的手性多氯联苯对映体的分离测定研究[J]. 分析测试学报, 36(6): 744-749. |
 2020, Vol. 40
2020, Vol. 40


